Дистанционный репетитор — онлайн-репетиторы России и зарубежья
КАК ПРОХОДЯТ
ОНЛАЙН-ЗАНЯТИЯ?
Ученик и учитель видят и слышат
друг друга, совместно пишут на
виртуальной доске, не выходя из
дома!
КАК ВЫБРАТЬ репетитора
Выбрать репетитора самостоятельно
ИЛИ
Позвонить и Вам поможет специалист
8 (800) 333 58 91
* Звонок является бесплатным на территории РФ
** Время приема звонков с 10 до 22 по МСК
ПОДАТЬ ЗАЯВКУ
Россия +7Украина +380Австралия +61Белоруссия +375Великобритания +44Израиль +972Канада, США +1Китай +86Швейцария +41
Выбранные репетиторы
Заполните форму, и мы быстро и бесплатно подберем Вам дистанционного репетитора по Вашим пожеланиям.
Менеджер свяжется с Вами в течение 15 минут и порекомендует специалиста.
Отправляя форму, Вы принимаете Условия использования и даёте Согласие на обработку персональных данных
Вы также можете воспользоваться
расширенной формой подачи заявки
Как оплачивать и СКОЛЬКО ЭТО СТОИТ
от
800 до 5000 ₽
за 60 мин.
и зависит
ОТ ОПЫТА и
квалификации
репетитора
ОТ ПОСТАВЛЕННЫХ ЦЕЛЕЙ ОБУЧЕНИЯ
(например, подготовка к олимпиадам, ДВИ стоит дороже, чем подготовка к ЕГЭ)
ОТ ПРЕДМЕТА (например, услуги репетиторовиностранных языков дороже)
Оплата непосредственно репетитору, удобным для Вас способом
Почему я выбираю DisTTutor
БЫСТРЫЙ ПОДБОР
РЕПЕТИТОРА И
ИНДИВИДУАЛЬНЫЙ ПОДХОД
ОПТИМАЛЬНОЕ
СООТНОШЕНИЕ ЦЕНЫ И
КАЧЕСТВА
ПРОВЕРЕНЫ ДОКУМЕНТЫ ОБ ОБРАЗОВАНИИ У ВСЕХ РЕПЕТИТОРОВ
НАДЕЖНОСТЬ И ОПЫТ.
DisTTutor на рынке с 2008 года.
ПРОВЕДЕНИЕ БЕСПЛАТНОГО, ПРОБНОГО УРОКА
ЗАМЕНА РЕПЕТИТОРА, ЕСЛИ ЭТО НЕОБХОДИМО
376065 УЧЕНИКОВ ИЗ РАЗНЫХ СТРАН МИРА
И вот, что УЧЕНИКИ ГОВОРЯТ
о наших репетиторах
Владимир Александрович Кузьмин
«
Тренинг у Кузьмина В. А. проходил в экстремальных условиях. Мой модем совершенно не держал соединение. За время часового тренинга связь прерывалась практически постоянно. Ясно, что в таких условиях чрезвычайно непросто чему-то учить.
Однако Владимир Александрович проявил удивительную выдержку и терпение. Неоднократно он перезванивал мне на сотовый телефон, чтобы дать пояснения или комментарии.
Ценой больших усилий нам удалось рассмотреть три программы: ConceptDraw MINDMAP Professional Ru, GeoGebra и Ultra Flash Video FLV Converter. Владимир Александрович открыл мне курс на платформе dist-tutor.info и научил подключать и настраивать Виртуальный кабинет, порекомендовав изучать возможности этого ресурса, чтобы постепенно уходить от использования Skype.
«
Вячеслав Юрьевич Матыкин
Чулпан Равилевна Насырова
«
Я очень довольна репетитором по химии. Очень хороший подход к ученику,внятно объясняет. У меня появились сдвиги, стала получать хорошие оценки по химии. Очень хороший преподаватель. Всем , кто хочет изучать химию, советую только её !!!
«
Алина Крякина
Надежда Васильевна Токарева
«
Мы занимались с Надеждой Васильевной по математике 5 класса. Занятия проходили в удобное для обоих сторон время. Если необходимо было дополнительно позаниматься во внеурочное время, Надежда Васильевна всегда шла навстречу. Ей можно было позванить, чтобы просто задать вопрос по непонятной задачке из домашнего задания.
«
Эльмира Есеноманова
Ольга Александровна Мухаметзянова
«
Подготовку к ЕГЭ по русскому языку мой сын начал с 10 класса. Ольга Александровна грамотный педагог, пунктуальный, ответственный человек. Она всегда старается построить занятие так, чтобы оно прошло максимально плодотворно и интересно. Нас абсолютно все устраивает в работе педагога. Сотрудничество приносит отличные результаты, и мы его продолжаем. Спасибо.
«
Оксана Александровна
Клиентам
- Репетиторы по математике
- Репетиторы по русскому языку
- Репетиторы по химии
- Репетиторы по биологии
- Репетиторы английского языка
- Репетиторы немецкого языка
Репетиторам
- Регистрация
- Публичная оферта
- Библиотека
- Бан-лист репетиторов
Партнеры
- ChemSchool
-
PREPY.
 RU
RU
- Class
Урок 27. Состав и физические свойства воды – HIMI4KA
Архив уроков › Химия 8 класс
В уроке 27 «Состав и физические свойства воды» из курса «Химия для чайников» узнаем, что из себя представляет вода, выясним её состав, а также физические свойства.
Наиболее распространенным оксидом на Земле является оксид водорода H2O, или вода. Без воды, как и без кислорода, невозможна жизнь человека, животных и растений.
Вода — единственное вещество, существующее на Земле одновременно в трех агрегатных состояниях: жидком, твердом и газообразном. Она является основным компонентом морей и океанов, ледников и айсбергов, облаков и тумана.
Около 70 % поверхности Земли покрыто океанами, морями, реками и озерами — природными хранилищами воды. Из космоса толстый слой воды имеет голубой цвет (рис. 104), вот почему нашу планету называют голубой. Вода входит в состав всех живых организмов, а также очень многих минералов.
104), вот почему нашу планету называют голубой. Вода входит в состав всех живых организмов, а также очень многих минералов.
Содержание
- Состав и строение воды
- Физические свойства воды
- Вода как растворитель
Состав и строение воды
Как вы уже знаете, молекула воды состоит из трех атомов — двух атомов водорода и одного атома кислорода (рис. 105). Относительная молекулярная масса воды равна:
Следовательно, молярная масса воды равна:
Вода — это вещество с молекулярным строением. В твердом (рис. 106) и жидком агрегатных состояниях молекулы воды прочно связаны друг с другом. Этим во многом объясняется целый ряд удивительных физических свойств воды.
Физические свойства воды
При комнатных условиях вода представляет собой жидкость без вкуса и запаха. В тонком слое вода не имеет цвета. Однако при толщине более 2 м она имеет голубой цвет. Совершенно чистая вода очень плохо проводит электрический ток.
На заметку: По тому, как проводит электрический ток вода, можно судить о ее чистоте — чем ниже электропроводность, тем чище вода.
У большинства веществ в твердом состоянии плотность выше, чем в жидком. В отличие от них вода в твердом агрегатном состоянии (лед) имеет более низкую плотность, чем в жидком. При 0 °С плотность льда равна примерно 0,92 г/см3, а плотность жидкой воды — примерно 1,00 г/см3. Это означает, что лед легче воды, поэтому он не тонет в ней (рис. 107). Такая особенность воды объясняет, почему водоемы начинают замерзать не со дна, а с поверхности и очень редко промерзают до самого дна. Это защищает живые организмы, обитающие в реках и морях, от гибели.
У воды высокая теплоемкость, поэтому она медленно нагревается, но и медленно остывает. Это позволяет морям и океанам накапливать тепло летом (и днем) и высвобождать его зимой (и ночью), что предотвращает резкие колебания температуры воздуха на нашей планете в течение года (и суток). Моря и океаны служат своеобразными аккумуляторами тепла на нашей планете.
Моря и океаны служат своеобразными аккумуляторами тепла на нашей планете.
При нормальном давлении (101,3 кПа) температура кипения воды равна 100 °С. При понижении давления температура кипения воды понижается. Например, в горах на высоте около 5000 м давление существенно ниже нормального (примерно в два раза), поэтому вода закипает в этих условиях при температуре около 84 °С. Понятно, что варить продукты до готовности в горах необходимо более длительное время. И наоборот, в скороварке, где создается высокое давление, вода закипает при температуре выше 100 °С, что позволяет быстрее приготавливать пищу.
Вода как растворитель
С совершенно чистой водой, не содержащей никаких других веществ, большинство людей никогда не встречается. Такая вода используется только в специальных целях.
Почти все жидкости, с которыми мы сталкиваемся в повседневной жизни и деятельности, представляют собой растворы различных веществ.
Раствор — это однородная смесь двух и более веществ.
Одно из веществ, входящих в состав раствора, называется растворителем, а остальные — растворенными веществами. Очень часто растворителем является вода. Вода может растворять твердые, жидкие и газообразные вещества.
Все природные воды содержат растворенные соли. Их легко обнаружить экспериментально, выпарив воду на часовом стекле. Кроме солей, вода может растворять различные газы. Их присутствие (правда, не всегда) можно обнаружить экспериментально. Например, поместив пробирку с холодной водой из-под крана в теплое место, через некоторое время можно заметить у стенок пробирки пузырьки. Это растворенные газы (преимущественно кислород) выделяются из раствора при его нагревании до комнатной температуры (рис. 108).
Многие жидкости также хорошо растворимы в воде. Например, серная кислота и спирт неограниченно растворяются в воде. В таком случае говорят, что вещество смешивается с водой в любых соотношениях. Из-за хорошей растворимости многих веществ в воде ее иногда называют универсальным растворителем.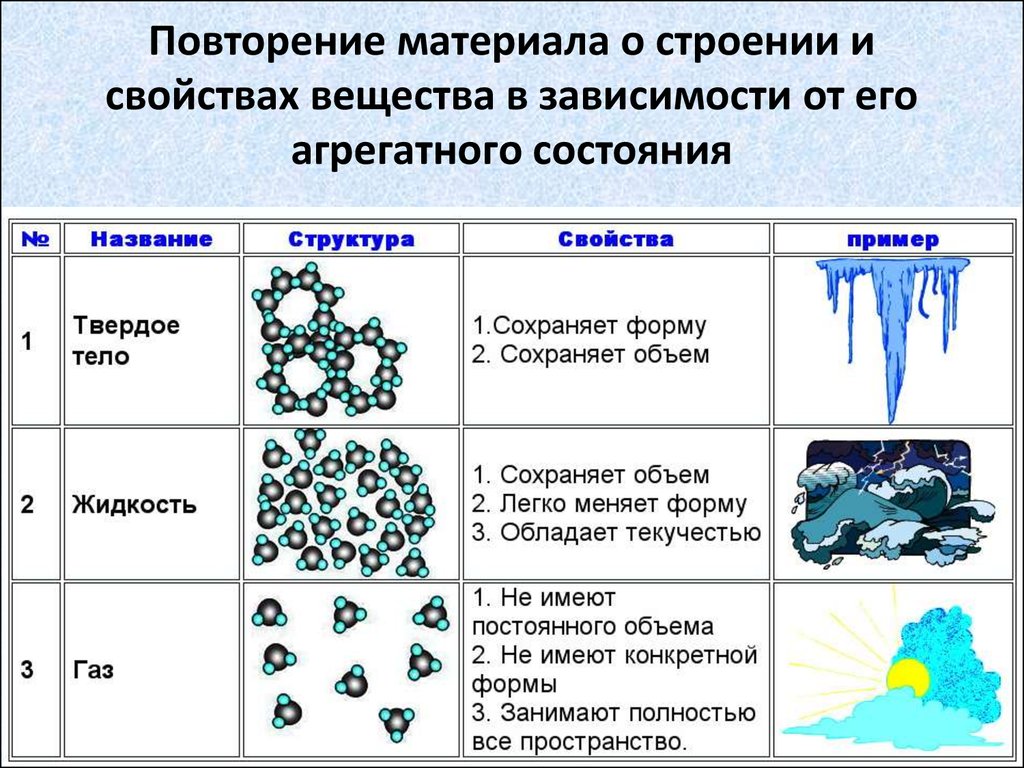
Краткие выводы урока:
- Вода не имеет вкуса, цвета (в тонком слое) и запаха, кипит при 100 °С, а переходит в твердое состояние при 0 °С.
- Плотность твердой воды меньше, чем жидкой.
- Раствор — это однородная смесь двух и более веществ.
- Вода является универсальным растворителем — она хорошо растворяет многие твердые, жидкие и газообразные вещества.
Надеюсь урок 27 «Состав и физические свойства воды» был понятным и познавательным. Если у вас возникли вопросы, пишите их в комментарии.
Урок 28. Химические свойства воды →
← Урок 26. Получение водорода и его применение
Структура и свойства воды | Водная химия оксидов
Фильтр поиска панели навигации Oxford AcademicThe Water Chemistry of OxidesInorganic ChemistryBooksJournals Термин поиска мобильного микросайта
Закрыть
Фильтр поиска панели навигации Oxford AcademicThe Water Chemistry of OxidesInorganic ChemistryBooksJournals Термин поиска на микросайте
Расширенный поиск
Иконка Цитировать Цитировать
Разрешения
- Делиться
- Твиттер
- Подробнее
CITE
Bunker, Bruce C и William H Casey,
‘Структура и свойства воды’
,
Водная химия оксидов
(
, Нью -Йорк,
2016;
онлайн онлайн. edn,
edn,
Oxford Academic
, 12 ноября 2020 г.
), https://doi.org/10.1093/oso/9780199384259.003.0008,
, по состоянию на 10 декабря 2022 г.
Выберите формат Выберите format.ris (Mendeley, Papers, Zotero).enw (EndNote).bibtex (BibTex).txt (Medlars, RefWorks)
Закрыть
Фильтр поиска панели навигации Oxford AcademicThe Water Chemistry of OxidesInorganic ChemistryBooksJournals Термин поиска мобильного микросайта
Закрыть
Фильтр поиска панели навигации Oxford AcademicThe Water Chemistry of OxidesInorganic ChemistryBooksJournals Термин поиска на микросайте
Advanced Search
Abstract
Вода — одна из самых сложных жидкостей на Земле. Даже после интенсивных исследований остается много аспектов структуры, свойств и химического состава воды, которые до конца не изучены. В этой главе мы выделяем свойства воды, которые определяют многие реакции, происходящие между водой и оксидами. Мы начинаем с одной молекулы воды и переходим к кластерам воды, а затем, наконец, к расширенным жидким и твердым фазам. Эта глава дает основу для оценки того, что происходит, когда вода сталкивается с простыми ионами, растворимыми оксидными комплексами, называемыми продуктами гидролиза, и протяженными оксидными фазами. Основным явлением, рассмотренным в этой главе, является водородная связь. Водородная связь доминирует в структуре и свойствах воды и влияет на многие взаимодействия вода-оксид. Одна молекула воды имеет восемь валентных электронов вокруг центрального аниона кислорода. Эти электроны содержатся в четырех sp3-гибридизированных молекулярных орбиталях, расположенных в виде лепестков, которые простираются от кислорода в тетраэдрической геометрии.
Даже после интенсивных исследований остается много аспектов структуры, свойств и химического состава воды, которые до конца не изучены. В этой главе мы выделяем свойства воды, которые определяют многие реакции, происходящие между водой и оксидами. Мы начинаем с одной молекулы воды и переходим к кластерам воды, а затем, наконец, к расширенным жидким и твердым фазам. Эта глава дает основу для оценки того, что происходит, когда вода сталкивается с простыми ионами, растворимыми оксидными комплексами, называемыми продуктами гидролиза, и протяженными оксидными фазами. Основным явлением, рассмотренным в этой главе, является водородная связь. Водородная связь доминирует в структуре и свойствах воды и влияет на многие взаимодействия вода-оксид. Одна молекула воды имеет восемь валентных электронов вокруг центрального аниона кислорода. Эти электроны содержатся в четырех sp3-гибридизированных молекулярных орбиталях, расположенных в виде лепестков, которые простираются от кислорода в тетраэдрической геометрии.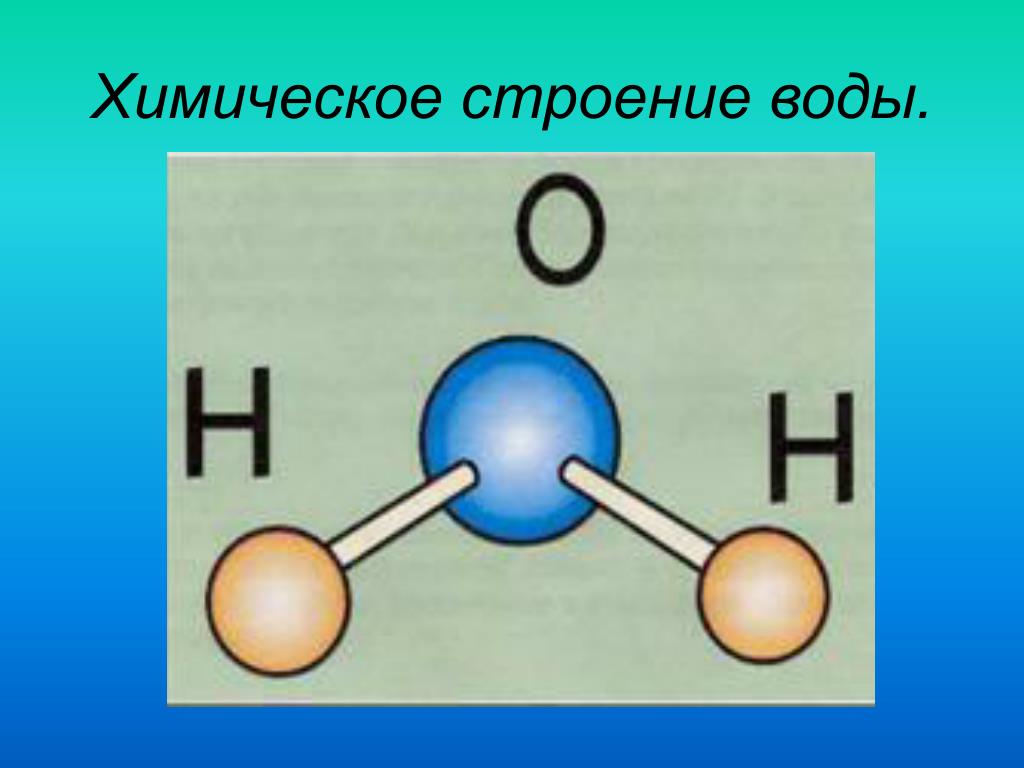
Ключевые слова: Механизм Гротгуса, амфолиты, диэлектрическая релаксация, диффузия, ион гидроксония, колебательная спектроскопия, вода
Тема
Неорганическая химия
В настоящее время у вас нет доступа к этой главе.
Войти
Получить помощь с доступом
Получить помощь с доступом
Доступ для учреждений
Доступ к контенту в Oxford Academic часто предоставляется посредством институциональных подписок и покупок. Если вы являетесь членом учреждения с активной учетной записью, вы можете получить доступ к контенту одним из следующих способов:
Доступ на основе IP
Как правило, доступ предоставляется через институциональную сеть к диапазону IP-адресов. Эта аутентификация происходит автоматически, и невозможно выйти из учетной записи с IP-аутентификацией.
Войдите через свое учреждение
Выберите этот вариант, чтобы получить удаленный доступ за пределами вашего учреждения. Технология Shibboleth/Open Athens используется для обеспечения единого входа между веб-сайтом вашего учебного заведения и Oxford Academic.
- Нажмите Войти через свое учреждение.
- Выберите свое учреждение из предоставленного списка, после чего вы перейдете на веб-сайт вашего учреждения для входа.
- При посещении сайта учреждения используйте учетные данные, предоставленные вашим учреждением. Не используйте личную учетную запись Oxford Academic.
- После успешного входа вы вернетесь в Oxford Academic.
Если вашего учреждения нет в списке или вы не можете войти на веб-сайт своего учреждения, обратитесь к своему библиотекарю или администратору.
Войти с помощью читательского билета
Введите номер своего читательского билета, чтобы войти в систему. Если вы не можете войти в систему, обратитесь к своему библиотекарю.
Члены общества
Доступ члена общества к журналу достигается одним из следующих способов:
Войти через сайт сообщества
Многие общества предлагают единый вход между веб-сайтом общества и Oxford Academic.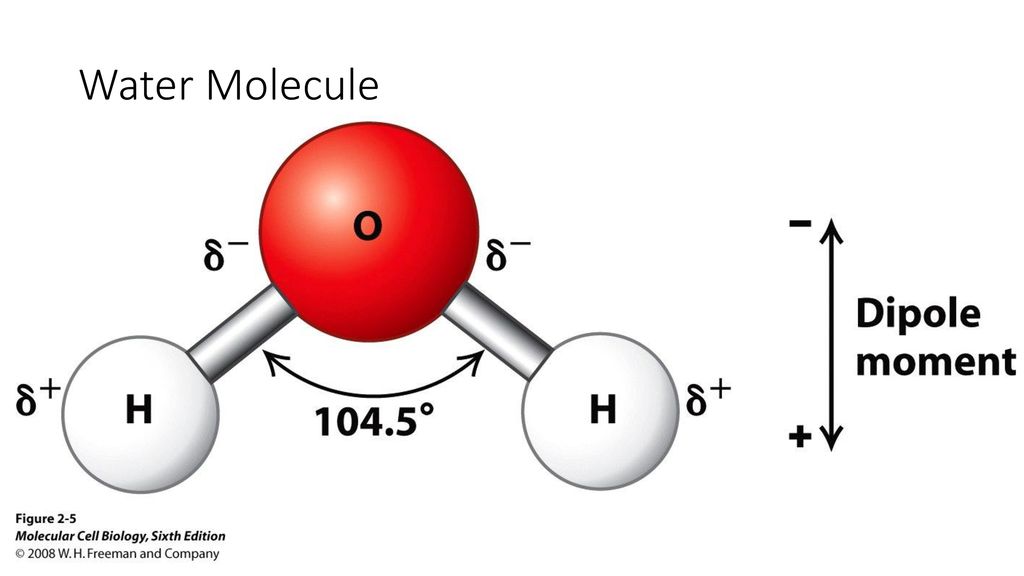 Если вы видите «Войти через сайт сообщества» на панели входа в журнале:
Если вы видите «Войти через сайт сообщества» на панели входа в журнале:
- Щелкните Войти через сайт сообщества.
- При посещении сайта общества используйте учетные данные, предоставленные этим обществом. Не используйте личную учетную запись Oxford Academic.
- После успешного входа вы вернетесь в Oxford Academic.
Если у вас нет учетной записи сообщества или вы забыли свое имя пользователя или пароль, обратитесь в свое общество.
Войти с помощью личного кабинета
Некоторые общества используют личные аккаунты Oxford Academic для предоставления доступа своим членам. Смотри ниже.
Личный кабинет
Личную учетную запись можно использовать для получения оповещений по электронной почте, сохранения результатов поиска, покупки контента и активации подписок.
Некоторые общества используют личные аккаунты Oxford Academic для предоставления доступа своим членам.
Просмотр учетных записей, вошедших в систему
Щелкните значок учетной записи в правом верхнем углу, чтобы:
- Просмотр вашей личной учетной записи и доступ к функциям управления учетной записью.
- Просмотр институциональных учетных записей, предоставляющих доступ.
Выполнен вход, но нет доступа к содержимому
Oxford Academic предлагает широкий ассортимент продукции. Подписка учреждения может не распространяться на контент, к которому вы пытаетесь получить доступ. Если вы считаете, что у вас должен быть доступ к этому контенту, обратитесь к своему библиотекарю.
Ведение счетов организаций
Для библиотекарей и администраторов ваша личная учетная запись также предоставляет доступ к управлению институциональной учетной записью. Здесь вы найдете параметры для просмотра и активации подписок, управления институциональными настройками и параметрами доступа, доступа к статистике использования и т. д.
д.
Покупка
Наши книги можно приобрести по подписке или приобрести в библиотеках и учреждениях.
Информация о покупке
Структура воды: свойства
Печать
Структура воды: свойства
Исследования показали, что кластеризация молекул воды в растворах происходит за счет так называемых водородных связей (слабое взаимодействие), которые составляют около 10% прочность ковалентной связи с водой. Это немаловажно, и для разрыва связей требуется энергия, или она выделяется при образовании водородных связей. Такие связи не являются постоянными, и происходит постоянный разрыв и восстановление связей, которые, по оценкам, длятся несколько триллионных долей секунды. Тем не менее, большая часть молекул воды в любой момент времени связана в растворе. Но эта структура приводит к другим важным свойствам воды.
В рамках данного курса мы рассмотрим только шесть из этих важных свойств:
- Теплоемкость
- Скрытая теплота (плавления и испарения)
- Тепловое расширение и плотность
- Поверхностное натяжение
- Точки замерзания и кипения
- Свойства растворителя
Как упоминалось выше, эти свойства важны для физических и биологических процессов на Земле. По сути, большое количество воды сдерживает изменения окружающей среды на поверхности Земли, а это означает, что изменения температуры поверхности Земли, например, относительно незначительны. Таким образом, высокая теплоемкость воды способствует непрерывности жизни на Земле, поскольку вода охлаждается/нагревается медленно по сравнению с сушей, способствуя сохранению и переносу тепла, сводя к минимуму экстремальные температуры и помогая поддерживать постоянную температуру тела в организмах. Однако есть и другие эффекты свойств воды. Его низкая вязкость позволяет быстрому потоку выравнивать перепады давления. Его высокое поверхностное натяжение позволяет передавать энергию ветра на поверхность моря, способствуя нисходящему смешиванию кислорода в больших водоемах, таких как океан. Кроме того, это высокое поверхностное натяжение помогает отдельным клеткам в организме сохранять свою форму и контролировать поведение при падении (вы видели «Жизнь муравья»?). Кроме того, высокая скрытая теплота испарения очень важна для переноса тепла/воды в атмосфере и является существенной составляющей переноса тепла из низких широт, где приток солнечной энергии более интенсивен, в высокие широты, испытывающие дефицит солнечной энергии.
По сути, большое количество воды сдерживает изменения окружающей среды на поверхности Земли, а это означает, что изменения температуры поверхности Земли, например, относительно незначительны. Таким образом, высокая теплоемкость воды способствует непрерывности жизни на Земле, поскольку вода охлаждается/нагревается медленно по сравнению с сушей, способствуя сохранению и переносу тепла, сводя к минимуму экстремальные температуры и помогая поддерживать постоянную температуру тела в организмах. Однако есть и другие эффекты свойств воды. Его низкая вязкость позволяет быстрому потоку выравнивать перепады давления. Его высокое поверхностное натяжение позволяет передавать энергию ветра на поверхность моря, способствуя нисходящему смешиванию кислорода в больших водоемах, таких как океан. Кроме того, это высокое поверхностное натяжение помогает отдельным клеткам в организме сохранять свою форму и контролировать поведение при падении (вы видели «Жизнь муравья»?). Кроме того, высокая скрытая теплота испарения очень важна для переноса тепла/воды в атмосфере и является существенной составляющей переноса тепла из низких широт, где приток солнечной энергии более интенсивен, в высокие широты, испытывающие дефицит солнечной энергии.
Видео: Вода — жидкость Потрясающе: ускоренный курс биологии №2 (11:16)
Потратьте несколько минут, чтобы узнать, почему вода — самое интересное и важное вещество во Вселенной.
Вода — жидкость Потрясающе: ускоренный курс биологии №2
Щелкните здесь, чтобы просмотреть стенограмму видеоролика «Вода — жидкость» вся наша планета Земля, которая встречается в природе в твердой жидкой и газообразной формах, и чтобы отпраздновать эту волшебную связь между двумя атомами водорода и одним атомом кислорода здесь, сегодня мы собираемся отпраздновать чудесные поддерживающие жизнь свойства воды, но мы собираемся сделайте это чуть более одетым. Намного лучше.
Мы остановились здесь, на ускоренном курсе биологии, мы говорим о жизни и о довольно важном факте, что вся жизнь, какой мы ее знаем, зависит от того, есть ли вокруг вода. выяснить, есть ли жизнь где-то еще, потому что вы знаете, что это самый важный вопрос, который у нас есть прямо сейчас, я был очень взволнован, когда они находят воду где-то особенно в жидкой воде, и это одна из причин, почему я и многие другие люди в декабре прошлого года, когда семилетний марсоход Opportunity обнаружил на Марсе 20-дюймовую жилу гипса, которая почти наверняка была отложена, как долгоживущая жидкая вода на поверхности Марса, и это было, вероятно, миллиарды лет назад. . И поэтому будет трудно сказать, привела ли вода, которая была там, к какой-то жизни, но, возможно, мы сможем понять это, и это было бы действительно интересно. Но почему мы думаем, что вода необходима для жизни? Почему вода на других планетах нас так чертовски волнует?
. И поэтому будет трудно сказать, привела ли вода, которая была там, к какой-то жизни, но, возможно, мы сможем понять это, и это было бы действительно интересно. Но почему мы думаем, что вода необходима для жизни? Почему вода на других планетах нас так чертовски волнует?
Итак, давайте начнем с изучения некоторых удивительных свойств воды. Чтобы сделать это, нам придется начать с этой самой популярной в мире молекулы или, по крайней мере, самой запоминающейся молекулы в мире, мы все знаем о ней, старой доброй воде. Два атома водорода один кислород каждый водород делит электрон с кислородом в том, что мы называем ковалентной связью. Итак, как вы можете видеть, вы нарисовали мою молекулу воды особым образом, и на самом деле она выглядит именно так, как будто она имеет форму буквы V, потому что этот большой атом кислорода немного более жаден к электронам. Она имеет небольшой отрицательный заряд, в то время как эта область с атомами водорода имеет небольшой положительный заряд, благодаря этой полярности все молекулы воды настолько сильно притягиваются друг к другу, что фактически слипаются, и это называется водородными связями, и мы говорили о них. в последний раз, по сути, происходит то, что положительный полюс вокруг этих атомов водорода связывается с отрицательным полюсом вокруг атомов кислорода другой молекулы воды, и поэтому это слабая связь, но посмотрите, они связаны серьезно, я не могу переоценить важность этой водородной связи. поэтому, когда ваш учитель спросит вас, что важно в воде, начните с водородных связей, и вы должны поместить ее во все промежутки и, возможно, несколько блесток вокруг нее. Когезия поверхностного натяжения — это притяжение между такими вещами, как притяжение между одной молекулой воды и другой молекулой воды. самое высокое сцепление любой неметаллической жидкости, и вы можете увидеть это, если налейте немного воды на вощеную бумагу, или на тефлон, или на что-то еще, где вода собирается в бусинки, вот так некоторые листья растений делают это очень хорошо. Это довольно круто, так как вода слабо прилипает к вощеной бумаге или к растению, но сильно прилипает к самой себе, молекулы воды удерживают эти капли вместе в конфигурации, которая создает наименьшую площадь поверхности.
в последний раз, по сути, происходит то, что положительный полюс вокруг этих атомов водорода связывается с отрицательным полюсом вокруг атомов кислорода другой молекулы воды, и поэтому это слабая связь, но посмотрите, они связаны серьезно, я не могу переоценить важность этой водородной связи. поэтому, когда ваш учитель спросит вас, что важно в воде, начните с водородных связей, и вы должны поместить ее во все промежутки и, возможно, несколько блесток вокруг нее. Когезия поверхностного натяжения — это притяжение между такими вещами, как притяжение между одной молекулой воды и другой молекулой воды. самое высокое сцепление любой неметаллической жидкости, и вы можете увидеть это, если налейте немного воды на вощеную бумагу, или на тефлон, или на что-то еще, где вода собирается в бусинки, вот так некоторые листья растений делают это очень хорошо. Это довольно круто, так как вода слабо прилипает к вощеной бумаге или к растению, но сильно прилипает к самой себе, молекулы воды удерживают эти капли вместе в конфигурации, которая создает наименьшую площадь поверхности. Именно это высокое поверхностное натяжение позволяет некоторым жукам и даже мне подумайте, что одна ящерица, а также один Иисус могут ходить по тому, что Кюи силы воды делает в своих пределах.
Именно это высокое поверхностное натяжение позволяет некоторым жукам и даже мне подумайте, что одна ящерица, а также один Иисус могут ходить по тому, что Кюи силы воды делает в своих пределах.
Конечно, есть и другие вещества, к которым вода прилипает. Возьмем, к примеру, стекло, это называется адгезией, и вода здесь растекается, а не бьется, потому что силы сцепления между водой и стеклом сильнее, чем силы сцепления отдельных молекул воды в капельке воды. Адгезия — это притяжение между водой и стеклом. два разных вещества, так что в этом случае молекулы воды и молекулы стекла эти свойства приводят к одной из моих любимых вещей в воде — тому факту, что она может бросить вызов гравитации. Эта действительно крутая вещь, которая только что произошла, называется капиллярным действием, и ее можно легко объяснить тем, что мы теперь знаем о когезии и адгезии, благодаря адгезии молекулы воды притягиваются к молекулам в соломинке, но когда молекулы воды прилипают к соломинке. другие молекулы втягиваются за счет когезии вслед за другими молекулами воды, благодаря когезии, поверхностное натяжение, созданное здесь, заставляет воду подниматься вверх по соломинке, и она будет продолжать подниматься до тех пор, пока в конечном итоге гравитация не потянет вниз вес воды, и соломинка не преодолеет силу. поверхностное натяжение. Тот факт, что вода является полярной молекулой, также делает ее действительно хорошей растворяющей жидкостью.
поверхностное натяжение. Тот факт, что вода является полярной молекулой, также делает ее действительно хорошей растворяющей жидкостью.
Это хороший растворитель, заметьте, что вода не очень хороший растворитель, это потрясающий растворитель! Есть больше веществ, которые можно растворить в воде, чем в любой другой жидкости на Земле, и да, это включает в себя самую сильную кислоту, которую мы когда-либо создавали. Эти вещества, которые растворяются в воде, — это сахар или соль, и те, с которыми мы знакомы, называются гидрофильными. и они гидрофильны, потому что они полярны, и их полярность сильнее, чем силы сцепления стенки, поэтому, когда вы помещаете одно из этих полярных веществ в воду, оно достаточно сильное, чтобы разрушить все небольшие силы сцепления. Все эти маленькие водородные связи, и вместо водородных связей друг с другом вода будет водородной связью вокруг этих полярных веществ. Поваренная соль является ионом, и прямо сейчас она разделяется на ионы, поскольку полюса наших молекул воды взаимодействуют с ней, но что происходит, когда есть молекула, которая не может разрушить силы сцепления воды, она не может проникнуть в нее и проникнуть в нее, в основном, что происходит, когда это вещество не может преодолеть сильные силы сцепления воды и не может проникнуть внутрь воды? Вот и получается то, что мы называем гидрофобным веществом или будто бы чем-то, что боится воды.
Эти молекулы лишены заряженных полюсов они неполярны и не растворяются в воде, потому что по существу они выталкиваются из воды силами сцепления воды воду мы можем назвать универсальным растворителем но это не значит что она растворяет все что есть В истории было много эксцентричных ученых, но все эти разговоры о воде заставили меня задуматься о, пожалуй, самом эксцентричном из эксцентриков человеке по имени Генри Кавендиш, он общался со своими служанками только с помощью записок и добавил лестницу к задней части своего дома, чтобы избегать контакта с его домработницей. Некоторые считают, что он, возможно, страдал от формы аутизма, но почти каждый признает, что он был научным гением. Его лучше всего помнят как первого человека, распознавшего газообразный водород как отдельное вещество и определившего состав воды в 1700-х годах. Большинство людей думали, что вода сама по себе является элементом, но Кавендиш заметил, что водород, который он назвал горючим воздухом, реагировал с кислородом, известным тогда как Устрашающее название размораживания закрытого воздуха для образования воды. Кавендиш не совсем понял, что он здесь открыл, отчасти потому, что он не верил в химические соединения. Он объяснил свои эксперименты с водородом с точки зрения огнеподобного элемента, называемого флогистоном. гравитация в основном сравнительная плотность водорода и других газов по отношению к обычному воздуху это особенно впечатляет, если учесть грубые инструменты, с которыми он работал, например, это то, с чем он делал свой газообразный водород, он продолжал не только устанавливать точный состав атмосферу, но и открыл плотность земли неплохо для парня, который был настолько болезненно застенчив, что единственный существующий его портрет был нарисован без его ведома, так что за все его десятилетия экспериментов было опубликовано всего около 20 работ в годы после его Исследователи смерти выяснили, что Кавендиш на самом деле открыл закон Рихтера, закон Ома, закон Кулона и несколько других законов. законов, это много чертовых законов, и если бы он получил признание за них все, нам пришлось бы иметь дело с восьмым недостатком Кавендиша и четвертым законом Кавендиша.
Кавендиш не совсем понял, что он здесь открыл, отчасти потому, что он не верил в химические соединения. Он объяснил свои эксперименты с водородом с точки зрения огнеподобного элемента, называемого флогистоном. гравитация в основном сравнительная плотность водорода и других газов по отношению к обычному воздуху это особенно впечатляет, если учесть грубые инструменты, с которыми он работал, например, это то, с чем он делал свой газообразный водород, он продолжал не только устанавливать точный состав атмосферу, но и открыл плотность земли неплохо для парня, который был настолько болезненно застенчив, что единственный существующий его портрет был нарисован без его ведома, так что за все его десятилетия экспериментов было опубликовано всего около 20 работ в годы после его Исследователи смерти выяснили, что Кавендиш на самом деле открыл закон Рихтера, закон Ома, закон Кулона и несколько других законов. законов, это много чертовых законов, и если бы он получил признание за них все, нам пришлось бы иметь дело с восьмым недостатком Кавендиша и четвертым законом Кавендиша. Так что я лично рад, что он на самом деле не получил кредит.
Так что я лично рад, что он на самом деле не получил кредит.
Прямо сейчас мы проведем довольно удивительную науку, вы, ребята, не поверите, хорошо, вы готовы, он плывет. Да, я знаю, что вы не удивлены этим, но вы должны быть удивлены, потому что все остальное, когда оно твердое, гораздо более плотное, чем когда оно жидкое, точно так же, как газы намного менее плотны, чем жидкости, но та простая характеристика воды, что она плавает в твердой форме, одна из причин, почему жизнь на этой планете, какой мы ее знаем, возможна, и почему твердая вода менее плотна, чем жидкая вода, в то время как все остальное является полной противоположностью этому. Что ж, вы можете поблагодарить свои водородные связи еще раз, так что при температуре около 32 градусов по Фаренгейту или нулю градусов по Цельсию, если вы ученый или из той части мира, где все имеет смысл, молекулы воды начинают затвердевать, и образуются водородные связи в этих молекулах воды. кристаллические структуры, которые распределяют молекулы более равномерно, что, в свою очередь, делает замороженную воду менее плотной, чем ее жидкая форма, поэтому почти во всех случаях плавающий водяной лед — это действительно хорошо, если я клянусь, что он плотнее воды, он замерзнет, а затем утонет, а затем замерзнет, чем утонет чем замерзнуть, чем утонуть, так что просто поверьте мне в этом, вы не хотите жить в мире, где я тону, это не только нанесет полный ущерб водным экосистемам, которые в основном являются тем, как жизнь сформировалась на земле, в первую очередь, это также Вы знаете, что весь лед и Северный полюс утонут, а затем вся вода повсюду поднимется, и у нас не будет земли, которая будет раздражать.
Есть еще одно удивительное свойство воды, о котором я забыл, так почему здесь так жарко. О, теплоемкость, да, у воды очень высокая теплоемкость, и, вероятно, это ничего не значит для вас, но в основном это означает, что вода действительно хорошо удерживает тепло, поэтому мы любим класть грелки в нашу кровать и с ними, когда мы вы одиноки, но кроме того, что вы искусственно согреваете свою постель, также очень важно, что океаны трудно нагревать и охлаждать, они становятся гигантскими поглотителями тепла, которые регулируют температуру и климат нашей планеты, поэтому, например, это намного приятнее. в Лос-Анджелесе, где температура океана постоянно держится на одном уровне, и, скажем, в Небраске в меньшем масштабе, мы можем очень легко и визуально увидеть высокую теплоемкость воды, поставив кастрюлю без воды на плиту и увидев, как плохо это проходит, но затем вы добавляете в него немного воды, и он кипит, черт возьми, целую вечность, о, и если вы еще этого не заметили, или когда вода испаряется с вашей кожи, она охлаждает вас теперь, это принцип за потоотделением, которое является чрезвычайно эффективной, хотя и несколько смущающей частью жизни, но это пример еще одной невероятно крутой вещи о воде, когда мое тело нагревается, и оно потеет, что тепло возбуждает некоторые молекулы воды на моей коже до такой степени, что они ломаются эти водородные связи и они испаряются, и когда они убегают, они забирают эту тепловую энергию с собой, оставляя меня прохладнее, прекрасно, это не было упражнением, хотя я не знаю, почему так сильно потею, это может быть пульверизатор, которым я продолжаю опрыскивать себя она, может быть, это просто потому, что это такое предприятие с высоким уровнем стресса, пытающееся научить вас людям вещам, я думаю, мне нужно немного воды, но пока я пью, а есть обзор всех вещей, о которых мы говорили сегодня, если у вас есть пара вещи, в которых вы не совсем уверены, просто вернитесь и посмотрите их, это не займет у вас много времени, и вы станете умнее.


 RU
RU