Электролиз расплавов и растворов — схема, правила и уравнения
Электролиз расплавов и растворов встречается в заданиях на ЕГЭ, а значит, если вы планируете сдавать экзамен по химии, эту тему нужно знать на отлично. Наша статья поможет узнать или повторить, что такое электролиз, его правила и схема протекания.
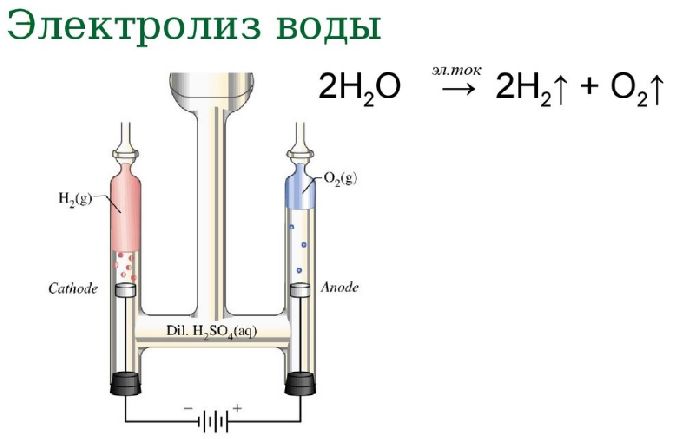
Электролиз — это окислительно-восстановительная реакция, которая протекает на электродах и основана на пропускании электрического тока через раствор или расплав.
Не менее важными участниками электролиза являются электроды: катод и анод. Если вы вдруг забыли, что такое катод и анод в химии, напомним.
Катод — это отрицательно заряженный электрод, который притягивает положительно заряженные ионы (катионы). А анод — это положительно заряженный электрод, который притягивает к себе отрицательно заряженные ионы (анионы). Таким образом, на катоде всегда происходит процесс восстановления, а на аноде всегда происходит процесс окисления.
Таким образом, на катоде всегда происходит процесс восстановления, а на аноде всегда происходит процесс окисления.
Электроды бывают растворимые и инертные. Растворимые изготавливаются из металлов, например, меди и подвергаются химическим превращениям в ходе электролиза. А вот инертные или нерастворимые электроды не подвергаются химическим превращениям и остаются в неизменном виде как до реакции, так и после нее. Как правило, такие электроды изготавливают из графита или платины.
Виды электролиза
Различают два вида электролиза:
Электролиз расплава.
Электролиз водного раствора.
Прежде чем мы рассмотрим каждый процесс отдельно, давай познакомимся с общими для двух видов процессами на электродах.
Процесс на катоде K (−) Катион принимает электроны и восстанавливается: Me+n + ne− → Me0 (восстановление). Процесс на аноде A (+) Анион отдает электроны и окисляется: неMe−n − ne− → неMe0 (окисление). К− : Ме+n + ne− → Ме0; А+ : неМе−n − ne− → неМе0. Суммарное уравнение электролиза: |
|---|
Практикующий детский психолог Екатерина Мурашова
Бесплатный курс для современных мам и пап от Екатерины Мурашовой. Запишитесь и участвуйте в розыгрыше 8 уроков
Электролиз расплава
Рассмотрим электролиз расплава пищевой соли — хлорида натрия. При сильном нагревании кристаллический твердый хлорид натрия плавится. Полученный расплав содержит подвижные ионы хлора и натрия, освободившиеся из кристаллической решетки, и проводит электрический ток.
К−: 2Na+ + 2e− = 2Na0
А+: 2Cl− − 2e− = Cl2
Суммарное уравнение электролиза:
При опускании в расплав угольных (инертных) электродов, присоединенных к источнику тока, ионы приобретают направленное движение: катионы движутся к отрицательно заряженному электроду (катоду), анионы — к положительно заряженному электроду (аноду) и отдают электроны.
Теперь давайте рассмотрим электролиз расплава гидроксида калия.
На катоде происходит восстановление калия за счет принятия электронов. А на аноде протекает более сложная реакция. Гидроксогруппы отдают свой электрон и становятся нейтральными, но такое состояние для них крайне невыгодно, так как неустойчиво, и они объединяются в группы, чтобы потом разложиться с выделением газообразного кислорода и воды
Итог электролиза расплава — металлический калий на катоде, газообразный кислород и пары воды на аноде.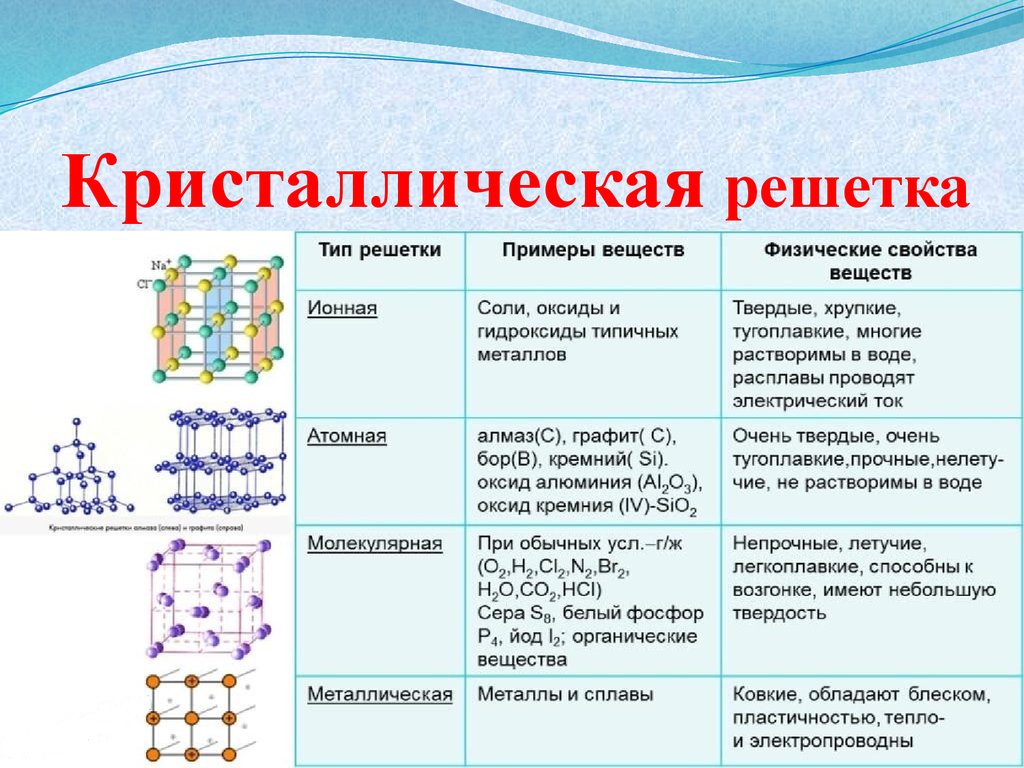
Электролиз раствора
Основным отличием водного раствора от расплава является присутствие молекул воды и ионов H+ и OH— как продуктов диссоциации воды. В связи с этим возле катода и анода скапливаются ионы, которые конкурируют как друг с другом, так и с молекулами воды. Рассмотрим электролиз на примере водного раствора KF:
К−: 4H2O + 4e− = 2H20 + 4OH−
А+: 2H2O − 4e− = O2 + 4H+
Суммарное уравнение электролиза:
Как видно, ни калий, ни фтор не фигурируют в продуктах электролиза. Почему так происходит?
Наиболее активные металлы — сильные восстановители. Калий — как раз такой металл, поэтому обратный процесс восстановления активных металлов из соединений осуществить сложно. При электролизе водных растворов солей активных металлов на катоде протекает восстановление не катионов этих металлов, а воды с образованием водорода.
Разберем порядок восстановления катионов металлов на катоде в зависимости от их активности.
Последовательность разрядки катионов зависит от положения металла в электрохимическом ряду напряжения.
Если у катода накапливаются молекулы воды и катионы металла, который находится в ряду напряжения после водорода, то восстанавливаются ионы металла.
Если у катода накапливаются молекулы воды и катионы металла, который стоит в начале ряда напряжения от лития до алюминия включительно, то восстанавливаются ионы водорода из молекул воды. Катионы металла не восстанавливаются, остаются в растворе.
Если у катода накапливаются молекулы воды и катионы металла, который расположен в ряду напряжения между алюминием и водородом, то восстанавливаются и ионы металла, и частично ионы водорода из молекул воды.

Если в растворе находится смесь катионов разных металлов, то сначала восстанавливаются катионы менее активного металла.
При электролизе раствора кислоты на катоде восстанавливаются катионы водорода до газообразного водорода.
Для удобства мы собрали информацию об электролизе в таблице:
Теперь разберемся, что происходит с анионами в водных растворах при электролизе. Для начала познакомимся с последовательностью восстановления анионов на аноде:
Чем меньше выражена восстановительная активность, тем хуже анионы могут окисляться на аноде. К тому же процесс на аноде зависит от материала анода и от природы аниона.
Если анод инертный или нерастворимый, то на нем протекают следующие реакции:
При электролизе растворов солей бескислородных кислот (кроме фторидов!), на аноде происходит процесс окисления аниона.

При электролизе растворов солей кислородсодержащих кислот и фторидов на аноде выделяется газообразный кислород вследствие окисления молекул воды. Анион при этом не окисляется, оставаясь в растворе.
При электролизе растворов щелочей происходит окисление гидроксид-ионов.
Если анод растворимый, то на нем всегда происходит окисление металла анода — независимо от природы аниона.
Исключением является электролиз солей карбоновых кислот. Таблица выше не описывает происходящее на аноде. Давайте рассмотрим, что же там происходит.
В общем виде электролиз солей карбоновых кислот можно записать так:
На катоде образуется газообразный водород, а на аноде — углекислый газ, углеводород, полученный удвоением радикала. В катодном пространстве накапливается щелочь.
В катодном пространстве накапливается щелочь.
В случае разделения катодного и анодного пространства углекислый газ реагирует со щелочью с образованием гидрокарбоната.
Бесплатные занятия по английскому с носителем
Занимайтесь по 15 минут в день. Осваивайте английскую грамматику и лексику. Сделайте язык частью жизни.
Применение электролиза
А теперь самое главное: зачем вообще нужен электролиз? Рассмотрим применение этого вида ОВР:
С помощью электролиза расплавов природных соединений в металлургической промышленности получают активные металлы (калий, натрий, бериллий, кальций, барий). С помощью электролиза растворов солей — цинк, кадмий, кобальт и другие.
В химической промышленности электролиз используют для получения фтора, хлора, водорода, кислорода, щелочей, бертолетовой соли и других веществ.
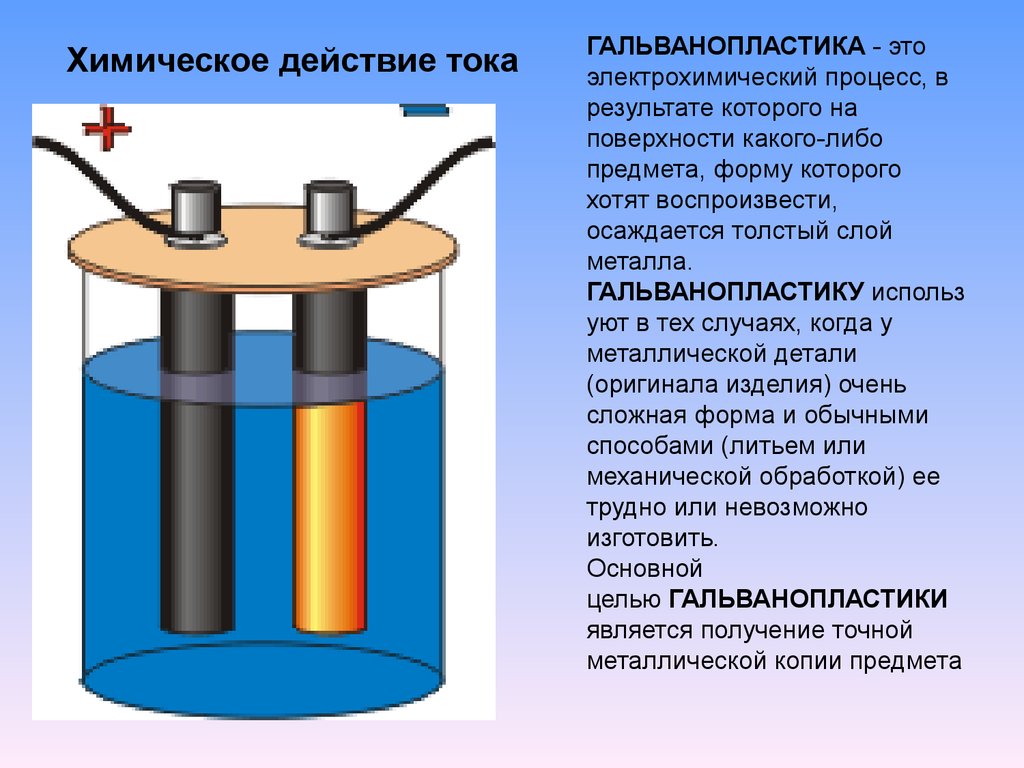
Электролиз с растворимым анодом используют для нанесения металлических покрытий (из хрома, золота, никеля, серебра), что предохраняет металлические изделия от коррозии и придает им декоративный вид.

Вопросы для самопроверки
1. Выберите верное продолжение фразы «катод — это…»:
Положительно заряженный электрод, к которому притягиваются положительно заряженные ионы.
Положительно заряженный электрод, к которому притягиваются отрицательно заряженные ионы.
Отрицательно заряженный электрод, к которому притягиваются положительно заряженные ионы.
Отрицательно заряженный электрод, к которому притягиваются отрицательно заряженные ионы.
2. Продолжите фразу «электролиз — это…»:
ОВР с применением тока.
Реакция без изменения степеней окисления с применением тока.
ОВР с применением катализаторов.

Обменная реакция.
3. Как заряжен анион?
Положительно.
Отрицательно.
Нейтрально.
Не имеет заряда.
4. Чем отличается электролиз раствора от электролиза расплава?
Ничем.
В расплаве плавится твердое.
Присутствием молекул воды и продуктов ее диссоциации.
5. Если металл стоит в ряду активности металлов между алюминием и водородом, что выделится на катоде?
Этот металл.
Водород.
Металл и водород.

Оксид металла.
При электролиза водного раствора фторида лития что на аноде выделится?
Фтор.
Водород.
Кислород.
Вода.
Ответы
c
a
b
c
c
с
ТВЕРДЫЕ ОКСИДНЫЕ ЭЛЕКТРОЛИТЫ — НОВЫЕ ГОРИЗОНТЫ ЭЛЕКТРОХИМИИ
В 1820 году Ханс Кристиан Эрстед обнаружил магнитное действие электрического тока.
Растворы кислот, щелочей и солей образуют электролит — смесь положительных катионов (черные кружки) и отрицательных анионов (белые).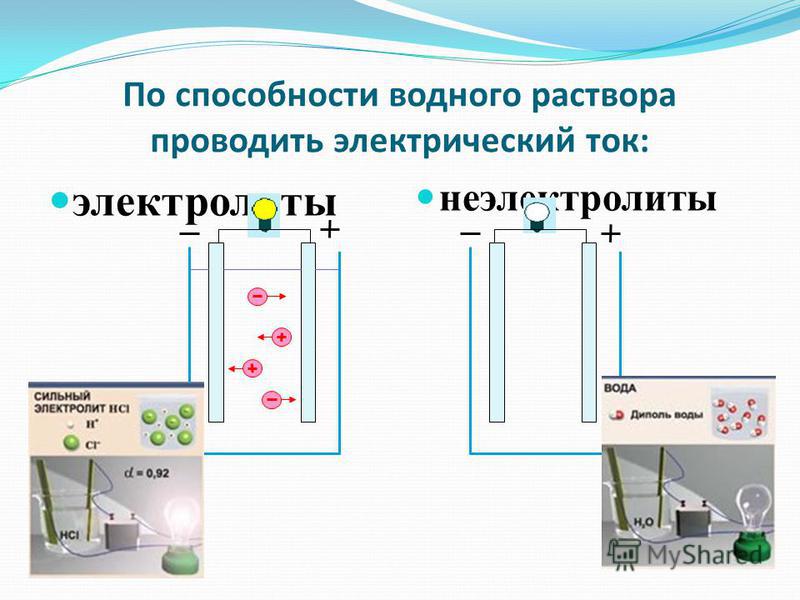
Двумерная решетка соединения типа MG<sub>2</sub>(например, ZrО<sub>2</sub>)(А).
Модель типичного ионного кристалла — знакомой всем поваренной соли NaCl (А).
Схема электрохимического устройства.
На основе твердых оксидных электролитов можно создавать разные электрохимические устройства.
‹
›
Открыть в полном размере
Жидкие электролиты — водные растворы, или
расплавы, солей, кислот и оснований — известны
давно. Они работают в аккумуляторах и
«сухих» батарейках, применяются для
получения и очистки металлов, щелочей,
органических соединений, для никелирования и
анодирования. Свойства жидких электролитов
знакомы многим — их изучают даже в школе. Но есть
еще один класс подобных веществ — так называемые
твердые электролиты. Знают о них в основном
только специалисты-химики, история их изучения
коротка, широкое применение только начинается.
Твердые электролиты связывают в основном с
надеждой создать легкий и емкий аккумулятор для
электромобиля.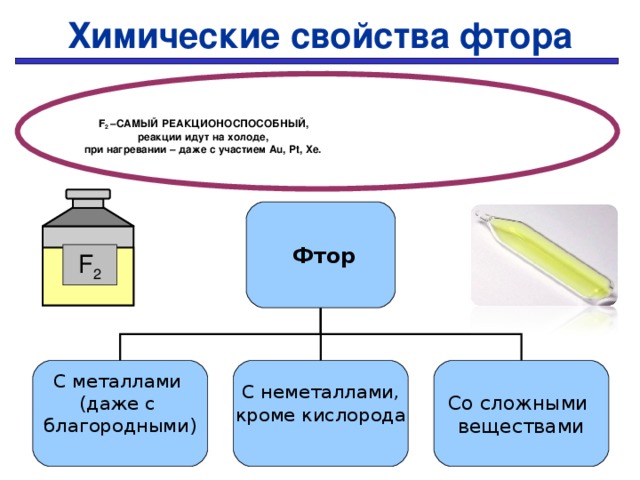 Сегодня аккумулятор массой 50-60
килограммов способен запасти гораздо меньше
энергии, чем ее «хранится» в бензобаке.
Источник тока на твердом электролите, над
созданием которого работают ведущие компании
мира, по удельной энергоемкости обещает
сравняться с топливом.
Сегодня аккумулятор массой 50-60
килограммов способен запасти гораздо меньше
энергии, чем ее «хранится» в бензобаке.
Источник тока на твердом электролите, над
созданием которого работают ведущие компании
мира, по удельной энергоемкости обещает
сравняться с топливом.
Спектр применения твердых электролитов очень широк. На их основе можно делать «вечные» печи и источники света, анализаторы газов, устройства для получения чистого кислорода, генераторы электричества и многое другое. Будущее твердых электролитов представляется весьма многообещающим, поэтому знать о них следует.
Электролиты
В конце прошлого века Вальтер Нернст, известный
немецкий исследователь, много сделавший для
развития электрохимии, использовал в
осветительных лампах спресованную смесь оксидов
циркония и кальция. Электрический ток, проходя
через стерженек из этой «массы Нернста»,
нагревал его до белого каления. Так нашел свое
первое практическое применение твердый
электролит.
Так нашел свое
первое практическое применение твердый
электролит.
Как известно, в металлах электрический ток создают покинувшие свои атомы, то есть свободные, электроны. В электролитах это делают другие заряженные частицы — ионы — целые атомы с недостающими электронами (положительные ионы, катионы) или с лишними (отрицательные ионы, анионы).
Если в жидкий электролит погрузить два электрода и приложить напряжение, то в электролите возникнет ток, направленное движение ионов: катионы пойдут к отрицательному («-«) электроду, к катоду; анионы — к положительному («+»), к аноду.
Возможен и обратный процесс: если погрузить в
жидкий электролит два электрода из определенным
образом подобранных металлов, то на одном из них
в результате химических реакций появится
избыток электронов («-«), а на другом -
недостаток («+»). Между электродами будет
действовать электродвижущая сила, и, значит, вся
система электроды -электролит превратится в
химический генератор электрического тока. Так
работал первый химический источник тока -
гальванический элемент из медной и цинковой
пластин, погруженных в раствор поваренной соли
или серной кислоты. Так работают все нынешние
гальванические элементы, батарейки и
аккумуляторы.
Так
работал первый химический источник тока -
гальванический элемент из медной и цинковой
пластин, погруженных в раствор поваренной соли
или серной кислоты. Так работают все нынешние
гальванические элементы, батарейки и
аккумуляторы.
В принципе то же самое происходит в химических электрогенераторах с твердыми электролитами.
Особенности твердых электролитов
Твердых электролитов известно великое множество — это оксиды, соли, кислоты и даже полимеры. В твердых растворах оксидов металлов разной валентности ток создается отрицательными ионами (анионами) кислорода.
Большинство этих твердых растворов — ионные кристаллы: в узлах кристаллической решетки находятся не нейтральные атомы, а заряженные ионы. Они образуют две подрешетки — катионную и анионную. Ионы совершают колебательные движения, но перемещаться по кристаллу, как в жидкости, не могут. Как же тогда в твердых электролитах возникает ток — движение заряженных частиц?
Ситуация меняется, если основное вещество
«разбавить» другим похожим соединением, в
котором анионов меньше, а катионов — столько же.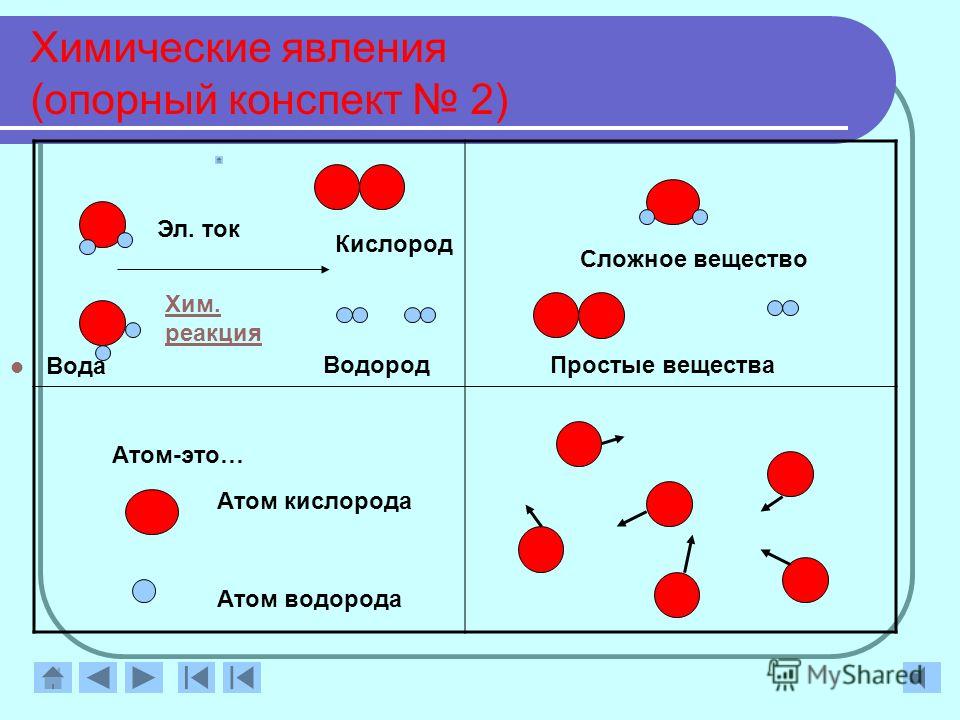 Тогда катионная решетка этого твердого раствора
остается прежней, а в анионной появляются
свободные места — вакансии. Пустые места в
отрицательно заряженной решетке можно
рассматривать как положительные заряды. Под
действием внешнего напряжения в них начнут
переходить анионы с
достаточно большой энергией, а вакансии
«побегут» в противоположном направлении — к
катоду. Возникнет электрический ток,
обусловленный движением ионов только одного
сорта. Это одна из особенностей твердых
электролитов.
Тогда катионная решетка этого твердого раствора
остается прежней, а в анионной появляются
свободные места — вакансии. Пустые места в
отрицательно заряженной решетке можно
рассматривать как положительные заряды. Под
действием внешнего напряжения в них начнут
переходить анионы с
достаточно большой энергией, а вакансии
«побегут» в противоположном направлении — к
катоду. Возникнет электрический ток,
обусловленный движением ионов только одного
сорта. Это одна из особенностей твердых
электролитов.
Ионная проводимость тем выше, чем больше в кристалле вакансий. Однако с ростом их количества уменьшается подвижность анионов, причем довольно быстро, поэтому проводимость сначала достигает максимума, а потом начинает падать. Для твердых оксидных электролитов на основе ZrO2, например, максимум электропроводности соответствует концентрации катионов 10-15%.
Свойства твердых оксидных электролитов
Анионы с достаточной кинетической энергией
есть всегда, но при комнатной температуре их
очень мало, и твердые оксидные электролиты ведут
себя как хороший изолятор.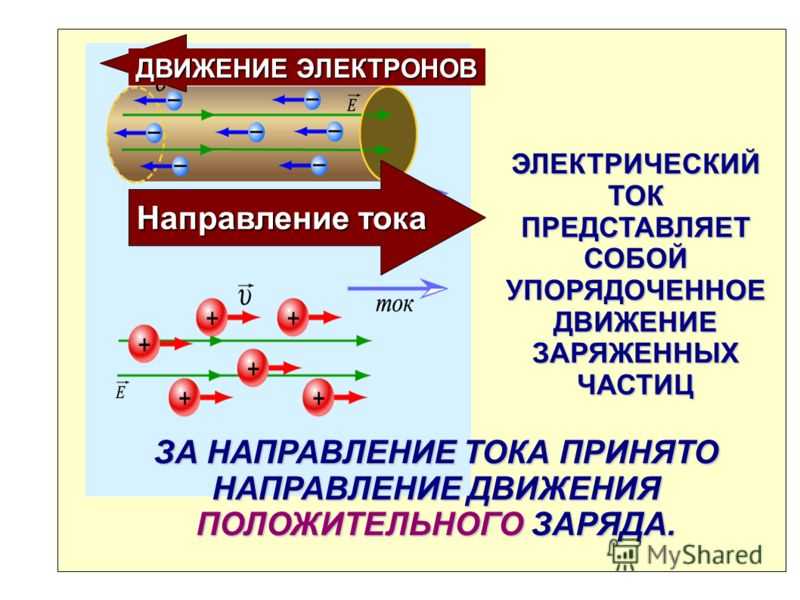 По мере нагрева
подвижность анионов увеличивается очень быстро,
и при 150оС проводимость электролитов
становится уже вполне ощутимой. Но основная их
рабочая температура лежит между 700 и 1000оС, в
связи с чем они и называются
высокотемпературными электролитами.
По мере нагрева
подвижность анионов увеличивается очень быстро,
и при 150оС проводимость электролитов
становится уже вполне ощутимой. Но основная их
рабочая температура лежит между 700 и 1000оС, в
связи с чем они и называются
высокотемпературными электролитами.
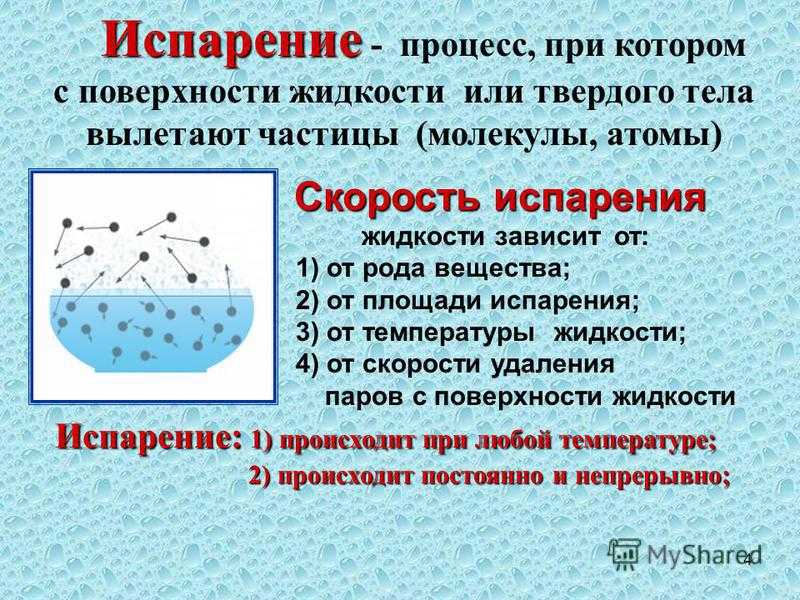
Твердые электролиты всегда находятся в атмосфере определенных газов, состав которой меняет их свойства. Чтобы понять, в чем тут дело, вспомним, что такое динамическое равновесие. В жидкости, например, всегда есть «быстрые» молекулы, которые с ее поверхности переходят в пар. Но и из пара молекулы возвращаются в жидкость — между ними происходит непрерывный обмен молекулами. Пар находится в равновесии с жидкостью, и, чтобы подчеркнуть, что оно сопряжено с движением на молекулярном уровне, его называют динамическим.
Характер обмена между твердым телом и газом
сложнее. Ион кислорода в поверхностном слое
превращается в нейтральный атом. Два атома
соединяются в молекулу кислорода, которая
отрывается от поверхности и переходит в газ.
Возвращение кислорода из газа в твердое тело
происходит в обратном порядке. Обе эти реакции
идут одновременно: между электролитом и газом,
содержащим определенное количество кислорода,
существует динамическое равновесие. Оно
нарушается, когда концентрация кислорода в газе
меняется.
Два атома
соединяются в молекулу кислорода, которая
отрывается от поверхности и переходит в газ.
Возвращение кислорода из газа в твердое тело
происходит в обратном порядке. Обе эти реакции
идут одновременно: между электролитом и газом,
содержащим определенное количество кислорода,
существует динамическое равновесие. Оно
нарушается, когда концентрация кислорода в газе
меняется.
Немного истории
Итак, твердый электролит в виде смеси оксидов
циркония и кальция проводит ток только при
высоких температурах. Поэтому лампы Нернста
включали, предварительно сильно прогрев их
стержень. И появление в 1905 году лампы
«немедленного действия» с вольфрамовой
нитью предопределило ее абсолютный успех. Однако
известно, что кое-где и сегодня можно встретить
странный электрический фонарь, который нужно
поджигать спичкой. Это, судя по всему, лампы Нернста, дожившие до
наших дней: твердые растворы на основе диоксида
циркония — исключительно стойкие вещества, они
могут работать на воздухе десятилетиями, не
окисляясь. Кстати, вполне современные печи с
такими нагревателями были разработаны в
свердловском Восточном институте огнеупоров в
начале 80-х годов.
Кстати, вполне современные печи с
такими нагревателями были разработаны в
свердловском Восточном институте огнеупоров в
начале 80-х годов.
Главное предназначение твердых оксидных
электролитов виделось в создании топливных
элементов — химических источников тока, в которых
энергия газа непосредственно превращается в
электрическую. Топливные элементы — близкие
родственники гальванических элементов. Но те
служат, пока в их электролите и электродах есть
активные вещества, а топливные элементы могут
работать сколь угодно долго, пока к ним
подводится горючее. Систематические
исследования твердых оксидных электролитов
начались в Германии в начале 50-х годов, а с конца
50-х развернулись в СССР, США и Канаде. В нашей
стране эти работы с самого начала вел Институт
химии Уральского филиала АН СССР (Свердловск,
ныне Екатеринбург), и школа высокотемпературной
электрохимии твердых электролитов, созданная на
Урале, стала уникальной по широте охвата
проблемы и глубине ее изучения.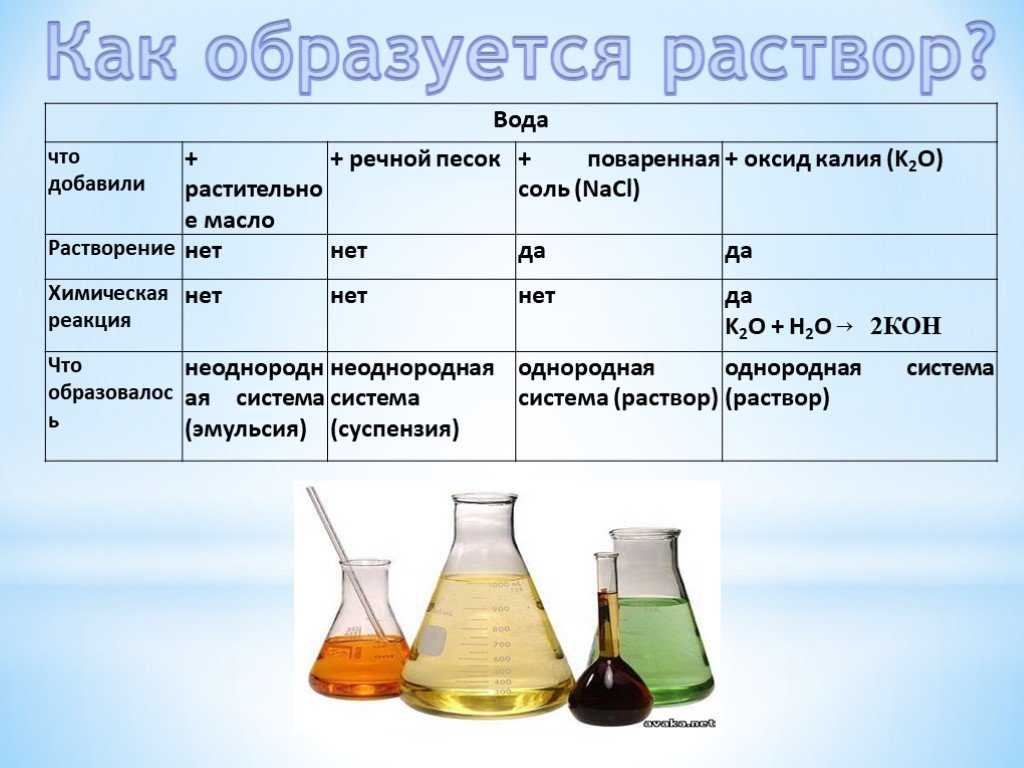
Устройства с твердыми оксидными электролитами
Конструкций, в основе которых лежат твердые оксидные электролиты, запатентовано очень много, но принцип их действия одинаков и довольно прост. Это пробирка с парой электродов на стенке, снаружи и внутри. Она помещена в нагреватель; внутрь пробирки и в пространство, ее окружающее, можно подводить газ. Посмотрим, какие функции могут выполнять такие устройства.
Потенциометрические датчики состава газа. Наверное, они наиболее просты. Мы уже знаем, что электроды в разных газах приобретают разные потенциалы. Если, скажем, внутри пробирки находится чистый кислород, а снаружи — газ с неизвестной его концентрацией, то по разности потенциалов электродов можно эту концентрацию определить.
Потенциометрические датчики позволяют
определять состав и более сложных газовых
смесей, содержащих углекислый и угарный газы,
водород и водяной пар. Если стерженек из твердого
электролита с электродами на торцах нагрет
неравномерно, он начнет терять кислород и между
электродами возникнет разность потенциалов. По
ее величине можно определить, например, состав
выхлопных газов автомобильного двигателя. На
Западе, где требования к чистоте выхлопных газов
очень строги, такие датчики выпускаются
миллионами. У нас же на такие «пустяки» пока
не обращают внимания.
Если стерженек из твердого
электролита с электродами на торцах нагрет
неравномерно, он начнет терять кислород и между
электродами возникнет разность потенциалов. По
ее величине можно определить, например, состав
выхлопных газов автомобильного двигателя. На
Западе, где требования к чистоте выхлопных газов
очень строги, такие датчики выпускаются
миллионами. У нас же на такие «пустяки» пока
не обращают внимания.
Кислородные датчики пока единственные устройства с твердыми оксидными электролитами, нашедшие практическое применение.
Кислородные насосы. Пусть во внешнее пространство пробирки подается воздух или газ, содержащий кислород. Если внешний электрод стал анодом, а внутренний — катодом, то из газа в пробирку пойдет чистый кислород. Подобные устройства — кислородные насосы — могут найти применение там, где потребление кислорода невелико или требуется его высокая чистота.
В медицине, например, используется и чистый
кислород, и воздух с пониженным содержанием
кислорода — так называемая «гипоксическая
смесь», или «горный воздух». Электрохимические насосы наряду с мембранными
оксигенаторами (см. «Наука и жизнь» № 2, 1999 г.)
позволят решить массу проблем, особенно в
медицинских учреждениях, удаленных от
промышленных центров. В атмосфере с пониженным
содержанием кислорода значительно дольше
хранятся продукты питания, и устройства с
кислородными насосами могут стать экономичней
привычных холодильников.
Электрохимические насосы наряду с мембранными
оксигенаторами (см. «Наука и жизнь» № 2, 1999 г.)
позволят решить массу проблем, особенно в
медицинских учреждениях, удаленных от
промышленных центров. В атмосфере с пониженным
содержанием кислорода значительно дольше
хранятся продукты питания, и устройства с
кислородными насосами могут стать экономичней
привычных холодильников.
Электролизеры. Теперь к внешнему электроду - катоду — подводят водяной пар или углекислый газ. На катоде будет происходить разложение пара или углекислого газа, а на аноде в обоих случаях выделяется кислород. Уникальная способность этого высокотемпературного электролизера одновременно разлагать водяной пар и углекислый газ позволяет создать систему жизнеобеспечения, скажем, на космических объектах.
Теплоэлектрогенераторы . Человек сделал
первый шаг к независимости от природы,
научившись сохранять огонь, поистине
универсальный источник энергии. Костер давал
тепло и свет, на нем готовили пищу, он расходовал
ровно столько топлива, сколько было необходимо.
Костер тысячелетиями оставался главной энергетической
установкой человека, и неудивительно, что мы
испытываем какую-то ностальгию по очагу с
горящими дровами.
Костер давал
тепло и свет, на нем готовили пищу, он расходовал
ровно столько топлива, сколько было необходимо.
Костер тысячелетиями оставался главной энергетической
установкой человека, и неудивительно, что мы
испытываем какую-то ностальгию по очагу с
горящими дровами.
Еще в конце прошлого века свет давали свечи и
керосиновые лампы, а тепло — печи. Лишь немногим
более ста лет назад на человека начало работать
электричество, которое могло давать свет, тепло,
механическую работу. Одно время казалось, что
достаточно подвести к жилищу только
электрическую энергию, а уж там преобразовывать
ее во что угодно. Но сказала свое слово экономика:
кпд электростанции менее 40%, потери при передаче
и обратном превращении электричества в другие
виды энергии тоже значительны. Ясно, что там, где
нужно только тепло, его целесообразно получать
прямо из топлива. И не случайно сегодня
обсуждается простая идея: вернуть «очаг» в
дом в виде электрохимического генератора с
топливным элементом, преобразующим энергию
топлива в электричество и тепло.
Топливные элементы. Пусть к внешним стенкам пробирки подается водород, а внутрь ее — кислород. Между электродами возникнет напряжение около вольта, по соединяющей их цепи потечет ток, и на электродах пойдут реакции, обратные тем, что проходят в электролизере. Внешний электрод станет анодом, внутренний — катодом, а устройство превратится в источник тока — твердооксидный топливный элемент.
Одно и то же устройство может служить и топливным элементом, и электролизером, позволяя аккумулировать электрическую энергию. В период низкого ее потребления невостребованная мощность электростанций используется для получения водорода. В пике потребления электролизер начинает работать как топливный элемент, производя электричество из водорода.
Топливом в элементе может быть и угарный газ. В
него нетрудно превратить уголь, нефть, различные
газы и спирты (которые, например, в Бразилии
используют как горючее для автомобилей). Элемент
послужит основой электрохимического генератора,
способного существенно изменить концепцию
снабжения жилища энергией. Наиболее прост в
техническом отношении генератор на природном
газе — метане или пропане.
Элемент
послужит основой электрохимического генератора,
способного существенно изменить концепцию
снабжения жилища энергией. Наиболее прост в
техническом отношении генератор на природном
газе — метане или пропане.
Как показывают исследования, его электрический кпд достигает 70%. Остальные 30% энергии топлива выделяются в виде тепла, которое можно использовать в паровых турбинах. Кпд такой комбинированной установки способно превысить 80% — столь высокой эффективности нет ни у одного генератора.
Восемь лет назад в Институте
высокотемпературной электрохимии Уральского
отделения РАН был изготовлен демонстрационный
генератор на метане мощностью один киловатт. Но
до практической реализации дело никак не дойдет.
Опытно-конструкторские работы, которые уже
начинались, до конца так и не доведены. Задача
очень сложна, ее необходимо решать в рамках
национальной программы, попытки
разработать которую оказались пока
безуспешными.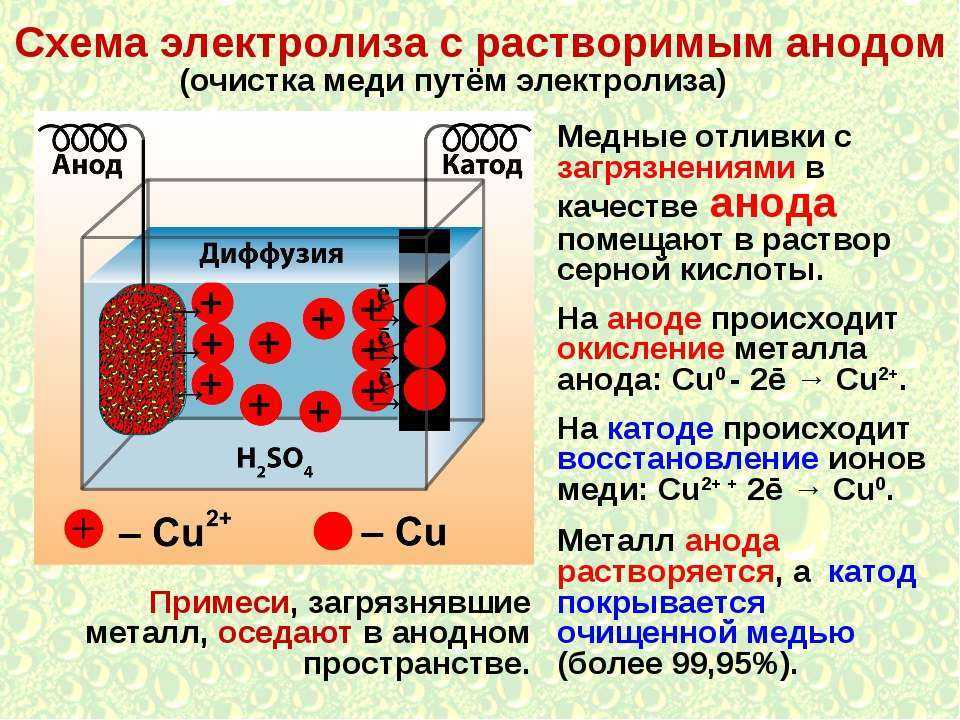
Новый способ управления кислородом для электронных свойств
Исследователи из Аргоннской национальной лаборатории Министерства энергетики США (DOE) обнаружили, что они могут использовать слабый электрический ток для введения кислородных пустот или вакансий, которые резко изменяют проводимость тонких оксидных пленок. . Результаты опубликованы в Nature Communications .
Открытие улучшает наше понимание того, как работают эти материалы, и может быть полезно для новой электроники, катализаторов и многого другого.
Ученые всегда ищут необычные свойства материалов, которые могли бы лечь в основу новых технологий. Оксиды — это класс материалов, который в последнее время вызвал большой интерес, потому что они иногда демонстрируют такое необычное поведение — переключение между изолирующим и проводящим состояниями, включение и выключение магнетизма или даже превращение в сверхпроводник: идеально проводят электричество без каких-либо потерь в виде тепла.
Мы считаем, что некоторые из этих свойств связаны с кислородными вакансиями. Структура оксида представляет собой повторяющуюся кристаллическую решетку с атомами кислорода, усеянными повсюду, но иногда могут быть пустоты там, где отсутствует атом кислорода.
Структура оксида представляет собой повторяющуюся кристаллическую решетку с атомами кислорода, усеянными повсюду, но иногда могут быть пустоты там, где отсутствует атом кислорода.
Обычный способ создания кислородных вакансий — нагревание материалов и добавление или удаление кислорода из окружающей среды.
«Но необходимость контролировать газовую среду ограничивает, где и когда вы можете изменить свойства материала», — сказал Джефф Истман, ученый-материаловед из Аргонны и соответствующий автор статьи.
Команда из Аргонна хотела узнать, можно ли контролировать вакансии альтернативным методом.
Они построили двухслойный материал: слой кристаллов оксида индия поверх блока циркония, стабилизированного оксидом иттрия. Когда исследователи применили небольшое электрическое поле, они наблюдали, как электрическая проводимость резко возросла на два порядка вдоль границы, где встречаются два слоя. Эффект обратим; без поля он возвращается в исходное, менее проводящее состояние.
«Вы можете представить себе приложения для электроники или строительных катализаторов — например, способ расщепления воды или углекислого газа», — сказал Истман.
Теория, основанная на компьютерном моделировании, состоит в том, что разница между свойствами двух материалов создает между ними вертикальное напряжение, а отрицательно заряженные ионы кислорода в оксиде индия притягиваются к потоку и перемещаются по поверхности раздела, оставляя вакансии позади.
Группа планирует дальнейшее исследование того, проявляются ли такие же эффекты в других материалах и может ли этот метод управлять другими свойствами, сказал Истман.
Соавторами статьи «Межфазный контроль легирования кислородных вакансий и электропроводности в тонкопленочных оксидных гетероструктурах» являются ученые из Аргонны Бойд Вил, Питер Запол, Хаким Иддир и Питер Бальдо, а также Сон Кеун Ким, Аргоннский постдокторант во время этого исследования, в настоящее время научный сотрудник Корейского института науки и технологий.
Команда использовала лучевую линию 12-ID в Advanced Photon Source, пользовательском центре Министерства энергетики США, для определения характеристик и анализа. Они также использовали кластер Fusion в Центре вычислительных ресурсов Аргоннской лаборатории для оценки разработанной теории.
Исследование проводилось при поддержке Управления науки Министерства энергетики, Управления фундаментальных энергетических наук.
Аргоннская национальная лаборатория занимается поиском решений насущных национальных проблем в области науки и техники. Первая в стране национальная лаборатория, Аргонн, проводит передовые фундаментальные и прикладные научные исследования практически во всех научных дисциплинах. Исследователи Аргонны тесно сотрудничают с исследователями из сотен компаний, университетов, а также федеральных, государственных и муниципальных учреждений, чтобы помочь им решить их конкретные проблемы, укрепить научное лидерство Америки и подготовить нацию к лучшему будущему. Компания Argonne, в которой работают сотрудники из более чем 60 стран, находится под управлением UChicago Argonne, LLC для Управления науки Министерства энергетики США.
Компания Argonne, в которой работают сотрудники из более чем 60 стран, находится под управлением UChicago Argonne, LLC для Управления науки Министерства энергетики США.
Управление науки Министерства энергетики США является крупнейшим сторонником фундаментальных исследований в области физических наук в Соединенных Штатах и работает над решением некоторых из самых насущных проблем нашего времени. Для получения дополнительной информации посетите веб-сайт Управления науки.
a Какова электронная конфигурация i атома натрия и ii атома кислорода b Какое число…
Перейти к
- Упражнение
- Глава 1 Химические реакции и уравнения
- Глава 2 Кислоты, основания и соли
- Глава 3 Металлы и неметаллы
- Глава 4 Углерод и его соединения
- Глава 5 Периодическая классификация элементов
Главная > Лахмир Сингх Солюшнс Класс 10 Химия > Глава 3 — Глава 3 Металлы и неметаллы > Упражнение > Вопрос 158
Вопрос 158. Упражнение
Упражнение
(a) Какова электронная конфигурация (i) атома натрия и (ii) атома кислорода?
(b) Каково число самых удаленных электронов в (i) атоме натрия и (ii) атоме кислорода?
(c) Покажите образование Na 2 O путем переноса электронов между соединяющимися атомами.
(d) Почему ионные соединения обычно твердые?
(e) Как получилось, что ионные соединения в твердом состоянии не проводят электричество, а в расплавленном — проводят?
Ответ:
(a) (i) Натрий: 2,8,1 (ii) Кислород: 2,6
(b) (i) Натрий :1 (ii) Кислород: 6
(c)
(d) Ионные соединения обычно твердые, потому что их противоположно заряженные ионы сильно притягиваются друг к другу и образуют кристаллическую структуру.
(e) Твердые ионные соединения состоят из ионов, но не проводят электричество. Ионы удерживаются вместе сильной электростатической силой, и их движение ограничено. Когда он растворяется в воде, его кристаллическая структура нарушается, и ионы начинают свободно двигаться, таким образом проводя электричество.
Когда он растворяется в воде, его кристаллическая структура нарушается, и ионы начинают свободно двигаться, таким образом проводя электричество.
Связанные вопросы
**Назовите один металл и один неметалл, которые существуют в жидком состоянии при комнатной температуре.**
**Назовите металл, который является самым плохим проводником тепла.**
**(а) Что имеется в виду, когда говорят, что металлы ковкие и пластичные? Объясните примерами.****(b…
**Назовите два металла, которые бурно реагируют с холодной водой. Напишите любые три наблюдения, которые вы бы сделали…
В данной реакции оксид натрия взаимодействует с водой. Какой продукт образуется в данной реакции?.