Неоадъювантная химиолучевая терапия местно-распространенного рака прямой кишки
Успешное лечение больных местно-распространенным раком прямой кишки определяется тщательным дооперационным обследованием по разработанному протоколу с применением магнитно-резонансной томографии (МРТ) органов малого таза, проведенной по показаниям предоперационной лучевой терапией, выполненным в соответствии с современными принципами хирургическим вмешательством и тщательным патоморфологическим исследованием. От слаженной работы всей «мультидисциплинарной» команды зависят качество жизни и онкологические результаты лечения больных. Будущее такого подхода к лечению во многом будет определяться появлением более эффективных радиосенсибилизаторов, новых химиопрепаратов, а главное увеличением числа хирургов-онкологов, ориентирующихся в возможностях вспомогательных методов лечения и владеющих современной хирургической техникой [1].
После опубликования результатов рандомизированного исследования Немецкой группой исследователей, в котором было показано преимущество предоперационной химиолучевой терапии над послеоперационной химиолучевой терапией, она стала стандартом лечения для больных местно-распространенным раком прямой кишки.

Капецитабин — пероральный фторпиримидин, препарат, который превращается в активный 5-ФУ посредством ферментативных реакций в печени и в опухолевых клетках [10, 11]. Прием препарата 2 раза в день может имитировать фармакокинетику длительного введения 5-ФУ. В нескольких исследованиях II фазы капецитабин использовался в сочетании с предоперационной лучевой терапией местно-распространенного рака прямой кишки. В этих исследованиях было показано, что данную схему лечения хорошо переносят больные, а ответная реакция опухоли была сравнима с лучевой терапией на фоне длительной инфузии 5-ФУ и лейковорина [12—15]. Тем не менее рандомизированные исследования, в которых непосредственно бы сравнивались, по целому ряду показателей, результаты этих двух схем лечения, в литературе отсутствуют. В нашем Центре с 2003 г. проводится исследование по сравнительной оценке эффективности химиолучевой терапии местно-распространенного рака прямой кишки на основе длительной инфузии 5-ФУ с лейковорином и перорального приема капецитабина.
Цель настоящего исследования — анализ эффективности двух схем предоперационной лучевой терапии у больных местно-распространенным раком прямой кишки по уровню токсичности, выраженности патоморфоза в опухоли, частоте местных рецидивов и выживаемости.
Материал и методы
В исследование включили 124 больных раком прямой кишки T3/T4 и N–/N+, проходивших лечение в клинике МРНЦ с 2003 по 2013 г., с морфологически подтвержденной аденокарциномой прямой кишки различной степени дифференцировки. Всем больным проводили клинико-инструментальное обследование для установления распространенности опухолевого процесса по классификации TNM. При обследовании использовали пальцевое исследование, ректоскопию, колоноскопию, рентгенографию грудной клетки, УЗИ брюшной полости и малого таза, эндоскопическое УЗИ, СКТ малого таза, МРТ малого таза, основные биохимические и гематологические исследования, уровень раково-эмбрионального антигена сыворотки. Пациенты в зависимости от применяемого химиотерапевтического агента были разделены на две группы: больные, получавшие лучевую терапию с длительной инфузией 5-ФУ и лейковорина (ХЛТ-5-ФУ, 64 пациента), и больные, получавшие лучевую терапию в сочетании с приемом капецитабина (ХЛТ-CAP, 60 больных).
Схема химиолучевой терапии (ХЛТ) с использованием 5-ФУ и лейковорина (исторический контроль) представлена на рис. 1. Больные получали 5-ФУ в виде длительной 120-часовой внутривенной инфузии в дозе 500 мг/м2 и лейковорин 20 мг/м2 болюсно с 1-го по 5-й день и с 36-го по 40-й день цикла лечения. Лучевую терапию начинали через 24 ч после окончания инфузии 5-ФУ и проводили в течение 5 нед в РОД 2 Г.до СОД 50 Гр.
Рис. 1. Схема комбинированного лечения больных с 5-ФУ.
Топометрическую подготовку осуществляли с помощью компьютерной томографии с использованием симулятора фирмы «Philips». При этом ампулу прямой кишки обязательно контрастировали бариевой взвесью. Далее «срез» тела на уровне центра пересечения полей при помощи дигитайзера переносили на дисплей компьютерной планирующей системы Theraplan. Расчет производили в точке дозирования ICRU пересечения центральных лучей. Применяли четырехпольную методику облучения.
Поля облучения.
Краниальная граница поля проходила на уровне LV/SI, а латеральная на 1 см кнаружи от внутреннего края тазового кольца.
Границы дорсального поля включали задний край крестцовой кости. При планировании вентрального поля было важно, чтобы его граница проходила на 2 см кнаружи от переднего края опухоли. Для включения в зону облучения зон регионарного метастазирования краниальная граница проходила на 2,5 см вентральнее от промонториума, каудально — на дорсальной границе нижнего края симфиза. Использовали оборудование с низкой энергией пучка (менее 8 МэВ).
Использовали оборудование с низкой энергией пучка (менее 8 МэВ).
Таким образом, в зону 95% изодозы включали первичную опухоль и основные лимфатические коллекторы: лимфатические узлы параректальной клетчатки, пресакральные, лимфатические узлы вдоль дистальной части общей подвздошной артерии и вдоль внутренней подвздошной артерии и лимфатические узлы в средней части обтураторной ямки.
С 2009 г. мы изменили схему химиолучевой терапии больных раком прямой кишки; на основании данных литературы мы заменили длительную инфузию 5-ФУ на капецитабин в дозе 825 мг/м2 2 раза в день в дни проведения лучевой терапии (рис. 2). При этом схема и методика лучевой терапии остались прежними. По данной программе нами пролечены 60 больных в период с 2009 по 2013 г.
Рис. 2. Схема комбинированного лечения больных с капецитабином.
Клиническая характеристика больных, включенных в данное ретроспективное исследование, представлена в табл. 1. Группы больных не отличались друг от друга по основным клинико-морфологическим показателям.
Таблица 1. Клиническая характеристика больных
Адъювантная химиотерапия. В группе больных, получавших ХЛТ-5-ФУ, адъювантную химиотерапию проводили всем больным с поражением лимфатических узлов по схеме Мейо или капецитабин. В группе пациентов ХЛТ-САР адъювантную химиотерапию назначали всем больным независимо от патоморфологического заключения. Схемы адъювантной терапии включали капецитабин в монорежиме или оксалиплатин + капецитабин (XELOX).
Результаты
Всем больным курс лучевой терапии был реализован в полном объеме. У 12 из 64 больных ХЛТ-5-ФУ из-за развившейся токсичности после первой инфузии заключительные инфузии 5-ФУ и лейковорина были исключены из схемы лечения. В группе больных с капецитабином только у 3 он был отменен из-за развившейся токсичности. Побочные реакции оценивали по критериям CTCAE v. 3. По видам токсических проявлений в обеих группах превалировали общие реакции. В целом нежелательные явления 2-й степени выраженности в группе с 5-ФУ отмечены у 50 (81,2%) больных.
Таблица 2. Структура токсических реакций
После перерыва в лечении всем больным проводили оценку эффективности лечения по RECIST-критериям, которая осуществлялась через 6—8 нед с помощью СКТ или МРТ малого таза. По данным эндоскопического и рентгенологического исследования полная клиническая регрессия опухоли отмечена у 5 (8%) больных из группы 5-ФУ и у 13 (21%) из группы с капецитабином, частичная регрессия опухоли зафиксирована у 27 (42%) и у 38 (63%) больных соответственно. Стабилизация процесса была отмечена у 30 (47%) больных с 5-ФУ и у 9 (15%) в группе с капецитабином.
Хирургический этап лечения проводили в группе ХЛТ-5-ФУ через 6 нед, а в группе ХЛТ-САР через 8 нед. В обеих группах хирургический этап выполняли с соблюдением основных требований, предъявляемых на сегодняшний день к хирургии рака прямой кишки: острый способ диссекции с сохранением целостности «футляра» удаляемого органа, выполнение тотальной или частичной мезоректумэктомии, высокое лигирование нижних брыжеечных сосудов, полное или частичное сохранение вегетативной нервной системы малого таза, максимальная органосохранная направленность. Необходимо отметить, что оперативное вмешательство в обеих группах выполнялось одним коллективом хирургов.
В обеих группах хирургический этап выполняли с соблюдением основных требований, предъявляемых на сегодняшний день к хирургии рака прямой кишки: острый способ диссекции с сохранением целостности «футляра» удаляемого органа, выполнение тотальной или частичной мезоректумэктомии, высокое лигирование нижних брыжеечных сосудов, полное или частичное сохранение вегетативной нервной системы малого таза, максимальная органосохранная направленность. Необходимо отметить, что оперативное вмешательство в обеих группах выполнялось одним коллективом хирургов.
Позитивные изменения в опухоли после предоперационного лечения позволили выполнить удаление первичной опухоли у 53 больных из группы с 5-ФУ и у 58 из группы с капецитабином. Таким образом, резектабельность в группах составила 83 и 97%. В связи с недостаточным эффектом лекарственного и лучевого лечения и прогрессирования метастатического процесса у 8 больных в группе с 5-ФУ оперативное лечение не выполнялось. Удаление первичной опухоли в объеме R0-резекции выполнено у 45 (80%) и у 48 (80%) больных в группах соответственно. Линия резекции, проходившая в 1 мм или меньше от латерального края опухоли (R1-резекция), была у 5 (9%) больных в группе с 5-ФУ и у 10 (17%) больных в группе с капецитабином [16] (табл. 3).
Линия резекции, проходившая в 1 мм или меньше от латерального края опухоли (R1-резекция), была у 5 (9%) больных в группе с 5-ФУ и у 10 (17%) больных в группе с капецитабином [16] (табл. 3).
Таблица 3. Виды и типы операций
При изучении влияния ХЛТ на течение послеоперационного периода мы не получили существенного увеличения послеоперационных осложнений и летальности. Так, в группе ХЛТ-5-ФУ частота послеоперационных осложнений отмечена у 18 (32%), а в группе с капецитабином у 14 (23%) больных. Причиной одного летального исхода в группе с капецитабином стал инфаркт миокарда. Нагноение промежностной раны развилось в группе с 5-ФУ у 4 (16%) больных, в группе с капецитабином у 7 (25%), различия недостоверны. Несостоятельность анастомоза выявлена у 2 больных в каждой группе (табл. 4).
Таблица 4. Послеоперационные осложнения
После операции больным проводилось морфологическое исследование удаленного препарата с использованием стандартизованного протокола, в котором определяли глубину инвазии опухоли, состояние латерального и дистального краев резекции, лимфатических узлов, наличие или отсутствие сосудистой или периневральной инвазии, а также выраженность лечебного патоморфоза в опухоли после ХЛТ (табл. 5). Из представленных данных табл. 5 обращает на себя внимание большее число пораженных лимфатических узлов и более выраженные патоморфологические изменения в опухоли в группе с капецитабином. На наш взгляд, это связано с механизмом действия капецитабина и увеличением интервала между ХЛТ и операцией, так как методика лучевой терапии и оборудование для нее оставались без изменений.
5). Из представленных данных табл. 5 обращает на себя внимание большее число пораженных лимфатических узлов и более выраженные патоморфологические изменения в опухоли в группе с капецитабином. На наш взгляд, это связано с механизмом действия капецитабина и увеличением интервала между ХЛТ и операцией, так как методика лучевой терапии и оборудование для нее оставались без изменений.
Таблица 5. Морфологическая характеристика опухоли и патоморфоз
Более выраженные изменения в опухоли после ХЛТ-CAP подтверждаются данными табл. 6. После ХЛТ-CAP достоверно больше больных с полной патоморфологической регрессией первичной опухоли и лимфатических узлов, что подтверждается также более выраженной глубиной инвазии опухоли в стенку кишки после ХЛТ.
Таблица 6. Распределение больных в зависимости от стадии заболевания Примечание. * — различия статистически достоверны (р=0,03).
Одними из важнейших показателей эффективности лечения являются частота возникновения местных рецидивов, отдаленных метастазов и безрецидивной выживаемости.
Анализ частоты развития местных внутритазовых рецидивов у больных с R0—R1-резекцией показал, что в группе c 5-ФУ частота рецидивов составила 11,3% (6 больных), при этом у 5 (9,4%) больных рецидивы сочетались с отдаленными метастазами. В группе с капецитабином у 2 больных развился рецидив заболевания и у одного больного — в сочетании с метастазами. Следует отметить, что ни у одного больного рецидива в зоне анастомоза выявлено не было, рецидивы в сочетании отдаленными метастазами развились в лимфатических узлах на стенках малого таза.
Частота отдаленного метастазирования в группах с R0—R1-резекцией составила 15% (7 больных) в группе с 5-ФУ и 10% (у 5 больных) в группе с капецитабином. Надо заметить, что, несмотря на достаточно агрессивное предоперационное лечение, уменьшить частоту метастазирования удалось весьма незначительно.
Показатели общей 5-летней безрецидивной выживаемости составили 57,2±7,3% в группе с 5-ФУ и 62,4±9,0% в группе с капецитабином. При оценке выживаемости больных после R0—R1-резекции при I—III стадии заболевания 5-летний показатель составил 60,5±7,5 и 86,6±5,8% соответственно (р>0,05).
Обсуждение
В этом ретроспективном исследовании была отмечена идентичность влияния предоперационной ХЛТ-5-ФУ и ХЛТ-CAP на результаты лечения больных местно-распространенным раком прямой кишки. Несмотря на достоверно большую частоту полных ответов, у больных в схеме с капецитабином при оценке реакции на терапию первичной опухоли не выявлено существенных различий. Частота местных рецидивов и безрецидивная выживаемость были сопоставимы в обеих группах. Обе схемы лечения хорошо переносились, с низкими показателями токсичности 3-й и 4-й степени в процессе лечения.
Существуют три различных варианта использования 5-ФУ в сочетании с лучевой терапией рака прямой кишки. Первый вариант — болюсное введение 5-ФУ с лейковорином в течение 5 дней в первую и пятую недели лучевой терапии. Это схема была использована в двух европейских исследованиях III фазы: EORTC 22921 [4] и FFCD 9203 [5]. Второй вариант — непрерывное введение 5-ФУ в течение 5 дней в первую и пятую недели. Вариант прерывистой инфузии 5-ФУ был применен немецкой исследовательской группой CAO/ARO/AIO-94 [2]. Третий вариант — длительная постоянная инфузия 5-ФУ в течение всего курса лучевой терапии [6—8]. M. О’Connell и соавт. [9] при сравнении постоянной непрерывной инфузии 5-ФУ и прерывистого курса в первую и пятую недели лучевой терапии в исследовании III фазы показали улучшение безрецидивной и общей выживаемости у больных с непрерывной инфузией. Поэтому во многих учреждениях стали использовать длительную инфузию 5-ФУ как стандартную схему химиолучевой терапии рака прямой кишки [17]. Однако в последующем исследовании INT GI 0144, которое было разработано для сравнения длительной инфузии 5-ФУ с прерывистой инфузией 5-ФУ и болюсным введением лейковорина, не было получено никакой разницы в безрецидивной и общей выживаемости между тремя различными режимами ХЛТ на основе 5-ФУ: (1) длительная инфузия 5-ФУ до, во время и после лучевой терапии; (2) длительная инфузия в сочетании с болюсным введением 5-ФУ и лейковорина при комнатной температуре до и после лучевой терапии и (3) болюсное введение 5-ФУ и лейковорина при комнатной температуре до, во время и после лучевой терапии [18].
Вариант прерывистой инфузии 5-ФУ был применен немецкой исследовательской группой CAO/ARO/AIO-94 [2]. Третий вариант — длительная постоянная инфузия 5-ФУ в течение всего курса лучевой терапии [6—8]. M. О’Connell и соавт. [9] при сравнении постоянной непрерывной инфузии 5-ФУ и прерывистого курса в первую и пятую недели лучевой терапии в исследовании III фазы показали улучшение безрецидивной и общей выживаемости у больных с непрерывной инфузией. Поэтому во многих учреждениях стали использовать длительную инфузию 5-ФУ как стандартную схему химиолучевой терапии рака прямой кишки [17]. Однако в последующем исследовании INT GI 0144, которое было разработано для сравнения длительной инфузии 5-ФУ с прерывистой инфузией 5-ФУ и болюсным введением лейковорина, не было получено никакой разницы в безрецидивной и общей выживаемости между тремя различными режимами ХЛТ на основе 5-ФУ: (1) длительная инфузия 5-ФУ до, во время и после лучевой терапии; (2) длительная инфузия в сочетании с болюсным введением 5-ФУ и лейковорина при комнатной температуре до и после лучевой терапии и (3) болюсное введение 5-ФУ и лейковорина при комнатной температуре до, во время и после лучевой терапии [18]. Было показано, что длительная инфузия 5-ФУ превосходит прерывистое введение в сочетании с болюсным введением 5-ФУ без лейковорина, но эквивалентна по эффективности прерывистому болюсному введению 5-ФУ с лейковорином.
Было показано, что длительная инфузия 5-ФУ превосходит прерывистое введение в сочетании с болюсным введением 5-ФУ без лейковорина, но эквивалентна по эффективности прерывистому болюсному введению 5-ФУ с лейковорином.
Капецитабин в связи с большей простотой использования был введен в лечебную схему в качестве потенциальной замены 5-ФУ. В двух рандомизированных исследованиях III фазы при метастатическом колоректальном раке капецитабин показал одинаковую эффективность с внутривенным введением 5-ФУ и лейковорина, но с более мягким профилем токсичности и более лучшей переносимостью для пациентов. В другом рандомизированном исследовании по оценке эффективности послеоперационной адъювантной терапии рака толстой кишки (X-ACT) капецитабин показал улучшение безрецидивной выживаемости и меньшее число развития токсических реакций 3-й и 4-й степени, чем при внутривенном введении 5-ФУ и лейковорина [19—21]. Капецитабин с тех пор используется в качестве альтернативы 5-ФУ и лейковорину в схемах предоперационного лучевого лечения больных местно-распространенным раком прямой кишки. В настоящее время нет сводных данных их исследований III фазы при раке прямой кишки. В одноцентровом ретроспективном исследовании D. Kim и соавт. [22] показали сопоставимые непосредственные и отдаленные результаты лечения ХЛТ с капецитабином и ХЛТ с внутривенным введением 5-ФУ. Проводилось сравнение результатов лечения 133 пациентов ХЛТ + капецитабин и 145 больных ХЛТ + 5-ФУ и лейковорин, при этом 5-ФУ вводили в виде прерывистой болюсной инъекции в течение 3 дней в первую и пятую недели лучевой терапии. Частота полного ответа составила 16,1% в группе с капецитабином и 11,3% с 5-ФУ и лейковорином. Общий положительный ответ опухоли по глубине инвазии при морфологическом исследовании составил 50% в группе c капецитабином и 44% в группе с 5-ФУ и лейковорином. В процессе исследования не было выявлено никаких существенных различий по профилю токсичности и реакции опухоли на сочетанную лучевую терапию.
В настоящее время нет сводных данных их исследований III фазы при раке прямой кишки. В одноцентровом ретроспективном исследовании D. Kim и соавт. [22] показали сопоставимые непосредственные и отдаленные результаты лечения ХЛТ с капецитабином и ХЛТ с внутривенным введением 5-ФУ. Проводилось сравнение результатов лечения 133 пациентов ХЛТ + капецитабин и 145 больных ХЛТ + 5-ФУ и лейковорин, при этом 5-ФУ вводили в виде прерывистой болюсной инъекции в течение 3 дней в первую и пятую недели лучевой терапии. Частота полного ответа составила 16,1% в группе с капецитабином и 11,3% с 5-ФУ и лейковорином. Общий положительный ответ опухоли по глубине инвазии при морфологическом исследовании составил 50% в группе c капецитабином и 44% в группе с 5-ФУ и лейковорином. В процессе исследования не было выявлено никаких существенных различий по профилю токсичности и реакции опухоли на сочетанную лучевую терапию.
R. Yerushalmi и соавт. [23] продемонстрировали сравнительные результаты лечения 43 больных после ХЛТ с капецитабином и 46 больных после ХЛТ с длительной инфузией 5-ФУ. Частота полных ответов составила 30% в группе с капецитабином и 17% в группе с длительной инфузией 5-ФУ, но разница статистически была недостоверна (р=0,15). Частота регрессии опухоли была значительно выше в группе с капецитабином, чем в группе с 5-ФУ, 70% против 50% (р=0,009). Частота гастроинтестинальной токсичности 3-й степени была схожа в обеих группах. P. Das и соавт. [24] провели сравнение между 89 парами пациентов, которые получали ХЛТ с капецитабином или ХЛТ с длительной инфузией 5-ФУ. Пациенты были сопоставимы по распространенности заболевания. В исследовании не было получено разницы по частоте полных ответов: 21% в группе с капецитабином и 12% в группе с 5-ФУ (р=0,19). Частота регрессии опухоли по Т составила 52% в группе с капецитабином и 62% при длительном введении 5-ФУ (р=0,2). Уровень токсичности 3-й и 4-й степени при ХЛТ составил 6% в обеих группах. Трехлетняя безрецидивная выживаемость составила 94,4% в группе с капецитабином и 98,6% в группе с длительной инфузией 5-ФУ (р=0,15).
Частота полных ответов составила 30% в группе с капецитабином и 17% в группе с длительной инфузией 5-ФУ, но разница статистически была недостоверна (р=0,15). Частота регрессии опухоли была значительно выше в группе с капецитабином, чем в группе с 5-ФУ, 70% против 50% (р=0,009). Частота гастроинтестинальной токсичности 3-й степени была схожа в обеих группах. P. Das и соавт. [24] провели сравнение между 89 парами пациентов, которые получали ХЛТ с капецитабином или ХЛТ с длительной инфузией 5-ФУ. Пациенты были сопоставимы по распространенности заболевания. В исследовании не было получено разницы по частоте полных ответов: 21% в группе с капецитабином и 12% в группе с 5-ФУ (р=0,19). Частота регрессии опухоли по Т составила 52% в группе с капецитабином и 62% при длительном введении 5-ФУ (р=0,2). Уровень токсичности 3-й и 4-й степени при ХЛТ составил 6% в обеих группах. Трехлетняя безрецидивная выживаемость составила 94,4% в группе с капецитабином и 98,6% в группе с длительной инфузией 5-ФУ (р=0,15). Общая 3-летняя выживаемость составила 89,8% при лечении с капецитабином и 96,4% при длительной инфузии 5-ФУ (р=0,12).
Общая 3-летняя выживаемость составила 89,8% при лечении с капецитабином и 96,4% при длительной инфузии 5-ФУ (р=0,12).
В нашем исследовании пациенты были сопоставимы по клиническим и морфологическим характеристикам опухоли. Мы использовали длительную инфузию 5-ФУ с болюсным введением лейковорина в первую и последнюю недели лечения. Наши выводы похожи на результаты других исследований. Частота полного ответа колебалась от 16 до 21% после ХЛТ с капецитабином, за исключением данных R. Yerushalmi и соавт. [23], которые сообщили о более высокой частоте полных ответов — 30%, и от 11 до 18% при ХЛТ с 5-ФУ. Частота местного локального контроля в течение 3 лет находилась в пределах от 93 до 94% для ХЛТ с капецитабином и от 92 до 98% для ХЛТ с инфузией 5-ФУ. Трехлетняя выживаемость варьировала от 86 до 89,8% после ХЛТ с капецитабином и от 77 до 96,4% для ХЛТ с 5-ФУ.
Как и во всех ретроспективных исследованиях, несмотря на все наши попытки свести различия к минимуму между сравниваемыми группами, все же отмечался некоторый дисбаланс между двумя когортами пациентов и в этом исследовании. Так, в группе с капецитабином опухоль чаще локализовалась в нижнеампулярном отделе прямой кишки, было больше среднее число пораженных лимфатических узлов. В связи небольшим числом больных в нашем исследовании не удалось выявить существенных различий в группах. Контролируемые многоцентровые рандомизированные исследования III фазы для оценки эффективности ХЛТ, у нас, к сожалению, не проводятся.
Так, в группе с капецитабином опухоль чаще локализовалась в нижнеампулярном отделе прямой кишки, было больше среднее число пораженных лимфатических узлов. В связи небольшим числом больных в нашем исследовании не удалось выявить существенных различий в группах. Контролируемые многоцентровые рандомизированные исследования III фазы для оценки эффективности ХЛТ, у нас, к сожалению, не проводятся.
Выводы
1. При местно-распространенном раке прямой кишки с признаками внеорганного распространения опухоли, вовлечения циркулярной границы резекции и (или) с метастатическим поражением лимфатических узлов на первом этапе лечения показана химиолучевая терапия.
2. Лучевую терапию следует проводить на современном оборудовании в условиях хорошего физико-технического сопровождения до СОД 50 Г.в течение 5 нед, предпочтительно в сочетании с капецитабином в дозе 1650 мг/м2 в сутки.
3. Применение капецитабина сопряжено с достоверно меньшей частотой развития токсических реакций (р<0,05) и большей (p<0,05) частотой полного ответа опухоли на лучевое воздействие.
Участие авторов:
Концепция и дизайн исследования: Д.В.Е., Б.А.Б.
Сбор и обработка материала: Д.В.Е., А.А.Н.
Статистическая обработка: Д.В.Е.
Написание текста: Д.В.Е., Л.Н.Т., С.Г. С.
Редактирование: Б.А.Б.
Конфликт интересов отсутствует.
Сегодня, 10 апреля, состоялось торжественное открытие Международной школы по лечению врожденных пороков сердца.
Сегодня, 10 апреля, состоялось торжественное открытие Международной школы по лечению врожденных пороков сердца.
Ведущие американские специалисты в детской кардиохирургии и кардиологии приехали в калининградский Центр высоких медицинских технологий для обмена самыми последними достижениями в детской кардиохирургии, кардиологии и послеоперационном уходе со своими российскими коллегами. Это визит – четвертый в рамках сотрудничества Центра и Международного медицинского альянса «HearttoHeart», известного в России уже более 20 лет.
Тема Международной школы в 2017 году — лечение врожденного порока сердца — Аномалии Эбштейна. Подобная масштабная тематическая школа уникальна для российской детской кардиохирургии. Аномалия Эбштейна – крайне редкая, но очень сложная врожденная патология, которая периодически встречается и у детей Калининградской области. При этом данный порок требует точной диагностики, сложного и выверенного хирургического вмешательства.
У пациентов с этим заболеванием аномально сформирован правый желудочек и трехстворчатый клапан. Степень тяжести порока может варьироваться от пациента к пациенту; симптомы могут проявляться в самое разное время их жизни. У некоторых симптомы проявляются при рождении; таким пациентам хирургическое лечение требуется уже в периоде новорожденности. Однако, многие с аномалией Эбштейна могут прожить много лет без хирургического вмешательства, не испытывая таких проблем, как сердечная недостаточность, аритмии или цианоз. Своевременный и точный диагноз заболевания гарантирует, что хирургическое лечение будет проведено в нужное время. С помощью операции возможно восстановить или протезировать аномальный клапан и повысить качество жизни пациента. Однако, поскольку порок встречается редко, немного хирургов имеют опыт хирургического лечения аномалии Эбштейна.
С помощью операции возможно восстановить или протезировать аномальный клапан и повысить качество жизни пациента. Однако, поскольку порок встречается редко, немного хирургов имеют опыт хирургического лечения аномалии Эбштейна.
Одним из таких хирургов является доктор Джозеф Дерани, руководитель отделения сердечно-сосудистой хирургии в клинике Мэйо г. Рочестер, штат Миннесота, США. Хирурги этой клиники проводят хирургическое лечение пациентов с аномалией Эбштейна с 1972 года.
Джозеф Дерани, а также еще целый ряд известных американских специалистов, представляющих команду альянса «От сердца к сердцу», проведут в Калининграде, в Центре высоких медицинских технологий лекции, мастер-классы, клиническую подготовку по таким темам как: постановка диагноза; подходы к принятию решения о хирургическом вмешательстве; уход за пациентами в отделении реанимации в послеоперационном периоде, а также послеоперационное лечение и наблюдение пациентов. Американские медики совместно с российскими коллегами осмотрят порядка 30 пациентов с аномалией Эбштейна. Кроме калининградских детей, в Центр высоких медицинских технологий специально приехали и пациенты данной патологией из других регионов нашей страны – Уфы, Казани, Ростова, Ульяновска, Волгограда для консультаций обследования и возможного хирургического лечения.
Кроме калининградских детей, в Центр высоких медицинских технологий специально приехали и пациенты данной патологией из других регионов нашей страны – Уфы, Казани, Ростова, Ульяновска, Волгограда для консультаций обследования и возможного хирургического лечения.
Участниками Международной школы стали более 60 врачей из многих российских клиник: Москвы, Санкт-Петербурга, Казани, Челябинска, Омска ,Ростова-на-Дону и других.
Напомним, что лекции и доклады американских специалистов в режиме он-лайн транслируются на нашем сайте
В составе команды альянса «От сердца к сердцу» в этом году:
Найлас Янг, основатель и медицинский директор альянса «От сердца к сердцу», профессор, заведующий отделением кардиоторакальной хирургии, Медицинский центр Дэвис, Калифорнийский университет, Джози Эверетт, исполнительный директор альянса «От сердца к сердцу», Альбина Попова – координатор альянса, Джосеф Дерани, хирург — клиника Мейо, Кейтлин Блау, перфузиолог — клиника Мейо, Фрэнк Сетта – кардиолог, клиника Мейо, Брайан Кэннон, кардиолог — клиника Мейо, Грейс Артега – реаниматолог, клиника Мейо, Джоан Вобиг, ассистент хирурга, клиника Мейо, Олеся Душкова, операционная сестра — Дейвис медицинский центр, Бренда Джарвис — медсестра реанимации, детская больница Атланты, Лори Ютни — медсестра реанимации — клиника Мейо, Эрик Эгглер, медбрат реанимации — клиника Мейо и другие.
View the embedded image gallery online at:
http://kldcardio.ru/o-tsentre/meditsinskaya-deyatelnost-tsentra/blog-with-right-sidebar/550-segodnya-10-aprelya-sostoyalos-torzhestvennoe-otkrytie-mezhdunarodnoj-shkoly-po-lecheniyu-vrozhdennykh-porokov-serdtsa%3ftemplate%3daccessibility#sigFreeId2afa05b765
- Новости
- Назад
- Вперёд
Практические постквантовые сигнатуры из карт масла и уксуса
Paper 2021/1144
MAYO: Практические постквантовые сигнатуры из карт масла и уксуса
Ward Beullens
Abstract
Схема масла и уксуса , предложенная в 1997 году Патарином, является одной из старейших и наиболее понятных многомерных квадратичных схем подписи. Он имеет превосходную производительность и размеры подписи, но страдает от больших размеров ключей порядка 50 КБ, что делает его менее практичным в качестве схемы подписи общего назначения. Для решения этой проблемы в данной статье предлагается MAYO, вариант схемы подписи UOV, открытые ключи которой на два порядка меньше. MAYO работает с использованием карты UOV с необычно малым масляным пространством, что позволяет очень компактно представлять открытый ключ. Обычный алгоритм подписи UOV дает сбой, если масляное пространство слишком мало, но MAYO решает эту проблему, «превращая» карту базового масла и уксуса в карту большего размера, которая имеет достаточно большое масляное пространство. С параметрами, нацеленными на уровень безопасности I NISTPQC, MAYO имеет размер открытого ключа всего 614 байт и размер подписи 39.2 байта. Это делает MAYO более компактным, чем современные схемы подписи на основе решетки, такие как Falcon и Dilithium. Более того, мы можем выбрать параметры MAYO таким образом, чтобы, в отличие от традиционных подписей UOV, подписи доказуемо пропускали лишь незначительное количество информации о закрытом ключе.
Он имеет превосходную производительность и размеры подписи, но страдает от больших размеров ключей порядка 50 КБ, что делает его менее практичным в качестве схемы подписи общего назначения. Для решения этой проблемы в данной статье предлагается MAYO, вариант схемы подписи UOV, открытые ключи которой на два порядка меньше. MAYO работает с использованием карты UOV с необычно малым масляным пространством, что позволяет очень компактно представлять открытый ключ. Обычный алгоритм подписи UOV дает сбой, если масляное пространство слишком мало, но MAYO решает эту проблему, «превращая» карту базового масла и уксуса в карту большего размера, которая имеет достаточно большое масляное пространство. С параметрами, нацеленными на уровень безопасности I NISTPQC, MAYO имеет размер открытого ключа всего 614 байт и размер подписи 39.2 байта. Это делает MAYO более компактным, чем современные схемы подписи на основе решетки, такие как Falcon и Dilithium. Более того, мы можем выбрать параметры MAYO таким образом, чтобы, в отличие от традиционных подписей UOV, подписи доказуемо пропускали лишь незначительное количество информации о закрытом ключе.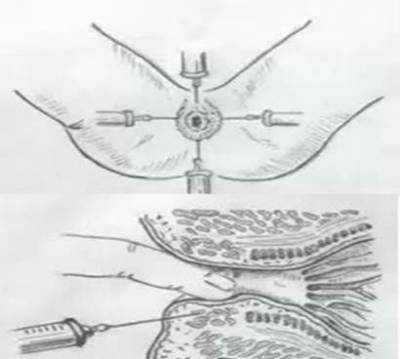
Примечание: 10.14.2021: Новая версия имеет более строгие доказательства безопасности. 25.08.2022: — В новой версии исправлен E_ij во время разработки, а не во время подписания. Это позволяет упростить реализацию. — Мы также изменили определение взбитой карты P*. Новый P* позволяет нам использовать поля характеристики 2. Для нечетной характеристики оба P* эквивалентны с точки зрения безопасности. — Добавлена ссылка на реализацию на GitHub. 30/09/2022: Исправлена опечатка во введении. 12.23.2022: Исправлено больше опечаток.
Метаданные
- Доступный(е) формат(ы)
- Категория
- Криптография с открытым ключом
- Информация о публикации
- Опубликовано в другом месте. САК 2021
- Ключевые слова
- постквантовая криптографияцифровые подписимногомерная квадратичная криптография
- Связаться с автором(ами)
- вард @ beullens ком
- История
- 23.
 12.2022: последняя из 5 ревизий
12.2022: последняя из 5 ревизий - 10.09.2021: получен
- Посмотреть все версии
- Короткий URL-адрес
- https://ia.cr/2021/1144
- Лицензия
-
СС BY
БибТекс
@misc{cryptoeprint:2021/1144,
автор = {Уорд Белленс},
title = {MAYO: практические постквантовые подписи на картах масла и уксуса},
какpublished = {Архив криптологии ePrint, документ 2021/1144},
год = {2021},
примечание = {\url{https://eprint.iacr.org/2021/1144}},
URL = {https://eprint.iacr.org/2021/1144}
}
Примечание. В целях защиты конфиденциальности читателей, eprint.iacr.org не использует файлы cookie или встроенный сторонний контент.
Стипендиаты по обмену Мэйо в Бирмингеме — Бирмингемский университет
Вы хотите улучшить и развить свою карьеру в области медицинских исследований благодаря зарубежному опыту?
Благодаря щедрому пожертвованию мы можем предложить клиницистам Бирмингемского университета, партнерам BHP и консультантам NHS возможность подать заявку на стипендию Mayo на срок от 2 до 6 месяцев, с оплатой заработной платы, проезда, проживания и расходных материалов в любом из три участка Майо в Рочестере, Миннесота; Феникс, Аризона или Джексонвилл, Флорида.
Как подать заявку
Заявки будут рассматриваться круглый год и по мере поступления будут представляться членам комиссии для утверждения. Пожалуйста, не стесняйтесь обращаться к Ивонн Доусон в первую очередь, чтобы подать заявку или задать любые вопросы, которые могут у вас возникнуть.
Кандидаты должны быть в состоянии сформулировать четкую исследовательскую программу и доказательную поддержку предложения от клинических связей в Mayo.
Если вы заинтересованы, ознакомьтесь с рекомендациями перед заполнением формы заявки. Эту форму заявки следует отправить Ивонн Доусон по адресу [email protected] вместе с письмом поддержки от ваших контактов в Mayo и вашим текущим резюме.
Пожалуйста, убедитесь, что информация, указанная в форме заявки, отражает концепцию вашего исследования и имя вашего научного руководителя из Бирмингемского университета.
Алессандро Прете — стипендиат Mayo, 2017 г.
«Мое искреннее желание и цель – развивать карьеру академического эндокринолога и проводить ведущие международные исследования, следуя подходу настоящего ученого-клинициста.


 12.2022: последняя из 5 ревизий
12.2022: последняя из 5 ревизий