Kvant. Размеры молекул — PhysBook
Кикоин А.К. Простой способ определения размеров молекул // Квант. — 1983. — № 9. — C.29-30.
По специальной договоренности с редколлегией и редакцией журнала «Квант»
В молекулярной физике главные «действующие лица» — это молекулы, невообразимо маленькие частицы, из которых состоят все на свете вещества. Ясно, что для изучения многих явлений важно знать, каковы они, молекулы. В частности каковы их размеры.
Когда говорят о молекулах, их обычно считают маленькими упругими твердыми шариками. Следовательно, знать размер молекул значит знать их радиус.
Несмотря на малость молекулярных размеров, физики сумели разработать множество способов их определения. В «Физике 9» рассказывается о двух из них. В одном используется свойство некоторых (очень немногих) жидкостей растекаться в виде пленки толщиной в одну молекулу. В другом размер частицы определяется с помощью сложного прибора — ионного проектора.
Существует, однако, очень простой, хотя и не самый точный, способ вычисления радиусов молекул (или атомов) Он основан на том, что молекулы вещества, когда оно находится в твердом или жидком состоянии, можно считать плотно прилегающими друг к другу. В таком случае для грубой оценки можно считать, что объем
Число молекул в теле массой m равно, как известно, \(~N_a \frac{m}{M}\), где М — молярная масса вещества NA — число Авогадро. Отсюда объем V0 одной молекулы определяется из равенства
\(~V_0 = \frac{V}{N} = \frac{V M}{m N_A}\) .Плотность практически любого вещества можно найти в доступных всем таблицах. Молярную массу легко определить, если известна химическая формула вещества.
Объем одной молекулы, если считать ее шариком, равен \(~\frac{4}{3} \pi r^3\), где r — радиус шарика. Поэтому
\(~\frac{4}{3} \pi r^3 = \frac{M}{\rho N_A}\) .откуда мы и получаем выражение для радиуса молекулы:
\(~r = \sqrt[3] {\frac{3M}{4 \pi \rho N_A}} = \sqrt[3] {\frac{3}{4 \pi N_A}} \sqrt[3] {\frac{M}{\rho}}\) .Первый из этих двух корней — постоянная величина, равная ≈ 7,4 · 10-9 моль1/3, поэтому формула для r ринимает вид
\(~r \approx 7,4 \cdot 10^{-9} \sqrt[3] {\frac{M}{\rho}} (m)\) .Например, радиус молекулы воды, вычисленный по этой формуле, равен rВ ≈ 1,9 · 10-10 м.
Описанный способ определения радиусов молекул не может быть точным уже потому, что шарики нельзя уложить так, чтобы между ними не было промежутков, даже если они соприкасаются друг с другом. Кроме того, при такой «упаковке» молекул- шариков были бы невозможны молекулярные движения. Тем не менее вычисления размеров молекул по формуле, приведенной выше, дают результаты, почти совпадающие с результатами других методов, несравненно более точных.
| Вода | |||
|---|---|---|---|
| |||
Вода в бассейне({{{изображение}}}) | |||
| Систематическое наименование | Оксид водорода Вода[1] | ||
| Традиционные названия | вода | ||
| Хим. формула | H2O | ||
| Состояние | жидкость | ||
| Молярная масса | 18,01528 г/моль | ||
| Плотность | 0,9982 г/см3[2] | ||
| Твёрдость | 1,5[4] | ||
| Динамическая вязкость | 0,00101 Па·с | ||
| Кинематическая вязкость | 0,01012 см²/с (при 20 °C) | ||
| Скорость звука в веществе | (дистиллированная вода) 1348 м/с | ||
| Температура | |||
| • плавления | 273,1 K (0 ° C) | ||
| • кипения | 373,1 K (99,974 ° C) °C | ||
| • разложения | 2200 °C | ||
| Тройная точка | 273,2 K (0,01 ° C), 611,72 Па | ||
| Критическая точка | 647,1 K (374 ° C), 22,064 МПа | ||
| Мол. теплоёмк. | 75,37 Дж/(моль·К) | ||
| Теплопроводность | 0,56 Вт/(м·K) | ||
| Энтальпия | |||
| • образования | -285,83 кДж/моль | ||
| Удельная теплота испарения | 2256,2 кДж/кг[3] | ||
| Удельная теплота плавления | 332,4 кДж/кг[3] | ||
| Показатель преломления | 1,3945, 1,33432, 1,32612, 1,39336, | ||
Размеры атомов и молекул
Размеры атомов и молекул, найденные другими методами, оказываются примерно такими же.
Эти размеры так малы, что их невозможно себе представить. Что вам может сказать, например, число 2,3·10-8см — размер молекулы водорода? В таких случаях прибегают к помощи сравнений. Если, например, вашу голову увеличить до размеров средней звезды типа Солнца, то молекула при этом увеличится до размеров головы.
А вот еще сравнение. Если представить себе, что все размеры в мире возросли в 108 раз, то молекула водорода будет выглядеть как шарик диаметром всего в 2,3 см (средних размеров слива), а рост человека стал бы равным 170 000 км, размер мухи — 10 000 км, толщина волоса — 10км, размер красного кровяного тельца (эритроцита) — 700 м.
Число молекул
При столь малых размерах молекул число их в любом макроскопическом теле чрезвычайно велико. Подсчитаем приблизительное число молекул в капле воды массой 1 г и, следовательно, объемом 1 см3. Диаметр молекулы воды равен приблизительно 3·10-8
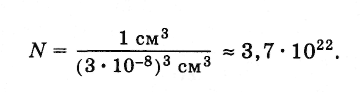
Представьте себе, что поверхность земного шара твердая и гладкая. На всей поверхности вплотную друг к другу стоят люди. Число людей при этом будет чуть меньше числа молекул в 1 см3 воздуха при нормальном атмосферном давлении и температуре 0 °С.
Надо помнить основные положения молекулярно-кинетической теории. Атомы имеют размеры порядка
§ 2.2. Масса молекул. Постоянная Авогадро
Массы молекул очень малы, если выражать их в граммах или килограммах, а число молекул в макроскопических телах огромно. С очень маленькими и очень большими числами иметь дело неудобно. Ученые нашли довольно простой способ избежать этого неудобства и характеризовать массы молекул и их число вполне обозримыми числами, не выходящими далеко за пределы сотни. Сейчас вы познакомитесь с тем, как это делается.
Масса молекулы воды
В предыдущем параграфе мы выяснили, что в 1 г воды содержится 3,7·1022 молекул. Следовательно, масса одной молекулы равна:
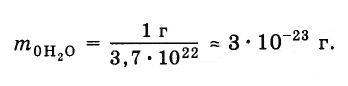
Массы такого же порядка имеют и молекулы других веществ, исключая огромные молекулы органических соединений. Например, масса молекулы гемоглобина превышает массу молекулы воды в несколько десятков тысяч раз.
Относительная молекулярная масса
Так
как массы молекул очень малы, удобно
использовать не абсолютные значения
масс, а относительные. По международному
соглашению, принятому в 1961 г., массы всех
молекул сравнивают с 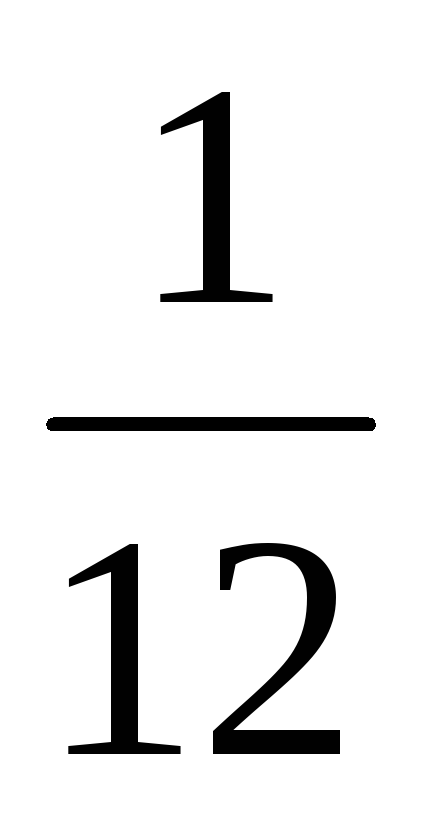 массы атома углерода* (так называемая
углеродная шкала атомных масс). Главная
причина выбора углеродной шкалы атомных
масс состоит в том, что углерод входит
в огромное число различных органических
соединений. Этот выбор позволяет очень
точно сравнивать массы атомов тяжелых
элементов с массой атома углерода.
Множитель
массы атома углерода* (так называемая
углеродная шкала атомных масс). Главная
причина выбора углеродной шкалы атомных
масс состоит в том, что углерод входит
в огромное число различных органических
соединений. Этот выбор позволяет очень
точно сравнивать массы атомов тяжелых
элементов с массой атома углерода.
Множитель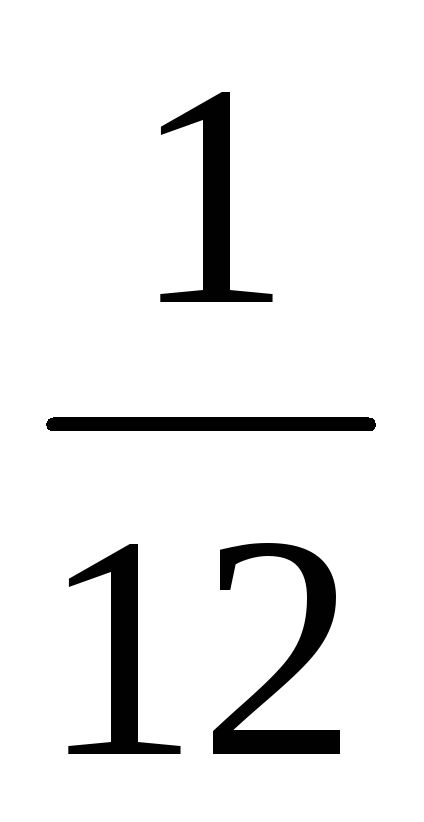
*
Точнее, с 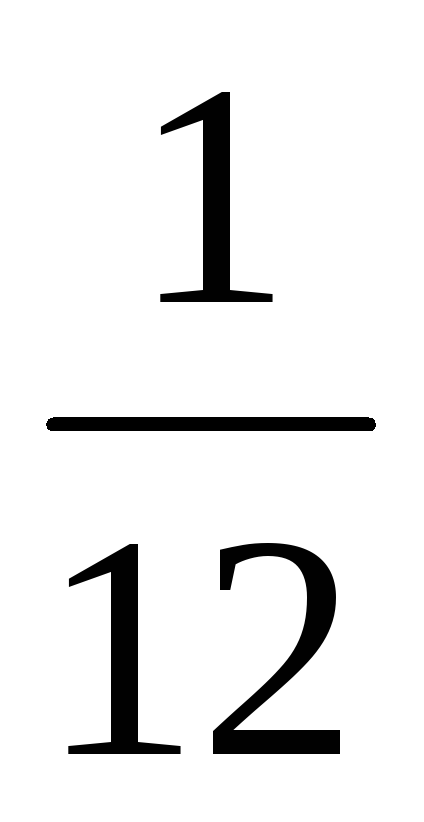 массы атома наиболее
распространенного изотопа углерода-12.
массы атома наиболее
распространенного изотопа углерода-12.
Относительной
молекулярной (или атомной) массой
вещества Мr называют
отношение массы молекулы (или атома)
данного вещества к  массы
атома углерода т0С:
массы
атома углерода т0С:
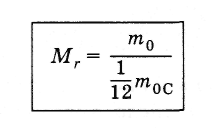 (2.2.1)
(2.2.1)
Относительные
атомные массы всех химических элементов
точно измерены. Складывая относительные
атомные массы, можно вычислить
относительную молекулярную массу.
Например, относительная молекулярная
масса воды Н
Эффективный диаметр молекулы — Википедия
Материал из Википедии — свободной энциклопедии
Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 22 сентября 2019; проверки требует 1 правка. Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 22 сентября 2019; проверки требует 1 правка.Эффективный диаметр молекулы — минимальное расстояние, на которое сближаются центры двух молекул при столкновении.
При столкновении, молекулы сближаются до некоторого наименьшего расстояния, которое условно считается суммой радиусов взаимодействующих молекул. Столкновение между одинаковыми молекулами может произойти только в том случае, если их центры сблизятся на расстояние, меньшее или равное диаметру d{\displaystyle d} — эффективному диаметру молекулы.
Через эффективный диаметр молекулы можно выразить эффективное сечение молекулы — как круг радиусом d. Столкновение между молекулами возможно только в том случае, когда центр молекулы окажется внутри круга, представляющего собой эффективное сечение молекулы.
С точки зрения теории межмолекулярных взаимодействий эффективный радиус, представляющий собой половину эффективного диаметра — расстояние от условного центра молекулы, отвечающее минимуму потенциальной энергии в поле этой молекулы.
Для молекул, имеющих точечную симметрию, условный центр может быть определен как центр масс молекулы, для сложных молекул он определяется феноменологически.
В общем случае эффективный радиус — усредненная величина, т.к. в случае, когда молекула не является концентрически симметричной (одноатомная молекула), радиус является функцией от угла в системе, связанной с молекулой.
<r>=∬r(φ,θ)dφdθ2π2{\displaystyle <r>={\frac {\iint r(\varphi ,\theta )d\varphi d\theta }{2\pi ^{2}}}}
Определение диаметра молекул (стр. 1 из 2)
Муниципальное общеобразовательное учреждение
«Основная общеобразовательная школа №10»
Определение диаметра молекул
Лабораторная работа
Исполнитель: Масаев Евгений
7 класс «А»
Руководитель: Резник А. В.
Гурьевский район
2010
Введение
В этом учебном году я начал изучать физику. Я узнал, что тела, которые нас окружают, состоят из мельчайших частиц – молекул. Меня заинтересовало, каковы размеры молекул. Из-за очень малых размеров молекулы нельзя увидеть невооруженным глазом или с помощью обыкновенного микроскопа. Я прочитал, что молекулы можно увидеть только с помощью электронного микроскопа. Ученые доказали, что молекулы разных веществ отличаются друг от друга, а молекулы одного и того же вещества одинаковы. Мне захотелось на практике измерить диаметр молекулы. Но к сожалению, в школьной программе не предусматривает изучение проблем такого рода, а рассмотреть её одному оказалось нелёгкой задачей и пришлось изучать литературу о методах определения диаметра молекул.
Глава I. Молекулы
1.1 Из теории вопроса
Молекула в современном понимании – это наименьшая частица вещества, обладающая всеми его химическими свойствами. Молекула способна к самостоятельному существованию. Она может состоять как из одинаковых атомов, например кислород О2, озон О3, азот N2, фосфор P4, сера S6 и т. д., так и из различных атомов: сюда относятся молекулы всех сложных веществ. Простейшие молекулы состоят из одного атома: это молекулы инертных газов – гелия, неона, аргона, криптона, ксенона, радона. В так называемых высокомолекулярных соединениях и полимерах каждая молекула может состоять из сотен тысяч атомов.
Экспериментальное доказательство существования молекул первым наиболее убедительно дал французский физик Ж. Перрен в 1906 г. при изучении броуновского движения. Оно, как показал Перрен, является результатом теплового движения молекул – и ничем иным.
Сущность молекулы можно описать и с другой точки зрения: молекула – устойчивая система, состоящая из ядер атомов (одинаковых или различных) и окружающих электронов, причем химические свойства молекулы определяются электронами внешних оболочек в атомах. Атомы объединяются в молекулы в большинстве случаев химическими связями. Обычно такая связь создается одной, двумя или тремя парами электронов, которыми владеют сообща два атома.
Атомы в молекулах соединены друг с другом в определенной последовательности и определённым образом распределены в пространстве. Связи между атомами имеют различную прочность; она оценивается величиной энергии, которую необходимо затратить для разрыва межатомных связей.
Молекулы характеризуются определёнными размером и формой. Различными способами было определено, что в 1 см3 любого газа при нормальных условиях содержится около 2,7×1019 молекул.
Чтобы понять, насколько велико это число, можно представить, что молекула – это «кирпич». Тогда если взять количество кирпичей, равное числу молекул в 1 см3 газа при нормальных условиях, и плотно уложить ими поверхность суши всего земного шара, то они покрыли бы поверхность слоем высотой 120 м, что почти в 4 раза превосходит высоту 10-этажного дома. Огромное число молекул в единице объёма указывает на очень малые размеры самих молекул. Например, масса молекулы воды m=29,9 x 10-27 кг. Соответственно малы и размеры молекул. Диаметром молекулы принято считать минимальное расстояние, на которое им позволяет сблизиться силы отталкивания. Однако понятие размера молекулы является условным, так как на молекулярных расстояниях представления классической физики не всегда оправданы. Средний размер молекул порядка 10-10м.
Молекула как система, состоящая из взаимодействующих электронов и ядер, может находиться в различных состояниях и переходить из одного состояния в другое вынужденно (под влиянием внешних воздействий) или самопроизвольно. Для всех молекул данного вида характерна некоторая совокупность состояний, которая может служить для идентификации молекул. Как самостоятельное образование молекула обладает в каждом состоянии определенным набором физических свойств, эти свойства в той или иной степени сохраняются при переходе от молекул к состоящему из них веществу и определяют свойства этого вещества. При химических превращениях молекулы одного вещества обмениваются атомами с молекулами другого вещества, распадаются на молекулы с меньшим числом атомов, а также вступают в химические реакции других типов. Поэтому химия изучает вещества и их превращения в неразрывной связи со строением и состоянием молекул.
Обычно молекулой называют электрически нейтральную частицу. В веществе положительные ионы всегда сосуществуют вместе с отрицательными.
По числу входящих в молекулу атомных ядер различают молекулы двухатомные, трехатомные и т.д. Если число атомов в молекуле превосходит сотни и тысячи, молекула называется макромолекулой. Сумма масс всех атомов, входящих в состав молекулы, рассматривается как молекулярная масса. По величине молекулярной массы все вещества условно делят на низко- и высокомолекулярные.
1.2 Методы измерения диаметра молекул
В молекулярной физике главные «действующие лица» — это молекулы, невообразимо маленькие частицы, из которых состоят все на свете вещества. Ясно, что для изучения многих явлений важно знать, каковы они, молекулы. В частности, каковы их размеры.
Когда говорят о молекулах, их обычно считают маленькими упругими твердыми шариками. Следовательно, знать размер молекул, значит знать их радиус.
Несмотря на малость молекулярных размеров, физики сумели разработать множество способов их определения. В «Физике 7» рассказывается о двух из них. В одном используется свойство некоторых (очень немногих) жидкостей растекаться в виде пленки толщиной в одну молекулу. В другом размер частицы определяется с помощью сложного прибора — ионного проектора.
Строение молекул изучают различными экспериментальными методами. Электронография, нейтронография и рентгеновский структурный анализ позволяют получать непосредственную информацию о структуре молекул. Электронографии, метод, исследующий рассеяние электронов на пучке молекул в газовой фазе, позволяет рассчитать параметры геометрической конфигурации для изолированных сравнительно простых молекул. Нейтронография и рентгеновский структурный анализ ограничены анализом структуры молекул либо отдельных упорядоченных фрагментов в конденсированной фазе. Рентгенографические исследования кроме указанных сведений дают возможность получить количественные данные о пространственном распределении электронной плотности в молекулах.
Спектроскопические методы основаны на индивидуальности спектров химических соединений, которая обусловлена характерным для каждой молекулы набором состояний и отвечающих им энергетических уровней. Эти методы позволяют проводить качественный и количественный спектральный анализ веществ.
Спектры поглощения или испускания в микроволновой области спектра позволяют изучать переходы между вращательными состояниями, определять моменты инерции молекул, а на их основе — длины связей, валентные углы и другие геометрические параметры молекул. Инфракрасная спектроскопия исследует, как правило, переходы между колебательно-вращательными состояниями и широко используется для спектрально-аналитических целей, поскольку многие частоты колебаний определенных структурных фрагментов молекул являются характеристическими и слабо меняются при переходе от одной молекулы к другой. В то же время инфракрасная спектроскопия позволяет судить и о равновесной геометрической конфигурации. Спектры молекул в оптическом и ультрафиолетовом диапазонах частот связаны главным образом с переходами между электронными состояниями. Результатом их исследований являются данные об особенностях потенциальных поверхностей для различных состояний и значения молекулярных постоянных, определяющих эти потенциальные поверхности, также времена жизни молекул в возбужденных состояниях и вероятности переходов из одного состояния в другое.
О деталях электронного строения молекул уникальную информацию дают фото- и рентгеноэлектронные спектры, а также оже-спектры, позволяющие оценить тип симметрии молекулярных орбиталей и особенности распределения электронной плотности. Широкие возможности для изучения отдельных состояний молекул открыла лазерная спектроскопия (в различных диапазонах частот), отличающаяся исключительно высокой селективностью возбуждения. Импульсная лазерная спектроскопия позволяет анализировать строение короткоживущих молекул и их превращения в электромагнитное поле.
Разнообразную информацию о строении и свойствах молекул дает изучение их поведения во внешних электрических и магнитных полях.
Существует, однако, очень простой, хотя и не самый точный, способ вычисления радиусов молекул (или атомов) Он основан на том, что молекулы вещества, когда оно находится в твердом или жидком состоянии, можно считать плотно прилегающими друг к другу. В таком случае для грубой оценки можно считать, что объем V некоторой массы m вещества просто равен сумме объемов содержащихся в нем молекул. Тогда объем одной молекулы мы получим, разделив объем V на число молекул N.
Число молекул в теле массой m равно, как известно,
, где М — молярная масса вещества NA — число Авогадро. Отсюда объем V0 одной молекулы определяется из равенства .В это выражение входит отношение объема вещества к его массе. Обратное же отношение
есть плотность вещества, так чтоКакое число молекул воды содержится в сосуде? Найти массу молекулы и оценить ее размер. | Интерактивное сообщество — Решение задач по физике
Данные задачи: Вода в сосуде
| Объем воды | V | $10^{-5}$ | м3 |
|---|---|---|---|
| Температура воды | t | 4 | °C |
| Число молекул | N | ? | |
| Масса молекулы | $m_{0}$ | ? | |
| Размер молекулы | d | ? |
Число молекул можно найти, если определить число молей воды в занимаемом ею объеме
$ N = N_{A}ν $
Зная химическую формулу воды
$ H_{2}O $
с помощью периодической системы элементов Д.И. Менделеева находим ее молярную массу
$ μ = (1×2+16)×10^{-3}=18×10^{-3}\frac{кг}{моль} $
Число молей
$ ν = \frac{m}{μ} $
Массу вещества находим
$ m = ρV $
$ρ — плотность воды$ узнаем из таблиц физических величин, ее значение заданное при определенной температуре
Откуда находим число молекул
$ N = N_{A}\frac{ρV}{μ}=6,02×10^{23}\frac{1000×10^{-5}}{18×10^{-3}}=3,34×10^{23} молекул $
Масса одной молекулы
$ m_{0} = \frac{μ}{N_{A}}=\frac{18×10^{-3}}{6,02×10^{23}}=2,99×10^{-26} кг $
Чтобы оценить размер молекулы d, сделаем допущение: молекулы плотно прилегают друг к другу и образуют кубическую ячейку. Тогда объем молекулы
$ V_{0} = d^{3} $,
а
$ d = \sqrt{V_{0}} $
С другой стороны, объем занимаемый одной молекулой, можно найти зная объем воды и число молекул в этом объеме
$ V_{0} = \frac{V}{N}=\frac{μ}{ρN_{A}} $
И тогда находим
$ d = \sqrt{\frac{V}{N}}=\sqrt{\frac{10^{-5}}{3,34×10^{23}}}=\sqrt{\frac{μ}{ρN_{A}}}=3,11×10^{-10} м $
Ответ:
$ 3,34×10^{23} — число молекул; $
$ 2,99×10^{-26} кг — масса молекулы $
и
$ размер молекулы 3,11×10^{-10} м $
Каков диаметр любой молекулы? Если можно, каков диаметр молекулы масла
Молекула — это мельчайшая частичка вещества, которая может существовать отдельно и при этом сохранять его свойства. Например, если вы каким-либо образом разрушите молекулу сахара и она распадется на составляющие ее элементы, то они не будут обладать свойствами сахара, в том числе цветом и вкусом. Простые молекулы, например молекулы большинства газов, состоят из двух-трех атомов. А у некоторых газов, таких как гелий и неон, — вообще из одного. Однако существуют и такие, которые имеют в своем составе тысячи атомов, соединенных друг с другом в сложной последовательности. Часто бывает, что молекулы содержат несколько одинаковых атомов. Например, молекула воды состоит из двух атомов водорода и одного — кислорода. Молекула чистого природного каучука, из которого получают резину, состоит примерно из 75 000 атомов углерода и 100 000 атомов водорода. Так что, как видите, молекулы различных веществ сильно отличаются по своей величине. Так, размер молекулы воды измеряется миллиардными долями сантиметра. Молекула резины в тысячи раз больше. Форма молекул может быть так же самой разной: одни из них свернуты в клубочек, напоминающий футбольный мяч, а другие представляют собой длинные нити. Практически невозможно наглядно представить себе истинные размеры молекул. Всего лишь в 10 куб. см льда содержится более 300 миллионов миллиардов молекул (если записать это число цифрами, то получится тройка, после которой 20 нулей) . Вдобавок не следует забывать, что большую часть этого куска льда занимает пустое пространство.
Молекулы, за исключением фуллеренов (молекулы C_{60}), не шарообразные, чтобы измерять их диаметр. Характерный размер молекулы — примерно размер атома умноженный на количество атомов в молекуле, или надо смотреть на геометрическую форму молекулы. Например, ДНК вообще свёрнута в спираль, и её «размер» в нормальном состоянии определяется структурой этой спирали. Размер (диаметр) атома водорода примерно 0.1 нм, или 1 ангстрем (=2 боровских радиуса) . Более тяжёлые элементы, как углерод, имеют больший размер. У углерода около 0.3 нм.
только нет понятия молекула масла. масло это жир+вода (упрощенно, без белков) молекула жира очень широкая и длинная (этаки плоская) ДНК вон вообще 2 метра в длину
Размер частиц твёрдого вещества можно оценить по его плотности. Один моль вещества имеет массу M (молярная масса) , и плотность r, тогда объём этого количества вещества V = M / r. При этом в 1 моле вещества содержится число Авогадро частиц, т. е. на одну частицу приходится объём V0 = V / Na = M / r Na. Диаметр — корень кубический из этой величины. А размеры молекул масла были оценены в опыте Рэлея. Определённый объём масла разливается на поверхности воды в пятно некоторой площади. Зная объём и площадь можно найти толщину слоя. Рэлей предположил, что она равна размеру молекулы масла. Поищите в интернете. P.S. кстати, масло — это не жир и вода, а чистый жир (триглицерид ненасыщенных карбоновых кислот) ; молекулы его на самом деле длинные, но это сути дела не меняет.
такие оценки делаются в опытах по измерению площади S поверхности растекающегося масла известного объема V по воде ( капля масла капается в широкий таз с водой) d= V:S ПОЛУЧАЕТСЯ ДИАМЕТР ПОРЯДКА 10^-10м
Размер частиц твёрдого вещества можно оценить по его плотности. Один моль вещества имеет массу M (молярная масса) , и плотность r, тогда объём этого количества вещества V = M / r. При этом в 1 моле вещества содержится число Авогадро частиц, т. е. на одну частицу приходится объём V0 = V / Na = M / r Na. Диаметр — корень кубический из этой величины. А размеры молекул масла были оценены в опыте Рэлея. Определённый объём масла разливается на поверхности воды в пятно некоторой площади. Зная объём и площадь можно найти толщину слоя. Рэлей предположил, что она равна размеру молекулы масла.


 (
(