Физики впервые рассмотрели шестиугольную структуру льда на поверхности графита
Китайские физики впервые рассмотрели кристаллическую структуру двумерного слоя льда, который возникает на поверхности графита при температуре около 160 кельвинов. Для этого ученые численно рассчитали муаровый узор, который образует слой льда и слой графита, а потом сравнили его с «фотографиями» сканирующего туннельного микроскопа. Оказалось, что молекулы воды выстраиваются в шестиугольники, однако ребра этих шестиугольников не касаются друг друга, и решетка сильно отличается от стандартной сотовой структуры. При этом плотность упаковки достигает 0,134 молекул на квадратный ангстрем — это самая высокая плотность среди двумерных кристаллических льдов. Статья опубликована в Physical Review Letters.
Когда молекулы воды «приклеиваются» к поверхности металлов, они обычно выстраиваются в двухслойную сотовую структуру — шестиугольную решетку с общими гранями. При этом молекулы, стоящие в вершинах решетки, ориентируются по-разному, так что атомы кислорода попадают на два уровня разной высоты, а плоская структура превращается в гофрированную (puckered). По крайней мере, так ученые обычно описывают этот процесс.
По крайней мере, так ученые обычно описывают этот процесс.
Тем не менее, более точные наблюдения с помощью сканирующего туннельного микроскопа показывают, что на практике идеальная структура заметно искажается. В частности, около десяти лет назад группа ученых под руководством Микеля Салмерона (Miquel Salmerón) обнаружила, что на поверхности кристалла палладия(111) молекулы воды образуют необычную плоскую структуру вместо обычной гофрированной. Впоследствии физики подтвердили эти эффекты для других металлов, а также объяснили их теоретически. К сожалению, исследовать неметаллические поверхности оказалось гораздо сложнее. В то же время, образование тонкого слоя льда играет важную роль при смачивании или коррозии поверхности, а также при фолдинге белка и гетерогенном катализе. Поэтому определить структуру льда и характер происходящих процессов очень важно.
Хороший пример неметаллической поверхности, на которой удобно изучать кристаллизацию воды — это поверхность графита или графена, обладающая морфологической плоскостью и высокой степенью однородности. К настоящему моменту физики уже выяснили, что при температурах менее 100 кельвинов на поверхности графита образуется тонкая пленка аморфного льда, которая при дальнейшем отжиге до диапазона 140–180 кельвинов превращается в двухслойный кристаллический лед. Аморфный лед — это твердая фаза воды, которая не имеет дальнего порядка (кристаллической структуры), то есть напоминает стекло или воск. К сожалению, установить, в какую решетку выстраиваются молекулы, ученые не смогли, поскольку полагались только на спектроскопические или дифракционные методы.
К настоящему моменту физики уже выяснили, что при температурах менее 100 кельвинов на поверхности графита образуется тонкая пленка аморфного льда, которая при дальнейшем отжиге до диапазона 140–180 кельвинов превращается в двухслойный кристаллический лед. Аморфный лед — это твердая фаза воды, которая не имеет дальнего порядка (кристаллической структуры), то есть напоминает стекло или воск. К сожалению, установить, в какую решетку выстраиваются молекулы, ученые не смогли, поскольку полагались только на спектроскопические или дифракционные методы.
Группа исследователей под руководством Шэна Мэна (Sheng Meng) впервые рассмотрела структуру льда, в который собираются молекулы воды на поверхности высокоориентированного пиролитического графита. Сначала ученые «вырастили» на поверхности графита слой аморфного льда с помощью газового осаждения ультрачистой воды при температуре около 80 кельвинов. Затем исследователи медленно повышали температуру образца, сублимируя лед и обнажая смачивающий слой (слой, который лежит между жидкой водой и графитом). Параллельно ученые наблюдали за поверхностью с помощью сканирующего туннельного микроскопа (СТМ) компании Unisoku, который работает при давлениях порядка 10−13 атмосфер (сверхвысокий вакуум). Когда образец нагрелся до 140 кельвинов, практически весь аморфный лед испарился. При температуре около 150 кельвинов смачивающий слой начал кристаллизоваться и формировать небольшие области обычного льда. При температуре выше 160 кельвинов смачивающий слой полностью исчез, превратившись в разрозненные двумерные островки кристаллического льда — структуру, ради которой затевалось исследование.
Параллельно ученые наблюдали за поверхностью с помощью сканирующего туннельного микроскопа (СТМ) компании Unisoku, который работает при давлениях порядка 10−13 атмосфер (сверхвысокий вакуум). Когда образец нагрелся до 140 кельвинов, практически весь аморфный лед испарился. При температуре около 150 кельвинов смачивающий слой начал кристаллизоваться и формировать небольшие области обычного льда. При температуре выше 160 кельвинов смачивающий слой полностью исчез, превратившись в разрозненные двумерные островки кристаллического льда — структуру, ради которой затевалось исследование.
Используя сканирующий туннельный микроскоп, ученые рассмотрели кристаллическую структуру сформировавшегося двумерного льда. Точнее, физики получили набор различных муаровых узоров — изображений, которые получаются при повороте слоя льда относительно верхнего слоя графита. Это указывало на то, что молекулы воды также объединяются в шестиугольную решетку, постоянная которой отличается от постоянной шестиугольной решетки графитового слоя. Рассчитывая муаровый узор при различных значениях постоянной решетки и угла поворота, ученые подогнали узоры под картинки, которые наблюдались на практике. К сожалению, такой метод не позволяет точно «разглядеть» строение решетки. Тем не менее, физики выяснили, что плотность упаковки молекул воды составляет примерно 0,134 молекулы на квадратный ангстрем. Это самое высокое значение среди всех наблюдавшихся на практике двумерных кристаллических льдов.
Рассчитывая муаровый узор при различных значениях постоянной решетки и угла поворота, ученые подогнали узоры под картинки, которые наблюдались на практике. К сожалению, такой метод не позволяет точно «разглядеть» строение решетки. Тем не менее, физики выяснили, что плотность упаковки молекул воды составляет примерно 0,134 молекулы на квадратный ангстрем. Это самое высокое значение среди всех наблюдавшихся на практике двумерных кристаллических льдов.
Затем исследователи численно смоделировали кристаллическую решетку льда с помощью теории функционала плотности, чтобы уточнить строение льда. Как и ожидалось, в описанных условиях молекулы воды объединялись в шестиугольники, однако ребра этих шестиугольников не касались друг друга. Назвать структуру плоской тоже было нельзя, поскольку ее толщина достигала 1,5 ангстрем. В результате строение решетки сильно отличалось от привычной сотовой структуры. Как бы то ни было, плотность упаковки и муаровые узоры для численно рассчитанной решетки совпали с экспериментом. Поэтому ученые считают, что эта структура действительно описывает реальность.
Поэтому ученые считают, что эта структура действительно описывает реальность.
В экстремальных условиях вода может находиться в огромном числе фазовых состояний, и ученые до сих пор открывают что-то новое. Например, в июле 2017 года американские физики изготовили лед с рекордно высокой долей кубической структуры, который считается метастабильным и практически не встречается в природе. В сентябре 2017 японские ученые с помощью численного моделирования показали, что цеолитный лед, который имеет низкую плотность (около 0,5 грамм на кубический сантиметр) и пористую структуру, остается стабильным при давлении порядка одного бара и температуре менее 80 кельвинов. Кроме того, в этом году исследователи из США экспериментально зафиксировали переход между различными жидкими фазами переохлажденной воды и объяснили расхождения экспериментов по образованию льда-VII.
Дмитрий Трунин
Нашли опечатку? Выделите фрагмент и нажмите Ctrl+Enter.
Ученые открыли новую кристаллическую форму льда
1427
Добавить в закладки
Исследователи из Инсбрукского университета (Австрия) определили кристаллическую структуру экзотического льда XIX, использовав метод нейтронной дифракции, сообщает пресс-служба вуза. Открытие подробно описано в журнале Nature Communications.
Лед – универсальное вещество. В снежинках или кубиках льда атомы
кислорода расположены гексагонально (в форме шестиугольника).
Такая форма известна как лед I. На самом деле это не идеальные
кристаллы, а неупорядоченные системы, в которых молекулы воды
случайным образом ориентированы в разных пространственных
направлениях. До сих пор было известно 18 кристаллических форм
льда, которые различаются расположением атомов. Различные типы
льда, известные как полиморфы, образуются в зависимости от
давления и температуры и обладают очень разными свойствами.
Например, их температуры плавления различаются на несколько сотен
градусов по Цельсию.
Когда обычный лед I сильно охлаждается, атомы водорода могут периодически располагаться в дополнение к атомам кислорода, если эксперимент проводится правильно. Если температура опускается ниже минус 200 градусов Цельсия, может получиться лёд XI, в котором все молекулы воды упорядочены по определенной схеме. Такие упорядоченные формы льда отличаются от неупорядоченных родительских форм, особенно электрическими свойствами.
В данной исследовании химики взяли в качестве родительской формы
лёд VI, которая образуется при высоком давлении, например, в
мантии Земли. Подобно гексагональному льду, эта форма льда под
высоким давлением не является полностью упорядоченным кристаллом.
Более 10 лет назад исследователи из Инсбрукского университета
создали вариант этого льда, упорядоченный по водороду, который
вошел в учебники как лед XV. Изменив производственный процесс,
три года назад учёным впервые удалось создать вторую производную
форму льда VI. Для этого они значительно замедлили процесс
охлаждения и увеличили давление примерно до 20 кбар. Это
позволило им расположить атомы водорода в кислородной решетке и
образовать лед XIX. «В то время мы нашли четкие доказательства
того, что это новый упорядоченный вариант, но мы не смогли
выяснить кристаллическую структуру», – отмечают авторы работы.
Теперь команде удалось сделать это, использовав нейтронную
дифракцию.
Изменив производственный процесс,
три года назад учёным впервые удалось создать вторую производную
форму льда VI. Для этого они значительно замедлили процесс
охлаждения и увеличили давление примерно до 20 кбар. Это
позволило им расположить атомы водорода в кислородной решетке и
образовать лед XIX. «В то время мы нашли четкие доказательства
того, что это новый упорядоченный вариант, но мы не смогли
выяснить кристаллическую структуру», – отмечают авторы работы.
Теперь команде удалось сделать это, использовав нейтронную
дифракцию.
При исследовании с помощью дифракции нейтронов необходимо заменить легкий водород в воде дейтерием («тяжелым водородом»). Но это, к сожалению, также меняет временные рамки для формирования льда.
Чтобы преодолеть эту трудность, ученые добавили немного обычной
воды в «тяжелую воду», что, как оказалось, значительно ускорило
процесс. Получив лед таким образом, ученые наконец смогли
измерить нейтронные данные на приборе высокого разрешения HRPD и
определить кристаллическую структуру льда XIX. Для этого
потребовалось найти лучшую кристаллическую структуру из
нескольких тысяч кандидатов по измеренным данным — очень похоже
на поиск иголки в стоге сена. Японская исследовательская группа
подтвердила результат коллег из Инсбрука в другом эксперименте
при других условиях давления. Обе статьи опубликованы совместно в
Для этого
потребовалось найти лучшую кристаллическую структуру из
нескольких тысяч кандидатов по измеренным данным — очень похоже
на поиск иголки в стоге сена. Японская исследовательская группа
подтвердила результат коллег из Инсбрука в другом эксперименте
при других условиях давления. Обе статьи опубликованы совместно в
Хотя на Земле много обычного льда и снега, никаких других форм, кроме основной – первой – на поверхности нашей планеты не встречается. Остальные можно получить только в исследовательских лабораториях. Тем не менее, лед VI и лед VII, находящиеся под высоким давлением, можно встретить как включения в алмазах. Многие разновидности водяного льда образуются на просторах космоса при особых условиях давления и температуры. Они встречаются, например, на небесных телах, таких как спутник Юпитера Ганимед, который покрыт слоями льда различных видов.
Лед XV и лед XIX представляют собой первую родственную пару в
физике льда, в которой решетка кислорода одинакова, но атомы
водорода расположены по-разному.
[Иллюстрация: UNI INNSBRUCK]
Автор Материал Оформила Татьяна Матвеева
вода дейтерий лед лед XIX нейтронная дифракция формы льда
Источник: www.uibk.ac.at
Информация предоставлена Информационным агентством «Научная Россия». Свидетельство о регистрации СМИ: ИА № ФС77-62580, выдано Федеральной службой по надзору в сфере связи, информационных технологий и массовых коммуникаций 31 июля 2015 года.
НАУКА ДЕТЯМ
Ученые разработали биоразлагаемые нетканые материалы для ускоренного заживления ран
14:00 / Медицина, Химия
Самая рождественская сказка. Эрнст Теодор Амадей Гофман, «Щелкунчик»
13:00 / Досуг, Персона, Чтение
Похолодание на 10 тысяч лет «изгнало» неандертальцев с Северо-Западного Кавказа
12:00 / Археология, Климат
«Уродилась Коляда накануне Рождества».
10:30 / История, Этнография
Нитрид бора очистит сточные воды от антибиотиков
14:00 / Химия
Ученые Пермского Политеха изучили стабильность «основы» для потенциального анальгетика
12:00 / Химия
Праздник на орбите
10:30 / Космонавтика, Наука и общество
Казанские ученые первыми в России вырастили кристалл LiGdF4 с заданными магнитными свойствами
14:00 / Физика
Тяжелые металлы и органические загрязнители активировали почвенную плесень
12:00 / Биология
Как в СССР заново создавали Новый год? Лекция кандидата исторических наук Марьяны Архиповой
10:30 / История, Наука и общество, Этнография
Памяти великого ученого. Наука в глобальном мире. «Очевиднное — невероятное» эфир 10.05.2008
04.03.2019
Памяти великого ученого. Нанотехнологии. «Очевидное — невероятное» эфир 3.08.2002
Нанотехнологии. «Очевидное — невероятное» эфир 3.08.2002
04.03.2019
Вспоминая Сергея Петровича Капицу
14.02.2017
История новогодних праздников
01.08.2014
Лед, вода и молекулы. Наш зимний мир
Почему у снежинок шесть сторон?
В 1611 году люди не знали о молекулах, но когда философ Иоганн Кеплер увидел у себя на рукаве шестиконечную снежинку, он подумал, что ее симметрия объясняется тем, что она состоит из мельчайших шестиугольных (шестигранных) частиц. Кеплер поднял несколько увлекательных вопросов о фундаментальной природе материи, и он был во многом прав. Изысканные шестигранные формы, которые снова и снова можно увидеть в падающих с неба снежинках и в снежном покрове, обусловлены природой и формой молекулы воды.
Наблюдения философа Иоганна Кеплера за 6-сторонней симметрией, наблюдаемой в снежинках, намекнули на основную молекулярную структуру воды. (Общественное достояние {{PD-old-100}})
Первая удачная фотография снежинки была сделана в 1885 году Уилсоном А. «Снежинка» Бентли. Основываясь на более чем 5000 фотографий снежинок, Бентли пришел к выводу, что нет двух абсолютно одинаковых снежинок. Фото Уилсона А. Бентли (Public Domain {{PD-US-old}})
«Снежинка» Бентли. Основываясь на более чем 5000 фотографий снежинок, Бентли пришел к выводу, что нет двух абсолютно одинаковых снежинок. Фото Уилсона А. Бентли (Public Domain {{PD-US-old}})
Кристаллы снега могут расти горизонтально вдоль своей основной грани, образуя плоскую шестиугольную пластину или дендрит. Они также могут расти вертикально вдоль своих граней призмы, в результате чего образуются кристаллы в форме столбцов и игл. Большинство снежных кристаллов растут в обоих направлениях, что приводит к ошеломляющему множеству различных типов снежных кристаллов. Иллюстрация Мэтью Штурма
Лед против воды
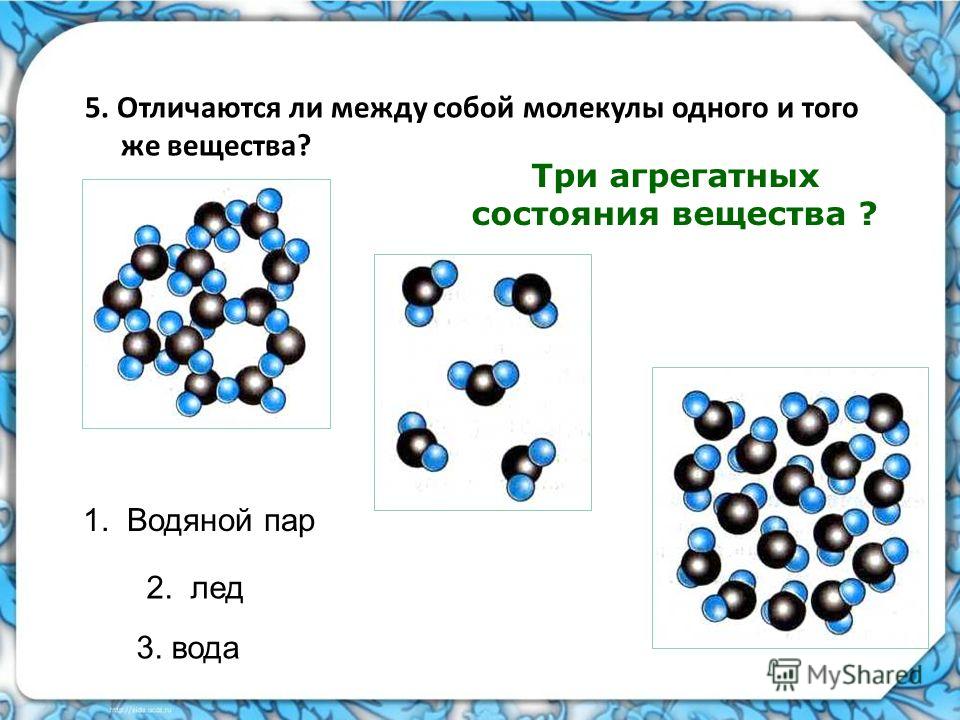
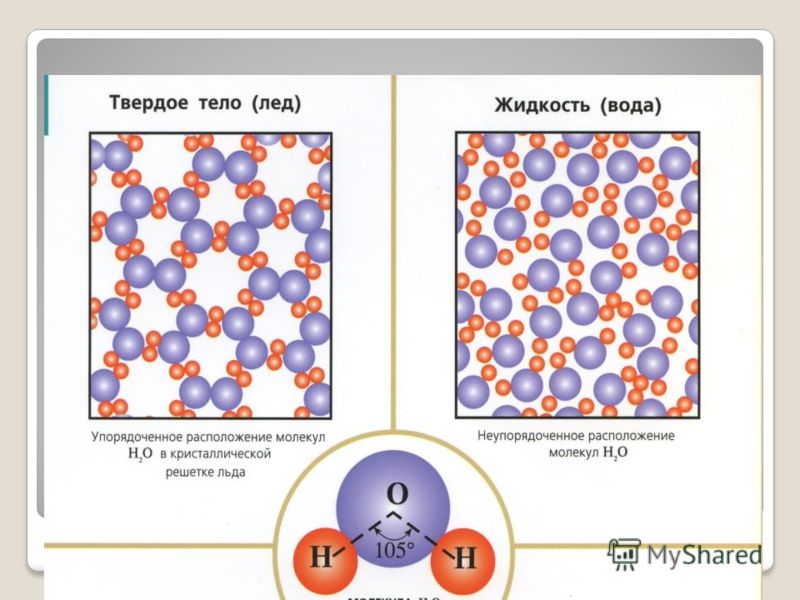
Землю, «водную планету», можно легко назвать «полуледяной планетой», потому что температура зимой на большей части Земли достаточно низка, чтобы вода замерзала, поэтому существуют огромные ледяные шапки в полярных районах. И вода, и лед состоят из тетраэдрических молекул, состоящих из двух атомов водорода и одного атома кислорода (H 2 0), связанных друг с другом прочными связями. Лед имеет более жесткую и организованную структуру, чем вода, которая состоит из более рыхлых цепочек связанных молекул, которые могут скользить ближе друг к другу. Вещества, в которых молекулы более плотно упакованы, имеют более высокую плотность, чем те, в которых молекулы имеют большее расстояние между собой. Вот почему лед (менее плотный) плавает в воде (более плотный).
Лед имеет более жесткую и организованную структуру, чем вода, которая состоит из более рыхлых цепочек связанных молекул, которые могут скользить ближе друг к другу. Вещества, в которых молекулы более плотно упакованы, имеют более высокую плотность, чем те, в которых молекулы имеют большее расстояние между собой. Вот почему лед (менее плотный) плавает в воде (более плотный).
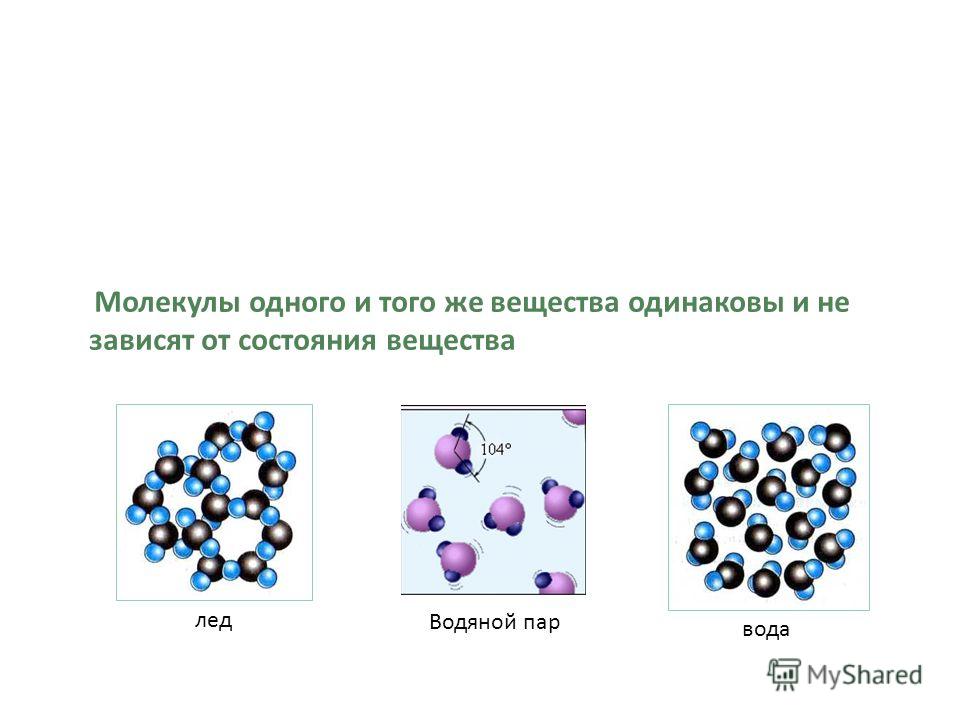
. Справа: жидкая вода (слева на изображении), молекулы h30 быстро перемещаются, потому что у них больше энергии, чем в твердой (ледяной) форме (на прямо на картинке). Когда h30 замерзает, молекулы замедляются, образуя организованную решетчатую структуру. Гексагональное расположение молекул h30 в твердом состоянии является причиной того, что снежные кристаллы имеют гексагональную симметрию. Изображение адаптировано из Британской энциклопедии Эндрю Старка на Quora (Условия предоставления услуг Quora)
Когда h30 замерзает, молекулы замедляются, образуя организованную решетчатую структуру. Гексагональное расположение молекул h30 в твердом состоянии является причиной того, что снежные кристаллы имеют гексагональную симметрию. Изображение адаптировано из Британской энциклопедии Эндрю Старка на Quora (Условия предоставления услуг Quora)
Молекула воды (H 2 0) состоит из одного атома кислорода (O) и двух атомов водорода (H). Атомы Н и О из разных молекул тоже притягиваются друг к другу. Связи между соседними молекулами H 2 0 называются водородными связями. Иллюстрация Мэтью Штурма
Что такого особенного в H
2 0? Некоторые важные характеристики водыЛюди на 60% состоят из воды, поэтому мы склонны считать свойства льда и воды само собой разумеющимися, но они являются экстремальными способами, которые влияют на всю жизнь и климат Земли.
Вода плотнее льда.
У большинства веществ твердое состояние более плотное, чем жидкое, но вода отличается! Лед менее плотный (917 кг на кубический метр), чем жидкая вода (1000 кг на кубический метр). Другой способ думать об этом состоит в том, что когда определенное количество жидкой воды замерзает в лед, он увеличивается в объеме. Вот почему:
Другой способ думать об этом состоит в том, что когда определенное количество жидкой воды замерзает в лед, он увеличивается в объеме. Вот почему:
Фото Lavivm на Pixabay (лицензия Pixabay)
Фото Доминикуса Йоханнеса Бергсма с Викисклада (CC-BY-SA-4.0)
Лед плавает, поэтому на дне океана нет ледников, и мы можем кататься на коньках по замерзшим прудам.
Когда трубы замерзают, они лопаются, а ледяная вода, замерзая в трещинах, раскалывает камни.
Вода обладает высокой теплоемкостью и скрытой теплотой
Из всех веществ на Земле вода обладает самой высокой теплоемкостью, которая представляет собой количество энергии (тепла), необходимое для повышения ее температуры. Он также имеет самую высокую скрытую теплоту, которая представляет собой количество энергии, необходимое для плавления твердого вещества в жидкость или жидкого вещества в газ. Вот почему:
Федеральное управление автомобильных дорог Фото / Martin Gyorgyfalvy (Public Domain) Фото Мэтью Штурма Снежные сугробы сохраняются в горах, где прохладнее, чем в долинах, в течение всего лета.
Снег в горах тает постепенно, стекая в ручьи и реки в течение всей весны и начала лета.
Вода и лед могут сосуществовать.
При низких температурах жидкая вода по-прежнему сосуществует со льдом в виде тонкого слоя. Вот почему:
Фото Гантаса Вайчуленаса из Pexels (лицензия Pexels)Снег и лед скользкие, что позволяет нам кататься на санках и коньках.
Снег отражает солнечный свет
Снег отражает видимый солнечный свет лучше, чем любое другое природное вещество на Земле, часто отбрасывая 85% света обратно в космос. Вот почему:
Фото Корди Вале на Pixabay (лицензия Pixabay)Снег помогает охлаждать планету, отражая, а не поглощая солнечную радиацию.
Исследовать — Все о льду
Исследовать — Все о льде — Удивительный расширяющийся ледО НАС
- События
- Исследовать
- Участие ученых
- Образовательные ресурсы
- Наша Солнечная система, наша Вселенная
- О нас
Новости науки о Земле и космосе
Преподаватели
Студенты
- Мероприятия
- Исследовать
- Участие ученых
- Образовательные ресурсы
- Наша Солнечная система, наша Вселенная
- О нас
- Новости науки о Земле и космосе для преподавателей
- Новости планетарной науки для студентов
Обзор
Дети экспериментируют с замерзающей водой, чтобы обнаружить еще одно особое свойство льда: он менее плотный в твердом состоянии (лед), чем в жидком (вода). Удивительный расширяющийся лед! — это «ночная» деятельность, требующая 20 минут подготовки, ночного замораживания эксперимента и 10 минут последующего обсуждения.
Удивительный расширяющийся лед! — это «ночная» деятельность, требующая 20 минут подготовки, ночного замораживания эксперимента и 10 минут последующего обсуждения.
Какой смысл?
- Вещества существуют в различных состояниях; т. е. твердое, жидкое, газообразное
- Вода — уникальное вещество, потому что ее твердое состояние — лед — менее плотное, чем ее жидкое состояние.
- Физические свойства — характеристики вещества. Они не меняются. Физические свойства включают цвет, запах, температуру замерзания/плавления и плотность. Физические свойства водяного льда отличаются от физических свойств жидкой воды.
- Плотность – это мера массы (количества вещества) на единицу объема (пространства) вещества.
Материалы
Для группы:
- Несколько кувшинов с водой
- Подносы для стаканов с водой
- Бумажные полотенца на случай пролива
- Доступ к кухонным или почтовым весам (дополнительно)
Для каждого ребенка:
- Его/ее Ice Investigator Journal
Для каждого ребенка или группы детей:
- 2 маленьких бумажных стаканчика (4 или 6 унций)
- Фольга для покрытия чашек
- Маркер для надписей на чашках
- Линейка
Для координатора:
- Справочная информация
Подготовка
- Наполните кувшины водой до уровня, который дети смогут налить в чашки.
 Каждому ребенку потребуется достаточно воды, чтобы наполнить обе чашки.
Каждому ребенку потребуется достаточно воды, чтобы наполнить обе чашки. - Если вы собираетесь выполнить задание Верхушка айсберга в другой день, запланируйте вернуть чашки со льдом в морозильную камеру, чтобы они оставались замороженными.
Задание
- Предложите детям подумать о том, что они узнали о льде и воде.
- Какое состояние воды у льда? Твердое тело.
- Что должно произойти, чтобы вода превратилась в лед? Он должен замерзнуть.
- При какой температуре вода превращается в лед? 32°F или 0°C.
- Могут ли они вспомнить примеры из своей жизни, когда они делают лед из воды? Некоторые дети могут рассказать, что они приготовили кубики льда или фруктовое мороженое в своих морозильных камерах.
- Что еще они знают из своего опыта о льде и воде? Некоторые дети могут заметить, что лед «растет» или расширяется в форме для кубиков льда.

- Раздайте детям материалы и их журналы Ice Investigator . Пусть каждый ребенок напишет на двух чашках свои имена сбоку.
- Пусть каждый ребенок наполнит свои две чашки водой до одинакового уровня от половины до трех четвертей. Они должны тщательно отметить уровень воды в чашках.
- Пусть аккуратно накроют каждую чашку фольгой и закрепят ее (как крышку).
- Попросите детей взвесить свои чашки с водой на кухонных весах и отметить вес на чашке.
- Расскажите детям, что теперь вы заморозите одну из чашек с водой для каждой группы на ночь или до следующей встречи.
- Что, по их мнению, произойдет?
- Почему они закрыли чашки фольгой? Это предотвращает другое изменение состояния — превращение жидкой воды в водяной пар в процессе испарения!

Примечание для ведущего: Если хотите, вы можете расширить это задание и изучить процесс испарения, предложив детям использовать три чашки вместо двух. Они должны приготовить третью чашку так же, как и две другие, но оставить ее открытой. Через несколько дней они обнаружат, что уровень воды падает. Часть воды испарилась или превратилась из жидкости в водяной пар.
- Попросите детей поставить одну из своих чашек с водой на поднос «идет в морозилку», а другую — на поднос «остается в комнате». Поместите чашки для заморозки в морозильную камеру на ночь. Достаньте их из морозилки непосредственно перед тем, как увидеть детей во время следующего сеанса.
- После того, как вода в чашках замерзнет, верните по две чашки в каждую группу. Предложите детям сравнить свои чашки.
- Что, по их наблюдениям, произошло? 901:10 Вода превратилась в лед.
- Как называется переход из одной формы вещества в другую? Изменение состояния!
- Что они заметили относительно уровня воды и льда по сравнению с линиями, которые они начертили, чтобы отметить уровни воды изначально? Лед выше линии, которую они нарисовали, но вода все еще на той же линии.

- Как это может быть? Являются ли лед и вода одной и той же «вещью» (составом)? Да. Что случилось, когда лед замерз? Он «вырос» или расширился. Некоторые дети могут сказать, что воды добавили больше, поэтому и льда больше.
- Попросите детей взвесить свои чашки.
- Есть ли разница в весе? Нет (кроме небольшой изменчивости шкалы, гири должны быть одинаковыми).
- Какой вывод могут сделать дети о количестве воды, содержащейся во льду? Это то же самое, что и количество воды, с которой они стартовали.
- Расскажите детям, что плотность льда и воды различается. В своем эксперименте у детей было одинаковое количество материала в обеих чашках — одинаковое количество воды, — но когда они заморозили воду, объем изменился. Количество воды было «растянуто», чтобы сделать больший объем льда.
- Что должны были сделать дети, чтобы лед наполнил чашку только до линии, когда вода замерзнет? Добавить меньше воды!
 Если бы у вас был такой же объем льда или лед, который доходил бы только до линии на чашке, он содержал бы меньше материала (воды), чем вода того же объема.
Если бы у вас был такой же объем льда или лед, который доходил бы только до линии на чашке, он содержал бы меньше материала (воды), чем вода того же объема.Примечание ведущего: Плотность — это масса на единицу объема или отношение количества вещества в объекте к его объему, или проще говоря:
- Масса = количество «вещей»
- Вес = насколько тяжел этот «материал» (Вес определяется силой гравитационного притяжения объекта, которая является свойством массы планеты, на которой находится «материал». Чем больше гравитационное притяжение, тем больше «вещь» весит.)
- Плотность = насколько плотно упакован материал
- Объем = площадь пространства, которое занимает «материал»
Если мы применим эту информацию к чашкам, чашка с водой и чашка со льдом имеют одинаковую массу, то есть количество «вещества». Поскольку у них было одинаковое количество «материала», они имеют одинаковый вес.
 0005
0005«Вещество» (молекулы) в воде более плотно упаковано, чем во льду, поэтому вода имеет большую плотность, чем лед. Не позволяйте тому факту, что лед является твердым, обмануть вас!
При замерзании вода расширяется. Итак, лед имеет больший объем (занимает больше места, но имеет меньшую плотность), чем вода.
Расскажите детям, что это особое свойство воды. По мере того как большинство веществ становятся холоднее, их материал (молекулы) сжимается все ближе и ближе друг к другу, как пингвины, прижавшиеся друг к другу, чтобы согреться. Молекулы воды, однако, не любят сжиматься. Они рассредоточиваются, как акробаты, формируя кристаллы льда, как мы видим в снежинках и морозе.Примечание ведущего: Молекулы воды в жидком состоянии словно свисают вместе, как капли, но в твердом (замороженном) состоянии им нужно свое пространство.
Молекула воды похожа по очертаниям на Микки Мауса, с двумя атомами водорода, расположенными на одном конце атома кислорода.
 Атомы кислорода заряжены положительно, а атомы водорода — отрицательно, поэтому молекулы воды прилипают друг к другу, как крошечные магниты. Водородные «уши» образуют рыхлые связи, называемые водородными связями, с кислородными «гранями» других молекул воды.
Атомы кислорода заряжены положительно, а атомы водорода — отрицательно, поэтому молекулы воды прилипают друг к другу, как крошечные магниты. Водородные «уши» образуют рыхлые связи, называемые водородными связями, с кислородными «гранями» других молекул воды. Каждая молекула воды состоит из двух атомов водорода (белый) и одного атома кислорода (красный). Атомы водорода не расположены по разные стороны от атома кислорода; они встречаются на одном конце. Изображение изменено с: http://commons.wikimedia.org/wiki/File:h3O_(water_molecule).jpg.
В кристаллах льда их водородные связи связывают их вместе, как акробатов, стоящих друг на друге с вытянутыми руками и ногами. Это обеспечивает большее пространство между молекулами в кристаллической структуре льда, чем молекулы жидкой воды. В результате 9Лед 0130 менее плотный, чем жидкая форма. Вода — единственное известное неметаллическое вещество, расширяющееся при замерзании; его плотность уменьшается, и он расширяется примерно на 9% по объему.



 Каждому ребенку потребуется достаточно воды, чтобы наполнить обе чашки.
Каждому ребенку потребуется достаточно воды, чтобы наполнить обе чашки.
 Если бы у вас был такой же объем льда или лед, который доходил бы только до линии на чашке, он содержал бы меньше материала (воды), чем вода того же объема.
Если бы у вас был такой же объем льда или лед, который доходил бы только до линии на чашке, он содержал бы меньше материала (воды), чем вода того же объема. 0005
0005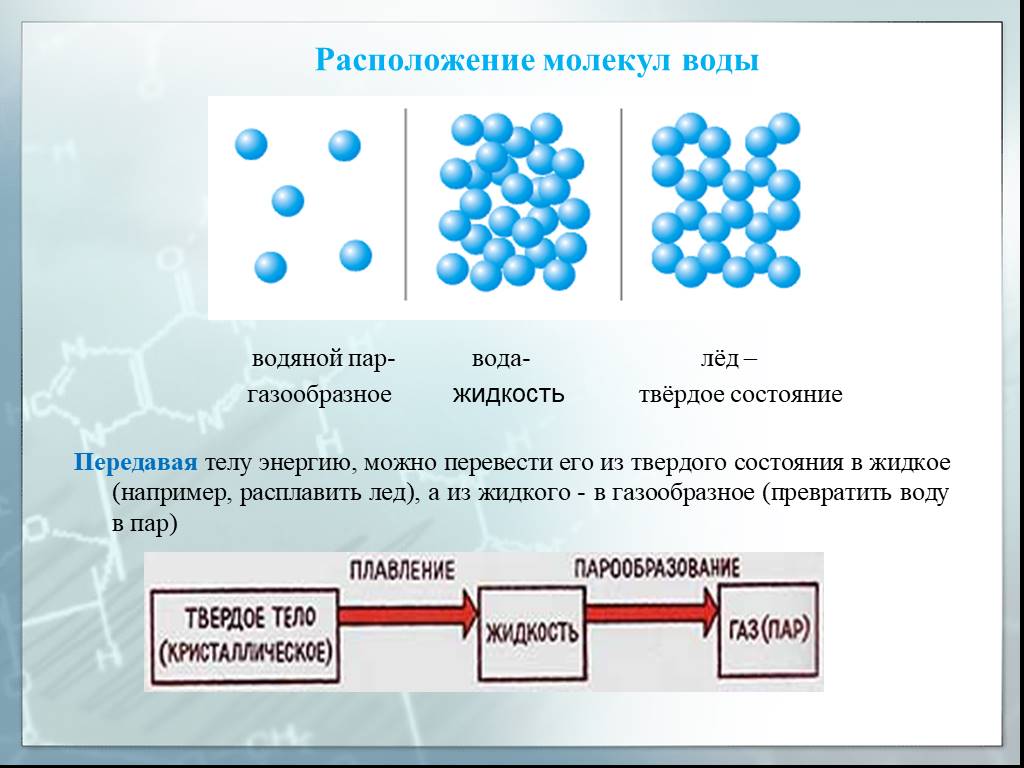 Атомы кислорода заряжены положительно, а атомы водорода — отрицательно, поэтому молекулы воды прилипают друг к другу, как крошечные магниты. Водородные «уши» образуют рыхлые связи, называемые водородными связями, с кислородными «гранями» других молекул воды.
Атомы кислорода заряжены положительно, а атомы водорода — отрицательно, поэтому молекулы воды прилипают друг к другу, как крошечные магниты. Водородные «уши» образуют рыхлые связи, называемые водородными связями, с кислородными «гранями» других молекул воды. 