Физики построили универсальную модель воды
Характерная гексагонально-кольцевая структура протонноупорядоченного льда II.
Иллюстрация NPL/University of Edinburgh
Исследователи из Национальной физической лаборатории (NPL) Великобритании, Эдинбургского университета и IBM заявили, что им удалось создать модель воды, в которой глобальные свойства жидкости выводятся из ее локального устройства. С соответствующей работой можно ознакомиться в Proceedings of the National Academy of SciencesВ 1900 году немецкий физик Пауль Друде предложил для описания свойств металлов модель, которая позже была названа его именем. В этой модели использовалась классическая кинетическая теоремя — электроны представляли собой твердые шарики, которые сталкиваются между собой и натыкаются на сравнительно массивные ионы. Позже модель была доработана Хендриком Лоренцом, поэтому иногда ее называют моделью Друде-Лоренца. Несмотря на простоту, эта модель способна описать эффект Холла, удельную проводимость, теплопроводность в металлах и многое другое.
В начале XXI века модель Друде была доработана для нужд моделирования взаимодействия молекул, например, в биологии — возникла так называемая частица Друде или осциллятор Друде. В новой схеме к модельным атомам (твердые сферы) с помощью пружинок присоединяются безмассовые частицы с дробным электрическим зарядом. Динамика взаимодействия молекул, таким образом, оказывается связана с колебанием этих самых частиц вокруг атомов. Такие модели способны демонстрировать, например, эффект поляризации. В середине 2000-х их применяли для создания довольно удобных для вычислений молекул воды.
Гармонический осциллятор в квантовой механике представляет собой квантовый аналог простого гармонического осциллятора. В нем рассматривают не силы, действующие на частицу, а гамильтониан, то есть полная энергию системы. При этом считается, чтопотенциальная энергия квадратично (как и в классическом случае) зависит от координат. Модель квантового гармонического осциллятора служит первым приближением для описания колебательного движения в молекулах и является одной из немногих систем, для которой может быть получено точное решение уравнения Шредингера.
Вода обладает целым рядом необычных свойств, нетипичных для других жидкостей и играющей важнейшую роль в химических и биологических процессах. Так, максимум ее плотности достигается при температуре в 4 градуса Цельсия (выше точки замерзания), позволяя водоемам замерзать сверху вниз, что позволяет их обитателям выживать зимой.
На данный момент многие из особенностей воды, благоприятные для известных форм жизни, с теоретической точки зрения остаются недостаточно ясными. Предпринимались многочисленные попытки понять, как именно молекула такой сравнительной простоты может вести себя столь сложным и необычным образом в широком диапазоне давлений и температур. Однако пока все разработанные учеными модели успешно описывали поведение этой жидкости только для каких-то конкретных диапазонов температуры и давлений.
Новая модель, разработанная группой Сохана, претендует на первое полноценное решение этой проблемы, охватывающее свойства воды от точки фазового перехода газ-жидкость до ее критической точки (374 градуса Цельсия при давлении 218 атмосфер). Ранее в этом году исследователи уже использовали эту модель для описания молекулярной структуры поверхности жидкой воды, соответствующая работа была опубликована в Physical Chemistry Chemical Physics.
Математическая модель воды
Здравствуйте, с большим удовольствием читаю статьи на вашем сайте о воде. Я недавно тоже заинтересовалась изучением воды и различных фиизческих процессов с ней связанных. Но, так как я занимаюсь теоретической физикой, меня в первую очередь волнует вопрос о построении теории воды. Может быть вы располагаете какой-нибудь информацией о работах в области построения математической модели жидкой воды ? Как я понимаю, в настоящее время такой теории не существует. Есть даже мнение некоторых учёных, что она вообще не будет построена.
Мария
Здравствуйте, Мария.
Спасибо за ваш интерес к нашему сайту.
Существует большое количество различных теорий и моделей, объясняющих структуру и свойства воды. Общим у них является представление о водородных связях как основном факторе, определяющем образование структурированных ассоциатов.
Первая модель воды появилась в 20-х годах прошлого века. Когда в 20-е годы определили структуру льда, оказалось, что молекулы воды в кристаллическом состоянии образуют трёхмерную непрерывную сетку, в которой каждая молекула имеет четырёх ближайших соседей, расположенных в вершинах правильного тетраэдра. В 1933 году Дж. Бернал и П. Фаулер предположили, что подобная сетка существует и в жидкой воде. Поскольку вода плотнее льда, они считали, что молекулы в ней расположены не так, как во льду, то есть подобно атомам кремния в минерале тридимите, а так, как атомы кремния в более плотной модификации кремнезёма — кварце. Увеличение плотности воды при нагревании от 0 до 4°C объяснялось присутствием при низкой температуре тридимитовой компоненты. Таким образом, модель Бернала — Фаулера сохранила элемент двухструктурности, но главное их достижение — идея непрерывной тетраэдрическои сетки. Тогда появился знаменитый афоризм И. Ленгмюра: „Океан — одна большая молекула“. Излишняя конкретизация модели не прибавила сторонников теории единой сетки.
Только в 1951 году Дж. Попл создал модель непрерывной сетки, которая была не так конкретна, как модель Бернала — Фаулера. Попл представлял воду как случайную тетраэдрическую сетку, связи между молекулами в которой искривлены и имеют различную длину. Модель Попла объясняет уплотнение воды при плавлении искривлением связей. Когда в 60–70-е годы появились первые определения структуры льдов II и IX, стало ясно, как искривление связей может приводить к уплотнению структуры. Модель Попла не могла объяснить немонотонность зависимости свойств воды от температуры и давления так хорошо, как модели двух состояний. Поэтому идею двух состояний ещё долго разделяли многие учёные.
Рис. Модель непрерывной сетки
Во второй половине XX века помимо „континуальных“ моделей (модель Попла), возникли две группы „смешанных“ моделей: кластерные и клатратные. В первой группе вода представала в виде кластеров из молекул, связанных водородными связями, которые плавали в море молекул, в таких связях не участвующих. Модели второй группы рассматривали воду как непрерывную сетку (обычно в этом контексте называемую каркасом) водородных связей, которая содержит пустоты; в них размещаются молекулы, не образующие связей с молекулами каркаса. Нетрудно было подобрать такие свойства и концентрации двух микрофаз кластерных моделей или свойства каркаса и степень заполнения его пустот клатратных моделей, чтобы объяснить все свойства воды, в том числе и знаменитые аномалии.
Среди кластерных моделей наиболее яркой оказалась модель Г. Немети и Х. Шераги: предложенные ими картинки, изображающие кластеры связанных молекул, которые плавают в море несвязанных молекул, вошли во множество монографий.
Первую модель клатратного типа в 1946 году предложил О.Я. Самойлов: в воде сохраняется подобная гексагональному льду сетка водородных связей, полости которой частично заполнены мономерными молекулами. Л. Полинг в 1959 году создал другой вариант, предположив, что основой структуры может служить сетка связей, присущая некоторым кристаллогидратам.
В течение второй половины 60-х годов и начала 70-х наблюдается сближение всех этих взглядов. Появлялись варианты кластерных моделей, в которых в обеих микрофазах молекулы соединены водородными связями. Сторонники клатратных моделей стали допускать образование водородных связей между пустотными и каркасными молекулами. То есть фактически авторы этих моделей рассматривают воду как непрерывную сетку водородных связей. И речь идёт о том, насколько неоднородна эта сетка (например, по плотности).
Представлениям о воде как о водородно-связанных кластерах, плавающих в море лишённых связей молекул воды, был положен конец в начале восьмидесятых годов, когда Г. Стэнли применил к модели воды теорию перколяции, описывающую фазовые переходы воды. Так появилась смешанная кластерно-фрактальная модель воды.
Рис. Современная клатратно-фрактальная модель воды. На рисунке представлены как отдельные кластерно-ассоциативные структуры молекул воды, так и отдельные молекулы воды, не связанные водородными связями.
В 1993 году американский химик Кен Джордан предложил свои варианты устойчивых “ассоциатов воды”, которые состоят из 6 её молекул [Tsai & Jordan, 1993]. Эти кластеры могут объединяться друг с другом и со “свободными” молекулами воды за счет экспонированных на их поверхности водородных связей. Интересной особенностью этой модели является то, что из нее автоматически следует, что свободно растущие кристаллы воды, хорошо известные нам снежинки, должны обладать 6-лучевой симметрией.
В 2002 году группе д-ра Хэд-Гордона методом рентгеноструктурного анализа с помощью сверхмощного рентгеновского источника Advanced Light Source (ALS) удалось показать, что молекулы воды способны за счет водородных связей образовывать структуры — «истинные кирпичики» воды, представляющие собой топологические цепочки и кольца из множества молекул воды. Интерпретируя полученные экспериментальные данные, исследователи считают их довольно долгоживущими элементами структуры. В основном же вода – это совокупность беспорядочных полимеров и «водяных кристаллов», где количество связанных в водородные связи молекул может достигать сотен и даже тысяч единиц.
«Водяные кристаллы» могут иметь самую разную форму, как пространственную, так и двухмерную (в виде кольцевых структур). В основе же всего лежит тетраэдр. Именно такую форму имеет молекула воды. Группируясь, тетраэдры молекул воды образуют разнообразные пространственные и плоскостные структуры. И из всего многообразия структур в природе базовой является гексагональная (шестигранная) структура, когда шесть молекул воды (тетраэдров) объединяются в кольцо. Такой тип структуры характерен для льда, снега и талой воды.
Рис. 1. Кристаллическая структура льда
Когда лёд плавится, его тетрагональная структура разрушается и образуется смесь полимеров, состоящая из три-, тетра-, пента-, и гексамеров воды и свободных молекул воды. Схематически этот процесс можно представить себе так.
Рис. справа — Структура жидкой воды. В воде кластеры периодически разрушаются и образуются снова. Время перескока составляет 10-12 секунд.
Изучить строение этих образующихся полимеров воды оказалось довольно сложно, поскольку вода – смесь различных полимеров, которые находятся в равновесии между собой. Сталкиваясь друг с другом, полимеры переходят один в другой, разлагаются и вновь образуются.
Разделить эту смесь на отдельные компоненты тоже практически невозможно. Лишь в 1993 году группа исследователей из Калифорнийского университета (г. Беркли, США) под руководством доктора Р.Дж.Сайкалли расшифровала строение триммера воды, в 1996 г. – тетрамера и пентамера, а затем и гексамера воды. К этому времени уже было установлено, что жидкая вода состоит из полимерных ассоциатов (кластеров), содержащих от трех до шести молекул воды.
Более сложным оказалось строение гексамера. Самая простая структура – шесть молекул воды в вершинах шестиугольника, – как выяснилось, не столь прочна, как структура клетки. Более того, структуры призмы, раскрытой книги или лодки тоже оказались менее устойчивыми. В шестиугольнике может быть только шесть водородных связей, а экспериментальные данные говорят о наличии восьми. Это значит, что четыре молекулы воды связаны перекрёстными водородными связями.
Структуры кластеров воды были найдены и теоретически, сегодняшняя вычислительная техника позволяет это сделать. Более того, именно сопоставлением экспериментально найденных и рассчитанных параметров удалось доказать, что полимеры имеют то строение, которое описано выше.
В 1999 г. Станислав Зенин провёл совместно с Б. Полануэром (сейчас в США) исследование воды в ГНИИ генетики, которые дали интереснейшие результаты. Применив современные методы анализа — рефрактометрию, протонный резонанс и жидкостную хроматографию им удалось обнаружить в воде полиассооциаты воды.
Рис. Возможные кластеры воды
Объединяясь друг с другом, кластеры могут образовывать более сложные структуры:
Рис. Более сложные ассоциаты кластеров воды
Кластеры, содержащие в своём составе 20 молекулу оказались более стабильными.
Анализируя полученные данные С.В. Зенин предложил, что вода представляет собой иерархию правильных объемных структур «ассоциатов» (clathrates), в основе которых лежит кристаллоподобный «квант воды», состоящий из 57 ее молекул, которые взаимодействуют друг с другом за счет свободных водородных связей. При этом 57 молекул воды (квантов), образуют структуру, напоминающую тетраэдр. Тетраэдр в свою очередь состоит из 4 додекаэдров (правильных 12-гранников). 16 квантов образуют структурный элемент, состоящий из 912 молекул воды. Вода на 80% состоит из таких элементов, 15% — кванты-тетраэдры и 3% — классические молекулы Н2О. Таким образом, структура воды связана с так называемыми платоновыми телами (тетраэдр, додекаэдр), форма которых связана с золотой пропорцией. Ядро кислорода также имеет форму платонова тела (тетраэдра).
Рис. Тетраэдр
Элементарной ячейкой воды являются тетраэдры, содержащие связанные между собой водородными связями четыре (простой тетраэдр) или пять молекул Н2О (объемно-центрированный тетраэдр).
При этом у каждой из молекул воды в простых тетраэдрах сохраняется способность образовывать водородные связи. За счет их простые тетраэдры могут объединяться между собой вершинами, ребрами или гранями, образуя различные кластеры со сложной структурой, например, в форме додекаэдра.
Рис. Додекаэдр
Таким образом, в воде возникают многочисленные кластеры, которые несут в себе очень большую энергию и информацию крайне высокой плотности.
Порядковое число таких структур воды так же высоко, как и порядковое число кристаллов (структура с максимально высоким упорядочением, которую мы только знаем), потому их также называют «жидкими кристаллами» или «кристаллической водой».
«Кванты воды» могут взаимодействовать друг с другом за счет свободных водородных связей, торчащих наружу из вершин “кванта” своими гранями.
При этом возможно образование уже двух типов структур второго порядка. Их взаимодействие друг с другом приводит к появлению структур высшего порядка.
Последние состоят из 912 молекул воды, которые по модели Зенина практически не способны к взаимодействию за счет образования водородных связей.
Этим и объясняется, например, высокая текучесть жидкости, состоящей из громадных полимеров.
Таким образом, водная среда представляет собой как бы иерархически организованный жидкий кристалл.
Рис. справа — Формирование отдельного кластера воды (компъютерное моделирование)
Следует отметить, что в настоящее время существуют и другие модели воды, описывающие её аномальные свойства.
Так, профессор Мартин Чаплин из Лондонского университета (Martin Chaplin Professor of Applied Science Water and Aqueous Systems Research of the London South Bank University) рассчитал и предположил иную структуру воды, в основе которой лежит икосаэдр.
Рис. Формирование икосаэдра воды
Согласно этой модели вода состоит из 1820 молекул воды — это в два раза больше, чем в модели Зенина. Гигантский икосаэдр в свою очередь состоит из 13 более мелких структурных элементов. Причем, так же как и у Зенина, структура гигантского ассоциата базируется на более мелких образованиях.
С уважением,
О. В. Мосин
Современная модель воды
К.х.н. О.В. Мосин
Особенности физических свойств воды и многочисленные короткоживущие водородные связи между соседними атомами водорода и кислорода в молекуле воды создают благоприятные возможности для образования особых структур-ассоциатов (кластеров), воспринимающих, хранящих и передающих самую различную информацию.
Одна из первых моделей воды – модель Фрэка и Уэна [Frank & Wen, 1957]. В соответствии с ней водородные связи в жидкой воде непрерывно образуются и рвутся, причем эти процессы протекают кооперативно в пределах короткоживущих групп молекул воды, названных “мерцающими кластерами”. Их время жизни оценивают в диапазоне от 10-10 до 10-11 с. Такое представление правдоподобно объясняет высокую степень подвижности жидкой воды и ее низкую вязкость. Считается, что благодаря таким свойствам вода служит одним из самых универсальных растворителей.
Однако модель “мерцающи кластеров” не может объяснить множество уже давно известных фактов, и тех, что стали стремительно нарастать в последнее время.
Но во второй половине XX века возникли две группы „смешанных“ моделей: кластерные и клатратные. В первой группе вода представала в виде кластеров из молекул, связанных водородными связями, которые плавали в море молекул, в таких связях не участвующих. Модели второй группы рассматривали воду как непрерывную сетку (обычно в этом контексте называемую каркасом) водородных связей, которая содержит пустоты; в них размещаются молекулы, не образующие связей с молекулами каркаса. Нетрудно было подобрать такие свойства и концентрации двух микрофаз кластерных моделей или свойства каркаса и степень заполнения его пустот клатратных моделей, чтобы объяснить все свойства воды, в том числе и знаменитые аномалии.
Среди кластерных моделей наиболее яркой оказалась модель Г. Немети и Х. Шераги: предложенные ими картинки, изображающие кластеры связанных молекул, которые плавают в море несвязанных молекул, вошли во множество монографий.
Модель клатратного типа предложил О.Я. Самойлов в 1946 году: в воде сохраняется подобная гексагональному льду сетка водородных связей, полости которой частично заполнены мономерными молекулами. Л. Полинг в 1959 году создал другой вариант, предположив, что основой структуры может служить сетка связей, присущая некоторым кристаллогидратам.
В течение второй половины 60-х годов и начала 70-х наблюдается сближение всех этих взглядов. Появлялись варианты кластерных моделей, в которых в обеих микрофазах молекулы соединены водородными связями. Сторонники клатратных моделей стали допускать образование водородных связей между пустотными и каркасными молекулами.
В 1990 г. чл.-корр. АН СССР Г.А. Домрачев (Ин-т металлоорганической химии РАН) и физик Д.А. Селивановский (Ин-т прикладной физики РАН) сформулировали гипотезу о существовании механохимических реакций радикальной диссоциации воды [Домрачев, 1995]. Они исходили из того, что жидкая вода представляет собой динамически нестабильную полимерную систему и что по аналогии с механохимическими реакциями в полимерах при механических воздействиях на воду поглощенная водой энергия, необходимая для разрыва Н-ОН, локализуется в микромасштабной области структуры жидкой воды. Реакцию разрыва Н-ОН связи можно записать так: (Н2О)n(Н2О…H-|-OH) (Н2О)m + E(Н2О)n+1(H ) + ( OH) (Н2О)m, где “ E” обозначает не спаренный электрон.
Поскольку диссоциация молекул воды и реакции с участием радикалов H и OH происходит в ассоциированном состоянии жидкой воды, радикалы могут иметь громадные (десятки секунд и более) продолжительности жизни до гибели в результате реакций рекомбинации [Blough et al., 1990].
Таким образом, существуют достаточно убедительные свидетельства в пользу того, что в жидкой воде присутствуют весьма устойчивые полимерные структуры. В 1993 году американский химик Кен Джордан предложил свои варианты устойчивых “квантов воды”, которые состоят из 6 её молекул [Tsai & Jordan, 1993]. Эти кластеры могут объединяться друг с другом и со “свободными” молекулами воды за счет экспонированных на их поверхности водородных связей. Интересной особенностью этой модели является то, что из нее автоматически следует, что свободно растущие кристаллы воды, хорошо известные нам снежинки, должны обладать 6-лучевой симметрией.
В 2002 году группе д-ра Хэд-Гордона методом рентгеноструктурного анализа с помощью сверхмощного рентгеновского источника Advanced Light Source (ALS) удалось показать, что молекулы воды способны за счет водородных связей образовывать структуры — «истинные кирпичики» воды, представляющие собой топологические цепочки и кольца из множества молекул.
Другая исследовательская группа Нильссона из синхротронной лаборатории всё того же Стенфордского университета, интерпретируя полученные экспериментальные данные как наличие структурных цепочек и колец, считает их довольно долгоживущими элементами структуры.
Несмотря на то, что разные модели предлагают отличающиеся по своей геометрии кластеры, все они постулируют, что молекулы воды способны объединяться с образованием полимеров. Но классический полимер – это молекула, все атомы которой объединены ковалентными связями, а не водородными, которые до недавнего времени считались чисто электростатическими. Однако в 1999 г. было экспериментально показано, что водородная связь между молекулами воды во льду имеет частично (на 10%) ковалентный характер [Isaacs E. D., et al.,1999]. Даже частично ковалентный характер водородной связи “разрешает”, по меньшей мере, 10% молекул воды объединяться в достаточно долгоживущие полимеры (неважно, какой конкретной структуры). А если в воде есть полимеры воды, то даже слабые воздействия на абсолютно чистую воду, а тем более ее растворы, могут иметь важные последствия.
В химии полимеров хорошо известен тот факт, что под действием механических напряжений, в частности – звуковой обработки, растяжения, продавливания полимера через тонкие отверстия, молекулы полимеров могут “рваться”. В зависимости от строения полимера, условий, в которых он находится, эти разрывы сопровождаются либо образованием новых беспорядочных связей между “обрывками” исходных молекул, либо уменьшением их молекулярной массы. Такие процессы служат, в частности, причиной старения полимеров. Редко уточняют, что фрагментация полимеров при подобных воздействиях – явление нетривиальное. Так, например, интактные молекулы ДНК, составленных из сотен тысяч и миллионов мономеров-нуклеотидов, легко распадаются на более мелкие фрагменты от простого перемешивания препарата палочкой. При этом, чем меньше фрагменты, тем более высокой плотности требуется энергия для дальнейшего дробления. Во всех случаях – и в длинных и в коротких полимерах разрываются химически идентичные ковалентные связи. Следовательно, если для разрыва ковалентной связи между двумя атомами в малой молекуле необходимо приложить энергию, эквивалентную энергии кванта УФили по меньшей мере видимого света, то такая же связь в полимере может разорваться при воздействии на него механических колебаний. В первом случае частота колебаний соответствует величинам порядка 1015 Гц, во втором – герцам – килогерцам. Значит, молекула полимера может выступать в роли своеобразного трансформатора энергии низкой плотности в энергию высокой плотности. Образно говоря, полимеры превращают тепло в свет. А тогда, если жидкая вода может хоть в какой-то степени рассматриваться как квази-полимер, то и в ней могут осуществляться подобные процессы.
Модель структурированной воды определяет почти все её аномальные свойства, имеющие огромное практическое значение — вода самое аномальное из всех известных природе веществ. Диаметр молекулы воды 2,8 А (1 ангстрем = 10-10м). Если рассматривать воду как простую совокупность молекул Н2О, то оказывается, что её удельный вес должен составлять 1,84 г/см3, а температура её кипения будет равна 63,5°С. Но, как известно, при нормальной температуре и давлении удельный вес воды равен 1 г/см3, а кипит вода при 100°С. Исходя из этого, следует предположить, что внутри воды должны быть пустоты, где нет молекул Н2О, то есть воде присуща особая структура. Это принципиальное открытие было сделано английским физиком Берналом. С тех пор в этой области проведено множество исследований, но полной ясности в этом вопросе еще нет.
Способность молекул воды образовывать определенные структуры, основана на наличии так называемых водородных связей. Эти связи не химической природы. Они легко разрушаются и быстро восстанавливаются, что делает структуру воды исключительно изменчивой. Именно благодаря этим связям в отдельных микрообъемах воды непрерывно возникают своеобразные ассоциаты воды, её структурные элементы. Связь в таких ассоциатах называется водородной. Она является очень слабой, легко разрушаемой, в отличие от ковалентных связей, например, в структуре минералов или любых химических соединений.
Интересно, что свободные, не связанные в ассоциаты молекулы воды присутствуют в воде лишь в очень небольшом количестве. В основном же вода – это совокупность беспорядочных ассоциатов и «водяных кристаллов», где количество связанных в водородные связи молекул может достигать сотен и даже тысяч единиц.
«Водяные кристаллы» могут иметь самую разную форму, как пространственную, так и двухмерную (в виде кольцевых структур). В основе же всего лежит тетраэдр (простейшая пирамида в четыре угла). Именно такую форму имеют распределенные положительные и отрицательные заряды в молекуле воды. Группируясь, тетраэдры молекул h3O образуют разнообразные пространственные и плоскостные структуры. И из всего многообразия структур в природе базовой, судя по всему (пока лишь не точно доказанное предположение) является всего одна – гексагональная (шестигранная), когда шесть молекул воды (тетраэдров) объединяются в кольцо.
Такой тип структуры характерен для льда, снега, талой воды, клеточной воды всех живых существ.
Рис. 1. Кристаллическая структура льда
Каждая молекула воды в кристаллической структуре льда участвует в 4 водородных связях, направленных к вершинам тетраэдра. В центре этого тетраэдра находится атом кислорода, в двух вершинах — по атому водорода, электроны которых задействованы в образовании ковалентной связи с кислородом. Две оставшиеся вершины занимают пары валентных электронов кислорода, которые не участвуют в образовании внутримолекулярных связей. При взаимодействии протона одной молекулы с парой неподеленных электронов кислорода другой молекулы возникает водородная связь, менее сильная, чем связь внутримолекулярная, но достаточно могущественная, чтобы удерживать рядом соседние молекулы воды. Каждая молекула может одновременно образовывать четыре водородные связи с другими молекулами под строго определенными углами, равными 109°28′, направленных к вершинам тетраэдра, которые не позволяют при замерзании создавать плотную структуру (при этом в структурах льда I, Ic, VII и VIII этот тетраэдр правильный).
Когда лёд плавится, его тетрагональная структура разрушается и образуется смесь полимеров, состоящая из три-, тетра-, пента-, и гексамеров воды и свободных молекул воды. Схематически этот процесс показан ниже.
Рис. слева — Структура жидкой воды. В воде кластеры периодически разрушаются и образуются снова. Время перескока составляет 10-12 секунд.
Изучить строение этих образующихся полимеров воды оказалось довольно сложно, поскольку вода – смесь различных полимеров, которые находятся в равновесии между собой. Сталкиваясь друг с другом, полимеры переходят один в другой, разлагаются и вновь образуются.
Разделить эту смесь на отдельные компоненты тоже практически невозможно. Лишь в 1993 году группа исследователей из Калифорнийского университета (г. Беркли, США) под руководством доктора Р.Дж.Сайкалли расшифровала строение триммера воды, в 1996 г. – тетрамера и пентамера, а затем и гексамера воды. К этому времени уже было установлено, что жидкая вода состоит из полимерных ассоциатов (кластеров), содержащих от трех до шести молекул воды.
На рисунке ниже показано строение три-, тетра-, пента-, и гексамера воды. Все они цикличны, т. е. образуют довольно устойчивые «кольца».
Более сложным оказалось строение гексамера. Самая простая структура – шесть молекул воды в вершинах шестиугольника, – как выяснилось, не столь прочна, как структура клетки. Более того, структуры призмы, раскрытой книги или лодки тоже оказались менее устойчивыми. В шестиугольнике может быть только шесть водородных связей, а экспериментальные данные говорят о наличии восьми. Это значит, что четыре молекулы воды связаны перекрёстными водородными связями.
Структуры кластеров воды были найдены и теоретически, сегодняшняя вычислительная техника позволяет это сделать. Более того, именно сопоставлением экспериментально найденных и рассчитанных параметров удалось доказать, что полимеры имеют то строение, которое описано выше.
В 1999 г. Станислав Зенин провёл совместно с Б. Полануэром (сейчас в США) исследование воды в ГНИИ генетики, которые дали интереснейшие результаты. Применив современные методы анализа, как-то рефрактометрического, протонного резонанса и жидкостной хроматографии исследователям удалось обнаружить полиассооциаты — «кванты» воды.
Рис. Возможные кластеры воды
Объединяясь друг с другом, кластеры могут образовывать более сложные структуры:
Рис. Более сложные ассоциаты кластеров воды
Кластеры, содержащие в своём составе 20 молекулу оказались более стабильными.
Рис. слева — Формирование кластера из 20 молекулы воды.
Согласно гипотезе С.В. Зенина вода представляет собой иерархию правильных объемных структур «ассоциатов» (clathrates), в основе которых лежит кристаллоподобный «квант воды», состоящий из 57 ее молекул, которые взаимодействуют друг с другом за счет свободных водородных связей. При этом 57 молекул воды (квантов), образуют структуру, напоминающую тетраэдр. Тетраэдр в свою очередь состоит из 4 додекаэдров (правильных 12-гранников). 16 квантов образуют структурный элемент, состоящий из 912 молекул воды. Вода на 80% состоит из таких элементов, 15% — кванты-тетраэдры и 3% — классические молекулы Н2О. Таким образом, структура воды связана с так называемыми платоновыми телами (тетраэдр, додекаэдр), форма которых связана с золотой пропорцией. Ядро кислорода также имеет форму платонова тела (тетраэдра).
Элементарной ячейкой воды являются тетраэдры, содержащие связанные между собой водородными связями четыре (простой тетраэдр) или пять молекул Н2О (объемно-центрированный тетраэдр).
Рис. слева — Тетраэдр
Рис. Тетраэдр воды
При этом у каждой из молекул воды в простых тетраэдрах сохраняется способность образовывать водородные связи. За счет их простые тетраэдры могут объединяться между собой вершинами, ребрами или гранями, образуя различные кластеры со сложной структурой, например, в форме додекаэдра.
Рис. справа — Додекаэдр
Таким образом, в воде возникают стабильные кластеры, которые несут в себе очень большую энергию и информацию крайне высокой плотности. Порядковое число таких структур воды так же высоко, как и порядковое число кристаллов (структура с максимально высоким упорядочением, которую мы только знаем), потому их также называют «жидкими кристаллами» или «кристаллической водой». акая структура энергетически выгодна и разрушается с освобождением свободных молекул воды лишь при высоких концентрациях спиртов и подобных им растворителей [Зенин, 1994]. «Кванты воды» могут взаимодействовать друг с другом за счет свободных водородных связей, торчащих наружу из вершин “кванта” своими гранями. При этом возможно образование уже двух типов структур второго порядка. Их взаимодействие друг с другом приводит к появлению структур высшего порядка. Последние состоят из 912 молекул воды, которые по модели Зенина практически не способны к взаимодействию за счет образования водородных связей. Этим и объясняется, например, высокая текучесть жидкости, состоящей из громадных полимеров. Таким образом, водная среда представляет собой как бы иерархически организованный жидкий кристалл.
Изменение положения одного структурного элемента в этом кристалле под действием любого внешнего фактора или изменение ориентации окружающих элементов под влиянием добавляемых веществ обеспечивает, согласно гипотезе Зенина, высокую чувствительность информационной системы воды. Если степень возмущения структурных элементов недостаточна для перестройки всей структуры воды в данном объеме, то после снятия возмущения система через 30-40 мин возвращается в исходное состояние. Если же перекодирование, т. е. переход к другому взаимному расположению структурных элементов воды оказывается энергетически выгодным, то в новом состоянии отражается кодирующее действие вызвавшего эту перестройку вещества [Зенин, 1994]. Такая модель позволяет Зенину объясненить «память воды» и ее информационные свойства [Зенин, 1997].
Рис. слева — Формирование отдельного кластера воды (компъютерное моделирование)
В дистиллированной воде кластеры практически электронейтральны. Однако Зенин обнаружил, что их электропроводность можно изменить. Если помешать магнитной мешалкой, связи между элементами клстеров будут разрушены и вода превратится в мертвое, неупорядоченное месиво.
Если поместить в воду предельно малое количество другого вещества (хоть одну молекулу) — кластеры начнут «перенимать» его электромагнитные свойства. Это свойство объясняет чрезвычайно лабильный, подвижный характер их взаимодействия. Его природа обусловлена дальними кулоновскими силами, определяющими новый вид зарядово-комплементарной связи. Именно за счет этого вида взаимодействий осуществляется построение структурных элементов воды в ячейки (клатраты) размером до 0,5-1 микрон. Их можно непосредственно наблюдать при помощи контрастно-фазового микроскопа.
Структурированное состояние воды оказалось чувствительным датчиком различных полей. С. Зенин считает, что мозг, сам состоящий на 90% из воды, может, тем не менее, изменять её структуру.
Опираясь на подобные представления о структуре воды, учёные выяснили интересные подробности. Недавно, как сообщил российские исследователи Высоцкий и Корнилова, развивая идеи Ю.И. Наберухина, провели расчет энергетических характеристик, необходимых для перехода свободных молекул воды из несвязанного состояния в полость клатрата и обратно.
С помощью этих расчетов они показали, что структурой воды — количеством свободных молекул воды в полостях клатратов и вне их, — можно управлять с помощью давления, температуры, магнитного поля и т. д. Причем вода может использоваться для медицинских целей, как самостоятельно, так и в качестве «упаковки» для молекул лекарственных веществ. Такой гипотетической «упаковкой», способной донести лекарства до внутренних органов больного, не растратив их по пути, служат клатраты, в полостях которых могут быть размещены лекарственные молекулы при определенных режимах их приготовления.
В природных условиях полости в клатратах воды могут занимать молекулы природных газов, образуя кристаллогидраты. Наиболее распространенным кристаллогидратом, встречающимся в вечной мерзлоте и на дне морей и океанов, является кристаллогидрат углеводородного газа метана. Он представляет собой массу, похожую на мокрый снег. Такие кристаллогидраты, в принципе, могут использоваться в качестве топлива альтернативного нефти и газу, но, вместе с тем, могут представлять большую опасность для жизни на Земле.
Модель кластерного строения воды имеет много спорных дискутируемых моментов, но отвергать её совершенно несправедливо. Например, Зенин предполагает, что основной структурный элемент воды — кластер из 57 молекул, образованный слиянием четырёх додекаэдров. Они имеют общие грани, а их центры образуют правильный тетраэдр. То, что молекулы воды могут располагаться по вершинам пентагонального додекаэдра, известно давно; такой додекаэдр — основа газовых гидратов. Поэтому ничего удивительного в предположении о существовании таких структур в воде нет, хотя уже говорилось, что никакая конкретная структура не может быть преобладающей и существовать долго. Поэтому странно, что этот элемент предполагается главным и что в него входит ровно 57 молекул. Из шариков, например, можно собирать такие же структуры, которые состоят из примыкающих друг к другу додекаэдров и содержат 200 молекул. Зенин же утверждает, что процесс трёхмерной полимеризации воды останавливается на 57 молекулах. Более крупных ассоциатов, по его мнению, быть не должно. Однако если бы это было так, из водяного пара не могли бы осаждаться кристаллы гексагонального льда, которые содержат огромное число молекул, связанных воедино водородными связями. Совершенно неясно, почему рост кластера Зенина остановился на 57 молекулах. Чтобы уйти от противоречий, Зенин упаковывает кластеры в более сложные образования — ромбоэдры — из почти тысячи молекул, причём исходные кластеры друг с другом водородных связей не образуют. Возникает вопрос почему? Чем молекулы на их поверхности отличаются от тех, что внутри? По мнению Зенина, узор гидроксильных групп на поверхности ромбоэдров и обеспечивает информационые свойства воды. Следовательно, молекулы воды в этих крупных комплексах жёстко фиксированы, и сами комплексы представляют собой твёрдые тела. Такая вода не будет течь, а температура её плавления, которая связана с молекулярной массой, должна быть весьма высокой. Поскольку в основе модели лежат тетраэдрические постройки, её можно в той или иной степени согласовать с данными по дифракции рентгеновских лучей и нейтронов. И хотя модель Зенина может объяснить уменьшение плотности при плавлении — упаковка додекаэдров плотнее, чем лёд, труднее согласуется модель с динамическими свойствами воды — текучестью, большим значением коэффициента самодиффузии, малыми временами корреляции и диэлектрической релаксации, которые измеряются пикосекундами.
Следует отметить, что в настоящее время существуют и другие модели воды, описывающие её аномальные свойства. Так, профессор Мартин Чаплин из Лондонского университета (Martin Chaplin Professor of Applied Science Water and Aqueous Systems Research of the London South Bank University) рассчитал и предположил иную структуру воды, в основе которой лежит икосаэдр.
Рис. Формирование икосаэдра воды
Согласно этой модели вода состоит из 1820 молекул воды — это в два раза больше, чем в модели Зенина. Гигантский икосаэдр в свою очередь состоит из 13 более мелких структурных элементов. Причем, так же как и у Зенина, структура гигантского ассоциата базируется на более мелких образованиях.
Совсем недавно д-р Анджелос Микаелидес (Angelos Michaelides) из Центра нанотехнологий в Лондоне и профессор Карина Моргенштерн (Karina Morgenstern) из университета им. Лейбница в Ганновере опубликовали в журнале Nature Materials работу, посвященную изучению свойств кристаллической воды на наноуровне.
Рис. слева — Изображение гексамера воды, полученное с помощью сканирующего туннельного микроскопа. Размер гексамера в поперечнике — около 1 нм. Фото London Centre for Nanotechnology
Ученые охлаждали водяной пар над поверхностью металлической пластины, находящейся при температуре 5 градусов Кельвина. Вскоре с помощью сканирующего туннельного микроскопа на пластине удалось наблюдать гексамер (шесть соединенных между собой молекул воды) — мельчайшую снежинку. Это самый маленький из возможных кластеров льда. Ученые наблюдали также кластеры, содержащие семь, восемь и девять молекул.
Разработка технологии, позволившей получить изображение гексамера воды — само по себе важное научное достижение. Для наблюдения пришлось сократить зондирующий ток до минимума, что и позволило предохранить слабые связи между отдельными молекулами воды от разрушения вследствие процесса наблюдения. Помимо экспериментов, в работе были использованы теоретические подходы квантовой механики. Комплексный подход дал впечатляющие результаты.
В отличие от кристаллического льда, где между всеми молекулами воды энергия связи одинакова, в нанокластерах есть чередование сильных и слабых связей (и соответствующих расстояний) между отдельными молекулами. Получены также важные результаты о способности молекул воды к распределению водородных связей и к их связи с поверхностью металла.
Рассматривая все эти модели, нужно чётко представлять, что они – пока не более чем модели, лучше всего объясняющие те или иные аномальные свойства воды.
К.х.н. О. В. Мосин
Современные модели воды — Дом Солнца
Их время жизни оценивают в диапазоне от 10-10 до 10-11 с. Такое представление правдоподобно объясняет высокую степень подвижности жидкой воды и ее низкую вязкость. Считается, что благодаря таким свойствам вода служит одним из самых универсальных растворителей.Однако модель “мигающих кластеров” не может объяснить громадного набора уже давно известных фактов, и тех, что стали стремительно нарастать в последнее время.
В 1990 г. чл.-корр. АН СССР Г.А. Домрачев (Ин-т металлоорганической химии РАН) и физик Д.А. Селивановский (Ин-т прикладной физики РАН) сформулировали гипотезу о существовании механохимических реакций радикальной диссоциации воды [Домрачев, 1995]. Они исходили из того, что жидкая вода представляет собой динамически нестабильную полимерную систему и что по аналогии с механохимическими реакциями в полимерах при механических воздействиях на воду поглощенная водой энергия, необходимая для разрыва Н-ОН, локализуется в микромасштабной области структуры жидкой воды. Реакцию разрыва Н-ОН связи можно записать так: (Н2О)n(Н2О…H-|-OH) (Н2О)m + E  (Н2О)n+1(H• ) + (• OH) (Н2О)m, где “• ” обозначает не спаренный электрон.
Поскольку диссоциация молекул воды и реакции с участием радикалов H• и OH• происходит в ассоциированном состоянии жидкой воды, радикалы могут иметь громадные (десятки секунд и более) продолжительности жизни до гибели в результате реакций рекомбинации [Blough et al., 1990].
Таким образом, существуют достаточно убедительные свидетельства в пользу того, что в жидкой воде присутствуют весьма устойчивые полимерные структуры. В 1993 году американский химик Кен Джордан предложил свои варианты устойчивых “квантов воды”, которые состоят из 6 её молекул [Tsai & Jordan, 1993]. Эти кластеры могут объединяться друг с другом и со “свободными” молекулами воды за счет экспонированных на их поверхности водородных связей. Интересной особенностью этой модели является то, что из нее автоматически следует, что свободно растущие кристаллы воды, хорошо известные нам снежинки, должны обладать 6-лучевой симметрией.
В 2002 году группе д-ра Хэд-Гордона методом рентгеноструктурного анализа с помощью сверхмощного рентгеновского источника Advanced Light Source (ALS) удалось показать, что молекулы воды способны за счет водородных связей образовывать структуры — «истинные кирпичики» воды, представляющие собой топологические цепочки и кольца из множества молекул.
Другая исследовательская группа Нильссона из синхротронной лаборатории всё того же Стенфордского университета, интерпретируя полученные экспериментальные данные как наличие структурных цепочек и колец, считает их довольно долгоживущими элементами структуры.
Несмотря на то, что разные модели предлагают отличающиеся по своей геометрии кластеры, все они постулируют, что молекулы воды способны объединяться с образованием полимеров. Но классический полимер – это молекула, все атомы которой объединены ковалентными связями, а не водородными, которые до недавнего времени считались чисто электростатическими. Однако в 1999 г. было экспериментально показано, что водородная связь между молекулами воды во льду имеет частично (на 10%) ковалентный характер [Isaacs E. D., et al.,1999]. Даже частично ковалентный характер водородной связи “разрешает”, по меньшей мере, 10% молекул воды объединяться в достаточно долгоживущие полимеры (неважно, какой конкретной структуры). А если в воде есть полимеры воды, то даже слабые воздействия на абсолютно чистую воду, а тем более ее растворы, могут иметь важные последствия.
В химии полимеров хорошо известен тот факт, что под действием механических напряжений, в частности – звуковой обработки, растяжения, продавливания полимера через тонкие отверстия, молекулы полимеров могут “рваться”. В зависимости от строения полимера, условий, в которых он находится, эти разрывы сопровождаются либо образованием новых беспорядочных связей между “обрывками” исходных молекул, либо уменьшением их молекулярной массы. Такие процессы служат, в частности, причиной старения полимеров. Редко уточняют, что фрагментация полимеров при подобных воздействиях – явление нетривиальное. Так, например, интактные молекулы ДНК, составленных из сотен тысяч и миллионов мономеров-нуклеотидов, легко распадаются на более мелкие фрагменты от простого перемешивания препарата палочкой. При этом, чем меньше фрагменты, тем более высокой плотности требуется энергия для дальнейшего дробления. Во всех случаях – и в длинных и в коротких полимерах разрываются химически идентичные ковалентные связи. Следовательно, если для разрыва ковалентной связи между двумя атомами в малой молекуле необходимо приложить энергию, эквивалентную энергии кванта УФ- или по меньшей мере видимого света, то такая же связь в полимере может разорваться при воздействии на него механических колебаний. В первом случае частота колебаний соответствует величинам порядка 1015 Гц, во втором – герцам – килогерцам. Значит, молекула полимера может выступать в роли своеобразного трансформатора энергии низкой плотности в энергию высокой плотности. Образно говоря, полимеры превращают тепло в свет. А тогда, если жидкая вода может хоть в какой-то степени рассматриваться как квази-полимер, то и в ней могут осуществляться подобные процессы. [/isaacs][/tsai][/blough][/frank]
[frank][blough][tsai][isaacs]
Модель структурированной воды определяет почти все её аномальные свойства, имеющие огромное практическое значение — вода самое аномальное из всех известных природе веществ. Диаметр молекулы воды 2,8 А (1 ангстрем = 10-10м). Если рассматривать воду как простую совокупность молекул Н2О, то оказывается, что её удельный вес должен составлять 1,84 г/см3, а температура её кипения будет равна 63,5°С. Но, как известно, при нормальной температуре и давлении удельный вес воды равен 1 г/см3, а кипит вода при 100°С. Исходя из этого, следует предположить, что внутри воды должны быть пустоты, где нет молекул Н2О, то есть воде присуща особая структура. Это принципиальное открытие было сделано английским физиком Берналом. С тех пор в этой области проведено множество исследований, но полной ясности в этом вопросе еще нет.
Способность молекул воды образовывать определенные структуры, основана на наличии так называемых водородных связей. Эти связи не химической природы. Они легко разрушаются и быстро восстанавливаются, что делает структуру воды исключительно изменчивой. Именно благодаря этим связям в отдельных микрообъемах воды непрерывно возникают своеобразные ассоциаты воды, её структурные элементы. Связь в таких ассоциатах называется водородной. Она является очень слабой, легко разрушаемой, в отличие от ковалентных связей, например, в структуре минералов или любых химических соединений.
Интересно, что свободные, не связанные в ассоциаты молекулы воды присутствуют в воде лишь в очень небольшом количестве. В основном же вода – это совокупность беспорядочных ассоциатов и «водяных кристаллов», где количество связанных в водородные связи молекул может достигать сотен и даже тысяч единиц.
«Водяные кристаллы» могут иметь самую разную форму, как пространственную, так и двухмерную (в виде кольцевых структур). В основе же всего лежит тетраэдр (простейшая пирамида в четыре угла). Именно такую форму имеют распределенные положительные и отрицательные заряды в молекуле воды. Группируясь, тетраэдры молекул воды образуют разнообразные пространственные и плоскостные структуры. И из всего многообразия структур в природе базовой, судя по всему (пока лишь не точно доказанное предположение) является всего одна – гексагональная (шестигранная), когда шесть молекул воды (тетраэдров) объединяются в кольцо. Такой тип структуры характерен для льда, снега, талой воды, клеточной воды всех живых существ.
Изучить строение полимеров воды оказалось довольно сложно, поскольку вода – смесь различных полимеров, которые находятся в равновесии между собой. Сталкиваясь друг с другом, полимеры переходят один в другой, разлагаются и вновь образуются.
Разделить эту смесь на отдельные компоненты тоже практически невозможно. Лишь в 1993 году группа исследователей из Калифорнийского университета (г. Беркли, США) под руководством доктора Р.Дж.Сайкалли расшифровала строение триммера воды, в 1996 г. – тетрамера и пентамера, а затем и гексамера воды. К этому времени уже было установлено, что жидкая вода состоит из полимерных ассоциатов (кластеров), содержащих от трех до шести молекул воды.
Более сложным оказалось строение гексамера. Самая простая структура – шесть молекул воды в вершинах шестиугольника, – как выяснилось, не столь прочна, как структура клетки. Более того, структуры призмы, раскрытой книги или лодки тоже оказались менее устойчивыми. В шестиугольнике может быть только шесть водородных связей, а экспериментальные данные говорят о наличии восьми. Это значит, что четыре молекулы воды используют для связывания по одной «руке», как и в циклических полимерах, а две молекулы воды – по две «руки». Приходится допустить, что к «поясу» двух молекул воды здесь протянуты по две «руки». Эта структура прочнее всех остальных.
Структуры кластеров воды были найдены и теоретически, сегодняшняя вычислительная техника позволяет это сделать. Более того, именно сопоставлением экспериментально найденных и рассчитанных параметров удалось доказать, что полимеры имеют то строение, которое описано выше.
В 1999 г. Станислав Зенин провёл совместно с Б. Полануэром (сейчас в США) исследование воды в ГНИИ генетики, которые дали интереснейшие результаты. Применив современные методы анализа, как-то рефрактометрического, протонного резонанса и жидкостной хроматографии исследователям удалось обнаружить полиассооциаты — «кванты» воды. Оказалось, что «квант» воды представляет собой структурное объединение 57 молекул воды, связанных друг с другом водородными связями. 16 квантов воды объединяются, создавая подобную льду кластерную структуру, в которую входит 912 молекул воды. Предполагается, что вода состоит из таких кластеров на 80% .[/isaacs][/tsai][/blough][/frank]
[frank][blough][tsai][isaacs]
Согласно гипотезе С.В. Зенина вода представляет собой иерархию правильных объемных структур «ассоциатов» (clathrates), в основе которых лежит кристаллоподобный «квант воды», состоящий из 57 ее молекул, которые взаимодействуют друг с другом за счет свободных водородных связей. При этом 57 молекул воды (квантов), образуют структуру, напоминающую тетраэдр. Тетраэдр в свою очередь состоит из 4 додекаэдров (правильных 12-гранников). 16 квантов образуют структурный элемент, состоящий из 912 молекул воды. Вода на 80% состоит из таких элементов, 15% — кванты-тетраэдры и 3% — классические молекулы воды. Хаотически двигаются не отдельные молекулы воды, а структурные элементы. Таким образом, структура воды связана с так называемыми платоновыми телами (тетраэдр, додекаэдр), форма которых связана с золотой пропорцией. Ядро кислорода также имеет форму платонова тела (тетраэдра).
Такая структура энергетически выгодна и разрушается с освобождением свободных молекул воды лишь при высоких концентрациях спиртов и подобных им растворителей [Зенин, 1994]. «Кванты воды» могут взаимодействовать друг с другом за счет свободных водородных связей, торчащих наружу из вершин “кванта” своими гранями. При этом возможно образование уже двух типов структур второго порядка. Их взаимодействие друг с другом приводит к появлению структур высшего порядка. Последние состоят из 912 молекул воды, которые по модели Зенина практически не способны к взаимодействию за счет образования водородных связей. Этим и объясняется, например, высокая текучесть жидкости, состоящей из громадных полимеров. Таким образом, водная среда представляет собой как бы иерархически организованный жидкий кристалл.
Изменение положения одного структурного элемента в этом кристалле под действием любого внешнего фактора или изменение ориентации окружающих элементов под влиянием добавляемых веществ обеспечивает, согласно гипотезе Зенина, высокую чувствительность информационной системы воды. Если степень возмущения структурных элементов недостаточна для перестройки всей структуры воды в данном объеме, то после снятия возмущения система через 30-40 мин возвращается в исходное состояние. Если же перекодирование, т. е. переход к другому взаимному расположению структурных элементов воды оказывается энергетически выгодным, то в новом состоянии отражается кодирующее действие вызвавшего эту перестройку вещества [Зенин, 1994]. Такая модель позволяет Зенину объясненить «память воды» и ее информационные свойства [Зенин, 1997].
В дистиллированной воде кластеры практически электронейтральны. Однако Зенин обнаружил, что их электропроводность можно изменить. Если помешать магнитной мешалкой, связи между элементами клстеров будут разрушены и вода превратится в мертвое, неупорядоченное месиво.
Если поместить в воду предельно малое количество другого вещества (хоть одну молекулу) — кластеры начнут «перенимать» его электромагнитные свойства. Это свойство объясняет чрезвычайно лабильный, подвижный характер их взаимодействия. Его природа обусловлена дальними кулоновскими силами, определяющими новый вид зарядово-комплементарной связи. Именно за счет этого вида взаимодействий осуществляется построение структурных элементов воды в ячейки (клатраты) размером до 0,5-1 микрон. Их можно непосредственно наблюдать при помощи контрастно-фазового микроскопа.
Структурированное состояние воды оказалось чувствительным датчиком различных полей. С. Зенин считает, что мозг, сам состоящий на 90% из воды, может, тем не менее, изменять её структуру.
Опираясь на подобные представления о структуре воды, учёные выяснили интересные подробности. Недавно, как сообщил российские исследователи Высоцкий и Корнилова, развивая идеи Ю.И. Наберухина, провели расчет энергетических характеристик, необходимых для перехода свободных молекул воды из несвязанного состояния в полость клатрата и обратно.
С помощью этих расчетов они показали, что структурой воды — количеством свободных молекул воды в полостях клатратов и вне их, — можно управлять с помощью давления, температуры, магнитного поля и т. д.
Причем «заряженная» таким образом вода сохраняет свою структуру в течение длительного времени и может использоваться для медицинских целей, как самостоятельно (вспомним «живую воду» из народных сказок), так и в качестве «упаковки» для молекул лекарственных веществ. [/isaacs][/tsai][/blough][/frank]
[frank][blough][tsai][isaacs]
Такой «упаковкой», способной донести лекарства до внутренних органов больного, не растратив их по пути, служат клатраты, в полостях которых могут быть размещены лекарственные молекулы при определенных режимах их приготовления.
В природных условиях полости в клатратах воды могут занимать молекулы природных газов, образуя кристаллогидраты. Наиболее распространенным кристаллогидратом, встречающимся в вечной мерзлоте и на дне морей и океанов, является кристаллогидрат углеводородного газа метана. Он представляет собой массу, похожую на мокрый снег. Такие кристаллогидраты, в принципе, могут использоваться в качестве топлива альтернативного нефти и газу, но, вместе с тем, могут представлять большую опасность для жизни на Земле.
Модель кластерного строения воды имеет много спорных дискутируемых моментов, но отвергать её совершенно несправедливо. Например, Зенин предполагает, что основной структурный элемент воды — кластер из 57 молекул, образованный слиянием четырёх додекаэдров. Они имеют общие грани, а их центры образуют правильный тетраэдр. То, что молекулы воды могут располагаться по вершинам пентагонального додекаэдра, известно давно; такой додекаэдр — основа газовых гидратов. Поэтому ничего удивительного в предположении о существовании таких структур в воде нет, хотя уже говорилось, что никакая конкретная структура не может быть преобладающей и существовать долго. Поэтому странно, что этот элемент предполагается главным и что в него входит ровно 57 молекул. Из шариков, например, можно собирать такие же структуры, которые состоят из примыкающих друг к другу додекаэдров и содержат 200 молекул. Зенин же утверждает, что процесс трёхмерной полимеризации воды останавливается на 57 молекулах. Более крупных ассоциатов, по его мнению, быть не должно. Однако если бы это было так, из водяного пара не могли бы осаждаться кристаллы гексагонального льда, которые содержат огромное число молекул, связанных воедино водородными связями. Совершенно неясно, почему рост кластера Зенина остановился на 57 молекулах. Чтобы уйти от противоречий, Зенин упаковывает кластеры в более сложные образования — ромбоэдры — из почти тысячи молекул, причём исходные кластеры друг с другом водородных связей не образуют. Возникает вопрос почему? Чем молекулы на их поверхности отличаются от тех, что внутри? По мнению Зенина, узор гидроксильных групп на поверхности ромбоэдров и обеспечивает информационые свойства воды. Следовательно, молекулы воды в этих крупных комплексах жёстко фиксированы, и сами комплексы представляют собой твёрдые тела. Такая вода не будет течь, а температура её плавления, которая связана с молекулярной массой, должна быть весьма высокой. Поскольку в основе модели лежат тетраэдрические постройки, её можно в той или иной степени согласовать с данными по дифракции рентгеновских лучей и нейтронов. И хотя модель Зенина может объяснить уменьшение плотности при плавлении — упаковка додекаэдров плотнее, чем лёд, труднее согласуется модель с динамическими свойствами воды — текучестью, большим значением коэффициента самодиффузии, малыми временами корреляции и диэлектрической релаксации, которые измеряются пикосекундами.
Следует отметить, что в настоящее время существуют и другие модели воды, описывающие её аномальные свойства. Так, профессор Мартин Чаплин из Лондонского университета (Martin Chaplin Professor of Applied Science Water and Aqueous Systems Research of the London South Bank University) рассчитал и предположил иную структуру воды, в основе которой лежит икосаэдр.
Согласно этой модели вода состоит из 1820 молекул воды — это в два раза больше, чем в модели Зенина. Гигантский икосаэдр в свою очередь состоит из 13 более мелких структурных элементов. Причем, так же как и у Зенина, структура гигантского ассоциата базируется на более мелких образованиях.
Совсем недавно д-р Анджелос Микаелидес (Angelos Michaelides) из Центра нанотехнологий в Лондоне и профессор Карина Моргенштерн (Karina Morgenstern) из университета им. Лейбница в Ганновере опубликовали в журнале Nature Materials работу, посвященную изучению свойств кристаллической воды на наноуровне.
Ученые охлаждали водяной пар над поверхностью металлической пластины, находящейся при температуре 5 градусов Кельвина. Вскоре с помощью сканирующего туннельного микроскопа на пластине удалось наблюдать гексамер (шесть соединенных между собой молекул воды) — мельчайшую снежинку. Это самый маленький из возможных кластеров льда. Ученые наблюдали также кластеры, содержащие семь, восемь и девять молекул. [/isaacs][/tsai][/blough][/frank]
[frank][blough][tsai][isaacs]
Разработка технологии, позволившей получить изображение гексамера воды — само по себе важное научное достижение. Для наблюдения пришлось сократить зондирующий ток до минимума, что и позволило предохранить слабые связи между отдельными молекулами воды от разрушения вследствие процесса наблюдения. Помимо экспериментов, в работе были использованы теоретические подходы квантовой механики. Комплексный подход дал впечатляющие результаты.
В отличие от кристаллического льда, где между всеми молекулами воды энергия связи одинакова, в нанокластерах есть чередование сильных и слабых связей (и соответствующих расстояний) между отдельными молекулами. Получены также важные результаты о способности молекул воды к распределению водородных связей и к их связи с поверхностью металла.
Рассматривая все эти модели, нужно чётко представлять, что они – пока не более чем модели, лучше всего объясняющие те или иные аномальные свойства воды.
К.х.н. О. В. Мосин[/isaacs][/tsai][/blough][/frank]
модель воды — Water model
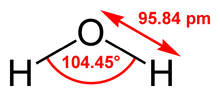
В вычислительной химии , А модель воды используется для моделирования и термодинамически расчета кластеров воды , жидкого воды и водных растворов с явным растворителем. Модели определяются из квантовой механики , молекулярной механики , результатов экспериментов, и этих комбинаций. Для того, чтобы имитировать специфическую природу молекул, было разработано много типов моделей. В общем, они могут быть классифицированы по следующим трем пунктам; (я) число точек взаимодействия называется
Альтернативой явных моделей воды является использование неявной сольватации модель, также называемая модель континуума, пример которого будет являться моделью КОСМО сольватации или модели поляризуемого континуума (РСМ) или гибридная модель сольватации.
Простые модели воды
Жесткие модели рассматриваются простейшие модели воды и полагаться на невалентных взаимодействиях . В этих моделях, склеивание взаимодействие неявно обрабатывают голономными ограничения . Электростатическое взаимодействие моделируется с помощью закона Кулона , и дисперсионные и силы отталкивания , используя потенциал Леннард-Джонса . Потенциал для моделей , таких как TIP3P (передача межмолекулярного потенциала с 3 точками) и TIP4P представлена
- Еaбзнак равноΣяна aΣJна бКСQяQJряJ+AрOO12-ВрOO6,{\ Displaystyle Е- {аЬ} = \ сумма _ {я} ^ {{\ текст {на}} в} \ сумма _ {j} ^ {{\ текст {на}} Ь} {\ гидроразрыва {k_ {C} q_ {я} q_ {j}} {r_ {IJ}}} + {\ гидроразрыва {A} {г _ {\ текст {OO}} ^ {12}}} — {\ гидроразрыва {B} {R _ {\ текст {ОО}} ^ {6}}}}
где к С , то электростатическим постоянному , имеет значение , равное 332,1 Å · ккал / (моль · е ²) в единицах , обычно используемых в молекулярном моделировании; д я и д J являются частичные заряды относительно заряда электрона; г IJ представляет собой расстояние между двумя атомами или заряженными участками; и и B являются параметры ЛД- . Заряженные сайты могут быть атомы или фиктивных сайты (например, неподеленный пар). В большинстве моделей водных термин Леннард-Джонса относится только к взаимодействию между атомами кислорода.
На приведенном ниже рисунке показан общий вид моделей от 3- до 6-сайта воды. Точные геометрические параметры (ОН расстояние и угол НОН) изменяются в зависимости от модели.
2-сайт
2-сайт модель воды на основе известной модели SPC-три сайта (см ниже), как была показана, чтобы предсказать диэлектрические свойства воды с использованием теории молекулярной жидкости сайта-перенормируются.
3-сайт
Модели Три сайта имеют три точки взаимодействия , соответствующую три атомов молекулы воды. Каждый сайт имеет точечный заряд, и участок , соответствующий атом кислорода также имеет параметры ЛД-Джонс. Так как модели 3-сайта достичь высокой вычислительной эффективности, они широко используются для многих применений молекулярной динамики моделирования. Большинство моделей использует жесткую геометрию соответствия , что реальные молекулы воды. Исключением является модель SPC, которая предполагает идеальную четырехгранную форму (НОН угол 109,47 °) , а не наблюдаемый угол 104,5 °.
В приведенной ниже таблице перечислены параметры для некоторых моделей 3-сайта.
| ЧАЕВЫЕ | SPC | TIP3P | SPC / E | |
|---|---|---|---|---|
| г (ОН), Å , | 0,9572 | 1,0 | 0,9572 | 1,0 |
| НОН, град | 104,52 | 109,47 | 104,52 | 109,47 |
| , 10 3 ккал в 12 / моль | 580,0 | 629,4 | 582,0 | 629,4 |
| Б , ккал в 6 / моль | 525,0 | 625,5 | 595,0 | 625,5 |
| д (О) | -0,80 | -0,82 | -0,834 | -0,8476 |
| д (Н) | +0,40 | 0,41 | 0,417 | 0,4238 |
/ Модель SPC E добавляет среднюю поправку поляризации к потенциальной функции энергии:
- ЕПолзнак равно12Σя(μ-μ0)2αя,{\ Displaystyle Е _ {\ текст {Pol}} = {\ гидроразрыва {1} {2}} \ сумма _ {I} {\ гидроразрыва {(\ му — \ му ^ {0}) ^ {2}} {\ альфа _ {я}}}}
где μ представляет собой электрический дипольный момент от эффективного поляризованной молекулы воды (2,35 D для модели SPC / E), ц 0 дипольного момент изолированной молекулы воды (1,85 D из эксперимента), и & alpha ; я является изотропной поляризуемостью постоянная , со значением 6960160800000000000 ♠1,608 × 10 -40 F · м 2 . Поскольку заряды в модели являются постоянными, эта коррекция просто приводит в добавлении 1,25 ккал / моль (5,22 кДж / моль) к полной энергии. ГПФ модели / Е приводит к лучшей плотности и коэффициента диффузии , чем модель SPC.
Модель TIP3P реализована в CHARMM силовом поле представляет собой слегка модифицированную версию оригинала. Отличие заключается в параметрах ЛД-: в отличие от TIP3P, версия CHARMM модели помещает параметры ЛД-на атомах водорода тоже, в дополнение к одному на кислород. Обвинения не изменяются. Модель Три сайта (TIP3P) имеет более высокую производительность в расчете теплоемкостей.
Гибкая модель SPC воды
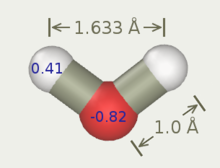 Гибкая модель SPC воды
Гибкая модель SPC водыГибкая простая модель воды точки-заряд (или гибкая модель воды SPC) является повторно параметризацией модели SPC воды три участка. SPC модель является жесткой, в то время как гибкий SPC модель является гибкой. В модели Тукан и Рахман, O-H , простирающейся выполнен ангармонический, и , следовательно, динамическое поведение хорошо описывается. Это одна из наиболее точных моделей трехцентровых вод без учета поляризации . В молекулярных динамиках моделирование дает правильную плотность и диэлектрическую проницаемость воды.
Гибкая SPC реализуется в программах MDynaMix и Abalone .
Другие модели
- Фергюсон (гибкий SPC)
- CVFF (гибкий)
- MG (гибкие и диссоциативный)
- KKY потенциал (гибкая модель).
- BLXL (мазок заряженный потенциал).
4-сайт
Модели четыре-сайта имеют четыре точки взаимодействия пути добавления одного фиктивный атома вблизи кислорода вдоль биссектрисы угла НОН моделей три-сайта (обозначенные М на рисунке). Фиктивная атом имеет только отрицательный заряд. Эта модель улучшает электростатическое распределение вокруг молекулы воды. Первая модель использовать этот подход был моделью Берналь-Фаулер опубликовал в 1933 году, который также может быть ранняя модель вода. Тем не менее, модель BF не воспроизводит хорошо объемные свойства воды, таких как плотность и теплота парообразования , и, таким образом , только исторический интерес. Это является следствием методы параметризации; новые модели, разработанные после современные компьютеры стали доступны, были настроены параметры, запустив Метрополис Монте — Карло или моделирования молекулярной динамики и корректировки параметров , пока объемные свойства не воспроизводятся достаточно хорошо.
Модель TIP4P, впервые опубликованная в 1983 году, широко применяется в вычислительных пакетах химии программного обеспечения и часто используется для моделирования биомолекулярных систем. Там были последующие заменами модели TIP4P для конкретных применений: модель TIP4P-РЭБ, для использования с методами суммирования Эвальда; TIP4P / Лед, для моделирования твердого водного льда; и TIP4P / 2005, общая параметризация для моделирования всей фазовой диаграммы конденсированной воды.
Большинство моделей четыре участка воды используют OH расстояние и угол НОН соответствия , что свободной молекулы воды. Исключением является OPC — модель, на которой нет геометрических ограничений не накладывается, кроме фундаментальной С 2v молекулярной симметрии молекулы воды. Вместо этого, точечные заряды и их позиции оптимизированы , чтобы наилучшим образом описать электростатики молекулы воды. ОРС воспроизводит полный набор объемных свойств более точно , чем обычно используются жесткие п -site модели воды. OPC модель реализуется в AMBER силовое поле.
| BF | TIPS2 | TIP4P | TIP4P-Еа | TIP4P / Ice | TIP4P / 2005 | OPC | TIP4P-Д | |
|---|---|---|---|---|---|---|---|---|
| г (ОН), Å , | 0,96 | 0,9572 | 0,9572 | 0,9572 | 0,9572 | 0,9572 | 0,8724 | 0,9572 |
| НОН, град | 105,7 | 104,52 | 104,52 | 104,52 | 104,52 | 104,52 | 103,6 | 104,52 |
| г (ОМ), Å , | 0,15 | 0,15 | 0,15 | 0,125 | 0,1577 | 0,1546 | 0,1594 | 0,1546 |
| , 10 3 ккал в 12 / моль | 560,4 | 695,0 | 600,0 | 656,1 | 857,9 | 731,3 | 865,1 | 904,7 |
| Б , ккал в 6 / моль | 837,0 | 600,0 | 610,0 | 653,5 | 850,5 | 736,0 | 858,1 | 900,0 |
| д (М) | -0,98 | -1,07 | -1,04 | -1,04844 | -1,1794 | -1,1128 | -1,3582 | -1,16 |
| д (Н) | 0,49 | 0,535 | 0,52 | 0,52422 | 0,5897 | 0,5564 | 0,6791 | 0,58 |
Другие:
- Q-TIP4P / F (гибкий)
5-сайт
Модели 5-сайта поместить отрицательный заряд на фиктивных атомах (меченый L ) , представляющих одинокие пары атома кислорода, с тетраэдрической-подобной геометрией. Ранняя модель такого типа была модель BNS Бен-Наим и Стиллингера, предложенный в 1971 году, вскоре сменил ST2 модели Стиллингера и Рахманом в 1974 году в основном из — за их более высокой стоимости вычислительной модели пять-сайт не были разработаны много до 2000 года, когда был опубликован модель TIP5P из Махони и Йоргенсен. По сравнению с более ранними моделями, в TIP5P модель приводит к улучшению в геометрии для димера воды , более «тетраэдрическая» вода структура , которая лучше воспроизводит экспериментальные функции радиального распределения от дифракции нейтронов , а температура максимальной плотности воды. Модель TIP5P-E является перепараметризацией TIP5P для использования с Эвальдом суммами .
| BNS | ST2 | TIP5P | TIP5P-E | |
|---|---|---|---|---|
| г (ОН), Å , | 1,0 | 1,0 | 0,9572 | 0,9572 |
| НОН, град | 109,47 | 109,47 | 104,52 | 104,52 |
| г (ПР), Å , | 1,0 | 0.8 | 0,70 | 0,70 |
| LOL, град | 109,47 | 109,47 | 109,47 | 109,47 |
| , 10 3 ккал в 12 / моль | 77,4 | 238,7 | 544,5 | 554,3 |
| Б , ккал в 6 / моль | 153,8 | 268,9 | 590,3 | 628,2 |
| д (л) | -0,19562 | -0,2357 | -0,241 | -0,241 |
| д (Н) | 0,19562 | 0,2357 | 0,241 | 0,241 |
| R L , Å , | 2,0379 | 2,0160 | ||
| R U , Å , | 3,1877 | 3,1287 |
Однако следует отметить, что модели BNS и ST2 не используют закон Кулона непосредственно для электростатических терминах, но модифицированную версию, которая уменьшенную на коротких расстояниях путем умножения на функции переключения S ( г ):
- S(ряJ)знак равно{0если ряJ≤рL,(ряJ-рL)2(3рU-рL-2ряJ)(рU-рL)2если рL≤ряJ≤рU,1если рU≤ряJ,{\ Displaystyle S (R_ {IJ}) = {\ BEGIN {случаи} 0 & {\ текст {если}} R_ {IJ} \ Leq R _ {\ текст {L}}, \\ {\ гидроразрыва {(R_ {IJ } -R_ {L}) ^ {2} (3R _ {\ текст {U}} — R _ {\ текст {L}} — 2r_ {IJ})} {(R _ {\ текст {U}} — R _ {\ текст {L}}) ^ {2}}} и {\ текст {если}} R _ {\ текст {L}} \ Leq r_ {IJ} \ Leq R _ {\ текст {U}}, \\ 1 & {\ текст {если}} R _ {\ текст {U}} \ Leq r_ {IJ}. \ конец {случаи}}}
Таким образом, R L и R U параметры применяются только к БНС и ST2.
6-сайт
Первоначально разработанный для изучения систем вода / лед, 6-сайт моделируют, который сочетает в себе все сайты моделей 4- и 5-сайт был разработан Нада и ван-дер-Eerden. Так как она имела очень высокую температуру плавления, при использовании при периодических электростатических условиях (Эвальд суммирования), модифицированная версия была опубликована позже, оптимизирована с помощью метода Эвальда для оценки кулоновского взаимодействия.
Другой
- Эффект явной модели растворенного вещества на поведении растворенного вещества в биомолекулярных моделированиях были также широко изучен. Было показано, что явные модели воды повлияли на специфическую сольватацию и динамики развернутых пептидов, в то время как конформационное поведение и гибкость складчатых пептидов остались нетронутыми.
- MB модель. Более абстрактные модели , напоминающие Mercedes-Benz логотип , который воспроизводит некоторые особенности воды в двумерных системах. Он не используется как таковой для моделирования «реальных» (то есть, трехмерных) систем, но это полезно для качественных исследований и в образовательных целях.
- Крупнозернистые модели. Одно- и два-сайта модели воды также были разработаны. В моделях крупнозернистых, каждый узел может представлять несколько молекул воды.
- Модели многих тел. Модели для воды, построенных с использованием учебно-набор конфигураций решаются квантовомеханический, которые затем используют протоколы обучения машины для извлечения поверхностей потенциальной энергии. Эти поверхности потенциальной энергии подают в МД для беспрецедентной степени точности при вычислении физических свойств конденсированных фазовых систем.
Вычислительная стоимость
Расчетная стоимость моделирования воды возрастает с увеличением числа сайтов взаимодействия в водной модели. Процессорное время приблизительно пропорционально числу межатомных расстояний, которые должны быть вычислено. Для модели 3-сайта, 9 расстояния требуются для каждой пары молекул воды (каждый атом одной молекулы с каждым атомом другой молекулы, или 3 × 3). Для модели 4-сайта, 10 расстояния требуется (каждый заряженный сайт с каждым заряженным сайтом, а также взаимодействием O-O, или 3 × 3 + 1). Для модели 5-сайта, 17 расстояния требуется (4 × 4 + 1). И, наконец, для модели 6-сайта, 26 расстояния требуется (5 × 5 + 1).
При использовании жестких моделей воды в молекулярных динамиках, есть дополнительные расходы , связанные с сохранением структуры с ограничениями, используя алгоритмы ограничений (хотя и с ограниченной длиной связей часто можно увеличить шаг по времени).
Смотрите также
Рекомендации
Разница между моделью воды и структурой воды
Доброе время суток. У меня вопрос: какая разница между моделью воды и структурой воды?
Спасибо.
С наилучшими пожеланиями, Богдан.
_____________
Термин структу́ра (от лат. structūra — «строение») имеет ряд значений, встречающихся в различных областях науки и человеческого знания.
Структура, совокупность устойчивых связей объекта, обеспечивающих его целостность и тождественность самому себе, т, е. сохранение основных свойств при различных внешних и внутренних изменениях.
В строгом смысле понятие структура впервые развивается в химии в связи с возникновением в 19 в. теории химического строения вещества.
В современной науке понятие структура обычно соотносится с понятиями системы и организации. Хотя единой точки зрения на соотношение этих понятий нет, однако в большинстве случаев в качестве наиболее широкого из них рассматривают понятие системы, характеризующее всё множество проявлений некоторого сложного объекта (его элементы, строение, связи, функции и т.д.). Структура выражает лишь то, что остаётся устойчивым, относительно неизменным при различных преобразованиях системы; организация же включает в себя как структурные, так и динамические характеристики системы, обеспечивающие её направленное функционирование.
В своём основном значении, структура есть внутреннее устройство чего-либо. Внутреннее устройство связано с категориями целого и его частей. Выявление связей, изучение взаимодействия и влияния составных частей различных по своей природе объектов позволяет выявить аналогии в их организации и изучать структуры абстрактно без связи с реальными объектами. Например, мы говорим об свойствах составляющих молекулы воды атомов водорода и кислорода образовывать водородные связи (ассоциаты) и выявляем в этих структурах общие свойства и т.д. и т.п.
В более узком понимании структура воды – это совокупность связывающих молекулы воды водородных связей, в результате которых в воде образуются структуры более сложного, чем сама вода порядка, состоящие от 2 до десятков и сотен молекул воды. Это как бы иной более высокий уровень организации.
Моде́ль (фр. modèle, от лат. modulus — «мера, аналог, образец») в отличие от структуры — материальный или мысленно представляемый объект, являющийся упрощённой версией моделируемого объекта или явления (прототипа) и в достаточной степени повторяющий все его свойства.
Модели обычно применяются для целей познания объективной реальности и конструирования. В качестве модели может выступать отображение, копия, макет, конструкция и др.
Модель в науке — любой образ, аналог (мысленный или условный: изображение, макет, схема, график, чертёж и т. п.) какого-либо объекта, процесса или явления оригинала данной модели. В данном случае модель – это абстрактная или конкретная копия объекта.
Следует подчеркнуть, однако, что иногда грань между этими двумя понятиями расплывчатая. Например, можно сказать модель структуры воды и т.п. Но это уже философия, а мы рассматриваем химию.
О. В. Мосин
Модели воды
Это продолжение статьи, начало — на предыдущих страницах данного раздела.
В настоящее время существуют и другие модели воды, объясняющие её аномальные свойства. Так, профессор Мартин Чаплин из Лондонского университета (Martin Chaplin Professor of Applied Science Water and Aqueous Systems Research of the London South Bank University) рассчитал и предположил иную структуру воды, в основе которой лежит икосаэдр (рис. 32).
Рис. 32. Формирование икосаэдра воды. Модель М. Чаплина.
Согласно этой модели вода состоит из 1820 молекул воды — это в два раза больше, чем в модели Зенина. Гигантский икосаэдр в свою очередь состоит из 13 более мелких структурных элементов. Причем, так же как и у Зенина, структура гигантского ассоциата базируется на более мелких образованиях.
См. ссылку: /article/learn/mathmodel.htm
В Черном море наблюдается другой интересный феномен. На глубинах в воде присутствует сероуглерод (H2S), концентрации которого настолько высоки, что ниже 120-200 метров в Чёрном море жизни почти нет. Причиной наличия таких высоких концентраций сероводорода в водах Черного моря является деятельность особых бактерий Bacterium hydrosuifureurn Penticum, Vibro sulfureus и Microspira aestuaria, способных выделять сероводород при восстановлении сульфатов, солей, растворенных в морской воде. В начале эволюции некоторые хемосинтетические бактерии использовали и энергию, полученную в результате окисления сероводорода (H2S) до серы (S).
В разные геологические эпохи сероводородные зоны занимали различную площадь. Около 3,5 — 3,7 миллиарда лет назад (самый ранний докембрий), когда атмосфера Земли содержала крайне мало кислорода, причем небиологического происхождения (образовывавшегося, например, при остывании базальтовой магмы, по гипотезе геохимика В.И. Вгатова), воды океана были полностью сероводородными. И первая жизнь в океане тоже была анаэробной. Первые живые простейшие, вероятно, мало отличались от современных нам анаэробных бактерий. Даже при отсутствии или малом количестве органического вещества, как это было в первичном океане, анаэробные бактерии могли выделять сероводород. Потом, по мере того как состав атмосферы изменялся, в ней скапливался кислород, сероводородные зоны уменьшались. Этот процесс продолжался сотни миллионов лет. Вероятно, вода Черного моря “сохранила” память о том первичном океане.
Биогенное происхождение имеет также и кислород атмосферы Земли, который образовался за счет процесса фотосинтеза зелеными растениями. Жизнь на Земле, как подтверждают данные палеогеологии, возникла в докембрийскую эпоху. Так, в научной литературе сообщалось о находках ископаемых водорослей в Южной Африке, возраст которых 2,7 млрд. лет. Обнаружены также остатки органического происхождения в южноафриканской формации Фиг-Три, возраст которой приблизительно 3,5 млрд. лет. Академик Б.С. Соколов на основе имеющихся сведений о развитии жизни на нашей планете в раннем докембрии сделал вывод, что биогенные накопления кислорода в океане начались 3,0 — 3,5 млрд. лет назад, а в атмосфере — 2 млрд. лет тому назад.
По мере того как атмосфера Земли в процессе её эволюции эволюционировала из восстановительной в окислительную, постепенно стало происходить „очищение” водной среды – гидросферы от дейтерия. По мнению Мосина, в те времена существовало два очень важных процесса. В первичной атмосфере Земли не было защитного кислородно-озонового слоя, защищающего поверхность Земли от жёсткого коротковолнового излучения Солнца. Поэтому, вследствие вулканических геотермальных и электрических процессов могло происходить обогащение гидросферы Земли дейтерием. Кроме того под действием излучения мог происходить фотолиз воды (Мосин, 1996).
На более позднем этапе вода могла очищаться от дейтерия при помощи горных пород. Большую роль в этом процессе, по-видимому, играли карстовые породы. В настоящее время содержание дейтерия в карстовых источниках равняется 30-35 г/тонна. В морской воде его содержание 130-150 г/тонна. Очевидно, что когда в воде меньше дейтерия, эволюция происходит быстрее. Если на Земле не начался бы природный процесс очищения от дейтерия, эволюция могла „застыть” на очень низком уровне.
С годами температура Земли понижалась. На определенном этапе эволюции Земли, температура воды была на10-15°C выше теперешней. А когда температура снизилась до 3,8 °C, в первую очередь замерзала тяжёлая вода. Это означает, что лед сначала встраивает в свою кристаллическую решётку атомы дейтерия (Д-р Игнатов, 2010). При этом природный лёд обычно значительно чище, чем вода, так как при кристаллизации воды в кристаллическую решётку встраиваются молекулы воды, а примеси вытесняются в жидкость. Растущий кристалл льда, тем самым, всегда стремится создать идеальную кристаллическую решетку и вытесняет посторонние вещества. В планетарном масштабе именно замечательный феномен замерзания и таяния воды играет роль гигантского очистительного процесса — вода на Земле постоянно очищает сама себя.


