§ 5. Углеводы. Биология 9 класс Пасечник
- ГДЗ
- 1 Класс
- Окружающий мир
- 2 Класс
- Литература
- Окружающий мир
- 3 Класс
- Окружающий мир
- 4 Класс
- Окружающий мир
- 5 Класс
- Биология
- География
- Литература
- Обществознание
- Технология
- Естествознание
- 6 Класс
- Биология
- История
- География
- Литература
- Обществознание
- 7 Класс
- Биология
- История
- ОБЖ
- География
- Литература
- Обществознание
- 8 Класс
- Биология
- История
- География
- Литература
- Обществознание
- 9 Класс
- Биология
- История
- География
- Литература
- 10 Класс
- Биология
- История
- Обществознание
- 11 Класс
- Английский язык
- Немецкий язык
Углеводы | Параграф 1.2
«Введение в общую биологию и экологию. 9 класс». А.А. Каменский (гдз)
Вопрос 1. Какой состав и строение имеют молекулы углеводов?
Сахара (углеводы) являются одной из наиболее важных и распространённых групп природных органических соединений. Они составляют до 80% массы сухого вещества растений и около 2% сухого вещества животных организмов. Молекулы углеводов состоят из атомов углерода, водорода и кислорода, причем соотношение водорода и кислорода в них 2:1, как в молекуле воды. Именно по этой причине эти вещества получили свое название «углеводы».
Вопрос 2. Какие углеводы называются моно-, ди- и полисахаридами
Моносахариды — это углеводы, в состав которых входит от трех до шести атомов углерода. Из шестиуглеродных сахаров известны глюкоза, фруктоза, галактоза, из пятиуглеродных сахаров — рибоза и дезоксирибоза. Последние входят в состав нуклеиновых кислот.
Дисахариды состоят из двух молекул моносахаридов. Например, сахароза (тростниковый сахар) состоит из молекул глюкозы и фруктозы. Из дисахаридов известны также мальтоза (солодовый сахар) и лактоза (молочный сахар). И моно — и дисахариды растворимы в воде и сладки на вкус.
Полисахариды — сложные сахара, состоящие из множества мономеров, которыми являются моносахариды. К полисахаридам относятся крахмал, гликоген, целлюлоза, хитин. Целлюлоза — линейный полимер, состоящий из множества молекул глюкозы. Крахмал и гликоген также состоят из глюкозы, только имеют разветвленную структуру.
Вопрос 3. Какие функции выполняют углеводы в живых организмах?
1. Энергетическая функция. Углеводы — основные источники энергии в клетке. При полном расщеплении 1 г глюкозы высвобождается 17,6 кДж энергии.
2. Запасающая функция. Крахмал и гликоген используются клетками растений и животных для запасания энергии.
3. Структурная функция. Целлюлоза и хитин обеспечивают прочность клеточных стенок растений и грибов. Некоторые сложные полисахариды, состоящие из двух типов простых сахаров, входят в состав сухожилий, хрящей, вещества кожи, придавая этим тканям прочность и эластичность, входят в состав ДНК, РНК и АТФ в виде дезоксирибозы и рибозы.
4. Защитная функция. Хитин является защитным компонентом тканей животных.
5. Рецепторная функция. Некоторые углеводы служат рецепторами в составе клеточных мембран и обеспечивают узнавание клетками друг друга при взаимодействии.
1.2. Углеводы | ВСЕ Сочинения.RU
Вопрос 1. Какой состав и строение имеют молекулы углеводов?
Молекулы углеводов состоят из атомов углерода, водорода и кислорода, причем соотношение водорода и кислорода в них 2:1, как в молекуле воды. Именно по этой причине эти вещества получили свое название «углеводы».
Вопрос 2. Какие углеводы называются моно-, ди- и полисахаридами?
Моносахариды — это углеводы, в состав которых входит от трех до шести атомов углерода. Из шестиуглеродных сахаров известны глюкоза, фруктоза, галактоза, из пятиуглеродных сахаров — рибоза и дезоксирибоза. Последние входят в состав нуклеиновых кислот.
Дисахариды состоят из двух молекул моносахаридов. Например, сахароза (тростниковый сахар) состоит из молекул глюкозы и фруктозы. Из дисахаридов известны также мальтоза (солодовый сахар) и лактоза (молочный сахар). И моно- и дисахариды растворимы в воде и сладки на вкус.
Полисахариды — сложные сахара, состоящие из множества мономеров, которыми являются моносахариды. К полисахаридам относятся крахмал, гликоген, целлюлоза, хитин. Целлюлоза — линейный полимер, состоящий из множества молекул глюкозы. Крахмал и гликоген также состоят из глюкозы, только имеют разветвленную структуру.
Вопрос 3. Какие функции выполняют углеводы в живых организмах?
Энергетическая функция. Углеводы — основные источники энергии в клетке. При полном расщеплении 1 г глюкозы высвобождается 17,6 кДж энергии.
Запасающая функция. Крахмал и гликоген используются клетками растений и животных для запасания энергии.
Структурная функция. Целлюлоза и хитин обеспечивают прочность клеточных стенок растений и грибов. Некоторые сложные полисахариды, состоящие из двух типов простых сахаров, входят в состав сухожилий, хрящей, вещества кожи, придавая этим тканям прочность и эластичность.
Защитная функция. Хитин является защитным компонентом тканей животных.
Рецепторная функция. Некоторые углеводы служат рецепторами в составе клеточных мембран и обеспечивают узнавание клетками друг друга при взаимодействии.
1.2. Углеводы
4.3 (86.15%) 13 votesНа этой странице искали :
- какой состав и строение имеют молекулы углеводов
- какие функции выполняют углеводы в живых организмах
- какой состав и строение имеют молекулы углеводов?
- какие углеводы называются моно ди и полисахаридами
- углеводы не выполняют функцию
Сохрани к себе на стену!
Углеводы, их строение и функции. Строение углеводов
- ГДЗ
- 1 Класс
- Окружающий мир
- 2 Класс
- Литература
- Окружающий мир
- 3 Класс
- Окружающий мир
- 4 Класс
- Окружающий мир
- 5 Класс
- Биология
- История
- География
- Литература
- Обществознание
- Человек и мир
- Технология
- Естествознание
- 6 Класс
- Биология
- История
- География
- Литература
- Обществознание
- Технология
- 7 Класс
- Биология
- История
- ОБЖ
- География
- Литература
- Обществознание
- 8 Класс
- Биология
- История
- География
- Литература
- Обществознание
- 9 Класс
- Биология
- История
- География
- Литература
- Обществознание
- 10 Класс
- Биология
- История
- География
- Обществознание
- 11 Класс
- Английский язык
Углеводы — Википедия
Углево́ды — органические вещества, содержащие карбонильную группу и несколько гидроксильных групп[1]. Название класса соединений происходит от слов «гидраты углерода», оно было предложено Карлом Шмидтом в 1844 году. Появление такого названия связано с тем, что первые из известных науке углеводов описывались брутто-формулой Cx(H2O)y, формально являясь соединениями углерода и воды.
Сахара́ — другое название низкомолекулярных углеводов: моносахаридов, дисахаридов и олигосахаридов.
Углеводы являются неотъемлемым компонентом клеток и тканей всех живых организмов представителей растительного и животного мира, составляя (по массе) основную часть органического вещества на Земле. Источником углеводов для всех живых организмов является процесс фотосинтеза, осуществляемый растениями.
Углеводы — весьма обширный класс органических соединений, среди них встречаются вещества с сильно различающимися свойствами. Это позволяет углеводам выполнять разнообразные функции в живых организмах. Соединения этого класса составляют около 80 % сухой массы растений и 2—3 % массы животных[1].
Все углеводы состоят из отдельных «единиц», которыми являются сахариды. По способности к гидролизу на мономеры углеводы делятся на две группы: простые и сложные. Углеводы, содержащие одну единицу, называются моносахариды, две единицы — дисахариды, от двух до десяти единиц — олигосахариды, а более десяти — полисахариды. Моносахариды быстро повышают содержание сахара в крови и обладают высоким гликемическим индексом, поэтому их ещё называют быстрыми углеводами. Они легко растворяются в воде и синтезируются в зелёных растениях. Углеводы, состоящие из 3 или более единиц, называются сложными. Продукты, богатые сложными углеводами, постепенно повышают содержание глюкозы и имеют низкий гликемический индекс, поэтому их ещё называют медленными углеводами. Сложные углеводы являются продуктами поликонденсации простых сахаров (моносахаридов) и, в отличие от простых, в процессе гидролитического расщепления способны распадаться на мономеры с образованием сотен и тысяч молекул моносахаридов.
Моносахариды[править | править код]
 Распространённый в природе моносахарид — бета-D-глюкоза.
Распространённый в природе моносахарид — бета-D-глюкоза.Моносахари́ды (от др.-греч. μόνος ‘единственный’, лат. saccharum ‘сахар’ и суффикса -ид) — простейшие углеводы, не гидролизующиеся с образованием более простых углеводов — обычно представляют собой бесцветные, легко растворимые в воде, плохо — в спирте и совсем нерастворимые в эфире, твёрдые прозрачные органические соединения[2], одна из основных групп углеводов, самая простая форма сахара. Водные растворы имеют нейтральный pH. Некоторые моносахариды обладают сладким вкусом. Моносахариды содержат карбонильную (альдегидную или кетонную) группу, поэтому их можно рассматривать как производные многоатомных спиртов. Моносахарид, у которого карбонильная группа расположена в конце цепи, представляет собой альдегид и называется альдоза. При любом другом положении карбонильной группы моносахарид является кетоном и называется кетоза. В зависимости от длины углеродной цепи (от трёх до десяти атомов) различают триозы, тетрозы, пентозы, гексозы, гептозы и так далее. Среди них наибольшее распространение в природе получили пентозы и гексозы[2]. Моносахариды — стандартные блоки, из которых синтезируются дисахариды, олигосахариды и полисахариды.
В природе в свободном виде наиболее распространена D-глюкоза (C6H12O6) — структурная единица многих дисахаридов (мальтозы, сахарозы и лактозы) и полисахаридов (целлюлоза, крахмал). Другие моносахариды, в основном, известны как компоненты ди-, олиго- или полисахаридов и в свободном состоянии встречаются редко. Природные полисахариды служат основными источниками моносахаридов[2].
Дисахариды[править | править код]
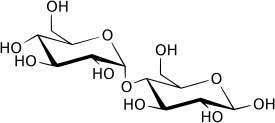
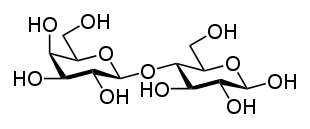
Дисахари́ды (от др.-греч. δία ‘два’, лат. saccharum ‘сахар’ и суффикса -ид) — сложные органические соединения, одна из основных групп углеводов, при гидролизе каждая молекула распадается на две молекулы моносахаридов, являются частным случаем олигосахаридов. По строению дисахариды представляют собой гликозиды, в которых две молекулы моносахаридов соединены друг с другом гликозидной связью, образованной в результате взаимодействия гидроксильных групп (двух полуацетальных или одной полуацетальной и одной спиртовой). В зависимости от строения дисахариды делятся на две группы: восстанавливающие и невосстанавливающие. Например, в молекуле мальтозы у второго остатка моносахарида (глюкозы) имеется свободный полуацетальный гидроксил, придающий данному дисахариду восстанавливающие свойства. Дисахариды наряду с полисахаридами являются одним из основных источников углеводов в рационе человека и животных[3].
Олигосахариды[править | править код]

О́лигосахари́ды (от греч. ὀλίγος — немногий) — углеводы, молекулы которых синтезированы из 2—10 остатков моносахаридов, соединённых гликозидными связями. Соответственно различают: дисахариды, трисахариды и так далее[3]. Олигосахариды, состоящие из одинаковых моносахаридных остатков, называют гомополисахаридами, а из разных — гетерополисахаридами. Наиболее распространены среди олигосахаридов дисахариды.
Среди природных трисахаридов наиболее распространена рафиноза — невосстанавливающий олигосахарид, содержащий остатки фруктозы, глюкозы и галактозы — в больших количествах содержится в сахарной свёкле и во многих других растениях[3].
Полисахариды[править | править код]
Полисахари́ды — общее название класса сложных высокомолекулярных углеводов, молекулы которых состоят из десятков, сотен или тысяч мономеров — моносахаридов. С точки зрения общих принципов строения в группе полисахаридов возможно различить гомополисахариды, синтезированные из однотипных моносахаридных единиц и гетерополисахариды, для которых характерно наличие двух или нескольких типов мономерных остатков[4].
Гомополисахариды (гликаны), состоящие из остатков одного моносахарида, могут быть гексозами или пентозами, то есть в качестве мономера может быть использована гексоза или пентоза. В зависимости от химической природы полисахарида различают глюканы (из остатков глюкозы), маннаны (из маннозы), галактаны (из галактозы) и другие подобные соединения. К группе гомополисахаридов относятся органические соединения растительного (крахмал, целлюлоза, пектиновые вещества), животного (гликоген, хитин) и бактериального (декстраны) происхождения[2].
Полисахариды необходимы для жизнедеятельности животных и растительных организмов. Это один из основных источников энергии организма, образующейся в результате обмена веществ. Полисахариды принимают участие в иммунных процессах, обеспечивают сцепление клеток в тканях, являются основной массой органического вещества в биосфере.
Крахма́л (C6H10O5)n — смесь двух гомополисахаридов: линейного — амилозы и разветвлённого — амилопектина, мономером которых является альфа-глюкоза. Белое аморфное вещество, не растворимое в холодной воде, способное к набуханию и частично растворимое в горячей воде[2]. Молекулярная масса 105—107 Дальтон. Крахмал, синтезируемый разными растениями в хлоропластах, под действием света при фотосинтезе, несколько различается по структуре зёрен, степени полимеризации молекул, строению полимерных цепей и физико-химическим свойствам. Как правило, содержание амилозы в крахмале составляет 10—30 %, амилопектина — 70—90 %. Молекула амилозы содержит в среднем около 1000 остатков глюкозы, связанных между собой альфа-1,4-связями. Отдельные линейные участки молекулы амилопектина состоят из 20—30 таких единиц, а в точках ветвления амилопектина остатки глюкозы связаны межцепочечными альфа-1,6-связями. При частичном кислотном гидролизе крахмала образуются полисахариды меньшей степени полимеризации — декстрины (C6H10O5)p, а при полном гидролизе — глюкоза[4].
 Структура гликогена
Структура гликогенаГликоге́н (C6H10O5)n — полисахарид, построенный из остатков альфа-D-глюкозы — главный резервный полисахарид высших животных и человека, содержится в виде гранул в цитоплазме клеток практически во всех органах и тканях, однако, наибольшее его количество накапливается в мышцах и печени. Молекула гликогена построена из ветвящихся полиглюкозидных цепей, в линейной последовательности которых, остатки глюкозы соединены посредством альфа-1,4-связями, а в точках ветвления межцепочечными альфа-1,6-связями. Эмпирическая формула гликогена идентична формуле крахмала. По химическому строению гликоген близок к амилопектину с более выраженной разветвлённостью цепей, поэтому иногда называется неточным термином «животный крахмал». Молекулярная масса 105—108 Дальтон и выше[4]. В организмах животных является структурным и функциональным аналогом полисахарида растений — крахмала. Гликоген образует энергетический резерв, который при необходимости восполнить внезапный недостаток глюкозы может быть быстро мобилизован — сильное разветвление его молекулы ведёт к наличию большого числа концевых остатков, обеспечивающих возможность быстрого отщепления нужного количества молекул глюкозы[2]. В отличие от запаса триглицеридов (жиров) запас гликогена не настолько ёмок (в калориях на грамм). Только гликоген, запасённый в клетках печени (гепатоцитах) может быть переработан в глюкозу для питания всего организма, при этом гепатоциты способны накапливать до 8 процентов своего веса в виде гликогена, что является максимальной концентрацией среди всех видов клеток. Общая масса гликогена в печени взрослых может достигать 100—120 граммов. В мышцах гликоген расщепляется на глюкозу исключительно для локального потребления и накапливается в гораздо меньших концентрациях (не более 1 % от общей массы мышц), тем не менее общий запас в мышцах может превышать запас, накопленный в гепатоцитах.
Целлюло́за (клетча́тка) — наиболее распространённый структурный полисахарид растительного мира, состоящий из остатков альфа-глюкозы, представленных в бета-пиранозной форме. Таким образом, в молекуле целлюлозы бета-глюкопиранозные мономерные единицы линейно соединены между собой бета-1,4-связями. При частичном гидролизе целлюлозы образуется дисахарид целлобиоза, а при полном — D-глюкоза. В желудочно-кишечном тракте человека целлюлоза не переваривается, так как набор пищеварительных ферментов не содержит бета-глюкозидазу. Тем не менее, наличие оптимального количества растительной клетчатки в пище способствует нормальному формированию каловых масс[4]. Обладая большой механической прочностью, целлюлоза выполняет роль опорного материала растений, например, в составе древесины её доля варьирует от 50 до 70 %, а хлопок представляет собой практически стопроцентную целлюлозу[2].
Хити́н — структурный полисахарид низших растений, грибов и беспозвоночных животных (в основном роговые оболочки членистоногих — насекомых и ракообразных). Хитин, подобно целлюлозе в растениях, выполняет опорные и механические функции в организмах грибов и животных. Молекула хитина построена из остатков N-ацетил-D-глюкозамина, связанных между собой бета-1,4-гликозидными связями. Макромолекулы хитина неразветвлённые и их пространственная укладка не имеет ничего общего с целлюлозой[2].
Пекти́новые вещества́ — полигалактуроновая кислота, содержится в плодах и овощах, остатки D-галактуроновой кислоты связаны альфа-1,4-гликозидными связями. В присутствии органических кислот способны к желеобразованию, применяются в пищевой промышленности для приготовления желе и мармелада. Некоторые пектиновые вещества оказывают противоязвенный эффект и являются активной составляющей ряда фармацевтических препаратов, например, производное подорожника «плантаглюцид»[2].
Мурами́н (лат. múrus — стенка) — полисахарид, опорно-механический материал клеточной стенки бактерий. По химическому строению представляет собой неразветвлённую цепь, построенную из чередующихся остатков N-ацетилглюкозамина и N-ацетилмурамовой кислоты, соединённых бета-1,4-гликозидной связью. Мурамин по структурной организации (неразветвлённая цепь бета-1,4-полиглюкопиранозного скелета) и функциональной роли весьма близок к хитину и целлюлозе[2].
Декстра́ны — полисахариды бактериального происхождения — синтезируются в условиях промышленного производства микробиологическим путём (воздействием микроорганизмов Leuconostoc mesenteroides на раствор сахарозы) и используются в качестве заменителей плазмы крови (так называемые клинические «декстраны»: Полиглюкин и другие)[2].
 |  | |
Слева D-глицеральдегид, справа L-глицеральдегид. | ||
Изомерия (от др.-греч. ἴσος — равный, и μέρος — доля, часть) — существование химических соединений (изомеров), одинаковых по составу и молекулярной массе, различающихся по строению или расположению атомов в пространстве и, вследствие этого, по свойствам.
Стереоизомерия моносахаридов: изомер глицеральдегида, у которого при проецировании модели на плоскость ОН-группа у асимметричного атома углерода расположена с правой стороны, принято считать D-глицеральдегидом, а зеркальное отражение — L-глицеральдегидом. Все изомеры моносахаридов делятся на D- и L- формы по сходству расположения ОН-группы у последнего асимметричного атома углерода возле СН2ОН-группы (кетозы содержат на один асимметричный атом углерода меньше, чем альдозы с тем же числом атомов углерода). Природные гексозы — глюкоза, фруктоза, манноза и галактоза — по стереохимической конфигурациям относят к соединениям D-ряда[5].
В живых организмах углеводы выполняют следующие функции:
- Структурная и опорная функции. Углеводы участвуют в построении различных опорных структур. Так, целлюлоза является основным структурным компонентом клеточных стенок растений, хитин выполняет аналогичную функцию у грибов, а также обеспечивает жёсткость экзоскелета членистоногих[1].
- Защитная роль у растений. У некоторых растений есть защитные образования (шипы, колючки и др.), состоящие из клеточных стенок мёртвых клеток.
- Пластическая функция. Углеводы входят в состав сложных молекул (например, пентозы (рибоза и дезоксирибоза) участвуют в построении АТФ, ДНК и РНК)[6].
- Энергетическая функция. Углеводы служат источником энергии: при окислении 1 грамма углеводов выделяются 4,1 ккал энергии и 0,4 г воды[6].
- Запасающая функция. Углеводы выступают в качестве запасных питательных веществ: гликоген у животных, крахмал и инулин — у растений[1].
- Осмотическая функция. Углеводы участвуют в регуляции осмотического давления в организме. Так, в крови содержится 100—110 мг/л глюкозы, от концентрации глюкозы зависит осмотическое давление крови.
- Рецепторная функция. Олигосахариды входят в состав воспринимающей части многих клеточных рецепторов или молекул-лигандов.
В суточном рационе человека и животных преобладают углеводы. Травоядные получают крахмал, клетчатку, сахарозу. Хищники получают гликоген с мясом.
Организмы животных не способны синтезировать углеводы из неорганических веществ. Они получают их от растений с пищей и используют в качестве главного источника энергии, получаемой в процессе окисления:
- Cx(h3O)y+xO2→xCO2+yh3O, ΔH<0.001{\displaystyle {\mathsf {C_{x}(H_{2}O)_{y}+xO_{2}\rightarrow xCO_{2}+yH_{2}O,\ \Delta H<0.001}}}
В зелёных листьях растений углеводы образуются в процессе фотосинтеза — уникального биологического процесса превращения в сахара неорганических веществ — оксида углерода (IV) и воды, происходящего при участии хлорофилла за счёт солнечной энергии:
- xCO2+yh3O→Cx(h3O)y+xO2{\displaystyle {\mathsf {xCO_{2}+yH_{2}O\rightarrow C_{x}(H_{2}O)_{y}+xO_{2}}}}
Обмен углеводов в организме человека и высших животных складывается из нескольких процессов[4]:
- Гидролиз (расщепление) в желудочно-кишечном тракте полисахаридов и дисахаридов пищи до моносахаридов, с последующим всасыванием из просвета кишки в кровеносное русло.
- Гликогеногенез (синтез) и гликогенолиз (распад) гликогена в тканях, в основном в печени.
- Аэробный (пентозофосфатный путь окисления глюкозы или пентозный цикл) и анаэробный (без потребления кислорода) гликолиз — пути расщепления глюкозы в организме.
- Взаимопревращение гексоз.
- Аэробное окисление продукта гликолиза — пирувата (завершающая стадия углеводного обмена).
- Глюконеогенез — синтез углеводов из неуглеводистого сырья (пировиноградная, молочная кислота, глицерин, аминокислоты и другие органические соединения).
Главными источниками углеводов из пищи являются: хлеб, картофель, макароны, крупы, сладости. Чистым углеводом является сахар. Мёд, содержит 65% фруктозы и 25-30% глюкозы.
Для обозначения количества углеводов в пище используется специальная хлебная единица.
К углеводной группе, кроме того, примыкают и плохо перевариваемые человеческим организмом клетчатка и пектины.
Список наиболее распространенных углеводов[править | править код]
- ↑ 1 2 3 4 Н. А. Абакумова, Н. Н. Быкова. 9. Углеводы // Органическая химия и основы биохимии. Часть 1. — Тамбов: ГОУ ВПО ТГТУ, 2010. — ISBN 978-5-8265-0922-7.
- ↑ 1 2 3 4 5 6 7 8 9 10 11 Н. А. Тюкавкина, Ю. И. Бауков. Биоорганическая химия. — 1-е изд. — М.: Медицина, 1985. — С. 349—400. — 480 с. — (Учебная литература для студентов медицинских институтов). — 75 000 экз.
- ↑ 1 2 3 Т. Т. Березов, Б. Ф. Коровкин. Биологическая химия / Под ред. акад. АМН СССР С. С. Дебова.. — 2-е изд., перераб. и доп. — М.: Медицина, 1990. — С. 234—235. — 528 с. — (Учебная литература для студентов медицинских институтов). — 100 000 экз. — ISBN 5-225-01515-8.
- ↑ 1 2 3 4 5 Т. Т. Березов, Б. Ф. Коровкин. Биологическая химия / Под ред. акад. АМН СССР С. С. Дебова.. — 2-е изд., перераб. и доп. — М.: Медицина, 1990. — С. 235—238. — 528 с. — (Учебная литература для студентов медицинских институтов). — 100 000 экз. — ISBN 5-225-01515-8.
- ↑ Т. Т. Березов, Б. Ф. Коровкин. Биологическая химия: Учебник / Под ред. акад. АМН СССР С. С. Дебова.. — 2-е изд., перераб. и доп. — М.: Медицина, 1990. — С. 226—276. — 528 с. — 100 000 экз. — ISBN 5-225-01515-8.
- ↑ 1 2 А. Я. Николаев. 9. Обмен и функции углеводов // Биологическая химия. — М.: Медицинское информационное агентство, 2004. — ISBN 5-89481-219-4.
- Углеводы (рус.) (недоступная ссылка). — строение и химические свойства. Дата обращения 1 июня 2009. Архивировано 25 июля 2001 года.
| Общие: | |||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Геометрия | |||||||||||||||
| Моносахариды |
| ||||||||||||||
| Мультисахариды | |||||||||||||||
| Производные углеводов | |||||||||||||||
Урок 32. состав – структура – свойства — Естествознание — 10 класс
Естествознание, 10 класс
Урок 32. Состав – структура — свойства
Перечень вопросов, рассматриваемых в теме:
- Какова структура вещества? Все ли вещества имеют молекулярную структуру?
- В чем причина многообразия веществ? Как структура молекул влияет на свойства веществ?
- Можно ли прогнозировать свойства вещества, зная его структуру (строение)?
Глоссарий по теме:
Генезис (греч. — genesis) — происхождение, становление и развитие, результатом которого является определенное состояние изучаемого объекта. Генезис природных и социальных явлений интересовал и интересует философию и науку с античности до наших дней (философский словарь).
Структу́ра (от лат. Structūra — «строение»), или строе́ние — внутреннее устройство чего-либо / Ожегов С.И. и Шведова Н.Ю. Толковый словарь русского языка. / Российская академия наук. Институт русского языка им. В.В.Виноградова. — М.:Азбуковник, 1999/.
Качественный состав – это перечень всех образующих вещество химических элементов.
Количественный состав – это число атомов каждого химического элемента в составе мельчайшей частицы вещества – его молекулы.
Запись, выражающая качественный и количественный состав вещества с помощью хими-ческих знаков, называется химической формулой.
Закон постоянства состава: Многие вещества, независимо от нахождения в природе или способа получения их в лаборатории, всегда имеют один и тот же состав.
Химическая связь – это совокупность сил, связывающих и удерживающих атомы или другие частицы в устойчивых структурах (молекулах и др.).
Гибридизация атомных орбиталей – это их перемешивание в пространстве с целью выравнивания и обеспечения наиболее полного перекрывания.
Аллотропия – это явление, при котором один и тот же химический элемент образует несколько простых веществ. Простые вещества, образованные одним элементом – это аллотропные модификации (видоизменения) этого элемента.
Изомерия – это явление, при котором существуют вещества, имеющие одинаковый состав, но разное химическое строение, а потому и свойства. Вещества, имеющие одинаковый состав, но разное химическое строение, а потому и разные свойства, называются изомерами.
Основная и дополнительная литература по теме урока:
Основные источники:
- Еремин В.В. Теоретическая и математическая химия для школьников. – М.: МЦНМО, 2007.
- Миттова И.Я., Самойлов А.М. История химии с древнейших времен до конца XX века: учебное пособие в 2-х томах. Т. 1. – Долгопрудный: ИД «Интеллект», 2009.
- Папулов Ю.Г, Левин В.П., Виноградова М.Г. Строение вещества в естественнонаучной картине мира: Молекулярные аспекты. Учебное пособие, 2-ое издание. Тверь: ТвГУ, 2005 — 208 с.
Дополнительные источники:
- Травень В. Ф. «Органическая химия», в 2-х томах. Москва, ИКЦ «Академкнига», 2004.
- Химия. Школьная энциклопедия. Гл. ред. Ю.А.Золотов. М.: Большая российская энциклопедия, 2003.
- Энциклопедия для детей. Том 17. Химия. Гл. ред. В.А.Володин. — М.: Аванта+, 2000.
Теоретический материал для самостоятельного изучения
Учение о молекуле лежит в основе всех
других обобщений, так что современную химию
можно по праву назвать молекулярной химией.
А. М. Бутлеров, (1828-1886), русский химик, создатель теории химического строения органических веществ, учёный-пчеловод и лепидоптеролог, общественный деятель
Установление взаимосвязи между свойствами веществ и строением молекул составляет фундаментальную научную проблему химии. В ходе химических реакций происходит перегруппировка атомов в молекулах реагентов и образуются новые соединения. Поэтому одна из фундаментальных химических проблем состоит в выяснении порядка расположения атомов (связей) в исходных соединениях и характера изменений при образовании из них других соединений.
Мы знаем, что молекула представляет собой микрочастицу, образованную из атомов и способную к самостоятельному существованию, обладающую его главными химическими свойствами. Она имеет постоянный состав входящих в нее атомных ядер и фиксированное число электронов и обладает совокупностью свойств, позволяющих отличать молекулы одного вида от молекул другого. Число атомов в молекуле может быть различным: от двух до сотен тысяч. Молекулы простых веществ состоят из одинаковых атомов, сложных – из разных атомов. Существует большое количество соединений, молекулы которых состоят из многих тысяч атомов — макромолекулы.
Первые представления о структуре молекул основывались на химическом анализе. Со времен М.В. Ломоносова (1741), который высказал мысль, что свойства вещества зависят от рода, числа и расположения «элементов» (атомов), составляющих его «корпускулу» (молекулу), представления усложнялись по мере накопления знаний о химических свойствах веществ. Применение основных законов химии позволило определить число и тип атомов, из которых состоит молекула данного соединения; эта информация содержится в химической формуле, составленной на основе качественного и количественного анализа, а также закона постоянства состава (Ж.Пруст). В дальнейшем А.М. Бутлеров (1861) ввел понятие химического строения (как порядка связи атомов в молекуле) и показал, что свойства вещества определяются его составом и химическим строением. Стереохимическая гипотеза Я. Вант-Гоффа и Ле Беля (1874) расширила понятие строения. Оказалось, что свойства вещества зависят как от химического (в топологическом плане), так и пространственного строения молекул. Со временем химики осознали, что одной химической формулы недостаточно для точной характеристики молекулы, поскольку существуют молекулы-изомеры, имеющие одинаковые химические формулы, но разные свойства. Этот факт навел ученых на мысль, что атомы в молекуле должны иметь определенную топологию, стабилизируемую связями между ними. Впервые эту идею высказал в 1858 немецкий химик Ф.Кекуле. Согласно его представлениям, молекулу можно изобразить с помощью структурной формулы, в которой указаны не только сами атомы, но и связи между ними. Межатомные связи должны также соответствовать пространственному расположению атомов. В таблице 1 отражена зависимость пространственного строения веществ от типа гибридизации.
«Пространственное строение частиц в зависимости от типа гибридизации». Приведите свои примеры веществ.
Тип гибриди-зации центрального атома | Пространственное строение частицы | Условное изображение | Примеры |
sp | Линейное |
| ВеС12, ZnCl2, С2Н2 |
sp2 | Плоскостно-тригональное |
| BCl3, N03—,CO32-, C2H4, C6H6 |
sp3 | Тетраэдр |
| CH4, NH4+, SO42-, CC14 |
sp3 | Тригональная пирамида |
| NH3, H30+ |
sp3 | Угловое |
| Н20 |
Чем различаются понятия «свойства молекулы» и «свойства вещества»?
Подсказка. Допустим, вы открыли химический справочник и в статье «Азот» прочитали: «N2 – газ без цвета и запаха, tкип = –196 °С, tпл = –210 °С, энергия химической связи 940 кДж/моль». Какие из этих характеристик относятся к свойствам молекулы азота, а какие к свойствам простого вещества?
В состав молекулы может входить различное число атомов. Так, молекулы благородных газов одноатомны, молекулы таких веществ, как водород, азот, — двухатомны, воды — трехатомны и т.д. Молекулы наиболее сложных веществ — высших белков и нуклеиновых кислот — построены их такого количества атомов, которое измеряется сотнями тысяч. При этом атомы могут соединяться друг с другом не только в различных соотношениях, но и различным образом. Поэтому при сравнительно небольшом числе химических элементов число различных веществ очень велико.
Все ли вещества состоят из молекул?
Подсказка. Для ответа на этот вопрос обратитесь к строению таких веществ как металлы, алмаз, графит, хлорид натрия.
Не во всех случаях частицы, образующие вещество, представляют собой молекулы.
Многие вещества в твердом и жидком состоянии, например, большинство солей, имеют не молекулярную, а ионную структуру. Некоторые вещества имеют атомное строение. В веществах, имеющих ионное или атомное строение, носителем химических свойств являются не молекулы, а те комбинации ионов или атомов, которые образуют данное вещество.
Вспомните, какие типы связей и кристаллических решеток существуют? Чем определяются свойства веществ?
В зависимости от природы частиц, образующих кристалл, различают атомные, молекулярные, ионные и металлические кристаллические решетки
Таблица 2 «Зависимость свойств веществ от типа связи и кристаллических решеток»
Тип кристаллической решетки | Характерный вид химической связи | Частицы, располагающиеся в узлах решетки | Примеры веществ и их характерные свойства |
Атомная | Ковалентная неполярная | Атомы | Некоторые неметаллы, оксиды и др. Чаще твердые вещества, обладающие высокой прочностью. Тугоплавки. Полупроводники и диэлектрики. |
Молекулярная | Ковалентная неполярная и полярная | Молекулы | Неметаллы, оксиды, кислоты и др. Разнообразны по агрегатному состоянию и другим свойствам. Легко переходят из одного агрегатного состояния в другое. Летучи, легкоплавки. |
Ионная | Ионная | Ионы | Соли, щелочи и др. Твердые вещества с высокими температурами плавления. Малолетучи. Хорошо растворяются в полярных растворителях. |
Металлическая | Металлическая | Атомы и катионы металла | Металлы. Твердые вещества (кроме ртути) с металлическим блеском. Ковки, пластичны. Обладают тепловой и электрической проводимостью. |
В настоящее время известен не один десяток миллионов разнообразных веществ. При этом все они образованы значительно меньшим числом химических элементов (современной науке достоверно известно 112 химических элементов).
Как объяснить такое разнообразие веществ?
Что такое аллотропия?
Приведите примеры аллотропных модификаций известных вам химических элементов. Дайте сравнительную характеристику их свойств.
Явление аллотропии характерно для большинства неметаллов и многих металлов. При этом образуемые ими аллотропные модификации могут различаться по составу, строению и типу кристаллических решеток.
Между аллотропными модификациями одного элементы возможны взаимные переходы. При этом все они имеют разную устойчивость. Как правило, при одних и тех же условиях более стабильна лишь одна из модификаций, обладающая минимальным запасом энергии. Остальные модификации при этих же условиях будут неустойчивы и рано или поздно перейдут в более устойчивую форму.
Что такое изомерия?
Изомерия – это явление, при котором существуют вещества, имеющие одинаковый состав, но разное химическое строение, а потому и свойства. Вещества, имеющие одинаковый состав, но разное химическое строение, а потому и разные свойства, называются изомерами.
Приведите примеры известных вам изомеров. Укажите, в чем заключаются различия их строения и свойств.
Явление изомерии характерно и для неорганических, и для органических веществ. Однако особенно ярко оно проявляется среди органических соединений, являясь важнейшей причиной их многообразия.
Таблица Изомерия органических соединений
Виды изомерии органических соединений | |||||
Структурная изомерия | |||||
Углеродного скелета | Положения функциональных групп | Положения кратных связей | Межклассовая | ||
Пространственная изомерия | |||||
Конформационная | Геометрическая | Оптическая | |||
Проиллюстрируйте указанные в таблице виды изомерии примерами.
Выводы:
- Молекулы — это очередной после атомов качественный уровень строения и эволюции вещества.
- Вещества имеют разный состав и строение.
- Свойства веществ определяются их строением: характером связей, типом кристаллической решетки, пространственным расположением, порядком соединения атомов.
- Зная строение вещества можно прогнозировать его свойства.
Примеры и разбор решения заданий тренировочного модуля:
Задание 1. Вещество, в узлах кристаллической решетки которого находятся ионы, это…
Тип вариантов ответов: (Текстовые, Графические, Комбинированные).
а) CaС12;
б) NH3;
в) I2;
г) C (графит).
Правильный вариант/варианты (или правильные комбинации вариантов): а
Подсказка: В узлах ионных решеток располагаются, чередуясь, положительно и отрицательно заряженные ионы. К соединениям с ионной связью, образующим ионные решетки, относится большинство солей и небольшое число оксидов.
Задание 2. Соедините попарно прямоугольники с овалами так, чтобы каждому типу гибридизации атомных орбиталей углерода соответствовал пример молекулы.
|
Правильный вариант:
Подсказка: Тип гибридизации атомных орбиталей углерода определяется числом заместителей при этом атоме углерода:
|
Состав и строение веществ
Состав веществ
Все вещества состоят из атомов.
Пример. Вода состоит из атомов водорода и кислорода в отношении 2:1. Графит и алмаз состоят из атомов углерода.
Атомы могут входить в состав веществ в незаряженном состоянии или в виде заряженных атомов (ионов).
Пример. Атомы аргона входят в состав аргона незаряженными, а атомы хлора и натрия в составе поваренной соли образуют ионы.
В состав многих веществ входят (и имеют очень важное значение для их свойств) свободные электроны.
Пример. В составе металлов электроны являются носителями заряда, а в составе особых ионных соединений (они называются электриды) электроны играют роль отрицательных ионов.
Строение веществ
В некоторых веществах соседние атомы объединены друг с другом в частицы, называемые молекулами. Связи между атомами в одной и той же молекуле гораздо прочнее, чем связи между атомами, входящими в соседние молекулы, поэтому молекулы способны к самостоятельному существованию при переходе вещества в различные агрегатные состояния и в растворах.
Пример. Вода, лёд, водяной пар состоят из молекул, а в графите, алмазе, аргоне молекул нет.
Все вещества состоят из атомов, но по своему строению все вещества делятся на вещества молекулярного и немолекулярного строения.
Общее название частиц, участвующих в строении вещества – структурные частицы. К структурным частицам относятся: молекулы, атомы, ионы, электроны.
Вещества молекулярного строения называются молекулярными веществами, а немолекулярного – немолекулярными веществами.
Молекулярные вещества – это вещества, мельчайшими структурными частицами которых являются молекулы.
Пример. Вода, кислород, водород, сахар – молекулярные вещества.
Немолекулярные вещества – это вещества, мельчайшими структурными частицами которых являются атомы, ионы, электроны.
Пример: поваренная соль, перманганат калия (марганцовка) – немолекулярные вещества (состоят из ионов). Алмаз, аргон – немолекулярные вещества (состоят из атомов). Алюминий, медь – немолекулярные вещества (металлы) – состоят из положительных ионов и свободных электронов.
Строение веществ в виде схемы:



















