Молекула ☑️ определение в химии и физике, строение и размеры, виды химической связи, свойства, структура и формы молекул для разных веществ
Одним из основополагающих понятий современной науки является понятие молекулы. Его введение европейскими учеными в 1860 г. дало толчок к развитию не только химии и физики, но и других естественных наук.
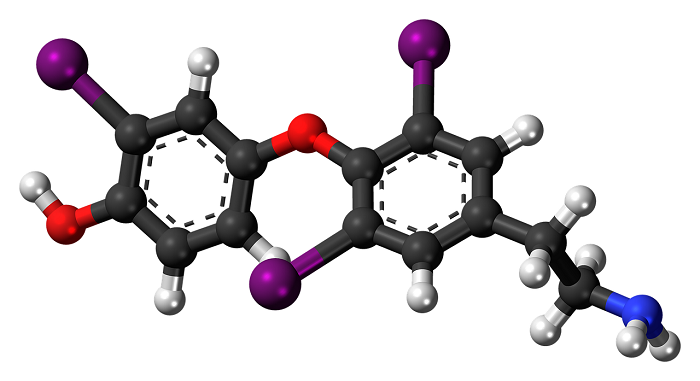
Молекулой, в наиболее общем определении, называется частица, образованная из нескольких (двух или более) атомов, объединенных между собой ковалентными связями. Она не имеет электрического заряда, все электроны в её составе имеют пару.
Молекулы, несущие заряд, называются ионами, неспаренные электроны – радикалами. Качественный и количественный состав их стабилен. Количество ядер атомов, электронов и их взаимное расположение позволяют отличать молекулы разных веществ друг от друга.
Что такое молекула в физике
В физике этим понятием оперируют при изучении свойств разных сред (газы, жидкости) и твердых тел.

Также их свойствами объясняются явления диффузии, теплопроводности и вязкость веществ.
Что такое молекула в химии
Учение о молекулах для химической науки является одним из самых главных. Именно химические исследования дали важнейшие сведения о составе и свойствах этой мельчайшей единицы вещества.
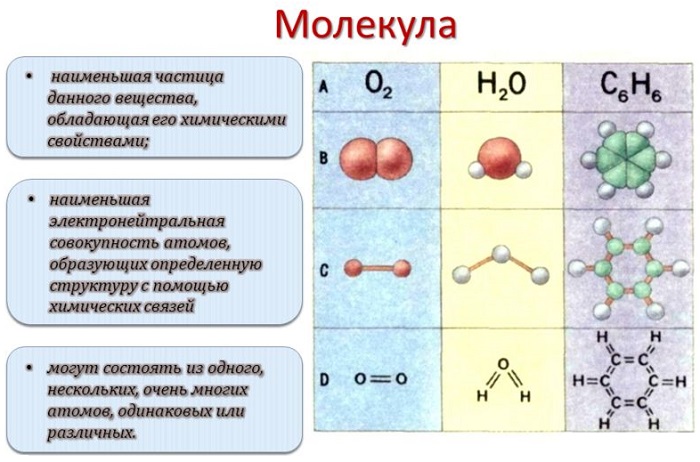
При прохождении химического превращения молекулы обмениваются атомами, распадаются. Поэтому знания о строении и состоянии этих частиц лежат в основе изучения химии веществ и их превращений.
На основании знаний о проходящей химической реакции можно предсказать строение молекул веществ, в ней участвующих. Противоположное заключение тоже будет верным: на основании сведений о строении молекулы вещества реально предсказать его поведение во время химической реакции.
Строение молекулы
Понятие о строении включает геометрическую структуру и распределение электронной плотности.
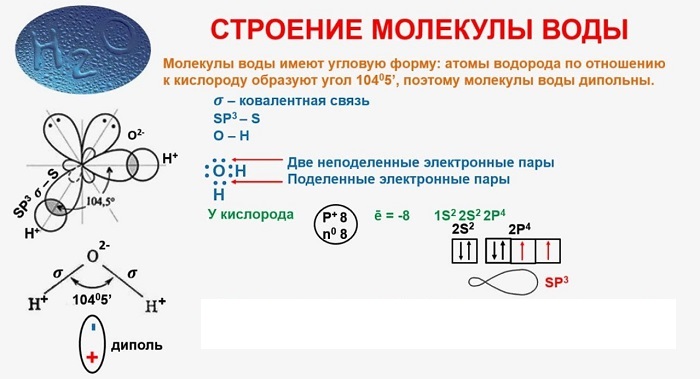
Существует несколько способов взаимодействия атомов. Основным способом являются химические связи, благодаря им поддерживается стабильное существование молекул. Прочие (неосновные) взаимодействия происходят между теми атомами, которые не связаны непосредственно.
Виды химической связи:
-
Металлическая — ядра атомов металлов, расположенные в узлах кристаллических решёток, объединены общим облаком электронов.
-
Водородная — основана на способности атома водорода образовывать дополнительную связь при смещении от него электронной плотности.
-
Ионная — имеет электрическую природу. Сильно поляризована. Возникает при притяжении ионов, несущих противоположный заряд.
-
Ковалентная — может быть полярной и неполярной. Образуется за счет пары электронов, совместно принадлежащей двум атомам. Отличается наибольшей устойчивостью и энергетической емкостью.
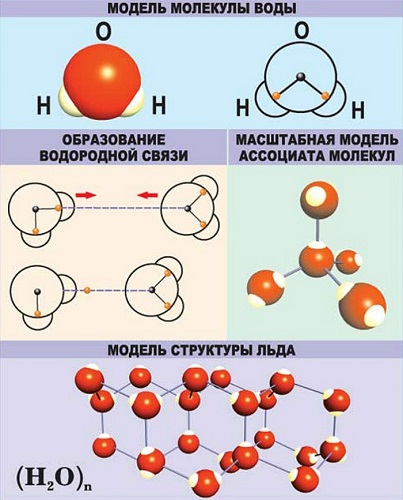
Связи характеризуются следующими показателями:
-
длина – степень удаления друг от друга ядер атомов, образовавших связь;
-
энергия – сила, прилагаемая для разрушения связи;
-
полярность – смещение электронного облака к одному из атомов;
-
порядок или кратность – количество пар электронов, образовавших связь.
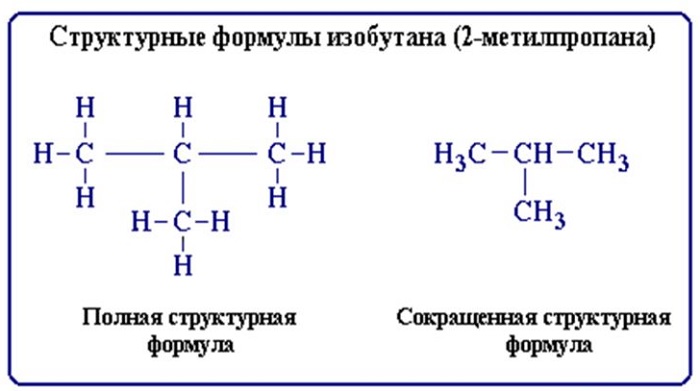
Строение молекул условно отражается структурными формулами. Основные взаимодействия атомов, при составлении таких формул, отображается черточками. В таких формулах связи образуют неразрывную цепь и иллюстрируют валентности образовавших их элементов (атомов).
Структурные формулы также отражают то, как выглядит молекула (линейная, циклическая, наличие радикалов и т. д.).
Строение частицы вещества активно изучается. Для этого используют различные экспериментальные и теоретические методы. К экспериментальным относят рентгеновский структурный анализ, спектроскопия, массспектрометрия и др. К теоретическим — расчётные методы квантовой химии.
Масса (размер) молекулы
В зависимости о количества ядер атомов, входящих в их состав, можно выделить молекулы двухатомные, трехатомные и т. д.

В том случае, если количество атомов велико, молекула носит название макромолекулы.
Путем сложения масс атомов, входящих в состав частицы, можно определить молекулярную массу. В зависимости от её величины, все вещества делят на высоко- и низкомолекулярные.
Свойства молекулы

Современная наука выделяет следующие свойства молекул:
-
Электрические — этими свойствами определяется то, как ведет себя вещество в электрическом поле. Атомы, входящие в состав молекулы, состоят, в свою очередь, из положительно заряженного ядра и электронов, несущих отрицательный заряд. Эти заряды внутри самой молекулы располагаются неравномерно, в связи с этим возникает так называемый дипольный момент и смещение электронной плотности в сторону одного из атомов.
-
Оптические — дают характеристику того, как ведет себя вещество в поле световой волны. К оптическим свойствам относят способность поляризовать свет, преломлять его и рассеивать.
-
Магнитные — объясняются распределением электронов в атомах.
Различают вещества:
Знания о свойствах и строении молекул являются основополагающими для развития теоретических и прикладных наук и играют важную роль в жизни человека.
Как устроены атомы и молекулы?
Как уже указывалось выше, молекулы состоят из атомов. Сколько же имеется атомов различных видов, или, как их называют, химических элементов.
В настоящее время известны 102 элемента, которые заполняют клетки периодической системы элементов Д. И. Менделеева.
Все разнообразные вещества, которые мы видим в окружающем мире, образованы в результате соединения друг с другом в различных комбинациях этих химических элементов (атомов).
Для удобства написания химического состава различных веществ и их химического взаимодействия между собой в химии приняты условные обозначения каждого элемента, которые образованы из начальных букв латинских названий этих элементов.
Латинский язык, который был первоначально разговорным языком древнего Рима, а затем и всей Римской империи, впоследствии, после распада Римской империи, в средние века продолжал употребляться учеными, а в некоторых науках он сохранился и до настоящего времени.
Так, в медицине пользуются латинским языком для названий болезней и лекарств, в ботанике — для названий растений.
При знакомстве с вопросами обработки воды наиболее часто встречаются следующие одиннадцать химических элементов:
Название элемента | Химическое обозначение | Читается |
Алюминий | А1 | алюминий |
Водород | Н | аш |
Железо | Fе | феррум |
Кальций | Са | кальций |
Кислород | О | о |
Кремний | Si | СИ |
Магний | Mg | магний |
Натрий | Nа | натрии |
Сера | s | ЭС |
Углерод | с | це |
Хлор | C1 | хлор |
С помощью этих условных обозначений (символов) химических элементов можно изображать молекулы любых веществ, а также различные химические процессы.
Цифра, стоящая справа внизу символа, указывает количество атомов в молекуле. Так, например, химическая реакция горения топлива в паровом котле может быть обозначена следующим образом:
С + О2 = СО2
углерод кислород углекислый газ, и читается так: це плюс о два равно це о два.
Первоначальные предположения ученых об атоме как о неделимой мельчайшей частице материи оказались неверными. В настоящее время физиками открыты еще более мелкие элементарные частички, из которых построены все атомы. Таких основных частиц имеется три: протоны, нейтроны и электроны.
По исследованиям последних десятилетий, помимо этих основных частиц открыто еще много различных мельчайших частиц (позитрон, фотон, нейтрино, мезоны и др.), возникающие при радиоактивных распадах и превращениях материи.
Как же построен атом из этих частиц? В центре каждого атома находится его ядро, состоящее из протонов и нейтронов. Вокруг ядра вращаются на различных расстояниях от него (орбитах) электроны, являющиеся самыми легкими из этих трех видов частиц.
Вес электрона равен 10-27 г. Протон и нейтрон имеют почти одинаковый вес, примерно в 1850 раз тяжелей электрона. Размеры протонов, нейтронов и электронов выражаются стотысячными долями ангстрема.
Размер же внешней орбиты вращающихся электронов, что и является по существу размером атома в целом, колеблется от 1 до 4 А. Следовательно, большая часть объема атома является пустой, не заполненной материей.
Но мы не видим не только атомов, но и молекул, и поэтому окружающие нас тела кажутся нам построенными из сплошной материи.
Основная масса атома сосредоточена в ядре. Если бы мы могли наполнить 1 см3 протонами и нейтронами так же плотно, как они находятся в ядрах атомов, то вес такого кубика был бы равен приблизительно весу высочайшей горы Кавказа Эльбрус. Такую плотность имеет материя в недрах некоторых звезд.
Протон и электрон имеют противоположные, но равные по величине электрические заряды: у протона — положительный заряд, у электрона — отрицательный. Нейтроны не имеют электрического заряда.
Так как атом в целом нейтрален, то количество вращающихся вокруг его ядра электронов равно количеству протонов в этом ядре. Таким образом, все известные нам различные химические элементы отличаются друг от друга количеством находящихся в их ядрах положительно заряженных протонов и соответственно равным количеством вращающихся вокруг них на разных орбитах электронов.
На рис. 3 изображены упрощенные схемы строения атомов некоторых элементов.
Рис. 3. Упрощенные схемы строения некоторых атомов: 1 — водород; 2 — кислород; 3 — натрий; 4 — хлор.
Атом водорода имеет один электрон, и соответственно этому в его ядре находится один протон. В ядре атома кислорода находятся восемь протонов, и окружают его восемь электронов, из которых два электрона вращаются по внутренней первой орбите, а шесть электронов — по наружной второй орбите.
У натрия, имеющего в ядре 11 протонов и столько же электронов, последние распределены по трем орбитам: первая — два электрона (так же, как у атома кислорода), вторая — восемь электронов и третья, наружная, — один электрон.
У атома хлора с 17 протонами в ядре имеется: два электрона в первой орбите, восемь электронов на второй орбите (столько же, сколько у кислорода и натрия) и семь электронов на третьей орбите.
Установлено, что на каждой орбите может разместиться только определенное предельное количество электронов. Первая орбита, непосредственно окружающая ядро, может вместить только два электрона, вторая — восемь, третья — восемнадцать, четвертая — тридцать два, пятая — восемнадцать и т. д.
При этом каждая следующая орбита может иметь электрон только при условии, что все предыдущие орбиты максимально заполнены. Обнаружено, что все химические свойства элементов определяются расположением его электронов и в первую очередь электронами, находящимися на наружной орбите.
Эта зависимость была гениально предугадана великим русским ученым Менделеевым в его периодической системе элементов, в которой порядковый номер положения элемента указывает число электронов в атоме, а в одном и том же столбце таблицы находятся атомы с одинаковым числом электронов во внешней орбите.
Поскольку основная масса атома сосредоточена в ядре, то и вес его приблизительно определяется весом ядра, состоящим из протонов и нейтронов. Вес нейтронов незначительно отличается от веса протонов.
Количество нейтронов в ядре атома равно числу протонов или несколько превышает его. Таким образом, вес атома определяется общим числом протонов и нейтронов в ядре и называется поэтому массовым числом атома.
В настоящее время определены абсолютные веса различных атомов, они выражаются чрезвычайно малыми величинами. Так, например, если взять даже самый тяжелый атом — урана, то его вес равен всего 0,4Х10-21 г.
Конечно, иметь дело с такими величинами при расчетах весьма неудобно. Поэтому в химии принята специальная условная мера веса атомов, равная весу самого легкого из них — атома водорода, вес которого принят равным 1,0 и тогда веса всех остальных атомов показывают, во сколько раз они тяжелее атома водорода.
В настоящее время за единицу атомных весов принимается 1/16 атомного веса кислорода, что удобнее, так как при этом атомные веса многих элементов становятся близкими целым числам. Но тогда атомный вес самого водорода оказывается равным 1,008; для грубых подсчетов он может быть приравнен 1,0.
Молекулы — урок. Химия, 8–9 класс.
Молекулы характеризуются качественным и количественным составом.
Качественный состав показывает, из каких атомов состоит молекула.
Пример:
молекулы воды и пероксида водорода состоят из атомов водорода и кислорода, а молекула углекислого газа — из атомов углерода и кислорода.
Количественный состав показывает, сколько атомов каждого вида содержится в молекуле.
Пример:
молекула воды состоит из двух атомов водорода и одного атома кислорода, а молекула пероксида водорода — из двух атомов водорода и двух атомов кислорода.
В молекулах может быть разное число атомов.
У инертных газов гелия, неона, аргона, криптона, ксенона, радона молекулы одноатомные.
Молекулы кислорода, водорода, азота, хлора, брома, иода двухатомные.
Молекула озона состоит из \(3\) атомов, а серы — из \(8\).
Молекула этилового спирта содержит \(2\) атома углерода, \(6\) атомов водорода и \(1\) атом кислорода, а молекула сахара — \(12\) атомов углерода, \(22\) атома водорода и \(11\) атомов кислорода.
Модели молекул: \(1\) — азота, \(2\) — кислорода,
\(3\) — неона, \(4\) — углекислого газа, \(5\) — воды,
\(6\) — озона, \(7\) — терпинеола
Химические свойства молекулы определяются тем, сколько и каких атомов в ней содержится, а также в каком порядке они соединены друг с другом.
Пример:
молекулы кислорода и озона отличаются только количественным составом. Кислород — газ без запаха. Необходим живым организмам для дыхания. Озон имеет запах, может вызывать отравление.
В химических реакциях молекулы не сохраняются, а разрушаются до атомов.
Что такое молекула. Понятие молекулы, ее свойства и состав. В данной статье дано разъяснение тому, что такое молекула. Также описано ее строение.
Все вещества в природе состоят из очень маленьких частиц, называемых молекулами. Эти частички в веществе постоянно взаимодействуют между собой. Невооруженным взглядом нельзя их увидеть. Понятие, основные свойства и характеристики молекул мы и рассмотрим в статье.
1
Молекулами называются частицы, имеющие нейтральный электрический заряд и состоящие из различного количества атомов. Число их, как правило, всегда больше двух, и связаны эти атомы между собой ковалентной связью. Впервые о существовании молекул стало известно во Франции. За это нужно отдать должное физику Жану Перрену, который и совершил это великое открытие в 1906 году.

2
Состав молекулы постоянен. Она не меняет его на протяжении всего своего существования. Строение этой маленькой частички зависит от того, какими физическими свойствами обладает образуемое ею вещество.

3
Каждая молекула индивидуальна тем, что атомы в ее составе наделены различными химическими взаимодействиями и конфигурациями, характерными для конкретного вещества. Связываются атомы валентно и невалентно. Благодаря валентности связей, частица обеспечивается базовыми характеристиками и постоянством. Невалентность связей оказывает большое влияние на характеристики молекул. Происходит это благодаря свойству вещества, состоящему из них.

4
Кроме того, в молекуле существуют двухцетровые связи и многоцентровые. Из последних наиболее распространены трех- и четырехцентровые.

5
Молекулы, по сути, являются подвижными системами, в них атомы вращаются вокруг ядра конфигурации, прибывающего в состоянии равновесия. А сами молекулы движутся хаотично. Если расстояние между ними большое, то они друг к другу притягиваются, а если интервал маленький, то тогда одна молекула отталкивает от себя другую.

6
В состав молекул входят частицы, называемые атомами. То, как они располагаются в этой частице, можно зафиксировать определенной структурной формулой. Передается молекулярный состав формулой брутто. К примеру, Н2О – это формула воды. Молекула этого вещества содержит в себе 2 атома водорода и 1 атом кислорода. O2 – это кислород, Н2CO3 – это угольная кислота. Встречаются и такие типы молекул, преобладание атомов в которых вычисляется ни единицами, ни десятками и даже ни сотнями, а тысячами. Эта особенность свойственна белковым частицам.

7
Изучением молекул в веществе занимается квантовая химия, теория о строении молекул. В ходе реакций, проводимых химиками между веществами, получаются сведения о строении и особенностях молекул. Не обходится здесь и без открытий в области квантовой физики, которые благотворно используются при исследовании этих частиц в науке.

8
При определении, из чего же состоит молекула, учеными применяются методики дифракционного типа. К ним относятся методики рентгеновского структурного исследования и нейтроновой дифракции. Это прямые формы методов. Также предполагается изучение молекул и другими научными способами.

Надеемся, что из этой статьи вы получили для себя много полезной и интересной информации о молекулах. Теперь вы точно знаете, что это за частица, и имеете представление о ее составе, основных свойствах и способах исследования молекул учеными в области химии.
Вещество, атом, молекула
Согласно современным представлениям основные положения атомно-молекулярной теории сводятся к следующим тезисам:
- Частицы веществ непрерывно движутся.
- Между частицами вещества действуют силы взаимного притяжения и отталкивания.
- Между составляющими частицами вещества существуют расстояния, размер которых зависит от агрегатного состояния.
- Молекулы состоят из атомов.
- Молекулы сохраняются при физических явлениях и разрушаются во время химических реакций.
- Атомы во время химических процессов остаются неделимыми, но перегруппировываются, в результате чего образуются новые соединения.
- Разнообразие веществ в природе обусловлена различными сочетаниями атомов, благодаря чему могут возникать вещества с молекулярным или немолекулярным строением.
Важнейшие понятия атомно-молекулярного учения
Согласно атомно-молекулярному учению, главными объектами химии являются атомы, молекулы, химические элементы, простые и сложные вещества.
Атом
Атомы — химически неделимые частицы, которые сохраняются при химических реакциях, но при этом частично может меняться строение электронной оболочки. Однако атомы разрушаются в процессе ядерных реакций.
Атом — это наименьшая, химически неделимая, электронейтральная частица элемента, которая состоит из положительно заряженного ядра и отрицательно заряженной электронной оболочки.
Атом — это система, состоящая из ядра и электронной оболочки. В состав атомного ядра, радиус которого в 10000 раз меньше (10-14 -10-15 м) радиуса атома (~ 10-10 м), входят ядерные частицы нуклоны.
Нуклоны — это положительно заряженные протоны и электронейтральные нейтроны. Электронная оболочка, размер которой определяет радиус всего атома — это совокупность электронов. Положительный заряд ядра определяется количеством протонов и равна по абсолютной величине отрицательному заряду электронной оболочки, который соответствует количеству электронов. Благодаря равенству по абсолютной величине зарядов протонов и электронов, атом электронейтрален. Протоны, нейтроны и электроны объединяются общим названием — субатомные частицы.
Массы протона и нейтрона практически одинаковы, а масса электрона в 1836 раз меньше, поэтому вся масса атома фактически сосредоточена в его ядре. По этой причине плотность вещества в ядре фантастически велика — порядка 1013 -1014 г / см3 . Массы атомов различных элементов колеблются от 1,67 · 10-27 кг (атом водорода) до 4,42 · 10-25 кг (атом мейтнерия — элемента № 109).
Количественными характеристиками атома является заряд ядра и относительная атомная масса Аr . Эти величины указываются в периодической системе элементов.
Заряд ядра атома равен порядковому номеру элемента (закон Мозли).
Поскольку массы атомов очень малы, в химии внедрена внесистемная единица измерения, называемая атомной единицей массы (а.е.м.) и равна одной двенадцатой массы атома изотопа углерода-12 (m (атома 12 С) = 19,92 · 10-27 кг):
Относительная атомная масса Аr — это физическая величина, равная отношению средней массы атома элемента к одной двенадцатой массы атома изотопа углерода-12:
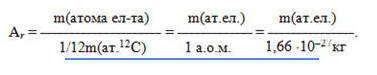
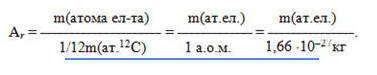
В системе измерений СИ Аr — безразмерная величина. Внесистемная единица измерения относительной атомной массы — а.е.м. Абсолютная масса атома равна произведению его относительной атомной массы на 1/12 массы атома углерода — 12 , например
m (ат.О) = А r (О) · 1,66 · 10— 27 = 16 · 1,66 · 10— 27 = 26,56 · 10— 27 кг.
Атом носителем химических свойств элемента . Вместе с этим у атомов одного элемента могут быть разные массы вследствие явления изотопии , при котором атомы одного элемента содержат одинаковое количество протонов в ядре, но разное количество нейтронов, что сказывается на их массе .
Молекула
Молекулы — это реально существующие природные объекты, что подтверждается многими экспериментально доказанными фактами.
Молекула — это наименьшая частица вещества, которая способна самостоятельно существовать и имеет все химические свойства вещества.
Как материальные частицы молекулы имеют размеры и массы. Размеры молекул колеблются в пределах 10-10 — 10-7 м. Масса отдельной молекулы чрезвычайно мала. Так, масса молекулы воды составляет 2,895×10-26 кг.
Молекула сохраняет химические свойства вещества. Известно, что вещество характеризуется определенными физическими и химическими свойствами. Физические свойства — это агрегатное состояние, плотность, температуры кипения и плавления, электропроводность, диэлектрическая проницаемость, цвет, запах, вкус и тому подобное. Понятно, что перечисленные свойства веществ могут быть присущи не одной молекуле, а достаточно большой их совокупности. Однако молекула имеет и собственные физические свойства: дипольный и магнитный моменты, способность к поляризации и тому подобное. А химические свойства вещества (способность вступать в химическое взаимодействие с другими веществами) в полной мере относятся и каждой отдельной молекуле.
Молекулы состоят из атомов, которые соединены между собой химическими связями в определенной последовательности и определенным образом ориентированы в пространстве. Количество атомов в молекуле колеблется от двух (Н2, О2, НСl) до нескольких тысяч (витамины, гормоны, белки). Атомы благородных газов (He, Ne, Ar, Kr, Xe, Rn) иногда называют одноатомными молекулами. Состав молекулы — важнейшая характеристика молекулы и вещества — описывается химическими формулами.
Схематическое модель молекулы Nh4Между молекулами есть расстояния, обусловленные агрегатным состоянием вещества: в газах они составляют 10-8 — 10-7 м, в твердых телах — примерно 10-10 м.
При физических явлениях молекулы сохраняются, а при химических превращениях — разрушаются, образуя новые вещества.
Количественной характеристикой молекулы является относительная молекулярная масса Мr .
Относительная молекулярная масса Мr— это отношение средней массы молекулы вещества к 1/12 массы атома углерода-12.
В системе СИ относительная молекулярная масса Mr — безразмерная величина, а внесистемной единицей ее измерения является а.е.м.
Относительная молекулярная масса Мr равна сумме относительных атомных масс Аr элементов, входящих в состав молекулы, с учетом количества атомов каждого элемента , например:
M r (SO 2 ) = A r (S) + 2 A r (O) = 32 + 2 · 16 = 64 а.е.м.
Абсолютная масса молекулы определяется как произведение Мr на атомную единицу массы:
m (молекулы SO 2 ) = M r (SO 2 ) · 1,66 · 10 — 27 = 64 · 1,66 · 10 — 27 = 1,06 · 10 — 25 кг.
Молекулярное строение имеют органические соединения и часть неорганических веществ, но большинство неорганических веществ состоит из ионов, в которых носителями химических свойств является условные частицы — ассоциаты ионов. Поэтому к веществам ионной строения невозможно применять понятие «молекула» так же как и к металлов и их сплавов, кристаллическая решетка которых имеет свои специфические особенности. Таким образом, с современной точки зрения молекула — это наименьшая электронейтральна замкнутая совокупность атомов, образует определенную структуру с помощью химических связей.
Химический элемент
Сейчас известно 118 химических элементов: из них 89 обнаружены в природе, а другие получены искусственно при проведении ядерных реакций.
Химический элемент — это вид атомов с одинаковым зарядом ядра.
Каждый элемент имеет свое название и символ. Названия элементов с порядковыми номерами 104-109 утверждены советом IUPAC (1997.) Позже были названы другие элементы. Теперь элемент №104 имеет следующие название и символ: Резерфорд Rf, №105 — Дубний Db, №106 — Сиборгий Sg, №107 — Борий Bh, элемент №108 — Хассий Hs, №109 — Мейтнерий Mt, №110 — Дармштадтий Ds. Химические элементы №№111-118 еще не получили официальных названий, поэтому их пока называют по порядковым номерам, например: №111 — Унунуний Uuu (один, один, один) №112 — Унунбий Uub (один, один, два) и т.д.
Химический символ означает, во-первых, название элемента, во-вторых, — один атом этого элемента при записях формул химических реакций.
Носителем свойств химических элементов является атом. Входя в состав различных веществ, атомы каждого элемента придают им определенных свойств. Так, вещества NaCl, Na2S, Na2O имеют некоторые общие свойства благодаря наличию иона Na+ , но также и различия за счет ионов Cl— , S2 , O2.
Основной количественной характеристикой элемента является заряд ядра его атомов Z , совпадающей с порядковым номером элемента. В природе отсутствуют различные химические элементы, которые должны одинаковый заряд ядра, поэтому можно однозначно определить элемент с зарядом ядра его атома. Относительная атомная масса Аr тоже в определенной степени может служить количественной характеристикой элемента, но не исчерпывающей, так как по величине Аr невозможно определить элемент. Существуют атомы различных элементов с одинаковыми Аr — так называемые изобары. С другой стороны, как уже упоминалось, существуют атомы одного и того же элемента с различными Аr — изотопы.
Формулы изотопов конечно записывают с помощью символа химического элемента, отметив заряд ядра (слева снизу) и массового числа (слева сверху). Исключением являются изотопы элемента водорода, для которых наряду с традиционной символикой допускаются и индивидуальные названия и обозначения.
Простые и сложные соединения
Поскольку вещество — это любая совокупность атомов или молекул, то по составу все соединения можно разделить на простые и сложные.
Простыми веществами называются вещества, которые состоят из атомов одного элемента; простые вещества — это форма существования химического элемента в свободном состоянии.
Насчитывается более 500 простых веществ, а элементов известно всего 118. Такое расхождение объясняется явлением под названием аллотропия.
Аллотропия — это способность элемента образовывать несколько простых, отличающихся по свойствам веществ, которые называются аллотропными модификациями, или алотропамы.
Простые вещества могут иметь молекулярное и немолекулярное строение — атомное или металлическое. Молекулярное строение присуще кислороду, галогенам; атомное — благородным газам, алмазу, графиту; металлическое — металлам в разном состоянии.
Сложными веществами называются вещества, содержащие атомы различных элементов, то есть это форма существования элементов в связанном состоянии.
Сложные вещества могут иметь как молекулярное строение (Н2S, CH4, HCl, H2O), так и немолекулярное: ионное (NaCl, Na2O, NaOH) или металлическое (Fe3C — карбид железа).
Химические реакции, их классификация
Химическими реакциями являются процессы, при которых изменяется состав соединений вследствие разрушения связей в одних веществах и образования новых соединений.
Химические реакции — это явления, при которых происходят превращения одних веществ в другие без изменения состава атомных ядер.
Для условного записи химических реакций применяют уравнения химических реакций, где в левой части указывают формулы исходных веществ, а в правой — конечных продуктов, образовавшихся в результате реакции Перед формулами всех веществ проставляют необходимые стехиометрические коэффициенты — числа, с помощью которых сравнивают количества атомов каждого элемента слева и справа.
Итак, уравнение химической реакции — условный запись, в которой с помощью химических формул соединений и стехиометрических коэффициентов отмечают состав и количество исходных веществ и продуктов реакции .
Химические реакции всегда сопровождаются физическими эффектами, которые подтверждают протекание реакции. Визуальными признаками химических реакций обычно является выделение газа, выпадение осадка, изменение окраски реакционной среды или тепловой эффект.
Для химических реакций, проходящих между неорганическими реагентами, чаще всего используются такие классификации:
- По признаку изменения количества и состава исходных веществ и конечных продуктов все реакции делятся на типы:
- реакции разложения, в которых из одного сложного вещества образуется несколько продуктов. В общем виде:
- реакции соединения , в которых из нескольких веществ относительно простого состава образуется одна сложное вещество:
- реакции замещения, в которых простое вещество замещает составную часть сложного вещества, в результате чего образуются другие простая и сложная вещества: A + B C→ A B + CA+BC→AB+C.
- реакции обмена, в которых молекулы сложных веществ обмениваются своими составными частями: A B + CD → A D + B CAB+CD→AD+BC.
- По признаку изменения валентных состояний атомов выделяют:
- окислительно-восстановительные реакции, при которых происходит изменение степеней окисления у атомов одного или нескольких исходных веществ. Этот тип реакций подробно будет рассматриваться позже, а здесь мы ограничимся только примером окислительно-восстановительной реакции с указанием степеней окисления:
- реакции невалентных преобразований, в процессе которых меняется только состав веществ, а электронные оболочки отдельных атомов остаются неизменными, а значит и степени окисления в атомах всех элементов не изменяются. Типичными случаями реакций невалентных преобразований являются реакции обмена, а также некоторые реакции соединения и разложения.
- В зависимости от направления течения реакции делятся на:
- оборотные, при которых протекание реакций происходит как в прямом, так и в обратном направлении. Следует помнить, что при записи оборотных реакций вместо знаков равенства или стрелочки (= или →→) Ставят две стрелки, направленные в противоположные стороны (↔↔ или ⇔⇔).
- необратимые, идущие в одном направлении до полного расходования хотя бы одного из реагентов. Как правило, необратимые реакции имеют одну из следующих признаков: а) продукты, получаемые, выходят из реакционной среды в виде осадка или газа; b) образуются малодиссоциированные соединения (то есть слабые электролиты: вода, слабая кислота или слабое основание) с) выделяется большое количество теплоты (горение, взрыв).
- По агрегатному или фазовым состоянием реакции делятся на следующие группы:
- гомогенные, при которых вещества, содержащиеся в системе, не отделяются друг от друга поверхностью раздела фаз;
- гетерогенные, характеризующихся наличием поверхности раздела фаз, то есть хоть одно соединение находится в другом агрегатном состоянии, чем остальные веществ.
- По характеру энергетического воздействия выделяют следующие реакции:
- термохимические, которые сопровождаются тепловым эффектом, то есть энергия подводится или отводится в форме теплоты. По знаку тепловых эффектов реакции делятся на следующие типы:
- экзотермические, сопровождающиеся выделением теплоты;
- эндотермические, при которых теплота поглощается;
- фотохимические, которые происходят под действием света сопровождаются излучением световой энергии
- электрохимические, протекающих под действием электрической энергии или сами являются источником электрического тока. Электрохимические реакции происходят в гальванических элементах, при электролизе и при коррозии металлов.
- термохимические, которые сопровождаются тепловым эффектом, то есть энергия подводится или отводится в форме теплоты. По знаку тепловых эффектов реакции делятся на следующие типы:
- В зависимости от природы реагирующих частиц реакции могут быть:
- молекулярными, при которых взаимодействие между веществами проходит результате столкновения отдельных молекул реагирующих веществ;
- ионными, протекающих при взаимодействии между ионами;
- радикальными, при которых одной из взаимодействующих частиц является радикал. Радикалы при записи обозначают с помощью точки рядом с формулой (∙∙).
- При наличии постороннего влияния на скорость реакции они делятся на:
- каталитические, протекающих в присутствии катализаторов — специальных веществ, которые ускоряют реакцию;
- некаталитические, в которых ускоряющий влияние катализатора отсутствует.
Одна и та же реакция в зависимости от признака рассматриваемого может классифицироваться по-разному. Например, синтез NH3 с N2 и H2 в присутствии железного катализатора является реакцией сообщения и одновременно относится к окислительно-восстановительным, гомогенным, молекулярным, каталитическим, термохимическим и оборотным реакциям.
Атом — Википедия
 Сравнительный размер атома гелия и его ядра
Сравнительный размер атома гелия и его ядраА́том (от др.-греч. ἄτομος «неделимый[1], неразрезаемый[2]») — частица вещества микроскопических размеров и массы, наименьшая часть химического элемента, являющаяся носителем его свойств[1][3].
Атомы состоят из ядра и электронов (точнее электронного «облака»). Ядро атома состоит из протонов и нейтронов. Количество нейтронов в ядре может быть разным: от нуля до нескольких десятков. Если число электронов совпадает с числом протонов в ядре, то атом в целом оказывается электрически нейтральным. В противном случае он обладает некоторым положительным или отрицательным зарядом и называется ионом[1]. В некоторых случаях под атомами понимают только электронейтральные системы, в которых заряд ядра равен суммарному заряду электронов, тем самым противопоставляя их электрически заряженным ионам[3][4].
Ядро, несущее почти всю (более чем 99,9 %) массу атома, состоит из положительно заряженных протонов и незаряженных нейтронов, связанных между собой при помощи сильного взаимодействия. Атомы классифицируются по количеству протонов и нейтронов в ядре: число протонов Z соответствует порядковому номеру атома в периодической системе Менделеева и определяет его принадлежность к некоторому химическому элементу, а число нейтронов N — определённому изотопу этого элемента. Единственный стабильный атом, не содержащий нейтронов в ядре — лёгкий водород (протий). Число Z также определяет суммарный положительный электрический заряд (Z×e) атомного ядра и число электронов в нейтральном атоме, задающее его размер[5].
Атомы различного вида в разных количествах, связанные межатомными связями, образуют молекулы.
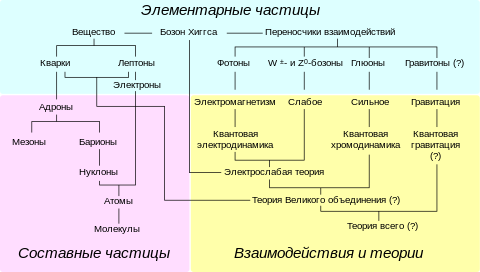
Понятие об атоме как о наименьшей неделимой части материи было впервые сформулировано древнеиндийскими и древнегреческими философами (см.: атомизм). В XVII и XVIII веках химикам удалось экспериментально подтвердить эту идею, показав, что некоторые вещества не могут быть подвергнуты дальнейшему расщеплению на составляющие элементы с помощью химических методов. Однако в конце XIX — начале XX века физиками были открыты субатомные частицы и составная структура атома, и стало ясно, что реальная частица, которой было присвоено имя атома, в действительности не является неделимой.
На международном съезде химиков в Карлсруэ (Германия) в 1860 году были приняты определения понятий молекулы и атома. Атом — наименьшая частица химического элемента, входящая в состав простых и сложных веществ.
- Кусочки материи. Демокрит полагал, что свойства того или иного вещества определяются формой, массой, и пр. характеристиками образующих его атомов. Так, скажем, у огня атомы остры, поэтому огонь способен обжигать, у твёрдых тел они шероховаты, поэтому накрепко сцепляются друг с другом, у воды — гладки, поэтому она способна течь. Даже душа человека, согласно Демокриту, состоит из атомов.[6]
- Модель атома Томсона 1904 г. (модель «Пудинг с изюмом»). Дж. Дж. Томсон предложил рассматривать атом как некоторое положительно заряженное тело с заключёнными внутри него электронами. Была окончательно опровергнута Резерфордом после проведённого им знаменитого опыта по рассеиванию альфа-частиц.
- Ранняя планетарная модель атома Нагаоки. В 1904 году японский физик Хантаро Нагаока предложил модель атома, построенную по аналогии с планетой Сатурн. В этой модели вокруг маленького положительного ядра по орбитам вращались электроны, объединённые в кольца. Модель оказалась ошибочной.
- Планетарная модель атома Бора-Резерфорда. В 1911 году[7] Эрнест Резерфорд, проделав ряд экспериментов, пришёл к выводу, что атом представляет собой подобие планетной системы, в которой электроны движутся по орбитам вокруг расположенного в центре атома тяжёлого положительно заряженного ядра («модель атома Резерфорда»). Однако такое описание атома вошло в противоречие с классической электродинамикой. Дело в том, что, согласно классической электродинамике, электрон при движении с центростремительным ускорением должен излучать электромагнитные волны, а, следовательно, терять энергию. Расчёты показывали, что время, за которое электрон в таком атоме упадёт на ядро, совершенно ничтожно. Для объяснения стабильности атомов Нильсу Бору пришлось ввести постулаты, которые сводились к тому, что электрон в атоме, находясь в некоторых специальных энергетических состояниях, не излучает энергию («модель атома Бора-Резерфорда»). Необходимость введения постулатов Бора была следствием осознания того, что для описания атома классическая механика неприменима. Дальнейшее изучение излучения атома привело к созданию квантовой механики, которая позволила объяснить подавляющее большинство наблюдаемых фактов.
Квантово-механическая модель атома[править | править код]
Современная модель атома является развитием планетарной модели Бора-Резерфорда. Согласно современной модели, ядро атома состоит из положительно заряженных протонов и не имеющих заряда нейтронов и окружено отрицательно заряженными электронами. Однако представления квантовой механики не позволяют считать, что электроны движутся вокруг ядра по сколько-нибудь определённым траекториям (неопределённость координаты электрона в атоме может быть сравнима с размерами самого атома).
Химические свойства атомов определяются конфигурацией электронной оболочки и описываются квантовой механикой. Положение атома в таблице Менделеева определяется электрическим зарядом его ядра (то есть количеством протонов), в то время как количество нейтронов принципиально не влияет на химические свойства; при этом нейтронов в ядре, как правило, больше, чем протонов (см.: атомное ядро). Если атом находится в нейтральном состоянии, то количество электронов в нём равно количеству протонов. Основная масса атома сосредоточена в ядре, а массовая доля электронов в общей массе атома незначительна (несколько сотых процента массы ядра).
Массу атома принято измерять в атомных единицах массы, равных 1⁄12 от массы атома стабильного изотопа углерода 12C.
Субатомные частицы[править | править код]
Хотя слово атом в первоначальном значении обозначало частицу, которая не делится на меньшие части, согласно научным представлениям он состоит из более мелких частиц, называемых субатомными частицами. Атом состоит из электронов, протонов, все атомы, кроме водорода-1, содержат также нейтроны.
Электрон является самой лёгкой из составляющих атом частиц с массой 9,11⋅10−31кг, отрицательным зарядом и размером, слишком малым для измерения современными методами.[8] Эксперименты по сверхточному определению магнитного момента электрона (Нобелевская премия 1989 года) показывают, что размеры электрона не превышают 10−18 м[9][10].
Протоны обладают положительным зарядом и в 1836 раз тяжелее электрона (1,6726⋅10−27 кг). Нейтроны не обладают электрическим зарядом и в 1839 раз тяжелее электрона (1,6749⋅10−27 кг).[11]
При этом масса ядра меньше суммы масс составляющих его протонов и нейтронов из-за явления дефекта массы. Нейтроны и протоны имеют сравнимый размер, около 2,5⋅10−15м, хотя размеры этих частиц определены плохо.[12]
В стандартной модели элементарных частиц как протоны, так и нейтроны состоят из элементарных частиц, называемых кварками. Наряду с лептонами, кварки являются одной из основных составляющих материи. И первые и вторые являются фермионами. Существует шесть типов кварков, каждый из которых имеет дробный электрический заряд, равный +2⁄3 или (−1⁄3) элементарного. Протоны состоят из двух u-кварков и одного d-кварка, а нейтрон — из одного u-кварка и двух d-кварков. Это различие объясняет разницу в массах и зарядах протона и нейтрона. Кварки связаны между собой сильными ядерными взаимодействиями, которые передаются глюонами.[13][14]
Электроны в атоме[править | править код]
При описании электронов в атоме в рамках квантовой механики обычно рассматривают распределение вероятности в 3n-мерном пространстве для системы n электронов.
Электроны в атоме притягиваются к ядру, между электронами также действует кулоновское взаимодействие. Эти же силы удерживают электроны внутри потенциального барьера, окружающего ядро. Для того чтобы электрон смог преодолеть притяжение ядра, ему необходимо получить энергию от внешнего источника. Чем ближе электрон находится к ядру, тем больше энергии для этого необходимо.
Электронам, как и другим частицам, свойственен корпускулярно-волновой дуализм. Иногда говорят, что электрон движется по орбитали, что неверно. Состояние электронов описывается волновой функцией, квадрат модуля которой характеризует плотность вероятности нахождения частиц в данной точке пространства в данный момент времени, или, в общем случае, оператором плотности. Существует дискретный набор атомных орбиталей, которым соответствуют стационарные чистые состояния электронов в атоме.
Каждой орбитали соответствует свой уровень энергии. Электрон в атоме может перейти на уровень с большей энергией при столкновении данного атома с другим атомом, электроном, ионом, или же поглотив фотон соответствующей энергии. При переходе на более низкий уровень электрон отдаёт энергию путём излучения фотона, либо путём передачи энергии другому электрону (безызлучательный переход, удары второго рода). Как и в случае поглощения, при излучательном переходе энергия фотона равна разности энергий электрона на этих уровнях (см.: постулаты Бора). Частота испускаемого излучения ν связана с энергией фотона E соотношением E = hν, где h — постоянная Планка.
По определению, любые два атома с одним и тем же числом протонов в их ядрах относятся к одному химическому элементу. Атомы с одним и тем же количеством протонов, но разным количеством нейтронов называют изотопами данного элемента. Например, атомы водорода всегда содержат один протон, но существуют изотопы без нейтронов (водород-1, иногда также называемый протием — наиболее распространённая форма), с одним нейтроном (дейтерий) и двумя нейтронами (тритий).[15] Известные элементы составляют непрерывный натуральный ряд по числу протонов в ядре, начиная с атома водорода с одним протоном и заканчивая атомом оганесона, в ядре которого 118 протонов.[16] Все изотопы элементов периодической системы, начиная с номера 83 (висмут), радиоактивны.[17][18]
Масса[править | править код]
Поскольку наибольший вклад в массу атома вносят протоны и нейтроны, суммарное число этих частиц называют массовым числом. Массу покоя атома часто выражают в атомных единицах массы (а. е. м.), которая также называется дальтоном (Да). Эта единица определяется как 1⁄12 часть массы покоя нейтрального атома углерода-12, которая приблизительно равна 1,66⋅10−24 г.[19]Водород-1 — наилегчайший изотоп водорода и атом с наименьшей массой, имеет атомный вес около 1,007825 а. е. м.[20] Масса атома приблизительно равна произведению массового числа на атомную единицу массы[21] Самый тяжёлый стабильный изотоп — свинец-208[17] с массой 207,9766521 а. е. м.[22]
Так как массы даже самых тяжёлых атомов в обычных единицах (например, в граммах) очень малы, то в химии для измерения этих масс используют моли. В одном моле любого вещества по определению содержится одно и то же число атомов (примерно 6,022⋅1023). Это число (число Авогадро) выбрано таким образом, что если масса элемента равна 1 а. е. м., то моль атомов этого элемента будет иметь массу 1 г. Например, углерод имеет массу 12 а. е. м., поэтому 1 моль углерода весит 12 г.[19]
Размер[править | править код]
Атомы не имеют отчётливо выраженной внешней границы, поэтому их размеры определяются по расстоянию между ядрами одинаковых атомов, которые образовали химическую связь (ковалентный радиус) или по расстоянию до самой дальней из стабильных орбит электронов в электронной оболочке этого атома (радиус атома). Радиус зависит от положения атома в периодической системе, вида химической связи, числа ближайших атомов (координационного числа) и квантово-механического свойства, известного как спин.[23] В периодической системе элементов размер атома увеличивается при движении сверху вниз по столбцу и уменьшается при движении по строке слева направо.[24] Соответственно, самый маленький атом — это атом гелия, имеющий радиус 32 пм, а самый большой — атом цезия (225 пм).[25] Эти размеры в тысячи раз меньше длины волны видимого света (400—700 нм), поэтому атомы нельзя увидеть в оптический микроскоп. Однако отдельные атомы можно наблюдать с помощью сканирующего туннельного микроскопа.
Малость атомов демонстрируют следующие примеры. Человеческий волос по толщине в миллион раз больше атома углерода.[26] Одна капля воды содержит 2 секстиллиона (2⋅1021) атомов кислорода, и в два раза больше атомов водорода.[27] Один карат алмаза с массой 0,2 г состоит из 10 секстиллионов атомов углерода.[28] Если бы яблоко можно было увеличить до размеров Земли, то атомы достигли бы исходных размеров яблока.[29]
Учёные из Харьковского физико-технического института представили первые в истории науки снимки атома. Для получения снимков учёные использовали электронный микроскоп, фиксирующий излучения и поля (field-emission electron microscope, FEEM). Физики последовательно разместили десятки атомов углерода в вакуумной камере и пропустили через них электрический разряд в 425 вольт. Излучение последнего атома в цепочке на фосфорный экран позволило получить изображение облака электронов вокруг ядра.[30]
Радиоактивный распад[править | править код]
Диаграмма времени полураспада (T½) в секундах для различных изотопов с Z протонами и N нейтронами.У каждого химического элемента есть один или более изотопов с нестабильными ядрами, которые подвержены радиоактивному распаду, в результате чего атомы испускают частицы или электромагнитное излучение. Радиоактивность возникает, когда радиус ядра больше радиуса действия сильных взаимодействий (расстояний порядка 1 фм[31]).
Существуют три основные формы радиоактивного распада[32][33]:
- Альфа-распад происходит, когда ядро испускает альфа-частицу — ядро атома гелия, состоящее из двух протонов и двух нейтронов. В результате испускания этой частицы возникает элемент с меньшим на два атомным номером.
- Бета-распад происходит из-за слабых взаимодействий, и в результате нейтрон распадается на протон, электрон и антинейтрино, во втором случае на протон, позитрон и нейтрино. Электрон и позитрон называют бета-частицами. Бета-распад увеличивает или уменьшает атомный номер на единицу. К бета-распаду относят и обратный процесс — электронный захват, когда один из протонов атомного ядра захватывает орбитальный электрон и превращается в нейтрон, испуская электронное нейтрино.
- Гамма-излучение происходит из-за перехода ядра в состояние с более низкой энергией с испусканием электромагнитного излучения. Гамма-излучение может происходить вслед за испусканием альфа- или бета-частицы после радиоактивного распада.
Каждый радиоактивный изотоп характеризуется периодом полураспада, то есть временем, за которое распадается половина ядер образца. Это экспоненциальный распад, который вдвое уменьшает количество оставшихся ядер за каждый период полураспада. Например, по прошествии двух периодов полураспада в образце останется только 25 % ядер исходного изотопа.[31]
Магнитный момент[править | править код]
Элементарные частицы обладают внутренним квантовомеханическим свойством, известным как спин. Оно аналогично угловому моменту объекта вращающегося вокруг собственного центра масс, хотя строго говоря, эти частицы являются точечными и нельзя говорить об их вращении. Спин измеряют в единицах приведённой планковской постоянной (ℏ{\displaystyle \hbar }), тогда электроны, протоны и нейтроны имеют спин, равный ½ ℏ{\displaystyle \hbar }. В атоме электроны обращаются вокруг ядра и обладают орбитальным угловым моментом помимо спина, в то время как ядро само по себе имеет угловой момент благодаря ядерному спину.[34]
Магнитное поле, создаваемое магнитным моментом атома, определяется этими различными формами углового момента, как и в классической физике вращающиеся заряженные объекты создают магнитное поле. Однако наиболее значительный вклад происходит от спина. Благодаря свойству электрона, как и всех фермионов, подчиняться правилу запрета Паули, по которому два электрона не могут находиться в одном и том же квантовом состоянии, связанные электроны спариваются друг с другом, и один из электронов находится в состоянии со спином вверх, а другой — с противоположной проекцией спина — в состоянии со спином вниз. Таким образом магнитные моменты электронов сокращаются, уменьшая полный магнитный дипольный момент системы до нуля в некоторых атомах с чётным числом электронов.[35]
В ферромагнитных элементах, таких как железо, нечётное число электронов приводит к появлению неспаренного электрона и к ненулевому полному магнитному моменту. Орбитали соседних атомов перекрываются, и наименьшее энергетическое состояние достигается, когда все спины неспаренных электронов принимают одну ориентацию, процесс известный как обменное взаимодействие. Когда магнитные моменты ферромагнитных атомов выравниваются, материал может создавать измеримое макроскопическое магнитное поле. Парамагнитные материалы состоят из атомов, магнитные моменты которых разориентированы в отсутствии магнитного поля, но магнитные моменты отдельных атомов выравниваются при приложении магнитного поля.[35][36]
Ядро атома тоже может обладать ненулевым полным спином. Обычно при термодинамическом равновесии спины ядер ориентированы случайным образом. Однако для некоторых элементов (таких как ксенон-129) возможно поляризовать значительную часть ядерных спинов для создания состояния с сонаправленными спинами —состояния называемого гиперполяризацией. Это состояние имеет важное прикладное значение в магнитно-резонансной томографии.[37][38]
Энергетические уровни[править | править код]
Электрон в атоме находится в связанном состоянии; находясь на возбуждённом уровне, он обладает потенциальной энергией, которая пропорциональна его расстоянию от ядра. Эта энергия обычно измеряется в электронвольтах (эВ), и максимальное её значение равно энергии, которую надо передать электрону, чтобы сделать его свободным (оторвать от атома). По мере перехода электрона (в атоме) на более низкие уровни потенциальная энергия уменьшается, но превращается не в кинетическую, а в энергию излучаемых фотонов. Согласно квантовомеханической модели атома связанный электрон может занимать только дискретный набор разрешённых энергетических уровней — состояний с определённой энергией. Наинизшее из разрешённых энергетических состояний называется основным (потенциальная энергия равна нулю — электрон глубже падать уже не может), а все остальные — возбуждёнными.[39]
Для перехода электрона с одного энергетического уровня на другой нужно передать ему или отнять у него энергию. Эту энергию можно сообщить атому путём удара другой частицей либо путём поглощения или, соответственно, испускания фотона, причём энергия этого фотона равна абсолютной величине разности энергий начального и конечного уровней электрона. Частота испускаемого излучения пропорциональна энергии фотона, поэтому переходы между разными энергетическими уровнями проявляются в различных областях электромагнитного спектра.[40] Каждый химический элемент имеет уникальный спектр испускания, который зависит от заряда ядра, заполнения электронных подоболочек, взаимодействия электронов, а также других факторов.[41]
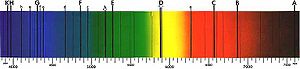 Пример линейного спектра поглощения
Пример линейного спектра поглощенияКогда излучение с непрерывным спектром проходит через вещество (например, газ или плазму), некоторые фотоны поглощаются атомами или ионами, вызывая электронные переходы между энергетическим состояниями, разность энергий которых равна энергии поглощённого фотона. Затем эти возбуждённые электроны спонтанно возвращаются на уровень, лежащий ниже по шкале энергии, снова испуская фотоны. Испущенные фотоны излучаются не в том направлении, в каком падал поглощённый, а произвольно в телесном угле 4 пи стерадиан. В результате в непрерывном спектре появляются участки с очень низким уровнем излучения, то есть темные линии поглощения. Таким образом, вещество ведёт себя как фильтр, превращая исходный непрерывный спектр в спектр поглощения, в котором имеются серии тёмных линий и полос. При наблюдении с тех углов, куда не направлено исходное излучение, можно заметить излучение с эмиссионным спектром, испускаемое атомами. Спектроскопические измерения энергии, амплитуды и ширины спектральных линий излучения позволяют определить вид излучающего вещества и физические условия в нём.[42]
Более детальный анализ спектральных линий показал, что некоторые из них обладают тонкой структурой, то есть расщеплены на несколько близких линий. В узком смысле «тонкой структурой» спектральных линий принято называть их расщепление, происходящее из-за спин-орбитального взаимодействия между спином и вращательным движением электрона.[43]
Взаимодействие магнитных моментов электрона и ядра приводит к сверхтонкому расщеплению спектральных линий, которое, как правило, меньше, чем тонкое.
Если поместить атом во внешнее магнитное поле, то также можно заметить расщепление спектральных линий на две, три и более компонент — это явление называется эффектом Зеемана. Он вызван взаимодействием внешнего магнитного поля с магнитным моментом атома, при этом в зависимости от взаимной ориентации момента атома и магнитного поля энергия данного уровня может увеличиться или уменьшиться. При переходе атома из одного расщеплённого состояния в другое будет излучаться фотон с частотой, отличной от частоты фотона при таком же переходе в отсутствие магнитного поля. Если спектральная линия при помещении атома в магнитное поле расщепляется на три линии, то такой эффект Зеемана называется нормальным (простым). Гораздо чаще в слабом магнитном поле наблюдается аномальный (сложный) эффект Зеемана, когда происходит расщепление на 2, 4 или более линий (аномальный эффект происходит из-за наличия спина у электронов). При увеличении магнитного поля вид расщепления упрощается, и аномальный эффект Зеемана переходит в нормальный (эффект Пашена — Бака).[44] Присутствие электрического поля также может вызвать сравнимый по величине сдвиг спектральных линий, вызванный изменением энергетических уровней. Это явление известно как эффект Штарка.[45]
Если электрон находится в возбуждённом состоянии, то взаимодействие с фотоном определённой энергии может вызвать вынужденное излучение дополнительного фотона с такой же энергией — для этого должен существовать более низкий уровень, на который возможен переход, и разность энергий уровней должна равняться энергии фотона. При вынужденном излучении эти два фотона будут двигаться в одном направлении и иметь одинаковую фазу. Это свойство используется в лазерах, которые могут испускать когерентный пучок света в узком диапазоне частот.[46]
Валентность[править | править код]
Внешняя электронная оболочка атома, если она не полностью заполнена, называется валентной оболочкой, а электроны этой оболочки называются валентными электронами. Число валентных электронов определяет то, как атом связывается с другими атомами посредством химической связи. Путём образования химических связей атомы стремятся заполнить свои внешние валентные оболочки.[47]
Чтобы показать повторяющиеся химические свойства химических элементов, их упорядочивают в виде периодической таблицы. Элементы с одинаковым числом валентных электронов формируют группу, которая изображается в таблице в виде столбца (движение по горизонтальному ряду соответствуют заполнению валентной оболочки электронами). Элементы, находящиеся в самом правом столбце таблицы, имеют полностью заполненную электронами внешнюю оболочку, поэтому они отличаются крайне низкой химической активностью и называются инертными или благородными газами.[48][49]
Дисперсионное притяжение[править | править код]
Важным свойством атома является его склонность к дисперсионному притяжению. Происхождение дисперсионных сил было объяснено в 1930 году Ф. Лондоном. Межатомное взаимодействие возникает вследствие флуктуаций заряда в двух атомах, находящихся близко друг от друга. Поскольку электроны движутся, каждый атом обладает мгновенным дипольным моментом, отличным от нуля. Если бы флуктуации электронной плотности в двух атомах были бы несогласованными, то не было бы результирующего притяжения между атомами. Однако мгновенный диполь на одном атоме наводит противоположно направленный диполь в соседнем атоме. Эти диполи притягиваются друг к другу за счёт возникновения силы притяжения, которая называется дисперсионной силой, или силой Лондона. Энергия такого взаимодействия прямо пропорциональна квадрату электронной поляризуемости атома α и обратно пропорциональна r6, где r — расстояние между двумя атомами.[50]
Деформационная поляризация атома[править | править код]
Деформационная поляризация проявляется в присущей атомам способности к упругой деформации их электронных оболочек под действием электромагнитных полей. Сегодняшнее понимание явления деформационной поляризации основано на представлениях о конечной упругости электронных оболочек атомов под действием электрического поля[51]. Снятие внешнего электрического поля приводит к восстановлению электронной оболочки атома.
Деформация электронной оболочки атома приводит к смещению электронной плотности в атоме, что сопровождается образованием наведённого электрического дипольного момента μ. Дипольный момент равен произведению величины положительного заряда q на расстояние между зарядами L и направлен от отрицательного заряда к положительному μ=qL. В относительно слабых электрических полях наведённый дипольный момент пропорционален напряжённости электрического поля E. μ =αeE, где αe — электронная поляризуемость атома. Наибольшее значение электронной поляризуемости наблюдается у атомов щелочных металлов, а минимальное у атомов благородных газов.
Ионизация атома[править | править код]
При высоких значениях напряжённости приложенного электрического поля наблюдается необратимая деформация атома, сопровождающаяся отрывом электрона.
Происходит ионизация атома, атом отдаёт электрон и превращается в положительно заряженный ион — катион. Отрыв электрона от атома требует затраты энергии, называемой потенциалом ионизации или энергией ионизации.
Энергия ионизации атома сильно зависит от его электронной конфигурации. Изменение энергии отрыва первого электрона в зависимости от порядкового номера элемента приведено на рисунке.
Наименьшей энергией ионизации обладают атомы щелочных металлов, наибольшей — атомы благородных газов.
Для многоэлектронных атомов энергия ионизации I1, I2, I3… соответствует отрыву первого, второго, третьего и т. д. электронов.
Взаимодействие атома с электроном[править | править код]
Атомы могут, в той или иной степени, присоединять добавочный электрон и превращаться в отрицательный ион — анион.
Энергетический эффект процесса присоединения к нейтральному атому (Э) принято называть энергией сродства к электрону. Э + e— → Э—
На рисунке представлена зависимость энергии сродства к электрону атомов от порядкового номера элемента. Наибольшим сродством к электрону обладают атомы галогенов (3-4 эВ):
| Атом | Энергия сродства к электрону, эВ[52] |
|---|---|
| F | 3,62 ± 0,09 |
| Cl | 3,82 ± 0,06 |
| Br | 3,54 ± 0,06 |
| I | 3,23 ± 0,06 |
Электроотрицательность атома (χ) — фундаментальное свойство атома смещать к себе общие электронные пары в молекуле. Способность атома данного элемента к оттягиванию на себя электронной плотности по сравнению с другими элементами соединения зависит от энергии ионизации атома и его сродства к электрону. Согласно одному из определений (по Малликену) электроотрицательность атома (χ) может быть выражена как полусумма его энергии ионизации (i) и сродства к электрону (F):
- χ=12(i+F){\displaystyle \chi ={\frac {1}{2}}(i+F)}
Имеется около двадцати шкал электроотрицательности атома, в основу расчёта значений которых положены различные свойства веществ. Полученные значения разных шкал отличаются, но относительное расположение элементов в ряду электроотрицательностей примерно одинаково.
Детальный поиск взаимосвязи между шкалами электроотрицательности позволил сформулировать новый подход к выбору практической шкалы электроотрицательностей атомов[53].
Одноатомная молекула — Википедия
Материал из Википедии — свободной энциклопедии
Одноатомная молекула — физическая абстракция, молекула, состоящая из одного атома, характеризующаяся тремя степенями свободы (i=3) и обладающая только упругими свойствами. Использовалась при разработке молекулярно-кинетической теории (сокращённо — МКТ) в середине XIX века. Вошла в основное уравнение МКТ:
E=i2kT{\displaystyle E={\frac {i}{2}}kT}
где E{\displaystyle E} — средняя кинетическая энергия молекул, k{\displaystyle k} — постоянная Больцмана; T{\displaystyle T} — абсолютная температура. Двухатомная молекула имеет 5 степеней свободы (i=5).
Термины «МКТ» и «одноатомная молекула» встречаются в учебниках по курсу общей физики. Термин «одноатомная молекула» используется в современной литературе[1], но вскользь, без расшифровки понятия. Это позволяет понять указанный термин в буквальном смысле: одноатомная молекула — это молекула, состоящая из одного атома, т.е атом, рассматриваемый как молекула. Тем не менее некоторые авторы утверждают, что причисление к молекулам одноатомных молекул, то есть свободных атомов, например, инертных газов, приводит к совмещению понятий «молекула» и «атом»[2], к игнорированию основного положения атомно-молекулярного учения — при взаимодействии атомов образуются молекулы — и не согласуется с определением молекулы, данным ИЮПАК[3].

