Ученые разработали эффективные фотокатализаторы для выделения кислорода из воды
10 августа, 2022 13:02
Источник: Атомная энергия
Группа ученых из Института катализа СО РАН (ИК СО РАН) и Института неорганической химии СО РАН (ИНХ СО РАН) при поддержке Российского научного фонда разработали активный и стабильный фотокатализатор окисления воды на основе оксидов иридия, который позволяет ускорить выделение кислорода из воды. Результаты опубликованы в высокорейтинговом журнале ACS Applied Materials & Interfaces (IF = 10,383).
Фотокаталитическое разложение воды с образованием водорода и кислорода – актуальная задача получения «зелёного» водорода, экологически чистого топлива.
«Нам удалось синтезировать стабильный комплекс иридия с нитро- и аква-лигандами, который далее мы использовали для получения композитных фотокатализаторов. Уникальность данного соединения заключается в отсутствии в его составе ионов хлора, которые могут снижать активность катализаторов. Кроме того, из данного соединения легко образуется активная форма иридия – достаточно нагревания при невысокой температуре», — рассказал старший научный сотрудник ИНХ СО РАН, кандидат химических наук Данила Васильченко.
По словам руководителя проекта, заместителя руководителя Центра НТИ «Водород как основа низкоуглеродной экономики» ИК СО РАН, доктора химических наук, профессора РАН Екатерины Козловой, проведенная работа продолжает сделанные ранее исследования, общая цель которых – разработка катализаторов полного разложения воды.
«Ранее мы уже получили высокоактивные фотокатализаторы на основе графитоподобного нитрида углерода с нанесенной платиной для выделения водорода. Исследование процесса образования кислорода является продолжением работы, конечная цель которой заключается в разработке катализаторов полного фотокаталитического разложения воды на водород и кислород. В данной работе были получены не только активные, но и стабильные фотокатализаторы получения кислорода с малым содержанием иридия – всего 0,25 %. Еще одно важное преимущество наших фотокатализаторов состоит в способности работать под действием видимого излучения, что открывает перспективы использования энергии солнца для разложения воды», — пояснила Екатерина Козлова.
Уникальность полученного фотокатализатора для выделения кислорода также в его гетерогенности. Обычно катализаторы для выделения кислорода гомогенные, что затрудняет процесс отделения катализатора от реакционной смеси.
Один из авторов статьи, студент НГУ, сотрудник ИК СО РАН Николай Сидоренко рассказал о практическом применении результатов исследования.
«Водород из воды получить достаточно легко, но при помощи доноров, то есть добавления, например, органики, в частности, спиртов, – рассказывает Николай. – Разложение же чистой воды на водород и кислород будет сильно удешевлять процесс получения водорода, потому что ничего дополнительно добавлять не нужно. Сначала мы работали над фотокатализатором получения водорода из воды, затем – над эффективным катализатором выделения кислорода, а следующий этап – создание «общего» катализатора для одновременного разложения чистой воды на водород и кислород».
Ученые планируют получать водород с использованием солнечной энергии путем фотокаталитического разложения чистой воды и затем использовать его, например, в качестве топлива для топливных элементов. В этом случае получится замкнутый экологически чистый цикл: водород, полученный из воды, будет питать топливные элементы, которые вырабатывают электричество посредством электрохимической реакции между водородом и кислородом с образованием воды.
В этом случае получится замкнутый экологически чистый цикл: водород, полученный из воды, будет питать топливные элементы, которые вырабатывают электричество посредством электрохимической реакции между водородом и кислородом с образованием воды.
Теги
Президентская программа, Химия и материалы, Молодежные группы
Получение водорода из морской воды с помощью солнечных панелей
Эффективное и экономически выгодное получение водорода и кислорода из морской воды с помощью электролиза было целью ученых на протяжении нескольких десятилетий, сообщает Newsweek.
Количество энергии, которое запасено в 1 кг одном килограмме водорода почти в 2.5 раза больше чем в природном газе, но что еще немаловажно, единственным продуктом сгорания водорода является вода. В недалёком будущем, с помощью водорода можно будет обеспечить энергией практически всё: от автомобилей до зданий и строений. Однако, получение водорода в таком глобальном масштабе может создать нагрузку на пресные источники воды, которые нужны как для питься, так и для использования в многочисленных промышленных процессах.
Команде ученых-химиков из Стэнфордского университета удалось разработать способ получения водорода из морской воды, которая, кстати, занимает 97% от запасов всей воды на Земле. Результаты своей работы опубликовали в Известиях Национальной академии наук США (PNAS).
Типичный электролизёр состоит из двух электродов – катода и анода, погружённых в электролит и разделённых мембраной. При пропускании электрического на этих электродах выделяются пузырьки газа, на аноде – кислород, на катоде – водород. Для снижения количества электричества, требуемого для разделения молекул вода на водород и кислород, электроды обычно покрывают специальным катализатором.
Электролизёр, разработанный командой из Стэнфорда во многом похож на коммерческие аналоги, только за одним исключением – их устройство может работать с солёной морской водой вместо пресно.
Если немного помните школьный курс химии, то знаете что соль NaCl состоит положительно заряженного атома натрия Na+ и отрицательно заряженного атома хлора Cl-.
Больше всего проблем ученым составлял Cl-, поскольку приводит к быстрой коррозии металлического анода. Соль можно удалить из морской воды с помощью опреснения, но это дорогой и затратный с энергетической точки зрения процесс. Чтобы избежать этапа опреснения, команда учёных разработала специальные электроды, который могут противостоять агрессивном условиях в процессе электролиза морской воды.
Анод, а именно токоприёмник они сделали из пористого никеля, который покрыли дешёвым, но высокоактивным катализатором на основе никеля и железа. Сам катализатор устойчив к коррозии, но нижележащий металлический проводит более активен и быстрее корродирует при контакте с раствором хлорида.
Чтобы решить проблему коррозии учёные нашли способ предотвратить миграцию хлорид-ионов через слой катализатора, тем самым предотвращая их попадание на металл. Хитрость заключалось в добавлении в границу раздела фаза катализатор-металл отрицательно заряженных молекул сульфита и карбоната. Поскольку одинаково заряженные частицы отталкиваются между собой, то эти молекулы сульфита и карбоната будут отталкивать хлор-ионы, тем самым не пропуская их к металлу.
Такой модифицированный анод способен отработать в течение 1000 часов в ходе электролиза морской воды при той же плотности тока, что применяется в коммерческих аппаратах. Ученые попробовали сделать еще более насыщенный растворов соли, где её концентрация была в три разы выше чем в морской воде, в таких условиях анод также отработал 1000 часов.
Чтобы электролиз воды был экологически чистым, энергия для него должна использоваться из возобновляемых источников. Поэтому ученые подключили к электролизёру коммерческую солнечную панель.
Испытания провели прямо на территории кампус Стэнфордского университета под естественным солнечных освещением. Плотность тока, протекающая через электролизёр составила прибл. 1А/см².
Как потом использовать этот самый водород и кислород? – можете
вы спросить. Можно подумать, что сжигать также как и природный газ – но нет. Это не эффективно. Водорода и кислород обратно в электричество преобразуется с помощью водородных топливных элементов (англ. , Fuel Cell). КПД таких элементов составляет 50-60%, что почти в 2 разе больше чем КПД двигателя внутреннего сгорания. Водород в них играет роль топлива, а кислород – окислителя. Активное использование водородных топливных элементов позволит стать на шаг ближе внедрению полноценной водородной энергетики.
, Fuel Cell). КПД таких элементов составляет 50-60%, что почти в 2 разе больше чем КПД двигателя внутреннего сгорания. Водород в них играет роль топлива, а кислород – окислителя. Активное использование водородных топливных элементов позволит стать на шаг ближе внедрению полноценной водородной энергетики.
Вообще, основная концепция водородной энергетики – это использование водорода в качестве аккумулятора энергии. Владельцы солнечных электростанций (даже маломощных) знают, что пик выработки электроэнергии приходится на дневное время, однако пик потребления электроэнергии приходится на вечернее время. Казалось бы есть выход, можно накапливать энергию в аккумуляторных батареях. Да, этот вариант подходит для частных домовладений, но не приемлем, когда речь идет о мега- и гигаваттных солнечных электростанция, поскольку в использовании аккумуляторов есть два главных недоставка. Первое, дороговизна, так
аккумуляторные батареи могут составлять почти 50% стоимости солнечной электростанции..jpg) Второе, короткой срок службы, который составляет не более 10 лет.
Второе, короткой срок службы, который составляет не более 10 лет.
Поэтому хранение энергии в виде водорода – это весьма перспективная альтернатива аккумуляторам. Избыточную энергию, которые вырабатывают солнечные панели в дневное время можно направить на получение водорода. В вечернее время, водород обратно преобразуется в электричество с помощью топливных элементов. Сказанное хорошо иллюстрирует картинка выше. Получается такой “альтернативный” цикл накопления и преобразования энергии.
Четыре способа введения растворенного кислорода в водоем
Четыре способа введения растворенного кислорода в ваш водоем
Озера и пруды помогают нам управлять ливневыми стоками, получать питьевую воду, обеспечивать возможности для рыбалки и отдыха, а также поддерживать красоту в наших сообществах. Но постоянное управление необходимо для обеспечения того, чтобы они продолжали нормально функционировать и оставались здоровыми. Для поддержания сбалансированного водоема необходимо присутствие одного важного элемента: кислорода.
1. Технология насыщения кислородом (OST)
Новая захватывающая инновация в отрасли — технология насыщения кислородом (OST). В отличие от других решений, этот инструмент направлен на устранение аноксии в озере и проблем с качеством воды в ее источнике — отложениях. Это решение для управления качеством воды премиум-класса впрыскивает кислород непосредственно в воду, что позволяет кислороду оставаться в растворе и рассеиваться, покрывая озерные отложения с высоким уровнем кислорода. Кроме того, эта система может подавать кислород на заданную глубину, не влияя на тепловую стратификацию или слои более холодной воды. Это позволяет размещать кислород и оставаться там, где он больше всего необходим, на границе отложений и воды.
Как работает OST:
Эта технология, меняющая правила игры, добавляет в пять-десять раз больше кислорода по сравнению с традиционными системами аэрации при сопоставимых или часто более низких затратах на электроэнергию.
2. Погружные аэраторы
С другой стороны, погружные аэраторы обеспечивают аэрацию посредством циркуляции. Сжатый воздух подается через диффузоры, размещенные на дне озера или пруда. Когда пузырьки поднимаются, они циркулируют в воде и выносят придонную воду с низким содержанием кислорода на поверхность, где кислород может поглощаться. Эта схема циркуляции смешивает воду и обеспечивает кислород на более низких глубинах.
3. Плавающие фонтаны
Плавающие фонтаны разбрызгивают воду в воздух с приятными узорами. Когда вода падает на поверхность, она создает турбулентность, которая способствует проникновению кислорода в толщу воды и одновременному выходу подводных газов. Фонтаны обладают многогранными преимуществами и даже могут быть украшены подсветкой для большей красоты.
4. Технология нанопузырьков
Системы нанопузырьковой технологии выкачивают воду из озера или пруда, вводят в нее нанопузырьки, а затем выпускают воду в водоем. Нанопузырьки микроскопичны — настолько малы, что не поднимаются на поверхность; вместо этого они дрейфуют и в конце концов растворяются, высвобождая кислород через несколько дней или недель. Обработка нанопузырьками лучше всего подходит для небольших неглубоких водоемов (примерно 3 акра или меньше). Каждый из этих инструментов работает по-разному, но все они предназначены для обработки хорошо сбалансированного водоема.
В заключение, растворенный кислород имеет решающее значение
Итак, как выглядит водоем, богатый кислородом? Кислород создает условия качества воды, которые помогают нейтрализовать фосфор и азот — обычные питательные вещества, которые в избытке могут загрязнять наши ценные водные ресурсы. Озера и пруды с более сбалансированным качеством воды менее благоприятны для роста водорослей и вредных сорняков. В свою очередь, это предотвращает выброс потенциальных токсинов водорослей, ограничивает образование донной грязи и неприятных запахов, а также способствует размножению полезных микробов, зоопланктона, местных рыб и других здоровых водных организмов.
Озера и пруды с более сбалансированным качеством воды менее благоприятны для роста водорослей и вредных сорняков. В свою очередь, это предотвращает выброс потенциальных токсинов водорослей, ограничивает образование донной грязи и неприятных запахов, а также способствует размножению полезных микробов, зоопланктона, местных рыб и других здоровых водных организмов.
Аэрация — важнейший инструмент в нашем наборе устойчивых решений, который также включает в себя научные лаборатории, беспилотные технологии, высокоточные гербициды и многое другое, но сам по себе он не может поддерживать баланс вашего водоема. Каждая водная экосистема уникальна и требует уникального сочетания стратегий для достижения триединства здоровья, красоты и функциональности. Самый эффективный и экономичный способ достижения ваших целей — это ежегодная программа управления, которая опирается на целый набор инструментов, чтобы ваш водоем получал наиболее эффективный и индивидуальный уход круглый год.
Кто мы
В SOLitude Lake Management мы стремимся сделать воду более здоровой и красивой частью нашей окружающей среды и нашего мира. В этом стремлении мы предлагаем устойчивые комплексные решения по управлению озерами и прудами.
В этом стремлении мы предлагаем устойчивые комплексные решения по управлению озерами и прудами.
Какой раствор растворенного кислорода подходит вам лучше всего?
Имя * Фамилия
Название компании
Адрес электронной почты * Номер телефона *
Штат/регион * — Пожалуйста, выберите -AKALARAZCACOCTDCDEFLGAHIIAIDILINKSKYLAMAMDMEMIMNMOMSMTNCNDNENHNJNMNVNYOHOKORPARISCSDTNTXUTVAVTWAWIWVWYINTLФизический почтовый индекс *
Сфера деятельности — Пожалуйста, выберите -VDCISOLitudeM & A
Источник потенциальных клиентов — Please Select -HUBSPOTInternet SearchInternet-HubspotCAIDirect MailEnewsFishing Expos or EventsGolf Course AssociationGolf Contact ListsGolf Course Superintendents AssocGoogle AdwordsInternetExisting ClientIndustry ConferenceLand ReportNewsletterOffice Staff ResearchOutdoor Sports ShowsPR / Media ExposurePrint AdvertisementProfessional ConferenceReferralsSales Person ProspectingSocial MediaMining for GoldStaff GeneratedTradeshowTruckTurfgrass Association/CouncilWineriesCabela’s Trophy Properties LeadsTurfgrass AssocColorado Mosquito ControlVDCICentral New York GCSADE Ассоциация питомников и ландшафтовNecoTechHRACREIREMRFPLandmark/JCM EnvironmentalNew Jersey CooperatorPond BossVirginia Lakes & WatershedsОбщество отдыха и парков штата ВирджинияДругоеPPC AdwordsVertexDIGITAL DISPLAY ADS
Контакт отправил новую формуДа Нет
Лид отправил форму обратной связиДа Нет
SOLitude Lake Management — общенациональная экологическая фирма, стремящаяся предоставлять устойчивые решения, которые улучшают качество воды, улучшают красоту, сохраняют природные ресурсы и уменьшают воздействие на окружающую среду. Команда SOLitude специалистов по управлению водными ресурсами специализируется на разработке и выполнении индивидуальных программ управления озерами, прудами, водно-болотными угодьями и рыболовством, которые включают проверку и восстановление качества воды, восстановление питательных веществ, борьбу с водорослями и водными сорняками, установку и обслуживание фонтанов и аэрации. системы, батиметрия, восстановление эрозии береговой линии, механический сбор и гидросгребание, исследования озерной растительности, биологические оценки, оценки среды обитания и управление инвазивными видами. Услуги и образовательные ресурсы доступны клиентам по всей стране, включая ассоциации домовладельцев, многоквартирные и многоквартирные дома, поля для гольфа, коммерческие объекты, ранчо, частных землевладельцев, водохранилища, рекреационные и общественные озера, муниципалитеты, органы питьевого водоснабжения, парки, а также государственные и федеральные агентства. SOLitude Lake Management является гордым членом семьи компаний Rentokil Steritech в Северной Америке.
Команда SOLitude специалистов по управлению водными ресурсами специализируется на разработке и выполнении индивидуальных программ управления озерами, прудами, водно-болотными угодьями и рыболовством, которые включают проверку и восстановление качества воды, восстановление питательных веществ, борьбу с водорослями и водными сорняками, установку и обслуживание фонтанов и аэрации. системы, батиметрия, восстановление эрозии береговой линии, механический сбор и гидросгребание, исследования озерной растительности, биологические оценки, оценки среды обитания и управление инвазивными видами. Услуги и образовательные ресурсы доступны клиентам по всей стране, включая ассоциации домовладельцев, многоквартирные и многоквартирные дома, поля для гольфа, коммерческие объекты, ранчо, частных землевладельцев, водохранилища, рекреационные и общественные озера, муниципалитеты, органы питьевого водоснабжения, парки, а также государственные и федеральные агентства. SOLitude Lake Management является гордым членом семьи компаний Rentokil Steritech в Северной Америке.
Высвобождение кислорода из воды: лучшие катализаторы для накопителей энергии исследования, которые дают новое понимание того, почему определенные катализаторы настолько эффективны в стимулировании выделения кислорода из воды во время электролиза — ключевого процесса во многих устройствах накопления энергии. Кредит: Стюарт Дарш
Исследователи Массачусетского технологического института и Лейденского университета в настоящее время представили однозначные экспериментальные доказательства того, что традиционная теория неточно описывает, как высокоэффективные катализаторы на основе оксидов металлов помогают высвобождать газообразный кислород из воды во время электролиза — критического процесса во многих технологиях хранения энергии. Используя особую форму кислорода в качестве маркера, они продемонстрировали, что газообразный кислород поступает не только из воды, но и из самого катализатора на основе оксида металла. Параллельно с теоретическими исследованиями они показали, что определенные электронные свойства таких высокоэффективных катализаторов допускают участие кислорода из катализатора. В настоящее время команда работает над определением последовательности химических реакций, которые приводят к выделению кислорода на этих специальных катализаторах. Их результаты уже дают новые ориентиры в продолжающемся поиске недорогих, эффективных материалов и конструкций для этих важных катализаторов.
В настоящее время команда работает над определением последовательности химических реакций, которые приводят к выделению кислорода на этих специальных катализаторах. Их результаты уже дают новые ориентиры в продолжающемся поиске недорогих, эффективных материалов и конструкций для этих важных катализаторов.
Многие системы хранения энергии основаны на электрохимических реакциях, вызывающих выделение газообразного кислорода из воды. Эти так называемые реакции выделения кислорода имеют решающее значение для эффективности устройств, которые расщепляют воду для извлечения водородного топлива, а также для работы регенеративных топливных элементов, металло-воздушных батарей и многого другого.
«Выделение кислорода — это одна из универсальных реакций, которая играет ключевую роль в разработке эффективных технологий накопления энергии путем сохранения энергии электронов в химической форме», — говорит Ян Шао-Хорн, исследователь W.M. Кека, профессор энергетики, профессор машиностроения, материаловедения и инженерии, а также содиректор Исследовательского центра энергосбережения MIT Energy Initiative.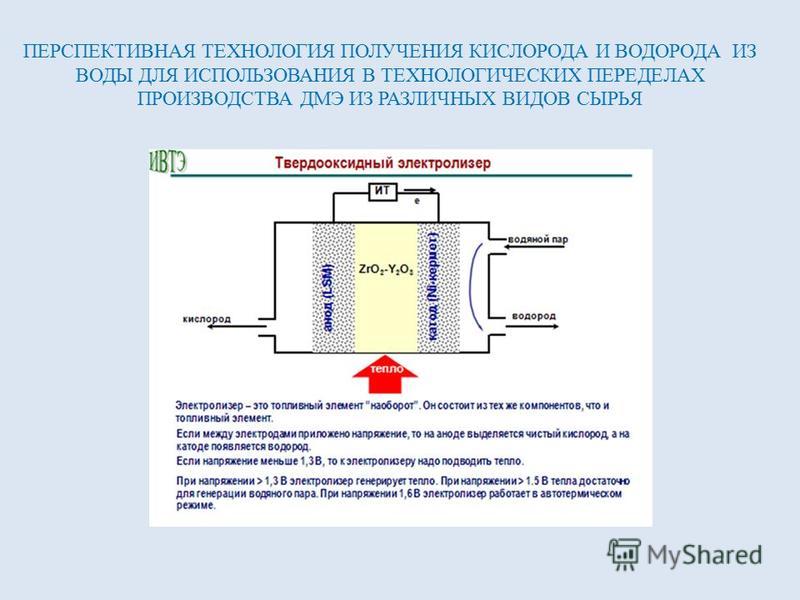
Кинетика реакций выделения кислорода обычно медленная, поэтому для ускорения химических реакций требуются катализаторы, такие как оксиды металлов (без расхода в процессе). При электролизе воды металлооксидный катализатор погружают в электролит на водной основе. При подаче потенциала молекулы воды вступают в реакцию с катализатором, разделяясь на положительно заряженные ионы водорода (протоны) и атомы кислорода, которые образуют газообразный кислород, выходящий из системы пузырьками.
Многие исследования были сосредоточены на выявлении оксидов металлов, которые будут выполнять эту задачу. Работают многие соединения, но каталитическая активность одних на порядки выше, чем у других. После трех лет интенсивных экспериментальных и теоретических исследований Шао-Хорн и ее коллеги из Лаборатории электрохимической энергии по-новому поняли, почему некоторые катализаторы на основе оксидов металлов работают так хорошо, и подготовили практические рекомендации по поиску новых, более эффективных катализаторов в будущее.
Эта электрохимическая ячейка лежит в основе экспериментальной установки, показанной на первой фотографии в этой статье. В его центре зонд, содержащий образец катализатора, погружен в электролит на водной основе. Через входящие провода подается напряжение, начинается электролиз, на поверхности катализатора образуются пузырьки газообразного кислорода и регистрируется результирующий ток. Зонд быстро вращается, чтобы предотвратить скопление пузырьков на катализаторе, которые могли бы остановить электрохимическую реакцию. Фото: Стюарт Дарш
Экспериментальное свидетельство: отслеживание кислорода
В своей работе Шао-Хорн, Бинхонг Хан, доктор философии ’16, бывший постдоктор Алексис Гримо, приглашенный профессор Ливия Джордано из Университета Милано-Бикокка в Италии, и их сотрудники исследовали многообещающий класс каталитических материалов, известных как перовскиты, которые, в отличие от современных современных катализаторов, состоят из недорогих материалов с высоким содержанием земли. Чтобы понять, что определяет эффективность катализатора, они хотели сравнить поведение двух перовскитов, один из которых более каталитически активен, чем другой. Поэтому они испытали катализаторы на основе того же переходного металла — кобальта — в сочетании с лантаном и стронцием. Известно, что сочетание кобальта, стронция и кислорода проявляет особенно высокую каталитическую активность — гораздо более высокую, чем смесь лантана.
Чтобы понять, что определяет эффективность катализатора, они хотели сравнить поведение двух перовскитов, один из которых более каталитически активен, чем другой. Поэтому они испытали катализаторы на основе того же переходного металла — кобальта — в сочетании с лантаном и стронцием. Известно, что сочетание кобальта, стронция и кислорода проявляет особенно высокую каталитическую активность — гораздо более высокую, чем смесь лантана.
Первый вопрос касается источника кислорода, который становится газообразным кислородом. Традиционная теория катализа на основе оксидов металлов утверждает, что весь кислород для реакций выделения кислорода поступает из воды и что все эти реакции происходят на атомах переходного металла, а не на атомах кислорода, на поверхности катализатора. Но может ли в реакциях с некоторыми материалами участвовать кислород из самого оксида металла, увеличивая выход кислорода? Эта гипотеза широко обсуждалась, но так и не была решена.
Чтобы ответить на этот вопрос, исследователи Массачусетского технологического института объединились с Оскаром Диас-Моралесом и Марком Т. Копером из Лейденского университета в Нидерландах. Вместе они проводят тесты, основанные на особой форме кислорода, которая служит экспериментальным маркером — изотопе кислорода-18 (кислород-16 — это форма, которая преобладает в обычной воде).
Копером из Лейденского университета в Нидерландах. Вместе они проводят тесты, основанные на особой форме кислорода, которая служит экспериментальным маркером — изотопе кислорода-18 (кислород-16 — это форма, которая преобладает в обычной воде).
Чтобы начать свои испытания, они сначала погружают образец металлооксидного катализатора в «тяжелую» воду, почти полностью содержащую кислород-18, а затем проводят электролиз, вызывая реакции на катализаторе. Во время этого процесса любые атомы кислорода, которые выходят из кристаллической решетки катализатора на основе оксида кобальта, оставляют вакансии, которые затем заполняются новыми атомами кислорода — в данном случае атомами кислорода-18 из тяжелой воды.
Затем исследователи удаляют катализатор из тяжелой воды, помещают его в обычную воду и снова проводят процесс электролиза. Затем они анализируют образующийся газообразный кислород с помощью масс-спектрометра, который разделяет различные изотопы на основе их атомного веса. Результаты показывают, сколько кислорода-18 присутствует в газообразных продуктах — кислороде, который должен был храниться в оксиде металла в первой части эксперимента. Исследователи провели этот тест с катализаторами, изготовленными из кобальта и кислорода, а также различных пропорций лантана и стронция, и результаты заметно отличались. Как показано на рисунках ниже, версии, содержащие стронций, не только проявляли большую каталитическую активность во время электролиза (измеряемую по протеканию тока), но также давали различные смеси продуктов кислорода.
Результаты показывают, сколько кислорода-18 присутствует в газообразных продуктах — кислороде, который должен был храниться в оксиде металла в первой части эксперимента. Исследователи провели этот тест с катализаторами, изготовленными из кобальта и кислорода, а также различных пропорций лантана и стронция, и результаты заметно отличались. Как показано на рисунках ниже, версии, содержащие стронций, не только проявляли большую каталитическую активность во время электролиза (измеряемую по протеканию тока), но также давали различные смеси продуктов кислорода.
Испытания с катализаторами на основе оксида кобальта, содержащими лантан и стронций
На этих рисунках представлены результаты экспериментов с катализаторами на основе оксида лантана-кобальта и стронция-оксида кобальта. Слева: здесь ток — показатель каталитической активности во время электролиза — измеряется как функция движущей силы. (Движущая сила определяется как приложенное напряжение относительно электрода сравнения, в частности, обратимого водородного электрода. ) По мере увеличения движущей силы активность катализатора на основе стронция намного превышает активность катализатора на основе лантана. Справа: в тех же экспериментах концентрации кислорода-36, образованного из кислорода, высвобождаемого из решетки оксида металла, значительно возрастают с движущей силой в тестах на стронций, но остаются практически постоянными с лантаном.
) По мере увеличения движущей силы активность катализатора на основе стронция намного превышает активность катализатора на основе лантана. Справа: в тех же экспериментах концентрации кислорода-36, образованного из кислорода, высвобождаемого из решетки оксида металла, значительно возрастают с движущей силой в тестах на стронций, но остаются практически постоянными с лантаном.
В газообразной форме молекулы кислорода состоят из пары атомов кислорода, связанных вместе. Анализ образцов, собранных в ходе экспериментов с катализатором на основе оксида лантана и кобальта, выявил кислород-32 — комбинацию двух атомов кислорода-16. Таким образом, кислород в газообразных продуктах поступает из воды, как это и предписывается общепринятой теорией.
Напротив, испытания с высокоактивным катализатором на основе оксида стронция-кобальта дали продукты, содержащие значительное количество кислорода-36, т. е. комбинации двух атомов кислорода-18 — атомов, которые могли произойти только из кристаллической решетки оксид металла (см. схему ниже).
схему ниже).
Схема, показывающая выделение кислорода из решетки оксида металла
На этой схеме октаэдры представляют структуру катализатора оксида стронция-кобальта с интересующими атомами в их вершинах. Сверху поступают молекулы воды, состоящие из атомов водорода и кислорода-16. Во время электрохимической реакции атомы кислорода-18 высвобождаются из катализатора и объединяются в пары, образуя кислород-36, обнаруженный в экспериментах.
Эти результаты убедительно показывают, что кислород в кристаллической решетке принимает участие в реакции выделения кислорода. Интересно, что комбинированный лантан-стронциевый вариант катализатора производил кислород-34. В этом молекулярном соединении один кислород-16 из воды объединился с одним кислородом-18 из решетки оксида металла.
Одна возможность состоит в том, что кислород-18 адсорбируется и высвобождается только на поверхности катализатора. Чтобы проверить, исследователи подсчитали, сколько кислорода-18 может содержаться в объеме катализатора на основе оксида стронция-кобальта. Затем они определили, сколько материала потребуется для адсорбции и высвобождения количества кислорода-18, которое они измерили в газообразном кислороде. Их анализ подтверждает, что в поверхностных слоях недостаточно места для хранения. Действительно, кислород-18, который участвует, должен был появиться глубоко внутри катализатора на основе стронция.
Затем они определили, сколько материала потребуется для адсорбции и высвобождения количества кислорода-18, которое они измерили в газообразном кислороде. Их анализ подтверждает, что в поверхностных слоях недостаточно места для хранения. Действительно, кислород-18, который участвует, должен был появиться глубоко внутри катализатора на основе стронция.
Испытания со стронциевым катализатором принесли еще один интересный вывод: изменение кислотности воды вызывало значительные изменения каталитической активности. Для большинства катализаторов на основе оксидов металлов, включая оксид лантана и кобальта, изменение pH воды не влияет на скорость реакции. Но с высокоактивным катализатором на основе оксида стронция-кобальта повышение pH (то есть повышение его щелочности) увеличивало скорость выделения кислорода.
На рисунке ниже представлены результаты этих экспериментов с катализаторами. Влияние изменения рН почти незначительно в случае оксида лантана-кобальта, несколько больше, когда стронций заменяет часть лантана, и весьма заметно в тестах с оксидом стронция-кобальта.
Влияние pH на каталитическую активность
На этом рисунке показано, как изменение pH воды влияет на каталитическую активность катализаторов на основе оксида кобальта. В то время как активность катализатора на основе оксида лантана-кобальта не зависит от повышения pH, добавление стронция к катализатору меняет этот результат. В опытах с катализатором на основе оксида стронция-кобальта каталитическая активность вначале выше, а затем повышается быстрее по мере увеличения рН.
Копаем глубже
Очевидно, что высокоактивный катализатор не соответствует общепринятому мнению, согласно которому весь кислород для реакций выделения кислорода поступает из воды и что реакции происходят только на металлических участках на поверхности катализатора. Что отличает катализатор на основе оксида стронция-кобальта от катализатора на основе оксида лантана-кобальта?
Основываясь на своем теоретическом моделировании, исследователи пришли к выводу, что ответ лежит в электронной структуре двух оксидов металлов: в версии стронция связи металл-кислород гораздо более ковалентны. В любом материале существуют определенные энергетические уровни, которые могут занимать электроны, и электроны с наивысшим энергетическим уровнем легче всего удалить. В оксидах металлов с рекордно высокой каталитической активностью, таких как оксид стронция-кобальта, наивысшие уровни электронной энергии металла и кислорода совпадают, и говорят, что материалы являются ковалентными.
В любом материале существуют определенные энергетические уровни, которые могут занимать электроны, и электроны с наивысшим энергетическим уровнем легче всего удалить. В оксидах металлов с рекордно высокой каталитической активностью, таких как оксид стронция-кобальта, наивысшие уровни электронной энергии металла и кислорода совпадают, и говорят, что материалы являются ковалентными.
«В нашем катализаторе на основе стронция и металл, и кислород способны отдавать электроны на энергетическом уровне, необходимом для соединения пар освобожденных атомов кислорода с образованием молекул», — говорит Шао-Хорн. «В результате и металл, и кислород в катализаторе являются активными центрами для реакций выделения кислорода».
Выводы исследователей предполагают необходимость пересмотра теоретического механизма реакции, описывающего последовательность химических изменений, происходящих при выделении кислорода на металлооксидном катализаторе. Преобразование воды в кислород на катализаторе требует переноса четырех электронов и четырех протонов. Обычный механизм реакции говорит, что электроны и протоны должны двигаться одновременно. То есть их передача должна быть согласованной. «Но этот механизм не допускает участия кислорода из кристаллической решетки или зависимости от pH», — говорит Джордано.
Обычный механизм реакции говорит, что электроны и протоны должны двигаться одновременно. То есть их передача должна быть согласованной. «Но этот механизм не допускает участия кислорода из кристаллической решетки или зависимости от pH», — говорит Джордано.
Исследователи пришли к выводу, что при выделении кислорода на высокоактивном катализаторе из оксида металла должен происходить несогласованный перенос. Разделение переноса протонов и электронов допускает участие атомов кислорода из кристаллической решетки, и это объясняет, почему они наблюдали рН-зависимую реакционную способность. «Если механизм не согласован — скажем, сначала идет протон, а затем электрон, — тогда активность может зависеть от pH», — говорит Джордано. «Когда мы изменяем pH, мы изменяем концентрацию протонов в нашем электролите, и это повлияет на скорость реакции, но только если протоны и электроны могут двигаться независимо».
Руководство по проектированию
Новое понимание реакций выделения кислорода открывает новые направления для разработки эффективных катализаторов. Например, исследователи могут исследовать другие материалы, в том числе альтернативы кобальту, чтобы найти комбинации с более высокой ковалентностью. «Мы показали, что выделение кислорода из оксида металла увеличивает каталитическую активность», — говорит Джордано. «Поэтому для разработки особенно активных катализаторов мы должны попытаться увеличить ковалентность оксида металла, чтобы вызвать активацию кислорода в решетке и обеспечить несогласованный перенос протон-электрон». В этих условиях влияние на реактивность путем изменения pH воды становится еще одним направлением для изучения.
Например, исследователи могут исследовать другие материалы, в том числе альтернативы кобальту, чтобы найти комбинации с более высокой ковалентностью. «Мы показали, что выделение кислорода из оксида металла увеличивает каталитическую активность», — говорит Джордано. «Поэтому для разработки особенно активных катализаторов мы должны попытаться увеличить ковалентность оксида металла, чтобы вызвать активацию кислорода в решетке и обеспечить несогласованный перенос протон-электрон». В этих условиях влияние на реактивность путем изменения pH воды становится еще одним направлением для изучения.
Их выводы дают еще один практический совет. В начале проекта основной целью было определить этап, ограничивающий скорость выделения кислорода. Скорость любой химической реакции определяется скоростью самой медленной стадии процесса. Таким образом, ускорение этого шага является ключом к ускорению общей реакции.
При использовании многих катализаторов на основе оксидов металлов скорость электролиза воды ограничена тем, насколько быстро кислород выходит из катализатора. Но в их высококовалентном материале перенос электронов, необходимый для освобождения молекул кислорода, должен быть довольно легким. «Итак, мы предполагаем, что удаление протонов с поверхности может на самом деле ограничивать скорость протекания реакции», — говорит Джордано. Они пока не могут подтвердить эту гипотезу, в основном потому, что нет единого мнения о том, как теоретически моделировать несогласованные этапы реакции на этих сложных материалах. «Это то, что мы действительно хотели бы сделать», — говорит она. Их следующая задача — выяснить, как это сделать.
Но в их высококовалентном материале перенос электронов, необходимый для освобождения молекул кислорода, должен быть довольно легким. «Итак, мы предполагаем, что удаление протонов с поверхности может на самом деле ограничивать скорость протекания реакции», — говорит Джордано. Они пока не могут подтвердить эту гипотезу, в основном потому, что нет единого мнения о том, как теоретически моделировать несогласованные этапы реакции на этих сложных материалах. «Это то, что мы действительно хотели бы сделать», — говорит она. Их следующая задача — выяснить, как это сделать.
В исследовательскую группу для этой работы также входили Уэсли Хонг, доктор философии 16 года, бывший постдоктор Юэ-Лин Ли и Келси Стоерзингер, доктор философии 16 года. Исследование проводилось при поддержке Центра электрохимической энергетики Сколтеха и Массачусетского технологического института, Сингапурского альянса по исследованиям и технологиям Массачусетского технологического института, Министерства энергетики США и Национальной лаборатории энергетических технологий.

