Доклад — Атомы и молекулы
Все вещества состоят из крошечных частиц — атомов. Атомы соединяются в молекулы, крупнейшие из которых имеют сложное строение, состоящее из тысяч атомов.
О том, что все сущее состоит из частиц, знали еще древние греки. Около 420 г. до н. э. философ Демокрит поддержал гипотезу, что материя состоит из крошечных, неделимых частиц. По-гречески atomos означает «неделимый», поэтому эти частицы назвали атомами.
Другие философы придерживались иной точки зрения, и в IV веке до н. э. Аристотель высказался в поддержку мнения, согласно которому материя состоит из различных сочетаний так называемых четырех стихий — земли, воздуха, огня и воды. Эта идея получила широкое распространение и легла в основу алхимии — примитивной формы химии, господствовавшей в науке до XVII века.
Одной из главных задач алхимии было создание «эликсира жизни» — снадобья, которое позволило бы человеку жить вечно. Другая заключалась в создании богатств путем превращения обычных металлов в золото. Многие алхимики утверждали, что решили эти задачи, однако никто из них так и не добился реального успеха.
Переворот в науке
Некоторые ученые продолжали придерживаться мнения, что материя состоит из атомов, но только в начале XIX века были получены экспериментальные данные, подтверждающие эту теорию. Английский химик и писатель Джон Дальтон проводил опыты с газами и изучал пути их соединения. Так, он обнаружил, что кислород и водород, образуя воду, всегда соединяются в одних и тех же пропорциях по массе. Другие ученые также сталкивались с подобными данными, но именно Дальтон впервые осознал их значение. Он сделал вывод, что вещества состоят из атомов, и что все атомы простого вещества имеют одинаковую массу. При соединении простых веществ количества соединяющихся атомов находятся в определенной неизменной пропорции. Атомистика Дальтона объясняла, почему вещества соединяются в неизменной массовой пропорции, а также явилась основой для детального изучения материи. Вещества состоят из атомов, а из чего состоят атомы? Первые ключи к разгадке этой тайны появились в конце XIX века, когда исследователи изучали прохождение электричества через разрядные трубки, содержащие разреженный воздух. Иногда стенки трубки излучали зеленый свет при подаче высокого напряжения на две металлические пластины — электроды. Свечение возникало при попадании невидимых лучей от отрицательного электрода, или катода, на стенки трубки.
В 1890-х годах английский физик Дж. Томсон доказал, что эти катодные лучи (как их тогда называли) — не что иное, как потоки отрицательно заряженных частиц. Предполагалось, что эти частицы исходят из атомов, хотя их расположение внутри атомов оставалось неясным. Томсон высказал предположение, что атом может быть похож на рождественский пудинг, в котором большая, но легкая по массе положительно заряженная сфера усеяна многочисленными отрицательно заряженными частицами (электронами). Однако различные опыты по изучению строения атома доказали, что это — безусловно ошибочная теория.
Строение атома
В 1911 году Эрнест Резерфорд, британский физик, уроженец Новой Зеландии, работавший вместе с Томсоном, предложил строение атома, реально объясняющее его поведение во время экспериментов. Резерфорд предположил, что центр (или ядро) атома имеет положительный заряд и относительно большую массу, а вокруг ядра вращаются крайне легкие и отрицательно заряженные электроны.
Однако Резерфорд не осознавал, что обычно в ядре атома находятся как положительно заряженные, так и нейтральные частицы. Существование положительно заряженных частиц было признано в 1920 г., и они получили название протоны. В 1932 г. английский физик Джеймс Чэдвик открыл незаряженные частицы и назвал их нейтронами. В результате картина строения атома была завершена и с тех пор является основой нашего понимания материи.
Элементы
Любое вещество, в котором все атомы имеют одинаковое количество протонов, называется элементом. Число протонов в каждом атоме — атомный номер элемента. Существуют 92 природных элемента, их атомы имеют от 1 до 92 протонов. Кроме того, некоторые другие элементы с еще большим числом протонов в атоме можно получить с помощью устройства под названием ускоритель элементарных частиц. К природным элементам относятся железо, ртуть и водород.
| Профессиональная химчистка диванов в Москве |
Во многих веществах атомы объединяются в группы, называемые молекулами. Так, газ водород состоит из молекул, каждая из которых содержит два атома водорода. Часто, однако, молекулы вещества состоят из атомов более одного элемента. Такие вещества называются соединениями. Например, вода является соединением, где каждая молекула состоит из двух атомов водорода и одного атома кислорода. Во многих молекулах насчитывается гораздо большее количество атомов. Некоторые белковые молекулы представляют собой сложные соединения из нескольких тысяч атомов. Некоторые природные элементы встречаются только в соединениях. Так, натрий — это металл, настолько легко соединяющийся с другими веществами, что его нельзя обнаружить в чистом виде. Он широко известен в сочетании с хлором в виде хлорида натрия — поваренной соли.
Связи
Атомы в молекулах связываются различными путями, при этом они разделяют между собой электроны или обмениваются ими. Двумя простыми видами химической связи являются ковалентная и ионная.
Ковалентная связь возникает, когда атомы имеют общие электроны. Так, молекула водородного газа состоит из двух атомов водорода, связанных ковалентной связью. Единственный электрон каждого атома водорода вращается вокруг ядер обоих атомов, связывая их воедино.
В случае ионной связи один атом передает электроны другому атому. В результате возникает электрическая сила, связывающая атомы воедино. Как правило, количество положительно заряженных протонов и отрицательно заряженных электронов в атоме одинаково. Их положительные и отрицательные заряды уравновешивают друг друга, и поэтому атом не имеет общего заряда. Однако в атоме, отдающем электроны, создается избыток положительного заряда, а атом, получающий электроны, приобретает общий отрицательный заряд. Такие заряженные атомы называются ионами. Ионы противоположных зарядов притягиваются друг к другу, и именно это электрическое притяжение удерживает атомы вместе при ионной связи. Например, молекула поваренной соли формируется с помощью ионной связи, когда атом натрия передает электрон атому хлора.
Все атомы одного вещества имеют одинаковое количество протонов, но различное количество нейтронов. Так, в углероде ядро большинства атомов содержит шесть нейтронов, но примерно в каждом сотом из них имеется семь нейтронов. Эти различные типы атомов одного и того же элемента называются изотопами. Все изотопы данного элемента обладают одинаковыми химическими свойствами — все они соединяются с другими веществами и образуют одни и те же химические соединения. Но отдельные физические свойства изотопов различаются — например, они имеют разные точки замерзания или кипения.
Говоря о конкретном изотопе того или иного элемента, ученые называют его массовое число. Например, углерод-12 — это обычный природный изотоп углерода. Его атом содержит шесть протонов и шесть нейтронов. Более редкий природный изотоп, в ядре каждого атома которого находится лишний нейтрон, называется углерод-13.
Атомный вес
Протон и нейтрон имеют почти одинаковую массу, которая более чем в 1800 раз превышает массу электрона. Поэтому когда речь идет о массе атома, как правило, не будет ошибкой ссылаться на его массовое число.
Атомный вес элемента, или его относительная атомная масса, обычно представляет собой среднюю массу смеси изотопов, встречающихся в природе. Молекулярный вес вещества, или его относительная молекулярная масса, — это сумма атомных весов всех атомов в одной молекуле данного вещества.
Многосложный атом
С тех пор экспериментировавшие с ускорителями ученые открыли сотни других видов частиц в атомах. Но, к счастью, простая модель атома достаточна для того, чтобы объяснить большую часть свойств материи.
Атомно-молекулярное учение — Википедия
Атомно-молекулярное учение
В развитие атомно-молекулярного учения большой вклад внесли М. В. Ломоносов, Дж. Дальтон, А. Лавуазье, Ж. Пруст, А. Авогадро, Й. Берцелиус, Д. И. Менделеев, А. М. Бутлеров и многие другие.
Античная атомистика[править | править код]
Представление о том, что материя состоит из отдельных частиц — атомов возникло ещё в древней Греции в V в. до н. э. Атомизм был создан представителями древнегреческой философии Левкиппом (500—440 до н. э.) и его учеником Демокритом (460—370 до н. э.).
Левкипп задался вопросом, можно ли каждую частичку материи, какая бы малая она ни была, разделить на еще более мелкие частицы. Левкипп считал, что в результате такого деления можно получить настолько малую частицу, что дальнейшее деление станет невозможным.
Ученик Левкиппа философ Демокрит назвал эти крошечные частицы «атомами» (атомос-неделимый). Он считал, что атомы каждого элемента имеют особые размеры и форму и что именно этим объясняются различия в свойствах веществ. Вещества, которые мы видим и ощущаем, образуется при соединение между собой атомов различных элементов, и, изменив природу этого соединения, можно одно вещество превратить в другое.
Левкипп, Демокрит и Эпикур, полагали, что твердость материала соответствовала форме атомов, из которых он состоит. Таким образом, атомы железа являются твердыми и прочными с крючками, которые фиксируют их в твердом теле, атомы воды гладкие и скользкие, атомы соли, из-за их вкуса, острые и заостренные и атомы воздуха являются легкими и вращающимися, проникая во все другие материалы. Именно Демокрит был главным сторонником этой точки зрения. Используя аналогии, основанные на чувственном опыте, он описывал атомы различных веществ, как отличными друг от друга по форме, размеру и расположению их частей. Кроме того, связи объяснялись материальными связями, в которых отдельные атомы снабжались насадками: некоторые с крючками и ушками, другие с шариками и гнездами.
Другим воплощением идеи дискретности стали теории Эмпедокла, Платона и Аристотеля об элементах-качествах, однако, они составляли отдельное направление развития представления о веществе и его составе, создав тем самым основу алхимических представлений о трасмутации веществ.
Становление атомистической гипотезы в XVII—XVIII веках[править | править код]
XVII век[править | править код]
С ростом влияния схоластики и упадка Римской империи атомная теория была отвергнута на многие века в пользу различных четырехэлементных теорий и более поздних алхимических теорий. Однако, в 17 веке исследователи вновь вернулись к атомной теории, прежде всего благодаря работам Пьерра Гассенди и Исаака Ньютона. Среди других ученых того времени П. Гассенди глубоко изучил древнюю историю, написал основные труды о натурфилософии Эпикура и стал пропагандистом его идеи. Он рассуждал, что для учета размеров и формы атомов, движущихся в пустоте, могут быть учтены и свойства самого вещества. Тепло было связано с маленькими круглыми атомами, а холод – с пирамидальными атомами с острыми концами, что объясняло ощущение уколов от сильного холода, а твердые тела удерживались вместе переплетающимися крючками.
Ньютон, хотя и признавал различные теории присоединения атомов, находившиеся в то время в моде, т. е. теорию «зацепленных атомов», «склеенных атомов» (тела в состоянии покоя) и теорию «слипания посредством согласованных движений», скорее всего, полагал, как это хорошо сказано в его «Оптике» 1704 года, что частицы притягиваются друг к другу некоторой силой, которая «в непосредственном контакте чрезвычайно сильна, на малых расстояниях выполняет химические взаимодействия и действует на частицы с любым ощутимым эффектом.»
Однако, более конкретно, концепция агрегатов или единиц связанных атомов, то есть «молекул», как сказали бы сегодня, берет свое начало от гипотезы Роберта Бойля 1661 года, в его знаменитом трактате «The Sceptical Chymist», что материя состоит из скоплений частиц (кластеров), и что химические изменения являются результатом перестройки этих кластеров. Р. Бойль утверждал, что основные элементы материи состоят из частиц различного типа и размера, называемых «корпускулами», которые способны организовываться в группы.
В 1680 году французский химик Николя Лемери, взяв за основу корпускулярную теорию, установил, что кислотность любого вещества состоит в его заостренных частицах, а щелочи наделены порами различных размеров. Молекула, согласно этой точке зрения, состояла из корпускул, Объединенных геометрическим соединением точек и пор.
XVIII век[править | править код]
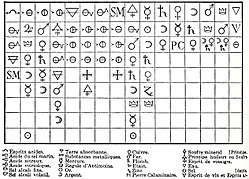 Таблица сродства Этьена Франсуа Жоффруа 1718 года: во главе колонки (столбца) находится вещество, с которым могут сочетаться все перечисленные ниже вещества.
Таблица сродства Этьена Франсуа Жоффруа 1718 года: во главе колонки (столбца) находится вещество, с которым могут сочетаться все перечисленные ниже вещества.Ранним предшественником идеи связанных «комбинаций атомов» была теория «объединения через химическое сродство». Например, в 1718 году, основываясь на концепции Бойля о комбинациях кластеров, французский химик Этьен Франсуа Жоффруа разработал теорию химического сродства для объяснения комбинаций частиц, полагая, что определенная алхимическая «сила» притягивает определенные алхимические компоненты. Имя Жоффруа наиболее известно в связи с его таблицами «сродства» (tables des rapports), которые он представил Французской академии в 1718-1720 годах. Это были списки, составленные путем сопоставления наблюдений за действием веществ друг на друга, показывающие различные степени сродства, проявляемые аналогичными телами для различных реагентов. Эти таблицы сохраняли свою актуальность до конца столетия, пока не были вытеснены более глубокими концепциями, введенными Клодом Бертолле.
Атомистическая гипотеза в XIX веке[править | править код]
Атомистическая теория Дальтона[править | править код]
Перечень символов химических элементов и их атомных весов Дж. Дальтона (1808)Создание научной теории стало возможно только в XVIII-XIX веках, когда физика и химия стали базироваться на точных экспериментальных данных.
Экспериментальное подтверждение атомной гипотезы нашёл английский химик Джон Дальтон. В начале XIX века Дальтон открыл несколько новых эмпирических закономерностей: закон парциальных давлений (закон Дальтона), закон растворимости газов в жидкостях (закон Генри-Дальтона) и, наконец, закон кратных отношений (1803). Объяснить эти закономерности (прежде всего закон кратных отношений), не прибегая к предположению о дискретности материи, невозможно. В 1808 году Дальтон изложил свою атомистическую гипотезу в труде «Новая система химической философии».
Основные положения теории Дальтона состояли в следующем (в основе атомно-молекулярного учения лежит принцип дискретности (прерывности строения) веществ)[1]:
- Всякое вещество не является чем-то сплошным, а состоит из отдельных очень малых частиц — все вещества состоят из большого числа атомов (простых или сложных).
Различие между веществами обусловлено различием между их частицами - Атомы одного вещества полностью тождественны. Простые атомы абсолютно неизменны и неделимы.
- Частицы (атомы) различных веществ различны — как по массе, так и по свойствам
- Атомы различных элементов способны соединяться между собой в определённых соотношениях.
- Важнейшим свойством атомов является атомный вес.
Уже в 1803 году в лабораторном журнале Дальтона появилась первая таблица относительных атомных весов некоторых элементов и соединений (атомный вес водорода был принят равным единице). Дальтон ввёл символы химических элементов в виде окружностей с различными фигурами внутри. Впоследствии Дальтон неоднократно корректировал атомные веса элементов, однако для большинства элементов им приводились неверные значения.
Работы А. Авогадро[править | править код]
Амедео Авогадро предложил новое слово «молекула». Согласно «Краткой историей химии» Партингтона, в своей статье 1811 года «Эссе по определению относительных масс элементарных тел молекул» он, по сути, утверждает:
 | Мельчайшие частицы газов не обязательно являются простыми атомами, но состоят из определенного числа этих атомов, соединенных притяжением, чтобы образовать единую молекулу. |  |
Обратите внимание, что эта цитата не является буквальным переводом. Авогадро использует название «молекула» как для атомов, так и для молекул. В частности, он использует название «элементарная молекула», когда ссылается на атомы, и для усложнения этого вопроса также говорит о «составных атомах» и «составных молекулах».
Во время своего пребывания в Верчелли Авогадро написал краткую записку (меморандум), в которой изложил гипотезу о том, что мы теперь называем законом Авогадро: равные объемы газов при одинаковой температуре и давлении содержат одинаковое число молекул. Этот закон подразумевает, что соотношение, возникающее между весами одинаковых объемов различных газов при одинаковых температуре и давлении, соответствует соотношению между соответствующими молекулярными весами. Следовательно, относительные молекулярные веса можно было теперь вычислить по массам образцов газа.
Авогадро разработал эту гипотезу, чтобы согласовать закон Дж. Л. Гей-Люссака 1808 года об объемах и сочетании газов с атомной теорией Дальтона 1803 года. Самая большая трудность, с которой Авогадро пришлось столкнуться, заключалась в огромной путанице в то время в отношении атомов и молекул. Одним из самых важных вкладов работы Авогадро было четкое разграничение одного от другого, допускающее, что простые вещества тоже могут состоять из молекул, состоящих из атомов. Дальтон же, напротив, не рассматривал такую возможность. Любопытно, что Авогадро рассматривает только молекулы, содержащие четное число атомов; он не говорит, почему нечетные числа опущены.
В 1826 году, опираясь на работу Авогадро, французский химик Жан-Батист Дюма утверждает:
 | Газы при одинаковых условиях состоят из молекул или атомов, расположенных на одинаковом расстоянии, что равносильно тому, что они содержат одинаковое их количество в одном и том же объеме. |  |
В соответствии с этими концепциями в 1833 году французский химик Марк Антуан Огюст Годен представил ясный отчет о гипотезе Авогадро относительно атомных весов, используя «объемные диаграммы», которые ясно показывают как полу-корректную молекулярную геометрию (линейная молекула воды), так и правильные молекулярные формулы, например, H2O:
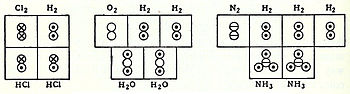
В двух работах, описывающих его «теорию атомности элементов» (1857-1858 гг.), Фридрих Август Кекуле был первым, кто предложил теорию того, как каждый атом в органической молекуле связан с каждым другим атомом. Он предположил, что атомы углерода в органических соединениях являются четырехвалентными и могут связываться друг с другом, образуя углеродные скелеты молекул.
Съезд химиков в Карлсруэ[править | править код]
С 3 по 5 сентября 1860 года состоялся Международный съезд химиков в Карлсруэ. Это была первая международная конференция, посвященная химии. Большое влияние на ход конгресса оказал итальянский химик Канниццаро. Он на основе закона Авогадро чётко разграничил понятия «атом», «молекула» и «эквивалент» и предложил рациональную систему атомной массы. Свою теорию он изложил в брошюре, которую лично раздал всем участникам конгресса. В своих выступлениях Канниццаро отстаивал закон Авогадро и систему Жерара и указывал на то, что возвращать химию к принципам Берцелиуса нецелесообразно. В целом конгресс положительно отнесся к идеям Канниццаро. Результатом съезда химиков в Карлсруэ стало утверждение атомно-молекулярного учения, были определены понятия атомного веса, а также молекулы и атома. Было установлено, что молекула — это наименьшее количество вещества, вступающее в реакции и определяющее физические свойства, а атом — наименьшее количество элемента, содержащееся в молекулах.
Работы химиков второй половине XIX века[править | править код]
В 1856 году шотландский химик Арчибальд Купер начал исследования по бромированию бензола в лаборатории Шарля Вюрца в Париже. Через месяц после выхода второй статьи Кекуле была опубликована независимая и в значительной степени идентичная теория молекулярного строения Купера. Он предложил очень конкретную идею молекулярной структуры, предположив, что атомы соединяются друг с другом подобно конструктору в определенных трехмерных конструкциях. Купер был первым, кто использовал линии между атомами, в сочетании со старым методом использования скобок, для представления связей, а также постулировал прямые цепочки атомов как структуры одних молекул, кольцеобразные молекулы других, таких как винная кислота и циануровая кислота. В более поздних публикациях связи Купера были представлены с помощью прямых пунктирных линий (хотя неизвестно, является ли это предпочтением наборщика), например, спирт или щавелевая кислота:
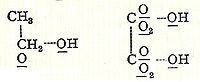 Молекулярные структуры Арчибальда Купера для спирта и щавелевой кислоты, использующие элементарные символы для атомов и линии для связей (1858).
Молекулярные структуры Арчибальда Купера для спирта и щавелевой кислоты, использующие элементарные символы для атомов и линии для связей (1858).В 1861 году неизвестный учитель Венской средней школы по имени Йозеф Иоганн Лошмидт опубликовал за свой счет брошюру под названием «Chemische Studien I», содержащую новаторские молекулярные изображения, которые показывали, как «кольцевые» структуры, так и структуры с двойной связью, такие как:
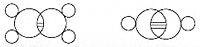 Изображения Й. И. Лошмидта молекул этилена h3C=Ch3 и ацетилена HC≡CH (1861).
Изображения Й. И. Лошмидта молекул этилена h3C=Ch3 и ацетилена HC≡CH (1861).Лошмидт также предложил возможную формулу бензола, но оставил этот вопрос открытым. Первое предложение о современной структуре бензола было сделано Августом Кекуле в 1865 году. Циклическая природа бензола была окончательно подтверждена кристаллографом Кэтлин Лонсдейл. Бензол представляет собой особую проблему в том смысле, что для учета всех связей необходимо наличие чередующихся двойных углеродных связей:
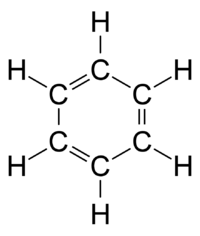 Молекула бензола с чередующимися двойными связями.
Молекула бензола с чередующимися двойными связями.В 1865 году немецкий химик Август Вильгельм фон Гофманн был первым, кто сделал шаростержневые модели молекул, которые он использовал в лекции в Королевском институте Великобритании, такие как метан:
 Модель молекулы метана CH4, созданная Гофманом в 1865 году.
Модель молекулы метана CH4, созданная Гофманом в 1865 году.В основу этой модели легло высказанное ранее в 1855 году его коллегой Уильямом Одлингом предположение о том, что углерод является четырехвалентным. Следует отметить, что цветовая схема Гофмана используется и по сей день: азот – синий, кислород – красный, хлор – зеленый, сера – желтый, водород – белый. Недостатки в модели Гофмана были в основном геометрическими: углеродные связи была показаны в одной плоскости, а не тетраэдрическими, и размеры атомов были непропорциональны, например, углерод был меньше по размеру, чем водород.
В 1864 году шотландский химик-органик Александр Крум Браун начал рисовать изображения молекул, в которых он заключил символы атомов в круги и использовал ломаные линии, чтобы соединить атомы вместе таким образом, чтобы удовлетворить валентность каждого атома. 1873 год, по многим отзывам, стал переломным моментом в истории развития понятия «молекула». В этом году известный шотландский физик Джеймс Клерк Максвелл опубликовал свою знаменитую статью «Молекулы» в сентябрьском номере журнала Nature. Во вступительном разделе к этой статье Максвелл ясно заявляет:
 | Атом — это тело, которое нельзя разрезать пополам; молекула — это наименьшая возможная часть определенного вещества. |  |
После разговора об атомной теории Демокрита Максвелл продолжает говорить нам, что слово «молекула» — это современное слово.
В 1874 году Якоб Хендрик Вант-Гофф и Джозеф Ахилл Ле Бель[en] независимо друг от друга предположили, что явление оптической активности можно объяснить, предположив, что химические связи между атомом углерода и его соседями направлены к углам правильного тетраэдра. Это привело к лучшему пониманию трехмерной природы молекул.
Эмиль Фишер разработал собственную методику проецирования трехмерной структуры молекул на плоскость:

В 1898 году Людвиг Больцман в своих лекциях по теории газа использовал теорию валентности для объяснения феномена молекулярной диссоциации газовой фазы и при этом нарисовал один из первых примитивных, но детальных рисунков перекрывания атомных орбиталей. Отмечая прежде всего известный факт, что пары молекулярного йода диссоциируют на атомы при более высоких температурах, Больцман утверждает, что мы должны объяснить существование молекул, состоящих из двух атомов, «двойного атома», как называет его Больцман, силой притяжения, действующей между двумя атомами. Больцман утверждает, что это химическое притяжение, вследствие определенных фактов химической валентности, должно быть связано с относительно небольшой областью на поверхности атома, называемой чувствительной областью.
Больцман утверждает, что эта «чувствительная область» будет лежать на поверхности атома или может частично находиться внутри атома и будет прочно связана с ним. В частности, он утверждает: «только когда два атома расположены так, что их чувствительные области соприкасаются или частично перекрываются, между ними будет существовать химическое притяжение. Затем мы говорим, что они химически связаны друг с другом.Эта картина подробно описана ниже, показывая α-чувствительную область атома А, перекрывающуюся с β-чувствительной областью атома B:
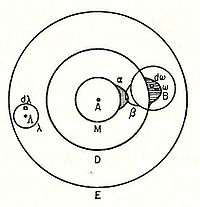 Схема Больцмана 1898 года молекулы I2, показывающая атомную «чувствительную область» (α, β) перекрывания.
Схема Больцмана 1898 года молекулы I2, показывающая атомную «чувствительную область» (α, β) перекрывания.В начале 20-го века американский химик Гильберт Ньютон Льюис, когда преподавал студентам Гарварда, чтобы представлять электроны вокруг атомов, стал символически изображать их точками. Его ученики отдавали предпочтение этим рисункам, что стимулировало его в этом направлении. Из этих лекций Льюис отметил, что элементы с определенным количеством электронов, по-видимому, обладают особой стабильностью. Этот феномен был отмечен немецким химиком Ричардом Абеггом[en] в 1904 году, на который Льюис ссылался как на «закон валентности Абега» (ныне широко известный как правило Абегга[en]). Льюису казалось, что как только вокруг ядра образуется ядро из восьми электронов, слой заполняется и начинается новый слой. Льюис также отметил, что различные ионы с восемью электронами также, по-видимому, обладают особой стабильностью. Исходя из этих взглядов, он предложил «правило восьми» или «правило октета»: ионы или атомы с заполненным слоем из восьми электронов обладают особой стабильностью.
Более того, заметив, что куб имеет восемь углов, Льюис представил себе атом как имеющий восемь сторон, доступных для электронов, подобно углу куба. Впоследствии, в 1902 году, он разработал концепцию, в которой кубические атомы могут соединяться на своих сторонах, образуя кубически структурированные молекулы.
Другими словами, электронно-парные связи образуются, когда два атома имеют общую границу, как в структуре С (ниже). Это приводит к разделению двух электронов. Аналогично, заряженные ионные связи образуются при переносе электрона из одного куба в другой, не разделяя ребра A. промежуточное состояние B, в котором разделяется только один угол, также было постулировано Льюисом.
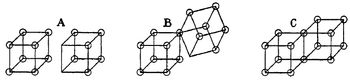 Кубические атомы Льюиса, образующие кубические молекулы
Кубические атомы Льюиса, образующие кубические молекулыСледовательно, двойные связи образуются при совместном использовании грани между двумя кубическими атомами. Это приводит к разделению четырех электронов.
В 1913 году, работая заведующим кафедрой химии в Калифорнийском университете в Беркли, Льюис прочитал предварительный набросок статьи английского аспиранта Альфреда Лаука Парсона[en], который посещал Беркли в течение года. В этой статье Парсон предположил, что электрон – это не просто электрический заряд, но и небольшой магнит (или «Магнетон», как он его называл), и более того, что химическая связь возникает в результате совместного использования двух электронов между двумя атомами. А уже это, согласно Льюису, означало, что связывание происходит, когда два электрона образуют общий край между двумя полными кубами.
Исходя из этих взглядов, в своей знаменитой статье 1916 года «Атом и молекула» Льюис ввел «структуру Льюиса» для представления атомов и молекул, где точки представляют электроны, а линии – ковалентные связи. В этой статье он разработал концепцию электронно-парной связи, в которой два атома могут делиться от одного до шести электронов, образуя таким образом единственную электронную связь, одинарную, двойную, или тройную связь
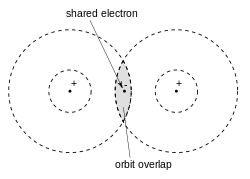 Иллюстрация химической связи по Льюису
Иллюстрация химической связи по ЛьюисуПо словам самого Льюиса:
 | Электрон может быть частью оболочки двух различных атомов, и нельзя сказать, что он принадлежит исключительно одному из них». |  |
Более того, он предположил, что атом имеет тенденцию образовывать ион, получая или теряя некоторое количество электронов, необходимых для завершения куба. Таким образом, структуры Льюиса показывают каждый атом в структуре молекулы, используя его химический символ. Линии рисуются между атомами, которые связаны друг с другом; иногда вместо линий используются пары точек. Избыточные электроны, образующие одиночные пары, представляются в виде пар точек и помещаются рядом с атомами, на которых они находятся:
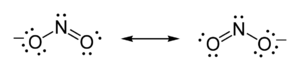 Точечные структуры Льюиса нитрит-иона
Точечные структуры Льюиса нитрит-ионаПодводя итог своим взглядам на новую модель связи, Льюис утверждает:
 | Два атома могут соответствовать «правилу восьми», или «правилу октета», не только путем переноса электронов от одного атома к другому, но и путем совместного использования одной или нескольких пар электронов… Два электрона, соединенные таким образом между двумя атомными центрами и удерживаемые вместе в оболочках двух атомов, я рассматривал как химическую связь. Таким образом, мы имеем конкретную картину этой физической сущности, того «крючка и глаза», который является частью убеждений химика-органика. |  |
На следующий год, в 1917 году, тогда ещё неизвестный американский инженер-химик по имени Лайнус Полинг изучал в Орегонском сельскохозяйственном колледже метод соединения «крючком и ушком» Дальтона, который в то время был актуальным описанием связей между атомами. Каждый атом имел определенное количество «крючков», которые позволяли ему прикрепляться к другим атомам, и определенное количество «ушек», которые позволяли другим атомам прикрепляться к нему. Химическая связь возникла, когда «крючок» и «ушко» соединились. Однако Л. Полинг не был удовлетворен этим архаичным методом и обратился за новым методом к недавно возникшей области знаний — квантовой физике.
В 1927 году немецкие физики Фриц Лондон и Вальтер Гайтлер применили методы квантовой механики для исследования насыщаемых, нединамических сил притяжения и отталкивания, т. е. их обработка валентной связи этой проблемы в их совместной работе была знаковой в том, что она привела химию к квантовой механике. Их работа оказала влияние на Л. Полинга, который только что получил докторскую степень и посетил В. Гайтлера и Ф. Лондона в Цюрихе на стипендии Гуггенгейма.
Впоследствии, в 1931 году, опираясь на работу В. Хайтлера и Ф. Лондона и на теории, найденные в знаменитой статье Г. Льюиса, Полинг опубликовал свою новаторскую статью «Природа химической связи», в которой он использовал квантовую механику для расчета свойств и структур молекул, таких как углы между связями и вращение вокруг связей. На основе этих концепций Л. Полинг разработал теорию гибридизации для учета связей в молекулах, таких как CH4, в которой четыре гибридизованные орбитали sp3 перекрываются орбиталями водорода 1s, образуя четыре σ-связи. Эти четыре связи имеют одинаковую длину и прочность, что дает молекулярную структуру, как показано ниже:
Схематическое представление гибридизованных орбиталей, перекрывающих орбитали атомов водородаБлагодаря этим уникальным теориям, Л. Полинг получил в 1954 году Нобелевскую премию по химии. Примечательно, что он был единственным человеком, который когда-либо выиграл две неразделенные Нобелевские премии, получив ещё Нобелевскую премию мира в 1963 году.
В 1926 году французский физик Жан Перрен получил Нобелевскую премию по физике за убедительное доказательство существования молекул. Он сделал это, вычислив число Авогадро с помощью трех различных методов, каждый из которых включали жидкофазные системы. Во-первых, он использовал мыльную эмульсию гиммигута, во-вторых, проводя экспериментальные работы по броуновскому движению, и в-третьих, подтверждая теорию Эйнштейна о вращении частиц в жидкой фазе.
Атомно-молекулярная теория базируется на следующих законах и утверждениях:
- Все вещества состоят из атомов
- Атомы одного химического вещества (химический элемент) обладают одинаковыми свойствами, но отличаются от атомов другого вещества
- При взаимодействии атомов образуются молекулы (гомоядерные — простые вещества, гетероядерные — сложные вещества)
- При физических явлениях молекулы не изменяются, при химических происходит изменение их состава
- Химические реакции заключаются в образовании новых веществ из тех же самых атомов, из которых состояли исходные вещества
- Закон сохранения массы — масса веществ, вступающих в химическую реакцию, равна массе веществ, образующихся в результате реакции
- Закон постоянства состава (закон кратных отношений) — любое определенное химически чистое соединение независимо от способа его получения состоит из одних и тех же химических элементов, причем отношения их масс постоянны, а относительные числа их атомов выражаются целыми числами
- Аллотропия — существование одного и того же химического элемента в виде нескольких простых веществ, различных по строению и свойствам.
Вытекающие законы и положения[править | править код]
Согласно современным квантово-механическим представлениям, у атомов в молекуле более или менее неизменным остается только остов, то есть ядро и внутренние электронные оболочки, тогда как характер движения внешних (валентных) электронов коренным образом изменяется так, что образуется новая (как бы отдельная), молекулярная электронная оболочка, охватывающая всю молекулу (см. Химическая связь). В этом смысле никаких неизменных атомов в молекулах нет.
Доказательство существования атомов и молекул[править | править код]
Теории Левкипп и Демокрита об атомах не была подтверждена экспериментально, поскольку древние греки вообще не проводили экспериментов, они ставили размышления выше наблюдений.
Первый эксперимент, подтверждающий атомную природу вещества, был проведен лишь спустя 2000 лет. В 1662 г. ирландский химик Роберт Бойль (1627—1691) при сжатии воздуха в U-образной трубке под давлением столбика ртути обнаружил, что объем воздуха в трубке обратно пропорционален давлению:
- pV=Const{\displaystyle pV=Const}
Французский физик Эдм Мариотт (1620—1684) подтвердил это соотношение через 14 лет после Бойля и заметил, что оно выполняется только при постоянной температуре.
Результаты, полученные Бойлем Мариоттом, можно объяснить, только если признать, что воздух состоит из атомов, между которыми имеется пустое пространство. Сжатие воздуха обусловлено сближением атомов и уменьшением объема пустого пространства.
- Начала химии / Н.Е.Кузьменко.: В.В.Еремин, В.А.Попков. — М.: Лаборатория знаний, 2016. — 704 с. — ISBN 978-5-906828-17-0.
Биологические молекулы • Джеймс Трефил, энциклопедия «Двести законов мироздания»
Жизнь — таинственная, сложная, загадочная — не что иное как совокупность достаточно крупных молекул и довольно простых химических реакций. Если бы вам понадобилось конструировать крупные молекулы, вы пошли бы по одному из двух путей. Либо, как в кустарном ювелирном деле, вы стали строить каждую молекулу «с нуля», проделывая каждый раз уникальную работу. Либо — этот путь используется в современных строительных технологиях — вы бы изготовили набор простых молекул, из которых можно собирать самые разнообразные молекулы большего размера, сочетая модули тем или иным образом. Оказывается, именно такое модульное строение имеют биологические молекулы. Согласно теории эволюции, таким и должен был быть самой простой путь к крупным молекулам, поскольку в начале эволюционного процесса необходимость в конструировании очень сложных молекул отсутствовала. Со временем же могли добавляться новые модули, расширяя коллекцию крупных разнородных элементов, что вполне соответствует духу эволюции.
Белки
Основной структурной единицей белков являются молекулы аминокислот. Чтобы понять, что такое аминокислота, представьте себе совокупность атомов, у которых с одной стороны наружу выступает водород, с другой — соединенные между собой кислород и водород, а посередине расположены разнообразные другие компоненты. Подобно тому как бусины нанизываются на нить, из этих аминокислот собираются белки — ион водорода (Н+) одной аминокислоты объединяется с ионом гидроксила (ОН–) другой аминокислоты с образованием молекулы воды. (Представьте, как каждый раз при соединении двух аминокислотных молекул между ними пробегает капелька воды.) Среди белков самую важную роль играют белки-ферменты (см. Катализаторы и ферменты), регулирующие химические реакции в клетках; но белки также являются важными структурными компонентами живых организмов. Например, ваши волосы и ногти состоят из белков.
Углеводы
Углеводы содержат кислород, водород и углерод в соотношении 1:2:1. Во многих живых системах молекулы углеводов выполняют роль источников энергии. Одним из важнейших углеводов можно считать сахар глюкозу, содержащую шесть атомов углерода (С6Н12О6). Глюкоза — конечный продукт фотосинтеза и, следовательно, основа всей пищевой цепи в биосфере. Соединяя молекулы глюкозы, как основные строительные модули, можно получить сложные углеводы. Как и белки, углеводы играют вспомогательную роль в клетках, поскольку входят в клеточные структуры. Например, растительные волокна состоят из целлюлозы, которая представляет собой вереницу сцепленных особым образом молекул глюкозы.
Липиды
Липиды — это нерастворимые в воде органические молекулы. Вы получите правильное представление о липидах, если вообразите капельки жира, плавающие на поверхности бульона. В живых организмах липиды выполняют две важные функции. Один класс молекул — фосфолипиды — состоят из маленькой головки, содержащей фосфатную группу (атом фосфора, соединенный с четырьмя атомами кислорода), и длинного углеводородного хвоста. Углеводородный хвост этой молекулы гидрофобен, то есть энергетическое состояние молекулы минимально, когда этот хвост находится не в воде. Напротив, фосфатная головка гидрофильна, то есть энергетическое состояние молекулы минимально при контакте головки с водой . Если поместить молекулы фосфолипидов в воду, они будут стремиться достичь минимального энергетического состояния и выстроятся таким образом, что их хвосты окажутся вместе, а головки — врозь. Такая двухслойная структура очень стабильна, поскольку головки будут в контакте с водой, но вода будет вытеснена из области, окружающей хвосты молекул. Для перемещения липидным молекулам необходима энергия — либо чтобы удалить гидрофильные участки из воды, либо чтобы поместить в воду гидрофобные участки. Из таких липидных двухслойных структур состоят клеточные мембраны и мембраны, разделяющие компоненты клетки. Эти пластичные и прочные молекулы отделяют живое от неживого.
Кроме того, в липидах запасается энергия. Липиды могут накапливать примерно вдвое больше энергии на единицу массы, чем углеводы. Вот почему, когда вы переедаете и ваш организм хочет запасти энергию на случай непредвиденных обстоятельств в будущем, когда пищи не будет, он станет запасать ее в форме жира. На этом простом факте строится многомиллиардная индустрия диетических продуктов.
Нуклеиновые кислоты
Молекулы ДНК и РНК (см. Центральная догма молекулярной биологии) переносят информацию о химических процессах, идущих в клетке, и участвуют в передаче содержащейся в ДНК информации в цитоплазму клетки. В ДНК живого организма закодированы белки-ферменты, которые катализируют все химические реакции, происходящие в этом организме.
Молекулы-переносчики энергии
Жизнедеятельность требует затрат энергии. В частности, нужно, чтобы энергия, произведенная в одном месте, могла быть использована в другом. Эту функцию в клетке осуществляет целая армия специализированных молекул. Пожалуй, самые важные из них — аденозин трифосфат (АТФ) и аденозин дифосфат (АДФ). Обе молекулы устроены так: группа из атомов углерода, водорода и азота (она называется аденин) присоединена к молекуле рибозы (это сахар), и все это вместе крепится к хвосту из фосфатов. Из названий молекул понятно, что в хвосте АДФ содержится два фосфата, а в хвосте АТФ — три. Когда в клетке происходит химический процесс, например фотосинтез, образующаяся энергия идет на присоединение третьего фосфата к хвосту АДФ. Полученная молекула АТФ затем переносится в другие части клетки. Там запасенная энергия может быть использована в других химических процессах: она выделяется при отщеплении последнего фосфата от АТФ, в результате чего АТФ вновь превращается в АДФ.
Как мы уже упоминали, существуют и другие молекулы, которые переносят энергию в клетке. Набор таких молекул чем-то напоминает разные варианты оплаты счетов. Вы можете выбрать наличные, банковский перевод, кредитную карту и т. д. — в зависимости от того, какой способ вам удобнее. Так же и клетка для поддержания своей жизнедеятельности может использовать АТФ (эквивалент наличных денег) или любую другую из большого набора более сложных молекул.
См. также:
Урок 3. Схема образования молекул – HIMI4KA
В уроке 3 «Схема образования молекул» из курса «Химия для чайников» выясним из чего состоят молекулы и как образуется ковалентная химическая связь; кроме того рассмотрим структурную и молекулярную формулы молекулы; научимся вычислять относительную молекулярную массу веществ. Настоятельно рекомендую перед тем, как приступить к прочтению данного урока, внимательно изучить предыдущие, так как они содержат необходимые основы химии для начинающих и буду весьма полезны в изучении курса. Напомню, что в прошлом уроке мы обсуждали изотопы элементов.


Молекулы состоят из атомов
Здесь все просто и понятно: все вещества во вселенной состоят из молекул, в свою очередь молекулы состоят из атомов, а атомы состоят из положительно заряженного ядра и электронных оболочек, на которых расположены отрицательно заряженные электроны.

Представьте, что два атома достаточно сблизились друг с другом. В таком случае электроны на внешней оболочке одного атома начинают взаимодействовать с внешними электронами другого. Подобное взаимодействие внешних электронов и образует молекулы, так как оно способно удерживать взаимодействующие атомы вместе, притягивая их друг к другу.
Связь атомов в молекулах
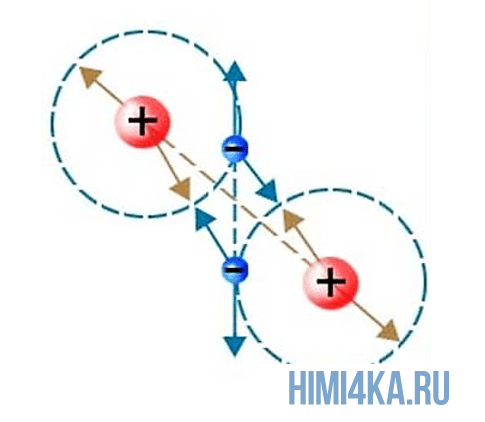

Как было сказано выше, образование молекул происходит из-за внешних электронов взаимодействующих атомов, так как они создают силы притяжения между ними. Когда образуются данные силы притяжения происходит образование химической связи. В природе существует несколько видов химической связи атомов в молекулах, но пока рассмотрим простейший из них.
Ковалентная химическая связь
Химическая связь, возникающая при обобществлении внешних электронов взаимодействующих атомов, называется ковалентной химической связью. Обобществленные электроны называются электронной парой. Объяснение ковалентной химической связи простыми словами: два атома положили в общую копилку по монетке (электрону) и схватились за нее «руками», причем оба атома не хотят отдавать копилку друг другу, поэтому так и продолжают держаться за нее.
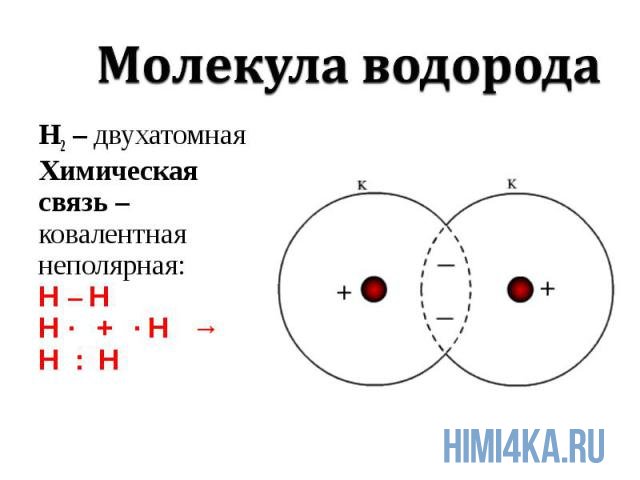

Ковалентная химическая связь подразделяется на два вида: неполярную и полярную. В этом уроке рассмотрим ковалентную неполярную химическую связь, которая возникает, когда в состав молекулы входят два абсолютно одинаковых атома неметалла, потому как одинаковые атомы владеют электронной парой в равной степени. А «Неполярная» — означает что заряд атомов не изменился, после образовании ковалентной связи. Приведем примеры молекул, образованных ковалентной неполярной химической связью: H2, O2, N2, Cl2. В редких случаях ковалентная химическая связь может образовываться между атомами разных неметаллов, но подробнее об этом в следующем уроке, где мы изучим электроотрицательность, и вам станет понятнее механизм образования химических связей атомов в молекулах.
Молекулярная и структурная формула
Графическое изображение структуры молекулы называется структурной формулой. Обычно ковалентная химическая связь в структурных формулах молекул изображается прямой линией, которая соединяет связанные атомы.
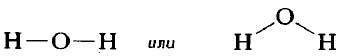
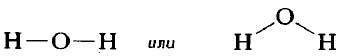
Структурную формулу молекулы воды H2O, к примеру, изображают двумя способами. Второй вариант структурной формулы воды, учитывает тот факт, что на самом деле молекула воды не линейна; две связи Н—О образуют угол 105° друг с другом. Молекулы газообразного водорода, сероводорода, аммиака, метана и метанола (метилового спирта) имеют следующие структурные формулы:
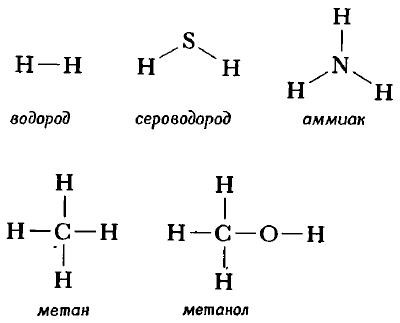

Структурная формула молекулы лишь схематично изображает связи между атомами, но не дает информации о реальной форме молекулы. Заметим, что угол между связями в молекулах, содержащих более двух атомов, может принимать различные значения. Так, угол между связями в молекуле воды равен 105°, а угол в молекуле сероводорода равен 92°; четыре атома, присоединенных к центральному атому углерода в метане и метаноле, направлены к четырем вершинам тетраэдра. Структурная формула неразветвленного октана, одного из компонентов бензина, такова:
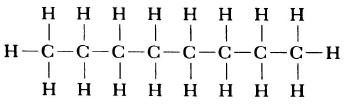
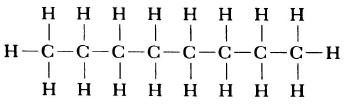
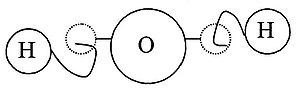
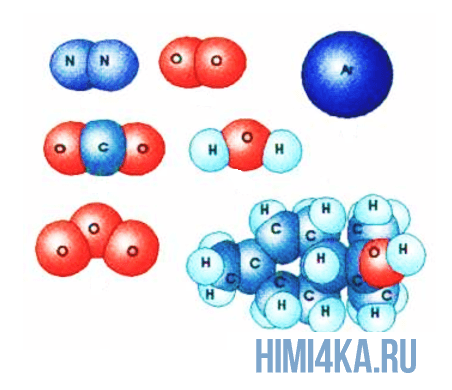
Изображение ниже дает более реальное представление о форме и относительном объеме некоторых простых молекул. Каждая пара связанных атомов как бы проникает друг в друга, потому что их электронные облака перекрываются между собой. Принято изображать молекулы таким образом, что расширяющаяся линия указывает связь, направленную от плоскости рисунка в сторону наблюдателя, а пунктирная линия указывает связь, уходящую за плоскость рисунка в сторону от наблюдателя.
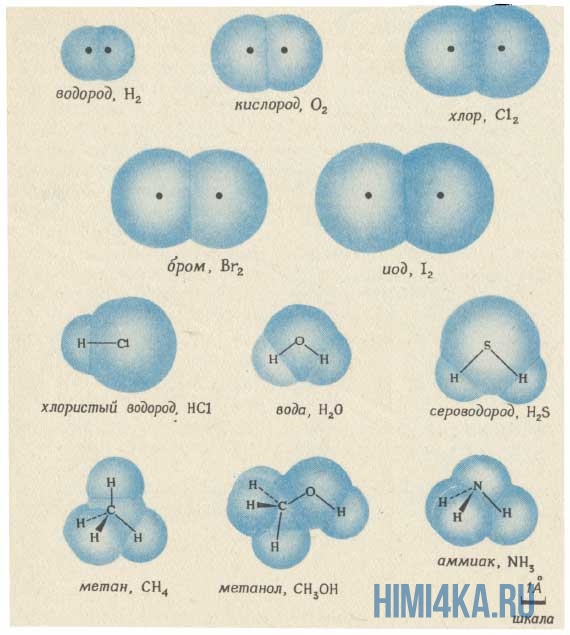

Каждая из указанных выше структурных формул может быть сведена к сжатой молекулярной формуле, которая указывает, сколько атомов каждого элемента имеется в молекуле, но совсем или почти совсем не дает сведений о том, как эти атомы соединены между собой. Молекулярная формула водорода Н2, воды Н2O, сероводорода H2S, аммиака NH3, метана СН4, метанола (метилового спирта) СН3ОН или СН4O, а октана С8Н18. Формула октана может быть также записана в такой форме:
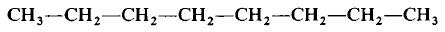
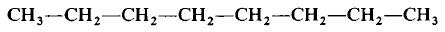
Относительная молекулярная масса вещества
Под молекулярной массой вещества понимается масса молекулы, вычисленная через сумму всех атомных масс, входящих в нее атомов; измеряется, как и атомная масса, в а.е.м. Если молекулярную массу вещества вычислять через относительные атомные массы, то и называться масса молекулы будет относительной молекулярной массой вещества. Относительная молекулярная масса — величина безразмерная.
Пример 1: Какая относительная молекулярная масса у воды?
Решение: Заходим в таблицу Менделеева и выписываем относительные атомные массы водорода и кислорода, округляя до целого значения. У водорода = 1, а у кислорода = 16. Так как молекулярная формула воды имеет вид H2O, то ее молекулярная масса равна:
Ответ: относительная молекулярная масса воды равна 18.
Пример 2: Вычислите молекулярную массу метанола (метилового спирта).
Решение: Молекулярная формула метанола СН3ОН или СН4O. Следовательно,
- 1 углерод: 1 × 12,011 а.е.м. = 12,011 а.е.м.
- 4 водорода: 4 × 1,008 а.е.м. = 4,032 а.е.м.
- 1 кислород: 1 × 15,999 а.е.м. = 15,999 а.е.м.
Ответ: Суммарная молекулярная масса равна 32,04 а.е.м.
В примере 2 следует обратить внимание на то, что естественная атомная масса углерода равна не 12,000, а 12,011 а.е.м., поскольку природный углерод представляет собой смесь, содержащую 98,89% углерода-12 и 1,11% углерода-13, а также следы углерода-14.
Пример 3: Чему равна молекулярная масса чистого октана?
Решение: Молекулярная формула октана С8Н18, поэтому его молекулярная масса равна
- (8 × 12,011) + (18 × 1,008) = 114,23 а.е.м.
Надеюсь урок 3 «Схема образования молекул» был понятным и познавательным. Если у вас возникли вопросы, пишите их в комментарии.
Атомно — молекулярная теория
Атомно-молекулярное учение – совокупность положений, аксиом и законов, которые описывают все вещества как набор молекул, состоящих из атомов.
 Древнегреческие философы задолго до начала нашей эры в своих трудах уже выдвигали теорию существования атомов. Отвергая существование богов и потусторонних сил, они пытались объяснить все непонятные и загадочные явления природы естественными причинами – соединением и разъединением, взаимодействием и смешиванием невидимых человеческому глазу частичек – атомов. Но служители церкви на протяжении многих веков преследовали приверженцев и последователей учения об атомах, подвергали их гонениям. Но из-за отсутствия необходимых технических приспособлений философы древности не могли скрупулезно изучить природные явления, и под понятием «атом» у них скрывалось современное понятие «молекула».
Древнегреческие философы задолго до начала нашей эры в своих трудах уже выдвигали теорию существования атомов. Отвергая существование богов и потусторонних сил, они пытались объяснить все непонятные и загадочные явления природы естественными причинами – соединением и разъединением, взаимодействием и смешиванием невидимых человеческому глазу частичек – атомов. Но служители церкви на протяжении многих веков преследовали приверженцев и последователей учения об атомах, подвергали их гонениям. Но из-за отсутствия необходимых технических приспособлений философы древности не могли скрупулезно изучить природные явления, и под понятием «атом» у них скрывалось современное понятие «молекула».
Лишь в середине ХVIII века великий русский учёный М.В. Ломоносов обосновал атомно-молекулярные представления в химии. Основные положения его учения изложены в работе «Элементы математической химии» (1741 г.) и ряде других. Ломоносов назвал теорию корпускулярно-кинетической теорией.
М.В. Ломоносов четко разграничивал две ступени в строении вещества: элементы (в современном понимании – атомы) и корпускулы (молекулы). В основе его корпускулярно-кинетической теории (современного атомно-молекулярного учения) лежит принцип прерывности строения (дискретности) вещества: любое вещество состоит из отдельных частиц.
 В 1745 году М.В. Ломоносов писал: «Элемент есть часть тела, не состоящая из каких-либо меньших и отличных между собою тел… Корпускулы есть собрание элементов в одну небольшую массу. Они однородны, если состоят из одинакового числа одних и тех же элементов, соединённых одинаковым образом. Корпускулы разнородны, когда элементы их различны и соединены различным образом или в различном числе; от этого зависит бесконечное разнообразие тел.
В 1745 году М.В. Ломоносов писал: «Элемент есть часть тела, не состоящая из каких-либо меньших и отличных между собою тел… Корпускулы есть собрание элементов в одну небольшую массу. Они однородны, если состоят из одинакового числа одних и тех же элементов, соединённых одинаковым образом. Корпускулы разнородны, когда элементы их различны и соединены различным образом или в различном числе; от этого зависит бесконечное разнообразие тел.
Молекула является наименьшей частицей вещества, обладающей всеми его химическими свойствами. Вещества, имеющие молекулярную структуру, состоят из молекул (большинство неметаллов, органические вещества). Значительная часть неорганических веществ состоит из атомов (атомная решётка кристалла) или ионов (ионная структура). К таким веществам относятся оксиды, сульфиды, различные соли, алмаз, металлы, графит и др. Носителем химических свойств в этих веществах является комбинация элементарных частиц (ионы или атомы), то есть кристалл представляет собой гигантскую молекулу.
Молекулы состоят из атомов. Атом – мельчайшая, далее химически неделимая составная часть молекулы.
Получается, молекулярная теория объясняет физические явления, которые происходят с веществами. Учение об атомах приходит на помощь молекулярной теории при объяснении химических явлений. Обе эти теории – молекулярная и атомная – объединяются в атомно-молекулярное учение. Сущность этого учения можно сформулировать в виде нескольких законов и положений:
- вещества состоят из атомов;
- при взаимодействии атомов образуются простые и сложные молекулы;
- при физических явлениях молекулы сохраняются, их состав не изменяется; при химических – разрушаются, их состав изменяется;
- молекулы веществ состоят из атомов; при химических реакциях атомы в отличие от молекул сохраняются;
- атомы одного элемента сходны друг с другом, но отличаются от атомов любого другого элемента;
- химические реакции заключаются в образовании новых веществ из тех же самых атомов, из которых состояли исходные вещества.
Благодаря своей атомно-молекулярной теории М.В. Ломоносов по праву считается родоначальником научной химии.
© blog.tutoronline.ru, при полном или частичном копировании материала ссылка на первоисточник обязательна.

