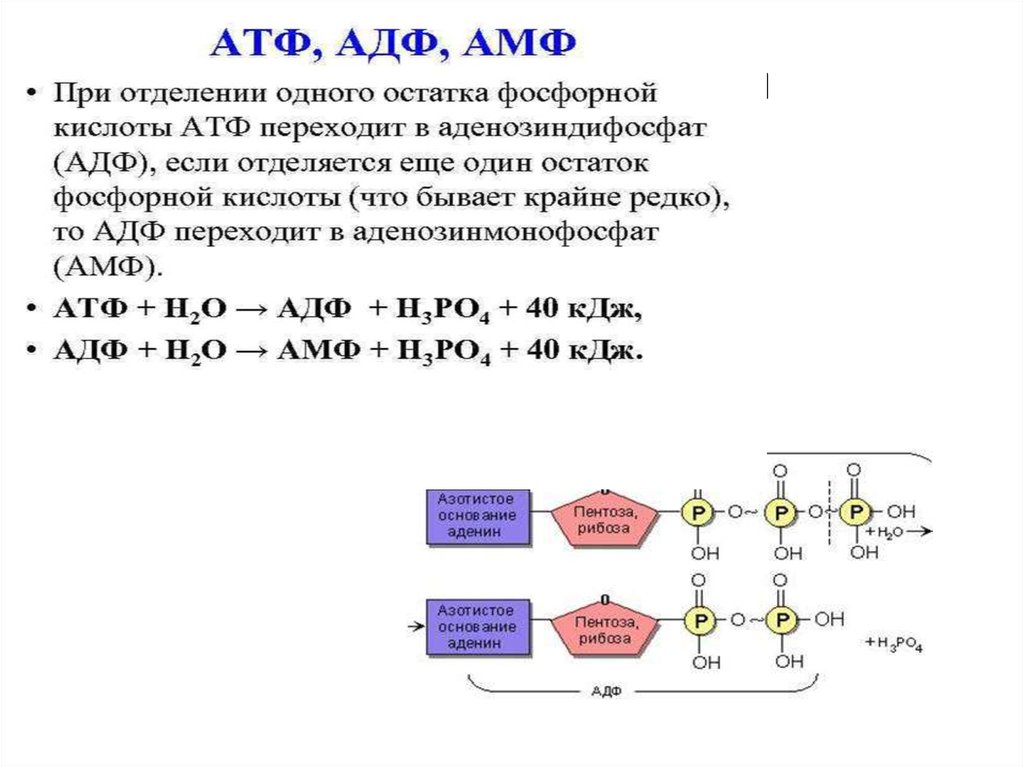
распад молекулы
Этот процесс сам по себе может привести к распаду молекулы жирной кислоты (очередная реакция со свободным радикалом, отделение водорода, образование перекиси жирной кислоты), но он еще и ускоряется за счет того, что перекисный радикал липида (перекись жирной кислоты), реагируя с другой молекулой жирной кислоты, образует ее перекись И — ООН и новый свободный липидный радикал (свободный радикал жирной кислоты). Цепная реакция продолжается до полного переокисления жирной кислоты. В течение этого процесса в среде постоянно присутствуют свободные радикалы, которые могут вступать в реакцию с ненасыщенными жирными кислотами.[ …]
Совокупность процессов поглощения кванта и распада молекулы называют фотодиссоциацией. Энергия связи атомов в молекулах различных атмосферных газов может быть рассчитана с помощью термодинамической характеристики — энтальпии образования А Я®, приводимой во многих справочных изданиях.[ …]
Пламя горелки является атомизатором, в нем происходит распад молекул анализируемого вещества до свободных атомов. Анализируемое вещество в виде раствора подается в пламя горелки с помощью пневматического распылителя.[ …]
Анализируемое вещество в виде раствора подается в пламя горелки с помощью пневматического распылителя.[ …]
В обычных условиях вода достаточно устойчивое соединение. Распад молекул воды (термическая диссоциация) становится заметным лишь выше 1500°С. Разложение воды происходит также под действием ультрафиолетового (фотодиссоциации) или радиоактивного излучения (радиолиза). При радиолизе воды кроме Ш и Ог образуется также перекись водорода и ряд свободных радикалов.[ …]
Давайте подсчитаем, может ли в действительности происходить распад молекул воды на составные атомы при ураганном ветре, скорость которого приближается -к 200 км/ч… Чтобы ответить на этот вопрос, прежде всего необходимо узнать, какую энергию надо приложить к молекуле воды, чтобы получить желанный эффект, т. е. разложить ее на водород и кислород. Величина эта называется энергией диссоциации молекулы воды. Она должна быть равной той энергии, которая выделяется при сгорании молекулы водорода в кислороде.[ … ]
]
В живой микробиальной клетке непрерывно и одновременно протекают два процесса — распад молекул (катаболизм) и их синтез (анаболизм), составляющие в целом процесс обмена веществ — метаболизм. Иными словами, процессы деструкции потребляемых микроорганизмами органических соединений неразрывно связаны с процессами биосинтеза новых микробиальных клеток, различных промежуточных или конечных продуктов, на проведение которых расходуется энергия, получаемая микробиальной клеткой в результате потребления питательных веществ. Источником питания для гетеротрофных микроорганизмов являются углеводы, жиры, белки, спирты и т.д., которые могут расщепляться ими либо в аэробных, либо в анаэробных условиях. Значительная часть продуктов микробной трансформации может выделяться клеткой в окружающую среду или накапливаться в ней. Некоторые промежуточные продукты служат питательным резервом, который клетка использует после истощения основного питания.[ …]
В дизелях углеводороды образуются в переобога-щенных зонах, где происходит пиролиз молекул топлива (распад молекул топлива под действием высоких температур при отсутствии химических реагентов). Если в процессе расширения в эти зоны не поступит достаточное количество кислорода, то СН окажется в составе ОГ. При значительном содержании легких СН в ОГ при запуске и прогреве двигателя на выпуске наблюдается белый дым. Углеводороды могут выбрасываться в атмосферу вследствие пропусков воспламенения, негерметичности выпускного клапана или системы вентиляции картера, а также из-за испарения бензина в топливном баке и карбюраторе.[ …]
Если в процессе расширения в эти зоны не поступит достаточное количество кислорода, то СН окажется в составе ОГ. При значительном содержании легких СН в ОГ при запуске и прогреве двигателя на выпуске наблюдается белый дым. Углеводороды могут выбрасываться в атмосферу вследствие пропусков воспламенения, негерметичности выпускного клапана или системы вентиляции картера, а также из-за испарения бензина в топливном баке и карбюраторе.[ …]
Что же касается самой воды, то она тоже в известной .степени подвержена диссоциации, т. е. распаду молекул на ионы. При этом молекула воды распадается не на 2 иона водорода и 1 ио« кислорода, а на 1 ион водорода й 1 гидроксильный ион ОН.[ …]
РАДИКАЛЫ СВОБОДНЫЕ [лат. radicalis коренной] — электрически нейтральные неустойчивые осколхи молекул, представляющие собой группы атомов или отдельные атомы, обладающие свободной валентностью (напр., не соединенные в молекулы атомы водорода Н, кислорода О, азота N, группы атомов СНз, С2Н5). Р. с. образуются при диссоииаиии (распаде) молекул, происходящей под воздействием высоких температур, некоторых видов излучения и других причин; процесс, как правило, сопровождается значительным поглощением энергии извне. При воссоединении Р. с. в молекулы эта энергия выделяется.[ …]
При воссоединении Р. с. в молекулы эта энергия выделяется.[ …]
Газ с резким запахом, сгущается в светло-желтую жидкость при —188 °С и затвердевает при —220°С. Распад молекул Р2 на отдельные атомы осуществляется легко. Фтор используют главным образом при фторировании органических соединений.[ …]
С другой стороны, поскольку время испарения х растет с увеличением радиуса, в то время как время распада молекул вещества не должно зависеть от радиуса, следует ожидать, что шаровые молнии больших размеров должны жить в среднем дольше, чаще доживая до своего предельного срока жизни. В этом случае должна наблюдаться положительная корреляция между размерами шаровой молнии и временем ее жизни. Вопрос о том, существует ли такая корреляция, будет рассмотрен в следующем параграфе этой главы.[ …]
Согласно этой гипотезе процесс образования левоглюкозана при термолизе целлюлозы в вакууме состоит из распада молекулы целлюлозы по 1,4-р-глюкозидным связям и последующей изомеризации полученного фрагмента цепи в молекулу левоглюкозана. [ …]
[ …]
При облучении О-глюцитола в водном растворе ультрафиолетовым светом ртутной лампы среднего давления происходит распад молекулы, при этом длительное облучение полностью превращает первоначальный продукт в двуокись углерода [55].[ …]
Наиболее благоприятные условия протекания этой реакции находятся в пределах озонового слоя атмосферы, где в процессе распада молекул озона на О и 02 генерируется атомарный кислород. В результате в стратосфере на высоте порядка 18 км присутствует слой с высокой концентрацией 803.[ …]
Полнота использования озона возрастает по мере увеличения концентрации фенола в растворе, так как при этом повышается вероятность взаимодействия реагирующих веществ до момента распада молекулы озона.[ …]
Выполненный расчет имеет ориентировочный характер, но все же он убедительно свидетельствует, что еще рано говорить о разгадке тайны «красных волн». Если такие волны действительно есть, то распад молекул воды в них происходит за счет какого-то другого физического явления. Рассмотрим один из возможных механизмов.[ …]
Рассмотрим один из возможных механизмов.[ …]
Некоторые неорганические препараты могут выноситься из почвы только растениями. Органические соединения, находящиеся в почве, способны разлагаться на простейшие вещества практически с полным распадом молекулы. Некоторые органические: соединения с высоким давлением паров могут испаряться с поверхности почвы в атмосферу и подвергаться фотохимическому разложению или окислению под влиянием солнечного света. На скорость испарения препаратоЕ; существенное влияние оказывает скорость движения воздуха над поверхностью почвы и состав почвы. Некоторые пестициды, например производные тио- и дитиофосфорной и фосфоновой кислот, а также молекулы пестицидов, содержащих сульфидные и другие легко окисляющиеся группы, окисляются кислородом воздуха Значительную роль в разрушении химических соединений в почве играют растения. На рис. 1У-2 показаны пути естественного обезвреживания пастицидов в окружающей среде.[ …]
Меченый азот в конституционных и запасных белках корней был обнаружен уже при 2-часовой экспозиции растений на 1М15, что указывает на исключительно высокую скорость вовлечения внесенного источника азота в белковые молекулы корней растений. В конституционных белках зеленых листьев меченый азот был обнаружен через 8 часов после внесения меченой азотной подкормки. Таким образом, в условиях этого опыта весь путь превращений азота в растении, начиная от поступления его из почвы и кончая включением его в состав белковой молекулы листьев растений, был пройден в течение 8 часов. Как видно из данных изотопного анализа, в зеленой массе ржи происходило непрерывное обновление азотистого состава белка и хлорофилла. Масштаб этого процесса в несколько раз превосходил интенсивность новообразования белка и хлорофилла (,новообразования, приводящего к увеличению общей ¡массы белка и хлорофилла в растении). Поэтому с достаточным основанием можно считать, что обновление белка и хлорофилла в этом опыте, так же как и в рассмотренном выше опыте с овсом, в основном обусловлено самопроизвольным частичным или полным распадом молекулы белка или пиррольного ядра хлорофилла с одновременно протекающим процессом их воссоздания. В корнях ржи интенсивность обновления белка значительно ниже, чем в зеленой массе, что указывает на существенное различие в белковом обмене корней и зеленых частей растений.
В конституционных белках зеленых листьев меченый азот был обнаружен через 8 часов после внесения меченой азотной подкормки. Таким образом, в условиях этого опыта весь путь превращений азота в растении, начиная от поступления его из почвы и кончая включением его в состав белковой молекулы листьев растений, был пройден в течение 8 часов. Как видно из данных изотопного анализа, в зеленой массе ржи происходило непрерывное обновление азотистого состава белка и хлорофилла. Масштаб этого процесса в несколько раз превосходил интенсивность новообразования белка и хлорофилла (,новообразования, приводящего к увеличению общей ¡массы белка и хлорофилла в растении). Поэтому с достаточным основанием можно считать, что обновление белка и хлорофилла в этом опыте, так же как и в рассмотренном выше опыте с овсом, в основном обусловлено самопроизвольным частичным или полным распадом молекулы белка или пиррольного ядра хлорофилла с одновременно протекающим процессом их воссоздания. В корнях ржи интенсивность обновления белка значительно ниже, чем в зеленой массе, что указывает на существенное различие в белковом обмене корней и зеленых частей растений. Но особенно интересные данные в этом опыте получены для запасных белков корней. Из приведенных в таблице 5 данных химического анализа следует, что содержание азота запасных белков в корнях интенсивно возрастает по мере удлинения экспозиции растений на меченой азотной подкормке. В то же время обновление азота этой фракции белка, вычисленное по данным изотопного анализа, начиная с первых двух часов экспозиции и до конца опыта, характеризуется сравнительно малой величиной.[ …]
Но особенно интересные данные в этом опыте получены для запасных белков корней. Из приведенных в таблице 5 данных химического анализа следует, что содержание азота запасных белков в корнях интенсивно возрастает по мере удлинения экспозиции растений на меченой азотной подкормке. В то же время обновление азота этой фракции белка, вычисленное по данным изотопного анализа, начиная с первых двух часов экспозиции и до конца опыта, характеризуется сравнительно малой величиной.[ …]
Представитель департамента науки и техники Индии Н. Р. Криш-нан высказал следующее предположение: энергия циклона была настолько велика, что, возможно, временами при скорости ветра в 200 км в час, при грозе и урагане происходил распад молекул воды на атомы кислорода и водорода, а электрические разряды воспламенили водород» ?2.[ …]
Радиационное обезвреживание токсичных примесей в разбавленных водных растворах или газах, содержащих пары воды, заключается в косвенном действии ионизирующего излучения на водные системы. Вначале в результате облучения при распаде молекул воды образуются активные свободные радикалы и ионы (ОН, Н, гидратированные электроны и др.). Затем эти активные частицы взаимодействуют с токсичными примесями и превращают их в безвредные продукты.[ …]
Вначале в результате облучения при распаде молекул воды образуются активные свободные радикалы и ионы (ОН, Н, гидратированные электроны и др.). Затем эти активные частицы взаимодействуют с токсичными примесями и превращают их в безвредные продукты.[ …]
Другие природные синтезы свободного кислорода тоже биогенного характера имеют несравненно меньшее значение и в общем балансе исчезают. Это количества другого порядка по массе. С одной стороны, малоизученные выделения свободного кислорода некоторыми нехлорофильными организмами [26], а с другой — выделение свободного кислорода в плавательных пузырях главным образом глубоководных рыб [27] (§ 149). Свободный кислород создается и вне влияния жизни под влиянием ультрафиолетовых лучей в стратосфере и в верхних частях тропосферы, точно также при радиоактивном распаде молекул воды, наблюдаемом всюду, где находятся в воде радий и мезоторий (§ 149). Но все эти процессы меркнут перед количеством свободного кислорода, который создается хлорофильной растительностью. [ …]
[ …]
Физики нащупали границу квантового и классического мира при распаде молекул стронция
Физика Химия Физики смогли
Сложность 6.9
S. Kondov et al. / Physical Review A
Американские физики определили, при каких условиях распад молекулы стронция Sr2 можно описать с помощью аппарата классической физики, а в каких уже нельзя обойтись без учета квантовых эффектов. Оказалось, что квантовые эффекты становятся существенными только при температуре, при которой вращательная энергия молекулы сравнима с энергией ее распада — диссоциации.
Обычно в химических реакциях участвует макроскопически много молекул, которые случайным образом сталкиваются и взаимодействуют друг с другом. Однако в последнее время физики научились так точно управлять атомами и молекулами, что смогли проводить реакции между отдельными частицами реагентов, охлажденных до очень низких температур. Например, в апреле этого года американские физики «собрали» молекулу NaCs из отдельных атомов натрия и цезия — для этого ученые захватывали и сталкивали частицы с помощью оптического пинцета. Это позволило ученым подробно исследовать эффекты, которые определяют ход химической реакции.
Как правило, для описания взаимодействия атомов, вовлеченных в химическую реакцию, ученые используют квазиклассическое приближение, разработанное в середине 1920-х годов Грегором Вентцелем, Хендриком Крамерсом и Леоном Бриллюэном (поэтому его иногда называют приближением ВКБ). Грубо говоря, в этом приближении молекула моделируется шариками-атомами, которые связаны «пружинкой» — химической связью, описываемой потенциалом взаимодействия. Если бы квазиклассическое приближение выполнялось, атомы диссоциировавшей («развалившейся») молекулы всегда бы разлетались в строго противоположные стороны. При больших температурах обычно так и происходит, однако при приближении к абсолютному нулю, когда тепловые колебания молекулы затухают, начинают играть роль более тонкие эффекты.
Грубо говоря, в этом приближении молекула моделируется шариками-атомами, которые связаны «пружинкой» — химической связью, описываемой потенциалом взаимодействия. Если бы квазиклассическое приближение выполнялось, атомы диссоциировавшей («развалившейся») молекулы всегда бы разлетались в строго противоположные стороны. При больших температурах обычно так и происходит, однако при приближении к абсолютному нулю, когда тепловые колебания молекулы затухают, начинают играть роль более тонкие эффекты.
В частности, в 2016 году группа ученых под руководством Тани Зелевински (Tanya Zelevinsky) показала, что диссоциацию молекулы Sr2, охлажденной до температуры порядка 50 микрокельвинов, нельзя объяснить, ограничиваясь квазиклассическим приближением — построенное учеными угловое распределение атомов стронция-88, разлетающихся после распада молекулы, выглядело сложнее, чем предсказывает эта модель. Это позволило физикам показать, что при низких температурах взаимодействие частиц определяется квантовыми эффектами — в частности, резонансным рассеянием и подбарьерным туннелированием.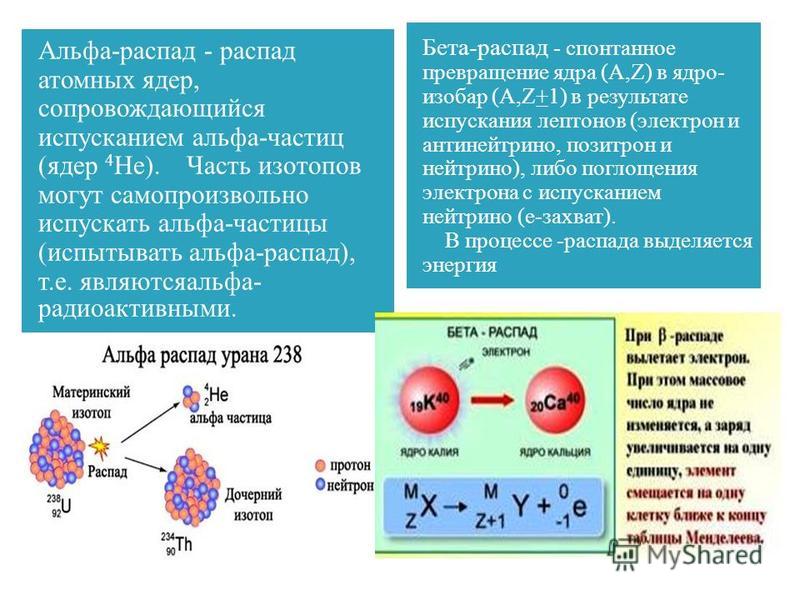
Два года спустя группа Зелевински вернулась к опыту с диссоциацией молекул стронция, чтобы изучить его более детально. Для этого ученые захватывали несколько тысяч молекул Sr
Перед распадом молекула могла находиться в одном из двух возбужденных состояний — либо в состоянии, в котором потенциал взаимодействия не имеет барьера (0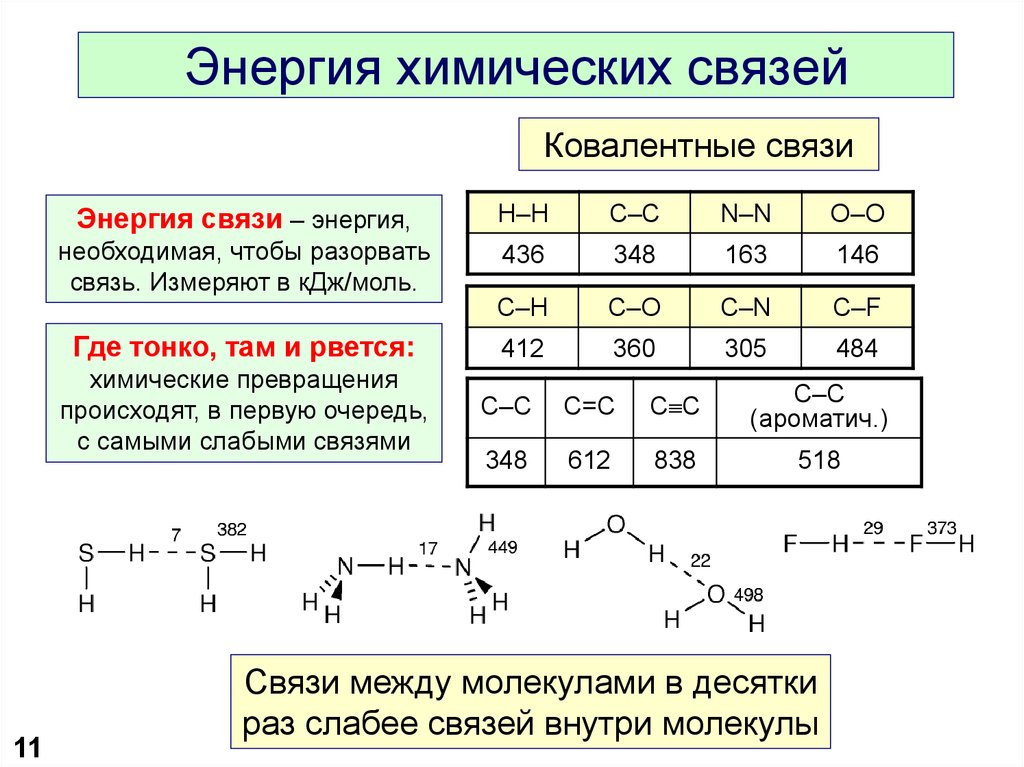 Кроме того, состояния могли иметь различные колебательные квантовые числа (vibrational quantum number). В зависимости от формы потенциала и значения квантового числа вид распределения немного изменялся. Наконец, исследователи сравнивали полученные распределения с теоретическими расчетами, выполненными в рамках «чистой» квантовой механики или метода ВКБ.
Кроме того, состояния могли иметь различные колебательные квантовые числа (vibrational quantum number). В зависимости от формы потенциала и значения квантового числа вид распределения немного изменялся. Наконец, исследователи сравнивали полученные распределения с теоретическими расчетами, выполненными в рамках «чистой» квантовой механики или метода ВКБ.
Угловое распределение атомов, образовавшихся при распаде возбужденной молекулы Sr
S. Kondov et al. / Physical Review A
Поделиться
Угловое распределение атомов, образовавшихся при распаде возбужденной молекулы Sr2, которая находилась в состоянии 1u.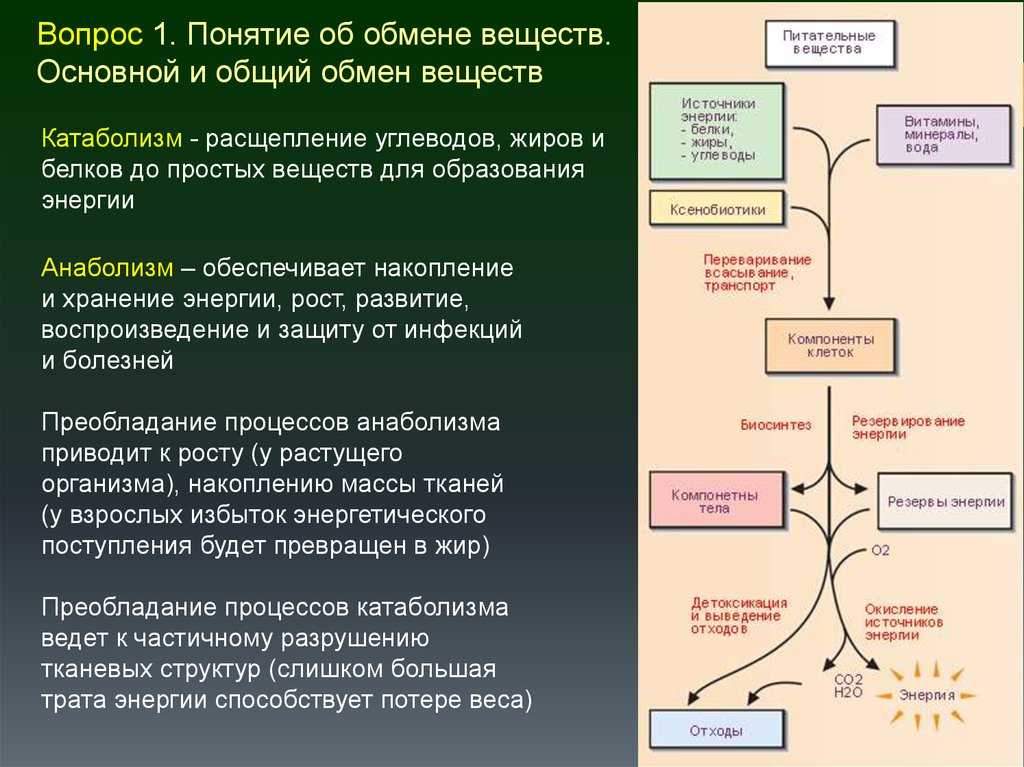
S. Kondov et al. / Physical Review A
Поделиться
В результате физики обнаружили, что квазиклассическое приближение достаточно хорошо описывает распад молекулы вплоть до температур порядка пяти кельвинов — при такой высокой температуре можно пренебречь квантовой статистикой, которой подчиняются атомы стронция, а потому оба метода дают примерно одинаковое распределение. Однако при снижении температуры метод ВКБ переставал работать, поскольку он упускал из вида волны рассеяния с нечетными значениями углового момента. По оценкам ученых, переломный момент наступает, когда вращательная энергия тепловых колебаний молекулы оказывается меньше, чем энергия ее диссоциации.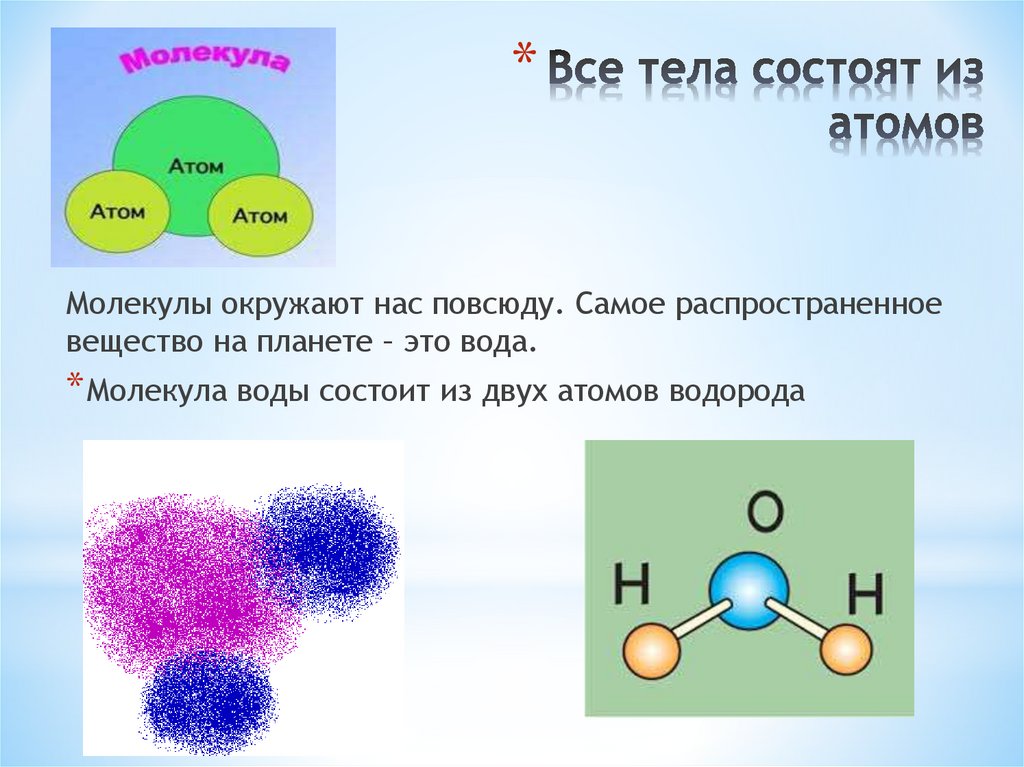
Сравнение углового распределения, измеренного в эксперимента (слева) с «честными» расчетами и расчетами с помощью метода ВКБ (справа). При высокой температуре (b) все три картинки совпадают, при низкой температуре (a) метод ВКБ дает направльное распределение
S. Kondov et al. / Physical Review A
Поделиться
Авторы статьи подчеркивают, что «классическая природа» траекторий, которые они наблюдали при большой температуре, обусловлена большой кинетической энергией атомов, а не усреднением по большому ансамблю. При большой температуре — следовательно, большой энергии вращения молекулы, — характерное время вращения во много раз превышает характерное время диссоциации, а потому для описания процесса можно использовать квазиклассическое приближение. Еще можно сказать, что при большой температуре энергия атомов много больше высоты потенциальных барьеров, а потому они преодолевают их практически беспрепятственно.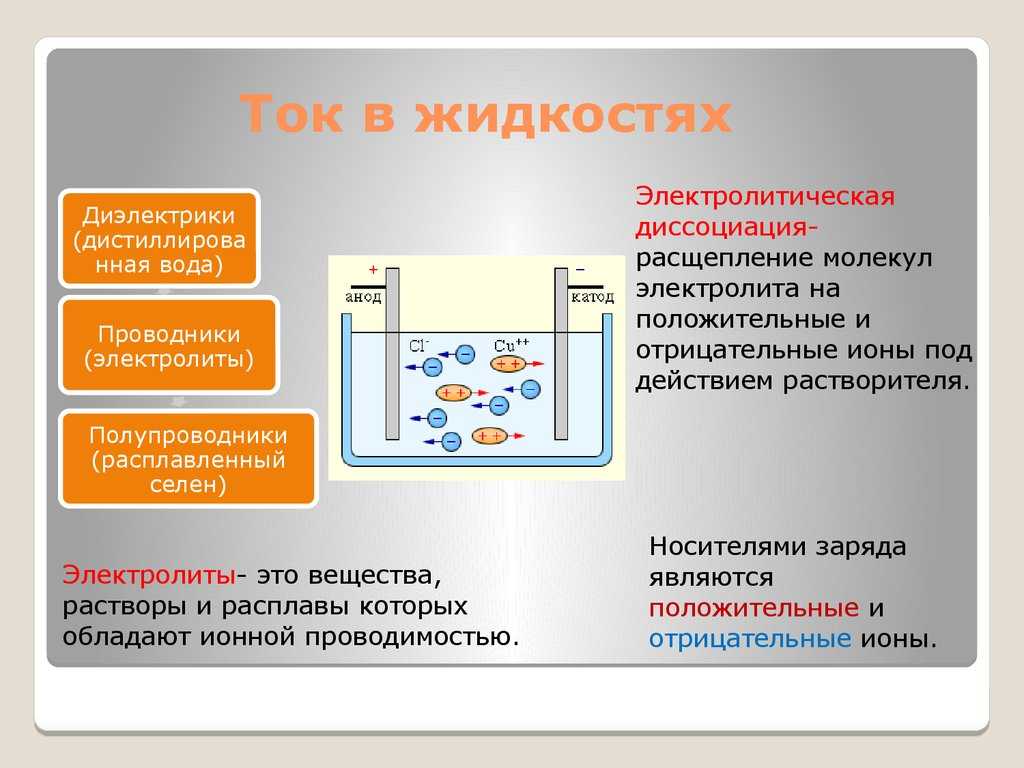
Вообще говоря, оптический пинцет, который группа Зелевински использовала для удерживания молекул, был придуман в середине 1980-х годов американским физиком Артуром Эшкиным. Изначально эта технология позволяла управлять только объектами микрометрового размера, однако в дальнейшем ученые увеличили ее точность в несколько тысяч раз. В настоящее время оптические пинцеты широко используются в биофизике и других областях науки для точного позиционирования мелких предметов. За эту разработку Шведская академия наук присудила вчера Артуру Эшкину Нобелевскую премию по физике. Подробнее про принцип работы оптического пинцета можно прочитать в материале «Скальпель и пинцет».
Дмитрий Трунин
Читайте также
Томские археологи обнаружили в Таре крупный православный некрополь XVII–XVIII века
Нобелевскую премию по физике присудили за квантовую запутанность
Нобелевскую премию по физиологии или медицине присудили за изучение древних людей
Человек, который собрал древних
Кто такой Сванте Паабо, лауреат Нобелевской премии по физиологии и медицине 2022 года
Энергия в клетке.
 Использование и хранение / Хабр
Использование и хранение / ХабрВсем привет! Эту статью я хотел посвятить клеточному ядру и ДНК. Но перед этим нужно затронуть то, как клетка хранит и использует энергию (спасибо spidgorny). Мы будем касаться вопросов связанных с энергией почти везде. Давайте заранее в них разберемся.
Из чего можно получать энергию? Да из всего! Растения используют световую энергию. Некоторые бактерии тоже. То есть органические вещества синтезируются из неорганических за счет световой энергии. + Есть хемотрофы. Они синтезируют органические вещества из неорганических за счет энергии окисления аммиака, сероводорода и др. веществ. А есть мы с вами. Мы — гетеротрофы. Кто это такие? Это те, кто не умеет синтезировать органические вещества из неорганических. То есть хемосинтез и фотосинтез, это не для нас. Мы берем готовую органику (съедаем). Разбираем ее на кусочки и либо используем, как строительный материал, либо разрушаем для получения энергии.
Что конкретно мы можем разбирать на энергию? Белки (сначала разбирая их на аминокислоты), жиры, углеводы и этиловый спирт (но это по желанию). То есть все эти вещества могут быть использованы, как источники энергии. Но для ее хранения мы используем жиры и углеводы. Обожаю углеводы! В нашем теле основным запасающим углеводом является гликоген.
То есть все эти вещества могут быть использованы, как источники энергии. Но для ее хранения мы используем жиры и углеводы. Обожаю углеводы! В нашем теле основным запасающим углеводом является гликоген.
Он состоит из остатков глюкозы. То есть это длинная, разветвленная цепочка, состоящая из одинаковых звеньев (глюкозы). При необходимости в энергии мы отщепляем по одному кусочку с конца цепи и окисляя его получаем энергию. Такой способ получения энергии характерен для всех клеток тела, но особенно много гликогена в клетках печени и мышечной ткани.
Теперь поговорим о жире. Он хранится в специальных клетках соединительной ткани. Имя им — адипоциты. По сути это клетки с огромной жировой каплей внутри.
При необходимости, организм достает жир из этих клеток, частично расщепляет и транспортирует. По месту доставки происходит окончательное расщепление с выделением и преобразованием энергии.
Довольно популярный вопрос: «Почему нельзя хранить всю энергию в виде жира, или гликогена?»
У этих источников энергии разное назначение. Из гликогена энергию можно получить довольно быстро. Его расщепление начинается почти сразу после начала мышечной работы, достигая пика к 1-2 минуте. Расщепление жиров протекает на несколько порядков медленней. То есть если вы спите, или медленно куда-то идете — у вас постоянный расход энергии, и его можно обеспечить расщепляя жиры. Но как только вы решите ускориться (упали сервера, побежали поднимать), резко потребуются много энергии и быстро ее получить расщепляя жиры не получится. Тут нам и нужен гликоген.
Есть еще одно важное различие. Гликоген связывает много воды. Примерно 3 г воды на 1 г гликогена. То есть, для 1 кг гликогена это уже 3 кг воды. Не оптимально… С жиром проще. Молекулы липидов (жиры=липиды), в которых запасается энергия не заряжены, в отличие от молекул воды и гликогена. Такие молекулы называется гидрофобными (дословно, боящимися воды). Молекулы воды же поляризованы. Примерно так это выглядит.
Молекулы воды же поляризованы. Примерно так это выглядит.
По сути, положительно заряженные атомы водорода взаимодействуют с отрицательно заряженными атомами кислорода. Получается стабильное и энергетически выгодное состояние.
Теперь представим молекулы липидов. Они не заряжены и не могут нормально взаимодействовать с поляризованными молекулами воды. Поэтому смесь липидов с водой энергетически невыгодна. Молекулы липидов не способны адсорбировать воду, как это делает гликоген. Они «кучкуются» в так называемые липидные капли, окружаются мембраной из фосфолипидов (одна их сторона заряжена и обращена к воде снаружи, вторая — не заряжена и смотрит на липиды капли). В итоге, у нас есть стабильная система, эффективно хранящая липиды и ничего лишнего.
Окей, мы разобрались с тем, в каких формах хранится энергия. А что с ней происходит дальше? Вот отщепили мы молекулу глюкозы от гликогена. Превратили ее в энергию. Что это значит?
Сделаем небольшое отступление.
В клетке происходит порядка 1.000.000.000 реакций каждую секунду. При протекании реакции одно вещество трансформируется в другое. Что при этом происходит с его внутренней энергией? Она может уменьшаться, увеличиваться или не меняться. Если она уменьшается -> происходит выделение энергии. Если увеличивается -> нужно взять энергию из вне. Организм обычно совмещает такие реакции. То есть энергия, выделившаяся при протекании одной реакции идет на проведение второй.
Так вот в организме есть специальные соединения, макроэрги, которые способны накапливать и передавать энергию в ходе реакции. В их составе есть одна, или несколько химических связей, в которых и накапливается эта энергия. Теперь можно вернуться к глюкозе. Энергия выделившаяся при ее распаде запасется в связях этих макроэргов.
Разберем на примере.
Самым распространенным макроэргом (энергетической валютой) клетки является АТФ (Аденозинтрифосфат).
Выглядит примерно так.
В его состав входит азотистое основание аденин (одно из 4, используемых для кодирования информации в ДНК), сахар рибоза и три остатка фосфорной кислоты (поэтому и АденозинТРИфосфат). Именно в связях между остатками фосфорной кислоты накапливается энергия. При отщеплении одного остатка фосфорной кислоты образуется АДФ (АденозинДИфосфат). АДФ может выделять энергию, отрывая еще один остаток и превращаясь в АМФ (АденозинМОНОфосфат). Но эффективность отщепленная второго остатка намного ниже. Поэтому, обычно, организм стремится из АДФ снова получить АТФ. Происходит это примерно так. При распаде глюкозы, выделяющаяся энергия тратится на образование связи между двумя остатками фосфорной кислоты и образование ATP. Процесс многостадийный и пока мы его опустим.
Именно в связях между остатками фосфорной кислоты накапливается энергия. При отщеплении одного остатка фосфорной кислоты образуется АДФ (АденозинДИфосфат). АДФ может выделять энергию, отрывая еще один остаток и превращаясь в АМФ (АденозинМОНОфосфат). Но эффективность отщепленная второго остатка намного ниже. Поэтому, обычно, организм стремится из АДФ снова получить АТФ. Происходит это примерно так. При распаде глюкозы, выделяющаяся энергия тратится на образование связи между двумя остатками фосфорной кислоты и образование ATP. Процесс многостадийный и пока мы его опустим.
Получившийся АТФ является универсальным источником энергии. Он используется везде, начиная от синтеза белка (для соединения аминокислот нужна энергия), заканчивая мышечной работой. Моторные белки, осуществляющие мышечное сокращение используют энергию, запасенную в АТФ, для изменения своей конформации. Изменение конформации это переориентация одной части большой молекулы относительно другой. Выглядит примерно так.
Выглядит примерно так.
То есть химическая энергия связи переходит в механическую энергию. Вот реальные примеры белков, использующих АТФ для осуществления работы.
Знакомьтесь, это миозин. Моторный белок. Он осуществляет перемещение крупных внутриклеточных образований и участвует в сокращении мышц. Обратите внимание, у него имеется две «ножки». Используя энергию запасенную в 1 молекуле АТФ он осуществляет одно конформационное изменение, по сути один шаг. Самый наглядный пример перехода химической энергии АТФ в механическую.
Второй пример — Na/K насос. На первом этапе он связывает три молекулы Na и одну АТФ. Используя энергию АТФ, он меняет конформацию, выбрасывая Na из клетки. Затем он связывает две молекулы калия и, возвращаясь к исходной конформации, переносит калий в клетку. Штука крайне важная, позволяет поддерживать уровень внутриклеточного Na в норме.
А если серьезно, то:
Пауза. Зачем нам АТФ? Почему мы не можем использовать запасенную в глюкозе энергию напрямую? Банально, если окислить глюкозу до CO2 за один раз, мгновенно выделится экстремально много энергии. И большая ее часть рассеется в виде тепла. Поэтому реакция разбивается на стадии. На каждой выделяется немного энергии, она запасается, и реакция продолжается пока вещество полностью не окислиться.
Зачем нам АТФ? Почему мы не можем использовать запасенную в глюкозе энергию напрямую? Банально, если окислить глюкозу до CO2 за один раз, мгновенно выделится экстремально много энергии. И большая ее часть рассеется в виде тепла. Поэтому реакция разбивается на стадии. На каждой выделяется немного энергии, она запасается, и реакция продолжается пока вещество полностью не окислиться.
Подитожу. Запасается энергия в жирах и углеводах. Из углеводов ее можно извлечь быстрее, но в жирах можно запасти больше. Для проведения реакций клетка использует высокоэнергетические соединения, в которых запасается энергия распада жиров, углеводов и тд… АТФ — основное такое соединение в клетке. По сути, бери и используй. Однако не единственное. Но об этом позже.
P.S. Я попытался максимально упростить материал, поэтому появились некоторые неточности. Прошу ревностных биологов меня простить.
Механизм повреждения энергетического обмена при гипоксии и возможные пути его коррекции фумаратсодержащими растворами
Л.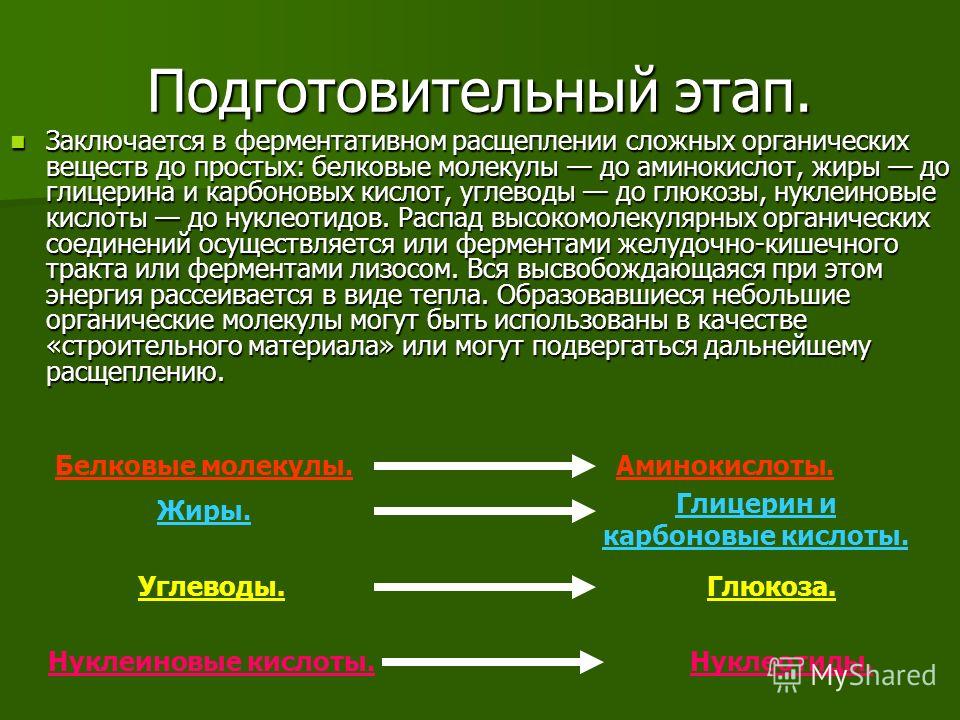 В. Слепнева, Г.А. Хмылова
В. Слепнева, Г.А. Хмылова
ФГБУ «Российский НИИ гематологи трансфузиологии ФМБА», г. Санкт-Петербург
Трансфузиология №2, 2013
Резюме
Статья посвящена вопросам механизма действия препаратов, влияющих на процессы энергообразования в организме. Показаны пути коррекции нарушений энергетического обмена и преимущества фумаратсодержащих инфузионных растворов.
Ключевые слова: гипоксия, цикл Кребса, сукцинат, фумарат, фумаратсодержащие инфузионные растворы, мафусол, полиоксифумарин, конфумин.
В настоящее время нарушения энергетического обмена рассматриваются как один из ведущих патологических процессов, приводящих к необратимым последствиям и гибели организма, что обусловливает исключительную важность рассматриваемой проблемы. Коррекция или устранение энергодефицита является обязательным компонентом в лечении большинства патологических состояний, и в связи с этим, понимание механизма действия препаратов, способных влиять на различные звенья энергообмена, для практикующих врачей приобретают особую ценность.
Жизнедеятельность организма с многообразием всех физиологических функций и биохимических процессов возможна лишь при условии его постоянного энергообеспечения. В настоящее время имеется значительный экспериментальный и клинический материал, свидетельствующий о том, что различные экстремальные воздействия на организм (тяжелая кровопотеря, ожог, травма, сердечная недостаточность, острое отравление и др.) вызывают однотипные повреждения в клеточной системе энергообразования. Это явление обусловлено тем, что результирующим эффектом различных по своей природе экстремальных факторов является развитие острого кислородного голодания тканей. Дефицит кислорода — акцептора электронов в митохондриальной дыхательной цепи, приводит к глубокому подавлению биоэнергетической функции митохондрий. Выходит из строя основная энергетическая система клетки, энергопродукция клетками резко снижается, и, как следствие, нарушается течение многочисленных энергозависимых процессов в организме [2, 6, 11, 13, 24, 34, 36, 37, 43].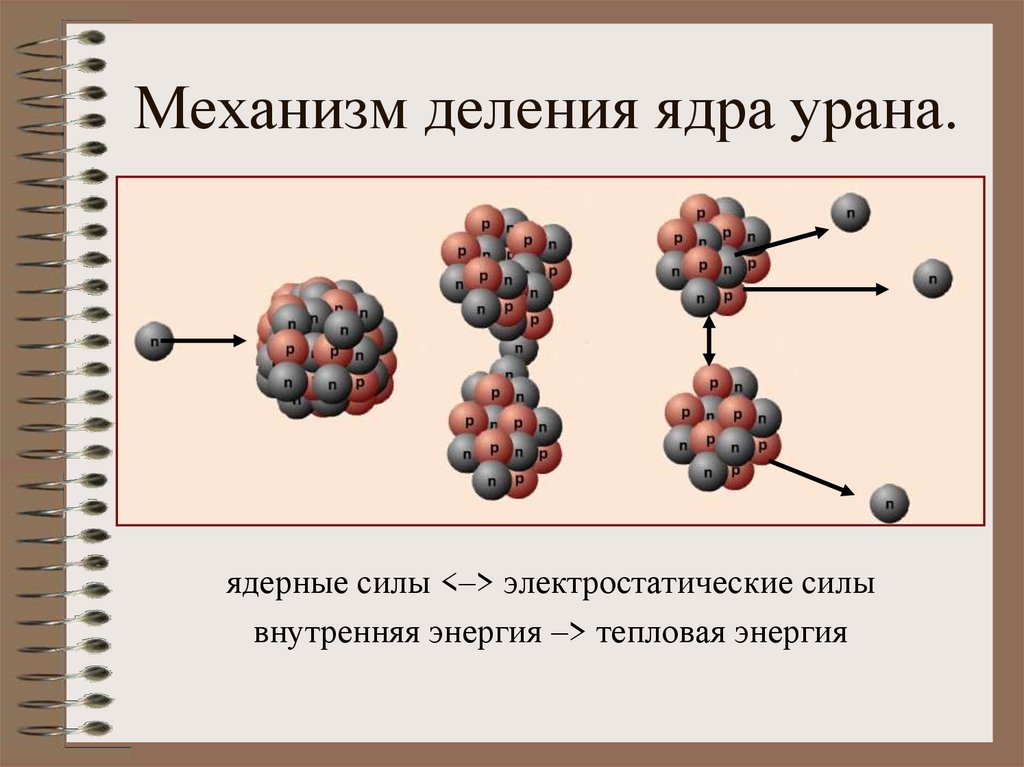
Недостаточность систем энергообразования в клетке составляет существенный элемент патогенеза многих заболеваний. По мнению ряда авторов, поддержание жизни в экстремальных условиях возможно до тех пор, пока дефицит энергии не достигнет критических величин. Истощение клеточных энергетических резервов ниже допустимого уровня сопровождается развитием в клетке необратимых процессов и гибелью организма.
Прежде чем перейти к рассмотрению вопросов, связанных с нарушением энергетического обмена в клетке при патологических состояниях и его коррекции применением различных лекарственных средств, кратко остановимся на описании процессов энергообразования в нормально функционирующей клетке [16, 41].
На рис. 1 схематически представлен сложный процесс распада питательных веществ, который обеспечивает ступенчатое постепенное освобождение энергии и аккумуляцию ее в виде макроэргической фосфатной связи аденозинтрифосфата (АТФ).
Распад сложных питательных веществ на более простые является необходимым условием для дальнейшего использования их в клетке в качестве источников энергии и пластического материала. В катаболизме основных питательных веществ (углеводов, белков и жиров) можно выделить три основные стадии.
В катаболизме основных питательных веществ (углеводов, белков и жиров) можно выделить три основные стадии.
На первой стадии крупные молекулы под влиянием сложных ферментативных систем расщепляются на более простые. В результате действия этих ферментативных систем углеводы расщепляются до гексоз и пентоз, липиды – до глицерина и жирных кислот, из белков образуется около 20-ти аминокислот.
На второй стадии происходит дальнейшее расщепление образовавшихся соединений. Из 20-ти различных аминокислот образуется лишь несколько конечных продуктов, а именно, ацетил-коэнзим А, α-кетоглютаровая и щавелевоуксусная кислоты.
Жирные кислоты в процессе β-окисления превращаются в ацетил-КоА. Гексозы под действием ферментативных систем гликолиза расцепляются до пировиноградной кислоты, которая затем в процессе окислительного декарбоксилирования превращается также в ацетил-КоА.
Гликолиз является тем механизмом, посредством которого многие организмы получают химическую энергию из глюкозы и других субстратов в отсутствие молекулярного кислорода.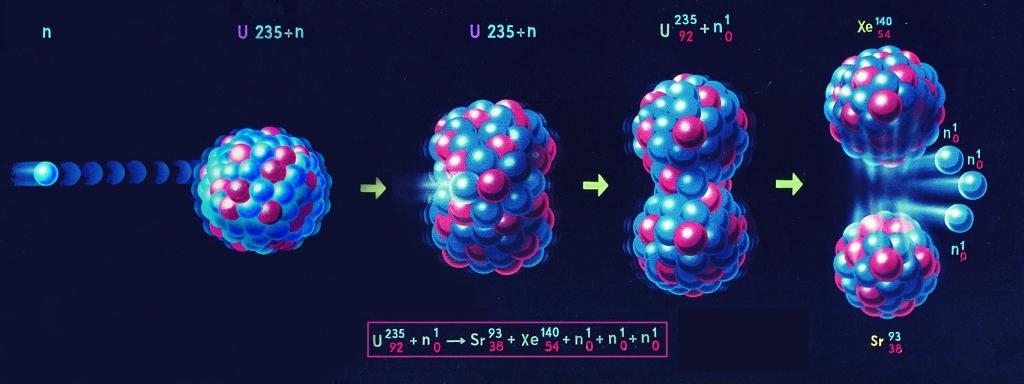 У большинства аэробных организмов процесс гликолиза является предварительной ступенью для дальнейшего окисления продуктов брожения кислородом в процессе дыхания.
У большинства аэробных организмов процесс гликолиза является предварительной ступенью для дальнейшего окисления продуктов брожения кислородом в процессе дыхания.
Метаболиты, образовавшиеся на второй стадии распада питательных веществ (ацетил-КоА, α-кето-глютаровая, щавелевоуксусная кислоты) вступают в третью стадию, которая для них является общей и на которой они в конечном итоге окисляются до СО2 и Н2О.
Третья стадия – стадия терминального окисления питательных веществ, во время которой освобождается основная масса энергии, осуществляется в митохондриях через цикл трикарбоновых кислот (ЦТК) и митохондриальную дыхательную цепь. ЦТК – общий конечный путь окислительного катаболизма всех видов клеточного топлива в аэробных условиях. В этом цикле под действием специфических дегидрогеназ протекают процессы дегидрирования субстратов, восстановительные эквиваленты от которых (протоны и электроны) поступают на митохондриальную дыхательную цепь. Дегидрирование – отщепление молекул Н2 от интермедиатов цикла Кребса происходит, в основном, при помощи дегидрогеназ, простетической группой которых является никотинамидаденин-динуклеотид (НАД), и лишь дегидрирование янтарной кислоты осуществляется ФАД-зависимой дегидрогеназой (сукцинатдегидрогеназой).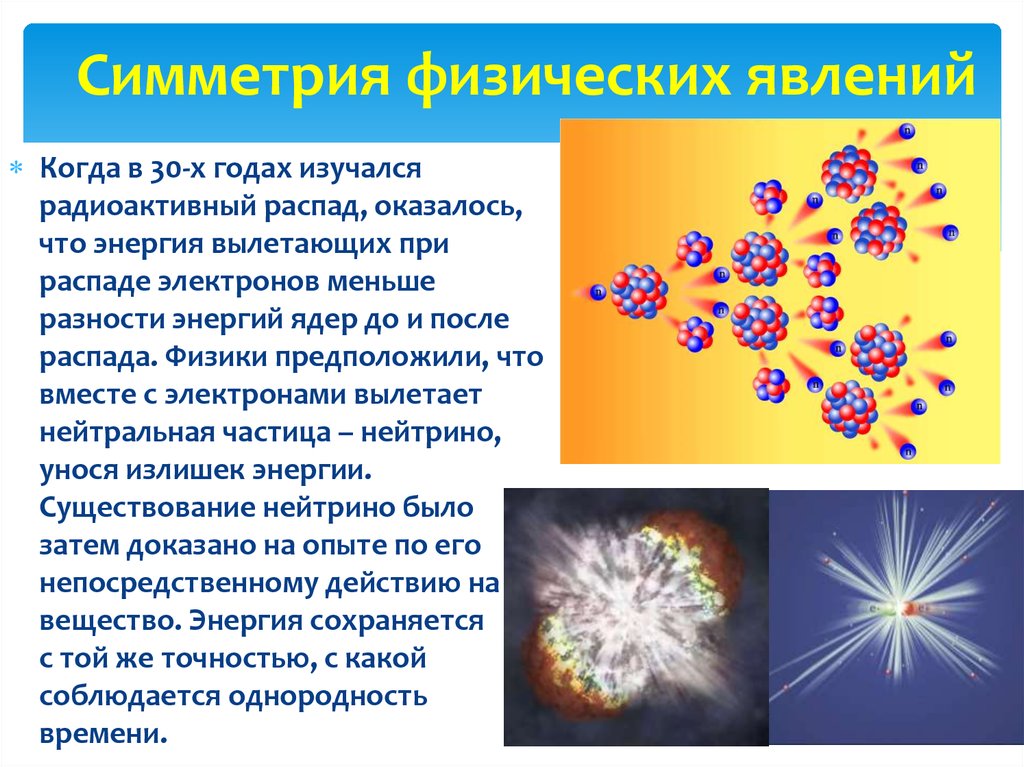
Дыхательная цепь, состоящая из серии переносчиков электронов, передает восстановительные эквиваленты конечному акцептору электронов – молекулярному кислороду. Дыхательная цепь – это полиферментная система, локализованная во внутренней мембране митохондрий, основными компонентами которой являются НАД-зависимые дегидрогеназы, флавопротеиды и цитохромы (рис. 1).
Сопряженно с транспортом электронов протекает процесс окислительного фосфорилирования, в котором значительная часть свободной энергии электронов, передаваемых редокс-цепью на кислород, аккумулируется и трансформируется в специфическую макроэргическую связь АТФ. Таким образом, необходимая для нужд организма энергия образуется благодаря функционированию взаимосвязанных процессов гликолиза и дыхания. В процессе гликолиза высвобождается лишь незначительная часть той химической энергии, которая потенциально может быть извлечена из молекулы глюкозы. Полное окисление глюкозы до СО2 и Н 2О, осуществляемое в процессе дыхания, приводит к синтезу значительно большего количества макроэргов.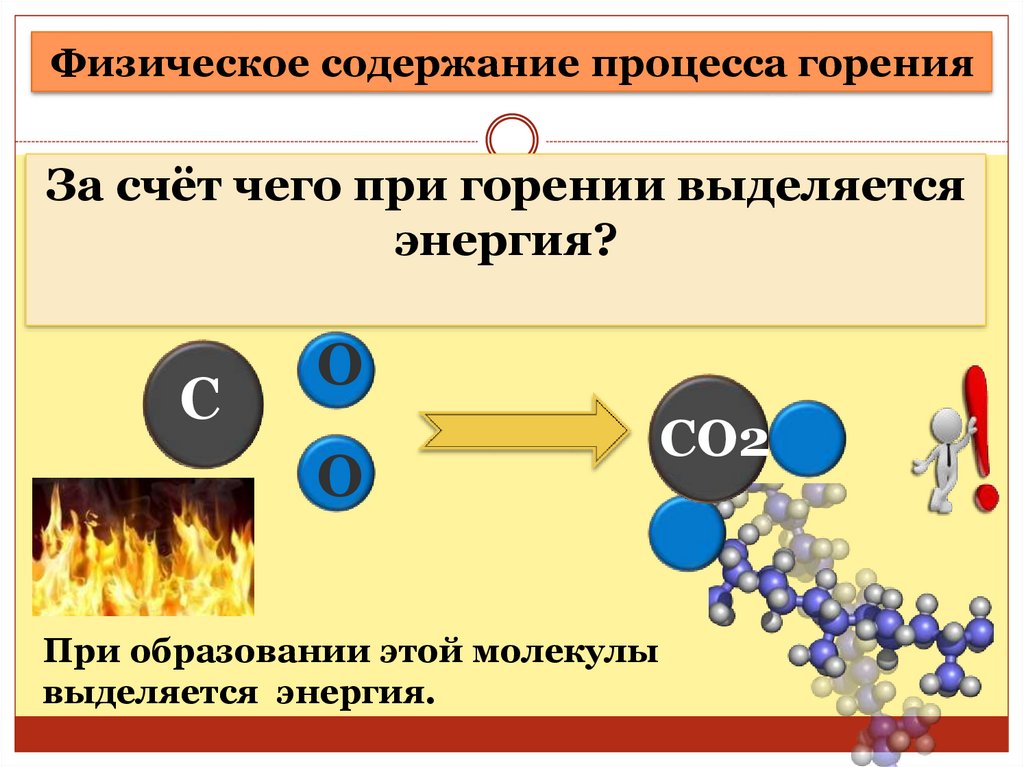 При окислении одной молекулы глюкозы в гликолитическом цикле образуется 2 молекулы АТФ, тогда как дальнейшее расщепление продуктов гликолиза в цикле Кребса сопровождается синтезом 38 молекул АТФ. Таким образом, митохондриальная дыхательная цепь является основным местом приложения и утилизации кислорода в клетке.
При окислении одной молекулы глюкозы в гликолитическом цикле образуется 2 молекулы АТФ, тогда как дальнейшее расщепление продуктов гликолиза в цикле Кребса сопровождается синтезом 38 молекул АТФ. Таким образом, митохондриальная дыхательная цепь является основным местом приложения и утилизации кислорода в клетке.
При дефиците кислорода – конечного акцептора электронов в редокс-цепи митохондрий – отмечается выраженная гиперредукция всех компонентов терминального звена окисления. Прекращаются транспорт электронов по дыхательной цепи и сопряженный с ним процесс образования макроэнергических фосфатов. Известно, что в условиях нормоксии НАД-звено дыхательной цепи митохондрий принимает восстановительные эквиваленты из различных источников:
1. от субстратов цикла Кребса при участии специфических дегидрогеназ;
2. оксиацил-КоА-дегидрогеназы поставляютионы водорода на НАД- звено при окислении жирных кислот;
3. сложная система пируват-дегидрогеназы, отщепляя ионы водорода в реакциях окислительного декарбоксилирования, передает их на НАД-звено редокс-цепи;
4.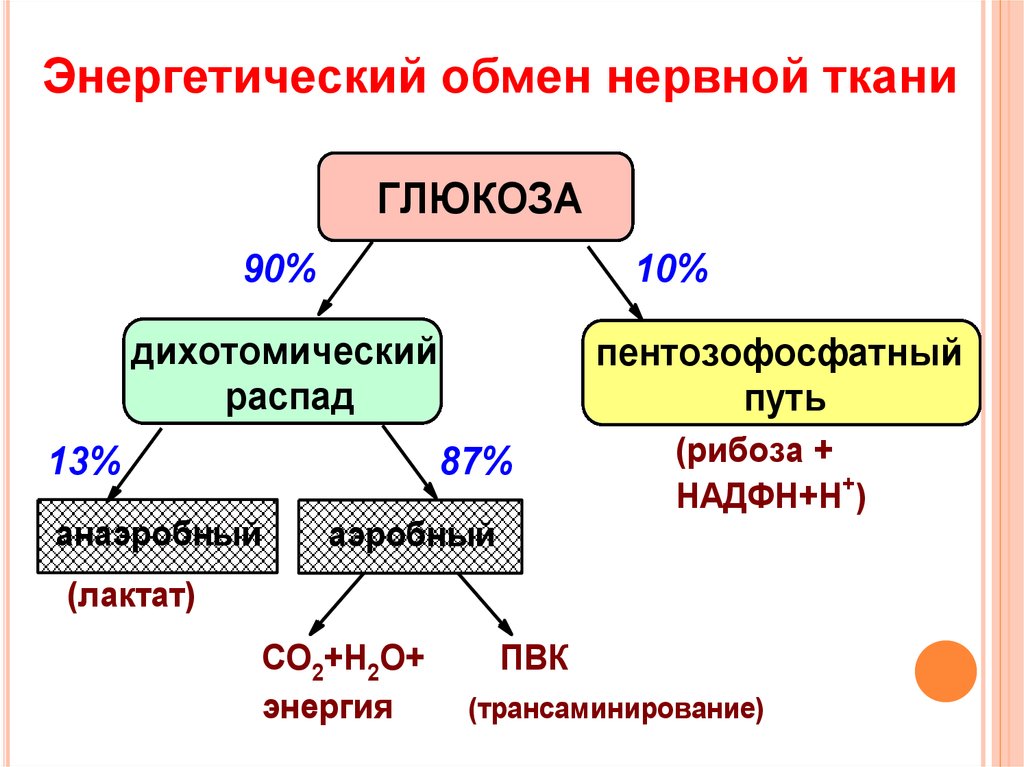 внемитохондриальный НАД-Н, образованный в центральной реакции гликолитической оксидоредукции, также отдает свои протоны на митохондриальную дыхательную цепь (рис.1).
внемитохондриальный НАД-Н, образованный в центральной реакции гликолитической оксидоредукции, также отдает свои протоны на митохондриальную дыхательную цепь (рис.1).
Мощный поток восстановительных эквивалентов в условиях кислородной недостаточности не может реализоваться из-за гипервосстановленности НАД-зависимого участка дыхательной цепи. Выключается из функционирования основная энергетическая система клетки, резко снижается продукция АТФ.
В анаэробных условиях клетка стремится восполнить энергетический дефицит за счёт активации гликолиза. Несмотря на то, что при анаэробном гликолизе продуцируется почти в 20 раз меньше АТФ, чем при полном сгорании глюкозы в цикле Кребса, потенциальная скорость процесса в основном может обеспечить энергозатраты организма. Однако для осуществления гликолитических реакций необходим постоянный приток окисленной формы НАД, который при нормоксии обеспечивается работой специфических челночных механизмов. Гликолитический НАД-Н проникает через митохондриальные мембраны посредством функционирования α-глицерофосфатного, β-оксибутиратного и других механизмов переноса восстановительных эквивалентов.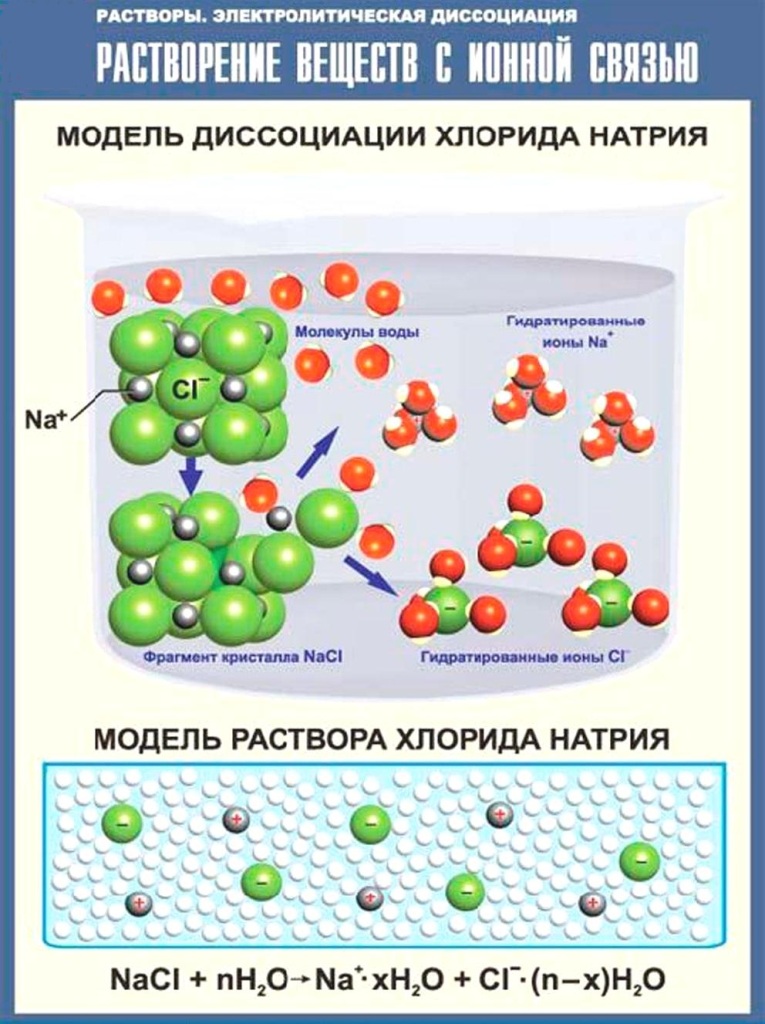
Оксибутиратный и глицерофосфатные шунты являются основными конкурентами лактатдегидрогеназного механизма окисления гликолитического НАД-Н, деятельность которого при нормальной концентрации кислорода в клетке подавлена более активными вышеназванными механизмами.
При нарушении электронтранспортной функции редокс-цепи и гиперредукции ее НАД-звена клетка вынуждена изыскивать другие пути реокисления цитоплазматического НАД-Н. В условиях острой гипоксии конечный продукт гликолиза – пируват – не подвергается декарбоксилированию и не вовлекается в цикл Кребса, а, принимая восстановительные эквиваленты от цитоплазматического НАД-Н, превращается в лактат с освобождением новых порций окисленной формы НАД (рис. 2).
Активация лактатдегидрогеназного механизма поставки НАД для гликолиза в конечном итоге приводит к истощению запасов гликогена и тканевому ацидозу вследствие накопления кислых продуктов метаболизма (лактата, пирувата, оксибутирата, глицерофосфата и др.). Избыточные концентрации конечного субстрата анаэробного гликолиза – лактата – тормозят последнюю реакцию гликолитического цикла.
Регенерация НАД прекращается, и, именно, дефицит пиридиннуклеотида останавливает гликолиз и анаэробную продукцию АТФ. Клеточный ацидоз способствует нарушению проницаемости мембран, вплоть до разрушения лизосом. В цитоплазму поступают аутолитические ферменты. Развивается процесс аутолиза клеток, сопровождающийся повреждением тканей и органов. В организме формируются необратимые изменения.
Таким образом, степень повреждения митохондриального метаболизма в условиях тяжелой кислородной недостаточности определяет тяжесть многих патологических состояний. Накопленный опыт лечения шока и кровопотери показывает, что существующие инфузионнотрансфузионные среды, проявляя лечебное действие в стадиях легкой и средней тяжести, оказываются недостаточными на поздних стадиях процесса. Особенности течения поздних стадий геморрагического шока связывают главным образом с генерализованными нарушениями метаболизма и возникающими в результате этого расстройствами энергообмена.
В связи с этим применение совместно с кровезаменителями препаратов, способных повысить энергетический потенциал клетки в условиях гипоксии, рассматривается как один из путей повышения эффективности инфузионной терапии гиповолемических состояний.
В ликвидации энергетического дефицита большое значение придается антигипоксантам. К настоящему времени не выработано единого общепринятого определения антигипоксантов и их классификации, так как в ответ на гипоксическое воздействие вовлекаются самые разные системы организма. Препараты биоэнергетического действия можно разделить на несколько групп.
К первой группе следует отнести препараты, являющиеся источником энергетического сырья (глюкоза, сорбит, АТФ, фосфорилированные гексозы и др.). Использование их показано при патологических состояниях, сопровождающихся истощением энергетических ресурсов в клетке. Включение в состав противошоковых кровезаменителей 5-10% глюкозы или фосфорилированных гексоз [1, 42] для поддержания гликолиза в клетках не позволяет существенно повысить эффективность инфузионной терапии из-за неизбежно возникающего накопления кислых продуктов метаболизма и дефицита окисленной формы пиридиннуклеотида (НАД). Отсюда понятно, что введение таких субстратов окисления, как глюкоза или гексозы, при гипоксии целесообразно лишь с препаратами, ускоряющими утилизацию лактата. Таким свойством обладают соединения группы гутимина. В эксперименте показан антигипоксический эффект гутимина и амтизола при геморрагическом шоке [8].
Таким свойством обладают соединения группы гутимина. В эксперименте показан антигипоксический эффект гутимина и амтизола при геморрагическом шоке [8].
Ко второй группе препаратов можно отнести средства, которые, не являясь энергетически богатыми соединениями, способны активно воздействовать на энергетический обмен посредством коррекции отдельных звеньев многоступенчатого процесса аккумуляции энергии в клетке. Данные о нарушении транспорта электронов в дыхательной цепи митохондрий при шоке и кровопотери [28] являются теоретической предпосылкой для применения антигипоксантов с электрон-акцепторными свойствами. В литературе имеются довольно обширные сведения о применении естественных и искусственных антигипоксантов – переносчиков электронов. К числу первых относится цитохром С, который, как известно, является одним из компонентов дыхательной цепи митохондрий и служит мобильным переносчиком электронов. Играя важную роль в энергетическом метаболизме клетки, цитохром С показал высокую лечебную эффективность в клинической практике при терапии шока, кровопотери и постишемической гипоксии [12, 32].
Разработке и исследованию искусственных переносчиков электронов посвящено значительное количество работ. Эти соединения способны модифицировать дыхательную цепь митохондрий так, чтобы осуществлять «сброс» восстановительных эквивалентов непосредственно на кислород, минуя заблокированные участки дыхательной цепи. К числу таких веществ относится ряд соединений из класса хинонов (ортопарабензохиноны, нафтохиноны, гексогидрохиноны). Высокий редокс-потенциал этих препаратов определяет их способность к транспорту электронов [30]. При проведении экспериментов на животных многие из этих соединений оказались токсичными, что не позволило рекомендовать их в качестве лечебных средств. Из всех средств, формирующих искус- ственные редокс-системы, в медицинскую практику внедрен препарат «Гипоксен», представляющий собой синтетический полихинон [9].
Известно, что антигипоксанты группы хинонов осуществляют перенос электронов с НАД-Н звена на кислород, минуя все 3 пункта фосфорилирования в дыхательной цепи и, следовательно, устранение дефицита энергии при введении этих препаратов может происходить лишь за счет активации гликолитической выработки АТФ.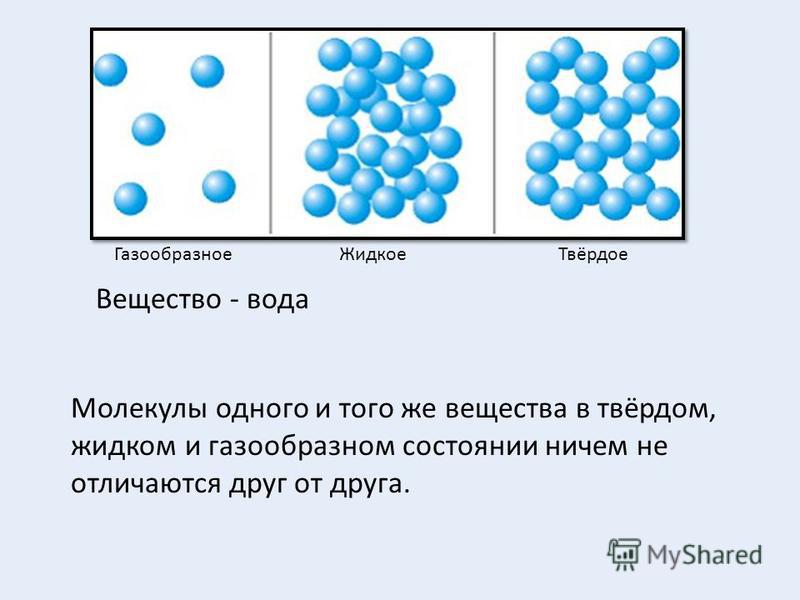 Однако для полноценного проявления антигипоксических свойств этих соединений необходим акцептор электронов – кислород. Наибольший интерес для включения в состав новых комплексных кровезаменителей представляют, так называемые, истинные антигипоксанты или антигипоксанты прямого действия, непосредственно влияющие на митохондриальный метаболизм при гипоксии.
Однако для полноценного проявления антигипоксических свойств этих соединений необходим акцептор электронов – кислород. Наибольший интерес для включения в состав новых комплексных кровезаменителей представляют, так называемые, истинные антигипоксанты или антигипоксанты прямого действия, непосредственно влияющие на митохондриальный метаболизм при гипоксии.
Согласно теоретическим предпосылкам, одна из возможностей поддержания биоэнергетики клетки может быть реализована посредством стимуляции адаптационных механизмов к гипоксии, работающих на последних этапах цикла Кребса. Из всех субстратов цикла Кребса только влияние сукцината на энергетический обмен подробно изучено в эксперименте на животных.
Исследование механизма действия сукцината при гипоксических состояниях проведено в работах М.Н. Кондрашовой с соавторами [5, 6]. Исследователи считают, что в условиях гипоксии сукцинат, не являясь НАД-зависимым субстратом, «монополизирует» дыхательную цепь и активно в ней окисляется.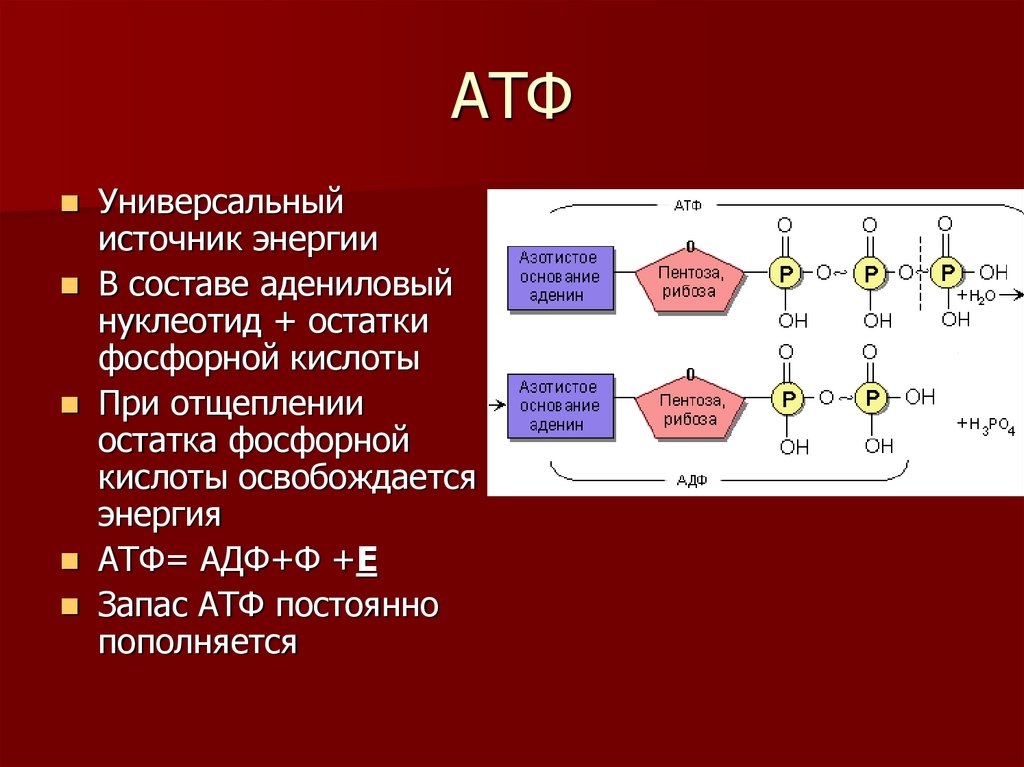 Высокая скорость реакции окисления сукцината, поставляющей 2 молекулы АТФ, позволяет компенсировать выработку 3-х молекул АТФ, образующихся при окислении НАД-зависимых субстратов. Однако в условиях прогрессирующей гипоксии дефицит кислорода, лимитирующий скорость окисления всех субстратов, снижает ценность сукцината и ставит его в один ряд с другими субстратами окисления. Поэтому применение сукцината в качестве антигипоксанта должно быть особенно эффективно в комплексе с препаратами, улучшающими кислородообеспечение организма. Преимущественное использование сукцината – естественная защита клетки против гипоксии. При этом пополнение фонда субстрата может происходить за счет реакций цикла Кребса, идущих как в прямом, так и в обратном направлениях (рис. 3).
Высокая скорость реакции окисления сукцината, поставляющей 2 молекулы АТФ, позволяет компенсировать выработку 3-х молекул АТФ, образующихся при окислении НАД-зависимых субстратов. Однако в условиях прогрессирующей гипоксии дефицит кислорода, лимитирующий скорость окисления всех субстратов, снижает ценность сукцината и ставит его в один ряд с другими субстратами окисления. Поэтому применение сукцината в качестве антигипоксанта должно быть особенно эффективно в комплексе с препаратами, улучшающими кислородообеспечение организма. Преимущественное использование сукцината – естественная защита клетки против гипоксии. При этом пополнение фонда субстрата может происходить за счет реакций цикла Кребса, идущих как в прямом, так и в обратном направлениях (рис. 3).
При обратном течении реакций имеющийся запас малата по мере необходимости превращается в фумарат, который восстанавливается в сукцинат. Восстановление фумарата сопровождается выработкой АТФ, и поэтому реакции обращения в системе «малат-фумарат-сукцинат» способны поддерживать окислительное фосфорилирование даже при аноксии.
В условиях же гипоксии инверсивные превращения фумарата выполняют роль триггера, который, в зависимости от концентрации кислорода регулирует течение конечных реакций цикла Кребса в прямом либо в обратном направлениях, и эти реакции сопровождаются синтезом АТФ. Механизм инверсивных превращений фумарата в цикле Кребса объясняет эффективность применения фумаратсодержащих инфузионных сред, таких как кристаллоидный раствор – мафусол, коллоидный кровезаменитель – полиоксифумарин и концентрированный раствор фумарата натрия – конфумин. Эти препараты разработаны и основательно изучены в Российском НИИ гематологии и трансфузиологии. Лечебная эффективность была изучена на моделях геморрагического и ожогового шока, а также при экспериментальном перитоните [17–20, 23, 25,45]. Оценку эффективности инфузионных растворов определяли по совокупности показателей системной гемодинамики, кислородного режима, кислотно-основного состояния (КОС), перекисного окисления липидов и митохондриального метаболизма в печени и сердце животных. Полярографическое исследование митохондрий, выделенных из печени и сердца животных, леченных фумаратсодержащими растворами, свидетельствовало о полном восстановлении энергопродуцирующих функций этих органелл. Следует отметить, что летальность животных в контрольной группе (тяжелый шок) составляло 100%, при лечении мафусолом или полиоксифумарином – 17–20%.
Полярографическое исследование митохондрий, выделенных из печени и сердца животных, леченных фумаратсодержащими растворами, свидетельствовало о полном восстановлении энергопродуцирующих функций этих органелл. Следует отметить, что летальность животных в контрольной группе (тяжелый шок) составляло 100%, при лечении мафусолом или полиоксифумарином – 17–20%.
Результаты исследования митохондриального метаболизма позволяют предположить, что парентеральное введение фумарата индуцирует суперкомпенсацию адаптационного механизма к гипоксии, функционирующих на последних этапах цикла Кребса. Фумарат в системе «малат-фумарат-сукцинат» способен поддерживать синтез АТФ как в аэробных, так и в анаэробных условиях. При дефиците кислорода фумарат, восстанавливаясь ФАД∙Н2-группой сукцинатдегидрогеазой, превращается в сукцинат и освобождает новые порции окисленной формы ФАД. Принимая восстановительные эквиваленты от НАД-Н, ФАД способствует снятию гипервосстановленности НАД звена дыхательной цепи и синтезу АТФ в бескислородной среде.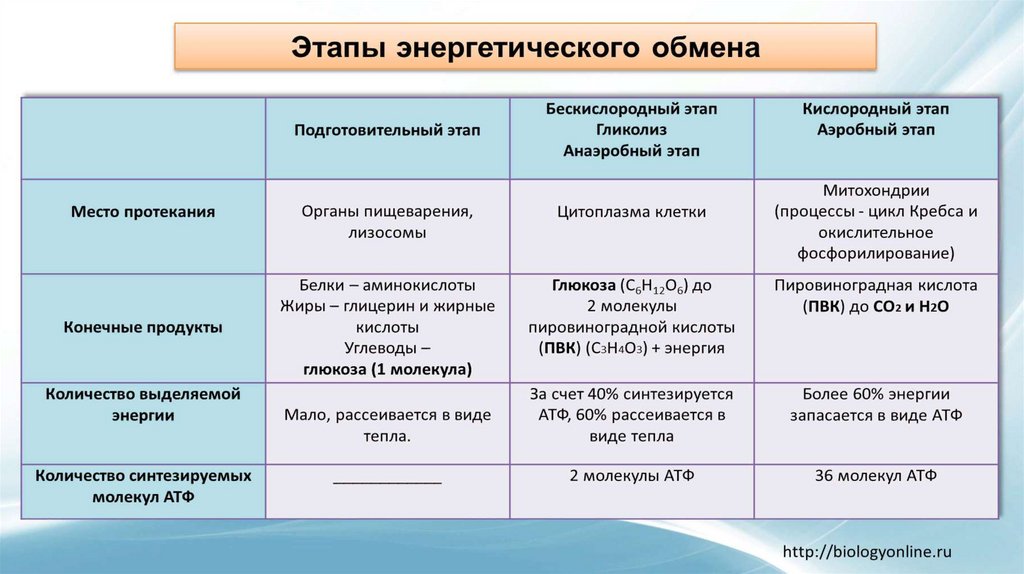 При поступлении кислорода в клетку сукцинат, синтезируемый из фумарата, монополизирует дыхательную цепь и, активно окисляясь в ней, продуцирует АТФ (рис. 3). К тому же, образование в этих реакциях окисленной формы НАД запускает также и механизм гликолитической продукции АТФ. Поддержание энергетического потенциала клетки при инфузия фумарата способствует удлинению периода обратимых изменений в организме и предотвращает развитие «необратимости» при патологических состояниях, отягощенных глубокой гипоксией.
При поступлении кислорода в клетку сукцинат, синтезируемый из фумарата, монополизирует дыхательную цепь и, активно окисляясь в ней, продуцирует АТФ (рис. 3). К тому же, образование в этих реакциях окисленной формы НАД запускает также и механизм гликолитической продукции АТФ. Поддержание энергетического потенциала клетки при инфузия фумарата способствует удлинению периода обратимых изменений в организме и предотвращает развитие «необратимости» при патологических состояниях, отягощенных глубокой гипоксией.
Парентеральное введение фумаратсодержащих растворов наряду с восстановлением биоэнергетики клетки, сопровождается «мягким» ощелачивающим действием препаратов на кислотно-основное состояние крови при ацидозе. Это действие обусловлено тем, что такие органические соли, как фумарат-, ацетат-, лактат-, сукцинат- и малат натрия являются соединениями, образованными сильным основанием (NaOH) и слабой кислотой. При гидролизе подобных солей в кровеносном русле освобождается соответствующая кислота и NaOH, который расходуется на нейтрализацию кислых продуктов метаболизма. Реакция гидролиза смещена вправо, так как постоянно происходит потребление продукта гидролитической реакции – NaOH (рис. 4).
Реакция гидролиза смещена вправо, так как постоянно происходит потребление продукта гидролитической реакции – NaOH (рис. 4).
Следует отметить, что вышеназванные соли оказывают мягкое ощелачивающие действие по сравнению с бикарбонатом натрия, широко используемым в клинической практике для ликвидации ацидоза. Реакция гидролиза NaHСО3 протекает значительно быстрее, так как в ходе реакции удаляются оба ее продукта: NaOH расходуется на нейтрализацию метаболитов, а второй продукт реакции – угольная кислота, нестоек и разлагается на Н2О и СО2. Образованная в избыточном количестве щелочь может способствовать развитию алкалоза, что имеет место в клинических условиях при передозировке бикарбоната натрия.
Все вышеперечисленные соли входят в состав различных инфузионных растворов (мафусол, полиоксифумарин, конфумин, лактасол, Рингер-лактат, ацесоль, реамберин, стерофундин и др.). Однако оказывая ощелачивающее действие при ацидозе, далеко не все эти препараты способны поддержать энергетический обмен при гипоксии.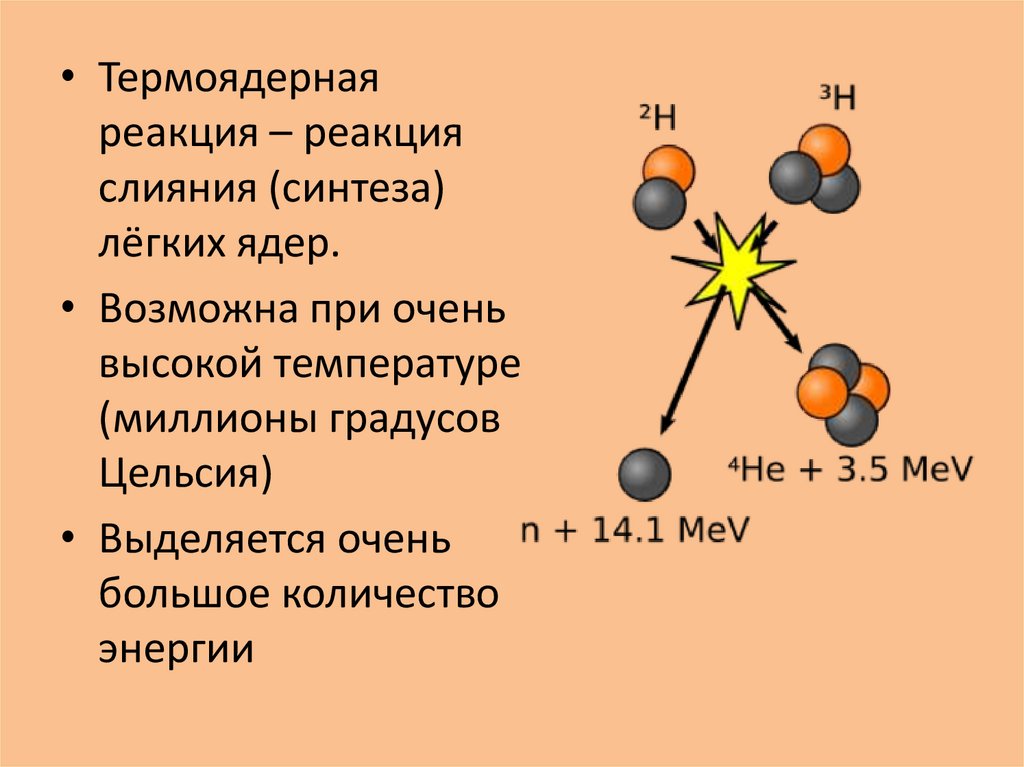 Восстановление показателей КОС «химическим путем» является недостаточным для успешной терапии шока.
Восстановление показателей КОС «химическим путем» является недостаточным для успешной терапии шока.
Следует к тому же учитывать, что при гидролизе лактата натрия выделяется молочная кислота, которая в сумме с эндогенной молочной кислотой, возникающей в больших концентрациях при гипоксии, могут способствовать подавлению реакций гликолиза, что, в свою очередь, вызывает снижение продукции гликолитической АТФ. Существуют также исследования, указывающие, что лактат может вызвать интерстициальный отек головного мозга и повышать агрегацию тромбоцитов и эритроцитов [14, 39, 44]. Лактатсодержащие инфузионные растворы нельзя использовать при печеночной недостаточности [35, 38, 40], а также в случаях шока, сопровождающегося гиперлактатемией или лактатным ацидозом [33].
Ацетат натрия, в отличие от лактата, не проявляет токсического действия при тяжелом шоке. Однако утилизация уксусной кислоты, образованной при гидролизе ацетата натрия, в условиях кислородной недостаточности затруднена вследствие постгипоксического дефекта в функционировании митохондриальной дыхательной цепи. Лечебное действие фумарата натрия в сравнении с лактатом и ацетатом представляется более физиологичным, так как при его введении наряду с ощелачивающим эффектом проявляется и его влияние на восстановление процессов генерации энергии в митохондриях, а, следовательно, устраняется причина возникновения метаболического ацидоза.
Лечебное действие фумарата натрия в сравнении с лактатом и ацетатом представляется более физиологичным, так как при его введении наряду с ощелачивающим эффектом проявляется и его влияние на восстановление процессов генерации энергии в митохондриях, а, следовательно, устраняется причина возникновения метаболического ацидоза.
Сукцинатсодержащие растворы, в частности «Реамберин», способствуют поддержанию энергетического обмена, однако, в условиях острого дефицита кислорода подавляется окисление сукцината и существенно снижается его энергопродуцирующая функция. Окисление малата в цикле Кребса осуществляется НАД-зависимой малатдегидрогеназой, и эта реакция тормозится из-за гипервосстановленности НАД-звена редокс-цепи митохондрий при гипоксии. Следовательно, в этих условиях субстрат не способен повысить энергетический потенциал клетки. К тому же, в инфузионном малатсодержащем растворе «Стерофундин» концентрация малата очень низкая, чтобы обеспечить достаточную продукцию АТФ. В условиях гипоксии повышение концентрации малата могло бы создать условия для обращения реакций в цикле Кребса с увеличением фонда фумарата, способного принимать восстановительные эквиваленты (Н2) и синтезировать АТФ.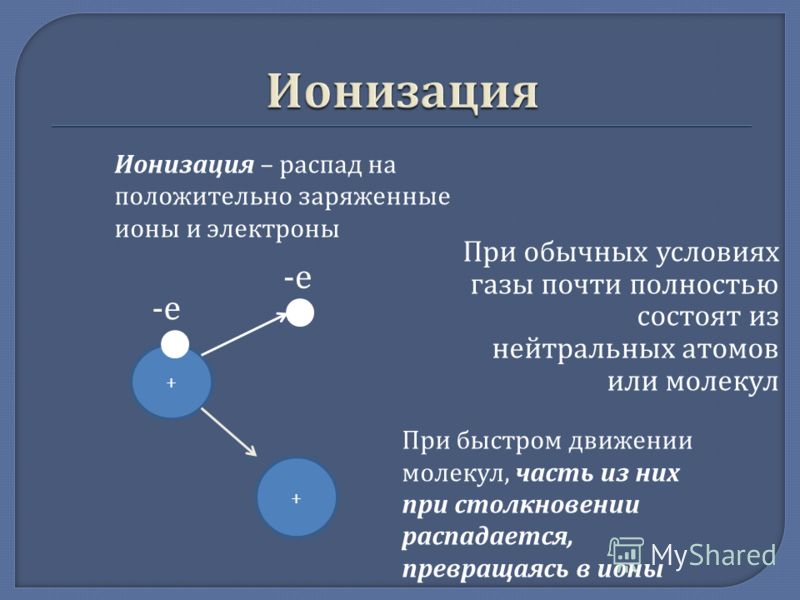 Однако концентрация малата в стерофундине (5 ммоль/л) незначительна для запуска реакций в цикле Кребса в обратном направлении.
Однако концентрация малата в стерофундине (5 ммоль/л) незначительна для запуска реакций в цикле Кребса в обратном направлении.
Фумаратсодержащие растворы (мафусол, полиоксифумарин) содержат высокие концентрации фумарата (86 ммоль/л), обеспечивающие как выработку АТФ, так и накопление сукцината, который активно окисляется при поступлении кислорода. Введение субстратов в организм при гипоксии показано еще и вследствие того, что кислородная недостаточность сопровождается значительным субстратным голодом клетки. Препараты «Мафусол» и «Полиоксифумарин» с высокой концентрацией фумарата и возможностью инфузий больших объемов этих растворов без побочных эффектов являются высокоэффективными средствами терапии шока различного генеза. Это подтверждено клинически. Так, кристаллоидный кровезаменитель «Мафусол» разрешен к медицинскому применению уже более 20 лет и широко используется в разных областях медицины (хирургия, неврология, кардиология, реаниматология, педиатрия, акушерство и гинекология, комбустиология, токсикология и др. ) [3, 15, 22, 27, 29, 31]. Отличительной особенностью этого препарата является то, что его можно переливать в больших количествах, не только внутривенно, но и внутриартериально, а также в смеси для заполнения контура АИК при открытых операциях на сердце. Ни один из существующих сейчас на фармацевтическом рынке инфузионных антигипоксических препаратов не обладает этими свойствами. Полифункциональный коллоидный плазмозаменитель «Полиоксифумарин» с 1999 года успешно применяется у взрослых и детей в клинической практике гиповолемических состояний различной степени тяжести [10, 21, 22]. Аналогов ему нет ни в России, ни зарубежом.
) [3, 15, 22, 27, 29, 31]. Отличительной особенностью этого препарата является то, что его можно переливать в больших количествах, не только внутривенно, но и внутриартериально, а также в смеси для заполнения контура АИК при открытых операциях на сердце. Ни один из существующих сейчас на фармацевтическом рынке инфузионных антигипоксических препаратов не обладает этими свойствами. Полифункциональный коллоидный плазмозаменитель «Полиоксифумарин» с 1999 года успешно применяется у взрослых и детей в клинической практике гиповолемических состояний различной степени тяжести [10, 21, 22]. Аналогов ему нет ни в России, ни зарубежом.
Применение концентрированного раствора фумарата натрия (препарата «Конфумин») в качестве антигипоксического компонента в схемах инфузионно-трансфузионной терапии существенно увеличивает уровень субстратов окисления в кровеносном русле и позволяет повысить лечебную эффективность общепринятых в клинической практике плазмозаменителей [3, 4, 22, 25-27]. Конфумин разрешен к широкому медицинскому применению у взрослых, промышленный выпуск препарата освоен в ОАО «Фирма Медполимер».
Страница не найдена
Размер:
AAA
Цвет: C C C
Изображения Вкл. Выкл.
Обычная версия сайта
RUENBY
Гомельский государственный
медицинский университет
- Университет
- Университет
- История
- Руководство
- Устав и Символика
- Воспитательная деятельность
- Организация образовательного процесса
- Международное сотрудничество
- Система менеджмента качества
- Советы
- Факультеты
- Кафедры
- Подразделения
- Первичная профсоюзная организация работников
- Издания университета
- Гордость университета
- Выпускник-2021
- Первичная организация «Белорусский союз женщин»
- Одно окно
- ГомГМУ в международных рейтингах
- Структура университета
- Абитуриентам
- Приёмная комиссия
- Целевая подготовка
- Заключение, расторжение «целевого» договора
- Льготы для молодых специалистов
- Архив проходных баллов
- Карта и маршрут проезда
- Порядок приёма на 2022 год
- Специальности
- Контрольные цифры приёма в 2022 году
- Стоимость обучения
- Информация о ходе приёма документов
- Приём документов и время работы приёмной комиссии
- Порядок приёма граждан РФ, Кыргызстана, Таджикистана, Казахстана
- Pепетиционное тестирование
- Горячая линия по вопросам вступительной кампании
- Студентам
- Первокурснику
- Расписание занятий
- Расписание экзаменов
- Информация для студентов
- Студенческий клуб
- Спортивный клуб
- Общежитие
- Нормативные документы
- Практика
- Стоимость обучения
- Безопасность жизнедеятельности
- БРСМ
- Профком студентов
- Учебный центр практической подготовки и симуляционного обучения
- Многофункциональная карточка студента
- Анкетирование студентов
- Выпускникам
- Интернатура и клиническая ординатура
- Докторантура
- Аспирантура
- Магистратура
- Распределение
- Врачам и специалистам
- Профессорский консультативный центр
- Факультет повышения квалификации и переподготовки
- Иностранным гражданам
- Факультет иностранных студентов
- Стоимость обучения
- Регистрация и визы
- Полезная информация
- Правила приёма
- Информация о возможностях и условиях приема в 2022 году
- Официальные представители ГомГМУ по набору студентов
- Страхование иностранных граждан
- Приём на Подготовительное отделение иностранных граждан
- Прием иностранных граждан для обучения на английском языке / Training of foreign students in English
- Повышение квалификации и переподготовка для иностранных граждан
- Научная деятельность
- Направления научной деятельности
- Научно-педагогические школы
- Студенчеcкое научное общество
- Инновационные технологии в ГомГМУ
- Научно-исследовательская часть
- Научно-исследовательская лаборатория
- Конкурсы, гранты, стипендии
- Работа комитета по этике
- Научные мероприятия
- В помощь исследователю
- Диссертационный совет
- «Горизонт Европа»
- Патенты
- Инструкции на метод
- Совет молодых ученых
- Госпрограмма (ЧАЭС)
- Главная
Биохимия мочи: сдать анализ по доступной цене
Фосфор считается одним из базовых микроэлементов человеческого организма. Он необходим для формирования молекул АТФ, обеспечивающих энергией все процессы, синтеза кислот ДНК и РНК, образования клеточных мембран и костной ткани.
Он необходим для формирования молекул АТФ, обеспечивающих энергией все процессы, синтеза кислот ДНК и РНК, образования клеточных мембран и костной ткани.
Где можно сдать:
В клинике
На дому
Материал
Моча
Фосфор является одним из базовых микроэлементов. Он является компонентом клеточных мембран (в составе фосфолипидов), костной ткани, ДНК и РНК, а также молекулы АТФ, которая является основным источником энергии в организме.
Срок выполнения
1-2 дня
Где можно сдать:
В клинике
На дому
Материал
Моча
С-пептид – это вещество, являющееся побочным продуктом синтеза инсулина. Этот белок выступает в роли связующего звена между альфа- и бета-пептидными цепями, которые образуют молекулу проинсулина. Это неактивный предшественник гормона.
Срок выполнения
1-2 дня
Где можно сдать:
В клинике
На дому
Материал
Моча
Ежедневно почки человека фильтруют сотни литров крови. Сначала жидкость вместе с растворенными в ней веществами проходит через нефроны (структурные элементы почки) с образованием первичной мочи.
Срок выполнения
1-2 дня
Где можно сдать:
В клинике
На дому
Материал
Моча
Осмолярность мочи – это концентрация всех растворенных в ней веществ. В отличие от удельного веса, она зависит только от числа частиц, тогда как плотность определяется не только количеством, но и особенностями строения примесей.
Срок выполнения
1-2 дня
Где можно сдать:
В клинике
На дому
Материал
Моча
Оксалаты – это производные щавелевой кислоты, которые образуются в организме при распаде глицина и аскорбиновой кислоты, а также поступают с пищей. В норме эти вещества выводятся с мочой.
В норме эти вещества выводятся с мочой.
Срок выполнения
1-2 дня
Где можно сдать:
В клинике
На дому
Материал
Моча
Общий белок – это один из базовых показателей работы почек. В норме крупные молекулы не проходят через почечный фильтр, а относительно небольшие соединения проходят в первичную мочу и затем подвергаются реабсорбции.
Срок выполнения
1-2 дня
Где можно сдать:
В клинике
На дому
Материал
Моча
Мочевина – азотсодержащее химическое соединение, конечный продукт обмена белков в человеческом организме. Азот входит в состав любого белка. При распаде белковой молекулы азот высвобождается, образуя токсичное вещество – аммиак.
Срок выполнения
1-2 дня
Где можно сдать:
В клинике
На дому
Материал
Моча
Мочевина – конечный продукт белкового обмена, соединение, содержащее азот. Являясь обязательным компонентом любой аминокислоты и белковой молекулы человеческого организма, образует при их распаде свободный азот.
Являясь обязательным компонентом любой аминокислоты и белковой молекулы человеческого организма, образует при их распаде свободный азот.
Срок выполнения
1-2 дня
Где можно сдать:
В клинике
На дому
Материал
Моча
Мочевая кислота образуется в организме после расщепления пуриновых оснований (пуринов). Они входят в состав большинства органов и тканей, где образуют ДНК и РНК.
Срок выполнения
1-2 дня
Где можно сдать:
В клинике
На дому
Материал
Моча
Мочевая кислота – это вещество, которое образуется в результате метаболизма пуринов. Они, в свою очередь, являются основным компонентом ДНК и РНК.
Срок выполнения
1-2 дня
Где можно сдать:
В клинике
На дому
Материал
Моча
Магний – это один из микроэлементов, принимающих участие в большинстве биохимических реакций в организме, в том числе, в энергетическом обмене.
Срок выполнения
1-2 дня
Где можно сдать:
В клинике
На дому
Материал
Моча
Креатинин – это вещество, которое образуется в ходе обмена азотистых соединений. Это, в первую очередь, различные виды белков, нуклеиновые кислоты, некоторые витамины и гормоны.
Срок выполнения
1-2 дня
Где можно сдать:
В клинике
На дому
Материал
Моча
Креатинин – это соединение, которое образуется при распаде креатинфосфата. Этот процесс происходит, в основном, в мышечной ткани, которая требует значительного количества энергии для сокращения.
Срок выполнения
1-2 дня
Где можно сдать:
В клинике
На дому
Материал
Моча
Кальций – один из важнейших минералов. Он обеспечивает прочность костей и зубной эмали, участвует в каскаде реакций, необходимых для передачи нервного импульса и мышечных сокращений, поддерживает способность крови к свертыванию.
Он обеспечивает прочность костей и зубной эмали, участвует в каскаде реакций, необходимых для передачи нервного импульса и мышечных сокращений, поддерживает способность крови к свертыванию.
Срок выполнения
1-2 дня
Где можно сдать:
В клинике
На дому
Материал
Моча
Желчные пигменты представляют собой продукты распада гемоглобина. В норме они в небольшом количестве циркулируют в крови, а затем подвергаются ряду химическим превращениям в печени.
Срок выполнения
1-2 дня
Где можно сдать:
В клинике
На дому
Материал
Моча
Бета-2-микроглобулин – это специфический белок, который входит в состав клеточных мембран. В норме он в небольшом количестве присутствует в сыворотке крови и выделяется с мочой.
Срок выполнения
1-2 дня
Где можно сдать:
В клинике
На дому
Материал
Моча
Амилаза – фермент, вырабатывающийся клетками преимущественно поджелудочной железы, входящий в состав панкреатического сока. Ее функция – расщеплять в кишечнике сложные углеводы до моно- и дисахаридов.
Срок выполнения
1-2 дня
Где можно сдать:
В клинике
На дому
Материал
Моча
Альфа-амилаза – фермент, секретируемый клетками поджелудочной и слюнных желез, выполняющий функцию расщепления сложных углеводов на моно- и дисахара. Панкреатическая амилаза вырабатывается экзокринными панкреатоцитами поджелудочной железы и через протоки выделяется в полость двенадцатиперстной кишки.
Срок выполнения
1-2 дня
Где можно сдать:
В клинике
На дому
Материал
Моча
Альбумины – это растворимые белки, которые синтезируются в печени и участвуют в транспортировке питательных и биологически активных веществ, а также некоторых лекарственных препаратов.
Срок выполнения
1-2 дня
Где можно сдать:
В клинике
На дому
Материал
Моча
Альбумин – это один из основных белков, находящихся в плазме крови. Он принимает участие в транспортировке витаминов, гормонов, билирубина, кальция, натрия, лекарственных препаратов, жирных кислот и других веществ.
Срок выполнения
1-2 дня
Где можно сдать:
В клинике
На дому
Материал
Моча
Показать все
Лицензии
Перейти в раздел лицензииПерейти в раздел правовая информация
Когда при разрыве химических связей выделяется энергия?
Категория: Химия Опубликовано: 27 июня 2013 г.
Разрыв химических связей никогда не высвобождает энергию во внешнюю среду. Энергия высвобождается только при образовании химических связей . В общем, химическая реакция включает две стадии: 1) разрываются исходные химические связи между атомами и 2) образуются новые связи. Эти два шага иногда для простоты объединяют в одно событие, но на самом деле это два отдельных события. Например, когда вы сжигаете метан (природный газ) в своей печи, метан вступает в реакцию с кислородом с образованием углекислого газа и воды. Химики часто записывают это как:
Энергия высвобождается только при образовании химических связей . В общем, химическая реакция включает две стадии: 1) разрываются исходные химические связи между атомами и 2) образуются новые связи. Эти два шага иногда для простоты объединяют в одно событие, но на самом деле это два отдельных события. Например, когда вы сжигаете метан (природный газ) в своей печи, метан вступает в реакцию с кислородом с образованием углекислого газа и воды. Химики часто записывают это как:
CH 4 + 2 O 2 → CO 2 + 2 H 2 O + энергия
Это сбалансированное химическое уравнение описывает химическую реакцию сжигания метана. Реагенты слева, продукты справа, а стрелка показывает момент, когда происходит реакция. Но за этой стрелой происходит много интересного. Более подробное уравнение будет выглядеть примерно так:
Ч. 4 + 2 O 2 + немного энергии → С + 4 Н + 4 О → CO 2 + 2 H 2 O + много энергии
Первая строка уравнения содержит исходные реагенты: молекулы метана и молекулы кислорода.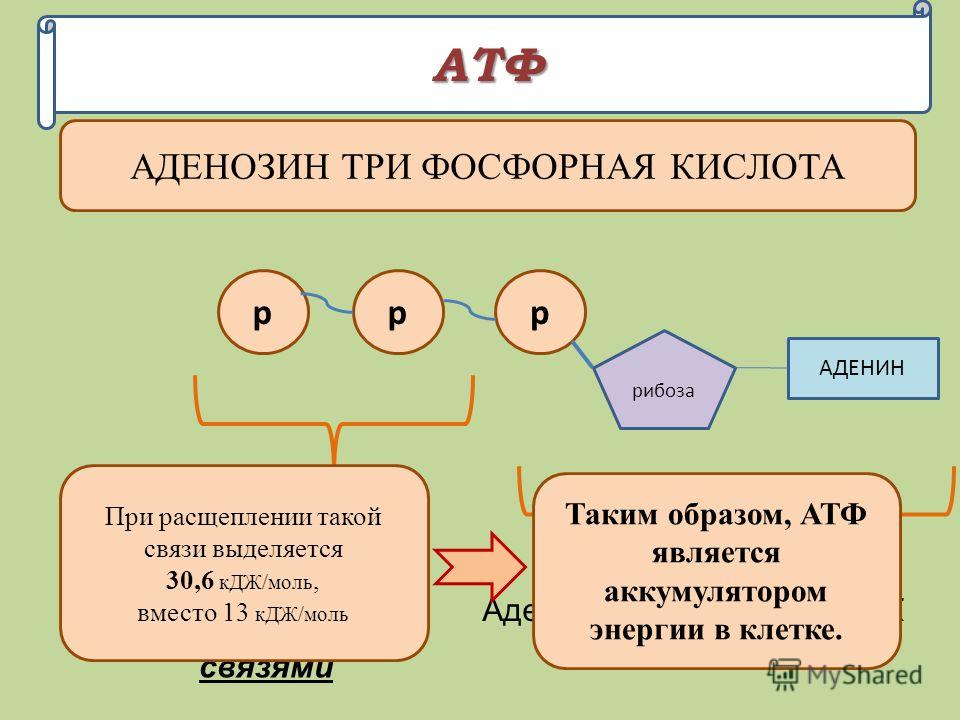 Первая стрелка представляет собой разрыв связей, требующий энергии. На средней линии находятся атомы, теперь отделившиеся от молекул и свободные для реакции. Вторая стрелка представляет собой формирование новых связей. В последней строке находятся конечные продукты. Чтобы запустить реакцию, требуется немного энергии, например искра от воспламенителя в вашей плите. Это связано с тем, что связи должны быть разорваны, прежде чем атомы смогут образовать новые связи, а для разрыва связей всегда требуется энергия. Как только реакция началась, выходная энергия одной сгоревшей молекулы метана становится входной энергией для следующей молекулы. Часть энергии, высвобождаемой каждой связью, которая образуется при образовании углекислого газа и воды, используется для разрыва дополнительных связей в молекулах метана и кислорода. Таким образом, реакция становится самоподдерживающейся (до тех пор, пока продолжают поступать метан и кислород). Зажигалку можно отключить. Если бы разрыв связей не требовал энергии, то топливу не требовалось бы устройство зажигания, чтобы начать гореть.
Первая стрелка представляет собой разрыв связей, требующий энергии. На средней линии находятся атомы, теперь отделившиеся от молекул и свободные для реакции. Вторая стрелка представляет собой формирование новых связей. В последней строке находятся конечные продукты. Чтобы запустить реакцию, требуется немного энергии, например искра от воспламенителя в вашей плите. Это связано с тем, что связи должны быть разорваны, прежде чем атомы смогут образовать новые связи, а для разрыва связей всегда требуется энергия. Как только реакция началась, выходная энергия одной сгоревшей молекулы метана становится входной энергией для следующей молекулы. Часть энергии, высвобождаемой каждой связью, которая образуется при образовании углекислого газа и воды, используется для разрыва дополнительных связей в молекулах метана и кислорода. Таким образом, реакция становится самоподдерживающейся (до тех пор, пока продолжают поступать метан и кислород). Зажигалку можно отключить. Если бы разрыв связей не требовал энергии, то топливу не требовалось бы устройство зажигания, чтобы начать гореть.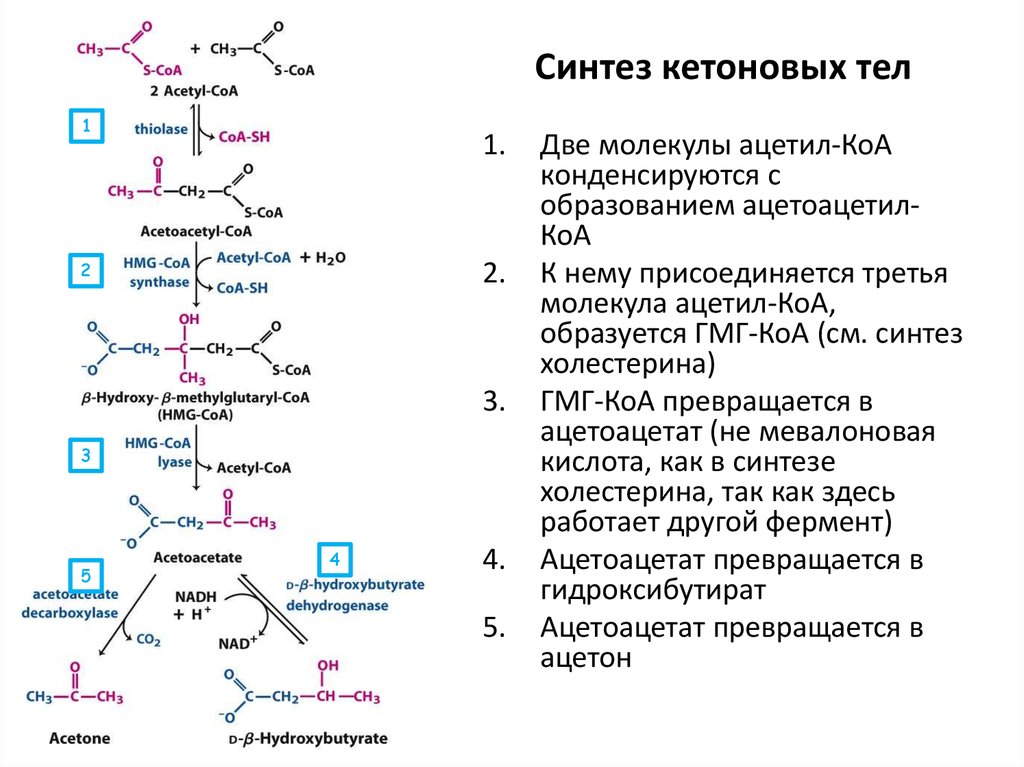 Они просто начнут гореть сами по себе. Наличие свечей зажигания в вашем автомобиле свидетельствует о том, что для разрыва химических связей требуется энергия. (Обратите внимание, что сжигание метана на самом деле включает в себя множество более мелких стадий, поэтому вышеприведенное уравнение можно было бы расширить до еще более подробных деталей.)
Они просто начнут гореть сами по себе. Наличие свечей зажигания в вашем автомобиле свидетельствует о том, что для разрыва химических связей требуется энергия. (Обратите внимание, что сжигание метана на самом деле включает в себя множество более мелких стадий, поэтому вышеприведенное уравнение можно было бы расширить до еще более подробных деталей.)
В учебнике Advanced Biology Майкла Робертса, Майкла Джонатана Рейсса и Грейс Монгер указано:
Биологи часто говорят об энергии, которая становится доступной при расщеплении сахара, подразумевая, что разрыв химических связей в молекулах сахара высвобождает энергию. И все же из химии мы узнаем, что энергия высвобождается не тогда, когда химические связи разрываются , а когда они образуются . На самом деле дыхание поставляет энергию не за счет разрыва связей в субстрате, а за счет образования прочных связей в продуктах. Однако общим результатом процесса является выделение энергии, и именно в этом смысле биологи говорят о распаде сахара, дающем энергию.
Для сжигания пропана требуется воспламенитель, чтобы запустить реакцию, потому что химические связи должны быть разрушены, прежде чем могут образоваться новые, а для разрыва связей всегда требуется энергия. Изображение общественного достояния, источник: Кристофер С. Бэрд.
Полная энергия, вводимая или выводимая в ходе реакции, равна энергии, выделившейся при образовании новых связей, за вычетом энергии, затраченной на разрыв первоначальных связей. Если для разрыва первоначальных связей требуется на энергии больше, чем выделяется при образовании новых связей, то чистая энергия реакции отрицательна. Это означает, что для продолжения реакции в систему необходимо накачивать энергию. Такие реакции называются эндотермическими. Если если занимает меньше энергии на разрыва первоначальных связей, чем высвобождается при образовании новых связей, то чистая энергия реакции положительна. Этот факт означает, что энергия будет утекать из системы по мере протекания реакции. Этот факт также означает, что реакция может протекать сама по себе без какой-либо внешней энергии после ее начала. Такие реакции известны как экзотермические. (Эндотермические реакции также могут протекать сами по себе, если для поглощения достаточно внешней энергии в виде окружающего тепла.) Экзотермические реакции имеют тенденцию нагревать окружающую среду, в то время как эндотермические реакции имеют тенденцию охлаждать ее. Сжигание топлива является экзотермическим, потому что есть чистое выделение энергии. Приготовление яйца является эндотермическим процессом, потому что для приготовления яйца требуется чистая энергия. Суть в том, что как эндотермические, так и экзотермические реакции включают разрыв связей, и поэтому обе требуют энергии для начала.
Этот факт также означает, что реакция может протекать сама по себе без какой-либо внешней энергии после ее начала. Такие реакции известны как экзотермические. (Эндотермические реакции также могут протекать сами по себе, если для поглощения достаточно внешней энергии в виде окружающего тепла.) Экзотермические реакции имеют тенденцию нагревать окружающую среду, в то время как эндотермические реакции имеют тенденцию охлаждать ее. Сжигание топлива является экзотермическим, потому что есть чистое выделение энергии. Приготовление яйца является эндотермическим процессом, потому что для приготовления яйца требуется чистая энергия. Суть в том, что как эндотермические, так и экзотермические реакции включают разрыв связей, и поэтому обе требуют энергии для начала.
Понятно, что разрыв связей всегда требует энергии. Химическая связь удерживает два атома вместе. Чтобы разорвать связь, вы должны бороться с ней, как будто растягиваете резиновую ленту, пока она не порвется. Это требует энергии. В качестве аналогии представьте атомы в виде баскетбольных мячей. Думайте об энергетическом ландшафте химических связей как о холмистой местности, по которой катятся баскетбольные мячи. Когда два шара помещаются рядом с круглым отверстием, гравитация тянет их вниз, где они встречаются и останавливаются. Два шара теперь остаются близко друг к другу из-за формы отверстия и силы тяжести. Это похоже на химическую связь, объединяющую атомы. Чтобы развести шарики друг от друга (чтобы разорвать связи), вы должны закатать их в противоположные стороны лунки. Требуется энергия вашей руки, толкающей шарики, чтобы они поднялись по краям лунки и разошлись. Энергия, которую вы вкладываете в систему, чтобы разорвать шары, теперь хранится в виде потенциальной энергии в шарах. Атомы в буквальном смысле не катятся вверх и вниз по холмам, но они ведут себя так, будто движутся в энергетическом ландшафте, очень похожем на настоящие холмы.
В качестве аналогии представьте атомы в виде баскетбольных мячей. Думайте об энергетическом ландшафте химических связей как о холмистой местности, по которой катятся баскетбольные мячи. Когда два шара помещаются рядом с круглым отверстием, гравитация тянет их вниз, где они встречаются и останавливаются. Два шара теперь остаются близко друг к другу из-за формы отверстия и силы тяжести. Это похоже на химическую связь, объединяющую атомы. Чтобы развести шарики друг от друга (чтобы разорвать связи), вы должны закатать их в противоположные стороны лунки. Требуется энергия вашей руки, толкающей шарики, чтобы они поднялись по краям лунки и разошлись. Энергия, которую вы вкладываете в систему, чтобы разорвать шары, теперь хранится в виде потенциальной энергии в шарах. Атомы в буквальном смысле не катятся вверх и вниз по холмам, но они ведут себя так, будто движутся в энергетическом ландшафте, очень похожем на настоящие холмы.
Темы: связь, связи, химическая связь, химическая реакция, эндотермическая, энергия, экзотермическая, реакция
Энергии связи — Химия LibreTexts
- Последнее обновление
- Сохранить как PDF
- Идентификатор страницы
- 1981
Атомы соединяются вместе, образуя соединения, потому что при этом они достигают более низких энергий, чем те, которыми они обладают как отдельные атомы. Количество энергии, равное разности энергий связанных атомов и энергий разъединенных атомов, выделяется обычно в виде тепла. То есть связанные атомы имеют более низкую энергию, чем отдельные атомы. Когда атомы объединяются в соединение, всегда выделяется энергия, и соединение имеет более низкую общую энергию.
Количество энергии, равное разности энергий связанных атомов и энергий разъединенных атомов, выделяется обычно в виде тепла. То есть связанные атомы имеют более низкую энергию, чем отдельные атомы. Когда атомы объединяются в соединение, всегда выделяется энергия, и соединение имеет более низкую общую энергию.
Когда происходит химическая реакция, молекулярные связи разрываются и образуются другие связи, образующие другие молекулы. Например, связи двух молекул воды разрываются с образованием водорода и кислорода.
\[ 2H_2O \стрелка вправо 2H_2 + O_2\]
Для разрыва связи всегда требуется энергия, известная как энергия связи. Хотя концепция может показаться простой, энергия связи служит очень важной цели при описании структуры и характеристик молекулы. Его можно использовать для определения наиболее подходящей точечной структуры Льюиса при наличии нескольких точечных структур Льюиса.
Чтобы разорвать связь, всегда требуется энергия.
Энергия высвобождается при образовании связи.
Хотя каждая молекула имеет свою характеристическую энергию связи, возможны некоторые обобщения. Например, хотя точное значение энергии связи C–H зависит от конкретной молекулы, все связи C–H имеют энергию связи примерно одинакового значения, поскольку все они являются связями C–H. Чтобы разорвать 1 моль связи С-Н, требуется примерно 100 ккал энергии, поэтому мы говорим об энергии связи связи С-Н, равной примерно 100 ккал/моль. Связь C – C имеет приблизительную энергию связи 80 ккал / моль, а C = C имеет энергию связи около 145 ккал / моль. Мы можем рассчитать более общую энергию связи, найдя среднее значение энергии связи конкретной связи в разных молекулах, чтобы получить среднюю энергию связи.
| Одинарные облигации | Множественные облигации | ||||||
|---|---|---|---|---|---|---|---|
| В—В | 432 | Н—Х | 391 | И—Я | 149 | С = С | 614 |
| В—Ф | 565 | Н—Н | 160 | I—Кл | 208 | С ≡ С | 839 |
| H—Cl | 427 | Н—Ф | 272 | И—Бр | 175 | О = О | 495 |
| H—Br | 363 | N—Cl | 200 | С = О* | 745 | ||
| H—I | 295 | Н—Бр | 243 | Ш-В | 347 | С ≡ О | 1072 |
| Н—О | 201 | Ю-Ф | 327 | Н = О | 607 | ||
| К—Ч | 413 | О—Н | 467 | S—Cl | 253 | Н = Н | 418 |
| К—К | 347 | О—О | 146 | S—Br | 218 | Н ≡ Н | 941 |
| C—N | 305 | О-Ф | 190 | СС | 266 | С ≡ С | 891 |
| К—О | 358 | O—Cl | 203 | С = Н | 615 | ||
| C—F | 485 | О—И | 234 | Si—Si | 340 | ||
| C—Cl | 339 | Si-H | 393 | ||||
| C—Br | 276 | Ф—Ф | 154 | Si-C | 360 | ||
| С—Я | 240 | F—Cl | 253 | Si-O | 452 | ||
| К—С | 259 | Ф—Бр | 237 | ||||
| Кл—Кл | 239 | ||||||
| Cl—Br | 218 | ||||||
| Бр—Бр | 193 | ||||||
*C == O(CO 2 ) = 799 | |||||||
Когда связь прочная, энергия связи выше, поскольку для ее разрыва требуется больше энергии. Это коррелирует с порядком связи и длиной связи. Когда порядок связи выше, длина связи короче, и чем короче длина связи, тем больше энергия связи из-за увеличения электрического притяжения. В общем чем короче длина связи, тем больше энергия связи.
Это коррелирует с порядком связи и длиной связи. Когда порядок связи выше, длина связи короче, и чем короче длина связи, тем больше энергия связи из-за увеличения электрического притяжения. В общем чем короче длина связи, тем больше энергия связи.
Средние энергии связи в таблице T3 являются средними значениями энергии диссоциации связи. Например, средняя энергия связи O-H в H 2 O составляет 464 кДж/моль. Это связано с тем, что для диссоциации связи Н-ОН требуется 498,7 кДж/моль, а связи ОН — 428 кДж/моль.
\[\dfrac{498.7\; кДж/моль + 428\; кДж/моль}{2}=464\; кДж/моль\]
Когда принимается во внимание большее количество энергий связи в различных молекулах, среднее значение будет более точным. Однако
- Средние значения связей не так точны, как удельная энергия диссоциации связи молекулы.
- Двойные связи имеют более высокую энергию связи по сравнению с одинарной связью (но не обязательно в 2 раза выше).
- Тройные связи имеют даже более высокую энергию, чем двойные и одинарные связи (но не обязательно в 3 раза выше).

Разрыв и образование связи
Когда происходит химическая реакция, атомы в реагентах перестраивают свои химические связи с образованием продуктов. Новое расположение связей не имеет такой же полной энергии, как связи в реагентах. Поэтому, когда происходят химические реакции, всегда будет сопровождать изменение энергии .
Рисунок 1: ( слева ) Экзотермические реакции. При экзотермической химической реакции энергия выделяется по мере того, как реагенты превращаются в продукты. (справа) Эндотермические реакции. Для эндотермической химической реакции энергия поглощается по мере того, как реагенты превращаются в продукты. В некоторых реакциях энергия продуктов меньше энергии реагентов. Таким образом, в ходе реакции вещества отдают энергию окружающей среде. Такие реакции являются экзотермическими и могут быть представлены 9Диаграмма уровней энергии 0005 на рисунке 1 (слева). В большинстве случаев энергия выделяется в виде тепла (хотя в некоторых реакциях энергия выделяется в виде света). В химических реакциях, где продукты имеют более высокую энергию, чем реагенты, реагенты должны поглощать энергию из окружающей среды, чтобы вступить в реакцию. Эти реакции являются эндотермическими и могут быть представлены диаграммами энергетических уровней, как на рисунке 1 (справа).
В химических реакциях, где продукты имеют более высокую энергию, чем реагенты, реагенты должны поглощать энергию из окружающей среды, чтобы вступить в реакцию. Эти реакции являются эндотермическими и могут быть представлены диаграммами энергетических уровней, как на рисунке 1 (справа).
Технически температура не является ни реагентом, ни продуктом
Нередко в учебниках и преподавателях тепло рассматривается как самостоятельный «вид» реакции. Хотя это совершенно неверно, потому что нельзя «добавить или убрать тепло» к реакции, как в случае с частицами, это служит удобным механизмом для предсказания сдвига реакций при изменении температуры. Например, если теплота является «реагентом» (\(\Delta{H} > 0 \)), то реакция способствует образованию продуктов при повышенной температуре. Точно так же, если теплота является «продуктом» (\(\Delta{H} < 0 \)), то реакция способствует образованию реагентов. Более точное и, следовательно, предпочтительное описание обсуждается ниже.
Экзотермические и эндотермические реакции можно рассматривать как имеющие энергию либо как «продукт» реакции, либо как «реагент». Экзотермические реакции высвобождают энергию, поэтому энергия является продуктом. Эндотермические реакции требуют энергии, поэтому энергия является реагентом.
Экзотермические реакции высвобождают энергию, поэтому энергия является продуктом. Эндотермические реакции требуют энергии, поэтому энергия является реагентом.
Пример \(\PageIndex{1}\): Экзотермическая или эндотермическая
Является ли каждая химическая реакция экзотермической или эндотермической?
- \(2H_{2(г)} + O_{2(г)} \rightarrow 2H_2O_{(ℓ)} + \text{135 ккал}\)
- \(N_{2(г)} + O_{2(г)} + \text{45 ккал} \rightarrow 2NO_{(г)}\)
- Потому что высвобождается энергия; эта реакция экзотермическая.
- Потому что энергия поглощается; эта реакция эндотермическая.
Упражнение \(\PageIndex{1}\)
Если энергия связи для H-Cl составляет 431 кДж/моль. Какова общая энергия связи 2 молей HCl?
Ответ
Просто умножьте среднюю энергию связи H-Cl на 2. Получится 862 кДж/моль (таблица T3).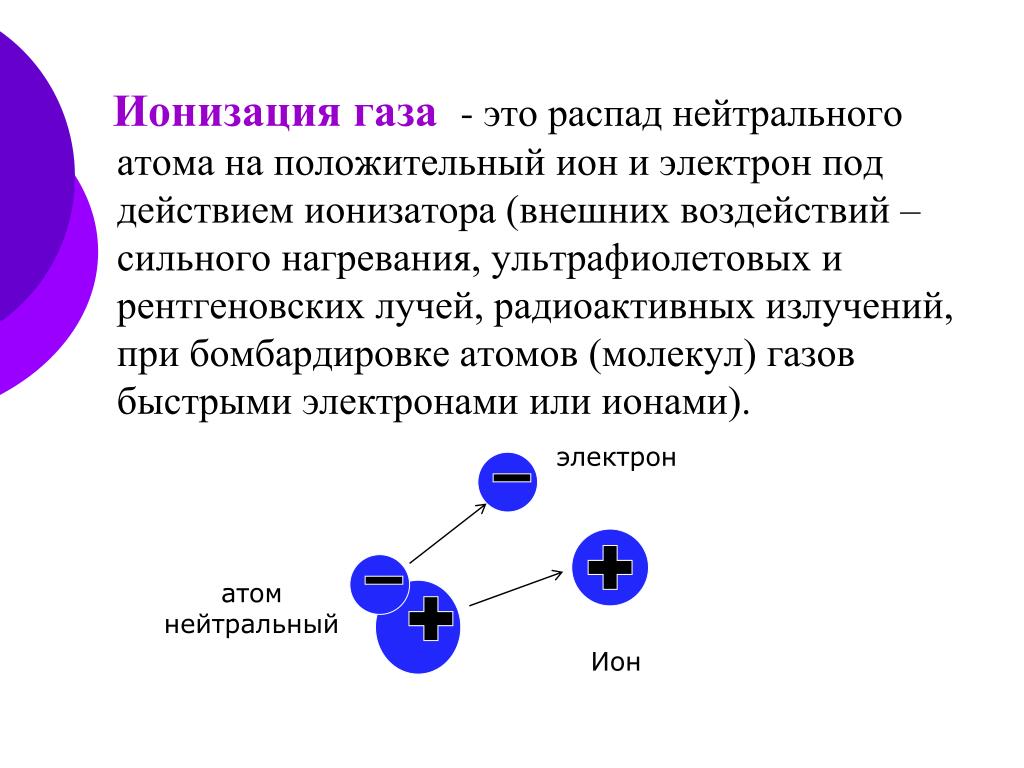
Пример \(\PageIndex{2}\): Получение йодистого водорода
Чему равно изменение энтальпии этой реакции и является ли она эндотермической или экзотермической?
\[H_2(g)+I_2(g) \rightarrow 2HI(g)\]
Решение
Сначала посмотрите на уравнение и определите, какие связи существуют в реагентах.
- одна связь H-H и
- одна облигация I-I
Теперь сделайте то же самое для продуктов
- две связи H-I
Затем определите энергии этих связей из таблицы выше:
- H-H связи: 436 кДж/моль
- I-I связи: 151 кДж/моль
Сумма энтальпий на стороне реакции:
436 кДж/моль + 151 кДж/моль = 587 кДж/моль.
Это количество энергии, необходимое для разрыва связей на стороне реагента. Затем смотрим на образование связи со стороны продукта:
- 2 моль H-I связи: 297 кДж/моль
Сумма энтальпий на стороне продукта:
2 x 297 кДж/моль = 594 кДж/моль
Это количество энергии высвобождается при образовании связей на стороне продукта. Таким образом, чистое изменение реакции составляет
Таким образом, чистое изменение реакции составляет
587-594 = -7 кДж/моль.
Поскольку результат отрицательный, реакция экзотермическая .
Пример \(\PageIndex{2}\): Разложение воды
Используя энергию связи, приведенную в таблице выше, найдите изменение энтальпии термического разложения воды:
\[ 2H_2O (г) \rightarrow 2H_2 + O_2 (г) \]
Реакция, описанная выше, экзотермическая или эндотермическая? Объяснять.
Раствор
Изменение энтальпии связано с разрывом двух молей связей O-H и образованием 1 моля связей O-O и двух молей связей H-H (таблица T3).
- Сумма энергий, необходимых для разрыва связей на стороне реагентов, составляет 4 x 460 кДж/моль = 1840 кДж/моль.
- Сумма энергий, выделяемых для образования связей на стороне продуктов, равна
- 2 моля связей Н-Н = 2 x 436,4 кДж/моль = 872,8 кДж/моль
- 1 моль связи O=O = 1 x 498,7 кДж/мил = 498,7 кДж/моль
что является выходной (высвобождаемой) энергией = 872,8 кДж/моль + 498,7 кДж/моль = 1371,5 кДж/моль.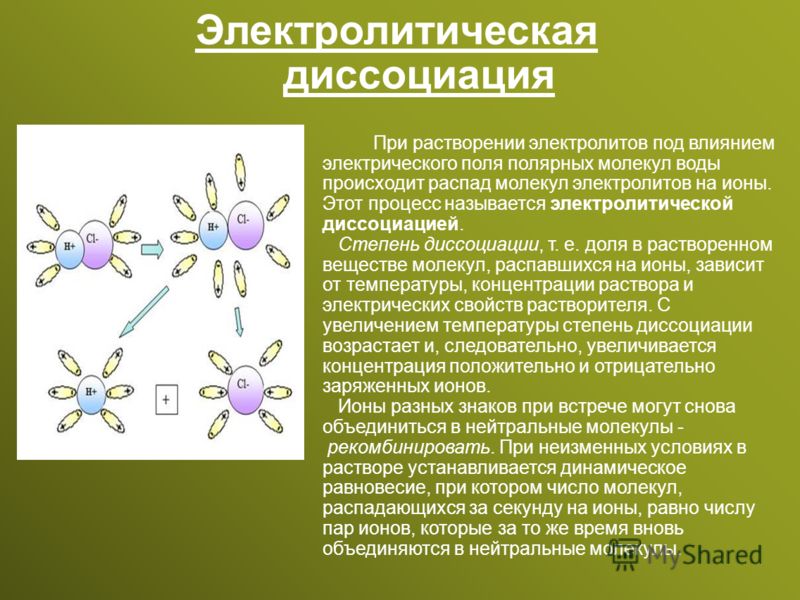
Полная разность энергий составляет 1840 кДж/моль – 1371,5 кДж/моль = 469 кДж/моль, что указывает на то, что реакция является эндотермической и что для проведения этой реакции необходимо подать 469 кДж тепла.
Эта реакция является эндотермической, поскольку для образования связей требуется энергия.
Резюме
Энергия высвобождается для образования связей, поэтому изменение энтальпии разрыва связей положительно. Для разрыва связей требуется энергия. Атомы намного счастливее, когда они «женятся» и высвобождают энергию, потому что легче и стабильнее находиться в отношениях (например, генерировать электронные конфигурации из октетов ). Изменение энтальпии отрицательно, потому что система высвобождает энергию при образовании связи.
Ссылки
- Петруччи, Ральф Х., Харвуд, Уильям С., Херринг, Ф. Г. и Мадура Джеффри Д. Общая химия: принципы и современные приложения. 9изд. Река Аппер-Сэдл: Pearson Education, Inc., 2007. .
- Каррут, Гортон, Эрлих, Юджин. «Энергия связи». Библиотека томов. Эд. Каррут, Гортон. Том 1. Теннесси: Юго-запад, 2002. .
- Больше практических задач: http://www.chalkbored.com/lessons/chemistry-11/bond-energies-worksheet.pdf

Авторы и ссылки
- Ким Сон (UCD), Дональд Ле (UCD)
Bond Energies распространяется по незадекларированной лицензии, автором, ремиксом и/или куратором является LibreTexts.
- Наверх
- Была ли эта статья полезной?
- Тип изделия
- Раздел или страница
- Показать страницу TOC
- нет на странице
- Метки

4.1 Энергия и обмен веществ – концепции биологии – 1-е канадское издание
Перейти к содержанию
Глава 4. Введение в то, как клетки получают энергию
Цели обучения
К концу этого раздела вы сможете:
- Объяснять, что такое метаболические пути
- Назовите первый и второй законы термодинамики
- Объясните разницу между кинетической и потенциальной энергией
- Опишите эндергонические и экзергонические реакции
- Обсудите, как ферменты функционируют как молекулярные катализаторы
Посмотрите видео о гетеротрофах.
Ученые используют термин биоэнергетика для описания концепции потока энергии (рис. 4.2) через живые системы, такие как клетки. Клеточные процессы , такие как построение и разрушение сложных молекул , происходят посредством ступенчатых химических реакций . Некоторые из этих химических реакций протекают самопроизвольно и высвобождают энергию, тогда как для протекания других требуется энергия. Точно так же, как живые существа должны постоянно потреблять пищу, чтобы пополнять свои запасы энергии, клетки должны постоянно производить больше энергии, чтобы пополнить ту, которая используется многими постоянно происходящими химическими реакциями, требующими энергии. Вместе все химические реакции, протекающие внутри клеток, в том числе те, которые потребляют или вырабатывают энергию, называются клеточный метаболизм .
Некоторые из этих химических реакций протекают самопроизвольно и высвобождают энергию, тогда как для протекания других требуется энергия. Точно так же, как живые существа должны постоянно потреблять пищу, чтобы пополнять свои запасы энергии, клетки должны постоянно производить больше энергии, чтобы пополнить ту, которая используется многими постоянно происходящими химическими реакциями, требующими энергии. Вместе все химические реакции, протекающие внутри клеток, в том числе те, которые потребляют или вырабатывают энергию, называются клеточный метаболизм .
Рассмотрим метаболизм сахара. Это классический пример одного из многих клеточных процессов, использующих и производящих энергию.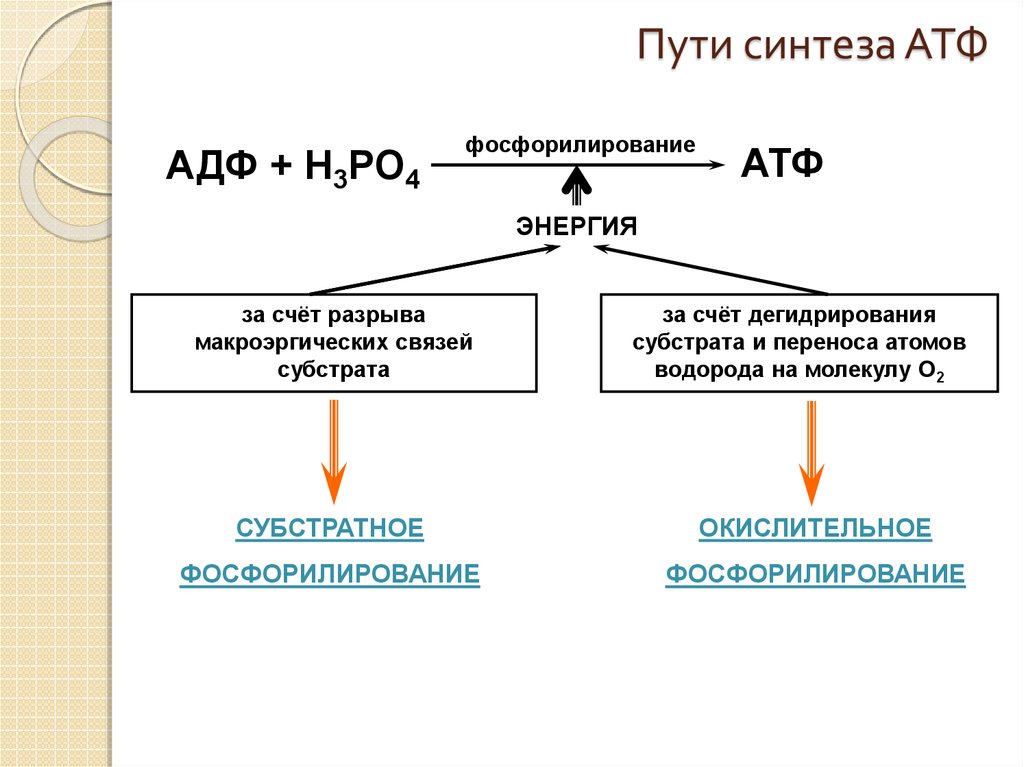 Живые существа потребляют сахара в качестве основного источника энергии, потому что молекулы сахара имеют большое количество энергии, хранящейся в их связях. По большей части фотосинтезирующие организмы, такие как растения, производят эти сахара. Во время фотосинтеза растения используют энергию (первоначально солнечного света) для преобразования углекислого газа (CO 2 ) на молекулы сахара (например, глюкоза: C 6 H 12 O 6 ). Они потребляют углекислый газ и производят кислород в качестве побочного продукта. Эта реакция резюмируется как:
Живые существа потребляют сахара в качестве основного источника энергии, потому что молекулы сахара имеют большое количество энергии, хранящейся в их связях. По большей части фотосинтезирующие организмы, такие как растения, производят эти сахара. Во время фотосинтеза растения используют энергию (первоначально солнечного света) для преобразования углекислого газа (CO 2 ) на молекулы сахара (например, глюкоза: C 6 H 12 O 6 ). Они потребляют углекислый газ и производят кислород в качестве побочного продукта. Эта реакция резюмируется как:
6CO 2 + 6H 2 O + энергия ——-> C 6 H 12 O 6 + 6O 2
Поскольку этот процесс включает в себя синтез молекулы, запасающей энергию, для его продолжения требуется затрата энергии. В световых реакциях фотосинтеза энергия обеспечивается молекулой под названием аденозинтрифосфат (АТФ) , которая является основной энергетической валютой всех клеток.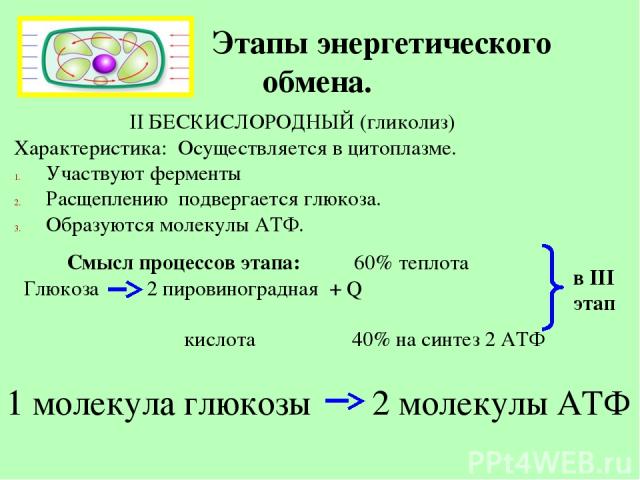 Точно так же, как доллар используется в качестве валюты для покупки товаров, клетки используют молекулы АТФ в качестве энергетической валюты для выполнения непосредственной работы. Напротив, молекулы-аккумуляторы энергии, такие как глюкоза, потребляются только для того, чтобы расщепляться для использования своей энергии. Реакция, которая собирает энергию молекулы сахара в клетках, нуждающихся в кислороде для выживания, может быть обобщена как реакция, обратная фотосинтезу. В этой реакции потребляется кислород, а в качестве побочного продукта выделяется углекислый газ. Реакция резюмируется как:
Точно так же, как доллар используется в качестве валюты для покупки товаров, клетки используют молекулы АТФ в качестве энергетической валюты для выполнения непосредственной работы. Напротив, молекулы-аккумуляторы энергии, такие как глюкоза, потребляются только для того, чтобы расщепляться для использования своей энергии. Реакция, которая собирает энергию молекулы сахара в клетках, нуждающихся в кислороде для выживания, может быть обобщена как реакция, обратная фотосинтезу. В этой реакции потребляется кислород, а в качестве побочного продукта выделяется углекислый газ. Реакция резюмируется как:
C 6 H 12 O 6 + 6O 2 —> 6CO 2 + 6H 2 O + энергия
Обе эти реакции включают много стадий.
Процессы создания и расщепления молекул сахара иллюстрируют два примера метаболических путей. Метаболический путь представляет собой серию химических реакций, в которых исходная молекула шаг за шагом модифицируется через ряд метаболических промежуточных продуктов, в конечном итоге давая конечный продукт. В примере метаболизма сахара первый метаболический путь синтезирует сахар из более мелких молекул, а другой путь расщепляет сахар на более мелкие молекулы. Эти два противоположных процесса — первый, требующий энергии, и второй, производящий энергию, — называются анаболические пути (строительные полимеры) и катаболические пути (расщепление полимеров на их мономеры) соответственно. Следовательно, метаболизм состоит из синтеза (анаболизма) и деградации (катаболизма) (рис. 4.3).
В примере метаболизма сахара первый метаболический путь синтезирует сахар из более мелких молекул, а другой путь расщепляет сахар на более мелкие молекулы. Эти два противоположных процесса — первый, требующий энергии, и второй, производящий энергию, — называются анаболические пути (строительные полимеры) и катаболические пути (расщепление полимеров на их мономеры) соответственно. Следовательно, метаболизм состоит из синтеза (анаболизма) и деградации (катаболизма) (рис. 4.3).
Важно знать, что химические реакции метаболических путей не происходят сами по себе. Каждый этап реакции облегчается или катализируется белком, называемым ферментом. Ферменты важны для катализа всех типов биологических реакций — те, которые требуют энергии, а также те, которые высвобождают энергию.
Рис. 4.3. Катаболические пути — это те, которые вырабатывают энергию за счет расщепления более крупных молекул. Анаболические пути — это те, которые требуют энергии для синтеза более крупных молекул. Оба типа путей необходимы для поддержания энергетического баланса клетки.
Оба типа путей необходимы для поддержания энергетического баланса клетки.Термодинамика относится к изучению энергии и передачи энергии с участием физической материи. Материя, относящаяся к конкретному случаю передачи энергии, называется системой, а все, что находится вне этой материи, — окружающей средой. Например, при нагревании кастрюли с водой на плите система включает плиту, кастрюлю и воду. Энергия передается внутри системы (между плитой, кастрюлей и водой). Существует два типа систем: открытые и закрытые. В открытой системе возможен обмен энергией с окружающей средой. Система плиты открыта, потому что тепло может отдаваться воздуху. Замкнутая система не может обмениваться энергией с окружающей средой.
Биологические организмы являются открытыми системами. Между ними и их окружением происходит обмен энергией, поскольку они используют энергию солнца для фотосинтеза или потребляют молекулы, хранящие энергию, и выделяют энергию в окружающую среду, выполняя работу и выделяя тепло.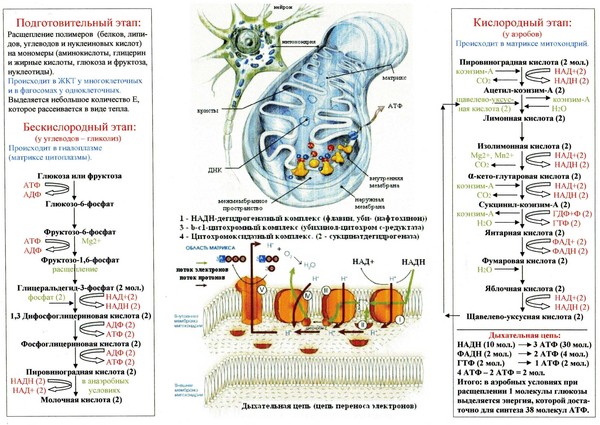 Как и все вещи в физическом мире, энергия подчиняется физическим законам. Законы термодинамики управляют передачей энергии во всех системах во Вселенной и между ними.
Как и все вещи в физическом мире, энергия подчиняется физическим законам. Законы термодинамики управляют передачей энергии во всех системах во Вселенной и между ними.
В целом энергия определяется как способность выполнять работу или создавать какие-либо изменения. Энергия существует в разных формах. Например, электрическая энергия, световая энергия и тепловая энергия — это разные виды энергии. Чтобы понять, как энергия поступает в биологические системы и выходит из них, важно понимать два физических закона, управляющих энергией.
Первый закон термодинамики гласит, что общее количество энергии во Вселенной постоянно и сохраняется. Другими словами, во Вселенной всегда было и всегда будет одинаковое количество энергии. Энергия существует во многих различных формах . Согласно первому закону термодинамики, энергия может передаваться с места на место или преобразовываться в различные формы , но не может быть создана или уничтожена . Передачи и преобразования энергии происходят вокруг нас все время.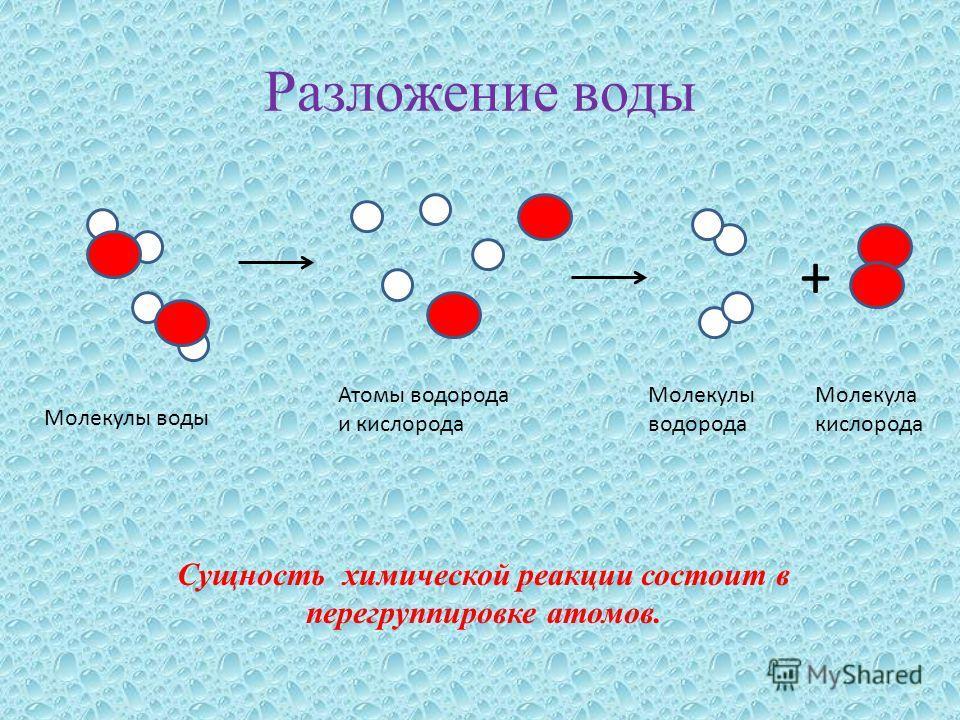 Лампочки преобразуют электрическую энергию в световую и тепловую энергию. Газовые плиты преобразуют химическую энергию природного газа в тепловую энергию. Растения осуществляют одно из наиболее биологически полезных преобразований энергии на Земле: преобразование энергии солнечного света в химическую энергию, хранящуюся в органических молекулах (рис. 4.2). Некоторые примеры преобразования энергии показаны на рис. 4.4.
Лампочки преобразуют электрическую энергию в световую и тепловую энергию. Газовые плиты преобразуют химическую энергию природного газа в тепловую энергию. Растения осуществляют одно из наиболее биологически полезных преобразований энергии на Земле: преобразование энергии солнечного света в химическую энергию, хранящуюся в органических молекулах (рис. 4.2). Некоторые примеры преобразования энергии показаны на рис. 4.4.
Задача всех живых организмов состоит в том, чтобы получать энергию из своего окружения в формах, которые они могут передавать или преобразовывать в полезную энергию для выполнения работы. Живые клетки эволюционировали, чтобы справиться с этой задачей. Химическая энергия, хранящаяся в органических молекулах, таких как сахара и жиры, передается и трансформируется посредством ряда клеточных химических реакций в энергию внутри молекул АТФ. Энергия молекул АТФ легко доступна для выполнения работы. Примеры типов работы, которую должны выполнять клетки, включают построение сложных молекул, транспортировку материалов, обеспечение движения ресничек или жгутиков и сокращение мышечных волокон для создания движения.
На рис. 4.4 показаны некоторые примеры передачи и преобразования энергии из одной системы в другую и из одной формы в другую. Пища, которую мы потребляем, обеспечивает наши клетки энергией, необходимой для выполнения функций организма, точно так же, как световая энергия дает растениям средства для создания необходимой им химической энергии. (кредит «мороженое»: модификация работы Д. Шэрон Прюитт; кредит «дети»: модификация работы Макса из Провиденса; кредит «лист»: модификация работы Кори Занкера)
Основные задачи живой клетки по получению, преобразованию и использованию энергии для выполнения работы могут показаться простыми. Однако второй закон термодинамики объясняет, почему эти задачи сложнее, чем кажутся. Все передачи и преобразования энергии никогда не бывают полностью эффективными . При каждой передаче энергии некоторое количество энергии теряется в непригодной для использования форме. В большинстве случаев такой формой является тепловая энергия. Термодинамически тепловая энергия определяется как энергия, передаваемая от одной системы к другой, которая не является работой. Например, когда включается лампочка, часть энергии, преобразуемой из электрической энергии в световую, теряется в виде тепловой энергии. Точно так же часть энергии теряется в виде тепловой энергии во время клеточных метаболических реакций.
Термодинамически тепловая энергия определяется как энергия, передаваемая от одной системы к другой, которая не является работой. Например, когда включается лампочка, часть энергии, преобразуемой из электрической энергии в световую, теряется в виде тепловой энергии. Точно так же часть энергии теряется в виде тепловой энергии во время клеточных метаболических реакций.
Важным понятием в физических системах является порядок и беспорядок. Чем больше энергии теряет система в своем окружении, тем менее упорядоченной и более случайной является система. Ученые называют мерой случайности или беспорядка в системе энтропию . Высокая энтропия означает высокий беспорядок и низкую энергию. Молекулы и химические реакции также имеют разную энтропию. Например, энтропия увеличивается по мере того, как молекулы с высокой концентрацией в одном месте диффундируют и распространяются. Второй закон термодинамики гласит, что энергия всегда будет теряться в виде тепла при передаче или превращении энергии.
Живые существа высоко упорядочены, и им требуется постоянное потребление энергии для поддержания состояния низкой энтропии.
Когда объект находится в движении, с ним связана энергия. Подумайте о разрушающем шаре. Даже медленно движущийся шар-разрушитель может нанести большой ущерб другим объектам. Энергия, связанная с движущимися объектами, называется кинетической энергией (рис. 4.5). Мчащаяся пуля, идущий человек и быстрое движение молекул в воздухе (выделяющее тепло) — все они обладают кинетической энергией.
А что, если тот самый неподвижный шар-вредитель поднять краном на два этажа над землей? Если подвешенный разрушающий шар неподвижен, связана ли с ним энергия? Ответ положительный. Энергия, необходимая для подъема шара-разрушителя, не исчезла, а теперь запасена в шаре-разрушителе благодаря его положению и действующей на него силе тяжести. Этот вид энергии называется потенциальной энергией (рис. 4.5). Если мяч упадет, потенциальная энергия будет преобразована в кинетическую энергию до тех пор, пока вся потенциальная энергия не будет исчерпана, когда мяч покоится на земле.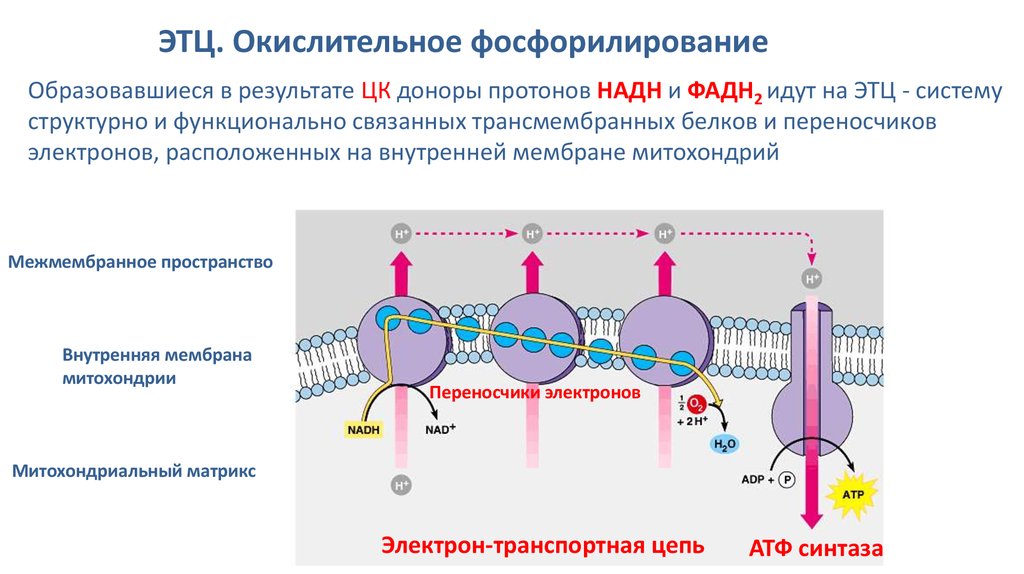 Разрушительные шары также качаются, как маятник; во время качелей происходит постоянное изменение потенциальной энергии (наибольшей в верхней части качелей) на кинетическую энергию (наибольшей в нижней части качелей). Другие примеры потенциальной энергии включают энергию воды, удерживаемой за плотиной, или энергию человека, собирающегося прыгнуть с парашютом из самолета.
Разрушительные шары также качаются, как маятник; во время качелей происходит постоянное изменение потенциальной энергии (наибольшей в верхней части качелей) на кинетическую энергию (наибольшей в нижней части качелей). Другие примеры потенциальной энергии включают энергию воды, удерживаемой за плотиной, или энергию человека, собирающегося прыгнуть с парашютом из самолета.
Потенциальная энергия связана не только с расположением материи, но и со структурой материи. Даже пружина на земле обладает потенциальной энергией, если ее сжать; то же самое делает и натянутая резинка. На молекулярном уровне связи, удерживающие атомы молекул вместе, существуют в определенной структуре, обладающей потенциальной энергией. Помните, что анаболические клеточные пути требуют энергии для синтеза сложных молекул из более простых, а катаболические пути высвобождают энергию при расщеплении сложных молекул. Тот факт, что энергия может высвобождаться при разрыве определенных химических связей, подразумевает, что эти связи обладают потенциальной энергией. На самом деле существует потенциальная энергия, хранящаяся в связях всех пищевых молекул, которые мы едим, и которая в конечном итоге используется для использования. Это потому, что эти связи могут высвобождать энергию при разрыве. Тип потенциальной энергии, которая существует внутри химических связей и высвобождается, когда эти связи разрываются, называется химической энергией. Химическая энергия отвечает за обеспечение живых клеток энергией из пищи. Высвобождение энергии происходит при разрыве молекулярных связей внутри молекул пищи.
Тот факт, что энергия может высвобождаться при разрыве определенных химических связей, подразумевает, что эти связи обладают потенциальной энергией. На самом деле существует потенциальная энергия, хранящаяся в связях всех пищевых молекул, которые мы едим, и которая в конечном итоге используется для использования. Это потому, что эти связи могут высвобождать энергию при разрыве. Тип потенциальной энергии, которая существует внутри химических связей и высвобождается, когда эти связи разрываются, называется химической энергией. Химическая энергия отвечает за обеспечение живых клеток энергией из пищи. Высвобождение энергии происходит при разрыве молекулярных связей внутри молекул пищи.
Посмотрите видео о килокалориях.
Концепция в действии
Посетите сайт и выберите «Маятник» в меню «Работа и энергия», чтобы увидеть изменение кинетической и потенциальной энергии маятника в движении.
Узнав, что химические реакции высвобождают энергию, когда разрушаются энергосберегающие связи, следующий важный вопрос заключается в следующем: как определяется и выражается энергия, связанная с этими химическими реакциями? Как можно сравнить энергию, выделяющуюся в одной реакции, с энергией другой реакции? Измерение свободной энергии используется для количественной оценки этих передач энергии. Вспомним, что согласно второму закону термодинамики все передачи энергии связаны с потерей некоторого количества энергии в непригодной для использования форме, такой как тепло. Свободная энергия конкретно относится к энергии, связанной с химической реакцией, которая доступна после учета потерь. Другими словами, свободная энергия — это полезная энергия, или энергия, доступная для выполнения работы.
Вспомним, что согласно второму закону термодинамики все передачи энергии связаны с потерей некоторого количества энергии в непригодной для использования форме, такой как тепло. Свободная энергия конкретно относится к энергии, связанной с химической реакцией, которая доступна после учета потерь. Другими словами, свободная энергия — это полезная энергия, или энергия, доступная для выполнения работы.
Если в ходе химической реакции выделяется энергия, то изменение свободной энергии, обозначаемое как ∆G (дельта G), будет отрицательным числом. Отрицательное изменение свободной энергии также означает, что продукты реакции имеют меньшую свободную энергию, чем реагенты, потому что они выделяют некоторую свободную энергию во время реакции. Реакции, которые вызывают отрицательное изменение свободной энергии и, следовательно, высвобождение свободной энергии, называются экзергоническими реакциями. Подумайте: ex ergonic означает, что энергия равна ex запускает систему.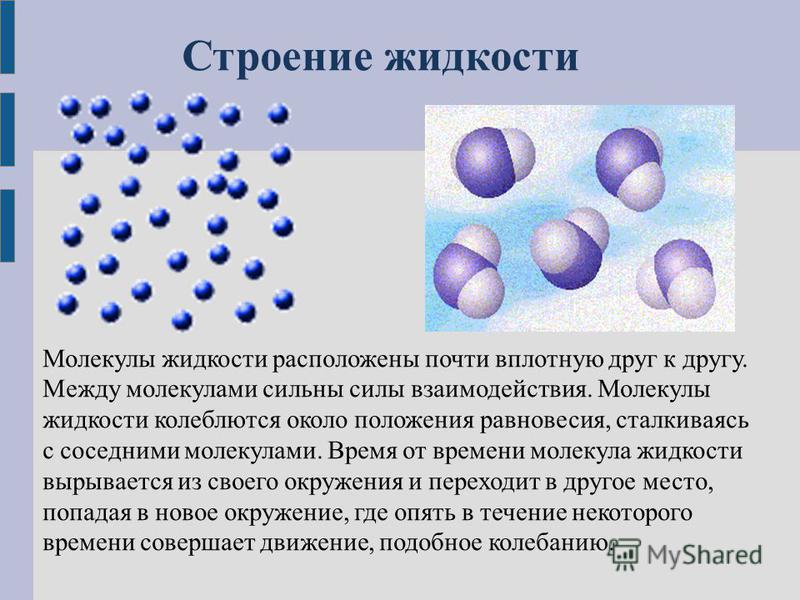 Эти реакции также называют самопроизвольными реакциями, и их продукты имеют меньший запас энергии, чем реагенты. Необходимо провести важное различие между термином «самопроизвольно» и идеей химической реакции, протекающей немедленно. Вопреки повседневному использованию этого термина спонтанная реакция не возникает внезапно или быстро. Ржавление железа является примером спонтанной реакции, которая происходит медленно, мало-помалу, с течением времени.
Эти реакции также называют самопроизвольными реакциями, и их продукты имеют меньший запас энергии, чем реагенты. Необходимо провести важное различие между термином «самопроизвольно» и идеей химической реакции, протекающей немедленно. Вопреки повседневному использованию этого термина спонтанная реакция не возникает внезапно или быстро. Ржавление железа является примером спонтанной реакции, которая происходит медленно, мало-помалу, с течением времени.
Если химическая реакция поглощает энергию, а не высвобождает энергию в балансе, то ∆G для этой реакции будет положительным значением. В этом случае продукты имеют больше свободной энергии, чем реагенты. Таким образом, продукты этих реакций можно рассматривать как запасающие энергию молекулы. Эти химические реакции называются эндергоническими реакциями и являются неспонтанными . Эндергоническая реакция не будет происходить сама по себе без добавления свободной энергии.
На рис. 4.
 6 показаны некоторые примеры эндергонических процессов (тех, которые требуют энергии) и экзергонических процессов (тех, которые высвобождают энергию). (кредит a: модификация работы Натали Мейнор; кредит b: модификация работы USDA; кредит c: модификация работы Кори Занкера; кредит d: модификация работы Гарри Мальша)
6 показаны некоторые примеры эндергонических процессов (тех, которые требуют энергии) и экзергонических процессов (тех, которые высвобождают энергию). (кредит a: модификация работы Натали Мейнор; кредит b: модификация работы USDA; кредит c: модификация работы Кори Занкера; кредит d: модификация работы Гарри Мальша)Посмотрите на каждый из показанных процессов и решите если он эндергонический или экзергонический.
Существует еще одна важная концепция, которую следует учитывать в отношении эндергонических и экзергонических реакций. Экзергонические реакции требуют небольшого количества энергии для запуска, прежде чем они смогут продолжить свои этапы высвобождения энергии. Эти реакции имеют чистое высвобождение энергии, но все же требуют некоторого подвода энергии в начале. Это небольшое количество энергии, необходимое для протекания всех химических реакций, называется энергией активации.
Концепция в действии
Посмотрите анимацию перехода от свободной энергии к переходному состоянию реакции.
Вещество, которое способствует протеканию химической реакции, называется катализатором, а молекулы, катализирующие биохимические реакции, называются ферментами. Большинство ферментов являются белками и выполняют важнейшую задачу по снижению энергии активации химических реакций внутри клетки. Большинство критических для живой клетки реакций протекают слишком медленно при нормальных температурах, чтобы быть полезными для клетки. Без ферментов до ускорить эти реакции , жизнь не может продолжаться. Ферменты делают это, связываясь с молекулами реагентов и удерживая их таким образом, чтобы облегчить процессы разрыва и образования химических связей. Важно помнить, что ферменты не изменяются, является ли реакция экзергонической (спонтанной) или эндергонической. Это потому, что они не изменяют свободную энергию реагентов или продуктов. Они лишь уменьшают энергию активации, необходимую для протекания реакции (рис. 4.7). Кроме того, сам фермент не изменяется в ходе реакции, которую он катализирует. После катализа одной реакции фермент может участвовать в других реакциях.
После катализа одной реакции фермент может участвовать в других реакциях.
Химические реагенты, с которыми связывается фермент, называются субстратами фермента. В зависимости от конкретной химической реакции может быть один или несколько субстратов. В некоторых реакциях один реагент-субстрат распадается на несколько продуктов. В других случаях два субстрата могут объединяться, образуя одну большую молекулу. Два реагента также могут вступить в реакцию и оба измениться, но они покинут реакцию как два продукта. Место внутри фермента, где связывается субстрат, называется ферментным 9-узлом.0101 активный сайт . Активный сайт — это место, где происходит «действие». Поскольку ферменты представляют собой белки, в активном центре имеется уникальная комбинация боковых цепей аминокислот. Каждая боковая цепь характеризуется различными свойствами. Они могут быть большими или маленькими, слабокислыми или основными, гидрофильными или гидрофобными, положительно или отрицательно заряженными или нейтральными.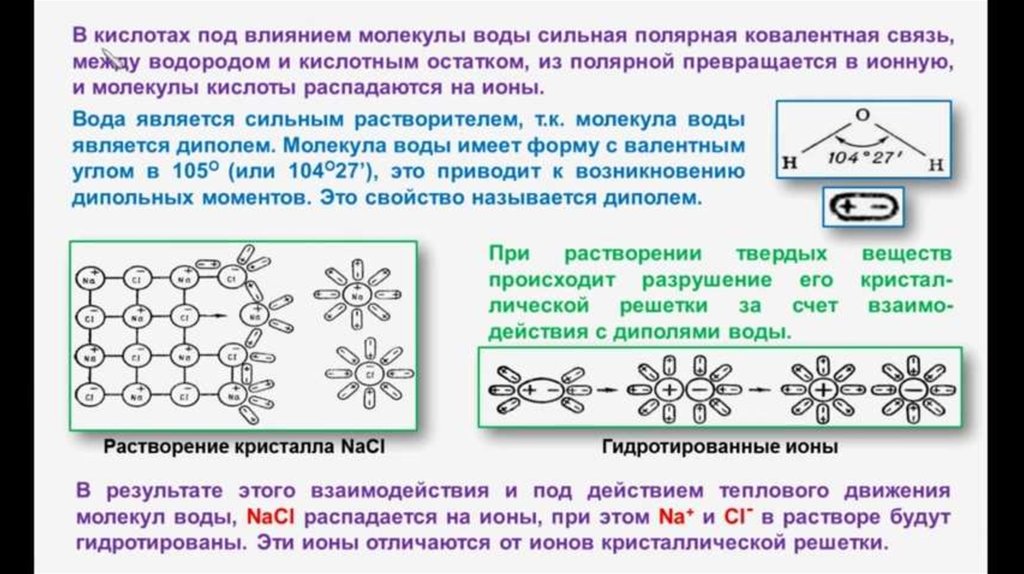 Уникальная комбинация боковых цепей создает очень специфическую химическую среду в активном центре. Эта конкретная среда подходит для связывания с одним конкретным химическим субстратом (или субстратами).
Уникальная комбинация боковых цепей создает очень специфическую химическую среду в активном центре. Эта конкретная среда подходит для связывания с одним конкретным химическим субстратом (или субстратами).
Активные сайты подвержены влиянию местной среды. Повышение температуры окружающей среды обычно увеличивает скорость реакции, катализируемой ферментами или иным образом. Однако температуры за пределами оптимального диапазона снижают скорость, с которой фермент катализирует реакцию. Горячие температуры в конечном итоге вызовут денатурацию ферментов, необратимое изменение трехмерной формы и, следовательно, функции фермента. Ферменты также подходят для наилучшего функционирования в пределах определенного диапазона pH и концентрации соли, и, как и в случае с температурой, экстремальный pH и концентрация соли могут вызвать денатурацию ферментов.
В течение многих лет ученые считали, что связывание фермента с субстратом происходит простым способом «замок и ключ». Эта модель утверждала, что фермент и субстрат идеально сочетаются друг с другом за один мгновенный шаг. Однако текущие исследования поддерживают модель, называемую индуцированной подгонкой (рис. 4.8). Модель индуцированного соответствия расширяет модель «замок и ключ», описывая более динамичное связывание между ферментом и субстратом. Когда фермент и субстрат объединяются, их взаимодействие вызывает небольшой сдвиг в структуре фермента, который формирует идеальную схему связывания между ферментом и субстратом.
Однако текущие исследования поддерживают модель, называемую индуцированной подгонкой (рис. 4.8). Модель индуцированного соответствия расширяет модель «замок и ключ», описывая более динамичное связывание между ферментом и субстратом. Когда фермент и субстрат объединяются, их взаимодействие вызывает небольшой сдвиг в структуре фермента, который формирует идеальную схему связывания между ферментом и субстратом.
Концепция в действии
Просмотрите анимацию индуцированной посадки.
Когда фермент связывается со своим субстратом, образуется фермент-субстратный комплекс. Этот комплекс снижает энергию активации реакции и способствует ее быстрому протеканию одним из многих возможных путей. На базовом уровне ферменты способствуют химическим реакциям, в которых участвует более одного субстрата, объединяя субстраты в оптимальной для реакции ориентации. Другой способ, с помощью которого ферменты способствуют реакции своих субстратов, заключается в создании оптимальной среды в активном центре для протекания реакции.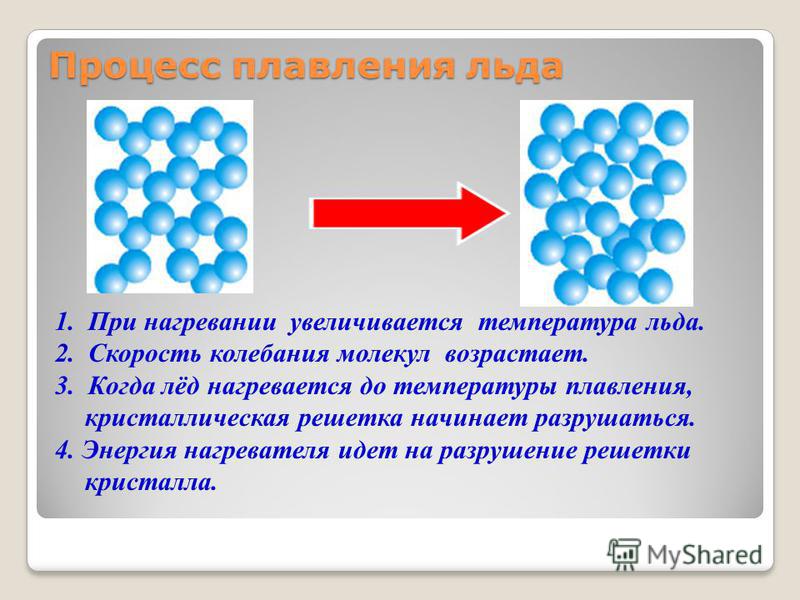 Химические свойства, возникающие из-за особого расположения аминокислотных групп R в активном центре, создают идеальную среду для реакции специфических субстратов фермента.
Химические свойства, возникающие из-за особого расположения аминокислотных групп R в активном центре, создают идеальную среду для реакции специфических субстратов фермента.
Комплекс фермент-субстрат также может снижать энергию активации, нарушая структуру связи, чтобы ее было легче разорвать. Наконец, ферменты также могут снижать энергию активации, участвуя в самой химической реакции. В этих случаях важно помнить, что фермент всегда возвращается в исходное состояние по завершении реакции. Одним из отличительных свойств ферментов является то, что они в конечном счете остаются неизменными в реакциях, которые они катализируют. После того, как фермент катализирует реакцию, он высвобождает свой продукт (продукты) и может катализировать новую реакцию.
Рисунок 4.8. Модель индуцированного соответствия представляет собой корректировку модели «замок и ключ» и объясняет, как ферменты и субстраты претерпевают динамические модификации во время переходного состояния, чтобы увеличить сродство субстрата к активному центру.
Казалось бы идеальным сценарий, при котором все ферменты организма существовали бы в изобилии и функционировали оптимально во всех клеточных условиях, во всех клетках, во все времена. Однако различные механизмы гарантируют, что этого не произойдет. Клеточные потребности и условия постоянно варьируются от клетки к клетке и меняются внутри отдельных клеток с течением времени. Необходимые ферменты клеток желудка отличаются от ферментов клеток хранения жира, клеток кожи, клеток крови и нервных клеток. Кроме того, клетки органов пищеварения работают гораздо усерднее, перерабатывая и расщепляя питательные вещества в течение времени, которое следует за приемом пищи, по сравнению со многими часами после приема пищи. Поскольку эти клеточные потребности и условия различаются, должны различаться количество и функциональность различных ферментов.
Поскольку скорость биохимических реакций контролируется энергией активации, а ферменты снижают и определяют энергию активации химических реакций, относительное количество и функционирование различных ферментов в клетке в конечном итоге определяют, какие реакции будут протекать и с какой скоростью.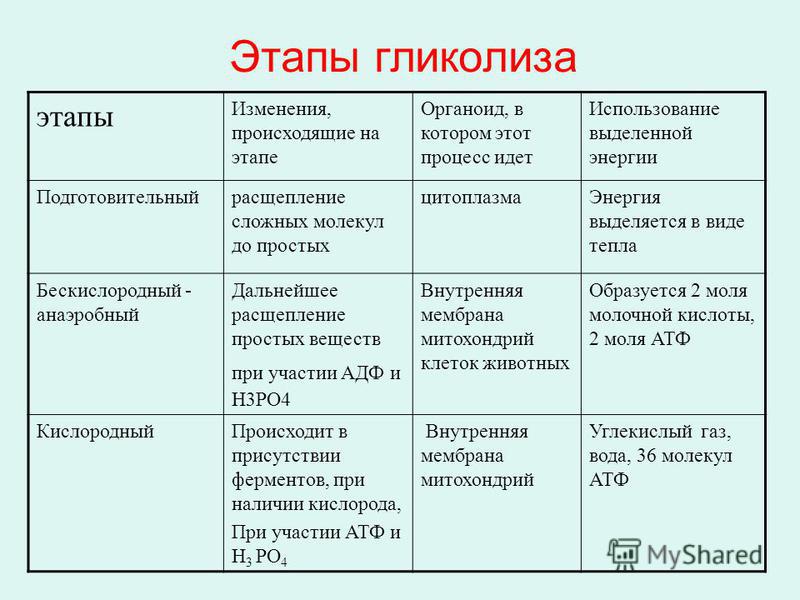 Это определение строго контролируется в клетках. В определенных клеточных средах активность ферментов частично контролируется такими факторами окружающей среды, как pH, температура, концентрация соли и, в некоторых случаях, кофакторами или коферментами.
Это определение строго контролируется в клетках. В определенных клеточных средах активность ферментов частично контролируется такими факторами окружающей среды, как pH, температура, концентрация соли и, в некоторых случаях, кофакторами или коферментами.
Ферменты также можно регулировать таким образом, чтобы стимулировать или снижать активность ферментов. Существует много видов молекул, которые ингибируют или стимулируют функцию фермента, и различные механизмы, с помощью которых они это делают. В некоторых случаях ингибирования фермента молекула ингибитора достаточно похожа на субстрат, поэтому она может связываться с активным центром и просто блокировать связывание субстрата. Когда это происходит, фермент ингибируется посредством конкурентного ингибирования , потому что молекула ингибитора конкурирует с субстратом за связывание с активным центром.
С другой стороны, при неконкурентном ингибировании молекула ингибитора связывается с ферментом в месте, отличном от активного сайта, называемого аллостерическим сайтом , но все же удается блокировать связывание субстрата с активным сайтом. Некоторые молекулы-ингибиторы связываются с ферментами в местах, где их связывание вызывает конформационные изменения, снижающие сродство фермента к его субстрату. Этот тип торможения называется аллостерическим торможением (рис. 4.9). Большинство аллостерически регулируемых ферментов состоят из более чем одного полипептида, а это означает, что они имеют более одной белковой субъединицы. Когда аллостерический ингибитор связывается с участком фермента, все активные центры белковых субъединиц слегка изменяются, так что они связывают свои субстраты с меньшей эффективностью. Существуют аллостерические активаторы, а также ингибиторы. Аллостерические активаторы связываются с участками фермента, удаленными от активного центра, вызывая конформационные изменения, повышающие сродство активного(ых) центра(ов) фермента к его субстрату(ам) (рис. 4.9).).
Некоторые молекулы-ингибиторы связываются с ферментами в местах, где их связывание вызывает конформационные изменения, снижающие сродство фермента к его субстрату. Этот тип торможения называется аллостерическим торможением (рис. 4.9). Большинство аллостерически регулируемых ферментов состоят из более чем одного полипептида, а это означает, что они имеют более одной белковой субъединицы. Когда аллостерический ингибитор связывается с участком фермента, все активные центры белковых субъединиц слегка изменяются, так что они связывают свои субстраты с меньшей эффективностью. Существуют аллостерические активаторы, а также ингибиторы. Аллостерические активаторы связываются с участками фермента, удаленными от активного центра, вызывая конформационные изменения, повышающие сродство активного(ых) центра(ов) фермента к его субстрату(ам) (рис. 4.9).).
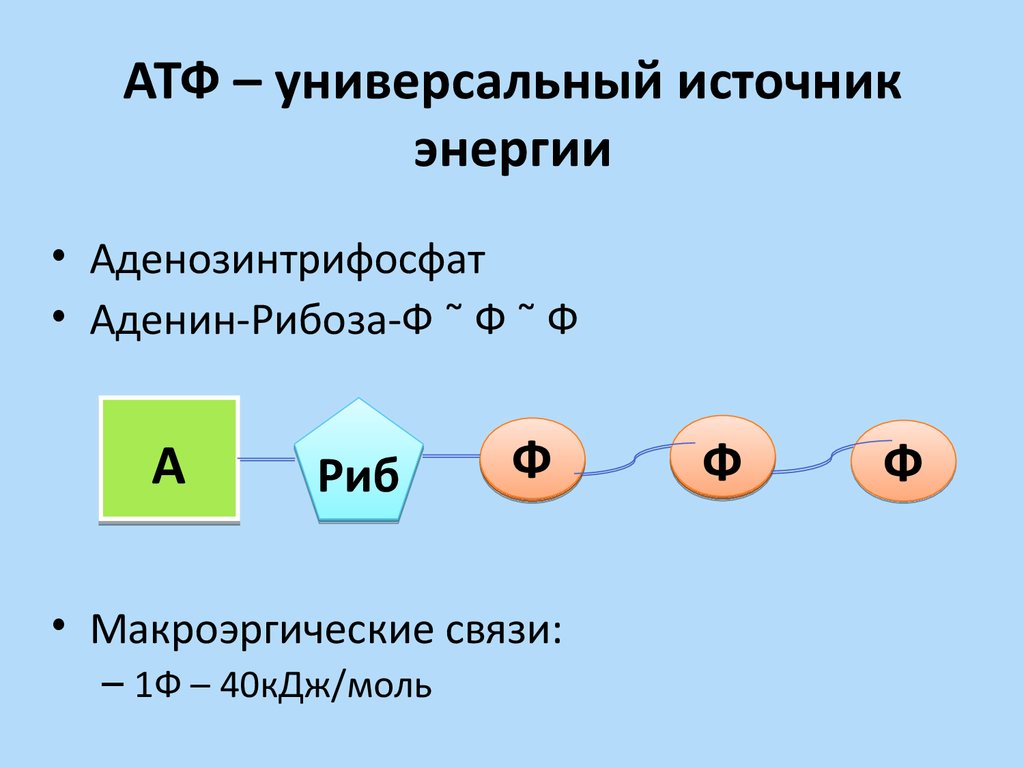 Напротив, при аллостерической активации молекула активатора изменяет форму активного центра, чтобы обеспечить лучшее прилегание к субстрату.
Напротив, при аллостерической активации молекула активатора изменяет форму активного центра, чтобы обеспечить лучшее прилегание к субстрату.Через призму коренных народов
Растения не могут убегать или прятаться от своих хищников и разработали множество стратегий, чтобы отпугнуть тех, кто их съест. Подумайте о шипах, раздражителях и вторичных метаболитах: это соединения, которые напрямую не помогают растению расти, но созданы специально для защиты от хищников. Вторичные метаболиты — наиболее распространенный способ, с помощью которого растения отпугивают хищников. Некоторыми примерами вторичных метаболитов являются атропин, никотин, ТГК и кофеин. Люди обнаружили, что эти соединения вторичного метаболита являются богатым источником материалов для лекарств. Подсчитано, что 90% лекарств в современной фармации имеют свои «корни» в этих вторичных метаболитах.
Лечение травами первых людей открыло миру эти вторичные метаболиты. Например, коренные народы издавна использовали кору ивы и ольхи для приготовления чая, тонизирующего средства или припарки для уменьшения воспаления.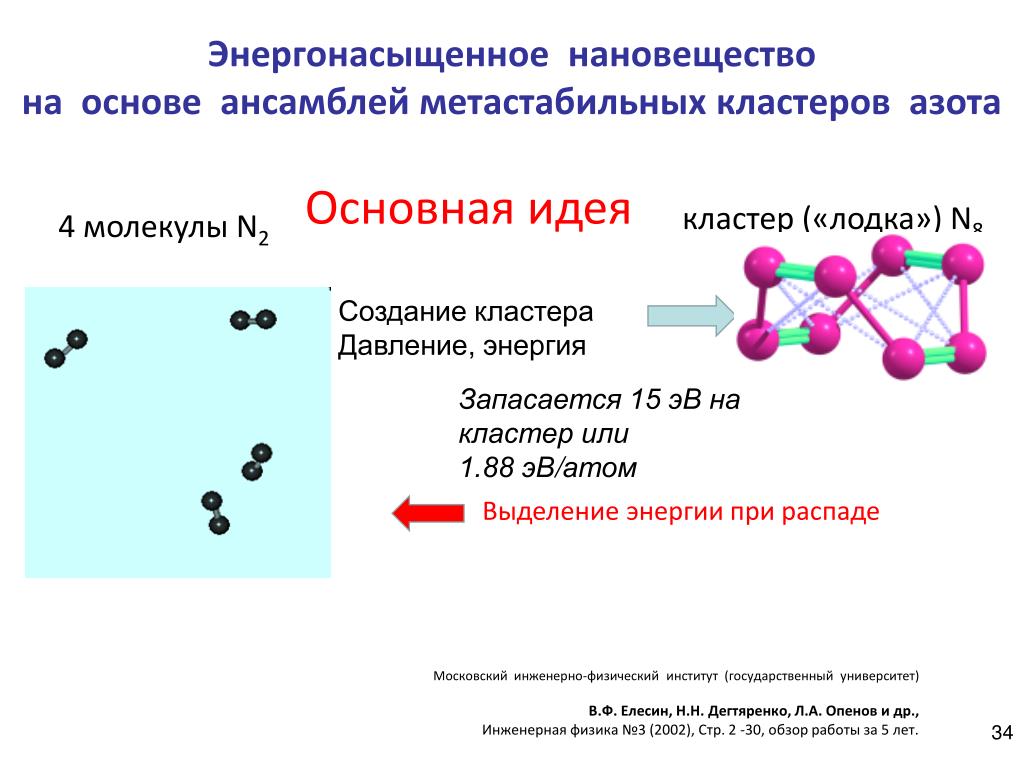 Вы узнаете больше о воспалительной реакции иммунной системы в главе 11.
Вы узнаете больше о воспалительной реакции иммунной системы в главе 11.
Рис. 4.10. Кора тихоокеанской ивы содержит соединение салицин.
Кора ивы и ольхи содержит соединение салицин. У большинства из нас это соединение есть в аптечке в виде салициловой кислоты или аспирина. Доказано, что аспирин уменьшает боль и воспаление, а в наших клетках салицин превращается в салициловую кислоту.
Так как же это работает? Салицин или аспирин действуют как ингибиторы ферментов. В воспалительной реакции два фермента, ЦОГ1 и ЦОГ2, играют ключевую роль в этом процессе. Салицин или аспирин специфически модифицируют аминокислоту (серин) в активном центре этих двух родственных ферментов. Эта модификация активных центров не позволяет нормальному субстрату связываться, поэтому воспалительный процесс прерывается. Как вы прочитали в этой главе, это делает его конкурентоспособным ингибитором ферментов.
Разработчик фармацевтических препаратов
Рисунок 4.11 Задумывались ли вы когда-нибудь, как разрабатываются фармацевтические препараты? (кредит: Дебора Остин) Ферменты являются ключевыми компонентами метаболических путей. Понимание того, как работают ферменты и как их можно регулировать, является ключевым принципом разработки многих фармацевтических препаратов, представленных сегодня на рынке. Биологи, работающие в этой области, совместно с другими учеными разрабатывают лекарства (рис. 4.11).
Понимание того, как работают ферменты и как их можно регулировать, является ключевым принципом разработки многих фармацевтических препаратов, представленных сегодня на рынке. Биологи, работающие в этой области, совместно с другими учеными разрабатывают лекарства (рис. 4.11).
Возьмем, к примеру, статины. Статины — это название, данное одному классу препаратов, которые могут снижать уровень холестерина. Эти соединения являются ингибиторами фермента ГМГ-КоА-редуктазы, фермента, который синтезирует холестерин из липидов в организме. Ингибируя этот фермент, можно снизить уровень холестерина, синтезируемого в организме. Точно так же ацетаминофен, широко продаваемый под торговой маркой Тайленол, является ингибитором фермента циклооксигеназы. Хотя он используется для облегчения лихорадки и воспаления (боли), его механизм действия до сих пор полностью не изучен.
Как изобретаются наркотики? Одной из самых больших проблем при открытии лекарств является определение мишени для лекарства. Лекарственная мишень — это молекула, которая буквально является мишенью лекарства. В случае статинов мишенью является ГМГ-КоА-редуктаза. Мишени для наркотиков идентифицируются путем кропотливых исследований в лаборатории. Одной идентификации цели недостаточно; ученым также необходимо знать, как мишень действует внутри клетки и какие реакции идут наперекосяк в случае болезни. Как только цель и путь определены, начинается фактический процесс разработки лекарства. На этом этапе химики и биологи работают вместе, чтобы разработать и синтезировать молекулы, которые могут блокировать или активировать определенную реакцию. Однако это только начало: если и когда прототип лекарства успешно выполняет свою функцию, он подвергается многочисленным испытаниям, от экспериментов in vitro до клинических испытаний, прежде чем он сможет получить одобрение от Управления по санитарному надзору за качеством пищевых продуктов и медикаментов США. магазин.
Лекарственная мишень — это молекула, которая буквально является мишенью лекарства. В случае статинов мишенью является ГМГ-КоА-редуктаза. Мишени для наркотиков идентифицируются путем кропотливых исследований в лаборатории. Одной идентификации цели недостаточно; ученым также необходимо знать, как мишень действует внутри клетки и какие реакции идут наперекосяк в случае болезни. Как только цель и путь определены, начинается фактический процесс разработки лекарства. На этом этапе химики и биологи работают вместе, чтобы разработать и синтезировать молекулы, которые могут блокировать или активировать определенную реакцию. Однако это только начало: если и когда прототип лекарства успешно выполняет свою функцию, он подвергается многочисленным испытаниям, от экспериментов in vitro до клинических испытаний, прежде чем он сможет получить одобрение от Управления по санитарному надзору за качеством пищевых продуктов и медикаментов США. магазин.
Многие ферменты не работают оптимально или вообще не работают, если они не связаны с другими специфическими небелковыми вспомогательными молекулами. Они могут связываться либо временно через ионные или водородные связи, либо постоянно через более сильные ковалентные связи. Связывание с этими молекулами способствует оптимальной форме и функционированию соответствующих ферментов. Двумя примерами этих типов вспомогательных молекул являются кофакторы и коферменты. Кофакторы представляют собой неорганические ионы, такие как ионы железа и магния. Коэнзимы — это органические вспомогательные молекулы, основная атомная структура которых состоит из углерода и водорода. Подобно ферментам, эти молекулы участвуют в реакциях, сами не изменяясь, и в конечном итоге перерабатываются и используются повторно. Витамины являются источником коферментов. Некоторые витамины являются предшественниками коферментов, а другие действуют непосредственно как коферменты. Витамин С является прямым коферментом для множества ферментов, которые принимают участие в построении важной соединительной ткани, коллагена. Следовательно, функция ферментов частично регулируется обилием различных кофакторов и коферментов, которые могут поступать с пищей организма или, в некоторых случаях, вырабатываться организмом.
Они могут связываться либо временно через ионные или водородные связи, либо постоянно через более сильные ковалентные связи. Связывание с этими молекулами способствует оптимальной форме и функционированию соответствующих ферментов. Двумя примерами этих типов вспомогательных молекул являются кофакторы и коферменты. Кофакторы представляют собой неорганические ионы, такие как ионы железа и магния. Коэнзимы — это органические вспомогательные молекулы, основная атомная структура которых состоит из углерода и водорода. Подобно ферментам, эти молекулы участвуют в реакциях, сами не изменяясь, и в конечном итоге перерабатываются и используются повторно. Витамины являются источником коферментов. Некоторые витамины являются предшественниками коферментов, а другие действуют непосредственно как коферменты. Витамин С является прямым коферментом для множества ферментов, которые принимают участие в построении важной соединительной ткани, коллагена. Следовательно, функция ферментов частично регулируется обилием различных кофакторов и коферментов, которые могут поступать с пищей организма или, в некоторых случаях, вырабатываться организмом.
Ингибирование обратной связи в метаболических путях
Молекулы могут регулировать функцию ферментов разными способами. Однако остается главный вопрос: что это за молекулы и откуда они берутся? Как вы узнали, некоторые из них являются кофакторами и коферментами. Какие другие молекулы в клетке обеспечивают ферментативную регуляцию, такую как аллостерическая модуляция, конкурентное и неконкурентное ингибирование? Возможно, наиболее важными источниками регуляторных молекул в отношении ферментативного клеточного метаболизма являются продукты самих клеточных метаболических реакций. Наиболее эффективным и элегантным способом клетки научились использовать продукты своих собственных реакций для ингибирования активности ферментов по принципу обратной связи. Ингибирование с обратной связью предполагает использование продукта реакции для регуляции собственного дальнейшего производства (рис. 4.12). Клетка реагирует на обилие продуктов замедлением производства во время анаболических или катаболических реакций. Такие продукты реакции могут ингибировать ферменты, катализирующие их продукцию, посредством механизмов, описанных выше.
Ингибирование с обратной связью предполагает использование продукта реакции для регуляции собственного дальнейшего производства (рис. 4.12). Клетка реагирует на обилие продуктов замедлением производства во время анаболических или катаболических реакций. Такие продукты реакции могут ингибировать ферменты, катализирующие их продукцию, посредством механизмов, описанных выше.
Производство как аминокислот, так и нуклеотидов контролируется ингибированием по принципу обратной связи. Кроме того, АТФ является аллостерическим регулятором некоторых ферментов, участвующих в катаболическом расщеплении сахара — процессе, который создает АТФ. Таким образом, когда АТФ в изобилии, клетка может предотвратить производство АТФ. С другой стороны, АДФ служит положительным аллостерическим регулятором (аллостерическим активатором) для некоторых из тех же ферментов, которые ингибируются АТФ. Таким образом, когда относительные уровни АДФ высоки по сравнению с АТФ, клетка начинает производить больше АТФ за счет катаболизма сахара.
Таким образом, когда относительные уровни АДФ высоки по сравнению с АТФ, клетка начинает производить больше АТФ за счет катаболизма сахара.
Клетки выполняют функции жизни посредством различных химических реакций. Метаболизм клетки относится к комбинации химических реакций, происходящих в ней. Катаболические реакции расщепляют сложные химические вещества на более простые и связаны с выделением энергии. Анаболические процессы строят сложные молекулы из более простых и требуют энергии.
При изучении энергии термин «система» относится к материи и окружающей среде, участвующим в передаче энергии. Энтропия есть мера беспорядка системы. Физические законы, описывающие передачу энергии, — это законы термодинамики. Первый закон гласит, что общее количество энергии во Вселенной постоянно. Второй закон термодинамики гласит, что каждая передача энергии связана с некоторой потерей энергии в непригодной для использования форме, такой как тепловая энергия. Энергия бывает разных форм: кинетической, потенциальной и свободной. Изменение свободной энергии реакции может быть отрицательным (высвобождение энергии, экзергоническое) или положительным (потребление энергии, эндергоническое). Для протекания всех реакций требуется первоначальный ввод энергии, называемой энергией активации.
Изменение свободной энергии реакции может быть отрицательным (высвобождение энергии, экзергоническое) или положительным (потребление энергии, эндергоническое). Для протекания всех реакций требуется первоначальный ввод энергии, называемой энергией активации.
Ферменты — это химические катализаторы, ускоряющие химические реакции за счет снижения энергии их активации. Ферменты имеют активный центр с уникальной химической средой, которая подходит для определенных химических реагентов для этого фермента, называемых субстратами. Считается, что ферменты и субстраты связываются в соответствии с моделью индуцированного соответствия. Действие фермента регулируется для сохранения ресурсов и оптимального реагирования на окружающую среду.
Глоссарий
энергия активации: количество начальной энергии, необходимой для протекания реакции
активный центр: специфический участок фермента, где связывается субстрат изменение в активном центре, предотвращающее связывание с субстратом
анаболический: описывает путь, который требует затрат чистой энергии для синтеза сложных молекул из более простых
биоэнергетика: концепция потока энергии через живые системы
катаболический: описывает путь, по которому сложные молекулы расщепляются на более простые с образованием энергии в качестве дополнительного продукта реакции
конкурентное ингибирование: общий механизм регуляции активности фермента, при котором молекула, отличная от субстрата фермента, способна связываться с активным центром и предотвращать связывание самого субстрата, тем самым подавляя общую скорость реакции фермента
эндергонический: описывает химическую реакцию, в результате которой образуются продукты, хранящие больше химической потенциальной энергии, чем реагенты.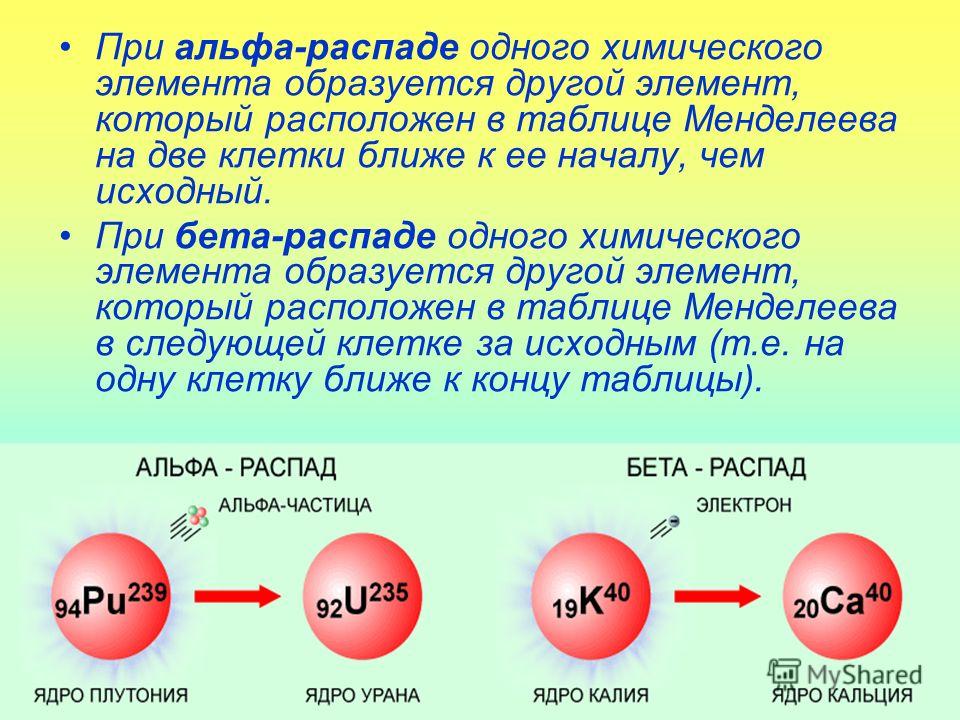
фермент: молекула, катализирующая биохимическую реакцию. с меньшей химической потенциальной энергией, чем у реагентов, плюс высвобождение свободной энергии
ингибирование по принципу обратной связи: механизм регуляции активности фермента, при котором продукт реакции или конечный продукт ряда последовательных реакций ингибирует фермент на некоторое время. более ранний шаг в серии реакций
тепловая энергия: энергия, передаваемая из одной системы в другую, которая не является работой
кинетическая энергия: вид энергии, связанный с движущимися объектами , в том числе использующие энергию и выделяющие энергию
неконкурентное ингибирование: общий механизм регуляции активности ферментов, при котором регуляторная молекула связывается с сайтом, отличным от активного центра, и предотвращает связывание активным центром субстрата; таким образом, молекула ингибитора не конкурирует с субстратом за активный центр; аллостерическое торможение является формой неконкурентного торможения
потенциальная энергия: тип энергии, относящийся к способности выполнять работу
субстрат: молекула, на которую действует фермент
Лицензия
Concepts of Biology — 1st Canadian Edition Чарльза Молнара и Джейн Гейр распространяется под лицензией Creative Commons Attribution 4.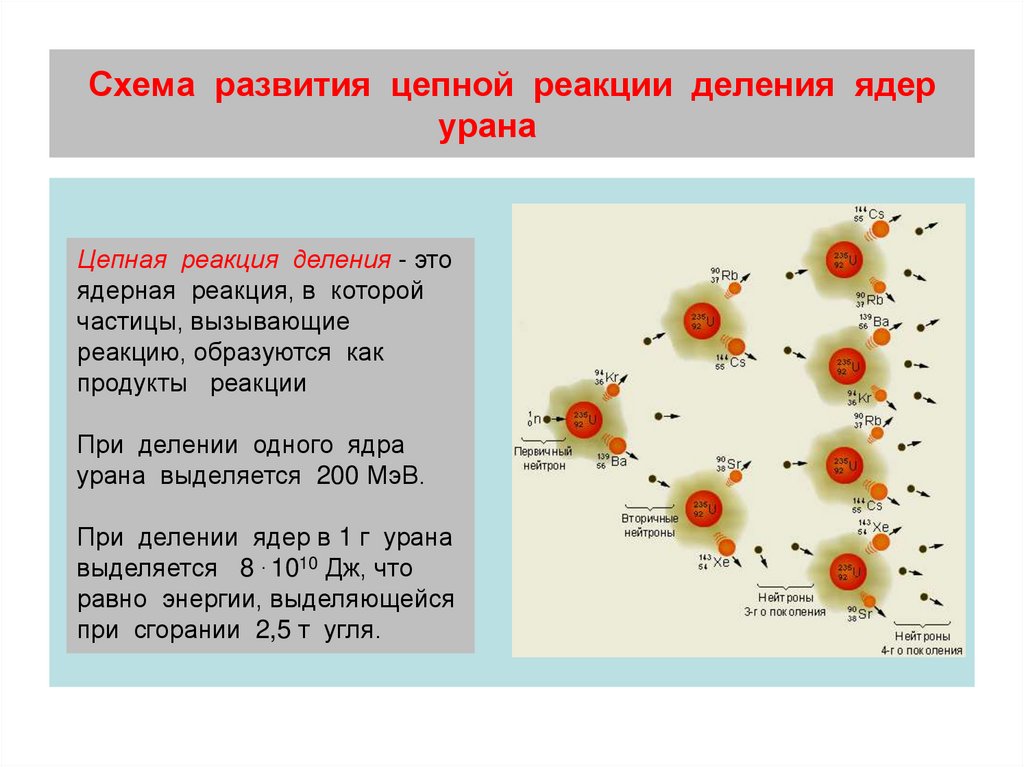 0 International License, если не указано иное.
0 International License, если не указано иное.
Поделиться этой книгой
Поделиться в Твиттере
Понимание химической энергии: полное руководство
Когда вы слышите термин «химическая энергия», вы можете вернуться к уроку химии в старшей школе или даже к уроку начальной школы с экспериментом с вулканом. Но даже если вы давно забыли об этой теме, химическая энергия всегда была с вами. Это энергия, которая лежит в основе большей части нашей повседневной жизни, от еды, которую мы едим, до производства электроэнергии для наших домов и предприятий. Когда вы слышите термин «химическая энергия», вы можете вернуться к школьному уроку химии или даже к начальной школе. класс с экспериментом с вулканом. Но даже если вы давно забыли об этой теме, химическая энергия всегда была с вами. Это энергия, которая лежит в основе большей части нашей повседневной жизни, от еды, которую мы едим, до производства электроэнергии для наших домов и предприятий.
Так что же такое химическая энергия? Мы поможем вам понять и идентифицировать этот жизненно важный источник энергии и изучить некоторые примеры химической энергии в растениях, ископаемом топливе, в нас самих и т.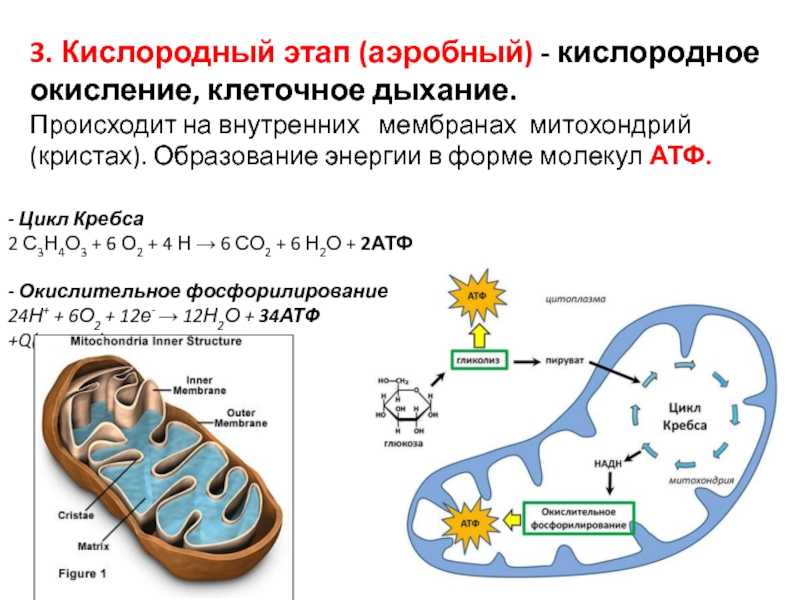 д.
д.
Что такое определение химической энергии?
Химическая энергия представляет собой форму потенциальной энергии или энергии, хранящейся в объекте. Это один из самых важных запасов энергии, которые мы используем.
Химическая энергия – это тип потенциальной энергии, хранящейся в химических связях между атомами и молекулами. Химическая энергия высвобождается или поглощается, когда эти связи разрываются или образуются при воздействии реагентов. Разрыв и образование связи называются химическими реакциями и приводят к созданию нового вещества.
Для разрыва и образования химической связи требуется энергия, чтобы начать преобразование потенциальной энергии в химическую. Мы можем использовать эту химическую потенциальную энергию.
Что такое потенциальная химическая энергия?
Как мы уже видели, потенциальная энергия — это энергия, хранящаяся внутри объекта. Потенциальная химическая энергия — это тот же запас энергии, но это потенциальная энергия химических связей вещества.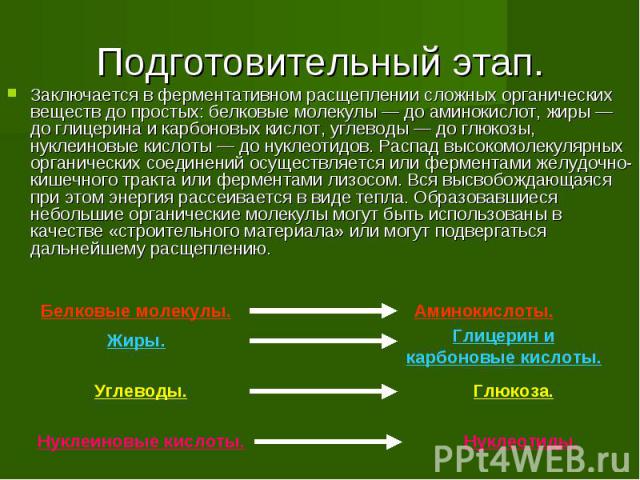
В качестве примера возьмем автомобиль. Теперь наполним его бак бензином, в состав которого входят различные химические соединения, обладающие потенциальной энергией, выделяющейся при сгорании. Двигатель внутреннего сгорания сжигает это топливо, вызывая экзотермическую реакцию. Некоторое количество выделяемой энергии приводит в движение автомобиль, а остальная часть преобразуется в тепло, которое прогревает двигатель.
Другие виды топлива обладают потенциальной химической энергией. Автомобили также движутся благодаря выделяемой химической энергии биотоплива и пропана. Электростанции вырабатывают электричество после высвобождения потенциальной химической энергии угля, природного газа и других ископаемых видов топлива.
Сколько видов энергии существует?
Существует множество различных форм энергии. Ученые исходят из двух основных типов энергии: потенциальной энергии, то есть запасенной энергии, и кинетической энергии, то есть энергии движения.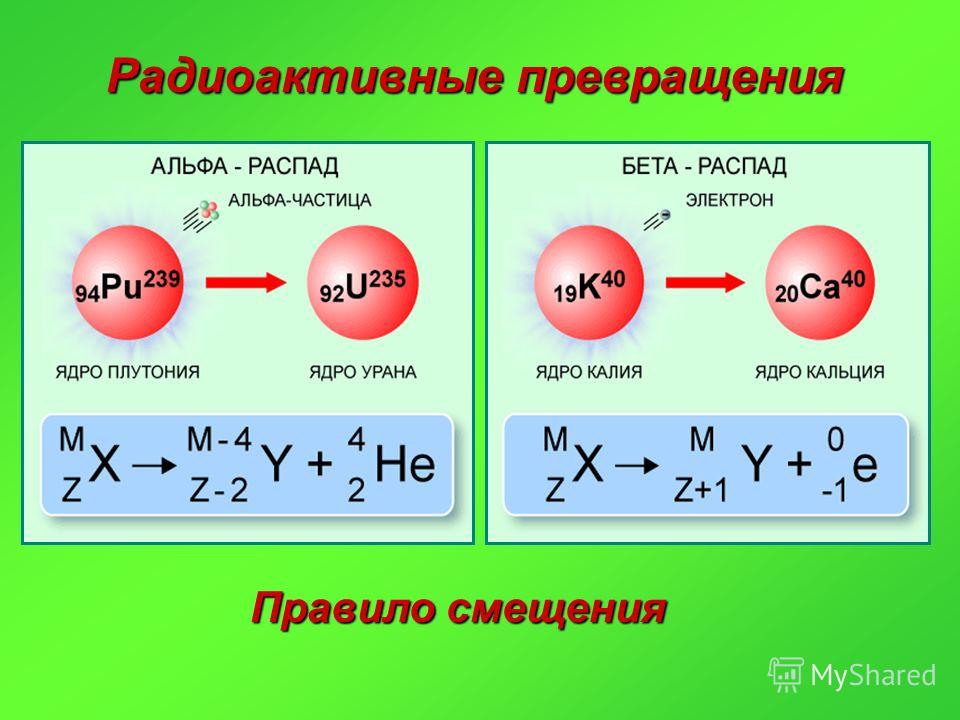
Отсюда несколько энергетических подразделений.
Потенциальная энергия может быть гравитационной потенциальной энергией, энергией положения или упругой потенциальной энергией, когда вы растягиваете или сжимаете что-либо, чтобы увеличить его потенциальную энергию.
Существует больше видов энергии, и химическая энергия является одним из них:
Существует несколько видов энергии:
- Ядерная энергия – это энергия, выделяющаяся в ходе химической реакции ядерного синтеза.
- Механическая энергия — это полная сумма энергии потенциальной и кинетической энергии, как при вращении педалей движущегося велосипеда.
- Химическая энергия — это запасенная энергия в таких веществах, как уголь или пища.
- Электрическая энергия может быть как потенциальной, так и кинетической и возникает в результате потока электрического заряда.
- Энергия излучения, также известная как электромагнитная энергия, исходит от электромагнитных волн, распространяющихся в пространстве.
 Солнце и лампочки излучают электромагнитные волны и, следовательно, лучистую энергию.
Солнце и лампочки излучают электромагнитные волны и, следовательно, лучистую энергию. - Тепловая энергия, также известная как тепло, производится за счет повышения температуры.
Как химическая энергия преобразуется из потенциальной энергии?
источник
Энергия, высвобождаемая в виде химической энергии, подчиняется закону сохранения энергии , , также известному как первый закон термодинамики. Закон гласит, что энергия не может быть уничтожена или создана, а только преобразована из одной формы энергии в другую.
Запасенная или потенциальная энергия вещества преобразуется в форму химической энергии, когда его атомы и молекулы перестраиваются для создания нового вещества.
Еда — отличный способ объяснить химическую энергию. Давайте подумаем о яблоке. Яблоня преобразует солнечную энергию в углеводы, такие как глюкоза, посредством фотосинтеза. Глюкоза является запасом потенциальной энергии.
Мы едим яблоко, и наш организм расщепляет потенциальную энергию глюкозы и других молекул, богатых энергией. Часть потенциальной энергии молекулы претерпевает химические изменения. Он превращается в вещество, называемое аденозинтрифосфатом (АТФ), молекулой, несущей энергию, которая содержится в клетках всех живых существ.
Часть потенциальной энергии молекулы претерпевает химические изменения. Он превращается в вещество, называемое аденозинтрифосфатом (АТФ), молекулой, несущей энергию, которая содержится в клетках всех живых существ.
Химические реакции также приводят к выделению или поглощению тепла. В термодинамике такие реакции называются экзотермическими или эндотермическими.
Что такое экзотермическая реакция?
Широко распространена химическая реакция, в результате которой в качестве побочного продукта выделяется тепло. Называемая экзотермической реакцией, эта химическая реакция высвобождает энергию из своих источников в окружающую среду, заставляя их нагреваться и повышать температуру.
Наиболее распространенными экзотермическими реакциями являются:
- Реакции горения : Горение, также известное как горение, происходит при сгорании топлива.
 Химические реакции выделяют тепло в виде тепловой энергии и световой энергии.
Химические реакции выделяют тепло в виде тепловой энергии и световой энергии. - Реакции окисления: Происходят, когда вещество вступает в реакцию с кислородом, и в результате этой химической реакции образуются оксиды. Во время сгорания топлива, такого как уголь, сжигаемый на электростанциях, объединяют накопленный углерод с кислородом, выделяя углекислый газ. В ходе этого процесса выделяется тепло.
- Реакции нейтрализации: Реакция нейтрализации происходит между кислотами и веществами, называемыми основаниями, которые производят воду и соль. Пчелиный яд кислый, поэтому его можно лечить щелочью, такой как пищевая сода.
Сжигание дров в традиционной кухонной печи представляет собой химическую реакцию, в результате которой потенциальная энергия древесины высвобождается в форме тепла. Эта экзотермическая реакция нагревает печь и кухню.
Эта экзотермическая реакция нагревает печь и кухню.
Что такое эндотермическая реакция?
Проще говоря, эндотермическая реакция противоположна экзотермической реакции. Это поглощает энергию из окружающей среды, заставляя их остывать.
Примером эндотермической реакции является фотосинтез. Растения поглощают солнечную тепловую энергию и превращают ее в глюкозу и другие вещества. Другим примером является тепловая энергия, поглощаемая сковородой для приготовления колбасы.
Что происходит с энергией при разрыве химических связей?
Разорванные связи химических соединений высвобождают энергию, поскольку они образуют новые химические связи. Часть этой энергии высвобождается в виде тепла при образовании нового вещества.
Некоторые реакции создают больше энергии для создания новых связей, чем для разрыва старых. Если мы сжигаем метан на электростанции, он вступает в реакцию с кислородом и производит углекислый газ и воду. Сжигание метана — это сжигание углеводорода, поэтому его атомы водорода соединяются с кислородом, образуя молекулы воды, а атомы углерода метана соединяются с кислородом, превращаясь в молекулы углекислого газа.
Сжигание метана — это сжигание углеводорода, поэтому его атомы водорода соединяются с кислородом, образуя молекулы воды, а атомы углерода метана соединяются с кислородом, превращаясь в молекулы углекислого газа.
Водородно-углеродные связи метана разрываются во время горения, а связи воды и углекислого газа образуются благодаря присутствию кислорода. После всех этих реакций высвобождается больше энергии, образуя новые связи после разрыва первоначальных связей метана.
Результатом является экзотермическая реакция, которая производит тепло и высвобождает больше энергии, чем было в начале. С химической точки зрения сжигание метана является отличным способом обогрева зданий.
Как мы используем химическую энергию для получения энергии?
источник
Мы используем химическую энергию для производства тепла и электричества по всему миру.
Мы сжигаем ископаемое топливо, такое как метан, природный газ, нефть и нефть, для производства пара, который вращает турбины, производящие электричество. Люди также сжигают это топливо в более мелких масштабах, чтобы производить тепло для обогрева зданий.
Люди также сжигают это топливо в более мелких масштабах, чтобы производить тепло для обогрева зданий.
Для получения тепла или электричества сжигание биомассы, биотоплива, биодизеля и других продуктов осуществляется по тому же принципу. Многие виды топлива также питают наши автомобили, самолеты, газонокосилки и многое другое. Мы также можем хранить химическую энергию в батареях.
Солнечные панели преобразуют солнечные лучи в химическую энергию для выработки электричества. Электричество может освещать, обогревать, охлаждать и питать наши здания.
Каковы 5 примеров химической энергии?
Есть много примеров химической энергии в нашей повседневной жизни. Вот пять примеров, которые, вероятно, будут вам хорошо знакомы:
- Еда: Наш организм расщепляет химические соединения для высвобождения энергии.
- Пропан: Мы сжигаем пропан для производства тепла и света.

- Автомобильные аккумуляторы: Аккумулируют химическую энергию и выделяют электрическую энергию.
- Взрывчатые вещества: Нестабильные соединения легко и быстро перестраиваются с образованием света и тепла в газообразных формах, вызывая взрывы.
- Нефть: Двигатели внутреннего сгорания реструктурируют атомы и молекулы для выделения тепла и энергии.
Использует ли телефон химическую энергию?
Да, мобильный телефон использует химическую энергию. В каждом сотовом телефоне есть аккумулятор, который мы заряжаем электричеством. Электричество вызывает химическую реакцию внутри батареи. Электроны переходят от отрицательного конца батареи к ее положительному концу, что позволяет ей снова пропускать электричество по своим цепям благодаря этим переданным электронам.
Электроны переходят от отрицательного конца батареи к ее положительному концу, что позволяет ей снова пропускать электричество по своим цепям благодаря этим переданным электронам.
Батарея снова разрядится, как только все электроны перейдут к отрицательному концу батареи. Мы исправляем это, заряжая аккумулятор еще раз и запуская ту же химическую реакцию.
Обладает ли древесина химической энергией?
Древесина является топливом из биомассы, что означает, что энергия поступает от живых растений и животных. Некоторые считают древесину устойчивым или возобновляемым источником энергии, потому что мы можем вырастить ее заново в течение нашей жизни.
У бревна есть химическая энергия. У него есть потенциальная химическая энергия, пока он сидит в дровяном сарае. Подожгите дрова, и вы высвободите эту потенциальную энергию в виде тепла.
Где хранится химическая энергия в растениях?
Мы знаем, что фотосинтез — это то, как растения преобразуют световую энергию солнца в химическую энергию.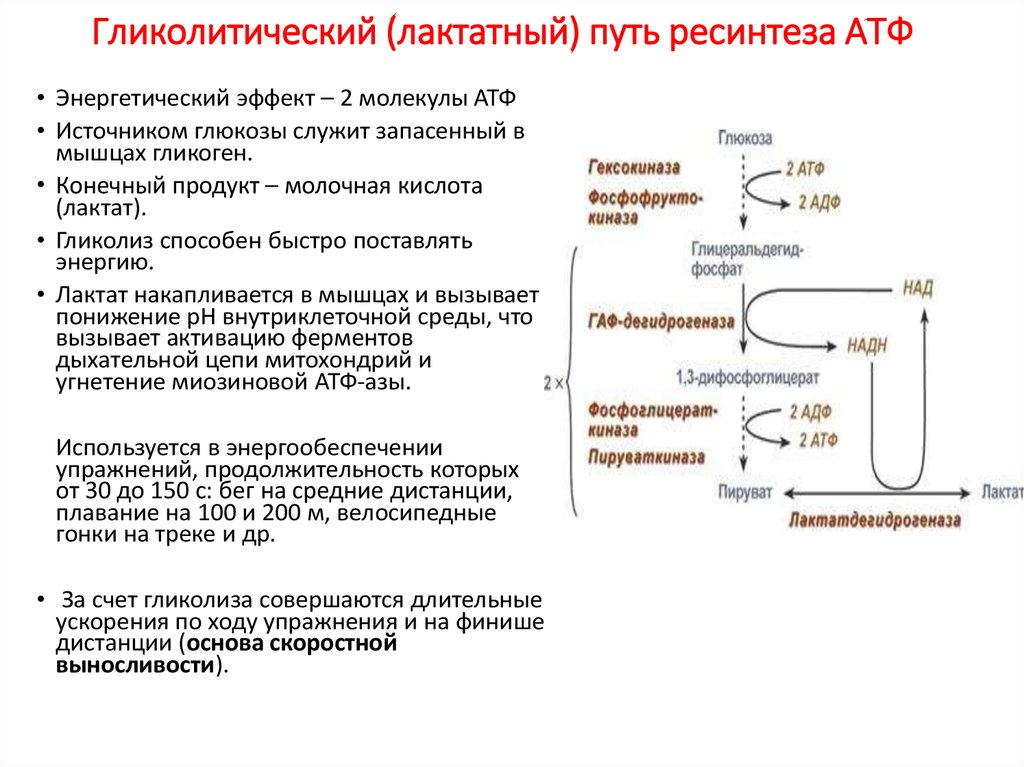
Растения хранят эту солнечную энергию в виде химической энергии в виде сахара (глюкозы) в клетках листьев, называемых хлоропластами. Эти клетки полны хлорофилла, который помогает поглощать свет. Как только происходит фотосинтез, растения производят сахар и кислород.
Где содержится химическая энергия в соединении?
Соединения содержат химическую энергию в связях, связывающих атомы вместе. Чтобы разорвать эти связи, мы говорим об энтальпии связи соединения или энергии связи, ранее известной как прочность связи.
Энтальпия связи — это количество энергии, необходимое для разрыва этой связи, когда она находится в газообразном состоянии. Это также известно как теплосодержание системы.
Каковы недостатки химической энергии?
Большинство химических преобразований энергии связано с ископаемым топливом, которое загрязняет планету и может быть дорогостоящим для добычи.
В 2020 году в Соединенных Штатах около 79% производства энергии в стране приходилось на ископаемое топливо, уголь, нефть и природный газ.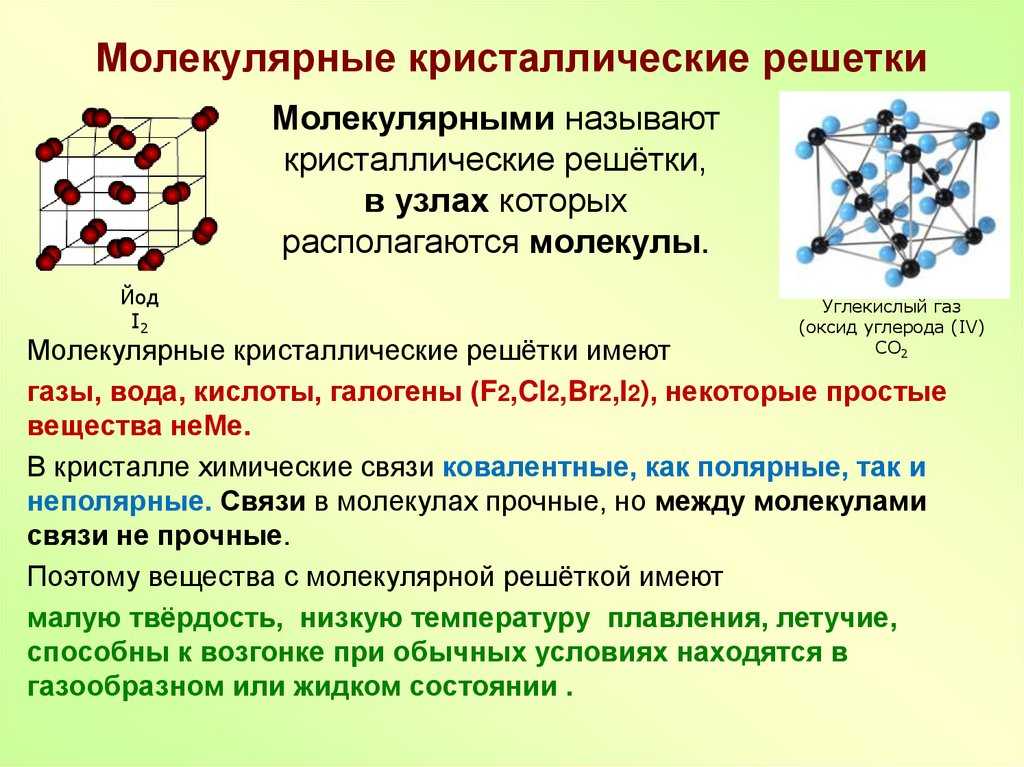 При сжигании этих материалов выделяется углекислый газ и другие парниковые газы, вызывающие глобальное потепление. В конечном счете, ископаемое топливо не является устойчивым, поэтому нам придется искать альтернативные источники энергии.
При сжигании этих материалов выделяется углекислый газ и другие парниковые газы, вызывающие глобальное потепление. В конечном счете, ископаемое топливо не является устойчивым, поэтому нам придется искать альтернативные источники энергии.
«Более экологичные» альтернативные источники энергии, такие как солнечные батареи, требуют материалов, добытых с помощью загрязняющих окружающую среду методов добычи, а также транспортировки. Другие источники, такие как древесина, означают вырубку лесов, транспортировку выбросов и выброс углекислого газа в атмосферу.
Химическая энергия, выделяемая ядерными бомбами, привела к разрушительным последствиям. Десятки тысяч человек погибли, когда Соединенные Штаты сбросили атомную бомбу на Хиросиму в Японии 6 августа 1945 года и Нагасаки тремя днями позже.
Аварии на атомных электростанциях загрязнили окружающую среду в печально известных местах, таких как Чернобыль в тогдашнем Советском Союзе, Фукусима-дайити в Японии и Три-Майл-Айленд в Соединенных Штатах.
Человеческое стремление к определенным продуктам изменяет экосистемы, начиная с интенсивных методов ведения сельского хозяйства, обеспечивающих более высокие урожаи, и заканчивая расчисткой лесов для выпаса скота. Водоснабжение, качество почвы и биоразнообразие могут пострадать из-за выращивания одной культуры.
Наша тяга и потребность в энергоемких продуктах, которые мы едим и превращаем в химическую энергию, может принести больше долгосрочных неудобств, чем краткосрочное удовлетворение от наслаждения нашей любимой едой.
Понимание химической энергии поможет вам ценить повседневные вещи
В нашей повседневной жизни есть много примеров химической энергии. Каждый раз, когда мы включаем свет, едем или идем куда-то или едим пищу, мы используем химическую энергию.
Химическая энергия легко хранится и может транспортироваться для удовлетворения наших потребностей. Солнечные панели помогают нам преобразовывать свободную энергию солнца в полезную химическую энергию для питания наших домов.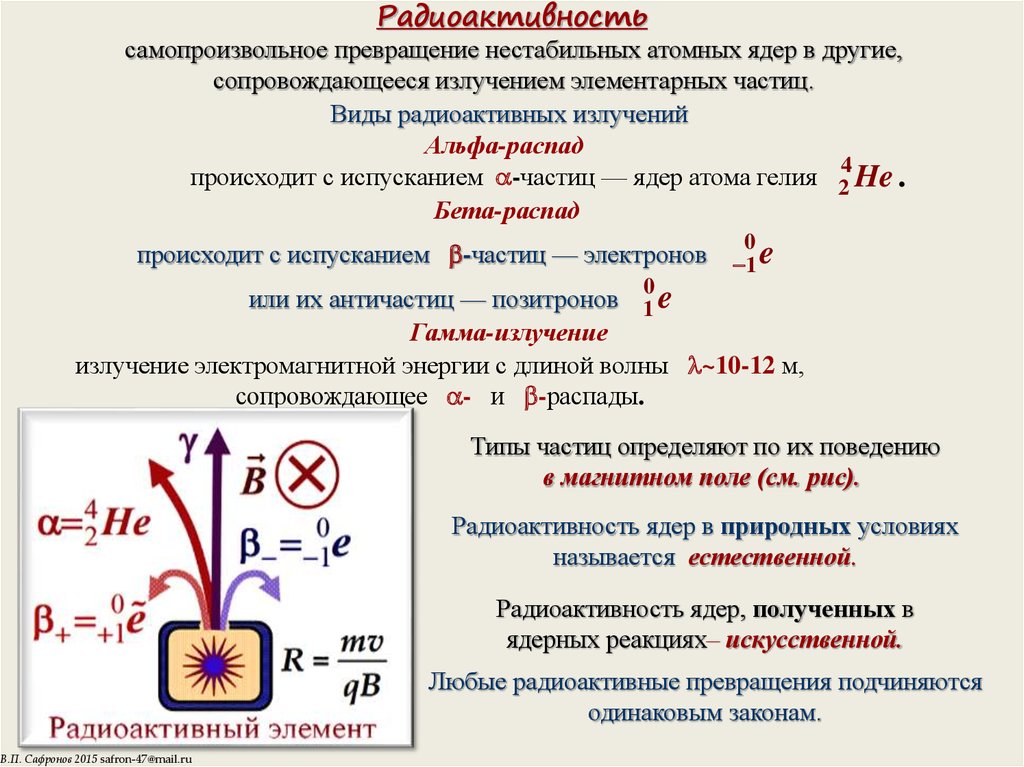 Вы можете использовать солнечную энергию с помощью планов зеленой энергии или употребления в пищу растений или животных.
Вы можете использовать солнечную энергию с помощью планов зеленой энергии или употребления в пищу растений или животных.
Некоторая химическая энергия вредна и загрязняет планету, например, сжигание угля или природного газа. Тем не менее, эти ископаемые виды топлива являются отличным примером того, как химическая энергия может храниться в течение миллионов лет, но все же высвобождать энергию при правильных условиях.
У использования химической энергии есть свои недостатки, создающие затруднения, на которые нам еще предстоит ответить. Однако сам процесс помог изменить жизнь, какой мы ее знаем.
Предоставлено вам taranergy.com
Все изображения предоставлены по лицензии Adobe Stock.
Избранное изображение
Как клетки получают энергию из пищи. Молекулярная биология клетки
Как мы только что видели, клеткам требуется постоянный приток энергии для создания и поддержания биологического порядка, поддерживающего их жизнь. Эта энергия получается из энергии химической связи в пищевых молекулах, которые, таким образом, служат топливом для клеток.
Эта энергия получается из энергии химической связи в пищевых молекулах, которые, таким образом, служат топливом для клеток.
Сахара являются особенно важными топливными молекулами, и они окисляются небольшими ступенями до двуокиси углерода (CO 2 ) и вода (). В этом разделе мы проследим основные этапы расщепления или катаболизма сахаров и покажем, как они производят АТФ, НАДН и другие активированные молекулы-носители в клетках животных. Мы концентрируемся на расщеплении глюкозы, так как она доминирует в производстве энергии в большинстве животных клеток. Очень похожий путь также действует в растениях, грибах и многих бактериях. Другие молекулы, такие как жирные кислоты и белки, также могут служить источниками энергии, если они проходят через соответствующие ферментативные пути.
Рисунок 2-69
Схематическое изображение контролируемого ступенчатого окисления сахара в клетке по сравнению с обычным сжиганием. (A) В клетке ферменты катализируют окисление посредством ряда небольших стадий, в ходе которых свободная энергия переносится в пакетах удобного размера (подробнее.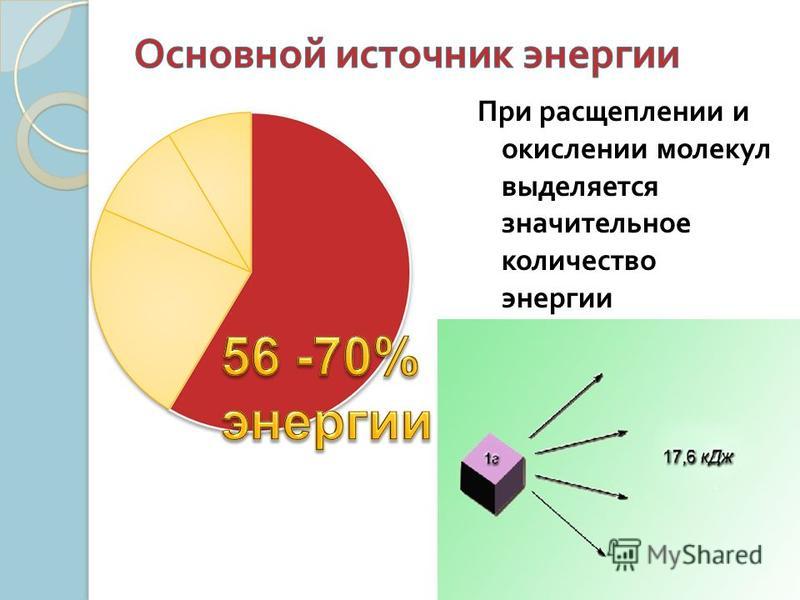 ..)
..)
Молекулы пищи расщепляются в три этапа с образованием АТФ
Белки, липиды и полисахариды, составляющие большую часть пищи, которую мы едим, должны быть расщеплены на более мелкие молекулы, прежде чем наши клетки смогут их использовать — либо в качестве источника энергии, либо в качестве строительных блоков для других молекул. Процессы распада должны воздействовать на поступающую извне пищу, а не на макромолекулы внутри наших собственных клеток. Таким образом, стадия 1 ферментативного расщепления пищевых молекул составляет пищеварение , которое происходит либо в нашем кишечнике вне клеток, либо в специализированной органелле внутри клеток — лизосоме. (Мембрана, окружающая лизосому, отделяет ее пищеварительные ферменты от цитозоля, как описано в главе 13.) В любом случае большие полимерные молекулы в пище расщепляются во время пищеварения на мономерные субъединицы — белки на аминокислоты, полисахариды на сахара, а жиры в жирные кислоты и глицерин — под действием ферментов. После переваривания небольшие органические молекулы, полученные из пищи, попадают в цитозоль клетки, где начинается их постепенное окисление. Как показано на рисунке, окисление происходит на двух следующих стадиях клеточного катаболизма: стадия 2 начинается в цитозоле и заканчивается в основной органелле, преобразующей энергию, — митохондрии; стадия 3 полностью ограничена митохондриями.
После переваривания небольшие органические молекулы, полученные из пищи, попадают в цитозоль клетки, где начинается их постепенное окисление. Как показано на рисунке, окисление происходит на двух следующих стадиях клеточного катаболизма: стадия 2 начинается в цитозоле и заканчивается в основной органелле, преобразующей энергию, — митохондрии; стадия 3 полностью ограничена митохондриями.
Рисунок 2-70
Упрощенная диаграмма трех стадий клеточного метаболизма, которые ведут от пищи к отходам в клетках животных. Эта серия реакций производит АТФ, который затем используется для управления биосинтетическими реакциями и другими энергозатратными процессами в (далее…)
На стадии 2 цепочка реакций, называемая гликолизом , превращает каждую молекулу глюкозы в две более мелкие молекулы пирувата. Сахара, отличные от глюкозы, аналогичным образом превращаются в пируват после их превращения в один из промежуточных сахаров в этом гликолитическом пути. При образовании пирувата образуются два типа активированных молекул-носителей — АТФ и НАДН. Затем пируват переходит из цитозоля в митохондрии. Там каждая молекула пирувата превращается в CO 2 плюс двухуглеродная ацетильная группа, которая присоединяется к коферменту А (КоА), образуя ацетил-КоА, другую молекулу активированного носителя (см. ). Большое количество ацетил-КоА также образуется в результате поэтапного распада и окисления жирных кислот, полученных из жиров, которые переносятся кровотоком, импортируются в клетки в виде жирных кислот, а затем перемещаются в митохондрии для производства ацетил-КоА.
Затем пируват переходит из цитозоля в митохондрии. Там каждая молекула пирувата превращается в CO 2 плюс двухуглеродная ацетильная группа, которая присоединяется к коферменту А (КоА), образуя ацетил-КоА, другую молекулу активированного носителя (см. ). Большое количество ацетил-КоА также образуется в результате поэтапного распада и окисления жирных кислот, полученных из жиров, которые переносятся кровотоком, импортируются в клетки в виде жирных кислот, а затем перемещаются в митохондрии для производства ацетил-КоА.
Стадия 3 окислительного распада пищевых молекул полностью происходит в митохондриях. Ацетильная группа в ацетил-КоА связана с коферментом А высокоэнергетической связью и поэтому легко переносится на другие молекулы. После переноса на четырехуглеродную молекулу оксалоацетата ацетильная группа вступает в серию реакций, называемых 9-й.1276 цикл лимонной кислоты . Как мы кратко обсудим, в этих реакциях ацетильная группа окисляется до CO 2 , и образуются большие количества переносчика электронов NADH.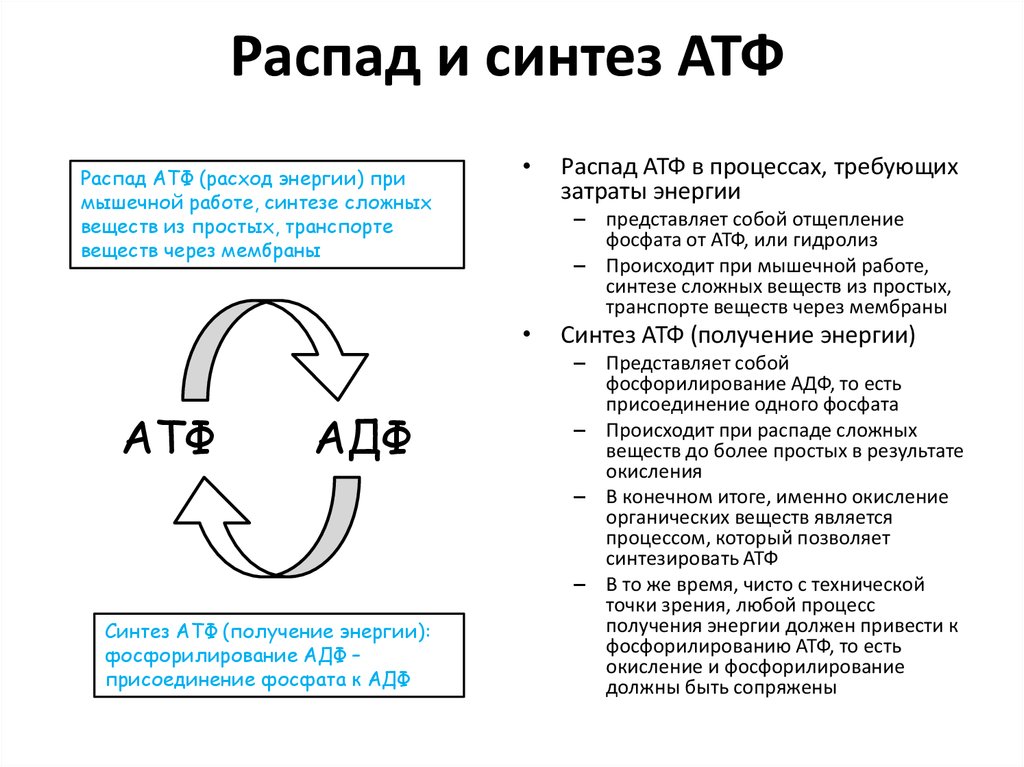 Наконец, высокоэнергетические электроны от NADH передаются по цепи переноса электронов внутри митохондриальной внутренней мембраны, где энергия, высвобождаемая при их переносе, используется для запуска процесса, который производит АТФ и потребляет молекулярный кислород (O 2 ). Именно на этих последних этапах большая часть энергии, высвобождаемой при окислении, используется для производства большей части клеточного АТФ.
Наконец, высокоэнергетические электроны от NADH передаются по цепи переноса электронов внутри митохондриальной внутренней мембраны, где энергия, высвобождаемая при их переносе, используется для запуска процесса, который производит АТФ и потребляет молекулярный кислород (O 2 ). Именно на этих последних этапах большая часть энергии, высвобождаемой при окислении, используется для производства большей части клеточного АТФ.
Поскольку энергия, необходимая для синтеза АТФ в митохондриях, в конечном итоге поступает от окислительного распада молекул пищи, фосфорилирование АДФ с образованием АТФ, которое управляется транспортом электронов в митохондриях, известно как окислительное фосфорилирование . Удивительные события, происходящие во внутренней митохондриальной мембране во время окислительного фосфорилирования, находятся в центре внимания главы 14.
Благодаря производству АТФ энергия, получаемая при расщеплении сахаров и жиров, перераспределяется в виде пакетов химической энергии в удобной форме.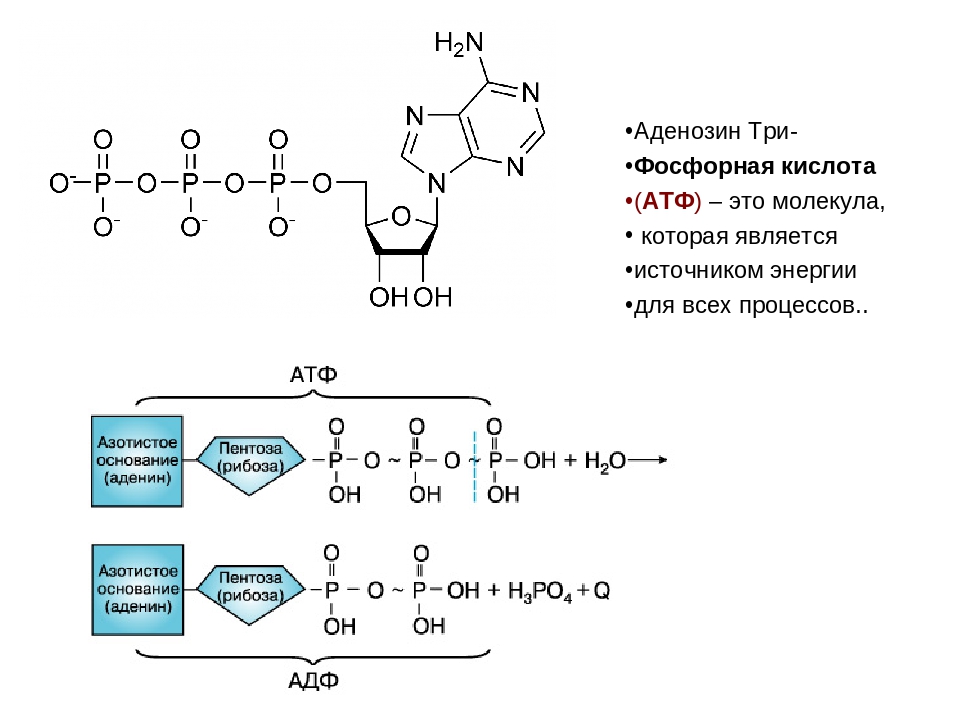 для использования в другом месте клетки. Примерно 10 9В типичной клетке в любой момент времени в растворе находится 1458 9 молекул АТФ, а во многих клетках вся эта АТФ переворачивается (т. е. расходуется и замещается) каждые 1–2 минуты.
для использования в другом месте клетки. Примерно 10 9В типичной клетке в любой момент времени в растворе находится 1458 9 молекул АТФ, а во многих клетках вся эта АТФ переворачивается (т. е. расходуется и замещается) каждые 1–2 минуты.
В целом почти половина энергии, которая теоретически может быть получена при окислении глюкозы или жирных кислот до H 2 O и CO 2 , улавливается и используется для запуска энергетически невыгодной реакции P i + АДФ → АТФ. (Напротив, типичный двигатель внутреннего сгорания, такой как автомобильный двигатель, может преобразовать в полезную работу не более 20 % имеющейся в его топливе энергии.) Остальная часть энергии высвобождается клеткой в виде тепла, заставляя наши тела тепло.
Гликолиз — центральный путь производства АТФ
Наиболее важным процессом на стадии 2 распада пищевых молекул является расщепление глюкозы в последовательности реакций, известных как гликолиз — от греческого glukus «сладкий».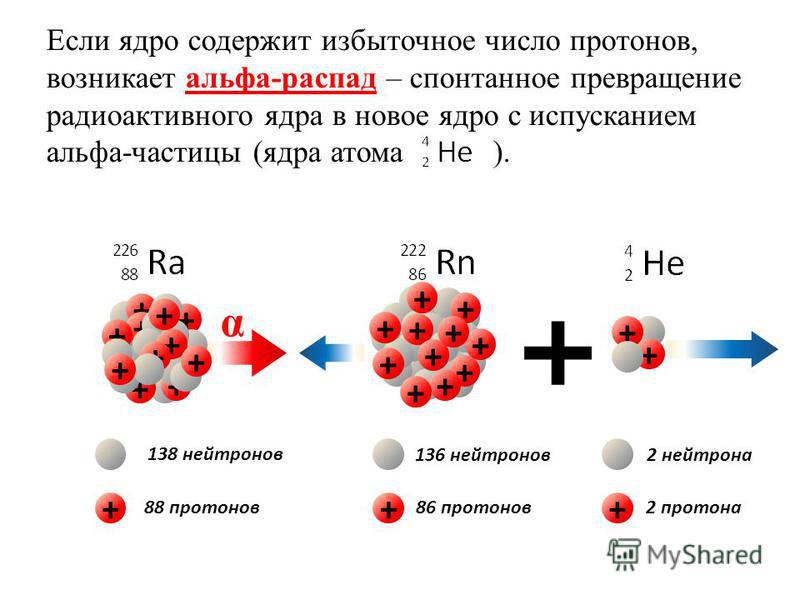 и lusis, «разрыв». Гликолиз производит АТФ без участия молекулярного кислорода (газ O 2 ). Он встречается в цитозоле большинства клеток, включая многие анаэробные микроорганизмы (те, которые могут жить без использования молекулярного кислорода). Гликолиз, вероятно, развился в начале истории жизни, до того, как деятельность фотосинтезирующих организмов привела к поступлению кислорода в атмосферу. В ходе гликолиза молекула глюкозы с шестью атомами углерода превращается в две молекулы по пируватов, каждый из которых содержит по три атома углерода. На каждую молекулу глюкозы гидролизуются две молекулы АТФ, чтобы обеспечить энергию для запуска первых стадий, но четыре молекулы АТФ образуются на более поздних стадиях. Следовательно, в конце гликолиза на каждую расщепленную молекулу глюкозы приходится две молекулы АТФ.
и lusis, «разрыв». Гликолиз производит АТФ без участия молекулярного кислорода (газ O 2 ). Он встречается в цитозоле большинства клеток, включая многие анаэробные микроорганизмы (те, которые могут жить без использования молекулярного кислорода). Гликолиз, вероятно, развился в начале истории жизни, до того, как деятельность фотосинтезирующих организмов привела к поступлению кислорода в атмосферу. В ходе гликолиза молекула глюкозы с шестью атомами углерода превращается в две молекулы по пируватов, каждый из которых содержит по три атома углерода. На каждую молекулу глюкозы гидролизуются две молекулы АТФ, чтобы обеспечить энергию для запуска первых стадий, но четыре молекулы АТФ образуются на более поздних стадиях. Следовательно, в конце гликолиза на каждую расщепленную молекулу глюкозы приходится две молекулы АТФ.
Путь гликолиза представлен в общих чертах на и более подробно на панели 2-8 (стр. 124-125). Гликолиз включает в себя последовательность из 10 отдельных реакций, каждая из которых производит разные промежуточные сахара и каждая катализируется другим ферментом. Как и большинство ферментов, все эти ферменты имеют названия, оканчивающиеся на 9.1276 аза — подобный изомеру аза и дегидроген аза — которые указывают тип реакции, которую они катализируют.
Как и большинство ферментов, все эти ферменты имеют названия, оканчивающиеся на 9.1276 аза — подобный изомеру аза и дегидроген аза — которые указывают тип реакции, которую они катализируют.
Рисунок 2-71
Схема гликолиза. Каждая из 10 показанных стадий катализируется другим ферментом. Обратите внимание, что на шаге 4 шестиуглеродный сахар расщепляется на два трехуглеродных сахара, так что количество молекул на каждом последующем этапе удваивается. Как указано, этап 6 (подробнее…)
Панель 2-8
Подробная информация о 10 этапах гликолиза.
Хотя молекулярный кислород не участвует в гликолизе, происходит окисление, при котором электроны удаляются NAD + (с образованием NADH) от некоторых атомов углерода, полученных из молекулы глюкозы. Ступенчатый характер процесса позволяет высвобождать энергию окисления небольшими порциями, так что большая ее часть может храниться в активированных молекулах-носителях, а не выделяться в виде тепла (см. Ресурсы). Таким образом, часть энергии, высвобождаемой при окислении, приводит к прямому синтезу молекул АТФ из АДФ и Р9.0009 i , а часть остается с электронами в высокоэнергетическом переносчике электронов НАДН.
Ресурсы). Таким образом, часть энергии, высвобождаемой при окислении, приводит к прямому синтезу молекул АТФ из АДФ и Р9.0009 i , а часть остается с электронами в высокоэнергетическом переносчике электронов НАДН.
Две молекулы НАДН образуются на одну молекулу глюкозы в процессе гликолиза. В аэробных организмах (тех, которым для жизни необходим молекулярный кислород) эти молекулы НАДН отдают свои электроны цепи переноса электронов, описанной в главе 14, а НАД + , образованный из НАДН, снова используется для гликолиза (см. шаг 6 в Панель 2–8, стр. 124–125).
Ферментации позволяют производить АТФ в отсутствие кислорода
Для большинства животных и растительных клеток гликолиз является лишь прелюдией к третьему и последнему этапу распада пищевых молекул. В этих клетках пируват, образующийся на последнем этапе стадии 2, быстро транспортируется в митохондрии, где превращается в СО 2 плюс ацетил-КоА, который затем полностью окисляется до СО 2 и Н 2 O
Напротив, для многих анаэробных организмов, которые не используют молекулярный кислород и могут расти и делиться без него, гликолиз является основным источником клеточного АТФ.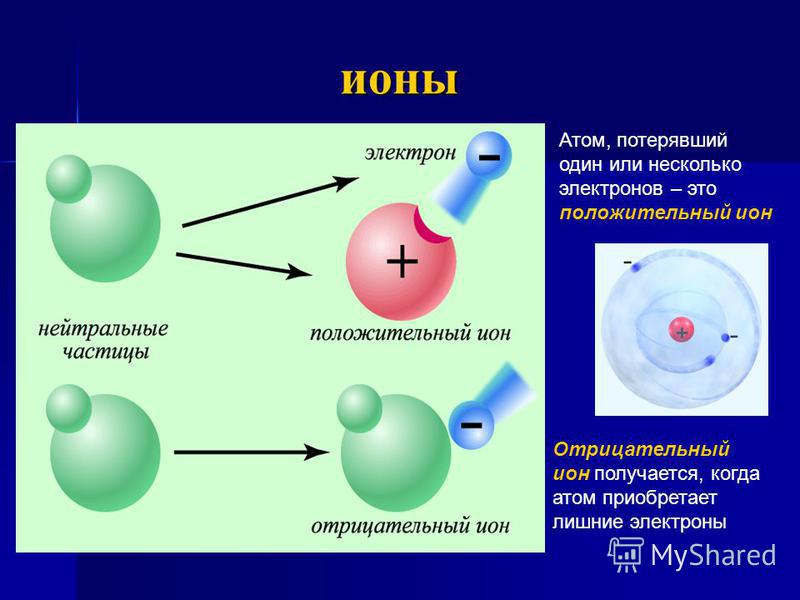 Это также верно для некоторых тканей животных, таких как скелетные мышцы, которые могут продолжать функционировать при ограничении молекулярного кислорода. В этих анаэробных условиях электроны пирувата и НАДН остаются в цитозоле. Пируват превращается в продукты, выделяемые клеткой, например, в этанол и СО 2 в дрожжах, используемых в пивоварении и выпечке хлеба, или в лактате в мышцах. В этом процессе НАДН отдает свои электроны и снова превращается в НАД + . Эта регенерация NAD + необходима для поддержания реакций гликолиза ().
Это также верно для некоторых тканей животных, таких как скелетные мышцы, которые могут продолжать функционировать при ограничении молекулярного кислорода. В этих анаэробных условиях электроны пирувата и НАДН остаются в цитозоле. Пируват превращается в продукты, выделяемые клеткой, например, в этанол и СО 2 в дрожжах, используемых в пивоварении и выпечке хлеба, или в лактате в мышцах. В этом процессе НАДН отдает свои электроны и снова превращается в НАД + . Эта регенерация NAD + необходима для поддержания реакций гликолиза ().
Рисунок 2-72
Два пути анаэробного распада пирувата. (A) При недостатке кислорода, например, в мышечной клетке, подвергающейся энергичному сокращению, пируват, образующийся в результате гликолиза, превращается в лактат, как показано. Эта реакция регенерирует (далее…)
Подобные анаэробные пути выработки энергии называются ферментациями. Исследования коммерчески важных ферментаций, осуществляемых дрожжами, во многом вдохновили раннюю биохимию. Работа в девятнадцатом веке привела в 1896 году к поразительному тогда открытию, что эти процессы можно изучать вне живых организмов, в клеточных экстрактах. Это революционное открытие в конечном итоге позволило проанализировать и изучить каждую из отдельных реакций в процессе ферментации. Сбор воедино полного гликолитического пути в 1930-е годы стали крупным триумфом биохимии, за которым вскоре последовало признание центральной роли АТФ в клеточных процессах. Таким образом, большинство фундаментальных концепций, обсуждаемых в этой главе, известны уже более 50 лет.
Работа в девятнадцатом веке привела в 1896 году к поразительному тогда открытию, что эти процессы можно изучать вне живых организмов, в клеточных экстрактах. Это революционное открытие в конечном итоге позволило проанализировать и изучить каждую из отдельных реакций в процессе ферментации. Сбор воедино полного гликолитического пути в 1930-е годы стали крупным триумфом биохимии, за которым вскоре последовало признание центральной роли АТФ в клеточных процессах. Таким образом, большинство фундаментальных концепций, обсуждаемых в этой главе, известны уже более 50 лет.
Гликолиз показывает, как ферменты связывают окисление с накоплением энергии (видеть ). Ферменты играют роль гребного колеса в нашей аналогии, и теперь мы вернемся к этапу гликолиза, который мы обсуждали ранее, чтобы проиллюстрировать, как именно происходят сопряженные реакции.
Две центральные реакции гликолиза (стадии 6 и 7) превращают трехуглеродный промежуточный сахар глицеральдегид-3-фосфат (альдегид) в 3-фосфоглицерат (карбоновую кислоту).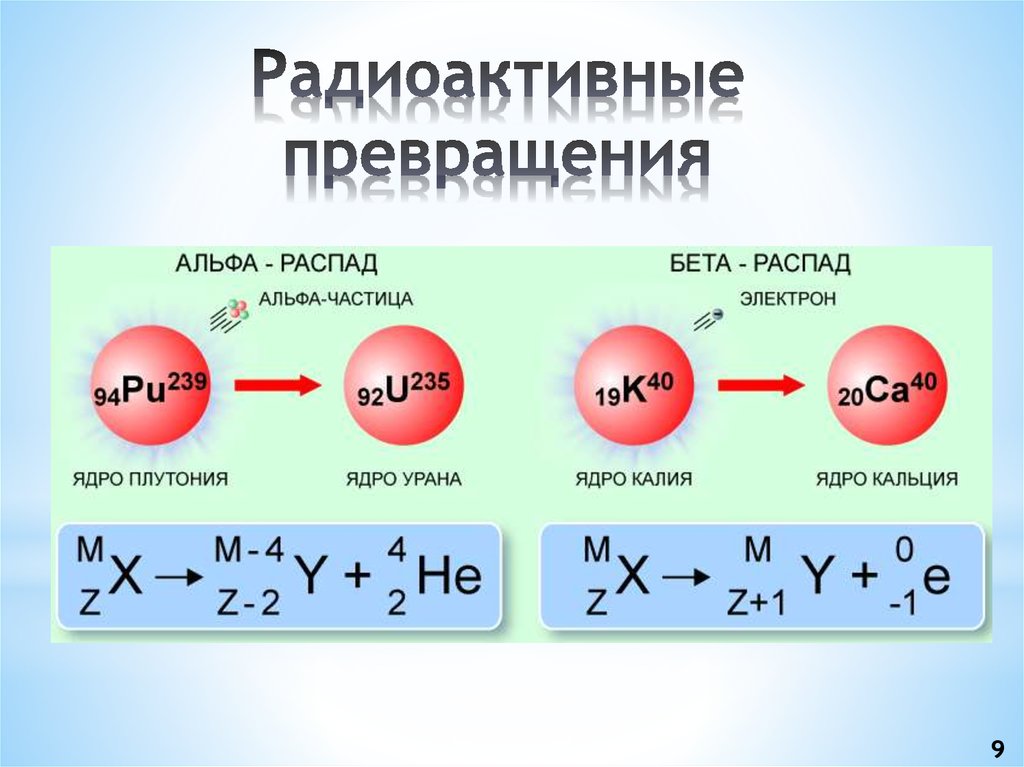 Это влечет за собой окисление альдегидной группы до группы карбоновой кислоты, которое происходит в две стадии. Общая реакция высвобождает достаточно свободной энергии для превращения молекулы АДФ в АТФ и для переноса двух электронов от альдегида к НАД + с образованием НАДН, при этом выделяется достаточно тепла в окружающую среду, чтобы сделать общую реакцию энергетически выгодной (Δ G ° для суммарной реакции -3,0 ккал/моль).
Это влечет за собой окисление альдегидной группы до группы карбоновой кислоты, которое происходит в две стадии. Общая реакция высвобождает достаточно свободной энергии для превращения молекулы АДФ в АТФ и для переноса двух электронов от альдегида к НАД + с образованием НАДН, при этом выделяется достаточно тепла в окружающую среду, чтобы сделать общую реакцию энергетически выгодной (Δ G ° для суммарной реакции -3,0 ккал/моль).
Путь, по которому совершается этот выдающийся подвиг, описан в . Химические реакции управляются двумя ферментами, с которыми прочно связаны промежуточные соединения сахаров. Первый фермент ( глицеральдегид-3-фосфатдегидрогеназа ) образует короткоживущую ковалентную связь с альдегидом через реакционноспособную -SH-группу фермента и катализирует окисление этого альдегида, пока еще находится в присоединенном состоянии. Высокоэнергетическая связь фермент-субстрат, созданная в результате окисления, затем замещается неорганическим ионом фосфата с образованием высокоэнергетического промежуточного продукта сахар-фосфат, который тем самым высвобождается из фермента. Это промежуточное соединение затем связывается со вторым ферментом ( фосфоглицераткиназа ). Этот фермент катализирует энергетически выгодный перенос только что созданного высокоэнергетического фосфата на АДФ, образуя АТФ и завершая процесс окисления альдегида в карбоновую кислоту (см. ).
Это промежуточное соединение затем связывается со вторым ферментом ( фосфоглицераткиназа ). Этот фермент катализирует энергетически выгодный перенос только что созданного высокоэнергетического фосфата на АДФ, образуя АТФ и завершая процесс окисления альдегида в карбоновую кислоту (см. ).
Рисунок 2-73
Накопление энергии на этапах 6 и 7 гликолиза. На этих стадиях окисление альдегида до карбоновой кислоты сопряжено с образованием АТФ и НАДН. (A) Стадия 6 начинается с образования ковалентной связи между субстратом (глицеральдегидом (подробнее…)
Мы показали этот конкретный процесс окисления довольно подробно, потому что он представляет собой наглядный пример опосредованного ферментами накопления энергии посредством связанных реакций (). Эти реакции (этапы 6 и 7) являются единственными в гликолизе, которые создают высокоэнергетическую фосфатную связь непосредственно из неорганического фосфата. Как таковые, они объясняют чистый выход двух молекул АТФ и двух молекул НАДН на молекулу глюкозы (см. панель 2–8, стр. 124–125).
панель 2–8, стр. 124–125).
Рисунок 2-74
Схематическое изображение сопряженных реакций образования НАДН и АТФ на стадиях 6 и 7 гликолиза. Энергия окисления связи C-H приводит к образованию как НАДН, так и высокоэнергетической фосфатной связи. Затем разрыв высокоэнергетической связи приводит к образованию АТФ. (подробнее…)
Как мы только что видели, АТФ может легко образовываться из АДФ, когда образуются промежуточные продукты реакции с более энергичными фосфатными связями, чем в АТФ. Фосфатные связи можно упорядочить по энергии, сравнив стандартное изменение свободной энергии ( Δ G° ) для разрыва каждой связи гидролизом. сравнивает высокоэнергетические фосфоангидридные связи в АТФ с другими фосфатными связями, некоторые из которых образуются во время гликолиза.
Рисунок 2-75
Некоторые энергии фосфатных связей. Перенос фосфатной группы с любой молекулы 1 на любую молекулу 2 энергетически выгоден, если стандартное изменение свободной энергии (Δ G °) для гидролиза фосфатной связи в молекуле 1 более отрицательно (подробнее.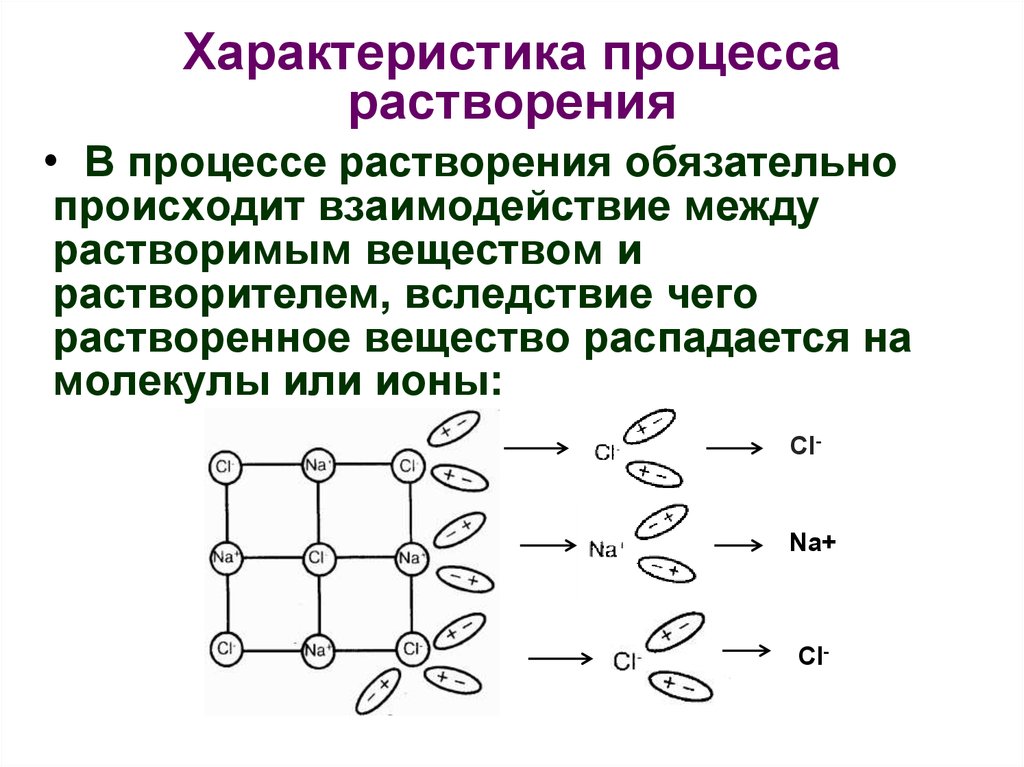 ..)
..)
Сахара и жиры расщепляются до ацетил-КоА в митохондриях
Теперь мы переходим к рассмотрению стадии 3 катаболизма, процесс, который требует большого количества молекулярного кислорода (газ O 2 ). Поскольку считается, что Земля создала атмосферу, содержащую газ O 2 , между одним и двумя миллиардами лет назад, в то время как многочисленные формы жизни, как известно, существовали на Земле в течение 3,5 миллиардов лет, использование O 2 в реакциях, которые мы обсуждаем далее, считается относительно недавним происхождением. Напротив, механизм, используемый для производства АТФ, не требует кислорода, и родственники этой изящной пары связанных реакций могли возникнуть очень рано в истории жизни на Земле.
В аэробном метаболизме пируват, образующийся в результате гликолиза, быстро декарбоксилируется гигантским комплексом из трех ферментов, называемым пируватдегидрогеназным комплексом . Продуктами декарбоксилирования пирувата являются молекулы СО 2 (отходы), молекула НАДН и ацетил-КоА. Трехферментный комплекс находится в митохондриях эукариотических клеток; его структура и способ действия описаны в .
Трехферментный комплекс находится в митохондриях эукариотических клеток; его структура и способ действия описаны в .
Рисунок 2-76
Окисление пирувата до ацетил-КоА и СО 2 . (А) Структура комплекса пируватдегидрогеназы, который содержит 60 полипептидных цепей. Это пример большого мультиферментного комплекса, в котором промежуточные продукты реакции передаются непосредственно из (далее…)
Ферменты, расщепляющие жирные кислоты, полученные из жиров, также производят ацетил-КоА в митохондриях. Каждая молекула жирной кислоты (как активированная молекула жирного ацил-КоА ) полностью расщепляется циклом реакций, в ходе которого от карбоксильного конца отщепляется по два атома углерода за раз, образуя одну молекулу ацетил-КоА на каждый оборот цикла. В этом процессе также образуются молекула НАДН и молекула ФАДН 2 ().
Рисунок 2-77
Окисление жирных кислот до ацетил-КоА. (А) Электронная микрофотография липидной капли в цитоплазме (вверху), и в структуре жиров (внизу). Жиры представляют собой триацилглицеролы. Часть глицерина, с которой три жирные кислоты связаны сложноэфирными связями, (подробнее…)
Жиры представляют собой триацилглицеролы. Часть глицерина, с которой три жирные кислоты связаны сложноэфирными связями, (подробнее…)
Сахара и жиры являются основными источниками энергии для большинства нефотосинтезирующих организмов, включая человека. Однако большая часть полезной энергии, которая может быть извлечена при окислении обоих типов пищевых продуктов, остается запасенной в молекулах ацетил-КоА, образующихся в результате только что описанных двух типов реакций. Лимоннокислотный цикл реакций, в которых ацетильная группа в ацетил-КоА окисляется до СО 2 и H 2 O, поэтому играет центральную роль в энергетическом метаболизме аэробных организмов. У эукариот все эти реакции протекают в митохондриях, органеллах, в которые направляются пируват и жирные кислоты для производства ацетил-КоА. Поэтому не следует удивляться, обнаружив, что митохондрия — это место, где в клетках животных вырабатывается большая часть АТФ. Напротив, аэробные бактерии осуществляют все свои реакции в одном компартменте, цитозоле, и именно здесь в этих клетках происходит цикл лимонной кислоты.
Рисунок 2-78
Пути производства ацетил-КоА из сахаров и жиров. Митохондрия в эукариотических клетках — это место, где ацетил-КоА вырабатывается из обоих типов основных пищевых молекул. Поэтому именно здесь протекает большинство клеточных реакций окисления (подробнее…)
В цикле лимонной кислоты образуется НАДН путем окисления ацетильных групп до СО
2 В девятнадцатом веке биологи заметили, что в отсутствие воздуха (анаэробные условия) клетки вырабатывают молочную кислоту (например, в мышцах) или этанол (например, в дрожжах), а в его присутствии (аэробные условия) потребляют О 2 и производить CO 2 и H 2 O. Интенсивные усилия по определению путей аэробного метаболизма в конечном итоге сосредоточились на окислении пирувата и привели в 1937 году к открытию цикла лимонной кислоты, также известного как . цикл трикарбоновой кислоты или цикл Кребса . На цикл лимонной кислоты приходится около двух третей всего окисления соединений углерода в большинстве клеток, и его основными конечными продуктами являются CO 2 и высокоэнергетические электроны в форме NADH. СО 2 высвобождается как побочный продукт, в то время как высокоэнергетические электроны от NADH передаются в связанную с мембраной цепь переноса электронов, в конечном итоге объединяясь с O 2 с образованием H 2 O. Хотя цикл лимонной кислоты сам по себе не использует O 2 , ему требуется O 2 , чтобы продолжить, потому что у NADH нет другого эффективного способа избавиться от своих электронов и, таким образом, регенерировать NAD + , который необходим для поддержания цикла. собирается.
СО 2 высвобождается как побочный продукт, в то время как высокоэнергетические электроны от NADH передаются в связанную с мембраной цепь переноса электронов, в конечном итоге объединяясь с O 2 с образованием H 2 O. Хотя цикл лимонной кислоты сам по себе не использует O 2 , ему требуется O 2 , чтобы продолжить, потому что у NADH нет другого эффективного способа избавиться от своих электронов и, таким образом, регенерировать NAD + , который необходим для поддержания цикла. собирается.
Цикл лимонной кислоты, происходящий внутри митохондрий эукариотических клеток, приводит к полному окислению атомов углерода ацетильных групп в ацетил-КоА, превращая их в CO 2 . Но ацетильная группа не окисляется напрямую. Вместо этого эта группа переносится от ацетил-КоА к более крупной четырехуглеродной молекуле, оксалоацетату, , с образованием шестиуглеродной трикарбоновой кислоты, лимонной кислоты, , в честь которой назван последующий цикл реакций. Затем молекула лимонной кислоты постепенно окисляется, позволяя использовать энергию этого окисления для производства богатых энергией активированных молекул-носителей. Цепь из восьми реакций образует цикл, потому что в конце оксалоацетат регенерируется и вступает в новый виток цикла, как показано в схеме на рис.
Затем молекула лимонной кислоты постепенно окисляется, позволяя использовать энергию этого окисления для производства богатых энергией активированных молекул-носителей. Цепь из восьми реакций образует цикл, потому что в конце оксалоацетат регенерируется и вступает в новый виток цикла, как показано в схеме на рис.
Рисунок 2-79
Простой обзор цикла лимонной кислоты. Реакция ацетил-КоА с оксалоацетатом запускает цикл с образованием цитрата (лимонной кислоты). В каждом обороте цикла в качестве отходов образуется две молекулы CO 2 плюс три молекулы NADH, одна (подробнее…)
До сих пор мы обсуждали только один из трех типов активированных молекул-носителей. продуцируемые циклом лимонной кислоты, пара НАД + -НАДН (см. ). В дополнение к трем молекулам NADH каждый оборот цикла также производит одну молекулу ФАДХ 2 (восстановленный флавинадениндинуклеотид) из FAD и одна молекула рибонуклеотида GTP (гуанозинтрифосфат) из GDP. Структуры этих двух активированных молекул-носителей показаны на рис. ГТФ является близким родственником АТФ, и перенос его концевой фосфатной группы на АДФ приводит к образованию одной молекулы АТФ в каждом цикле. Как и НАДН, ФАДН 2 является переносчиком высокоэнергетических электронов и водорода. Как мы кратко обсудим, энергия, запасенная в легко переносимых высокоэнергетических электронах НАДН и ФАДН 2 впоследствии будет использоваться для производства АТФ посредством процесса окислительного фосфорилирования, единственного этапа окислительного катаболизма пищевых продуктов, который напрямую требует газообразного кислорода (O 2 ) из атмосферы.
Структуры этих двух активированных молекул-носителей показаны на рис. ГТФ является близким родственником АТФ, и перенос его концевой фосфатной группы на АДФ приводит к образованию одной молекулы АТФ в каждом цикле. Как и НАДН, ФАДН 2 является переносчиком высокоэнергетических электронов и водорода. Как мы кратко обсудим, энергия, запасенная в легко переносимых высокоэнергетических электронах НАДН и ФАДН 2 впоследствии будет использоваться для производства АТФ посредством процесса окислительного фосфорилирования, единственного этапа окислительного катаболизма пищевых продуктов, который напрямую требует газообразного кислорода (O 2 ) из атмосферы.
Рисунок 2-80
Структуры GTP и FADH 2 . (A) GTP и GDP являются близкими родственниками АТФ и АДФ соответственно. (B) FADH 2 является переносчиком атомов водорода и высокоэнергетических электронов, таких как NADH и NADPH. Он показан здесь в окисленной форме (FAD) с водородсодержащим (далее. ..)
..)
Полный цикл лимонной кислоты представлен на панели 2-9 (стр. 126-127). Дополнительные атомы кислорода, необходимые для образования CO 2 из ацетильных групп, входящих в цикл лимонной кислоты, поставляются не молекулярным кислородом, а водой. Как показано на рисунке, в каждом цикле расщепляются три молекулы воды, и атомы кислорода некоторых из них в конечном итоге используются для образования CO 2 .
Панель 2-9
Полный цикл лимонной кислоты.
Помимо пирувата и жирных кислот некоторые аминокислоты переходят из цитозоля в митохондрии, где они также превращаются в ацетил-КоА или один из других промежуточных продуктов цикла лимонной кислоты. Таким образом, в эукариотической клетке митохондрия является центром, к которому ведут все энергетические процессы, начинаются ли они с сахаров, жиров или белков.
Цикл лимонной кислоты также служит отправной точкой для важных биосинтетических реакций, производя жизненно важные углеродсодержащие промежуточные продукты, такие как оксалоацетат и α-кетоглутарат. Некоторые из этих веществ, образующихся в результате катаболизма, переносятся обратно из митохондрий в цитозоль, где они служат в анаболических реакциях предшественниками для синтеза многих незаменимых молекул, таких как аминокислоты.
Некоторые из этих веществ, образующихся в результате катаболизма, переносятся обратно из митохондрий в цитозоль, где они служат в анаболических реакциях предшественниками для синтеза многих незаменимых молекул, таких как аминокислоты.
Электронный транспорт управляет синтезом большей части АТФ в большинстве клеток
Именно на последнем этапе деградации молекулы пищи высвобождается основная часть ее химической энергии. В этом заключительном процессе переносчики электронов НАДН и ФАДН 2 передают электроны, полученные ими при окислении других молекул, на электрон-транспортную цепь, встроенную во внутреннюю мембрану митохондрии. Когда электроны проходят по этой длинной цепи специализированных молекул-акцепторов и доноров электронов, они последовательно переходят в более низкие энергетические состояния. Энергия, выделяемая электронами в этом процессе, используется для накачки H + ионов (протонов) через мембрану — из внутреннего митохондриального компартмента наружу (). Таким образом создается градиент ионов H + . Этот градиент служит источником энергии, используемой как батарея для управления различными реакциями, требующими энергии. Наиболее известной из этих реакций является образование АТФ путем фосфорилирования АДФ.
Таким образом создается градиент ионов H + . Этот градиент служит источником энергии, используемой как батарея для управления различными реакциями, требующими энергии. Наиболее известной из этих реакций является образование АТФ путем фосфорилирования АДФ.
Рисунок 2-81
Генерация градиента H + через мембрану в результате реакций переноса электронов. Высокоэнергетический электрон (полученный, например, в результате окисления метаболита) последовательно передается переносчиками А, В и С в более низкое энергетическое состояние. На этой диаграмме (далее…)
В конце этой серии переносов электроны передаются молекулам газообразного кислорода (O 2 ), диффундировавшим в митохондрию, которые одновременно соединяются с протонами (H + ) из окружающего раствора в производят молекулы воды. Электроны теперь достигли своего самого низкого энергетического уровня, и поэтому вся доступная энергия была извлечена из окисляемой пищевой молекулы. Этот процесс, называемый окислительным фосфорилированием, также происходит в плазматической мембране бактерий. Как одно из самых замечательных достижений клеточной эволюции, оно станет центральной темой главы 14.
Этот процесс, называемый окислительным фосфорилированием, также происходит в плазматической мембране бактерий. Как одно из самых замечательных достижений клеточной эволюции, оно станет центральной темой главы 14.
Рисунок 2-82
Заключительные стадии окисления пищевых молекул. Молекулы НАДН и ФАДН 2 (ФАДН 2 не показаны) образуются в цикле лимонной кислоты. Эти активированные носители отдают высокоэнергетические электроны, которые в конечном итоге используются для восстановления газообразного кислорода до воды. A Major (подробнее…)
В общей сложности полное окисление молекулы глюкозы до H 2 O и CO 2 используется клеткой для производства около 30 молекул АТФ. Напротив, только 2 молекулы АТФ образуются на молекулу глюкозы только за счет гликолиза.
Организмы хранят молекулы пищи в специальных резервуарах
Всем организмам необходимо поддерживать высокое соотношение АТФ/АДФ, если необходимо поддерживать биологический порядок в их клетках. Тем не менее животные имеют лишь периодический доступ к пище, а растениям необходимо выживать в течение ночи без солнечного света, без возможности производства сахара в результате фотосинтеза. По этой причине и растения, и животные превращают сахара и жиры в специальные формы для хранения ().
Тем не менее животные имеют лишь периодический доступ к пище, а растениям необходимо выживать в течение ночи без солнечного света, без возможности производства сахара в результате фотосинтеза. По этой причине и растения, и животные превращают сахара и жиры в специальные формы для хранения ().
Рисунок 2-83
Хранение сахаров и жиров в животных и растительных клетках. (A) Структуры крахмала и гликогена, формы хранения сахаров у растений и животных соответственно. Оба являются запасными полимерами сахарной глюкозы и отличаются только частотой разветвления (подробнее…)
Чтобы компенсировать длительные периоды голодания, животные запасают жирные кислоты в виде капелек жира, состоящих из нерастворимых в воде триацилглицеролов, в основном в специализированных жировых клетках. А для более краткосрочного хранения сахар запасается в виде субъединиц глюкозы в большом разветвленном полисахариде гликогене, который присутствует в виде мелких гранул в цитоплазме многих клеток, включая печень и мышцы. Синтез и расщепление гликогена быстро регулируются в зависимости от потребности. Когда требуется больше АТФ, чем может быть произведено из молекул пищи, поступающих из кровотока, клетки расщепляют гликоген в результате реакции, в результате которой образуется глюкозо-1-фосфат, который вступает в гликолиз.
Синтез и расщепление гликогена быстро регулируются в зависимости от потребности. Когда требуется больше АТФ, чем может быть произведено из молекул пищи, поступающих из кровотока, клетки расщепляют гликоген в результате реакции, в результате которой образуется глюкозо-1-фосфат, который вступает в гликолиз.
В количественном отношении жир является гораздо более важной формой запасания, чем гликоген, отчасти потому, что при окислении грамма жира высвобождается примерно в два раза больше энергии, чем при окислении грамма гликогена. Кроме того, гликоген отличается от жира тем, что связывает большое количество воды, что приводит к шестикратной разнице в фактической массе гликогена, необходимой для хранения того же количества энергии, что и жир. Средний взрослый человек хранит достаточно гликогена только для одного дня нормальной деятельности, но достаточно жира, чтобы его хватило почти на месяц. Если бы наш основной топливный резервуар должен был быть гликогеном, а не жиром, вес тела должен был бы увеличиться в среднем примерно на 60 фунтов.
Большая часть нашего жира хранится в жировой ткани, из которой он высвобождается в кровоток для использования другими клетками по мере необходимости. Потребность возникает после периода воздержания от еды; даже обычное ночное голодание приводит к мобилизации жира, так что утром большая часть ацетил-КоА, поступающего в цикл лимонной кислоты, образуется из жирных кислот, а не из глюкозы. Однако после еды большая часть ацетил-КоА, поступающего в цикл лимонной кислоты, поступает из глюкозы, получаемой из пищи, и любой избыток глюкозы используется для пополнения истощенных запасов гликогена или для синтеза жиров. (Хотя клетки животных легко превращают сахара в жиры, они не могут превращать жирные кислоты в сахара.)
Хотя растения производят НАДФН и АТФ путем фотосинтеза, этот важный процесс происходит в специализированной органелле, называемой хлоропластом, который изолирован от остальной части растительной клетки мембраной, непроницаемой для обоих типов активированных молекул-носителей. Кроме того, в растении есть много других клеток, например, в корнях, в которых отсутствуют хлоропласты, и поэтому они не могут производить собственные сахара или АТФ. Следовательно, для производства большей части АТФ растение использует экспорт сахаров из своих хлоропластов в митохондрии, расположенные во всех клетках растения. Большая часть АТФ, необходимой растению, синтезируется в этих митохондриях и экспортируется из них в остальную часть растительной клетки, используя точно такие же пути окислительного расщепления сахаров, которые используются нефотосинтезирующими организмами.
Кроме того, в растении есть много других клеток, например, в корнях, в которых отсутствуют хлоропласты, и поэтому они не могут производить собственные сахара или АТФ. Следовательно, для производства большей части АТФ растение использует экспорт сахаров из своих хлоропластов в митохондрии, расположенные во всех клетках растения. Большая часть АТФ, необходимой растению, синтезируется в этих митохондриях и экспортируется из них в остальную часть растительной клетки, используя точно такие же пути окислительного расщепления сахаров, которые используются нефотосинтезирующими организмами.
Рисунок 2-84
Как производится АТФ, необходимый для метаболизма большинства растительных клеток. У растений хлоропласты и митохондрии совместно снабжают клетки метаболитами и АТФ.
В периоды избыточной фотосинтетической способности в течение дня хлоропласты превращают часть производимых ими сахаров в жиры и в крахмал, полимер глюкозы, аналогичный гликогену животных. Жиры в растениях представляют собой триацилглицеролы, как и жиры в животных, и различаются только типами преобладающих жирных кислот. Жир и крахмал хранятся в хлоропластах в качестве резервуаров для мобилизации в качестве источника энергии в периоды темноты (см. ).
Жир и крахмал хранятся в хлоропластах в качестве резервуаров для мобилизации в качестве источника энергии в периоды темноты (см. ).
Зародыши внутри семян растений должны жить за счет накопленных источников энергии в течение длительного периода, пока они не прорастут и не произведут листья, которые смогут собирать энергию солнечного света. По этой причине семена растений часто содержат особенно большое количество жиров и крахмала, что делает их основным источником пищи для животных, в том числе и для нас самих.
Рисунок 2-85
Семена некоторых растений, которые являются важной пищей для человека. Кукуруза, орехи и горох содержат богатые запасы крахмала и жира, которые обеспечивают зародыш молодого растения в семени энергией и строительными блоками для биосинтеза. (Предоставлено Фондом Джона Иннеса.) (подробнее…)
Аминокислоты и нуклеотиды являются частью азотного цикла
До сих пор в нашем обсуждении мы концентрировались в основном на углеводном обмене. Мы еще не рассматривали метаболизм азота или серы. Эти два элемента входят в состав белков и нуклеиновых кислот, которые являются двумя наиболее важными классами макромолекул в клетке и составляют примерно две трети ее сухого веса. Атомы азота и серы переходят от соединения к соединению и между организмами и окружающей их средой в серии обратимых циклов.
Мы еще не рассматривали метаболизм азота или серы. Эти два элемента входят в состав белков и нуклеиновых кислот, которые являются двумя наиболее важными классами макромолекул в клетке и составляют примерно две трети ее сухого веса. Атомы азота и серы переходят от соединения к соединению и между организмами и окружающей их средой в серии обратимых циклов.
Хотя молекулярный азот в изобилии содержится в атмосфере Земли, азот химически неактивен в виде газа. Лишь немногие живые виды способны включать его в органические молекулы, этот процесс называется фиксацией азота. Фиксация азота происходит у некоторых микроорганизмов и при некоторых геофизических процессах, например при разряде молнии. Он необходим для биосферы в целом, ибо без него не было бы жизни на этой планете. Однако лишь небольшая часть азотистых соединений в современных организмах обусловлена свежими продуктами фиксации азота из атмосферы. Большая часть органического азота уже некоторое время находится в обращении, переходя от одного живого организма к другому. Таким образом, можно сказать, что современные азотфиксирующие реакции выполняют функцию «пополнения» общего запаса азота.
Таким образом, можно сказать, что современные азотфиксирующие реакции выполняют функцию «пополнения» общего запаса азота.
Позвоночные животные получают практически весь свой азот с пищей, состоящей из белков и нуклеиновых кислот. В организме эти макромолекулы расщепляются на аминокислоты и компоненты нуклеотидов, а содержащийся в них азот используется для производства новых белков и нуклеиновых кислот или используется для создания других молекул. Около половины из 20 аминокислот, содержащихся в белках, являются незаменимыми аминокислотами для позвоночных (), что означает, что они не могут быть синтезированы из других ингредиентов рациона. Другие могут быть синтезированы таким образом с использованием различных исходных материалов, включая промежуточные продукты цикла лимонной кислоты, как описано ниже. Незаменимые аминокислоты производятся беспозвоночными организмами, как правило, длительными и энергетически затратными путями, утраченными в ходе эволюции позвоночных.
Рисунок 2-86
Девять незаменимых аминокислот. Они не могут быть синтезированы клетками человека и поэтому должны поступать с пищей.
Они не могут быть синтезированы клетками человека и поэтому должны поступать с пищей.
Нуклеотиды, необходимые для производства РНК и ДНК, могут быть синтезированы с использованием специализированных путей биосинтеза: не существует «необходимых нуклеотидов», которые должны поступать с пищей. Все атомы азота в пуриновых и пиримидиновых основаниях (а также некоторые атомы углерода) получены из многочисленных аминокислот глутамина, аспарагиновой кислоты и глицина, тогда как сахара рибозы и дезоксирибозы получены из глюкозы.
Аминокислоты, которые не используются в биосинтезе, могут окисляться для получения метаболической энергии. Большинство их атомов углерода и водорода в конечном итоге образуют CO 2 или H 2 O, тогда как их атомы азота проходят через различные формы и в конечном итоге появляются в виде мочевины, которая выводится из организма. Каждая аминокислота обрабатывается по-своему, и для их катаболизма существует целая совокупность ферментативных реакций.
Многие пути биосинтеза начинаются с гликолиза или цикла лимонной кислоты
Катаболизм производит как энергию для клетки, так и строительные блоки, из которых состоят многие другие молекулы клетки (см. ). До сих пор в наших дискуссиях о гликолизе и цикле лимонной кислоты основное внимание уделялось производству энергии, а не предоставлению исходных материалов для биосинтеза. Но многие из промежуточных продуктов, образующихся в этих путях реакции, также перекачиваются другими ферментами, которые используют их для производства аминокислот, нуклеотидов, липидов и других небольших органических молекул, в которых нуждается клетка. Некоторое представление о сложности этого процесса можно получить из рисунка, который иллюстрирует некоторые ответвления от центральных катаболических реакций, ведущих к биосинтезу.
Рисунок 2-87
Гликолиз и цикл лимонной кислоты дают предшественники, необходимые для синтеза многих важных биологических молекул. Аминокислоты, нуклеотиды, липиды, сахара и другие молекулы, представленные здесь как продукты, в свою очередь служат предшественниками (подробнее. ..)
..)
Существование стольких ветвящихся путей в клетке требует, чтобы выбор в каждой ветви быть тщательно отрегулированы, как мы обсудим далее.
Метаболизм организован и регулируется
О сложности клетки как химической машины можно судить по взаимосвязи гликолиза и цикла лимонной кислоты с другими метаболическими путями, описанными в . Этот тип диаграммы, который использовался ранее в этой главе для введения метаболизма, представляет только некоторые из ферментативных путей в клетке. Очевидно, что наше обсуждение клеточного метаболизма касается лишь небольшой части клеточной химии.
Рисунок 2-88
Гликолиз и цикл лимонной кислоты находятся в центре метаболизма. Около 500 метаболических реакций типичной клетки схематично показаны реакциями гликолиза и цикла лимонной кислоты красным цветом . Другие реакции ведут к этим двум (подробнее…)
Все эти реакции происходят в клетке диаметром менее 0,1 мм, и для каждой требуется свой фермент.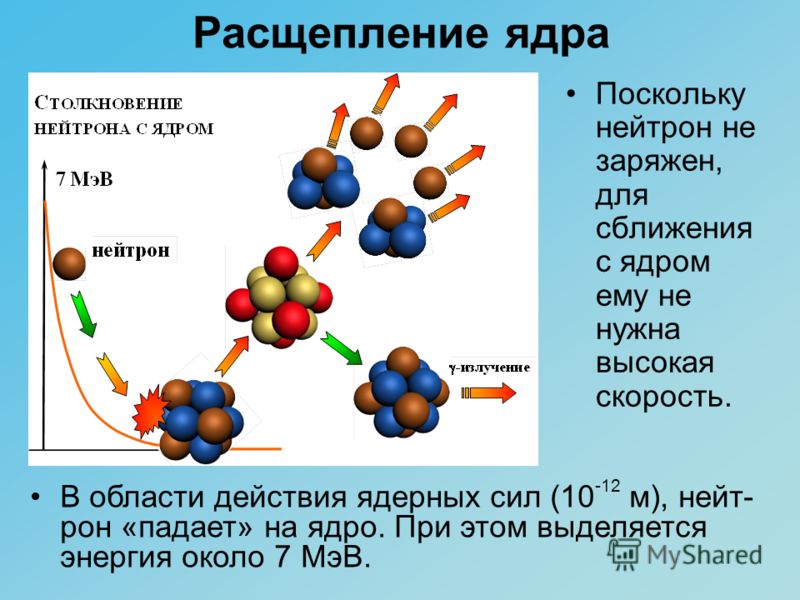 Как видно из , одна и та же молекула часто может быть частью многих различных путей. Пируват, например, является субстратом для полудюжины или более различных ферментов, каждый из которых химически модифицирует его по-своему. Один фермент превращает пируват в ацетил-КоА, другой — в оксалоацетат; третий фермент превращает пируват в аминокислоту аланин, четвертый — в лактат и так далее. Все эти разные пути конкурируют за одну и ту же молекулу пирувата, и одновременно происходят аналогичные соревнования за тысячи других малых молекул. Возможно, лучше понять эту сложность можно с помощью трехмерной метаболической карты, которая позволяет установить более прямые связи между путями (4).
Как видно из , одна и та же молекула часто может быть частью многих различных путей. Пируват, например, является субстратом для полудюжины или более различных ферментов, каждый из которых химически модифицирует его по-своему. Один фермент превращает пируват в ацетил-КоА, другой — в оксалоацетат; третий фермент превращает пируват в аминокислоту аланин, четвертый — в лактат и так далее. Все эти разные пути конкурируют за одну и ту же молекулу пирувата, и одновременно происходят аналогичные соревнования за тысячи других малых молекул. Возможно, лучше понять эту сложность можно с помощью трехмерной метаболической карты, которая позволяет установить более прямые связи между путями (4).
Рисунок 2-89
Представление всех известных метаболических реакций с участием малых молекул в дрожжевой клетке. Как и на рис. 2-88, реакции гликолиза и цикла лимонной кислоты выделены красным цветом . Эта метаболическая карта необычна тем, что использует трехмерное изображение, (подробнее.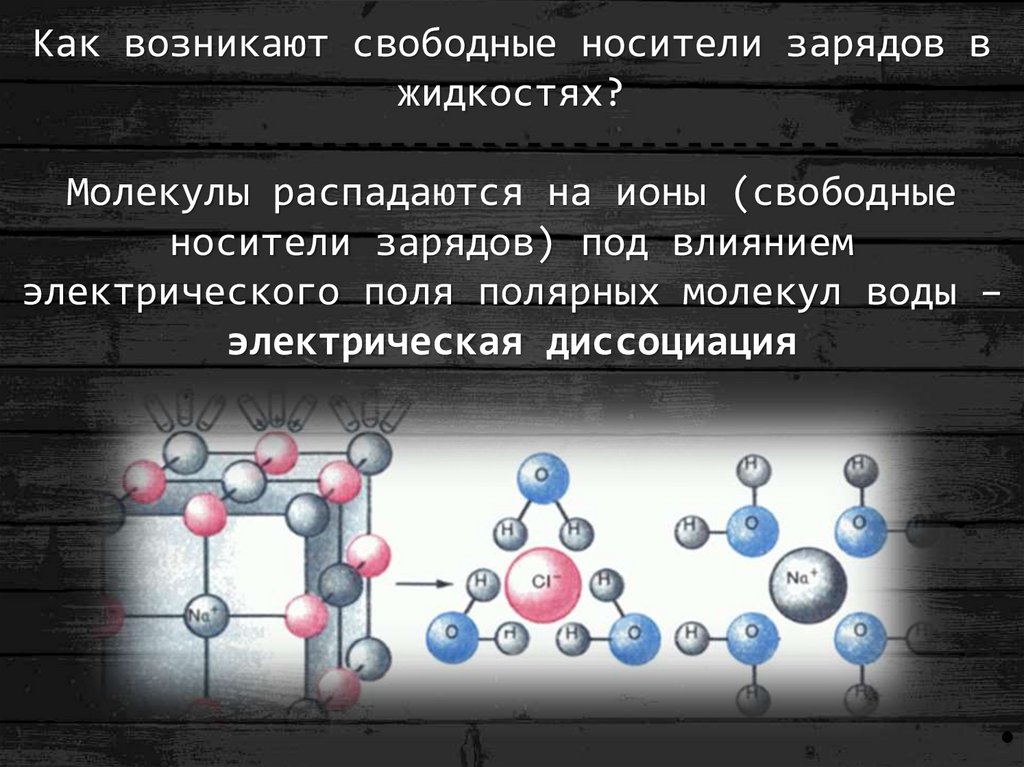 ..)
..)
В многоклеточном организме ситуация еще более усложняется. Разным типам клеток в целом потребуются несколько разные наборы ферментов. И разные ткани вносят различный вклад в химию организма в целом. В дополнение к различиям в специализированных продуктах, таких как гормоны или антитела, существуют значительные различия в «общих» метаболических путях между различными типами клеток одного и того же организма.
Хотя практически все клетки содержат ферменты гликолиза, цикла лимонной кислоты, синтеза и распада липидов и метаболизма аминокислот, уровни этих процессов, необходимых в разных тканях, неодинаковы. Например, нервные клетки, которые, вероятно, являются самыми привередливыми клетками в организме, почти не имеют запасов гликогена или жирных кислот и почти полностью зависят от постоянного поступления глюкозы из кровотока. Напротив, клетки печени снабжают глюкозой активно сокращающиеся мышечные клетки и перерабатывают молочную кислоту, вырабатываемую мышечными клетками, обратно в глюкозу. Все типы клеток имеют свои отличительные черты метаболизма, и они широко взаимодействуют в нормальном состоянии, а также в ответ на стресс и голодание. Можно подумать, что вся система должна быть настолько точно сбалансирована, что любое незначительное нарушение, такое как временное изменение рациона питания, будет иметь катастрофические последствия.
Все типы клеток имеют свои отличительные черты метаболизма, и они широко взаимодействуют в нормальном состоянии, а также в ответ на стресс и голодание. Можно подумать, что вся система должна быть настолько точно сбалансирована, что любое незначительное нарушение, такое как временное изменение рациона питания, будет иметь катастрофические последствия.
Рисунок 2-90
Схематическое изображение метаболического взаимодействия между клетками печени и мышц. Основным топливом активно сокращающихся мышечных клеток является глюкоза, большая часть которой поставляется клетками печени. Молочная кислота, конечный продукт анаэробного распада глюкозы в результате гликолиза (подробнее…)
Фактически, метаболический баланс клетки удивительно стабилен. Всякий раз, когда равновесие нарушается, клетка реагирует так, чтобы восстановить исходное состояние. Клетка может адаптироваться и продолжать функционировать во время голодания или болезни. Мутации многих видов могут повреждать или даже уничтожать определенные пути реакций, и тем не менее — при соблюдении определенных минимальных требований — клетка выживает. Это происходит потому, что сложная сеть из управляющих механизмов регулируют и координируют скорость всех своих реакций. В конечном счете, этот контроль основан на замечательной способности белков изменять свою форму и свой химический состав в ответ на изменения в их непосредственном окружении. Следующей нашей задачей станут принципы, лежащие в основе построения больших молекул, таких как белки, и химия, стоящая за их регуляцией.
Это происходит потому, что сложная сеть из управляющих механизмов регулируют и координируют скорость всех своих реакций. В конечном счете, этот контроль основан на замечательной способности белков изменять свою форму и свой химический состав в ответ на изменения в их непосредственном окружении. Следующей нашей задачей станут принципы, лежащие в основе построения больших молекул, таких как белки, и химия, стоящая за их регуляцией.
Резюме
Глюкоза и другие молекулы пищевых продуктов расщепляются контролируемым ступенчатым окислением с получением химической энергии в виде АТФ и НАДН. Это три основных набора реакций, которые действуют последовательно, продукты каждого из которых являются исходным материалом для следующего: гликолиз (который происходит в цитозоле), цикл лимонной кислоты (в митохондриальном матриксе) и окислительное фосфорилирование (на внутренняя митохондриальная мембрана). Промежуточные продукты гликолиза и цикла лимонной кислоты используются как в качестве источников метаболической энергии, так и для производства многих малых молекул, используемых в качестве сырья для биосинтеза.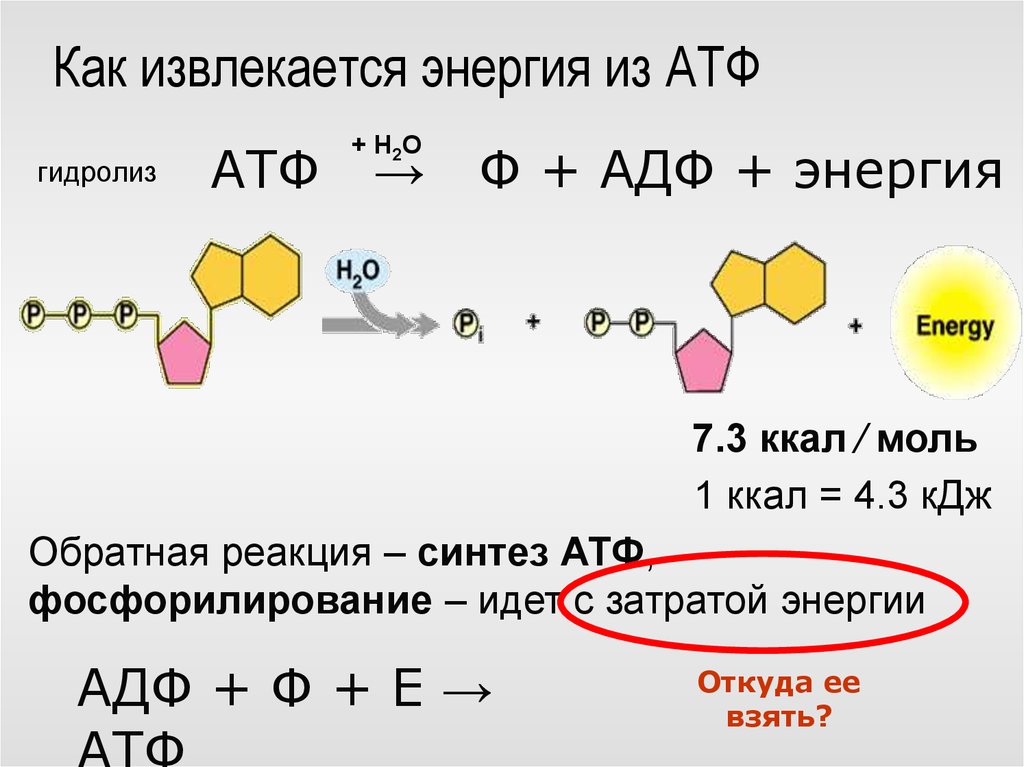 Клетки хранят молекулы сахара в виде гликогена у животных и крахмала у растений; как растения, так и животные также широко используют жиры в качестве продовольственного запаса. Эти материалы для хранения, в свою очередь, служат основным источником пищи для людей, наряду с белками, составляющими большую часть сухой массы клеток, которые мы едим.
Клетки хранят молекулы сахара в виде гликогена у животных и крахмала у растений; как растения, так и животные также широко используют жиры в качестве продовольственного запаса. Эти материалы для хранения, в свою очередь, служат основным источником пищи для людей, наряду с белками, составляющими большую часть сухой массы клеток, которые мы едим.
Что такое химическая энергия? Руководство для начинающих
Химическая энергия может вызвать в воображении образы лабораторий, горелок и пробирок. Но хотя изучение химической энергии, безусловно, связано с наукой, мы можем узнать больше о ее влиянии на нашу повседневную жизнь, даже если мы никогда не ступали в лабораторию.
Что такое химическая энергия? Это что-то в пище, которую мы едим, в электричестве, которое мы производим, и даже в растениях. Давайте поймем этот жизненно важный источник энергии, чтобы глубже оценить его присутствие и силу.
Что такое определение химической энергии?
Химическая энергия — это хранилище энергии, одно из наиболее важных доступных нам хранилищ энергии. Энергия, хранящаяся в объекте, является формой потенциальной энергии.
Энергия, хранящаяся в объекте, является формой потенциальной энергии.
Потенциальная энергия химической энергии хранится в химических связях, связывающих атомы в молекулах. Разрыв этих связей или преобразование их путем добавления топлива или реагентов высвобождает химическую энергию в связях. Мы называем это разрывом и образованием связей химической реакцией. Новое вещество создается после химической реакции.
Топливо или реагенты обеспечивают энергию, необходимую для преобразования химической потенциальной энергии в химическую энергию. Наша способность транспортировать химическую потенциальную энергию и использовать химическую энергию — вот почему она стала основой наших энергетических систем.
Что такое потенциальная химическая энергия?
Мы знаем потенциальную химическую энергию, запасенную в объекте, благодаря количеству и типу химических связей, которые он содержит. Понимание этих значений помогает нам выбрать, как использовать химическую энергию.
Ярким примером являются автомобили. Фургон с пустым топливным баком, припаркованный на вершине холма, обладает потенциальной энергией для движения вниз по склону. Тот же самый фургон у подножия холма имеет меньшую потенциальную энергию, потому что он не будет легко двигаться в гору.
Однако, если мы наполним его бак бензином, мы наполним его топливом, состоящим из различных химических соединений. Двигатель внутреннего сгорания фургона сжигает газ, создавая новые вещества путем разрыва и преобразования связей внутри молекул и атомов бензина. Определенное количество энергии используется для движения фургона, а часть ее создает тепло.
Многие виды топлива, такие как биотопливо, пропан, метан и другие, обладают потенциальной химической энергией. Мы вырабатываем электроэнергию на электростанциях, сжигая ископаемые виды топлива, такие как природный газ, уголь и нефть, высвобождая потенциальную химическую энергию этих материалов.
Эти реакции называются экзотермическими реакциями.
Что происходит во время экзотермической реакции?
Химическая реакция, при которой выделяется тепло, является экзотермической, нагревая окружающую среду благодаря энергии освободил во время процесса.
Экзотермические реакции являются частью нашей повседневной жизни. Мы уже видели, как происходят реакции горения или горения, когда мы сжигаем топливо. Эта химическая реакция высвобождает тепловую энергию в виде тепловой энергии — представьте себе пламя костра или электростанцию, работающую на природном газе.
У меня есть реферальный код
? Если вас направил другой клиент Amigo Energy, введите его личный реферальный код, чтобы получить кредит. Принять условия.
Еще одна экзотермическая реакция имеет решающее значение в борьбе с изменением климата. Сжигание угля на электростанции вызывает химическую реакцию между углеродом, хранящимся в угле, и кислородом окружающей среды, которые объединяются с выделением углекислого газа и тепла. Эти экзотермические реакции происходят, когда вещество реагирует с кислородом. Мы называем их реакциями окисления, и они также производят оксиды.
Эти экзотермические реакции происходят, когда вещество реагирует с кислородом. Мы называем их реакциями окисления, и они также производят оксиды.
Болезненное напоминание об очередной экзотермической реакции возникает, когда нас жалит пчела. Пчелиный яд имеет кислую реакцию, и старое средство — лечить его пищевой содой. То, что происходит на молекулярном уровне, называется реакцией нейтрализации. Эта реакция возникает, когда кислота, подобная пчелиному укусу, взаимодействует с веществами, называемыми основаниями, такими как пищевая сода. Мы называем это реакцией нейтрализации, когда в результате химической реакции образуется вода и соль.
При экзотермических реакциях при образовании новых связей высвобождается больше энергии, чем энергии, необходимой для разрыва связей в реагентах.
Что такое эндотермическая реакция?
Если экзотермическая реакция нагревает окружающую среду, то эндотермическая реакция протекает противоположно. Эндотермическая реакция поглощает тепловую энергию из окружающей среды, охлаждая их и используя энергию.
Самый простой способ изобразить эндотермические реакции — это фотосинтез. Растения поглощают солнечную тепловую энергию и превращают ее в глюкозу для последующего использования для роста. Другим примером является тепловая энергия, поглощаемая кастрюлей для кипячения воды и разогрева пищи.
Как потенциальная энергия преобразуется в химическую энергию?
источник
В термодинамике закон сохранения энергии, также известный как первый закон термодинамики, утверждает, что энергия не может быть уничтожена или создана. Скорее, энергия может только преобразовываться из одной формы энергии в другую.
Мы видели, как потенциальная энергия вещества превращается в химическую энергию при разрыве и восстановлении связей между атомами в молекулах. Появляется новая субстанция или субстанции. Мы называем это экзотермической реакцией, если в результате реакции образуется больше энергии, чем было запасено изначально. Эндотермическая реакция – это реакция, при которой поглощается или используется больше энергии, чем запасается.
Еда — это вкусный способ понять химическую энергию. Давайте отправимся в рощи Калифорнии и соберем сочный апельсин. Апельсиновое дерево выросло и произвело апельсин благодаря фотосинтезу. Дерево преобразовывало солнечную энергию в углеводы, такие как глюкоза, посредством фотосинтеза. Глюкоза — это хранилище потенциальной энергии дерева, и мы можем найти ее в апельсине.
Мы едим апельсин, и наш организм запускает химическую реакцию в желудке, расщепляя потенциальную энергию глюкозы вместе с другими молекулами, богатыми энергией. Химические изменения происходят на молекулярном уровне, высвобождая потенциальную энергию связей. Создано новое вещество под названием аденозинтрифосфат (АТФ). АТФ — это молекула, несущая энергию, которая содержится в клетках всех живых существ.
Что происходит с энергией при разрыве химических связей?
Разорванные связи химических соединений высвобождают энергию по мере образования новых химических связей, создавая новые вещества и тепло.
Те реакции, которые производят больше энергии, чем запасается, называются экзотермическими реакциями. Примером может служить сжигание метана на электростанции для обогрева наших домов. Метан — это углеводород. При сжигании он вступает в реакцию с кислородом и производит углекислый газ и воду в качестве побочных продуктов. Атомы углерода метана рекомбинируют с кислородом, образуя молекулы углекислого газа, а атомы водорода соединяются с кислородом, превращаясь в молекулы воды.
Горение разрушает связи, связывающие исходные водородные и углеродные связи метана. Атомы стремятся сформировать новые связи. Присутствие кислорода означает, что во время горения образуются молекулы воды и углекислого газа. В результате этих реакций высвобождается энергия; в новых связях, содержащихся в молекулах воды и углекислого газа, хранится меньше энергии, чем изначально запасалось в связях метана.
Эта экзотермическая реакция означает, что с химической точки зрения сжигание метана является отличным способом получения тепла. Однако метан является парниковым газом и очень вреден для атмосферы Земли.
Однако метан является парниковым газом и очень вреден для атмосферы Земли.
Где содержится химическая энергия в соединении?
Соединения содержат химическую энергию в связях, связывающих атомы вместе. Мы говорим об энтальпии связи соединения или энергии связи, когда разрываем эти связи.
Энтальпия связи — это количество энергии, необходимое для разрыва этой связи, когда она находится в газообразном состоянии. Это называется теплосодержанием системы.
Сколько видов энергии существует?
Энергия бывает разных форм и делится на две основные категории: накопленная энергия (потенциальная энергия) и энергия движения (кинетическая энергия).
Энергия существует во многих других формах:
- Ядерная энергия обеспечивает энергию благодаря химическим реакциям ядерного синтеза.
- Механическая энергия представляет собой сумму полной энергии потенциальной и кинетической энергии.
- Химическая энергия – это запасенная энергия в веществах, высвобождаемая при образовании и разрыве химических связей.

- Электрическая энергия исходит от потоков электрического заряда и может быть потенциальной или кинетической энергией.
- Лучистая энергия или электромагнитная энергия — это электромагнитные волны, распространяющиеся в пространстве от солнца или от лампочек.
- Тепловая энергия производится за счет повышения температуры и также известна как тепло.
Какие 5 примеров химической энергии?
Есть много примеров химической энергии в нашей повседневной жизни. Вот некоторые из них, которые вы, вероятно, узнаете:
- Еда: Наши тела создают химические реакции для расщепления химических соединений в пище с выделением энергии.
- Пропан : Тепло и свет возникают в результате сжигания пропана, используемого для отопления помещений, автобусов, приготовления пищи и многого другого.
- Автомобильные аккумуляторы: Химические вещества накапливают энергию в элементах аккумуляторов, которые затем преобразуются в электрическую энергию для обеспечения работы автомобилей.

- Взрывчатые вещества: Они накапливают химическую энергию. Взрывы производят свет и тепло в газообразных формах, предлагая пример того, как нестабильные соединения легко и быстро перестраивают свои связи.
- Нефть: Двигатели внутреннего сгорания вызывают выделение тепла и энергии путем реструктуризации атомов и молекул.
Как мы можем генерировать энергию с помощью химической энергии?
Химическая энергия является одним из столпов нашего энергоснабжения, производя тепло, электричество и приводя в действие транспорт по всему миру.
При сжигании ископаемого топлива образуется пар для вращения турбин, производящих электричество. Мы также сжигаем биомассу, биодизель, биотопливо и другие продукты с той же целью.
Наши самолеты, газонокосилки, автомобили и другие машины работают на топливе, которое мы сжигаем. Батареи хранят химическую энергию для последующего использования.
С изменением климата технология солнечных батарей быстро улучшила нашу способность преобразовывать солнечные лучи в химическую энергию, которую мы трансформируем в электрическую энергию.
Использует ли телефон химическую энергию?
Почти каждый каждый день носит с собой немного химической энергии в своем мобильном телефоне. Аккумулятор телефона хранит химическую энергию, которую мы заряжаем электричеством. Это электричество вызывает химическую реакцию внутри батареи, когда мы пользуемся мобильным телефоном, толкая электроны по его цепям.
Как известно, батарейки в телефонах садятся. Это происходит из-за того, что электроны перемещаются по цепи батареи к ее отрицательному концу. Электрическая зарядка подталкивает электроны к положительному концу батареи, чтобы мы могли воспроизвести химическую реакцию и снова использовать наши телефоны.
Является ли древесина источником химической энергии?
Древесина в любой форме обладает химической энергией. Он обладает потенциальной химической энергией, пока ожидает горения, а химическая энергия высвобождается во время горения в виде света и тепла.
Сжигание дров в традиционной кухонной печи представляет собой экзотермическую реакцию, при которой потенциальная энергия древесины высвобождается в виде тепла, согревая печь и кухню.
Деревья растут благодаря энергии солнца. Некоторые считают древесину возобновляемым источником энергии, потому что ее можно вырастить заново в течение нашей жизни. Древесина классифицируется как топливо из биомассы, потому что это энергия растений или животных.
Где хранится химическая энергия в растениях?
источник
Растения хранят солнечную энергию в виде химической энергии в сахаре (глюкозе) и производят кислород благодаря фотосинтезу. Глюкоза присутствует в клетках листьев (называемых хлоропластами), которые полны хлорофилла, облегчающего поглощение света.
Каковы недостатки химической энергии?
Как мы обнаружили, большая часть используемой нами химической энергии поступает из ископаемого топлива, добыча которого обходится дорого и загрязняет планету.
В 2020 году около 79% производства энергии в США приходилось на ископаемое топливо, уголь, нефть и природный газ. Использование огромного количества ископаемого топлива приводит к выбросу углекислого газа и других парниковых газов в атмосферу, что ускоряет глобальное потепление и изменение климата.
Даже альтернативные источники энергии, такие как солнечные батареи, увеличивают углеродный след людей. Минералы требуют добычи, транспортировки материалов и, в конечном счете, панелей потребуется замена и переработка. Добыча древесины требует расчистки леса, а производство биотоплива требует выращивания сельскохозяйственных культур.
У меня есть реферальный код
? Если вас направил другой клиент Amigo Energy, введите его личный реферальный код, чтобы получить кредит. Принять условия.
Энергия — не единственный недостаток химической энергии, как мы видели на примере ядерных бомб. Химическая энергия работала, когда десятки тысяч людей погибли, когда Соединенные Штаты сбросили атомную бомбу на Хиросиму в Японии в 1945 году и Нагасаки тремя днями позже.
Аварии на атомных электростанциях загрязнили огромные участки окружающей среды и унесли жизни многих людей. Печально известные места включают Чернобыль в бывшем Советском Союзе (который считается самой страшной ядерной катастрофой в истории), Фукусима-дайити в Японии и Три-Майл-Айленд в Соединенных Штатах.



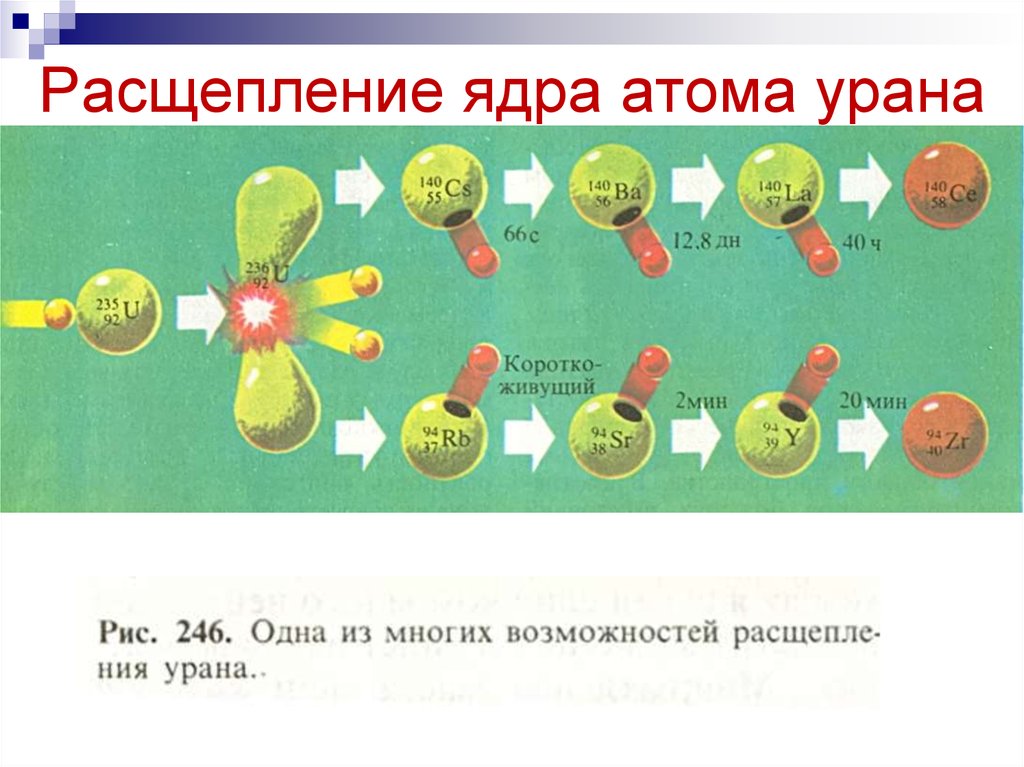 Энергия высвобождается при образовании связи.
Энергия высвобождается при образовании связи.

 Солнце и лампочки излучают электромагнитные волны и, следовательно, лучистую энергию.
Солнце и лампочки излучают электромагнитные волны и, следовательно, лучистую энергию. Химические реакции выделяют тепло в виде тепловой энергии и световой энергии.
Химические реакции выделяют тепло в виде тепловой энергии и световой энергии.