Структура атома: что такое нейтрон?
Что такое нейтрон? Каковы его структура, свойства и функции? Нейтроны — это самые большие из частиц, составляющих атомы, являющиеся строительными блоками всей материи.

Структура атома
Нейтроны находятся в ядре — плотной области атома, также заполненной протонами (положительно заряженными частицами). Эти два элемента удерживаются вместе при помощи силы, называем ядерной. Нейтроны имеют нейтральный заряд. Положительный заряд протона сопоставляется с отрицательным зарядом электрона для создания нейтрального атома. Несмотря на то что нейтроны в ядре не влияют на заряд атома, они все же обладают многими свойствами, которые влияют на атом, включая уровень радиоактивности.

Нейтроны, изотопы и радиоактивность
Частица, которая находится в ядре атома — нейтрон на 0,2% больше протона. Вместе они составляют 99,99% всей массы атома. Атомы одного и того же элемента могут иметь различное количество нейтронов. Когда ученые ссылаются на атомную массу, они имеют в виду среднюю атомную массу. Например, углерод обычно имеет 6 нейтронов и 6 протонов с атомной массой 12, но иногда он встречается с атомной массой 13 (6 протонов и 7 нейтронов). Углерод с атомным номером 14 также существует, но встречается редко. Итак, атомная масса для углерода усредняется до 12,011.
Когда атомы имеют различное количество нейтронов, их называют изотопами. Ученые нашли способы добавления этих частиц в ядро для создания больших изотопов. Теперь добавление нейтронов не влияет на заряд атома, так как они не имеют заряда. Однако они увеличивают радиоактивность атома. Это может привести к очень неустойчивым атомам, которые могут разряжать высокие уровни энергии.

Что такое ядро?
В химии ядро является положительно заряженным центром атома, который состоит из протонов и нейтронов. Слово «ядро» происходит от латинского nucleus, которое является формой слова, означающего «орех» или «ядро». Этот термин был придуман в 1844 году Майклом Фарадеем для описания центра атома. Науки, участвующие в исследовании ядра, изучении его состава и характеристик, называются ядерной физикой и ядерной химией.
Протоны и нейтроны удерживаются сильной ядерной силой. Электроны притягиваются к ядру, но двигаются так быстро, что их вращение осуществляется на некотором расстоянии от центра атома. Заряд ядра со знаком плюс исходит от протонов, а что такое нейтрон? Это частица, которая не имеет электрического заряда. Почти весь вес атома содержится в ядре, так как протоны и нейтроны имеют гораздо большую массу, чем электроны. Число протонов в атомном ядре определяет его идентичность как атома определенного элемента. Число нейтронов означает, какой изотоп элемента является атомом.
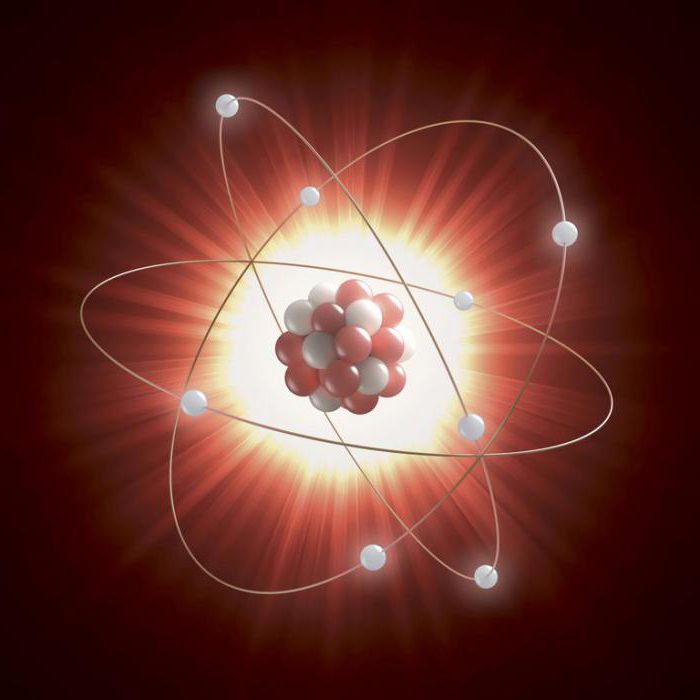
Размер атомного ядра
Ядро намного меньше общего диаметра атома, потому что электроны могут быть отдалены от центра. Атом водорода в 145 000 раз больше своего ядра, а атом урана в 23 000 раз больше своего центра. Ядро водорода является наименьшим, потому что оно состоит из одиночного протона.
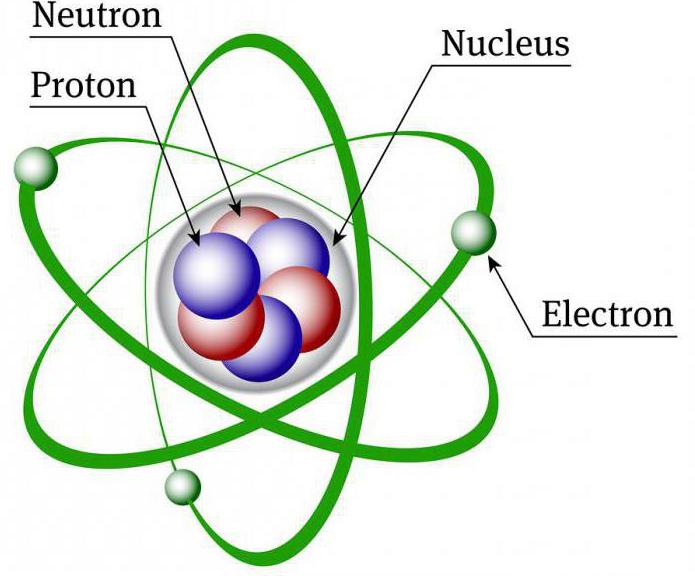
Расположение протонов и нейтронов в ядре
Протон и нейтроны обычно изображаются как уплотненные вместе и равномерно распределенные по сферам. Однако это упрощение фактической структуры. Каждый нуклон (протон или нейтрон) может занимать определенный уровень энергии и диапазон местоположений. В то время как ядро может быть сферическим, оно может быть также грушевидным, шаровидным или дисковидным.

Ядра протонов и нейтронов представляют собой барионы, состоящие из наименьших субатомных частиц, называемых кварками. Сила притяжения имеет очень короткий диапазон, поэтому протоны и нейтроны должны быть очень близки друг к другу, чтобы быть связанными. Это сильное притяжение преодолевает естественное отталкивание заряженных протонов.
Протон, нейтрон и электрон
Мощным толчком в развитии такой науки, как ядерная физика, стало открытие нейтрона (1932 год). Благодарить за это следует английского физика Д. Чедвика, который был учеником Резерфорда. Что такое нейтрон? Это нестабильная частица, которая в свободном состоянии всего за 15 минут способна распадаться на протон, электрон и нейтрино, так называемую безмассовую нейтральную частицу.
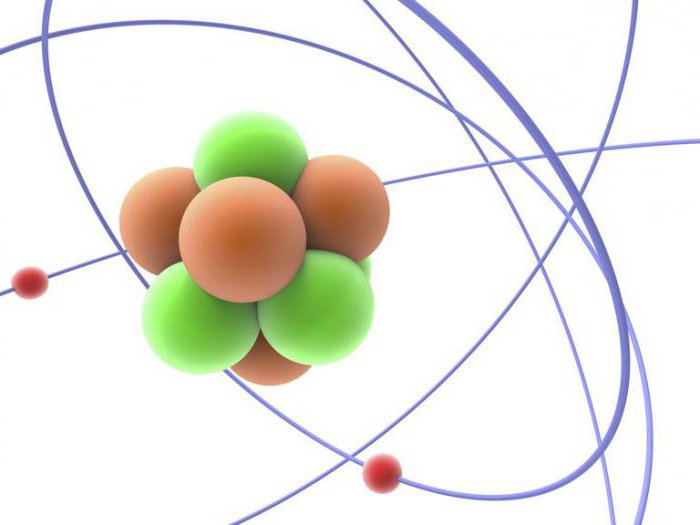
Частица получила свое название из-за того, что она не имеет электрического заряда, она нейтральна. Нейтроны являются чрезвычайно плотными. В изолированном состоянии один нейтрон будет иметь массу всего 1,67·10—27, а если взять чайную ложку плотно упакованную нейтронами, то получившийся кусок материи будет весить миллионы тонн.
Количество протонов в ядре элемента называется атомным номером. Это число дает каждому элементу свою уникальную идентичность. В атомах некоторых элементов, например углерода, число протонов в ядрах всегда одинаково, но количество нейтронов может различаться. Атом данного элемента с определенным количеством нейтронов в ядре называется изотопом.

Опасны ли одиночные нейтроны?
Что такое нейтрон? Это частица, которая наряду с протоном входит в состав ядра атома. Однако иногда они могут существовать сами по себе. Когда нейтроны находятся вне ядер атомов, они приобретают потенциально опасные свойства. Когда они двигаются с высокой скоростью, они производят смертельную радиацию. Так называемые нейтронные бомбы, известные своей способностью убивать людей и животных, при этом оказывают минимальное влияние на неживые физические структуры.
Нейтроны являются очень важной частью атома. Высокая плотность этих частиц в сочетании с их скоростью придает им чрезвычайную разрушительную силу и энергию. Как следствие, они могут изменить или даже разорвать на части ядра атомов, которые поражают. Хотя нейтрон имеет чистый нейтральный электрический заряд, он состоит из заряженных компонентов, которые отменяют друг друга относительно заряда.
Нейтрон в атоме — это крошечная частица. Как и протоны, они слишком малы, чтобы увидеть их даже с помощью электронного микроскопа, но они там есть, потому что это единственный способ, объясняющий поведение атомов. Нейтроны очень важны для обеспечения стабильности атома, однако за пределами его атомного центра они не могут существовать долго и распадаются в среднем всего лишь за 885 секунд (около 15 минут).
Тема №1 «Строение атома» | CHEM-MIND.com
- НОВОСТИ
- КУРС ХИМИИ
- Дополнительные уроки
- Курс химии
- Разбор заданий ЕГЭ
- ТЕСТЫ
- Вариаты ЕГЭ
- Тесты по заданиям
- Тесты по темам
- СТАТЬИ
- ОПЫТЫ
- ТАБЛИЦА МЕНДЕЛЕЕВА
Поиск
 CHEM-MIND.com
CHEM-MIND.com


- НОВОСТИ
-
 Новости
НовостиАлгоритм обучения для подготовки к ЕГЭ по химии

Ответы в тестах вновь правильно отображаются!
 Новости
НовостиТехнические проблемы
 Новости
НовостиНовый раздел на сайте

С 8 марта
-
- КУРС ХИМИИ
- ВсеДополнительные урокиКурс химииРазбор заданий ЕГЭ
 Разбор заданий ЕГЭ
Разбор заданий ЕГЭРазбор задания №11 ЕГЭ по химии

Разбор задания №10 ЕГЭ по химии
 Разбор заданий ЕГЭ
Разбор заданий ЕГЭРазбор задания №9 ЕГЭ по химии
 Разбор заданий ЕГЭ
Разбор заданий ЕГЭРазбор задания №8 ЕГЭ по химии
- ВсеДополнительные урокиКурс химииРазбор заданий ЕГЭ
- ТЕСТЫ
- ВсеВариаты ЕГЭТесты по заданиямТесты по темам
 Тесты по темам
Тесты по темамТест №40 «Высокомолекулярные соединения»
 Тесты по темам
Тесты по темамТест №39 «Химия и проблемы охраны окружающей среды»

Тест №38 «Общие научные принципы химического производства»
 Тесты по темам
Тесты по темамТест №37 «Химическая лаборатория»
- ВсеВариаты ЕГЭТесты по заданиямТесты по темам
- СТАТЬИ
-

Решение типовых задач по химии
 Статьи
СтатьиСовременная таблица Менделеева

Ионные уравнения реакций
 Статьи
СтатьиВнутренний экзамен МГМСУ по химии
 Статьи
СтатьиКниги для подготовки к химии
-
- ОПЫТЫ
-
 Опыты
ОпытыХимическая ракета
 Опыты
ОпытыНеньютоновская жидкость

Лодка на диоксиде углерода
 Опыты
ОпытыКак вырастить жеоду в домашних условиях
 Опыты
ОпытыГорящая рука/пузыри
-
- ТАБЛИЦА МЕНДЕЛЕЕВА
это элементарная частица :: SYL.ru
В этой статье вы найдете информацию о протоне, как элементарной частице, стоящей в основе мироздания наряду с другими её элементами, используемой в химии и физике. Будут определены свойства протона, его характеристика в химии и стабильность.
Что такое протон

Протон — это один из представителей элементарных частичек, который относят к барионам, э.ч. в которых фермионы сильно взаимодействуют, а сама частица состоит из 3-х кварков. Протон является стабильной частицей и имеет личный импульсный момент — спин ½. Физическое обозначение протона — p (или p+)
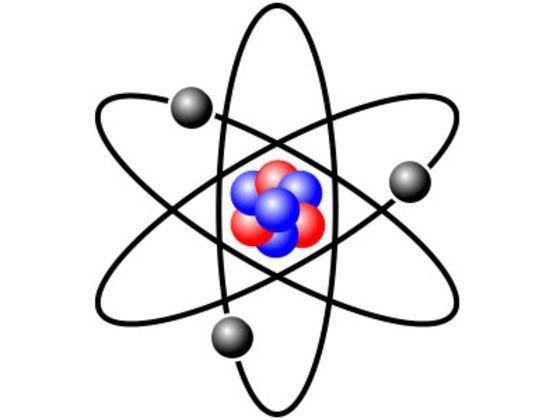
Протон – элементарная частица, принимающая участие в процессах термоядерного типа. Именно этот вид реакций по существу — главный источник энергии, генерируемый звездами во всей вселенной. Практически весь объем энергии, выделяемый Солнцем, существует только за счет объединения 4-х протонов в одно гелиевое ядро с образованием одного нейтрона из двух протонов.
Свойства присущие протону
Протон – это один из представителей барионов. Это факт. Заряд и масса протона – постоянные величины. Электрически протон заряжен +1, а его масса определена в различных единицах измерения и составляет в МэВ 938,272 0813(58), в килограммах протона вес заключен в цифрах 1,672 621 898(21)·10−27 кг, в единицах атомных масс вес протона равен 1,007 276 466 879(91) а. е. м., а в соотношении с массой электрона, протон весит 1836,152 673 89(17) в соотношении с электроном.
Протон, определение которого уже давалось выше, с точки зрения физики, – это элементарная частичка, имеющая проекцию изоспина +½, а ядерная физика воспринимает эту частицу с противоположным знаком. Сам протон является нуклоном, а состоит из 3-х кварков (двух кварков u и одного кварка d).
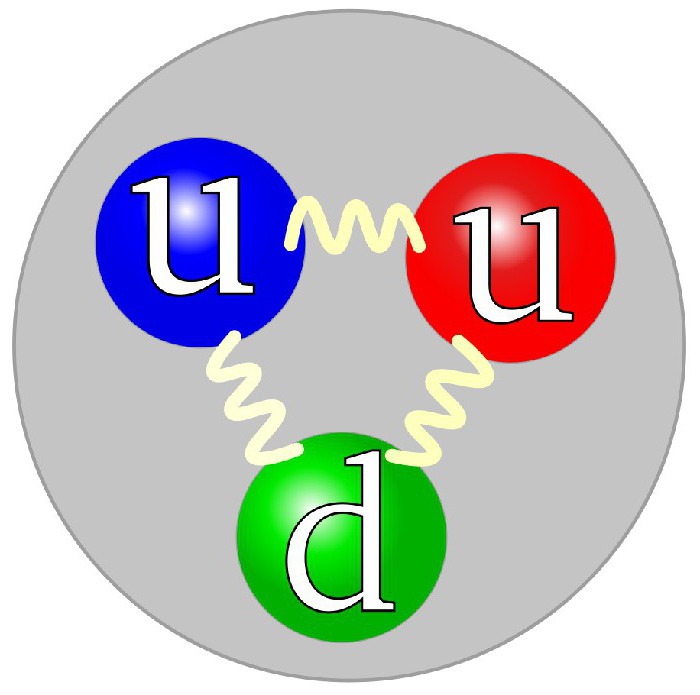
Экспериментально исследовал структуру протона ядерщик-физик из Соединенных Штатов Америки – Роберт Хофштадтер. Для достижения этой цели физик сталкивал протоны с электронами высоких энергий, а за описание был удостоен Нобелевской премии в области физики.
В состав протона входит керн (тяжелая сердцевина), который заключает в себе около тридцати пяти процентов энергии электрического заряда протона и имеет довольно большую плотность. Оболочка, окружающая керн, относительно разряжена. Состоит оболочка в основном из виртуальных мезонов типа и p и несет в себе около пятидесяти процентов электрического потенциала протона и находится на расстоянии, равном приблизительно от 0.25*1013 до 1,4*1013. Еще дальше, на расстоянии около 2,5*1013 сантиметров оболочка состоит из и w виртуальных мезонов и содержит в себе приблизительно оставшиеся пятнадцать процентов электрического заряда протона.
Устойчивость и стабильность протона
В свободном состоянии протон не проявляет никаких признаков распада, что свидетельствует о его стабильности. Стабильное состояние протона, как легчайшего представителя барионов, обусловлено законом сохранения числа барионов. Не нарушая закон СБЧ, протоны способны распадаться на нейтрино, позитрон и другие, более легкие элементарные частицы.
Протон ядра атомов имеет возможность захватывать некоторые виды электронов, имеющие K, L, M атомные оболочки. Протон, совершив электронный захват, переходит в нейтрон и в результате выделяет нейтрино, а образовавшаяся в результате электронного захвата «дыра» заполняется за счет электронов свыше лежащих атомных слоев.
В системах неинерциального отсчета протоны должны приобретать ограниченное время жизни, которое возможно рассчитать, это обусловлено эффектом (излучение) Унру, который в квантовой теории поля предсказывает возможное созерцание теплового излучения в системе отсчета, которая ускоряется при условии отсутствия данного вида излучения. Таким образом, протон при наличии конечного времени своего существования может подвергаться бета-распаду в позитрон, нейтрон или нейтрино, несмотря на то, что сам процесс такого распада запрещен ЗСЭ.
Использование протонов в химии
Протон — это H атом, построенный из единого протона и не имеющий электрона, так что в химическом понимании, протон — это одно ядро атома H. Нейтрон на пару с протоном создают ядро атома. В ПТХЭ Дмитрия Ивановича Менделеева номер элемента указывает число протонов в атоме конкретного элемента, а определяется номер элемента атомным зарядом.
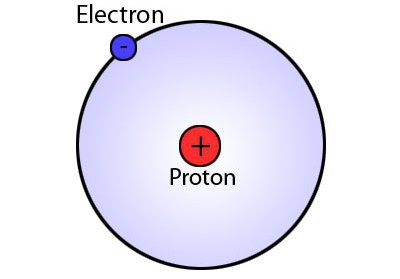
Катионы водорода представляют собой очень сильные электронные акцепторы. В химии протоны получают в основном из кислот органической и минеральной природы. Ионизация является способом получения протонов в газовых фазах.
Протон — это… Что такое Протон?
Прото́н (от др.-греч. πρῶτος — первый, основной) — элементарная частица. Относится к барионам, имеет спин 1/2, электрический заряд +1 (в единицах элементарного электрического заряда). В физике элементарных частиц рассматривается как нуклон с проекцией изоспина +1/2 (в ядерной физике принят противоположный знак проекции изоспина). Состоит из трёх кварков (один d-кварк и два u-кварка). Стабилен (нижнее ограничение на время жизни — 2,9·1029 лет независимо от канала распада, 1,6·1033
Масса протона, выраженная в разных единицах, составляет (рекомендованные значения CODATA 2010 года, в скобках указана погрешность величины в единицах последней значимой цифры, одно стандартное отклонение):
Протоны принимают участие в термоядерных реакциях, которые являются основным источником энергии, генерируемой звёздами. В частности, реакции pp-цикла, который является источником почти всей энергии, излучаемой Солнцем, сводятся к соединению четырёх протонов в ядро гелия-4 с превращением двух протонов в нейтроны.
 Кварковая структура протона
Кварковая структура протонаПротон в химии
Протоны (вместе с нейтронами) являются основными составляющими атомных ядер. Порядковый номер химического элемента в периодической таблице (и, соответственно, все его химические свойства) полностью определяются зарядом ядра его атомов, который, в свою очередь, равен количеству протонов в ядре (протонному числу).
Интересные факты
- Отношение масс протона и электрона, равное 1836,152 672 1(14)[5], с точностью до 0,002 % равно значению 6π5 = 1836,118 108 711 686…
- Ультрарелятивистские протоны (как и любые другие адроны, а также атомные ядра) для неподвижного наблюдателя имеют форму двояковогнутой линзы[6].
- Измерения радиуса протона с помощью атомов обычного водорода, проводимые разными методами с 1960-х годов, привели (CODATA-2006) к результату 0,8768±0,0069 фемтометра (1 фм = 10−15 м)[7]. Первые эксперименты с атомами мюонного водорода[8] дали для этого радиуса на 4 % меньший результат 0,8418±0,0007 фм.[9] Причины такого различия пока неясны.
См. также
Литература
- Многие известные свойства протона систематически изложены в публикации Particle Data Group. [1] (англ.)
Примечания
Протон — это… Что такое Протон?
Прото́н (от др.-греч. πρῶτος — первый, основной) — элементарная частица. Относится к барионам, имеет спин 1/2, электрический заряд +1 (в единицах элементарного электрического заряда). В физике элементарных частиц рассматривается как нуклон с проекцией изоспина +1/2 (в ядерной физике принят противоположный знак проекции изоспина). Состоит из трёх кварков (один d-кварк и два u-кварка). Стабилен (нижнее ограничение на время жизни — 2,9·1029 лет независимо от канала распада, 1,6·1033 лет для распада в позитрон и нейтральный пион).
Масса протона, выраженная в разных единицах, составляет (рекомендованные значения CODATA 2010 года, в скобках указана погрешность величины в единицах последней значимой цифры, одно стандартное отклонение):
Протоны принимают участие в термоядерных реакциях, которые являются основным источником энергии, генерируемой звёздами. В частности, реакции pp-цикла, который является источником почти всей энергии, излучаемой Солнцем, сводятся к соединению четырёх протонов в ядро гелия-4 с превращением двух протонов в нейтроны.
 Кварковая структура протона
Кварковая структура протонаПротон в химии
Ядро атома водорода состоит из одного протона. Протон в химическом смысле является ядром атома водорода (точнее, его лёгкого изотопа — протия) без электрона. В физике протон обозначается буквой p (или p+). Химическое обозначение протона (рассматриваемого в качестве положительного иона водорода) — H+, астрофизическое — HII.
Протоны (вместе с нейтронами) являются основными составляющими атомных ядер. Порядковый номер химического элемента в периодической таблице (и, соответственно, все его химические свойства) полностью определяются зарядом ядра его атомов, который, в свою очередь, равен количеству протонов в ядре (протонному числу).
Интересные факты
- Отношение масс протона и электрона, равное 1836,152 672 1(14)[5], с точностью до 0,002 % равно значению 6π5 = 1836,118 108 711 686…
- Ультрарелятивистские протоны (как и любые другие адроны, а также атомные ядра) для неподвижного наблюдателя имеют форму двояковогнутой линзы[6].
- Измерения радиуса протона с помощью атомов обычного водорода, проводимые разными методами с 1960-х годов, привели (CODATA-2006) к результату 0,8768±0,0069 фемтометра (1 фм = 10−15 м)[7]. Первые эксперименты с атомами мюонного водорода[8] дали для этого радиуса на 4 % меньший результат 0,8418±0,0007 фм.[9] Причины такого различия пока неясны.
См. также
Литература
- Многие известные свойства протона систематически изложены в публикации Particle Data Group. [1] (англ.)
Примечания
Позитрон — Википедия
| Позитрон (e+{\displaystyle e^{+}}) | |
|---|---|
 | |
| Состав | фундаментальная частица[1] |
| Семья | Фермион |
| Группа | Лептон |
| Поколение | первое |
| Участвует во взаимодействиях | гравитационное[2], слабое и электромагнитное |
| Античастица | Электрон |
| Масса | 9,10938356(11)⋅10−31кг[3], |
| Время жизни | ∞ |
| Теоретически обоснована | П. Дирак (1928) |
| Обнаружена | К. Д. Андерсон (1932) |
| Электрический заряд | +1e +1,6021766208(98)⋅10−19 Кл[3] |
| Барионное число | 0 |
| Лептонное число | −1 |
| B−L | +1 |
| Спин | 1/2 ħ |
| Магнитный момент | +9,274009994(57)⋅10−24Дж/Тл |
| Внутренняя чётность | −1 |
| Изотопический спин | 0 |
| Третья компонента слабого изоспина | +1/2 (правая хиральность), 0 (левая хиральность) |
| Слабый гиперзаряд | +1 (правая хиральность), +2 (левая хиральность) |
 Медиафайлы на Викискладе Медиафайлы на Викискладе | |
Позитро́н (от англ. positive «положительный» + electron «электрон») — античастица электрона. Относится к антивеществу, имеет электрический заряд +1, спин 1/2, лептонный заряд −1 и массу, равную массе электрона. При аннигиляции позитрона с электроном их масса превращается в энергию в форме двух (и гораздо реже — трёх и более) гамма-квантов.
Позитроны возникают в одном из видов радиоактивного распада (позитронная эмиссия), а также при взаимодействии фотонов, энергия которых больше 1,022 МэВ, с веществом. Последний процесс называется «рождением пар», ибо при его осуществлении фотон, взаимодействуя с электромагнитным полем ядра, образует одновременно электрон и позитрон. Также позитроны способны возникать в процессах рождения электрон-позитронных пар в сильном электрическом поле.
Существование позитрона впервые было предположено в 1928 году[4]Полем Дираком. Теория Дирака описывала не только электрон с отрицательным электрическим зарядом, но и аналогичную частицу с положительным зарядом. Отсутствие такой частицы в природе рассматривалось как указание на «лишние решения» уравнений Дирака. Зато открытие позитрона явилось триумфом теории.
В соответствии с теорией Дирака электрон и позитрон могут рождаться парой, и на этот процесс должна быть затрачена энергия, равная энергии покоя этих частиц, 2×0,511 МэВ. Поскольку были известны естественные радиоактивные вещества, испускавшие γ-кванты с энергией больше 1 МэВ, представлялось возможным получить позитроны в лаборатории, что и было сделано. Экспериментальное сравнение свойств позитронов и электронов показало, что все физические характеристики этих частиц, кроме знака электрического заряда, совпадают.
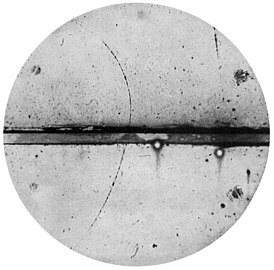
Позитрон был открыт в 1932 году американским физиком Андерсоном при наблюдении космического излучения с помощью камеры Вильсона, помещённой в магнитное поле. Он сфотографировал следы частиц, которые очень напоминали следы электронов, но имели изгиб под действием магнитного поля, противоположный следам электронов, что свидетельствовало о положительном электрическом заряде обнаруженных частиц. Вскоре после этого открытия, также с помощью камеры Вильсона, были получены фотографии, проливавшие свет на происхождение позитронов: под действием γ-квантов вторичного космического излучения позитроны рождались в парах с обычными электронами. Такие свойства вновь открытой частицы оказались в поразительном согласии с уже имевшейся релятивистской теорией электрона Дирака. В 1934 году Ирен и Фредерик Жолио-Кюри во Франции открыли ещё один источник позитронов — β+-радиоактивность.
Название «позитрон» придумал сам Андерсон. Андерсон также предлагал переименовать электроны в «негатроны»; этот термин в отношении электронов по-прежнему используют в случаях, когда электроны и позитроны рассматриваются совместно[5]; в этих случаях термин «электрон» часто относят к обеим частицам — электрону (негатрону) и позитрону[6].
Позитрон оказался первой открытой античастицей. Существование античастицы электрона и соответствие суммарных свойств двух античастиц выводам теории Дирака, которая могла быть обобщена на другие частицы, указывали на возможность парной природы всех элементарных частиц и ориентировало последующие физические исследования. Такая ориентация оказалась необычайно плодотворной, и в настоящее время парная природа элементарных частиц является точно установленным законом природы, обоснованным большим числом экспериментальных фактов.
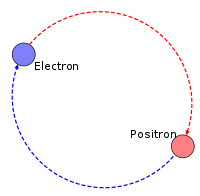
Из теории Дирака следует, что электрон и позитрон при столкновении должны аннигилировать с освобождением энергии, равной полной энергии сталкивающихся частиц. Оказалось, что этот процесс происходит главным образом после торможения позитрона в веществе, когда полная энергия двух частиц равна их энергии покоя 1,0221 МэВ. На опыте были зарегистрированы пары γ-квантов с энергией по 0,511 МэВ, разлетавшихся в прямо противоположных направлениях от мишени, облучавшейся позитронами. Необходимость возникновения при аннигиляции электрона и позитрона не одного, а как минимум двух γ-квантов вытекает из закона сохранения импульса. Суммарный импульс в системе центра масс позитрона и электрона до процесса превращения равен нулю, но если бы при аннигиляции возникал только один γ-квант, он бы уносил импульс, который не равен нулю в любой системе отсчёта.
С 1951 года известно, что в некоторых аморфных телах, жидкостях и газах позитрон после торможения в значительном числе случаев сразу не аннигилирует, а образует на короткое время связанную с электроном систему, получившую название позитроний. Позитроний в смысле своих химических свойств аналогичен атому водорода, так как представляет собой систему, состоящую из единичных положительного и отрицательного электрических зарядов, и может вступать в химические реакции. Поскольку электрон и позитрон — разные частицы, то в связанном состоянии с наинизшей энергией они могут находиться не только с антипараллельными, но и с параллельными спинами. В первом случае полный спин позитрония s = 0, что соответствует парапозитронию, а во втором — s = 1, что соответствует ортопозитронию. Интересно, что аннигиляция электрон-позитронной пары в составе ортопозитрония не может сопровождаться рождением двух γ-квантов. Два γ-кванта уносят друг относительно друга механические моменты, равные 1, и могут составить полный момент, равный нулю, но не единице. Поэтому аннигиляция в этом случае сопровождается испусканием трёх γ-квантов с суммарной энергией 1,022 МэВ. Образование ортопозитрония в три раза более вероятно, чем парапозитрония, так как отношение статистических весов (2s+1) обоих состояний позитрония 3:1. Однако даже в телах с большим процентом (до 50 %) аннигиляции пары в связанном состоянии, то есть после образования позитрония, преимущественно появляются два γ-кванта и лишь очень редко три. Дело в том, что время жизни парапозитрония около 10−10 с, а ортопозитрония — около 10−7 с. Долгоживущий ортопозитроний, непрерывно взаимодействующий с атомами среды, не успевает аннигилировать с испусканием трёх γ-квантов прежде, чем позитрон, входящий в его состав, аннигилирует с посторонним электроном в состоянии с антипараллельными спинами и с испусканием двух γ-квантов.
Возникающие при аннигиляции остановившегося позитрона два гамма-кванта несут энергию по 511 кэВ и разлетаются в строго противоположных направлениях. Этот факт позволяет установить положение точки, в которой произошла аннигиляция, и используется в позитрон-эмиссионной томографии.
В 2007 году экспериментально доказано существование связанной системы из двух позитронов и двух электронов (молекулярный позитроний). Такая молекула распадается ещё быстрее, чем атомарный позитроний.
Считается, что в первые мгновения после Большого взрыва количество позитронов и электронов во Вселенной было примерно одинаково, однако при остывании эта симметрия нарушилась. Пока температура Вселенной не понизилась до 1 МэВ, тепловые фотоны постоянно поддерживали в веществе определённую концентрацию позитронов путём рождения электрон-позитронных пар (такие условия существуют и сейчас в недрах горячих звёзд). После охлаждения вещества Вселенной ниже порога рождения пар оставшиеся позитроны аннигилировали с избытком электронов.
В космосе позитроны рождаются при взаимодействии с веществом гамма-квантов и энергичных частиц космических лучей, а также при распаде некоторых типов этих частиц (например, положительных мюонов). Таким образом, часть первичных космических лучей составляют позитроны, так как в отсутствие электронов они стабильны. В некоторых областях Галактики обнаружены аннигиляционные гамма-линии 511 кэВ, доказывающие присутствие позитронов.
В солнечном термоядерном pp-цикле (а также в CNO-цикле) часть реакций сопровождается эмиссией позитрона, который немедленно аннигилирует с одним из электронов окружения; таким образом, часть солнечной энергии выделяется в виде позитронов, и в ядре Солнца всегда присутствует некоторое их количество (в равновесии между процессами образования и аннигиляции).
Некоторые природные радиоактивные ядра (первичные, радиогенные, космогенные) испытывают бета-распад с излучением позитронов. Например, часть распадов природного изотопа 40K происходит именно по этому каналу. Кроме того, гамма-кванты с энергией более 1,022 МэВ, возникающие при радиоактивных распадах, могут рождать электрон-позитронные пары.
При взаимодействии электронного антинейтрино (с энергией больше 1,8 МэВ) и протона происходит реакция обратного бета-распада с образованием позитрона: p++ν¯e→n0+e+.{\displaystyle p^{+}+{\bar {\nu }}_{e}\rightarrow n^{0}+e^{+}.} Такая реакция происходит в природе, поскольку существует поток антинейтрино с энергией выше порога обратного бета-распада, возникающих, например, при бета-распаде природных радиоактивных ядер.
- Все известные свойства позитрона систематизированы в обзоре Particle Data Group [1].
- Климов А. Н. Ядерная физика и ядерные реакторы. М. Атомиздат, 1971.
Протон — это… Что такое Протон?
Прото́н (от др.-греч. πρῶτος — первый, основной) — элементарная частица. Относится к барионам, имеет спин 1/2, электрический заряд +1 (в единицах элементарного электрического заряда). В физике элементарных частиц рассматривается как нуклон с проекцией изоспина +1/2 (в ядерной физике принят противоположный знак проекции изоспина). Состоит из трёх кварков (один d-кварк и два u-кварка). Стабилен (нижнее ограничение на время жизни — 2,9·1029 лет независимо от канала распада, 1,6·1033 лет для распада в позитрон и нейтральный пион).
Масса протона, выраженная в разных единицах, составляет (рекомендованные значения CODATA 2010 года, в скобках указана погрешность величины в единицах последней значимой цифры, одно стандартное отклонение):
Протоны принимают участие в термоядерных реакциях, которые являются основным источником энергии, генерируемой звёздами. В частности, реакции pp-цикла, который является источником почти всей энергии, излучаемой Солнцем, сводятся к соединению четырёх протонов в ядро гелия-4 с превращением двух протонов в нейтроны.
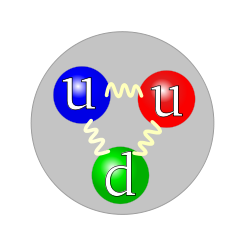 Кварковая структура протона
Кварковая структура протонаПротон в химии
Ядро атома водорода состоит из одного протона. Протон в химическом смысле является ядром атома водорода (точнее, его лёгкого изотопа — протия) без электрона. В физике протон обозначается буквой p (или p+). Химическое обозначение протона (рассматриваемого в качестве положительного иона водорода) — H+, астрофизическое — HII.
Протоны (вместе с нейтронами) являются основными составляющими атомных ядер. Порядковый номер химического элемента в периодической таблице (и, соответственно, все его химические свойства) полностью определяются зарядом ядра его атомов, который, в свою очередь, равен количеству протонов в ядре (протонному числу).
Интересные факты
- Отношение масс протона и электрона, равное 1836,152 672 1(14)[5], с точностью до 0,002 % равно значению 6π5 = 1836,118 108 711 686…
- Ультрарелятивистские протоны (как и любые другие адроны, а также атомные ядра) для неподвижного наблюдателя имеют форму двояковогнутой линзы[6].
- Измерения радиуса протона с помощью атомов обычного водорода, проводимые разными методами с 1960-х годов, привели (CODATA-2006) к результату 0,8768±0,0069 фемтометра (1 фм = 10−15 м)[7]. Первые эксперименты с атомами мюонного водорода[8] дали для этого радиуса на 4 % меньший результат 0,8418±0,0007 фм.[9] Причины такого различия пока неясны.
См. также
Литература
- Многие известные свойства протона систематически изложены в публикации Particle Data Group. [1] (англ.)



 Новости
Новости
 Новости
Новости Новости
Новости
 Разбор заданий ЕГЭ
Разбор заданий ЕГЭ
 Разбор заданий ЕГЭ
Разбор заданий ЕГЭ Разбор заданий ЕГЭ
Разбор заданий ЕГЭ Тесты по темам
Тесты по темам Тесты по темам
Тесты по темам
 Тесты по темам
Тесты по темам
 Статьи
Статьи
 Статьи
Статьи Статьи
Статьи Опыты
Опыты Опыты
Опыты
 Опыты
Опыты Опыты
Опыты