| ЭлектронElectron Электрон – самая
лёгкая отрицательно заряженная частица, составная часть атома. Основные характеристики электрона
Электрон – первая из открытых элементарных частиц – был открыт
Дж. Дж. Томсоном
в 1897 г. Изучая характеристики газового разряда, Томсон показал, что катодные
лучи, образующиеся в разрядной трубке, состоят из отрицательно заряженных
частиц вещества. Отклоняя катодные лучи в электрических и магнитных полях,
он определил отношение заряда к массе этих частиц e/m = 6. |
«объясните пятикласснику, что такое протон, электрон и другие частицы, что они делают и зачем нужны?» — Яндекс Кью
Дам свой вариант ответа.
Протон, электрон и другие частицы — это очень-очень-оооочень маленькие частицы. Можно представлять их, например, как круглые пылинки (хотя это будет не совсем точно, но это лучше, чем вообще никак). Такие маленькие, что невозможно просто так рассмотреть одну такую пылинку. Всё вещество, всё что мы видим, всё что можем потрогать — совершенно всё состоит из этих частиц. Земля состоит из них, воздух из них, Солнце из них, человек из них.
Земля состоит из них, воздух из них, Солнце из них, человек из них.
Люди всегда хотели разобраться, как весь мир устроен. Из чего он состоит. Вот у нас есть горстка песка. Очевидно, что песок состоит из песчинок. А из чего состоит песчинка? Песчинка — это прочно слипшийся комочек, очень маленький камешек. Оказалось, что песчинку можно разделить на части. А если эти части ещё раз разделить на более мелкие части? А потом ещё раз? Можно ли, в конце-концов, найти что-такое, что уже нельзя будет разделить?
Люди, действительно, обнаружили, что в конечном счёте всё состоит из «пылинок», которые уже нельзя просто так разделить. Эти пылинки назвали «молекулами». Есть молекула воды, есть молекула кварца (кстати, песок, в основном, состоит из кварца), есть молекула соли (той, которую мы едим) и очень много разных других молекул.
Если же попытаться разделить, например, молекулу воды на части, то окажется, что составляющие части ведут себя уже совсем не как вода. Люди назвали эти части «атомами». Оказалось, что вода всегда разделяется на 3 атома. При этом 1 атом — это кислород, а другие 2 атома — это водород (их в воде 2 штуки). Если соединить любой атом кислорода с любыми 2 атомами водорода — опять будет вода.
Оказалось, что вода всегда разделяется на 3 атома. При этом 1 атом — это кислород, а другие 2 атома — это водород (их в воде 2 штуки). Если соединить любой атом кислорода с любыми 2 атомами водорода — опять будет вода.
При этом из кислорода и водорода можно кроме воды сделать и другие молекулы. Например, 2 атома кислорода легко соединяются друг с другом в такой «двойной кислород» (называется «молекула кислорода»). Такого кислорода очень много в нашем воздухе, мы им дышим, он нам нужен для жизни.
То есть оказалось, что у молекул есть «части», которые должны работать вместе, чтобы получился нужный результат. Это, например, как игрушечная машинка. У машинки, допустим, должна быть кабина и 4 колеса. Только когда они все вместе собраны — это машинка. Если же чего-то не хватает, то это уже не машинка. Если же вместо колёс поставить гусеницы — то будет вообще не машина, а танк (ну почти). Так и с молекулами. Чтобы была вода, она обязательно должна состоять из 1 кислорода и 2 водорода. Но по отдельности — это не вода.
Но по отдельности — это не вода.
Когда люди поняли, что все молекулы состоят из разного набора атомов, это людей обрадовало. Поизучав атомы, люди увидели, что в природе существует всего лишь около 100 разных атомов. То есть, люди узнали что-то новое о мире. Что всё-всё, что мы видим — это всего лишь 100 разных атомов. Но из-за того, что они соединены по разному, получается огромное разнообразие молекул (миллионы, миллиарды и даже больше разных молекул).
А что дальше?
Можно ли взять и разделить какой-нибудь атом? Теми средствами, которые существовали в средневековье, разделить атом было невозможно. Поэтому какое-то время считалось, что атом разделить нельзя. Считалась, что «атомы» — это самые маленькие частицы, из которых состоит весь мир.
Однако, в итоге, атом разделить удалось. И обнаружилось (самое чудесное), что с атомами та же ситуация. Оказалось, что все 100 (их немного больше 100, на самом деле) разных атомов распадаются на всего лишь 3 разных вида частиц.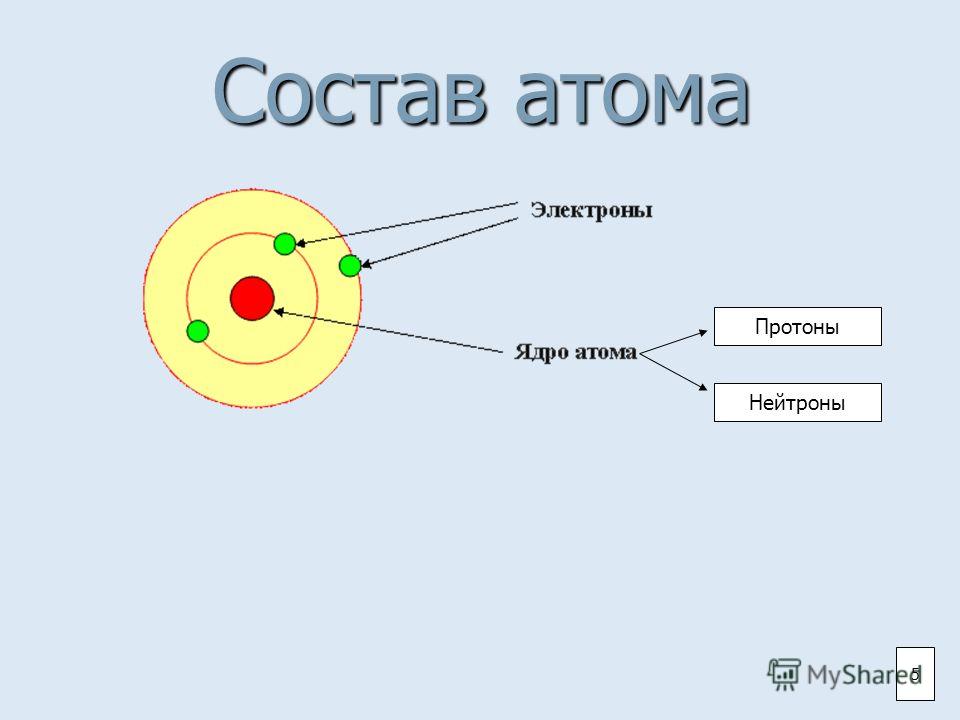 Всего 3! Оказалось, что все атомы — это набор из «протонов», «нейтронов» и «электронов», которые соединены в атоме определённым образом. Разное количество этих частиц, будучи соединёнными вместе, дают разные атомы.
Всего 3! Оказалось, что все атомы — это набор из «протонов», «нейтронов» и «электронов», которые соединены в атоме определённым образом. Разное количество этих частиц, будучи соединёнными вместе, дают разные атомы.
Есть чему радоваться: человечество докопалось до понимания, что всё-всё многообразие мира — это всего лишь 3 элементарные частицы.
А можно ли разделить какую-нибудь элементарную частицу? Например, можно ли разделить протон? Сейчас считается, что частицы (например, протон) тоже состоят из частей, которые назвали «кварки». Но, насколько я знаю, до сих пор ни разу не удалось отделить «кварк» от частицы, чтобы «посмотреть», что же это такое, когда оно находится отдельно, само по себе (а не в составе частицы). Похоже, что кварки не могут (или же очень не хотят) существовать иначе, кроме как внутри частицы.
Так что на данный момент протон, нейтрон и электрон — это самые маленькие части нашего мира, которые могут существовать отдельно, и из которых всё состоит. Это действительно, впечатляет.
Правда, радость длилась не очень долго. Потому что оказалось, что кроме протона, нейтрона и электрона существует множество других разновидностей частиц. Однако, в природе они почти никогда не встречаются. Не замечено, чтобы что-то большое в природе было построено из иных частиц, нежели чем протон, нейтрон и электрон. Но известно, что эти другие частицы можно получить искусственно, если несколько частиц разогнать до умопомрачительных скоростей (около миллиарда километров в час) и стукнуть ими по другим частицам.
Об устройстве атома.
Теперь можно немножко поговорить об атоме и его частицах (протонах, нейтронах, электронах).
Чем отличаются разные частицы? Протон и нейтрон — тяжёлые. А электрон — лёгкий. Конечно, поскольку все частицы очень маленькие — они все очень лёгкие. Но электрон, если не ошибаюсь, в тысячу раз легче, чем протон или нейтрон. А протон и нейтрон зато очень похожи по массе. Почти точь в точь (с чего бы? может быть, это не случайно?).
Протоны и нейтроны в атоме всегда соединяются вместе и образуют этакий «шарик», который называют «ядром». А вот электронов в ядре никогда не бывает. Вместо этого электроны вращаются вокруг ядра. Для наглядности часто говорят, что электроны вращаются вокруг ядра «как планеты вокруг Солнца». На самом деле, это не совсем так. Это примерно настолько же правда, насколько детский мультик похож на реальную жизнь. Вроде бы почти одинаково, но в реальности всё гораздо сложнее и непонятнее. В общем, 5-класснику полезно будет представить что электроны «летают вокруг ядра, как планеты вокруг Солнца». А потом где-нибудь в 7-9 классе можно будет прочитать про чудеса квантового микро-мира. Там ещё более чудесные чудеса, чем в Алисе в Стране Чудес. В том смысле, что там (на уровне атомов) всё происходит не так, как мы привыкли.
А вот электронов в ядре никогда не бывает. Вместо этого электроны вращаются вокруг ядра. Для наглядности часто говорят, что электроны вращаются вокруг ядра «как планеты вокруг Солнца». На самом деле, это не совсем так. Это примерно настолько же правда, насколько детский мультик похож на реальную жизнь. Вроде бы почти одинаково, но в реальности всё гораздо сложнее и непонятнее. В общем, 5-класснику полезно будет представить что электроны «летают вокруг ядра, как планеты вокруг Солнца». А потом где-нибудь в 7-9 классе можно будет прочитать про чудеса квантового микро-мира. Там ещё более чудесные чудеса, чем в Алисе в Стране Чудес. В том смысле, что там (на уровне атомов) всё происходит не так, как мы привыкли.
Также несколько электронов можно отделить от атома без очень уж больших усилий. Тогда получится атом без нескольких электронов. Эти электроны (их тогда называют «свободные электроны») будут летать сами по себе. Кстати, если взять много свободных электронов — получится электричество, с помощью которого в 21-м веке работает почти всё классное :).
Итак, протоны и нейтроны — тяжёлые. Электрон — лёгкий. Протоны и нейтроны — в ядре. Электроны — крутятся вокруг или же летают где-то сами по себе (обычно, немного полетав, они прицепляются к другим атомам).
А чем протон отличается от нейтрона? В целом они очень похожи, за исключением одной важной штуки. Протон имеет зяряд. А нейтрон — не имеет. Электрон, кстати, тоже имеет заряд, но другого типа…
А что такое «заряд»? Ну… Я думаю, что на этом вопросе нам лучше остановиться, потому что нужно же где-то остановиться.
Если ты захочешь узнать подробности, пиши, я отвечу. А пока что, я думаю, и этой информации на первый раз очень много.
Структура атома | Протоны, нейтроны, электроны
Учебные пособия
- Сообщение от Мелани Кац
27 Январь
Основные понятия:
Что такое атом? В этом уроке по атомной структуре вы узнаете о различных частях атома, а также о субатомных частицах, обнаруженных в каждой области. Вы также узнаете о свойствах, которые можно найти в субатомных частицах. Эти свойства включают атомный номер , атомная масса и чистый заряд . Вы также узнаете определения атомов — что такое электрон, что такое протон и что такое нейтрон.
Вы также узнаете о свойствах, которые можно найти в субатомных частицах. Эти свойства включают атомный номер , атомная масса и чистый заряд . Вы также узнаете определения атомов — что такое электрон, что такое протон и что такое нейтрон.
Описано в других статьях:
- Количественное определение протонов, нейтронов и электронов
- Ионные/ковалентные связи
- Как записать конфигурации электронов
- Периодические тренды
- Как была открыта периодическая таблица
- Как читать периодическую таблицу
- Модель атома Бора
- Модель атома Дальтона
- Ядерные реакции
Что такое атом?
Итак, , каково определение атома ? Атом — это строительный блок материи, используемый для определения характеристик элемента. Изучите определение элемента.
Атомы способны взаимодействовать друг с другом посредством связывания, образуя более сложные вещества, также известные как молекулы. Эти взаимодействия определяют состояние вещества, в котором находятся атомы, поскольку они могут быть твердыми, жидкими или газообразными.
Эти взаимодействия определяют состояние вещества, в котором находятся атомы, поскольку они могут быть твердыми, жидкими или газообразными.
Из каких частей состоит атом?
Атомы состоят из 3 основных компонентов, известных как субатомные частицы, состоящих из протонов (положительно заряженных), нейтронов (без заряда) и электронов (отрицательно заряженных). Это части атома.
Атомная структура этих строительных блоков очень интересна. Протоны и нейтроны расположены в центре атома, а электроны довольно далеко от центра. Рассмотрим эти атомарные частицы более подробно.
Важные понятия:
- Атомы состоят из очень маленьких частиц, называемых протонами, нейтронами и электронами – частями атома.
- Протоны и нейтроны находятся в центре атома и составляют ядро.
- Протоны имеют положительный заряд.
- Нейтроны имеют нейтральный заряд (без заряда).
- Электроны имеют отрицательный заряд и находятся далеко от ядра.

- Заряды протона и электрона абсолютно одинаковы по величине, но противоположны по знаку.
- Протоны и электроны притягиваются друг к другу, поскольку имеют противоположные заряды.
Что такое протоны?
Протон Определение: Протоны — это положительно заряженные субатомные частицы, находящиеся в ядрах всех атомов. Заряд протона +1. Атомный номер элемента равен количеству протонов в ядре. Протоны состоят из двух верхних кварков и одного нижнего кварка. Он имеет массу 1,007277 а.е.м. (атомные единицы массы).
Что такое нейтроны?
Определение нейтрона: Так что же такое нейтрон? Нейтрон — это нейтрально заряженная субатомная частица, присутствующая в ядре всех атомов, кроме водорода. Нейтрон имеет массу чуть больше массы протона.
Нейтрон — это тип адрона, который состоит из одного верхнего кварка и двух нижних кварков. Он имеет массу 1,008665 а.е.м. (атомные единицы массы). При бета-распаде нейтрон может превратиться в протон, электрон и антинейтрино. Протоны и нейтроны называются нуклонами .
Протоны и нейтроны называются нуклонами .
Нейтроны важны, потому что они определяют изотоп элемента. Например, углерод с 6 нейтронами — это углерод-12, но добавьте еще два нейтрона, и вы получите углерод-14, присутствие которого в органическом материале используется при радиоуглеродном датировании, известном как датирование по углероду-14.
Что такое электроны?
Определение электрона: Электроны — это субатомные частицы, вращающиеся вокруг ядра атома. Они имеют отрицательный заряд и намного меньше, чем протоны или нейтроны. На самом деле они в 1800 раз меньше. Они также несут электричество. Заряд электрона равен -1. Электрон несет заряд 1,6 х 10-19кулоны. У них нет известных компонентов или подструктуры. Они имеют массу 0,000549 а.е.м.
Что такое ядро
Поговорим подробнее об атомной структуре. Центр атома называется ядром и состоит из протонов и нейтронов. Эта часть атома способна определять широкий спектр свойств, таких как атомный номер и атомная масса .
Атомный номер элемента определяется по количеству протонов, присутствующих в ядре. Пример: углерод имеет 6 протонов в ядре, что делает его также шестым элементом в периодической таблице.
Как найти атомную массу
Самый простой способ найти атомную массу элемента — посмотреть в периодическую таблицу. Атомная масса также может быть рассчитана путем сложения количества нейтронов и протонов. Это связано с тем, что электроны имеют очень маленькую массу, поэтому не вносят существенного вклада в атомную массу. Пример: Атом кислорода, содержащий 8 протонов и 8 нейтронов, имеет атомную массу 16 а.е.м. (протоны и нейтроны имеют массу примерно 1 а.е.м.). Вы также можете рассчитать среднюю атомную массу, известную как атомный вес, если вы знаете распространенность каждого изотопа.
Вы можете узнать о том, как было открыто ядро.
Что такое электронные оболочки
электронных оболочек расположены в самой внешней области атома, окружающей ядро. Эта область содержит только электроны и способна определить суммарный заряд атома.
Эта область содержит только электроны и способна определить суммарный заряд атома.
Суммарный заряд атома определяется разностью общего числа электронов и протонов. Если атом содержит больше протонов, чем электронов, суммарный заряд положительный, и наоборот. Пример: атом, содержащий 5 протонов и 3 электрона, имеет суммарный заряд +2.
Части атома – словарь Определения:
Протоны : Положительно заряженные субатомные частицы, находящиеся в ядре.
Нейтроны : Нейтрально заряженные субатомные частицы, находящиеся в ядре.
Электроны : Отрицательно заряженные субатомные частицы, обнаруженные в электронных оболочках, окружающих ядро.
Ядро : Область, расположенная в центре атома, содержащая как протоны, так и нейтроны.
Электронные оболочки : Область, расположенная на самой внешней части атома, содержащая только электроны.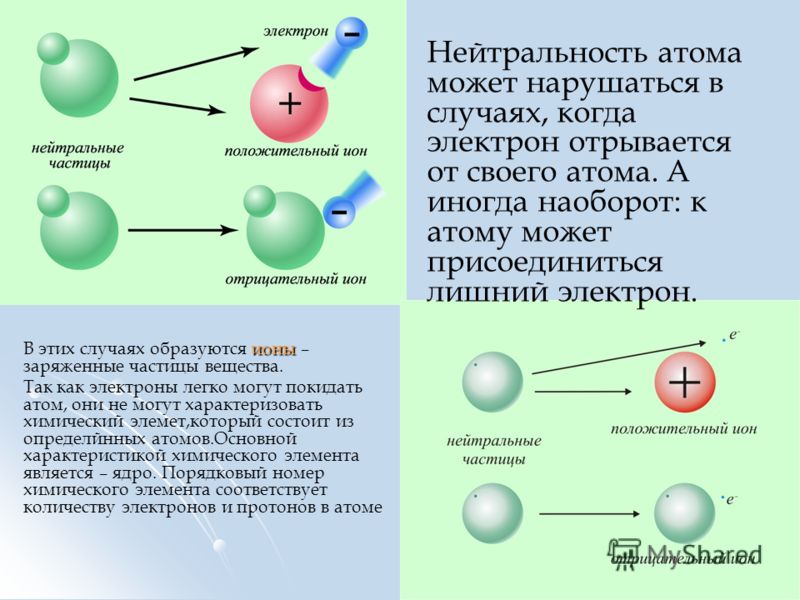
Атомная структура: Как протоны, нейтроны и электроны расположены в атоме
Chem4Kids.com: Атомы: Электроны
Материя | Атомы | Элементы | Периодическая таблица | Реакции | Биохимия | Все темы
Обзор | Структура | Орбиты | Электроны | Ионы | Нейтроны | Изотопы | Склеивание | Соединения | Составные имена | Радиоактивность и антиматерия
Электроны – это отрицательно заряженных частиц атома. Вместе все электроны атома создают отрицательный заряд , который уравновешивает положительный заряд протонов в атомном ядре. Электроны очень маленькие по сравнению со всеми остальными частями атома.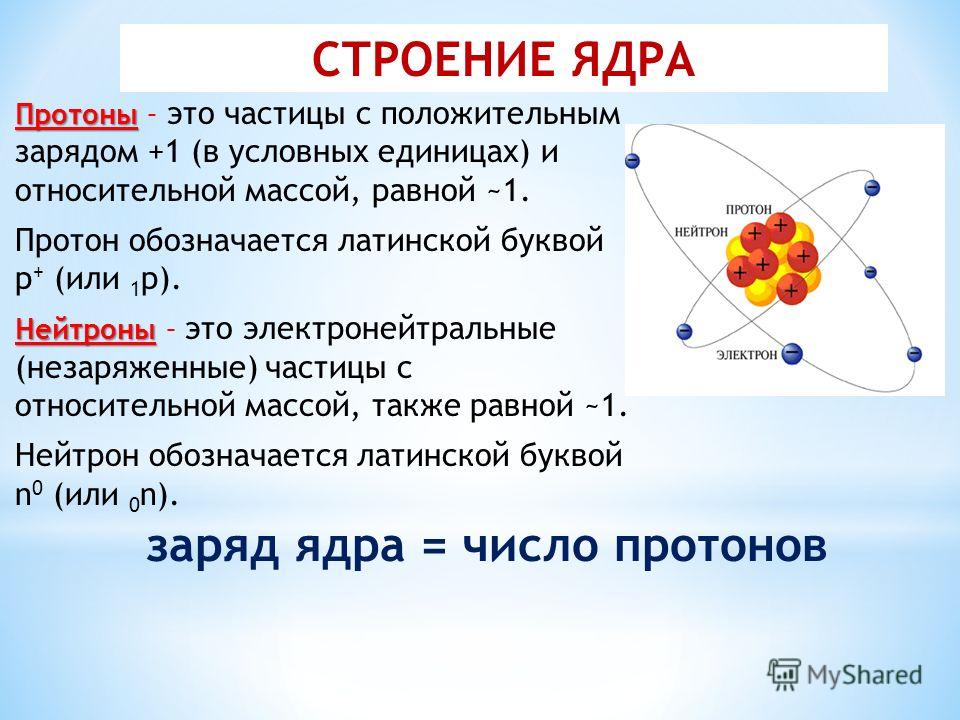 Масса электрона почти в 1000 раз меньше массы протона.
Масса электрона почти в 1000 раз меньше массы протона.
Электроны находятся в облаках , окружающих ядро атома. Эти облака находятся на определенном расстоянии от ядра и обычно организованы в виде оболочек. Поскольку электроны движутся так быстро, невозможно увидеть, где они находятся в конкретный момент времени. После многих лет экспериментов ученые обнаружили определенные области, в которых с большой вероятностью могут быть обнаружены электроны. Общая форма оболочек меняется в зависимости от того, сколько электронов имеет элемент. Чем выше атомный номер, тем больше оболочек и электронов будет иметь атом. Общая форма оболочки также будет более сложной (из-за суборбиталей ), так как у вас больше электронов.
Электроны играют главную роль во всех химических связях . Существует один тип связи, называемый электровалентной связью (ионной), когда электрон от одного атома передается другому атому. Вы в конечном итоге создаете два иона, поскольку один атом теряет электрон, а другой приобретает его. Второй тип связи называется ковалентной связью , когда электроны фактически распределяются между двумя или более атомами в облаке. Оба типа облигаций имеют определенные преимущества и недостатки.
Вы в конечном итоге создаете два иона, поскольку один атом теряет электрон, а другой приобретает его. Второй тип связи называется ковалентной связью , когда электроны фактически распределяются между двумя или более атомами в облаке. Оба типа облигаций имеют определенные преимущества и недостатки.
Электроны очень важны в мире электроники. Очень маленькие частицы могут течь по проводам и цепям, создавая токи электричества . Электроны движутся от отрицательно заряженных частей к положительно заряженным. Отрицательно заряженные части любой цепи имеют дополнительные электроны, в то время как положительно заряженные части нуждаются в большем количестве электронов. Затем электроны переходят из одной области в другую. Когда электроны движутся, ток может течь через систему.
► СЛЕДУЮЩАЯ СТРАНИЦА ПО АТОМАМ
► ВИКТОРИНА О СТРУКТУРЕ АТОМА
► ВЕРНУТЬСЯ НА НАЧАЛО СТРАНИЦЫ
► Или выполните поиск на сайтах.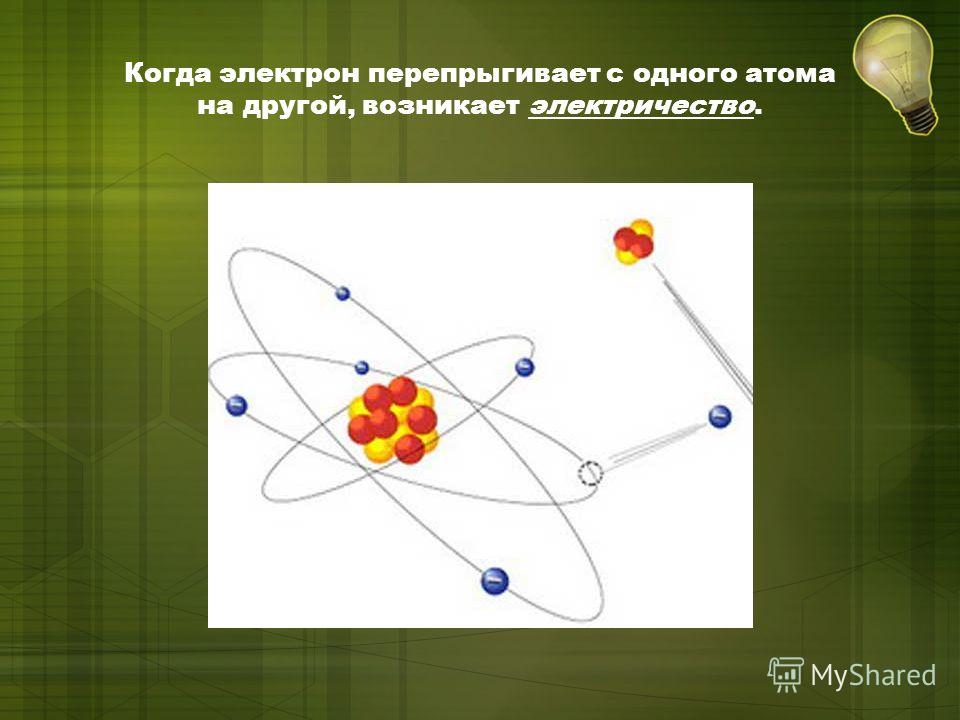


 Боттомоний
Боттомоний Чармоний
Чармоний Электрон
в атоме связан с центральным положительно заряженным ядром электростатическим
притяжением. Он имеет отрицательный заряд е = 1.602.10-19 Кл, массу mе = 0.511 МэВ/с2 = 9.11.10-28 г и спин 1/2 (в единицах ћ), т.е. является фермионом. Магнитный момент электрона
μе>>μВ, где μВ = ећ/2mес – магнетон
Бора (использована Гауссова система единиц), что согласуется с моделью точечноподобной
бесструктурной частицы (согласно опытным данным размер электрона < 10-17 см). В пределах точности эксперимента электрон стабильная частица. Его время
жизни
Электрон
в атоме связан с центральным положительно заряженным ядром электростатическим
притяжением. Он имеет отрицательный заряд е = 1.602.10-19 Кл, массу mе = 0.511 МэВ/с2 = 9.11.10-28 г и спин 1/2 (в единицах ћ), т.е. является фермионом. Магнитный момент электрона
μе>>μВ, где μВ = ећ/2mес – магнетон
Бора (использована Гауссова система единиц), что согласуется с моделью точечноподобной
бесструктурной частицы (согласно опытным данным размер электрона < 10-17 см). В пределах точности эксперимента электрон стабильная частица. Его время
жизни 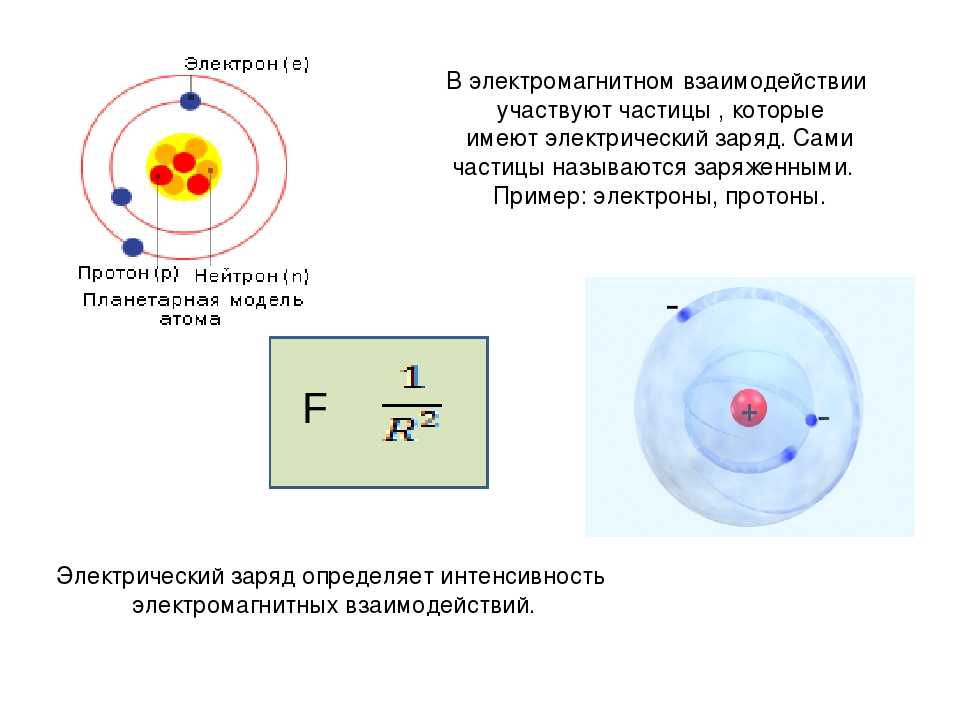 У электрона имеется специальная
характеристика, присущая лептонам, – электронное лептонное число + 1.
У электрона имеется специальная
характеристика, присущая лептонам, – электронное лептонное число + 1. 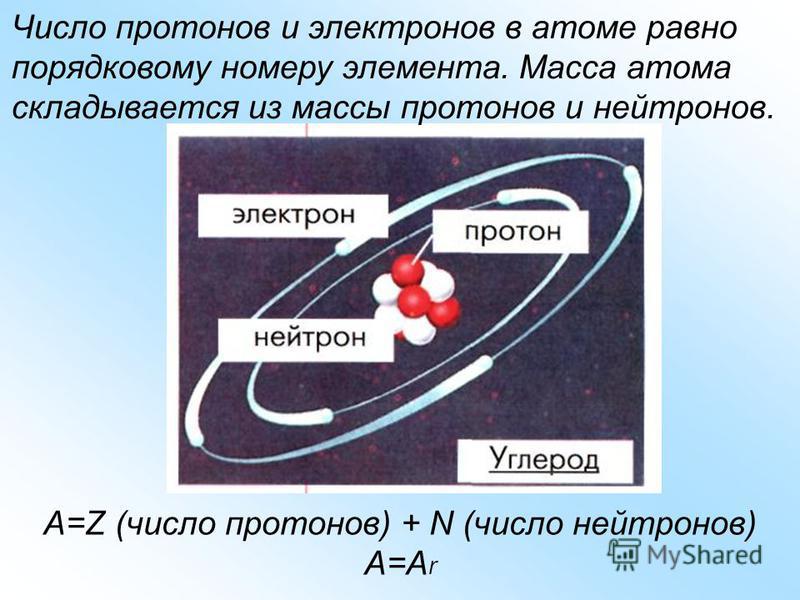 0011596521859± 0.0000000000038
0011596521859± 0.0000000000038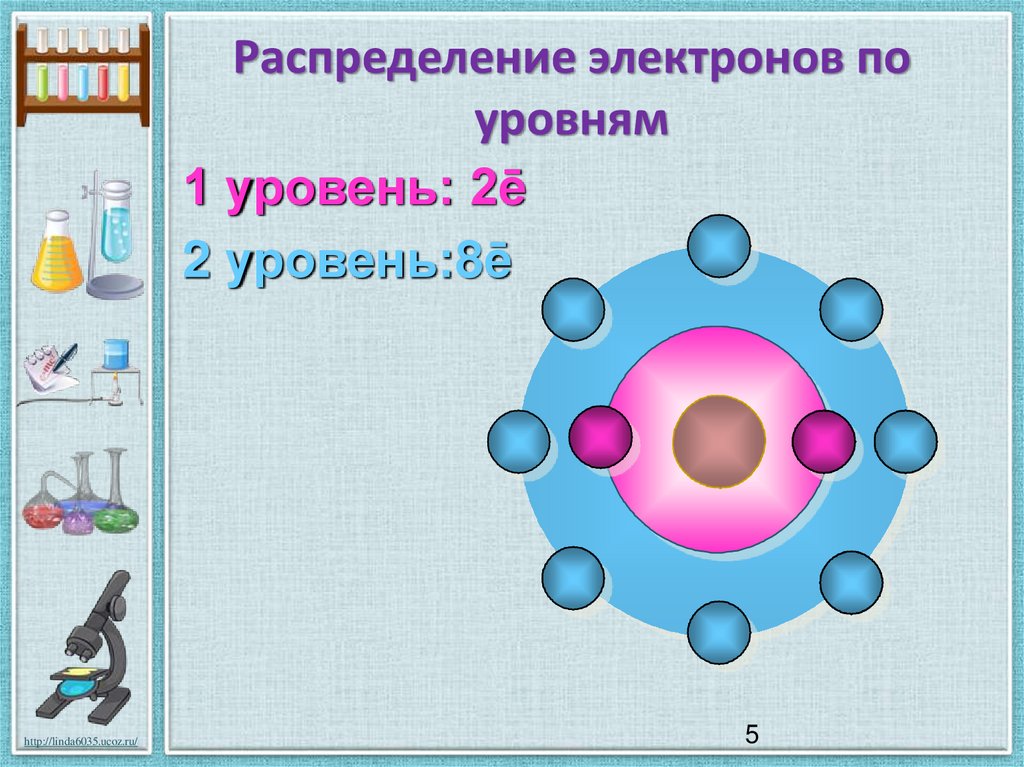 7·1017 ед. СГСЭ/г (современное значение 5.27·1017 ед. СГСЭ/г). Он показал,
что катодные лучи представляют собой поток более лёгких, чем атомы, частиц
и не зависят от состава газа. Эти частицы были названы электронами. Открытие
электрона и установление того факта, что все атомы содержат электроны, явилось
важной информацией о внутреннем строении атома.
7·1017 ед. СГСЭ/г (современное значение 5.27·1017 ед. СГСЭ/г). Он показал,
что катодные лучи представляют собой поток более лёгких, чем атомы, частиц
и не зависят от состава газа. Эти частицы были названы электронами. Открытие
электрона и установление того факта, что все атомы содержат электроны, явилось
важной информацией о внутреннем строении атома.