Электролиты вольт амперная характеристика
Сверхпроводимость — явление потери Ме электрического сопротивления при определенной температуре. Искровой разряд сопровождается выделением большого количества теплоты, ярким свечением газа, треском или громом. Коронный разряд возникает при нормальном давлении в газе, находящемся в сильно неоднородном электрическом поле например, около остриев или проводов линий высокого напряжения. Основной причиной дугового разряда является интенсивное испускание термоэлектронов раскаленным катодом. Эти электроны ускоряются электрическим полем и производят ударную ионизацию молекул газа. Решение задач по физике
Поиск данных по Вашему запросу:
Схемы, справочники, даташиты:
Прайс-листы, цены:
Обсуждения, статьи, мануалы:
Дождитесь окончания поиска во всех базах.
По завершению появится ссылка для доступа к найденным материалам.
Содержание:
- Энциклопедия по машиностроению XXL
- Справочник химика 21
- Электрический ток в различных средах.
Гальванический элемент. Постоянный электрический ток
- Электрический ток в различных средах. Гальванический элемент. Постоянный электрический ток
- Вы точно человек?
- Электрический ток в жидкостях
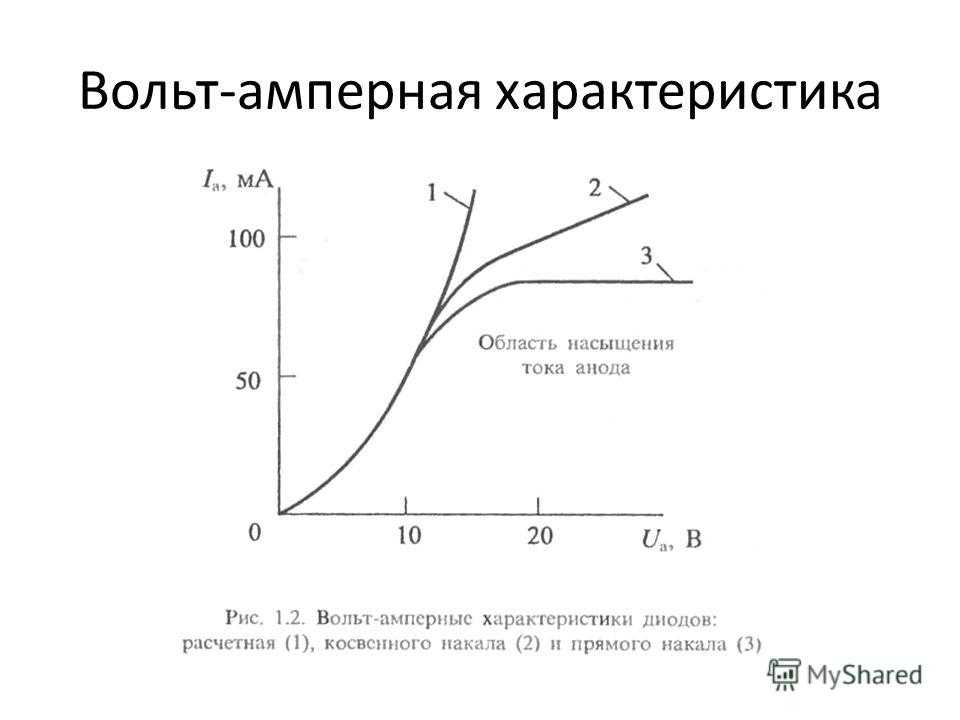
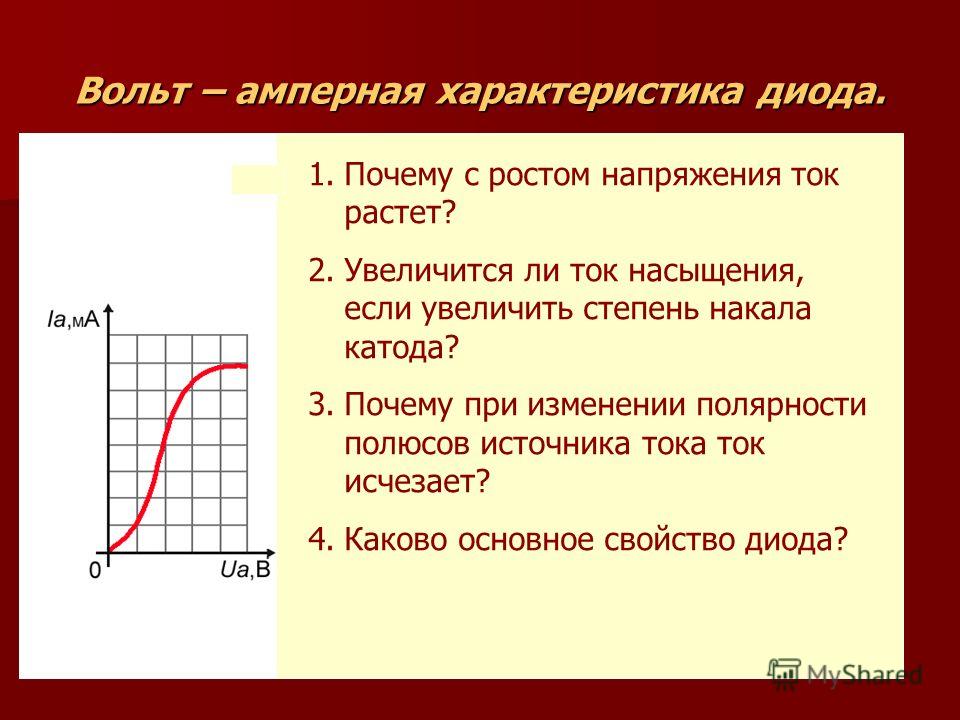
- Вольтамперная характеристика вакуумного диода.
ПОСМОТРИТЕ ВИДЕО ПО ТЕМЕ: ВАХ-Вольт Амперная характеристика all-audio.pro ее узнать и проверить светодиод.
Энциклопедия по машиностроению XXL
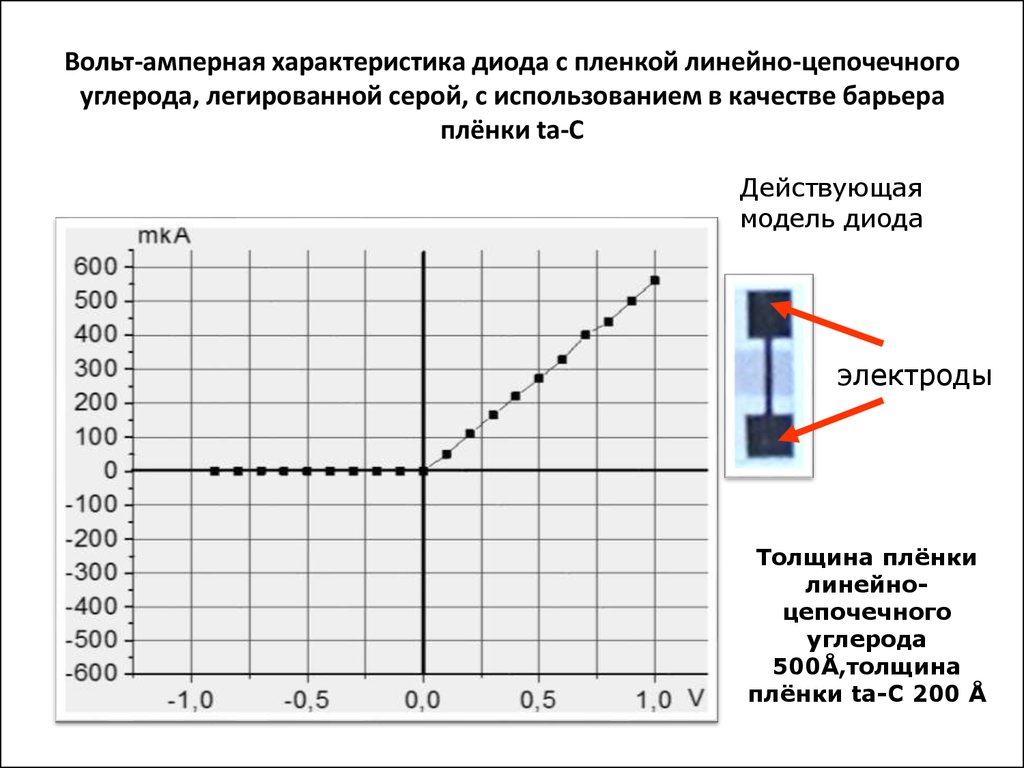
Наличие потенциального барьера на границе металл — полупроводник приводит к тому, что возможно явление выпрямления переменного тока, а ВАХ для постоянного тока будет несимметричной. За положительное напряжение U примем такое напряжение, когда металл имеет положительный потенциал относительно полупроводника. Так как в области объемного заряда L свободных электронов практически нет, то удельное сопротивление этой области очень велико и все внешнее напряжение будет падать в этой области.
За положительное напряжение U примем такое напряжение, когда металл имеет положительный потенциал относительно полупроводника. Так как в области объемного заряда L свободных электронов практически нет, то удельное сопротивление этой области очень велико и все внешнее напряжение будет падать в этой области.
Результирующий поток электронов направлен от полупроводника к металлу и увеличивается с ростом внешнего напряжения. Вследствие этого поток электронов jП со стороны полупроводника уменьшится, и при увеличении U этот поток станет очень мал. Поэтому через барьер будет проходить только постоянный поток электронов из металла. Из диаграммы, представленной на рис. Результирующий ток равен:. Вольт-амперная характеристика ВАХ , построенная по уравнению 8 , показана на рис.
Этот ток jS получил название тока насыщения. Вольт-амперная характеристика выпрямляющего контакта полупроводника с металлом. Приведенный вывод ВАХ получил название диодной теории. В рассматриваемом случае эти электроны вылетают не в вакуум, а должны пролететь через слой объёмного заряда толщиной L без столкновений с атомами решетки полупроводника.
Электрон будет двигаться через барьер под действием электрического поля напряжённостью E с дрейфовой скоростью. Так будет в области барьера, где объемный заряд, обусловленный контактной разностью потенциалов, делает поле E x неоднородным. Ток, протекающий через полупроводник, должен быть одинаков в любом поперечном сечении полупроводника. Согласно статистике электронов в энергетических зонах полупроводника известно, что концентрация электронов в зоне проводимости равна:.
Как видно из рис. При подаче напряжения U из тех же уравнений 11 , 13 и 14 получим, что диффузионный поток электронов из металла через барьерный слой в полупроводнике создает ток. Видно, что напряжение U увеличивает диффузионный ток сравните уравнения 14 и Связано это с тем, что напряжение U изменяет вид распределения n x. Однако обратный поток электронов из полупроводника в металл j изменяется из-за изменения высоты потенциального барьера со стороны полупроводника под влиянием напряжения U.
Используя 3 , получим:.
Поэтому соответственно говорят о прямых и обратных токах через контакт. Одностороннюю проводимость контактов металл — полупроводник используют для изготовления полупроводниковых усилителей переменного тока. Металлический электрод обычно состоит из сплава различных металлов например, Bi, Cd и Sn.
К пластине полупроводника прижимается или приваривается металлическая проволока малого диаметра микроны. Воспользуемся уравнением вольт-амперной характеристики диффузионной теории и определим дифференциальное сопротивление p-n перехода при очень малых значениях напряжения. Если все величины имеют размерность системы СИ, то величина контактной разности потенциалов Uк выражена в вольтах. Установка для определения контактной разности потенциалов представляет собой мостовую схему рис.
В качестве нулевого прибора используется узкополосный усилитель, настроенный на частоту 50 Гц. На выходе этого усилителя включен ламповый индикатор настройки. Момент балансировки моста отмечается по максимальному раскрытию сектора индикатора.
Температура измеряется контактным термометром. При прямом включении диода менять напряжение до 1 В. Переключатель выпрямителя должен находиться в положении 6 В. Напряжение регулируется потенциометром выпрямителя. При обратном включении диода менять напряжение до В при высоких температурах — до 70 0С ручкой потенциометра на плате 4,7 МОм.
Сила тока в проводниках по закону Ома прямо пропорциональна напряжению. Такая зависимость имеет место для проводников со строго заданным сопротивлением для резисторов. Тангенс угла наклона графика равен проводимости проводника. Проводимостью называется величина, обратная сопротивлению. Но так как сопротивление металлов зависит от температуры, то вольт-амперная характеристика металлов не является линейной.
Магнитное поле — особый вид материи. Его источником является любое переменное электрическое поле. Магнитное поле является силовым полем. Силовой характеристикой магнитного поля называют магнитную индукцию. Магнитная индукция — это некторная физическая величина, равная максимальной силе, действующей со стороны магнитного поля на единичный элемент тока:. Единичный элемент тока — это проводник длиной 1 м и силой тока в нем 1 А. Единицей измерения магнитной индукции является тесла Тл.
Магнитное поле является вихревым полем. Для графического изображения магнитных полей вводятся силовые линии, или линии магнитной индукции, — это такие линии, в каждой точке которых вектор магнитной индукции направлен по касательной.
Направление силовых линий находится по правилу буравчика. Если буравчик ввинчивать по направлению тока в проводнике, то направление вращения рукоятки совпадет с направлением силовых линий.
Напряженность магнитного поля [H] — это отношение магнитной индукции к магнитной проницаемости среды. Был установлен экспериментально в году Био и Саваром и сформулирован в общем виде Лапласом.
Был установлен экспериментально в году Био и Саваром и сформулирован в общем виде Лапласом.
Лаплас показал также, что с помощью этого закона можно вычислить магнитное поле движущегося точечного заряда считая движение одной заряженной частицы током. Если близко один к другому расположены проводники с токами одного направления, то магнитные линии этих проводников, охватывающие оба проводника, обладая свойством продольного натяжения и стремясь сократиться, будут заставлять проводники притягиваться Магнитные линии двух проводников с токами разных направлений в пространстве между проводниками направлены в одну сторону.
Магнитные линии, имеющие одинаковое направление, будут взаимно отталкиваться. Поэтому проводники с токами противоположного направления отталкиваются один от другого. Электрический ток может проходить через различные вещества при определенных условиях. Одним из условий возникновения электрического тока является наличие свободных зарядов, способных двигаться под действием электрического поля.
Вне электрического поля свободные электроны движутся хаотически, подобно молекулам идеального газа, а потому рассматриваются в классической электронной теории как электронный газ. Под действием внешнего электрического поля меняется характер движения свободных электронов внутри металла. Электроны, продолжая хаотичные движения, вместе с тем смещаются в направлении действия сил электрического поля. Следовательно, электрический ток в металлах — это упорядоченное движение электронов.
Плотность тока проводимости численно равна заряду, проходящему за 1с через единицу площади поверхности, перпендикулярной направлению тока. У большинства металлов практически каждый атом ионизирован. Явление распада молекул солей, щелочей и кислот в воде на ионы противоположных знаков называют электролитической диссоциацией. Полученные в следствие распада ионы служат носителями заряда в жидкости, а сама жидкость становятся проводником.
Вне электрического поля ионы движутся хаотически. Под действием внешнего электрического поля ионы, продолжая хаотичные движения, вместе с тем смещаются в направлении действия сил электрического поля: катионы к катоду, анионы — к аноду. Следовательно, электрический ток в растворах расплавах электролитов — это направленное перемещение ионов обоих знаков в противоположных направлениях.
Прохождение электрического тока через раствор электролита всегда сопровождается выделением на электродах веществ, входящих в его состав. Это явление называют электролизом. При движении внутри электролитов ионы взаимодействуют с молекулами воды и другими ионами, то есть электролиты оказывают некоторое противодействие движению, а, следовательно, обладают сопротивлением. Электрическое сопротивление электролитов зависит от концентрации ионов, величины заряда иона, от скорости движения ионов обоих знаков.
При увеличении температуры электролита уменьшается его вязкость, что ведет к увеличению скорости движения ионов.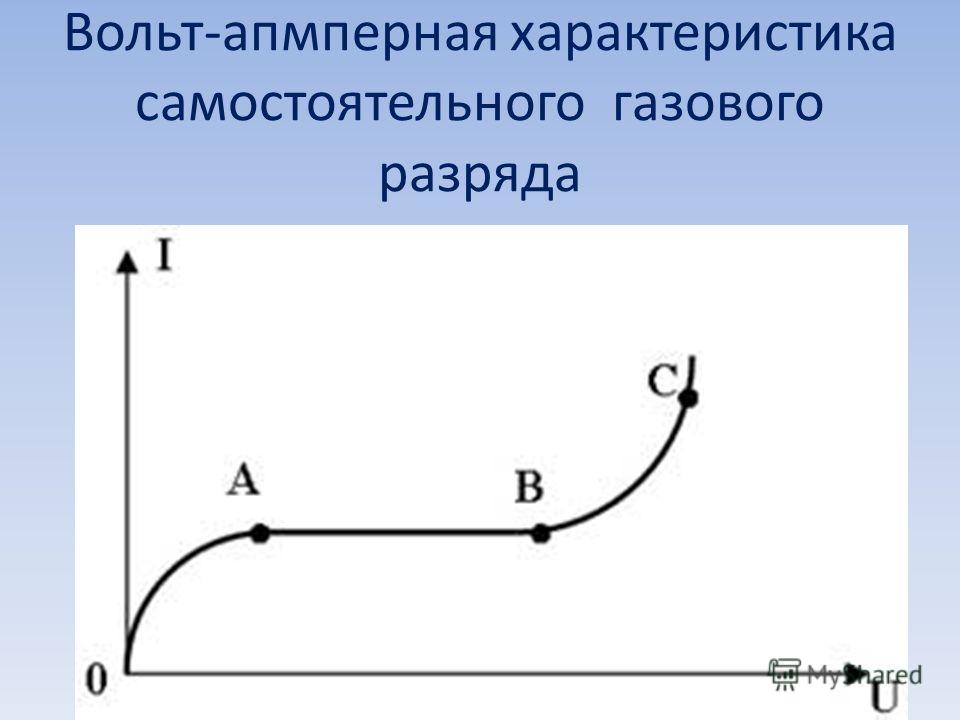 Масса вещества, выделяемого на электроде, прямо пропорциональна электрическому заряду, прошедшему через электролит. Электрохимический эквивалент вещества прямо пропорционален его химическому эквиваленту. Для ионизации молекул необходимо затратить энергию — энергию ионизации, количество которой зависит от рода вещества.
Масса вещества, выделяемого на электроде, прямо пропорциональна электрическому заряду, прошедшему через электролит. Электрохимический эквивалент вещества прямо пропорционален его химическому эквиваленту. Для ионизации молекул необходимо затратить энергию — энергию ионизации, количество которой зависит от рода вещества.
Так, энергия ионизации минимальна для атомов щелочных металлов, максимальна — для инертных газов. Ионизировать молекулы можно при нагревании газа, при облучении его различного рода лучами. Электроны, оторвавшись от молекулы могут присоединятся к нейтральным молекулам, образуя при этом отрицательно заряженные ионы. Следовательно, при ионизации появляются три типа носителей зарядов: положительные ионы, отрицательные ионы и электроны.
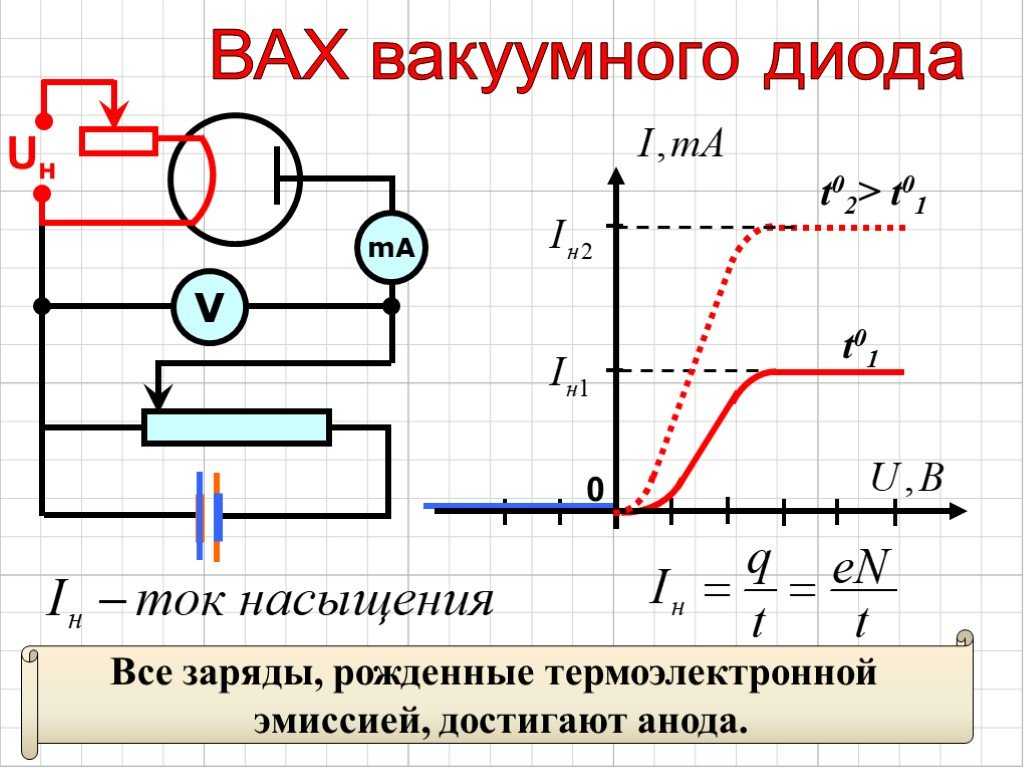
При малом напряжении сила тока мала, т. При определенном значении напряжения U1 все ионы имеют достаточные скорости и, не рекомбинируя, достигают электродов. Ток становится максимально возможным и не зависит от дальнейшего увеличения напряжения до значения U2.
Такой ток называют током насыщения, и ему соответствует участок графика АВ. При напряжении U2 в несколько тысяч вольт скорость электронов, возникающих при ионизации молекул, а следовательно, их кинетическая энергия значительно увеличиваются. Прохождение электрического тока без воздействия внешнего ионизатора называют самостоятельным разрядом. Такая зависимость выражена участком графика АС. В вакууме отсутствуют заряженные частиц, а следовательно, он является диэлектриком. Свободные электроны есть в металлах.
Для преодоления этих сил электрону необходимо затратить определенную энергию, которая называется работой выхода.
Справочник химика 21
Электрический ток в жидкостях обусловлен движением положительных и отрицательных ионов. В отличии от тока в проводниках где движутся электроны. Таким образом, если в жидкости нет ионов, то она является диэлектриком, например дистиллированная вода. Поскольку носителями заряда являются ионы, то есть молекулы и атомы вещества, то при прохождении через такую жидкость электрического тока неизбежно приведет к изменению химических свойств вещества. Вещества делятся на электролиты и неэлектролиты.
Вещества делятся на электролиты и неэлектролиты.
Электрический ток: Классификация, Характеристики, Основные типы Вольтамперная характеристика (зависимость силы тока от напряжения) является Для металлических проводников и электролитов она имеет простейший.
Электрический ток в различных средах. Гальванический элемент. Постоянный электрический ток
Природа электрического тока в растворах и расплавах электролитов. Электролитическая диссоциация. Аррениус г. Одновременно с диссоциацией наблюдается рекомбинация. Интенсивность электролитической диссоциации зависит: 1. От температуры раствора. От концентрации раствора. От рода раствора его диэлектрической проницаемости. Явление электролиза.
Электрический ток в различных средах. Гальванический элемент. Постоянный электрический ток
К электролитам относятся расплавы солей, оксидов или гидроксидов, а также что встречается значительно чаще растворы солей, кислот или оснований в полярных растворителях, например в воде. Прохождение электрического тока через электролит сопровождается выделением веществ на электродах. Это явление получило название электролиза. Электрический ток в электролитах представляет собой перемещение ионов обоих знаков в противоположных направлениях.
Прохождение электрического тока через электролит сопровождается выделением веществ на электродах. Это явление получило название электролиза. Электрический ток в электролитах представляет собой перемещение ионов обоих знаков в противоположных направлениях.
Теория и практика. Кейсы, схемы, примеры и технические решения, обзоры интересных электротехнических новинок.
Вы точно человек?
Отправить комментарий. Закон Ома. Рассмотрим некоторый элемент электрической цепи постоянного тока. Это может быть что угодно: металлический проводник, раствор электролита, лампочка накаливания, газоразрядная трубка. Получим функциональную зависимость.
Электрический ток в жидкостях
Каждый человек, постоянно пользуясь электроприборами, сталкивается с:. Отличительной чертой каждой из перечисленных групп является свойство электропроводности. Что такое проводник. К проводникам относят те вещества, которые имеют в своей структуре большое количество свободных, а не связанных электрических зарядов, способных начинать движение под воздействием приложенной внешней силы. Они могут быть в твердом, жидком или газообразном состоянии.
Они могут быть в твердом, жидком или газообразном состоянии.
В то время как для проводников, подчиняющихся закону Ома (в том числе и для электролитов), вольтамперная характеристика имеет вид наклонной.
Вольтамперная характеристика вакуумного диода.
Мы предполагаем, что вам понравилась эта презентация. Чтобы скачать ее, порекомендуйте, пожалуйста, эту презентацию своим друзьям в любой соц. Кнопочки находятся чуть ниже.
Разделы: Физика. Цели урока: разъяснить физическую природу электропроводности жидких проводников электролитов , закрепить и углубить практические навыки учащихся навыки пользования приборами , расширить научно-технический кругозор. Оборудование: химические стаканы с дистиллированной водой, растворами поваренной соли, сахара, соды, медного купороса. Источники постоянного тока, низковольтные лампы на подставке, амперметры, медные и угольные электроды с держателями, электролитические ванны, соединительные провода, ключи, спиртовки, снег. На предыдущих уроках мы изучали электрический ток в различных средах и выяснили, что у различных проводников природа тока разная.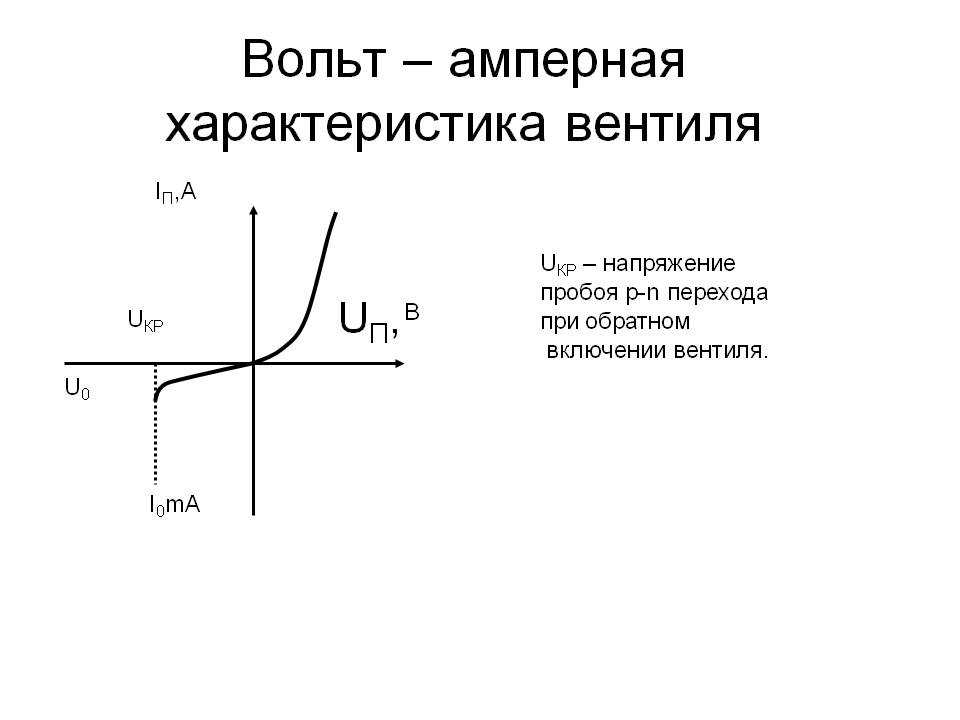
Александров, Т.
Регистрация Вход. Ответы Mail. Вопросы — лидеры Задача по физике 1 ставка. Провод КСПВ, вопрос к электрикам 1 ставка. Мощность рассеивания транзистора? Зачем электродрели нужен редуктор, точнее большая шестеренка? Лидеры категории Антон Владимирович Искусственный Интеллект.
Категория: Физика. Похожие презентации:. Электрический ток в растворах и расплавах электролитов. Электрический ток в жидкостях.
Задание 2. Расчет вольт — амперных характеристик стартерных аккумуляторных батарей.
Рассчитать и построить ВАХ аккумуляторной батареи.
2.1. Рассчитать ВАХ полностью заряженной аккумуляторной батареи для температуры +25оС.
2.2. Рассчитать для этой же АКБ вольт — амперные характеристики с учетом заданной степени разреженности и температуры электролита.
2.3.
Определить по ВАХ напряжение АКБ при
токе 3C20 и токе разряда батареи при напряжении
7,2 В.
Исходные данные:
Таблица 2.1
Тип аккумуляторной батареи | Число положительных пластин | Степень разреженности батареи, % | Температура электролита батареи, оС | ||
6СТ-90 | 6 | 25 | +25 | 0 | -35 |
Значение и коэффициентадля полностью заряженнных АКБ на первой попытке пуска:
Таблица 2.2
Тип аккумуляторной батареи | Ток замыкания при 0 оС, А | Коэффициент | |
от -40 оС до 0 оС | от 0 оС до +40 оС | ||
6СТ-90 | 222 | 4,0 | 1,7 |
Значение коэффициента в зависимости от температуры электролита и степени разреженности батареи:
Таблица
2. 3
3
, % | Коэффициент при температуре электролита,оС | ||
-35 | 0 | +25 | |
25 | 0,35 | 0,56 | 0,86 |
Значение коэффициента при токе разряда 35C20 равно 2,5, считая, что двигатель карбюраторный.
Значение коэффициента в зависимости от температуры электролита при разреженности батареи.
Таблица 2.4
Температура электролита, оС | -35 | 0 |
коэффициент , А/с | 0,3 | 1,2 |
Число
10-секундных попыток запуска принимаем
равным
. Продолжительность попытки пуска.
Продолжительность попытки пуска.
Рис. 5. ВАХ аккумуляторной батареи.
Значение условного начального разрядного напряжения может быть найдено по формуле:
При температуре +25оС:
При температуре 0оС:
При температуре -35оС:
Определяем условный ток короткого замыкания, приходящийся на один положительный электрод (пластину):
При температуре +25оС:
При температуре 0оС:
При температуре -35оС:
Условный ток короткого замыкания батареи:
При температуре +25оС:
При температуре 0оС:
При температуре -35оС:
Определим внутреннее сопротивление батареи:
При температуре +25оС:
При температуре 0оС:
При температуре -35оС
Определим максимальную полезную мощность:
При температуре +25оС:
При температуре 0оС:
При температуре -35оС:
Рис. 3. ВАХ аккумуляторной батареи.
3. ВАХ аккумуляторной батареи.
Напряжение АКБ при токе 3C20 и токе разряда батареи при напряжении 7,2В.
Таблица 2.5
Температура | -35оС | 0оС | +25оС |
При | 9,11В | 10,099 В | 10,269 В |
При | 391,5 А | 1024 А | 1236 А |
Пересчитать электромеханические характеристики стартера на новую ВАХ аккумуляторной батареи. Исходные данные в таблице 4.1 — 4.6.
4. 1.
Построить ВАХ U(I)
и U`(I).
Соединить точку UCТ с началом координат прямой UТ.
Найти ток I`СТ.
1.
Построить ВАХ U(I)
и U`(I).
Соединить точку UCТ с началом координат прямой UТ.
Найти ток I`СТ.
4.2. Построить зависимости n(I) и M(I).
4.3. Участок оси тока от IСХ до I`СТ разбить на интервалы, для каждого значения тока определить значение противо — ЭДС стартера E и E`. Полученные данные занести в таблицу.
4.4. Рассчитать частоту вращения вала стартера для новой ВАХ.
4.5. Рассчитать мощность стартера для двух ВАХ.
4.6. Результаты расчета занести в таблицу и построить на графике кривые n`(I), P(I) и P`(I).
4.7.
Найти значение максимальной мощности
стартера для двух ВАХ и рассчитать для
этих режимов следующие соотношения:
P`max/PCH;
M`max/MCH;
n`max/nCH;
I`max/ICH;
U`max/UCX,
а также UCH/UH;
U`max/UH. Данные расчета занести в таблицу и дать
заключение о результатах проведенных
расчетов.
Данные расчета занести в таблицу и дать
заключение о результатах проведенных
расчетов.
4.8. На графике нанести оси координат для оценки полученных результатов в системе.
Исходные данные:
таблица 4.1
Тип стартера | Тип АКБ | Исходные данные по ВАХ | ||||||
номинальной | новой* | |||||||
UHP | UCT | ICT | τ`Б | U`HP | U`CT | |||
СТ-221 | 6СТ-90 | 12,35 | 8,3 | 520 | -20 | 11,96 | 5,8 | |
Характеристика n(I) и M(I) стартера СТ-221
Таблица
4. 2
2
I, А | 25 | 100 | 150 | 200 | 250 | 300 | 350 | 400 | 450 | 520 |
n | 6500 | 3360 | 2450 | 1750 | 1300 | 900 | 640 | 400 | 200 | 0 |
M | 0 | 1,9 | 4 | 6,7 | 9,4 | 12,5 | 15,8 | 19 | 22,2 | 25,6 |
Строим
ВАХ U(I)
и U`(I). Соединяем точку UCТ с началом координат прямой UТ.
Получаем ток I`СТ. =
340 А.
Соединяем точку UCТ с началом координат прямой UТ.
Получаем ток I`СТ. =
340 А.
Строим зависимости n(I) и M(I).
Участок оси тока от IСХ до I`СТ. разбиваем на интервалы, для каждого значения тока определяем значение противо — ЭДС стартера E и E`. Полученные данные заносим в таблицу 4.3.
таблица 4.3
I, А | 50 | 79 | 108 | 137 | 166 | 195 | 224 | 253 | 282 | 311 | 340 |
E | 11,1 | 10,4 | 9,6 | 8,8 | 8,2 | 7,6 | 6,9 | 6,1 | 5,2 | 4,7 | 4 |
E` | 10,1 | 9,4 | 8,1 | 7 | 6,2 | 5,2 | 4 | 3,2 | 2,1 | 1,3 | 0 |
Рассчитываем частоту вращения вала для новой ВАХ по формуле:
Полученные
значения занесем в таблицу 4.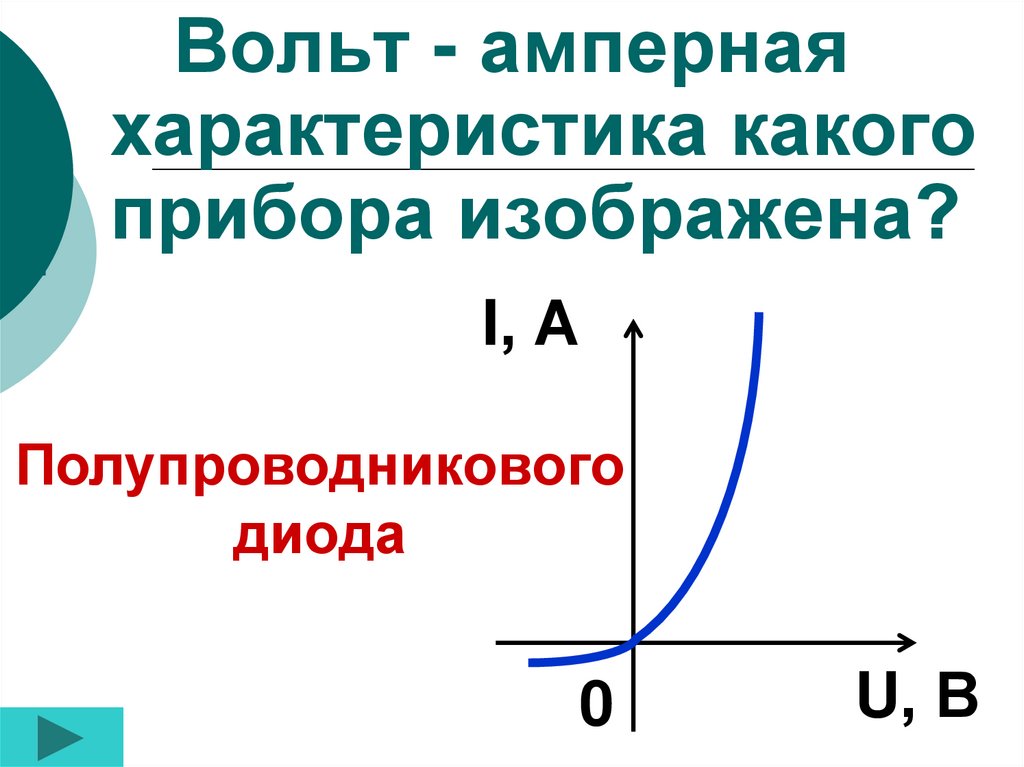 4.
4.
таблица 4.4
I, А | 50 | 79 | 108 | 137 | 166 | 195 | 224 | 253 | 282 | 311 | 340 |
n’ | 5914 | 3254 | 2784 | 2108 | 1701 | 1232 | 841 | 687 | 404 | 246 | 0 |
Рассчитываем мощность стартера для двух ВАХ, по формуле:
Полученные
значения занесем в таблицу 4. 5.
5.
I, А | 50 | 79 | 108 | 137 | 166 | 195 | 224 | 253 | 282 | 311 | 340 |
P | 11,1 | 10,4 | 9,6 | 8,8 | 8,2 | 7,6 | 6,9 | 6,1 | 5,2 | 4,7 | 4 |
P` | 10,1 | 9,4 | 8,1 | 7 | 6,2 | 5,2 | 4 | 3,2 | 2,1 | 1,3 | 0 |
таблица
4. 5
5
Строим кривые n`, Р и Р`.
По графику находим значение максимальной мощности стартера для двух ВАХ: PCH=1,28 кВт, P`max=0,9 кВт.
Рис. 4. Характеристика стартера на новой ВАХ.
Типы, назначение и нормальные уровни
Обзор
Что такое электролиты?
Электролиты представляют собой вещества, обладающие природным положительным или отрицательным электрическим зарядом при растворении в воде. Тело взрослого человека примерно на 60% состоит из воды, а это означает, что почти каждая жидкость и каждая клетка вашего тела содержат электролиты. Они помогают вашему телу регулировать химические реакции, поддерживать баланс между жидкостями внутри и снаружи ваших клеток и многое другое.
Ваш организм получает электролиты или их компоненты из того, что вы едите и пьете. Ваши почки фильтруют избыточные электролиты из вашего тела и попадают в мочу. Вы также теряете электролиты, когда потеете.
Ключевые термины, которые необходимо знать:
- Гипер-: Состояние, начинающееся с «гипер», означает, что оно включает в себя слишком много чего-то.
- Гипо-: Состояние, начинающееся с «гипо», означает, что в нем участвует слишком мало чего-то.
- Ион: Атом, имеющий электрический заряд.
- Катионы: Ионы с положительным зарядом.
- Анионы: Ионы с отрицательным зарядом.
- рН: Шкала, которая измеряет, является ли жидкость кислотой или основанием. Естественный рН крови вашего тела составляет от 7,36 до 7,44.
- Кислотный: имеет pH менее 7.
- Нейтральный: имеет рН 7.
- Основной: имеет рН более 7 (основной также известен как «щелочной»).
Что делают электролиты?
Ваши клетки используют электролиты для проведения электрических зарядов, благодаря которым ваши мышцы сокращаются. Те же электрические заряды также помогают в химических реакциях, особенно когда речь идет о гидратации и балансе жидкостей внутри и снаружи клеток.
Ключевой принцип, на котором основаны электролиты, заключается в том, что определенные химические элементы могут естественным образом удерживать положительный или отрицательный электрический заряд. Когда эти элементы растворяются в жидкости, эта жидкость может проводить электричество.
Примером этого является соленая вода, которая легко проводит электричество. Соль состоит из натрия (положительно заряженного) и хлора (отрицательно заряженного), и при объединении их заряды уравновешивают друг друга. Атомы с электрическим зарядом называются ионами (положительные ионы называются катионами, а отрицательные ионы называются анионами).
Растворение соли в воде приводит к расщеплению атомов натрия и хлора, что означает, что они снова становятся положительно и отрицательно заряженными. Электричество скачет между ионами натрия и хлора, а не между молекулами воды, потому что они имеют противоположные электрические заряды.
На самом базовом химическом уровне электролиты помогают вашему телу поддерживать баланс.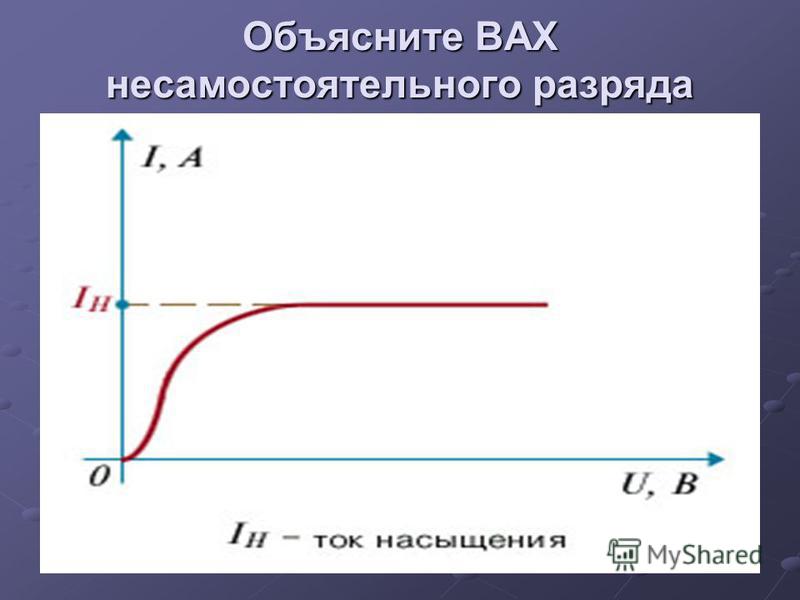 Точно так же, как электричество использует ионы для перемещения с места на место в соленой воде, ваше тело использует ионы для транспортировки химических соединений в клетки и из них.
Точно так же, как электричество использует ионы для перемещения с места на место в соленой воде, ваше тело использует ионы для транспортировки химических соединений в клетки и из них.
Каковы основные компоненты электролита?
Есть несколько ключевых элементов, которые необходимы вашему организму для поддержания нормального уровня электролитов. Следующий раздел включает в себя основные элементы, отмеченные как положительные (+) или отрицательные (-), и что происходит, когда этого элемента слишком много или слишком мало.
Натрий (+)
Натрий играет решающую роль, помогая вашим клеткам поддерживать правильный баланс жидкости. Он также используется, чтобы помочь клеткам поглощать питательные вещества. Это самый распространенный ион электролита в организме.
- Гипернатриемия (слишком много натрия): может вызвать спутанность сознания или изменение поведения, необычно сильные рефлексы и потерю мышечного контроля, судороги и кому.
- Гипонатриемия (недостаток натрия): спутанность сознания, раздражительность, ослабление рефлексов, тошнота и рвота, судороги и кома.

Магний (+)
Магний помогает клеткам превращать питательные вещества в энергию. Ваш мозг и мышцы в значительной степени зависят от магния, чтобы выполнять свою работу.
- Гипермагниемия (слишком много магния): изменения сердечного ритма и аритмии, ослабление рефлексов, снижение способности дышать и остановка сердца (остановка сердца).
- Гипомагниемия (недостаток магния): мышечная слабость, подергивания и потеря контроля, сердечные аритмии. Обычно это происходит в связи с дефицитом кальция и калия.
Калий (+)
Ваши клетки используют калий наряду с натрием. Когда ион натрия входит в клетку, ион калия выходит, и наоборот. Калий также особенно важен для работы сердца. Слишком много или слишком мало может вызвать серьезные проблемы с сердцем.
- Гиперкалиемия (слишком много калия): слабость, неспособность двигаться мышцами, спутанность сознания, нарушение сердечного ритма (аритмии).
- Гипокалиемия (недостаток калия): мышечная слабость и судороги, чувство необычной жажды и частая потребность в мочеиспускании, головокружение или потеря сознания при слишком быстром вставании.
 При более высоких уровнях мышечная ткань начинает разрушаться (состояние, называемое рабдомиолизом, которое может серьезно повредить ваши почки), и сердечные аритмии становятся серьезной угрозой.
При более высоких уровнях мышечная ткань начинает разрушаться (состояние, называемое рабдомиолизом, которое может серьезно повредить ваши почки), и сердечные аритмии становятся серьезной угрозой.
Кальций (+)
Кальций является ключевым элементом в организме, но он делает больше, чем просто укрепляет кости и зубы. Он также используется для управления мышцами, передачи сигналов по нервам, управления сердечным ритмом и многого другого. Слишком много или слишком мало кальция в крови может вызвать широкий спектр симптомов в различных системах организма.
Гиперкальциемия (слишком много кальция)- Головной мозг: Головная боль, усталость, апатия и спутанность сознания.
- Пищеварительный тракт: запор, боль в животе и рвота.
- Почки: частые позывы к мочеиспусканию, камни в почках и почечная недостаточность.
- Сердце: аритмии, некоторые из которых могут быть тяжелыми.
- Скелет: Боль в костях и суставах.

- Мозг: спутанность сознания и изменения поведения.
- Мышцы: необычно сильные рефлексы и потеря мышечного контроля, подергивание мышц, спазмы мышц горла, затрудняющие речь или дыхание.
Хлорид (-)
Хлор (название иона хлора) является вторым по распространенности ионом в организме. Это также ключевая часть того, как ваши клетки поддерживают внутренний и внешний баланс жидкости. Он также играет роль в поддержании естественного баланса рН организма.
Гиперхлоремия (слишком много хлоридов)
Это может вызвать ацидоз, когда кислотность вашей крови слишком высока. Это приводит к тошноте, рвоте и усталости, а также к учащенному и глубокому дыханию и спутанности сознания. Обычно это происходит в связи с избытком или недостатком калия.
- В связи с гиперкалиемией: При слишком большом количестве калия это может вызвать серьезные проблемы с почками или почечную недостаточность.

- В связи с гипокалиемией: в сочетании со слишком низким содержанием калия может вызвать диарею, утечку жидкости из поджелудочной железы и другие серьезные проблемы с мочевыводящими путями.
Гипохлоремия (недостаток хлорида)
- Это приводит к тому, что ваша кровь становится более щелочной, состояние, называемое алкалозом. Обычно это происходит при гипонатриемии или рвоте. Симптомами алкалоза являются апатия, спутанность сознания, аритмии и мышечные подергивания или потеря контроля.
Фосфат (-)
Фосфат — это молекула на основе фосфора, которая играет ключевую роль в транспортировке химических соединений и молекул за пределы ваших клеток. Он помогает вашим клеткам усваивать питательные вещества, а также является ключевой частью молекул, называемых нуклеотидами, которые являются строительными блоками, составляющими вашу ДНК.
- Гиперфосфатемия (слишком много фосфатов): Обычно это вызывает у вас гипокальциемию, потому что ваше тело пытается использовать кальций в качестве заменителя фосфора.
 Обычно это не вызывает симптомов, пока не становится тяжелым, и при этом также часто возникают симптомы гипокальциемии. Это также может быть связано с чрезмерным зудом.
Обычно это не вызывает симптомов, пока не становится тяжелым, и при этом также часто возникают симптомы гипокальциемии. Это также может быть связано с чрезмерным зудом. - Гипофосфатемия (недостаток фосфатов): ранним симптомом этого состояния обычно является мышечная слабость. По мере ухудшения состояния появляются более серьезные симптомы. К ним относятся рабдомиолиз (распад мышечной ткани, который может вызвать серьезное повреждение почек), судороги, снижение функции сердца и проблемы с дыханием (вызванные мышечной слабостью).
Бикарбонат (-)
Не весь углекислый газ, который вырабатывает ваше тело, попадает в ваши легкие, чтобы вы его выдыхали. Вместо этого некоторые из них перерабатываются в бикарбонат, который ваш организм использует для поддержания нормального уровня pH крови.
- Ацидоз. Слишком малое количество бикарбоната вызывает ацидоз, когда ваша кровь слишком кислая. Это вызывает усталость, тошноту и рвоту, и вы будете дышать быстрее и глубже.
 Это также может вызвать путаницу.
Это также может вызвать путаницу. - Алкалоз. Слишком много бикарбоната вызывает алкалоз, когда ваша кровь становится слишком щелочной. Симптомы включают спутанность сознания, апатию, аритмии и подергивания мышц.
Детали теста
Какие тесты помогают выявить проблемы с электролитом?
Проблемы с электролитом можно обнаружить с помощью нескольких различных видов лабораторных тестов. Тестирование обычно включает в себя более широкий тип теста, называемый метаболической панелью. Если эти результаты не соответствуют норме, ваш лечащий врач может назначить дополнительные тесты, которые могут сузить круг причин электролитного дисбаланса. Эти последующие тесты имеют решающее значение, поскольку конкретная причина дисбаланса электролитов может потребовать определенного типа лечения, которое не будет работать для других причин.
Более широкие тесты, которые могут выявить проблемы с электролитами, включают следующие анализы крови:
Базовая метаболическая панель
Этот тест рассматривает несколько различных процессов в вашем организме и показывает данные, связанные с:
- АМК (азот мочевины крови).
 Это тест, который показывает, насколько хорошо функционируют ваши почки, и может указывать на обезвоживание.
Это тест, который показывает, насколько хорошо функционируют ваши почки, и может указывать на обезвоживание. - Баланс жидкостей и некоторых электролитов, включая уровни натрия, калия, углекислого газа и хлоридов.
- Сахар в крови. Этот тест может указывать на диабет или преддиабет, если вы голодаете.
Полная метаболическая панель
Этот тест аналогичен базовой метаболической панели, но с дополнительными данными. Дополнительные собранные предметы включают:
- Уровни кальция.
- Альбумин (белок, вырабатываемый вашей печенью).
- Общий уровень белка в крови.
- Билирубин (химическое соединение, образующееся в печени).
- Уровни аспартатаминотрансферазы (АСТ) и аланинаминотрансферазы (АЛТ), ферментов, которые связаны с функцией вашей печени.
Панель электролитов
Это более широкий тест, как и вышеупомянутые панели метаболизма, но он ищет только электролиты. Анализируемые электролиты включают натрий, хлорид, калий и бикарбонат.
Анализы, более специфичные для проблем с электролитами, включают:
- Анализ крови на альдостерон. Этот тест ищет определенный гормон, вырабатываемый вашими почками. Результаты могут указывать на определенные типы проблем с электролитом.
- Суточный анализ мочи на альдостерон. Этот тест также ищет альдостерон, но использует несколько образцов мочи, собранных в течение 24 часов.
- Анализ крови на анионный разрыв. Тест сравнивает уровни конкретных электролитов, чтобы увидеть, есть ли разница между измеренными уровнями электролитов с положительным и отрицательным зарядом, что может быть признаком определенных состояний.
- Анализ на антидиуретический гормон (кровь). Этот тест определяет уровень антидиуретического гормона. Это может помочь исключить определенные заболевания, которые имеют общие симптомы — особенно чрезмерную жажду или дисбаланс жидкости — с состояниями, связанными с электролитами.

- Анализ крови на углекислый газ. Этот тест измеряет количество углекислого газа в крови. Этот уровень может указывать на то, является ли ваша кровь слишком кислой или слишком щелочной (основной).
- Анализ крови на хлориды. Этот тест анализирует образец крови на уровень хлорида, обнаруженного в вашей крови.
- Анализ мочи на хлориды. Этот тест измеряет количество хлоридов в образце мочи. В некоторых случаях это может включать в себя несколько образцов, взятых в течение 24 часов.
- Анализ крови на магний. Этот тест анализирует уровень магния в крови.
- Анализ осмоляльности крови. Этот тест измеряет количество определенных веществ в организме. Он часто используется в тех случаях, когда вы обезвожены, гипергидратированы или когда отравление возможно или подозревается.
- Анализ осмоляльности мочи. Этот тест проверяет баланс жидкости, особенно при изменении частоты мочеиспускания.
 В тестах на осмоляльность мочи используется метод «чистого улова», который требует получения образца таким образом, чтобы не было заражения микробами, которые могут быть на ваших гениталиях.
В тестах на осмоляльность мочи используется метод «чистого улова», который требует получения образца таким образом, чтобы не было заражения микробами, которые могут быть на ваших гениталиях. - Анализ крови на фосфор. Этот тест измеряет количество фосфора в крови.
- Анализ мочи на фосфор. Этот тест измеряет количество фосфора в моче. Это может включать более одного образца, взятого в течение 24-часового периода.
- Анализ крови на содержание натрия. Этот тест измеряет уровень натрия в крови.
- Анализ мочи на содержание натрия. Этот тест измеряет количество натрия в моче. Он может включать в себя несколько образцов, собранных в течение 24 часов.
- Анализ концентрации мочи. Этот тест показывает поставщикам медицинских услуг, насколько хорошо функционируют ваши почки, особенно их способность управлять количеством жидкости в организме. Он специально ищет концентрацию частиц в моче, уровень электролитов и концентрацию частиц (осмоляльность).

Результаты и последующие действия
Какие результаты я получу?
Большинство лабораторных результатов включают ваш номер результата и контрольный диапазон. Референтный диапазон имеет верхний и нижний пределы, и любой результат, находящийся между ними, считается «нормальным» результатом. Большинство этих результатов сообщается как «сколько вещества можно найти в образце определенного размера».
Масса — это единица измерения «сколько». Это не то же самое, что вес. В качестве единиц массы используются миллимоли, миллиэквиваленты или миллиграммы.
- Миллимоли являются наиболее постоянными и могут использоваться для всех атомов и молекул электролита.
- Миллиэквиваленты на литр часто используются вместо миллимолей. Это связано с тем, что миллиэквиваленты учитывают силу заряда иона, поэтому ионы с более сильным зарядом имеют разные количества, чем те же результаты испытаний в миллимолях.
- Миллиграммы на децилитр иногда могут использоваться для более крупных атомов и молекул.

Приставка «милли-» означает «1/1000». Единицы объема обычно отображаются как литр или доли литра, например децилитр (дл, что составляет 1/10 литра) или миллилитр (мл, что составляет 1/1000 литра). нормальные уровни электролитов
В крови нормальные количества электролитов следующие:0278
Meq/L)
(мг/дл)
(ммоль/л)
Калий
· Сыворотка (плазма)
· Цельная кровь
3,7–5,1 мэкв/л
3,5–5 мэкв/л
—
3,7–5,1 ммоль/л
3,5–5 ммоль/л
Кальций
· Всего
· Ионизированный
—
2,16 — 2,60 мэкв/л
8,5–10,2 мг/дл
2,12–2,54 ммоль/л
1,08–1,30 ммоль/л
Магний
· Сыворотка (плазма)
· Эритроциты
· Анализ газов крови
1,4–1,9 мэкв/л
3,3–5,34 мэкв/л
0,86–1,32 мэкв/л
1,7–2,3 мг/дл
4,0–6,5 мг/дл
1,04–1,6 мг/дл
0,7–0,95 ммоль/л
1,65–2,67 ммоль/л
0,43 — 0,66 ммоль/л
 Следует:
Следует:| Электролит | миллиграммы на децилитр (мг/дл) | миллимол на литр (ммоль/л) | — | 14 — 216 ммоль/л |
|---|---|---|
Калий · Моча (случайная) | — | 10–160 ммоль/л |
Хлорид · Моча (случайная) | — | 16–250 ммоль/л |
| Бикарбонат | — | Н/Д |
Кальций · Моча (случайная) | 0,0–21,0 мг/дл | — |
Магний · Моча (случайно) | 23,2 мг/дл или менее | — |
Фосфат · Моча (случайная) | 7 — 140 мг/дл | — |
Нормальный результат означает, что все в порядке, или ненормальный результат всегда означает, что у меня проблема?
Поскольку все люди разные, иногда вы можете получить результат, выходящий за пределы референсного диапазона. В других случаях у вас может быть нормальный результат, но симптомы, которые у вас есть, и результаты других анализов покажут, что у вас проблемы со здоровьем.
В других случаях у вас может быть нормальный результат, но симптомы, которые у вас есть, и результаты других анализов покажут, что у вас проблемы со здоровьем.
Один из способов понять это — вспомнить карнавальный трюк, когда артист крутит тарелку на конце деревянной палочки. Если тарелка наклонится слишком далеко в любом направлении, она упадет, поэтому баланс имеет решающее значение. Ваш уровень электролитов и результаты лабораторных анализов основаны на подобном уравновешивании, и ваше тело всегда пытается сохранить равновесие, насколько это возможно. Ваше тело может маскировать проблему, компенсируя ее другой системой или процессом. Если ваш поставщик медицинских услуг проводит более одного теста, они, вероятно, следят за тем, чтобы ваше тело не скрывало одну проблему, создавая другую.
Когда я должен узнать результаты теста?
Ваш лечащий врач или его персонал могут сообщить вам, когда ожидать результаты анализов.
Когда мне следует позвонить своему врачу?
Если вы не понимаете результаты своего теста или ваш результат выходит за пределы референтного диапазона, и у вас есть вопросы или опасения, вам следует позвонить своему поставщику медицинских услуг. Вам также следует позвонить своему лечащему врачу, если вы заметили внезапное изменение каких-либо симптомов, связанных с каким-либо тестом на уровень электролитов.
Вам также следует позвонить своему лечащему врачу, если вы заметили внезапное изменение каких-либо симптомов, связанных с каким-либо тестом на уровень электролитов.
Записка из клиники Кливленда
Электролиты являются неотъемлемой частью функционирования вашего тела, влияя на все, от гидратации до того, как бьется ваше сердце. Они также могут помочь врачам диагностировать широкий спектр заболеваний и проблем. Понимание электролитов и потенциальных проблем, которые их окружают, может помочь вам позаботиться о себе и избежать проблем со здоровьем в будущем. Таким образом, вы можете взять на себя ответственность за свои электролиты и не допустить их негативного влияния на вашу жизнь и распорядок дня.
5 советов начинающим йогам
Итак, вы решили попробовать занятия йогой. Поздравляем… вы стали на один шаг ближе к тому, чтобы сделать что-то великое для себя! Первое занятие йогой может быть очень пугающим, и мы хотим, чтобы вы получили наилучшие впечатления, поэтому вот 5 советов для начинающих:
Постарайтесь успокоить своего внутреннего критика
Вопрос/проблема, которую мы часто получаем в Mountain Yoga люди беспокоятся о том, что другие думают о том, как они выглядят на практике в качестве новичка. Прежде всего, это не то, за чем мы приходим в йогу. Знайте, что большинство людей в классе сосредоточены на себе и просто пытаются выжить в классе… как и вы! От этого страха осуждения можно отказаться в йоге, когда мы поймем, что йога-студия — одно из самых безопасных мест, где можно находиться и выражать себя. Пути у всех разные, и мы здесь, чтобы поддержать вас на любом уровне, на котором вы находитесь.
Прежде всего, это не то, за чем мы приходим в йогу. Знайте, что большинство людей в классе сосредоточены на себе и просто пытаются выжить в классе… как и вы! От этого страха осуждения можно отказаться в йоге, когда мы поймем, что йога-студия — одно из самых безопасных мест, где можно находиться и выражать себя. Пути у всех разные, и мы здесь, чтобы поддержать вас на любом уровне, на котором вы находитесь.
Вам не нужно выполнять каждую асану (позу)
Знайте, что вам не нужно делать все, что говорит инструктор. Они являются ориентиром, но это ваша практика, и поскольку все люди разные по способностям и анатомии, мы рекомендуем вам изменить столько, сколько необходимо, даже если это означает, что весь класс будет принимать позу ребенка. Не бойтесь спрашивать учителя после занятий, если у вас есть вопросы о конкретных позах или дыхательных упражнениях!
Правильная подготовка решает все
В нашей Большой Комнате Коттонвуд жарко, и вы вспотеете. Правильная подготовка изменит весь ваш опыт.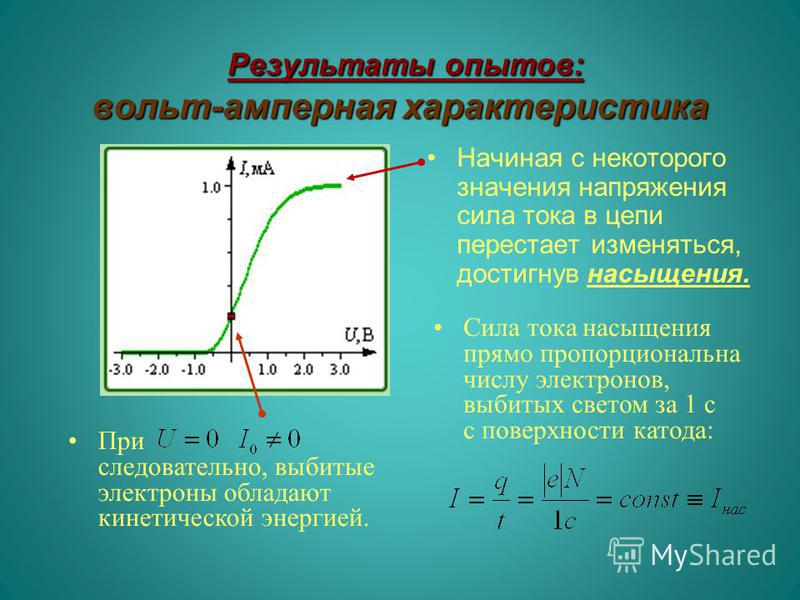 Это начинается с питания и увлажнения. В идеале не следует приходить на занятия слишком полными или слишком пустыми, если в вашей практике нет поста. Увлажнение в тренировочные дни с дополнительными добавками электролита (попробуйте в следующий раз ягоды и розовую гималайскую соль в воду, или мы продаем другие добавки электролита!). Принесите необходимое снаряжение на занятия. Повязки на голову и полотенца для лица отлично подходят для защиты глаз от пота, который может повлиять на ваше равновесие и комфорт в классе. Полотенце для коврика поможет вам не поскользнуться и не потерять равновесие. Мы предоставляем блоки и ремни в студии.
Это начинается с питания и увлажнения. В идеале не следует приходить на занятия слишком полными или слишком пустыми, если в вашей практике нет поста. Увлажнение в тренировочные дни с дополнительными добавками электролита (попробуйте в следующий раз ягоды и розовую гималайскую соль в воду, или мы продаем другие добавки электролита!). Принесите необходимое снаряжение на занятия. Повязки на голову и полотенца для лица отлично подходят для защиты глаз от пота, который может повлиять на ваше равновесие и комфорт в классе. Полотенце для коврика поможет вам не поскользнуться и не потерять равновесие. Мы предоставляем блоки и ремни в студии.
Приходить пораньше
Дайте себе время освоиться в студии, найти место в комнате и встретиться с инструктором. Рекомендуем приходить на 15-20 минут раньше. Кроме того, пожалуйста, запланируйте остаться на весь класс. Поза последнего отдыха, Шавасана (произносится как ша-ВАХ-сух-нух или са-ВАХ-сух-нух), широко известна как самая важная поза в йоге, и именно в ней ваше тело впитывает преимущества всей вашей практики йоги.
Попробуйте разные занятия
Мы хотим, чтобы вы попробовали и испытали все, что может предложить Горная йога. Наш класс «Земля» — отличный класс горячей йоги для всех начинающих, так как класс будет двигаться медленнее и предлагать больше инструкций, но доступен для всех типов телосложения. Если вы ищете что-то не отапливаемое, мы предлагаем различные занятия в нашей комнате Little Cottonwood. Помните, что в дополнение к различным классам, каждый из наших учителей йоги имеет свою индивидуальность, которая сияет на их занятиях!
Есть еще вопросы или проблемы? Ознакомьтесь с нашими часто задаваемыми вопросами на странице часто задаваемых вопросов для новых участников или отправьте нам письмо по электронной почте!
Все в студии любят говорить о йоге, поэтому спросите у них, что лучше всего подходит для них, и соберите все, что сможете, для своей практики! Мы сообщество, и мы хотим помочь вам добиться успеха.
Спасибо, что тренируетесь с нами!
Подробнее читайте здесь.



 Гальванический элемент. Постоянный электрический ток
Гальванический элемент. Постоянный электрический ток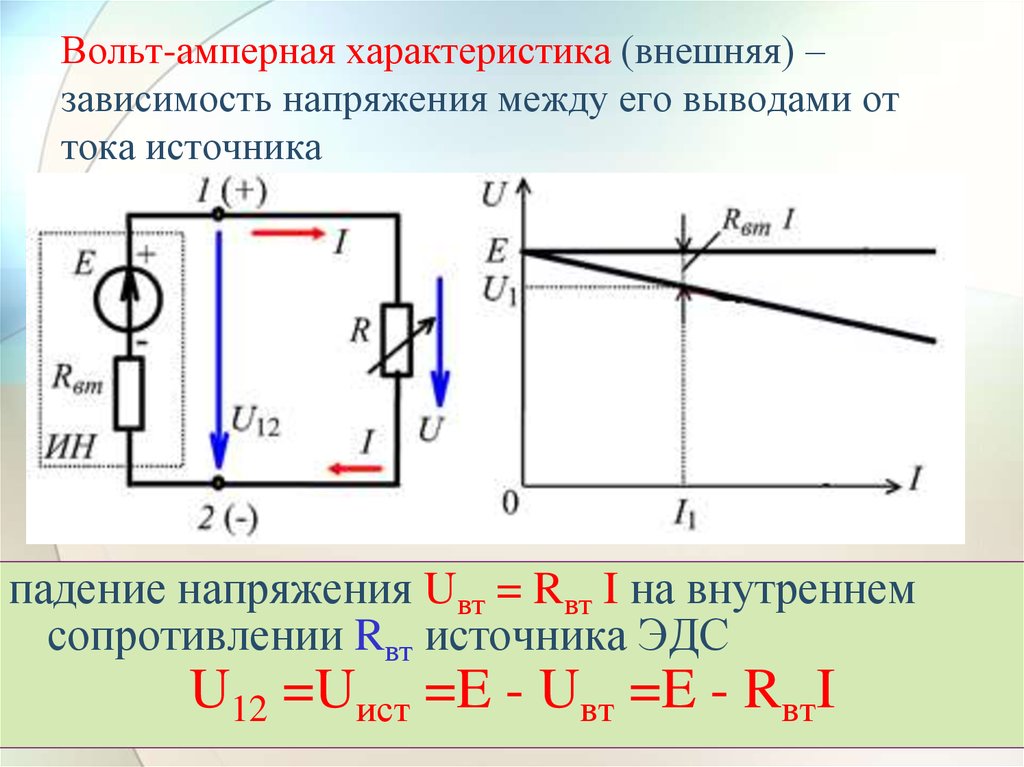
 При более высоких уровнях мышечная ткань начинает разрушаться (состояние, называемое рабдомиолизом, которое может серьезно повредить ваши почки), и сердечные аритмии становятся серьезной угрозой.
При более высоких уровнях мышечная ткань начинает разрушаться (состояние, называемое рабдомиолизом, которое может серьезно повредить ваши почки), и сердечные аритмии становятся серьезной угрозой.
 Обычно это не вызывает симптомов, пока не становится тяжелым, и при этом также часто возникают симптомы гипокальциемии. Это также может быть связано с чрезмерным зудом.
Обычно это не вызывает симптомов, пока не становится тяжелым, и при этом также часто возникают симптомы гипокальциемии. Это также может быть связано с чрезмерным зудом. Это также может вызвать путаницу.
Это также может вызвать путаницу. Это тест, который показывает, насколько хорошо функционируют ваши почки, и может указывать на обезвоживание.
Это тест, который показывает, насколько хорошо функционируют ваши почки, и может указывать на обезвоживание.
 В тестах на осмоляльность мочи используется метод «чистого улова», который требует получения образца таким образом, чтобы не было заражения микробами, которые могут быть на ваших гениталиях.
В тестах на осмоляльность мочи используется метод «чистого улова», который требует получения образца таким образом, чтобы не было заражения микробами, которые могут быть на ваших гениталиях.