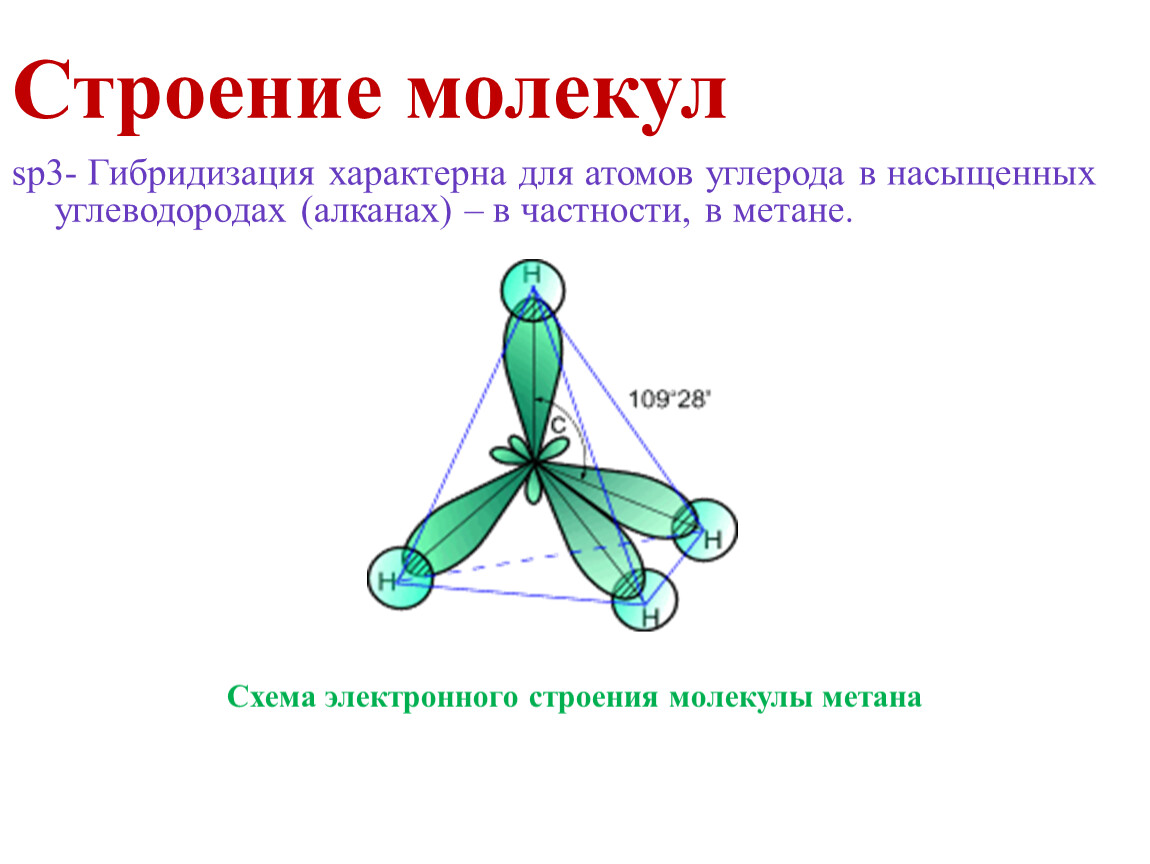
Строение молекул. Химическая связь
Молекула — электрически нейтральная частица, образованная из двух или более связанных ковалентными связями атомов.
Химическая связь — это взаимодействие атомов, обуславливающее устойчивость молекулы или кристалла как целого.
Химическая связь может образовываться путем предоставления от каждого из атомов по одному или нескольким неспаренным электронам (кратные связи) с образованием электронных пар (ковалентная связь). В образовании химической связи участвуют только электроны внешней электронной оболочки, а внутренние электронные уровни не затрагиваются. В результате, при образовании химической связи у каждого атома образуется заполненная электронная оболочка внешнего электронного уровня, состоящая из двух (дуплет) или восьми (октет) электронов.
Химическая связь характеризуется длиной и энергией. Длина химической связи это расстояние между ядрами связанных атомов. Энергия химической связи показывает сколько необходимо затратить энергии на разведение двух атомов, между которыми существует химическая связь, на расстояние, при котором эта химическая связь будет разорвана.
Виды химической связи
Ионная химическая связь
Ионная связь — очень прочная химическая связь, образующаяся между атомами с большой разностьюэлектроотрицательностей, при которой общая электронная пара переходит преимущественно к атому с большей электроотрицательностью.
Результатом этого является образование соединения противоположно заряженных ионов:
Это притяжение ионов как разноимённо заряженных тел. Ионная связь — крайний случай поляризации ковалентной полярной связи.
Образуется между типичными металлом и неметаллом (Me + неМе).
При этом электроны у металла полностью переходят к неметаллу, образуются ионы (частицы, имеющие заряд).
Например, типичные металлы литий (Li), натрий (Na), калий (K), кальций (Ca), стронций (Sr), барий (Ba) образуют ионную связь с типичными неметаллами, в основном с галогенами.
Кроме галогенидов щелочных металлов, ионная связь также образуется в таких соединениях, как щелочи и соли. Например, в гидроксиде натрия (NaOH) и сульфате натрия (Na2SO4) ионные связи существуют только между атомами натрия и кислорода (остальные связи — ковалентные полярные).
Например, в гидроксиде натрия (NaOH) и сульфате натрия (Na2SO4) ионные связи существуют только между атомами натрия и кислорода (остальные связи — ковалентные полярные).
Ковалентная химическая связь
Ковалентная полярная химическая связь образуется при взаимодействии атомов, значение электроотрицательностей которых отличаются, но не резко, происходит смещение общей электронной пары к более электроотрицательному атому.
Электроотрицательность (ЭО) — способность атома химических элемента смещать к себе общие электронные пары, участвующие в образовании химической связи.
Ковалентная полярная связь образуется между разными неметаллами (неМе + неMe).
Это наиболее распространенный тип химической связи, которой встречается как в неорганических, так и органических соединениях.
Такая связь существует в молекулах следующих сложных веществ: Н2О, h3S, Nh4 и др.
К ковалентным связям в полной мере относятся и те связи, которые образованы по донорно-акцепторному механизму, например в ионах гидроксония (Н3О+) и аммония (Nh5+).
Металлическая химическая связь
Связь в металлах и сплавах между атом-ионами посредством обобществленных электронов называется металлической.
Металлическая связь — химическая связь, которая обусловлена взаимодействием положительных ионов металлов, составляющих кристаллическую решётку, с электронным газом из валентных электронов.
Металлическая химическая связь образуется в простых веществах-металлах (Me).
Сущность процесса образования металлической связи состоит в следующем: атомы металлов легко отдают валентные электроны и превращаются в положительные заряженные ионы. Относительно свободные электроны, оторвавшиеся от атома, перемещаются между положительными ионами металлов. Между ними возникает металлическая связь, т.е. электроны как бы цементируют положительные ионы кристаллической решетки металлов.
Металлическая кристаллическая решетка Металлическая связь существует в металлах в твердом в жидком состоянии.
В узлах кристаллической решетки металлов находятся свободные атомы, положительно заряженные ионы, а часть валентных электронов, свободно перемещаясь в объеме кристаллической решетки, образует «электронный газ» , обеспечивающий связь между атомами металла.
Связь, которую осуществляют относительно свободные электроны между ионами металлов в кристаллической решетке, называется металлической связью.
Металлическая связь возникает за счет обобществления атомами валентных электронов. Однако между этими видами связи есть существенное различие. Электроны, осуществляющие ковалентную связь, в основном пребывают в непосредственной близости от двух соединенных атомов.
В случае металлической связи электроны, осуществляющие связь, перемещаются по всему куску металла. Этим определяются общие признаки металлов: металлический блеск, хорошая проводимость теплоты и электричества, ковкость, пластичность и т. д.
Этим определяются общие признаки металлов: металлический блеск, хорошая проводимость теплоты и электричества, ковкость, пластичность и т. д.
Общим химическим свойством металлов является их относительно высокая восстановительная способность.
Обобщение материала
Типы химической связи
Полезные ссылки
Источник материала
Ионная связь и её характеристики (видео)
Ковалентная связь и её характеристики (видео)
Металлическая связь и её характеристики (видео)
Схемы образования веществ с различным типом связи (видео)
Разбор видов связи
Ионная химическая связь (видео)
Ковалентная неполярная химическая связь (видео)
Ковалентная полярная химическая связь (видео)
Металлическая химическая связь (видео)
Дополнительные материалы
Ковалентная и ионная химическая связь (видео)
Металлическая и водородная химические связи (видео)
Ионная связь (видео)
Ковалентная связь (видео)
Ковалентная полярная связь (видео)
Теория Бутлерова: химическое строение органических соединений
Поможем понять и полюбить химию
Начать учиться Теория химического строения органических соединений — основа органической химии. В статье мы познакомимся с основоположником этой теории и изучим ее главные тезисы.
В статье мы познакомимся с основоположником этой теории и изучим ее главные тезисы.
Предпосылки возникновения
В 1860 году состоялся первый Международный съезд химиков в Карлсруэ, где ученые четко обозначили разницу между привычными для нас понятиями атома и молекулы. В это же время утвердили и атомно-молекулярное учение, которое позже легло в основу теории химического строения.
Чуть раньше, в 1853 году, английский химик Эдуард Франкленд ввел понятие «валентность», а спустя пять лет Фридрих Кекуле установил, что валентность углерода в органических соединениях равна четырем. К тому же Кекуле и Купер уже в 1857 году выдвигали предположения о том, что атомы углерода могут образовывать цепочки.
Однако у великих умов еще оставались вопросы. Например, как несколько химических элементов способны образовывать такое многообразие соединений? Или как вещества, имеющие одинаковую исходную формулу, могут иметь разные физические и химические свойства? Вот здесь-то и выдвинул свою теорию химического строения Александр Михайлович Бутлеров.
Практикующий детский психолог Екатерина Мурашова
Бесплатный курс для современных мам и пап от Екатерины Мурашовой. Запишитесь и участвуйте в розыгрыше 8 уроков
А. М. Бутлеров и его идеи
Александр Михайлович Бутлеров — великий русский химик, ученик Н. Н. Зинина, лауреат Ломоносовской премии и создатель теории химического строения органических веществ.
Еще в 1858 году на заседании Парижского химического общества Бутлеров, выступив с первым докладом, внес ясность в определение радикалов. Он утверждал, что радикалами следует считать не только органические группы атомов, но и характерные для различных классов сочетания атомов. Например, —OH или —NH2. Позже такие сочетания атомов получили название функциональных групп. В этом же докладе Александр Михайлович впервые употребил термин «структура».
В более развернутой и доработанной форме Бутлеров представил свою теорию на суд общественности в 1861 году в химической секции Съезда немецких естествоиспытателей и врачей. В его докладе «О химическом строении вещества» говорилось, что теоретическая сторона химии на текущий момент перестала отвечать фактическому развитию химии как науки. В частности, ученый отметил нестыковки в теориях, выдвинутых ранее.
В его докладе «О химическом строении вещества» говорилось, что теоретическая сторона химии на текущий момент перестала отвечать фактическому развитию химии как науки. В частности, ученый отметил нестыковки в теориях, выдвинутых ранее.
Нужно сказать, что сам Бутлеров не формулировал теорию химического строения по пунктам: мысли на этот счет он выдвигал в различных статьях, они же пронизывают все его практические эксперименты.
Основные положения теории Бутлерова
С Бутлеровым мы познакомились, теперь пришло время познакомиться с основными положениями теории химического строения органических веществ:
Атомы в молекулах соединены между собой химическими связями в соответствии с их валентностью.
Важно помнить
Валентность углерода в органических соединениях равна 4.
Атомы в молекулах органических веществ соединены в определенной последовательности, которую характеризует химическое строение молекулы.

Определенная последовательность соединений атомов в молекуле с учетом их валентностей называется химическим строением, которое, в свою очередь, отражают структурные формулы. А последовательное соединение атомов углерода друг с другом, образующее каркас молекулы, называется углеродным скелетом. Но есть одно но: структурные формулы не отражают пространственное расположение молекулы. Вот как можно изобразить строение одной и той же молекулы различными структурными формулами:
Структурные формулы чаще всего изображают в сокращенном виде, например CH3—CH2—CH2—CH3. Однако в сокращенном виде видна только связь «углерод — углерод» и не видны связи «углерод — водород» и «углерод — кислород».
Если в молекуле четыре атома углерода и более, то ее строение может быть не только линейным, но и разветвленным:
Давайте внимательно рассмотрим строение каждой молекулы.
 Атомы углерода одной из молекул связаны с одним или двумя соседними атомами углерода, как, например, в другой молекуле один из атомов углерода связан сразу с тремя атомами углерода. Отсюда можно предположить, что разному порядку связывания атомов при одинаковом количестве атомов углерода и водорода в данном случае должны соответствовать различные вещества с разными свойствами. Действительно, все так и есть:
Атомы углерода одной из молекул связаны с одним или двумя соседними атомами углерода, как, например, в другой молекуле один из атомов углерода связан сразу с тремя атомами углерода. Отсюда можно предположить, что разному порядку связывания атомов при одинаковом количестве атомов углерода и водорода в данном случае должны соответствовать различные вещества с разными свойствами. Действительно, все так и есть:Разницу в температурах кипения при одинаковом количественном и качественном составе подтверждают литературные данные.
Все это приводит нас к такому понятию, как изомеры. Изомерами называют вещества с одинаковым количественным и качественным составом, но с разными физико-химическими свойствами, которые обусловлены различным строением. Явление существования различных форм веществ или изомеров называется

Свойства органических веществ зависят не только от числа и природы входящих в состав атомов, но и от химического строения молекулы. Зная строение вещества, можно охарактеризовать его свойства.
В молекулах существует взаимное влияние как непосредственно связанных, так и не связанных между собой атомов.
Химическое строение вещества можно определить благодаря изучению его химических превращений.
Вопросы для самопроверки
Основоположником теории химического строения является…
Зинин
Ломоносов
Менделеев
Бутлеров
Какова валентность углерода в органических молекулах?
I
V
II
IV
Определенная последовательность соединений атомов в молекуле называется…
Изомерией
Гомологами
Углеродным скелетом
Химической формулой
Способны ли структурные формулы отображать пространственное строение молекулы?
Да
Нет
Это одно и то же
Верно ли утверждение: «Наличие изомеров зависит от общего количества атомов углерода в молекуле»?
Верно
Неверно
Изомеры есть у всех веществ
Можно ли предугадать химические свойства, зная строение молекулы?
Это невозможно
Можно, так как свойства зависят от строения
Только зная свойства, можно рассказать о строении молекулы
Глубже разобраться в положениях и значении теории Бутлерова можно на уроках химии в онлайн-школе Skysmart. Мы учим понимать химические явления на примерах из окружающей ученика реальности, показываем межпредметные связи и помогаем ответить на вопрос «Зачем все это учить?». Оставьте заявку и пройдите бесплатное тестирование, а мы подберем подходящий курс и рекомендации для самостоятельного обучения!
Мы учим понимать химические явления на примерах из окружающей ученика реальности, показываем межпредметные связи и помогаем ответить на вопрос «Зачем все это учить?». Оставьте заявку и пройдите бесплатное тестирование, а мы подберем подходящий курс и рекомендации для самостоятельного обучения!
Ответы на вопросы
d
d
c
b
a
b
Ксения Боброва
К предыдущей статье
Простые и сложные вещества
К следующей статье
Алканы
Получите план обучения, который поможет понять и полюбить химию
На вводном уроке с методистом
Выявим пробелы в знаниях и дадим советы по обучению
Расскажем, как проходят занятия
Подберём курс
Фермент рестрикции | Определение, функция и типы
Библиотека кДНК
Посмотреть все носители
- Ключевые люди:
- Гамильтон О.
 Смит
Вернер Арбер
Смит
Вернер Арбер
- Похожие темы:
- нуклеаза рестрикционный фермент I типа фермент рестрикции IV типа рестрикционный фермент II типа рестрикционный фермент III типа
См. все связанные материалы →
Рестриктазный фермент , также называемый рестриктазой , белок, вырабатываемый бактериями, который расщепляет ДНК в определенных участках молекулы. В бактериальной клетке ферменты рестрикции расщепляют чужеродную ДНК, тем самым уничтожая заражающие организмы. Ферменты рестрикции можно выделить из бактериальных клеток и использовать в лаборатории для манипулирования фрагментами ДНК, например, содержащими гены; по этой причине они являются незаменимыми инструментами технологии рекомбинантной ДНК (генной инженерии).
Бактерия использует фермент рестрикции для защиты от бактериальных вирусов, называемых бактериофагами или фагами. Когда фаг заражает бактерию, он вставляет свою ДНК в бактериальную клетку, чтобы она могла реплицироваться. Рестриктазы предотвращают репликацию ДНК фага, разрезая ее на множество частей. Ферменты рестрикции были названы в честь их способности ограничивать или ограничивать количество штаммов бактериофагов, которые могут инфицировать бактерию.
Рестриктазы предотвращают репликацию ДНК фага, разрезая ее на множество частей. Ферменты рестрикции были названы в честь их способности ограничивать или ограничивать количество штаммов бактериофагов, которые могут инфицировать бактерию.
Каждый рестрикционный фермент распознает короткую специфическую последовательность нуклеотидных оснований (четыре основные химические субъединицы линейной двухцепочечной молекулы ДНК — аденин, цитозин, тимин и гуанин). Эти участки называются последовательностями узнавания или сайтами узнавания и случайным образом распределены по всей ДНК. Различные виды бактерий вырабатывают ферменты рестрикции, которые распознают разные последовательности нуклеотидов.
Когда эндонуклеаза рестрикции распознает последовательность, она разрезает молекулу ДНК, катализируя гидролиз (расщепление химической связи путем добавления молекулы воды) связи между соседними нуклеотидами. Бактерии предотвращают таким образом деградацию собственной ДНК, маскируя свои последовательности распознавания. Ферменты, называемые метилазами, добавляют метильные группы (-CH 3 ) к адениновым или цитозиновым основаниям в последовательности распознавания, которая таким образом модифицируется и защищается от эндонуклеазы. Рестрикционный фермент и соответствующая ему метилаза составляют систему рестрикции-модификации бактериального вида.
Ферменты, называемые метилазами, добавляют метильные группы (-CH 3 ) к адениновым или цитозиновым основаниям в последовательности распознавания, которая таким образом модифицируется и защищается от эндонуклеазы. Рестрикционный фермент и соответствующая ему метилаза составляют систему рестрикции-модификации бактериального вида.
Традиционно выделяют четыре типа рестрикционных ферментов, обозначаемых I, II, III и IV, которые различаются, прежде всего, структурой, сайтом расщепления, специфичностью и кофакторами. Ферменты типа I и III сходны тем, что и рестрикционная, и метилазная активности осуществляются одним большим ферментным комплексом, в отличие от системы типа II, в которой рестрикционный фермент не зависит от своей метилазы. Рестриктазы типа II также отличаются от типов I и III тем, что они расщепляют ДНК в определенных сайтах внутри сайта узнавания; другие расщепляют ДНК случайным образом, иногда на сотни оснований от последовательности распознавания. Несколько тысяч ферментов рестрикции типа II были идентифицированы у различных видов бактерий. Эти ферменты распознают несколько сотен различных последовательностей, обычно длиной от четырех до восьми оснований. Ферменты рестрикции типа IV расщепляют только метилированную ДНК и проявляют слабую специфичность к последовательности.
Эти ферменты распознают несколько сотен различных последовательностей, обычно длиной от четырех до восьми оснований. Ферменты рестрикции типа IV расщепляют только метилированную ДНК и проявляют слабую специфичность к последовательности.
Ферменты рестрикции были открыты и охарактеризованы в конце 1960-х и начале 1970-х годов молекулярными биологами Вернером Арбером, Гамильтоном О. Смитом и Дэниелом Натансом. Способность ферментов разрезать ДНК в определенных местах позволила исследователям изолировать фрагменты, содержащие гены, и рекомбинировать их с другими молекулами ДНК, т. е. клонировать гены. Названия ферментов рестрикции происходят от обозначения рода, вида и штамма бактерий, которые их производят; например, фермент Eco RI продуцируется штаммом RY13 Escherichia coli . Считается, что рестрикционные ферменты произошли от общего предкового белка и эволюционировали, чтобы распознавать определенные последовательности посредством таких процессов, как генетическая рекомбинация и амплификация генов.
Оформите подписку Britannica Premium и получите доступ к эксклюзивному контенту.
Подпишитесь сейчас Редакция Британской энциклопедии Эта статья была недавно отредактирована и обновлена Карой Роджерс.Крупномасштабные представления химического языка фиксируют молекулярную структуру и свойства
Роджерс, Д. и Хан, М. Отпечатки пальцев с расширенными связями. J. Chem. Инф. Модель. 50 , 742–754 (2010).
Артикул Google Scholar
Рупп М., Ткатченко А., Мюллер К.-Р. и Фон Лилиенфельд, О. А. Быстрое и точное моделирование энергий атомизации молекул с помощью машинного обучения. Физ. Преподобный Летт. 108 , 058301 (2012).
Артикул Google Scholar
Weininger, D. SMILES, химический язык и информационная система.
 1. Введение в методологию и правила кодирования. J. Chem. Инф. вычисл. науч. 28 , 31–36 (1988).
1. Введение в методологию и правила кодирования. J. Chem. Инф. вычисл. науч. 28 , 31–36 (1988).Артикул Google Scholar
Goh, G.B., Hodas, N.O., Siegel, C. & Vishnu, A. SMILES2Vec: интерпретируемая глубокая нейронная сеть общего назначения для прогнозирования химических свойств. Препринт на https://arxiv.org/abs/1712.02034 (2017).
Озтюрк, Х., Озгюр, А. и Озкиримли, Э. DeepDTA: предсказание глубокого связывания лекарственного средства с мишенью. Биоинформатика 34 , i821–i829 (2018).
Артикул Google Scholar
Пол, А. и др. CheMixNet: смешанные архитектуры DNN для прогнозирования химических свойств с использованием нескольких молекулярных представлений. Препринт на https://arxiv.org/abs/1811.08283 (2018).
Шин Б.
 , Парк С., Канг К. и Хо Дж. К. Представление молекул на основе самоконтроля для прогнозирования взаимодействия лекарство-мишень. Проц. Мах. Учиться. Рез. 106 , 230–248 (2019).
, Парк С., Канг К. и Хо Дж. К. Представление молекул на основе самоконтроля для прогнозирования взаимодействия лекарство-мишень. Проц. Мах. Учиться. Рез. 106 , 230–248 (2019).Daylight Chemical Information Systems SMARTS — язык для описания молекулярных структур https://www.daylight.com/dayhtml/doc/theory/theory.smiles.html (2007).
Кренн, М., Хасе, Ф., Нигам, А., Фридерих, П. и Аспуру-Гузик, А. Самоссылающиеся встроенные строки (SELFIES): 100% надежное представление молекулярных строк. Маха. Учиться. науч. Технол. 1 , 045024 (2020).
Артикул Google Scholar
Гао, В., Фу, Т., Сан, Дж. и Коли, К.В. Эффективность выборки имеет значение: ориентир для практической молекулярной оптимизации. В Тридцать шестая конференция по наборам данных и контрольным показателям систем обработки нейронной информации Track (2022).

Джо Дж., Квак Б., Чой Х.-С. & Yoon, S. Нейронные сети, передающие сообщения для предсказания химических свойств на SMILES. Методы 179 , 65–72 (2020).
Артикул Google Scholar
Duvenaud, D. et al. Сверточные сети на графах для изучения молекулярных отпечатков пальцев. В NIPS’15: Proc. 28-я Международная конференция по системам обработки нейронной информации Vol. 2 (2015).
Дефферрар, М., Брессон, X. и Вандергейнст, П. Сверточные нейронные сети на графах с быстрой локализованной спектральной фильтрацией. Доп. Нейронная инф. Процесс. Сист. 29 (2016).
Кипф, Т. Н. и Веллинг, М. Полууправляемая классификация с использованием графовых сверточных сетей. В 5-я Международная конференция по обучающим представлениям (OpenReview.net, 2017).

Ли, Ю., Тарлоу, Д., Брокшмидт, М. и Земель, Р. Нейронные сети с последовательностью графов. В 4-я Международная конференция по представлениям обучения (редакторы Bengio, Y. & LeCun, Y.) (OpenReview.net, 2016).
Величкович, П. и др. Графические сети внимания. В Международная конференция по обучению Представления (2018).
Гамильтон, В., Ин, З. и Лесковец, Дж. Обучение индуктивному представлению на больших графах. Доп. Нейронная инф. Процесс. Сист. 30 , 1025–1035 (Curran Associates Inc., 2017).
Гилмер, Дж., Шенхольц, С.С., Райли, П.Ф., Виньялс, О. и Даль, Г.Э. Передача нейронных сообщений для квантовой химии. Проц. Мах. Узнать рез. 70 , 1263–1272 (2017).
Schlichtkrull, M. et al. Моделирование реляционных данных с помощью графовых сверточных сетей.
 В European Semantic Web Conference 593–607 (Springer, 2018).
В European Semantic Web Conference 593–607 (Springer, 2018).Ляо Р., Чжао З., Уртасун Р. и Земель Р. С. LanczosNet: многомасштабные сверточные сети с глубоким графом. В 7-й Международной конференции по обучающим представлениям (OpenReview.net, 2019).
Chen, P., Liu, W., Hsieh, C.-Y., Chen, G. & Zhang, S. Использование краевых функций в графовых нейронных сетях посредством вариационной максимизации информации. Препринт на https://arxiv.org/abs/1906.05488 (2019).
Киркпатрик П. и Эллис К. Химическое пространство. Природа 432 , 823–824 (2004).
Артикул Google Scholar
Васвани, А. и др. Внимание — это все, что вам нужно. Доп. Нейронная инф. Процесс. Сист. 30 , 6000–6010 (Curran Associates Inc., 2017).
Боммасани, Р.
 и др. О возможностях и рисках моделей фундаментов. Препринт на https://doi.org/10.48550/ARXIV.2108.07258 (2021 г.).
и др. О возможностях и рисках моделей фундаментов. Препринт на https://doi.org/10.48550/ARXIV.2108.07258 (2021 г.).Читрананда, С., Гранд, Г. и Рамсундар, Б. ЧемберТа: крупномасштабная предварительная подготовка с самоконтролем для предсказания молекулярных свойств. Препринт на https://arxiv.org/abs/2010.09885 (2020).
Ван, Ю., Ван, Дж., Цао, З. и Барати Фаримани, А. Молекулярно-сопоставительное обучение представлений с помощью графовых нейронных сетей. Нац. Мах. Интел. 4 , 279–287 (2022).
Артикул Google Scholar
Su, J., Lu, Y., Pan, S., Wen, B. & Liu, Y. RoFormer: усовершенствованный трансформатор с встраиванием поворотного положения. Препринт на https://arxiv.org/abs/2104.09864 (2021 г.).
Ву, З. и др. MoleculeNet: эталон молекулярного машинного обучения. Хим. науч.
 9 , 513–530 (2018).
9 , 513–530 (2018).Артикул Google Scholar
Лю, Ю. и др. RoBERTa: надежно оптимизированный подход к предварительному обучению BERT. Препринт на https://arxiv.org/abs/1907.11692 (2019).
Девлин Дж., Чанг М.-В., Ли К. и Тутанова К. БЕРТ: предварительное обучение глубоких двунаправленных преобразователей для понимания языка. В проц. Конференция NAACL 2019: HLT Том 1, 4171–4186 (Ассоциация вычислительной лингвистики, 2019 г.).
Katharopoulos, A., Vyas, A., Pappas, N. & Fleuret, F. Трансформаторы — это RNN: быстрые авторегрессионные преобразователи с линейным вниманием. Проц. Мах. Учиться. Рез. 119 , 5156–5165 (2020).
Hu, W. et al. Стратегии предобучения графовых нейронных сетей. В 8-я Международная конференция по обучающим представлениям (OpenReview.
 net, 2020).
net, 2020).Лю, С., Демирель, М. Ф. и Лян, Ю. N -граммовый граф: простое неконтролируемое представление графов с приложениями к молекулам. В NIPS’19: Proc. 33-я Международная конференция по системам обработки нейронной информации (ред. Уоллах, Х. и др.) 8464–8476 (Curran Associates, Inc., 2019).
Чен, Т., Корнблит, С., Норузи, М. и Хинтон, Г. Простая структура для контрастного обучения визуальным представлениям. Проц. Мах. Учиться. Рез. 119 , 1597–1607 (2020).
Оорд, А. В. Д., Ли, Ю. и Виньялс, О. Репрезентативное обучение с контрастным прогностическим кодированием. Препринт на https://arxiv.org/abs/1807.03748 (2018).
Лю, С. и др. Представление молекулярного графа перед обучением с помощью трехмерной геометрии. В Международная конференция по обучению Представления (2022).
«>Фанг, X. и др. Обучение молекулярному представлению с расширенным геометрическим строением для предсказания свойств. Нац. Мах. Интел. 4 , 127–134 (2022).
Артикул Google Scholar
Алтае-Тран, Х., Рамсундар, Б., Паппу, А. С. и Панде, В. Поиск лекарств с низким объемом данных с однократным обучением. АКЦ Цент. науч. 3 , 283–293 (2017).
Артикул Google Scholar
Xiong, Z. et al. Раздвигая границы молекулярного представления для открытия лекарств с помощью механизма внимания графа. J. Med. хим. 63 , 8749–8760 (2019).
Артикул Google Scholar
«>Ривз, А. и др. Биологическая структура и функция возникают в результате масштабирования неконтролируемого обучения до 250 миллионов белковых последовательностей. Проц. Натл. акад. науч. США 118 , e2016239118 (2021).
Виг, Дж. и др. BERTology встречается с биологией: интерпретация внимания в моделях белкового языка. В 9-я Международная конференция по обучающим представлениям (OpenReview.net, 2021 г.).
Урбина, Ф., Ленцос, Ф., Инверницци, К. и Экинс, С. Двойное использование открытия лекарств с помощью искусственного интеллекта. Нац. Мах. Интел. 4 , 189–191 (2022).
Артикул Google Scholar
«>Шоу П., Ушкорейт Дж. и Васвани А. Самовнимание с репрезентациями относительного положения. В проц. NAACL-HLT 464–468 (Ассоциация вычислительной лингвистики, 2018 г.).
Raffel, C. et al. Изучение ограничений трансферного обучения с помощью унифицированного преобразователя текста в текст. Дж. Маха. Учиться. Рез. 21 , 1–67 (2020).
МАТЕМАТИКА Google Scholar
Ке, Г., Хе, Д. и Лю, Т.-Ю. Переосмысление позиционного кодирования при предварительном обучении языку. В 9-й Международной конференции по обучающим представлениям (OpenReview.net, 2021).
Ким, С. и др. Обновление PubChem 2019: улучшен доступ к химическим данным.
 Рез. нуклеиновых кислот . 47 , Д1102–Д1109 (2018).
Рез. нуклеиновых кислот . 47 , Д1102–Д1109 (2018).Irwin, J.J. & Shoichet, B.K. ZINC — бесплатная база данных коммерчески доступных соединений для виртуального скрининга. J. Chem. Инф. Модель. 45 , 177–182 (2005).
Артикул Google Scholar
Schwaller, P. et al. Молекулярный преобразователь: модель для предсказания химических реакций с калибровкой по неопределенности. АКЦ Цент. науч. 5 , 1572–1583 (2019).
Артикул Google Scholar
Белтажи И., Петерс М. Э. и Кохан А. Лонгформер: преобразователь длинных документов. Препринт на https://arxiv.org/abs/2004.05150 (2020).
Китаев Н., Кайзер Л. и Левская А. Реформер: эффективный трансформатор. В 8-я Международная конференция по обучающим представлениям (OpenReview.

Кликпера Дж., Гросс Дж. и Гюннеманн С. Направленная передача сообщений для молекулярных графов. В 8-я Международная конференция по образовательным представлениям (OpenReview.net, 2020).
Schütt, K. et al. SchNet: сверточная нейронная сеть с непрерывным фильтром для моделирования квантовых взаимодействий. Доп. Нейронная инф. Процесс. Сист. 992–1002 (Curran Associates Inc., 2017).
Чороманский, К. и др. Переосмысление внимания с Исполнителями. В проц. 9-я Международная конференция по обучающим представлениям (OpenReview.net, 2021 г.).



 Атомы углерода одной из молекул связаны с одним или двумя соседними атомами углерода, как, например, в другой молекуле один из атомов углерода связан сразу с тремя атомами углерода. Отсюда можно предположить, что разному порядку связывания атомов при одинаковом количестве атомов углерода и водорода в данном случае должны соответствовать различные вещества с разными свойствами. Действительно, все так и есть:
Атомы углерода одной из молекул связаны с одним или двумя соседними атомами углерода, как, например, в другой молекуле один из атомов углерода связан сразу с тремя атомами углерода. Отсюда можно предположить, что разному порядку связывания атомов при одинаковом количестве атомов углерода и водорода в данном случае должны соответствовать различные вещества с разными свойствами. Действительно, все так и есть:
 Смит
Вернер Арбер
Смит
Вернер Арбер 1. Введение в методологию и правила кодирования. J. Chem. Инф. вычисл. науч. 28 , 31–36 (1988).
1. Введение в методологию и правила кодирования. J. Chem. Инф. вычисл. науч. 28 , 31–36 (1988). , Парк С., Канг К. и Хо Дж. К. Представление молекул на основе самоконтроля для прогнозирования взаимодействия лекарство-мишень. Проц. Мах. Учиться. Рез. 106 , 230–248 (2019).
, Парк С., Канг К. и Хо Дж. К. Представление молекул на основе самоконтроля для прогнозирования взаимодействия лекарство-мишень. Проц. Мах. Учиться. Рез. 106 , 230–248 (2019).

 В European Semantic Web Conference 593–607 (Springer, 2018).
В European Semantic Web Conference 593–607 (Springer, 2018). и др. О возможностях и рисках моделей фундаментов. Препринт на https://doi.org/10.48550/ARXIV.2108.07258 (2021 г.).
и др. О возможностях и рисках моделей фундаментов. Препринт на https://doi.org/10.48550/ARXIV.2108.07258 (2021 г.). 9 , 513–530 (2018).
9 , 513–530 (2018). net, 2020).
net, 2020). Рез. нуклеиновых кислот . 47 , Д1102–Д1109 (2018).
Рез. нуклеиновых кислот . 47 , Д1102–Д1109 (2018).