Урок 27. Состав и физические свойства воды – HIMI4KA
Архив уроков › Химия 8 класс
В уроке 27 «Состав и физические свойства воды» из курса «Химия для чайников» узнаем, что из себя представляет вода, выясним её состав, а также физические свойства.
Наиболее распространенным оксидом на Земле является оксид водорода H2O, или вода. Без воды, как и без кислорода, невозможна жизнь человека, животных и растений.
Вода — единственное вещество, существующее на Земле одновременно в трех агрегатных состояниях: жидком, твердом и газообразном. Она является основным компонентом морей и океанов, ледников и айсбергов, облаков и тумана.
Около 70 % поверхности Земли покрыто океанами, морями, реками и озерами — природными хранилищами воды. Из космоса толстый слой воды имеет голубой цвет (рис. 104), вот почему нашу планету называют голубой. Вода входит в состав всех живых организмов, а также очень многих минералов.
Содержание
- Состав и строение воды
- Физические свойства воды
- Вода как растворитель
Состав и строение воды
Как вы уже знаете, молекула воды состоит из трех атомов — двух атомов водорода и одного атома кислорода (рис. 105). Относительная молекулярная масса воды равна:
105). Относительная молекулярная масса воды равна:
Следовательно, молярная масса воды равна:
Вода — это вещество с молекулярным строением. В твердом (рис. 106) и жидком агрегатных состояниях молекулы воды прочно связаны друг с другом. Этим во многом объясняется целый ряд удивительных физических свойств воды.
Физические свойства воды
При комнатных условиях вода представляет собой жидкость без вкуса и запаха. В тонком слое вода не имеет цвета. Однако при толщине более 2 м она имеет голубой цвет. Совершенно чистая вода очень плохо проводит электрический ток.
На заметку: По тому, как проводит электрический ток вода, можно судить о ее чистоте — чем ниже электропроводность, тем чище вода.
У большинства веществ в твердом состоянии плотность выше, чем в жидком. В отличие от них вода в твердом агрегатном состоянии (лед) имеет более низкую плотность, чем в жидком. При 0 °С плотность льда равна примерно 0,92 г/см3, а плотность жидкой воды — примерно 1,00 г/см3.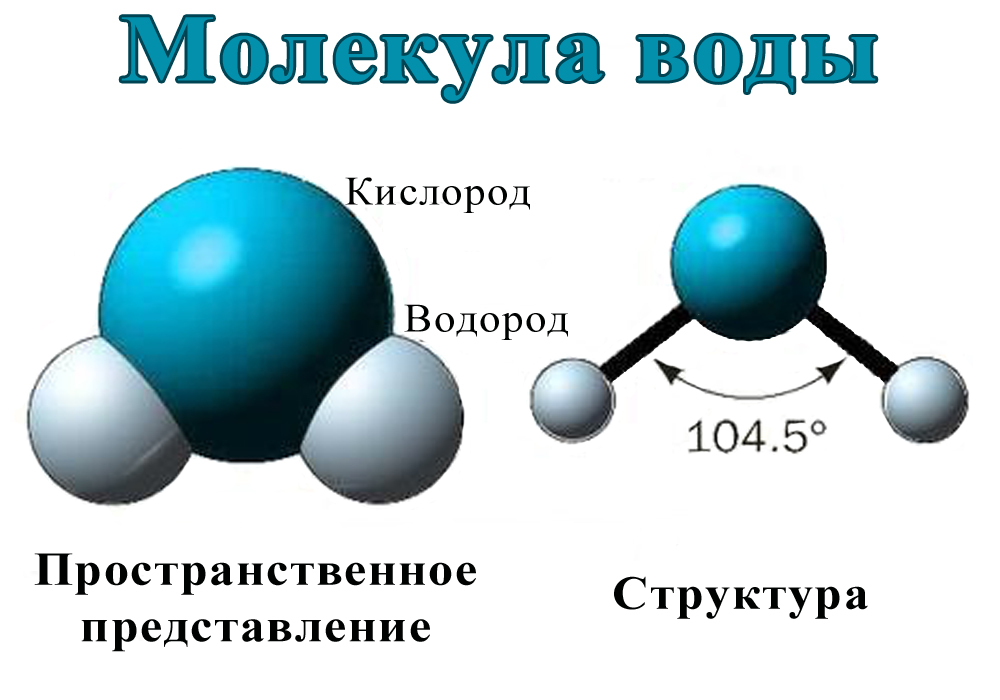 Это означает, что лед легче воды, поэтому он не тонет в ней (рис. 107). Такая особенность воды объясняет, почему водоемы начинают замерзать не со дна, а с поверхности и очень редко промерзают до самого дна. Это защищает живые организмы, обитающие в реках и морях, от гибели.
Это означает, что лед легче воды, поэтому он не тонет в ней (рис. 107). Такая особенность воды объясняет, почему водоемы начинают замерзать не со дна, а с поверхности и очень редко промерзают до самого дна. Это защищает живые организмы, обитающие в реках и морях, от гибели.
У воды высокая теплоемкость, поэтому она медленно нагревается, но и медленно остывает. Это позволяет морям и океанам накапливать тепло летом (и днем) и высвобождать его зимой (и ночью), что предотвращает резкие колебания температуры воздуха на нашей планете в течение года (и суток). Моря и океаны служат своеобразными аккумуляторами тепла на нашей планете.
При нормальном давлении (101,3 кПа) температура кипения воды равна 100 °С. При понижении давления температура кипения воды понижается. Например, в горах на высоте около 5000 м давление существенно ниже нормального (примерно в два раза), поэтому вода закипает в этих условиях при температуре около 84 °С. Понятно, что варить продукты до готовности в горах необходимо более длительное время. И наоборот, в скороварке, где создается высокое давление, вода закипает при температуре выше 100 °С, что позволяет быстрее приготавливать пищу.
И наоборот, в скороварке, где создается высокое давление, вода закипает при температуре выше 100 °С, что позволяет быстрее приготавливать пищу.
Вода как растворитель
С совершенно чистой водой, не содержащей никаких других веществ, большинство людей никогда не встречается. Такая вода используется только в специальных целях.
Почти все жидкости, с которыми мы сталкиваемся в повседневной жизни и деятельности, представляют собой растворы различных веществ.
Раствор — это однородная смесь двух и более веществ.
Одно из веществ, входящих в состав раствора, называется растворителем, а остальные — растворенными веществами. Очень часто растворителем является вода. Вода может растворять твердые, жидкие и газообразные вещества.
Все природные воды содержат растворенные соли. Их легко обнаружить экспериментально, выпарив воду на часовом стекле. Кроме солей, вода может растворять различные газы. Их присутствие (правда, не всегда) можно обнаружить экспериментально. Например, поместив пробирку с холодной водой из-под крана в теплое место, через некоторое время можно заметить у стенок пробирки пузырьки. Это растворенные газы (преимущественно кислород) выделяются из раствора при его нагревании до комнатной температуры (рис. 108).
Например, поместив пробирку с холодной водой из-под крана в теплое место, через некоторое время можно заметить у стенок пробирки пузырьки. Это растворенные газы (преимущественно кислород) выделяются из раствора при его нагревании до комнатной температуры (рис. 108).
Многие жидкости также хорошо растворимы в воде. Например, серная кислота и спирт неограниченно растворяются в воде. В таком случае говорят, что вещество смешивается с водой в любых соотношениях. Из-за хорошей растворимости многих веществ в воде ее иногда называют универсальным растворителем.
Краткие выводы урока:
- Вода не имеет вкуса, цвета (в тонком слое) и запаха, кипит при 100 °С, а переходит в твердое состояние при 0 °С.
- Плотность твердой воды меньше, чем жидкой.
- Раствор — это однородная смесь двух и более веществ.
- Вода является универсальным растворителем — она хорошо растворяет многие твердые, жидкие и газообразные вещества.
Надеюсь урок 27 «Состав и физические свойства воды» был понятным и познавательным. Если у вас возникли вопросы, пишите их в комментарии.
Если у вас возникли вопросы, пишите их в комментарии.
Урок 28. Химические свойства воды →
← Урок 26. Получение водорода и его применение
Последние публикации в коллективном блоге:Интернет-порталы, которые помогут вам успешно сдать ЕГЭ. 1 / Автор: MiriadaЕсли бы вы инвестировали 00 в Amazon 10 лет назад, вот сколько у вас было бы сейчас 2 / Автор: admin Методические рекомендации для выпускников по самостоятельной подготовке к ЕГЭ 2 / Автор: admin В Минпросвещения допустили повторный перенос даты сдачи ЕГЭ 1 / Автор: admin ЕГЭ не отменят из-за коронавируса, но проведут позже 1 / Автор: admin Рособрнадзор будет выявлять нарушения во время ЕГЭ 2020 с помощью нейросетей 1 / Автор: admin ФИПИ опубликовал проекты контрольных измерительных материалов ЕГЭ-2020, существенных изменений нет 4 / Автор: admin Рособрнадзор проанализировал поступившие предложения по совершенствованию ЕГЭ 2 / Автор: admin Посещаемые разделы форума: Последние обсуждаемые темы на форуме:Детские игровые комплексы 0 / Раздел: Помогаем друг другуОчень нужно купить права на трактор 0 / Раздел: Помогаем друг другу кто знает бактерицидные лампы где можно приобрести? 2 / Раздел: Помогаем друг другу мне нужен магазин со стройматериалами 3 / Раздел: Помогаем друг другу Можно ли накрутить голосование в конкурсе? 4 / Раздел: Помогаем друг другу Управление медиафайлами 0 / Раздел: Помогаем друг другу Скажите, пожалуйста, вот в маршрутках в которых мы ездим 3 / Раздел: ВУЗЫ РОССИИ Изучение итальянского языка 5 / Раздел: Помогаем друг другу |
|
Структура и свойства воды
Вода является ценным природным ресурсом. Вода необходима для выживания всех живых существ. Мы не можем представить мир без воды. Вода требуется животным и растениям для завершения их повседневной метаболической деятельности. Вода необходима растениям для синтеза пищи в процессе фотосинтеза. Мы все можем прожить дни без еды, но не можем представить дни без воды; без воды даже растения засыхают и сбрасывают листья.
Вода — бесцветное и прозрачное химическое вещество, которое является основным компонентом рек, океанов и озер земной коры. Это важная жидкость, которая играет важную роль в выживании жизни на Земле.
H 2 O — химическая формула воды. Он состоит из двух атомов водорода и одного атома кислорода, соединенных ковалентными связями. Эта жидкость составляет 71% земной поверхности.
Состояние воды
- Вода в твердом состоянии называется льдом. Вода замерзает, образуя лед, при 0 градусов по Цельсию (точка замерзания воды).
- Вода в жидком состоянии покрывает большую часть земной поверхности. Он используется в самых разных приложениях.
- Водяной пар представляет собой газообразное состояние воды. Вода достигает точки кипения при 100 градусах Цельсия и превращается в водяной пар.
Физические свойства воды
- Химическая формула: H 2 O — это химическая формула воды, как мы все знаем. Ковалентные связи существуют между атомами водорода и кислорода в молекуле воды. Один атом кислорода образует соединение с двумя атомами водорода.

- Внешний вид: В естественном состоянии вода представляет собой бесцветную жидкость без запаха и вкуса.
- Температура кипения: Температура кипения воды 100 градусов по Цельсию, как мы все знаем. Однако сравнительно высокая температура кипения воды нарушает тенденцию таблицы Менделеева. Водород (следующий гидрид) имеет относительно высокую температуру кипения по сравнению с теллуридом водорода и сероводородом, оба из которых имеют низкие температуры кипения. Это связано с чрезвычайно сильными водородными связями в молекуле воды. Для того, чтобы они сломались и начали кипеть, требуется много энергии.
- Температура замерзания: То же самое относится к температуре замерзания воды. Вода имеет температуру замерзания 0 градусов по Цельсию. Тот факт, что воде требуется много времени, чтобы замерзнуть (или даже закипеть), имеет решающее значение для существования нашей экосистемы.
- Плотность: Одним из замечательных свойств воды является то, что она плотная в проданном состоянии.
 Плотность воды увеличивается по мере ее охлаждения до 4°С. Однако после этого вода становится менее плотной. Из-за этого лед плавает в воде.
Плотность воды увеличивается по мере ее охлаждения до 4°С. Однако после этого вода становится менее плотной. Из-за этого лед плавает в воде. - Вязкость: Из-за очень сильных межмолекулярных взаимодействий вода имеет высокую вязкость.
- Растворимость: Вода является высокоэффективным растворителем. Его даже называют универсальным растворителем.
Химические свойства воды
- Амфотерная природа: Вода амфотерна по своей природе, потому что она может действовать как кислота и как основание. Следующие две реакции показывают, что вода имеет амфотерную природу.
Н 2 O (L) + HCl (AQ) ⇌ H 3 O + + CL —
H 2 O (L) + NH 3 (AQ) ⇌ NH 4 4 4 4 4 40012 3 (AQ) + + OH –
- Окислительно-восстановительные реакции: Вода восстанавливается до молекулы водорода с помощью электроположительных элементов.
 В результате вода является богатым источником водорода. Вода окисляется до O 2 в процессе фотосинтеза. Вода очень полезна в окислительно-восстановительных реакциях, потому что она может окисляться и восстанавливаться.
В результате вода является богатым источником водорода. Вода окисляется до O 2 в процессе фотосинтеза. Вода очень полезна в окислительно-восстановительных реакциях, потому что она может окисляться и восстанавливаться. - Реакция гидролиза: Из-за своей диэлектрической проницаемости вода имеет очень сильную склонность к гидратации. Он растворяет широкий спектр ионных соединений. Вода может гидролизовать некоторые ковалентные и ионные соединения.
Структура воды
Жидкая вода
Молекула воды состоит из двух атомов водорода, соединенных одной химической связью с атомом кислорода. Ядра большинства атомов водорода полностью состоят из протонов. Вода содержит две изотопные формы, дейтерий и тритий, в которых атомные ядра также содержат один и два нейтрона соответственно. Оксид дейтерия (D 2 O), также известная как тяжелая вода, используется в химических исследованиях и в качестве замедлителя нейтронов в некоторых ядерных реакторах.
Атомы водорода в молекулах воды притягиваются к областям с высокой электронной плотностью и могут образовывать слабые связи, известные как водородные связи, с этими областями. Это означает, что атомы водорода в одной молекуле воды притягиваются к несвязывающим электронным парам атома кислорода соседней молекулы воды. Считается, что структура жидкой воды состоит из агрегатов молекул воды, которые постоянно образуются и переформируются. Другие необычные свойства воды, такие как ее высокая вязкость и поверхностное натяжение, объясняются этим ближним порядком.
Структуры льда
Межмолекулярные взаимодействия в твердом состоянии (лед) приводят к высокоупорядоченной, но рыхлой структуре, в которой каждый атом кислорода окружен четырьмя атомами водорода, два из которых ковалентно связаны с атомом кислорода и два других (на больших расстояниях) связаны водородной связью с неподеленными электронными парами атома кислорода.
Из-за своей открытой структуры лед имеет меньшую плотность, чем жидкая вода, в которой упорядоченная структура частично нарушена, а молекулы воды (в среднем) расположены ближе друг к другу. В зависимости от условий вода может замерзнуть в различные структуры.
В зависимости от условий вода может замерзнуть в различные структуры.
Значение структуры жидкой воды
- Жидкое состояние воды имеет очень сложную структуру, которая, несомненно, включает значительную ассоциацию молекул. Из-за обширных водородных связей между молекулами в жидкой воде значения таких свойств, как вязкость, поверхностное натяжение и температура кипения, намного выше, чем можно было бы ожидать для типичной жидкости с небольшими молекулами. В отличие от конденсированных состояний воды (твердого и жидкого), которые имеют обширную связь между молекулами воды, газообразная (парообразная) фаза имеет относительно независимые молекулы воды, разделенные большими расстояниями.
- Полярность молекулы воды важна при растворении ионных соединений во время образования водного раствора. Океаны на Земле содержат огромное количество растворенных солей, которые являются ценными природными ресурсами. Кроме того, сотни химических реакций, которые происходят каждую секунду, чтобы поддерживать жизнь организмов, происходят в водных жидкостях.
 Кроме того, растворимость в воде таких веществ, как сахар и соль, позволяет придавать пищевым продуктам аромат во время их приготовления. Хотя растворимость растворенного вещества в воде является очень сложным процессом, решающее значение имеет взаимодействие между полярными молекулами воды и растворенным веществом.
Кроме того, растворимость в воде таких веществ, как сахар и соль, позволяет придавать пищевым продуктам аромат во время их приготовления. Хотя растворимость растворенного вещества в воде является очень сложным процессом, решающее значение имеет взаимодействие между полярными молекулами воды и растворенным веществом. - Когда ионное твердое вещество растворяется в воде, анионы притягивают положительные концы молекул воды, а катионы притягивают отрицательные концы. Это известно как гидратация. Гидратация ионов соли приводит к ее распаду (растворению) в воде. В процессе растворения сильные силы, существовавшие между положительными и отрицательными ионами твердого тела, заменяются сильными взаимодействиями ионов воды.
Значение воды
- Сельское хозяйство является наиболее важным видом использования воды. Орошение необходимо для сельского хозяйства, а вода является важнейшим компонентом в производстве продуктов питания.
- В зависимости от размера тела человеческое тело содержит от 50 до 78 % воды.
 Чтобы избежать обезвоживания, люди должны выпивать 7 литров воды в день.
Чтобы избежать обезвоживания, люди должны выпивать 7 литров воды в день. - Необходим для пищеварения, а также других биологических процессов, происходящих в живых организмах. Это необходимо для поддержания рН тела. Он также помогает в движении антител иммунной системы.
- Помогает регулировать температуру тела. Вода обеспечивает организму необходимый охлаждающий эффект.
- Через пот и мочеиспускание вода вымывает вредные токсины из организма. Он предотвращает накопление отходов в живых организмах.
- Применяется для создания эмульсий и растворов, используемых в процессе стирки.
- Бытовое потребление воды составляет 15% от общего водопотребления. Вода используется для питья, купания, приготовления пищи и мытья посуды, одежды, фруктов и овощей, а также для чистки зубов.
- Используется либо при создании продукта, либо для охлаждения оборудования, используемого при создании продукта. Промышленная вода используется для мытья, охлаждения, обработки, транспортировки, разбавления или изготовления продукта.
 Большая часть воды используется в производстве химикатов, бумаги и продуктов питания.
Большая часть воды используется в производстве химикатов, бумаги и продуктов питания. - Он используется в транспорте, производстве, гидроэнергетике, удалении отходов тела, туризме и отдыхе.
Образец
Вопрос sВопрос 1: Какое использование воды является наиболее важным?
Ответ:
Потребление воды в домашних условиях является наиболее значительным повседневным потреблением воды для большинства людей. Бытовое использование относится к воде, используемой в доме ежедневно, например, для питья, приготовления пищи, купания, мытья одежды и посуды, смыва туалетов и орошения газонов и садов.
Вопрос 2. Дает ли вода энергию?
Ответ:
Вода содержит два типа электричества, а также множество других веществ. Кинетическая энергия считается первым видом энергии. Это электричество, такое как действие, которое используется во время выполнения процесса.
Вода может течь в результате кинетической энергии, и могут образовываться волны.
Вопрос 3. Каков естественный источник воды?
Ответ:
Питьевую воду получают из природных источников, таких как подземные или морские воды. Подземные воды образуются, когда снег и дождь просачиваются сквозь землю. Вода собирается в открытых помещениях и порах, а также в песчано-гравийных отложениях, известных как водоносные горизонты.
Вопрос 4. Что такое водородная связь?
Ответ:
Водородная связь представляет собой электростатическую силу притяжения между атомом водорода, который ковалентно связан с более электроотрицательным атомом или группой, и другим электроотрицательным атомом с одной парой электронов — акцептором водородной связи.
Вопрос 5. Что такое внутримолекулярная водородная связь?
Ответ:
Внутримолекулярные водородные связи возникают в пределах одной молекулы.
Когда две функциональные группы молекулы могут образовывать водородные связи друг с другом, это происходит.
Источники воды, свойства, формула, структура, состояния и использование
Вода является наиболее распространенным предметом, изучаемым студентами в области физической химии. Здесь мы рассмотрели все важные моменты, связанные с водой, например, что такое вода, ее свойства, химическая формула и ее использование. Давайте сначала ответим на главный вопрос, что такое вода?? Вода является важнейшим природным ресурсом, более 70% площади земного шара занято водой. Однако вряд ли 2,5% составляют общемировые запасы пресной воды, включая замерзшую воду полярных шапок и ледников.
Sources of Water | Percentage of Water | ||||||||
Oceans | 97.33 | ||||||||
Saline lakes and inland seas | 0. | ||||||||
Полярные льды и ледники | 2,04 | ||||||||
Подземные воды |
Что такое вода с химической точки зрения?Вода представляет собой химическое соединение, состоящее из водорода и кислорода. Вода существует во всех трех состояниях: твердом, жидком и газообразном. Вода является основным компонентом всех живых существ (растений, животных и людей) и атмосферной среды, в которой мы живем. Из чего состоит вода? Самый частый вопрос, который задают студенты: из чего состоит вода? Изучая главу о растворителях в разделе физической химии, можно понять, из чего состоит вода? Вода состоит из двух атомов водорода и одного атома кислорода. Какова химическая формула воды?Как мы знаем, вода состоит из двух атомов водорода и одного атома кислорода, химическая формула воды – h3O. Химическое название молекулы воды – оксид дигидрогена. Вода представляет собой химическое соединение, состоящее из двух элементов водорода и кислорода, соединенных в соотношении 1:8 по массе. Структура молекулы воды[Изображение будет загружено в ближайшее время] Молекулы воды имеют изогнутую форму. Гибридизация молекулы воды представляет собой SP3. угол между двумя парами связей меньше 180 градусов из-за отталкивания между неподеленной парой и неподеленной парой. Свойства воды Физические и химические свойства воды зависят от природы и прочности связи, присутствующей в кислороде и водороде. Наличие неподеленной пары влияет на реакционную способность воды. Физические свойства воды
Химические свойства воды
Различные состояния водыВода существует в трех различных состояниях. Он обладает свойствами образования прочных водородных связей. Различные состояния воды:
Важность воды
Вода, присутствующая в природных телах, таких как реки, озера и океаны, удерживает растворенный в ней воздух. Этот растворенный воздух играет важную биологическую роль для водных животных. Водные растения используют растворенный углекислый газ для фотосинтеза для приготовления пищи.  |


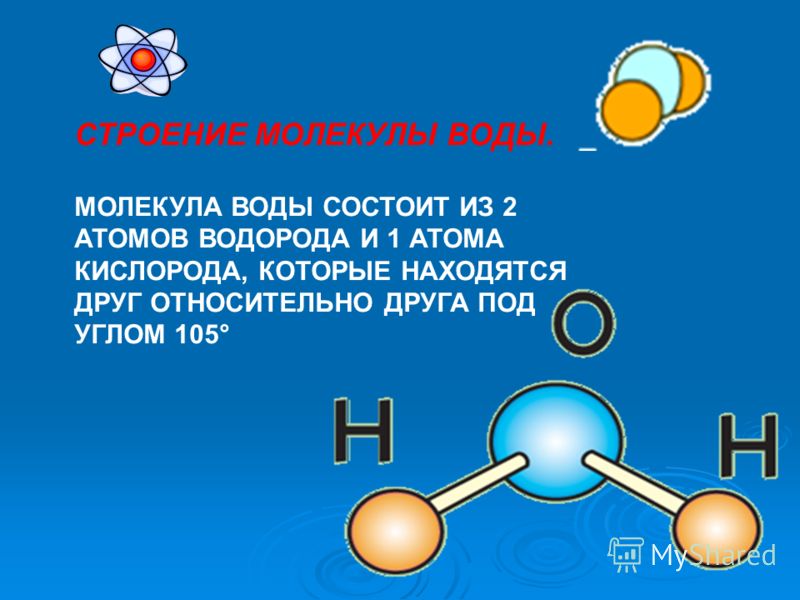
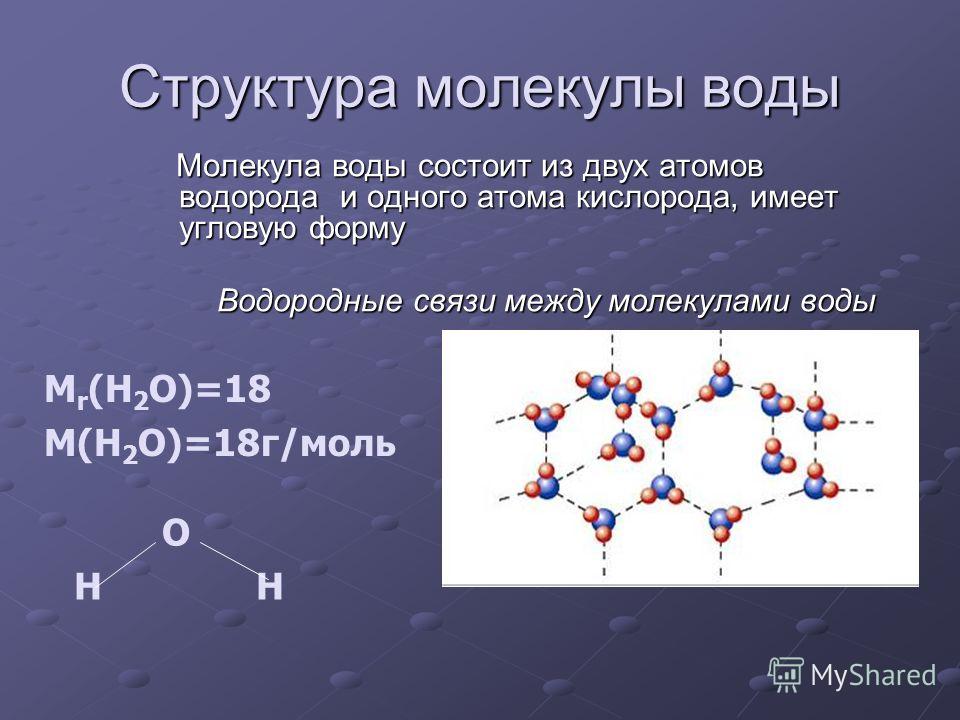
 Молекула ее состоит из двух атомов водорода и одного атома кислорода (Н2О).
Молекула ее состоит из двух атомов водорода и одного атома кислорода (Н2О).
 Эта стадия позволяет довести сточные и природные воды до такого уровня чистоты, что она отвечает стандартам на питьевую воду. Особое внимание в последнее время уделяется чистоте питьевой воды.
Эта стадия позволяет довести сточные и природные воды до такого уровня чистоты, что она отвечает стандартам на питьевую воду. Особое внимание в последнее время уделяется чистоте питьевой воды.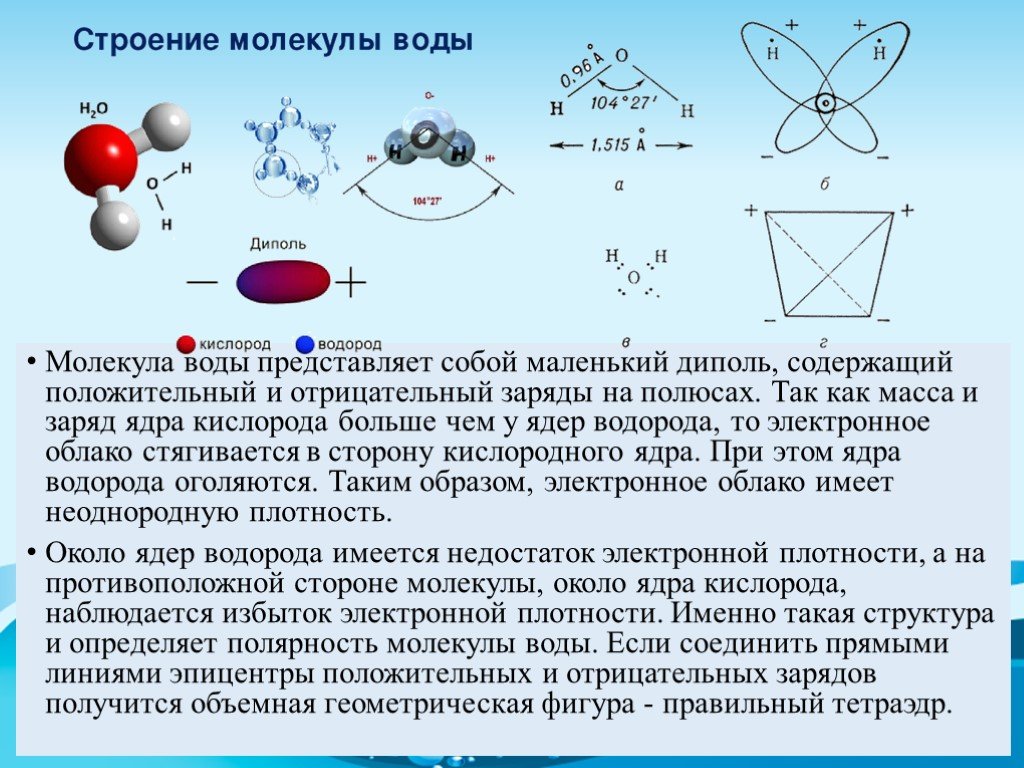

 Плотность воды увеличивается по мере ее охлаждения до 4°С. Однако после этого вода становится менее плотной. Из-за этого лед плавает в воде.
Плотность воды увеличивается по мере ее охлаждения до 4°С. Однако после этого вода становится менее плотной. Из-за этого лед плавает в воде. В результате вода является богатым источником водорода. Вода окисляется до O 2 в процессе фотосинтеза. Вода очень полезна в окислительно-восстановительных реакциях, потому что она может окисляться и восстанавливаться.
В результате вода является богатым источником водорода. Вода окисляется до O 2 в процессе фотосинтеза. Вода очень полезна в окислительно-восстановительных реакциях, потому что она может окисляться и восстанавливаться.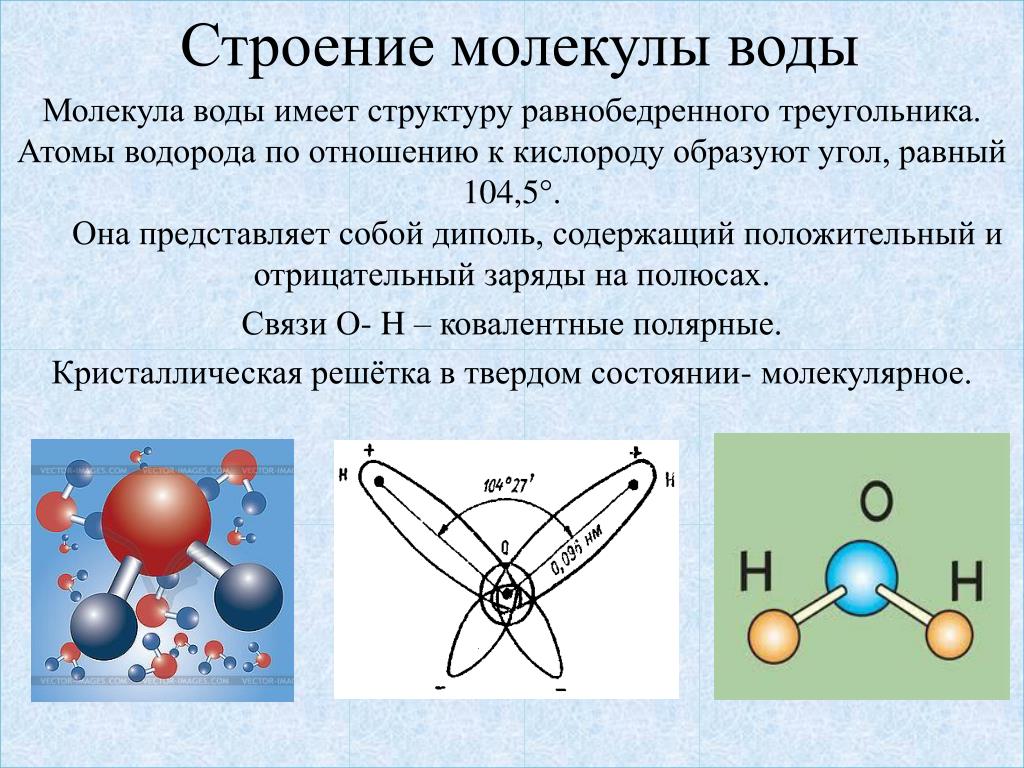 Кроме того, растворимость в воде таких веществ, как сахар и соль, позволяет придавать пищевым продуктам аромат во время их приготовления. Хотя растворимость растворенного вещества в воде является очень сложным процессом, решающее значение имеет взаимодействие между полярными молекулами воды и растворенным веществом.
Кроме того, растворимость в воде таких веществ, как сахар и соль, позволяет придавать пищевым продуктам аромат во время их приготовления. Хотя растворимость растворенного вещества в воде является очень сложным процессом, решающее значение имеет взаимодействие между полярными молекулами воды и растворенным веществом. Чтобы избежать обезвоживания, люди должны выпивать 7 литров воды в день.
Чтобы избежать обезвоживания, люди должны выпивать 7 литров воды в день.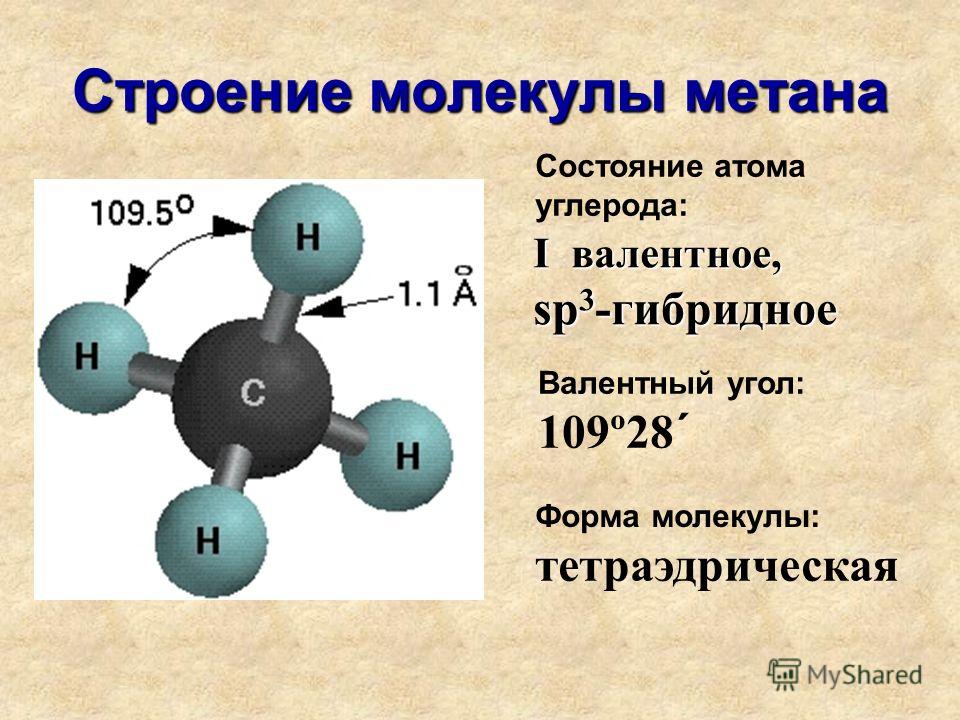 Большая часть воды используется в производстве химикатов, бумаги и продуктов питания.
Большая часть воды используется в производстве химикатов, бумаги и продуктов питания. Вода может течь в результате кинетической энергии, и могут образовываться волны.
Вода может течь в результате кинетической энергии, и могут образовываться волны.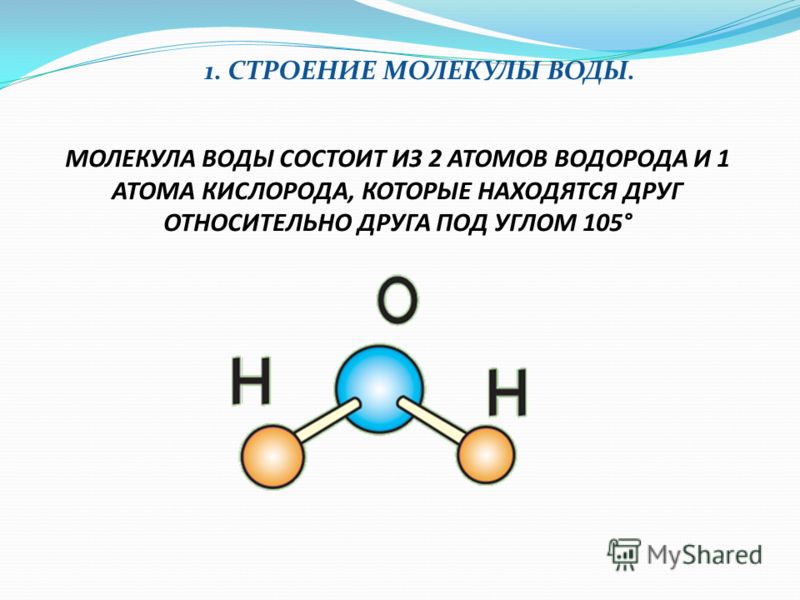 Когда две функциональные группы молекулы могут образовывать водородные связи друг с другом, это происходит.
Когда две функциональные группы молекулы могут образовывать водородные связи друг с другом, это происходит. 008
008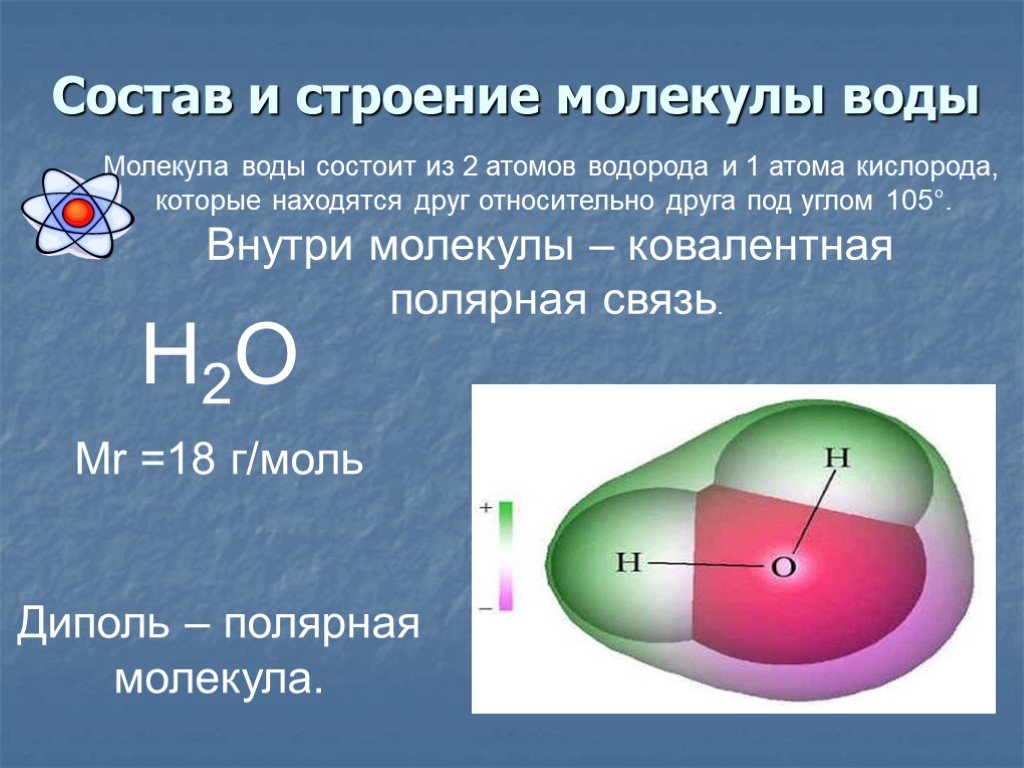 Вода бывает как в свободном, так и в связанном состоянии. Название воды по классификации ИЮПАК — оксидан.
Вода бывает как в свободном, так и в связанном состоянии. Название воды по классификации ИЮПАК — оксидан.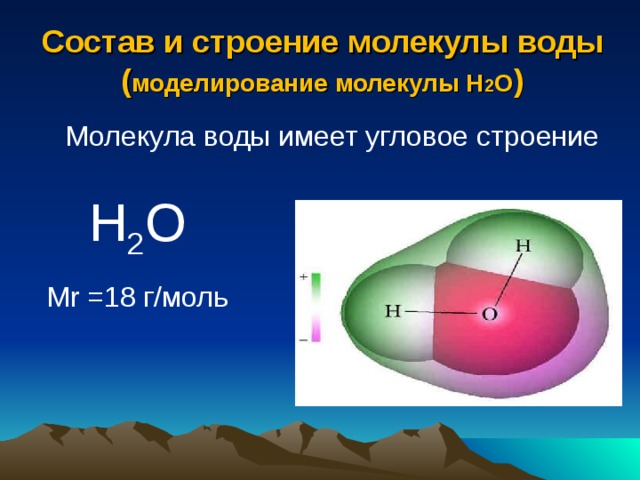 Физические и химические свойства воды приведены ниже:
Физические и химические свойства воды приведены ниже:
