Три состояния вещества. Видеоурок. Физика 7 Класс
Древние ученые считали, что всё на свете состоит из воды, земли, воздуха. Оказывается, в чем-то они были правы. Все вещества могут находиться в тех же состояниях, что вода, земля и воздух. Эти состояния называются жидким, твердым и газообразным. На этом уроке вы узнаете, чем отличаются эти состояния друг от друга и чем объясняются эти различия.
Тема: Первоначальные сведения о строении вещества
Урок: Три состояния вещества
Вспомним замечательную детскую сказку о Снегурочке. Когда Снегурочка прыгнула через костер, она растаяла. Ледяная внучка превратилась в лужицу воды, и эта вода очень быстро испарилась.
В этом фрагменте сказки идет речь о трех состояниях вещества: твердом, жидком и газообразном.

Рис. 1. Три состояния вещества
Каждый знает, что изменить форму твердого тела достаточно трудно, будь то металлическое тело, пластмасса или даже пластилин. Даже для изменения формы пластилина нам все равно приходится прикладывать определенное усилие. Можно сказать, что твердые тела сохраняют свою форму и объем.

Рис. 2. Отличительные признаки твердых тел
А что можно сказать о форме и объеме жидкостей? Жидкость, которую мы налили в один из сосудов, приняла форму этого сосуда. Если перелить ее в сосуд другой формы, то жидкость примет форму другого сосуда. Всякий раз жидкость принимает форму того сосуда, куда ее наливают. Можно сделать вывод:

Рис. 3. Отличительные признаки жидкостей
Совершенно по-иному ведет себя газ. И форму, и объем тел, состоящих из газа, изменить очень легко. Газ не обладает ни собственной формой, ни собственным объемом. Он принимает форму того сосуда, в который его поместили, и занимает весь предоставленный ему объем.

Рис. 4. Отличительные признаки газов
В чем причина столь разного поведения твердых, жидких тел и газов? Причина кроется в молекулярном строении вещества, а именно в расположении, движении и взаимодействии молекул, из которого вещество состоит.
Молекулы твердого тела упакованы очень близко друг к другу. Их расположение носит строго повторяющийся характер. Из-за того, что молекулы твердого тела расположены очень близко друг к другу, силы взаимного притяжения и отталкивания между ними очень велики. Именно поэтому изменить форму и объем твердого тела очень трудно. Взаимодействием молекул объясняется и характер их движения. Они не могут перемещаться по всему твердому телу, а лишь колеблются каждая вокруг своего положения равновесия. Молекулы твердого тела колеблются хаотично, пытаясь сдвинуться то в одну, то в другую сторону, но везде рядом с ними расположены точно т
Взаимодействие молекул. Агрегатные состояния вещества. Видеоурок. Физика 7 Класс
На данном уроке, тема которого «Взаимодействие молекул. Агрегатное состояние вещества», мы подробно узнаем, в каких агрегатных состояниях может перебывать одно и то же вещество и чем это обусловлено.
Как известно, молекула – это наименьшая частица, которая сохраняет свойства вещества. Однако не все свойства можно так описать: например, и лёд, и вода состоят из одних и тех же молекул воды (Рис. 1). Значит, знать, из каких молекул состоит вещество, бывает недостаточно, чтобы описать все его свойства.

Рис. 1. Разные свойства одного вещества
Вспомним, например, конструктор «Лего». Высыпав его из коробки, мы просто получим кучу деталей конструктора. И уже из этих деталей мы можем собрать или автомобиль, или дом. Результат будет зависеть от того, как эти детали будут соединены.
Аналогично и с веществом (Рис. 2). Чтобы описать его, нужно не только указать молекулярный или атомный состав, но еще и то, как частицы соединены, как взаимодействуют. Ярким примером этому являются графит и алмаз, свойства которых очень сильно отличаются (Рис. 3.). Но состоят они из одних и тех же атомов углерода.

Рис. 2. Разнообразие веществ
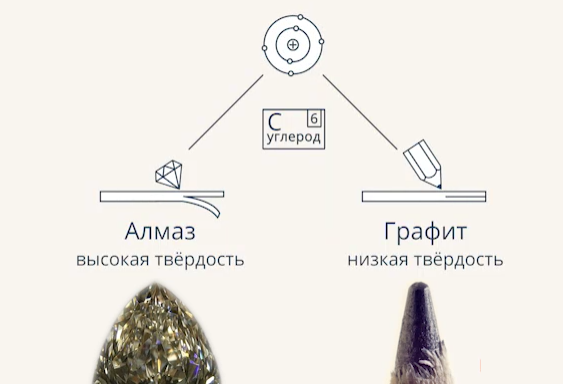
Рис. 3. Свойства алмаза и графита
Аллотропия
Свойство, когда разные простые вещества состоят из одних и тех же частиц, называется аллотропией (Рис. 4). Сами эти вещества называются аллотропными модификациями. Наибольшее число аллотропных модификаций имеет углерод. Своё название атом получил от вещества, которое состоит из этих атомов, – угля. Однако из тех же самых атомов состоит и графит, и сажа, и даже алмаз (Рис. 5). Просто в этих веществах атомы по-разному расположены и по-разному взаимодействуют. И получается, что их свойства существенно отличаются: алмаз – самый крепкий минерал в природе, из него делают инструменты, которые могут разрезать практически любой материал. А вот графит достаточно хрупкий, он легко разрушается, и графитовый стержень легко оставляет след на листе бумаги.

Рис. 4. Аллотропия
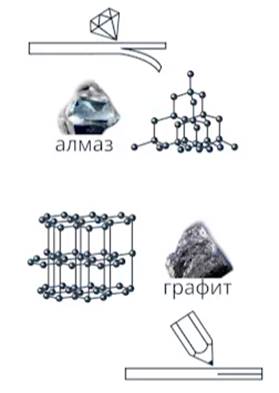
Рис. 5. Структура алмаза и графита
Кроме природных веществ, ученые научились искусственно создавать материалы, различным образом размещая атомы углерода. Такие материалы составляют основу наноматериалов (Рис. 6): это фулерен, углеродные нанотрубки и нановолокна.
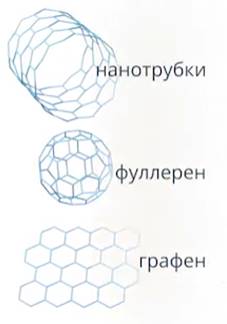
Рис. 6. Наноматериалы
Конечно, другие вещества также могут иметь аллотропные модификации. На данный момент известн
Агрегатные состояния воды. Методические материалы
Цифровой ресурс может использоваться для обучения в рамках программы основной школы.
Компьютерная модель позволяет рассмотреть микроструктуру воды в различных агрегатных состояниях.
Краткая теория
Одно и то же вещество может находится в твердом, жидком и газообразном состояниях. Примером могут служить лед, вода и водяной пар. Эти состояния называют агрегатными.
В твердых телах молекулы совершают беспорядочные колебания около фиксированных центров (положений равновесия). Эти центры могут быть расположены в пространстве нерегулярным образом (аморфные тела) или образовывать упорядоченные объемные структуры (кристаллические тела).
В жидкостях молекулы имеют значительно большую свободу для теплового движения. Они не привязаны к определенным центрам и могут перемещаться по всему объему. Этим объясняется текучесть жидкостей. Близко расположенные молекулы жидкости также могут образовывать упорядоченные структуры, содержащие несколько молекул. Это явление называется ближним порядком в отличие от дальнего порядка, характерного для кристаллических тел.
В газах расстояния между молекулами обычно значительно больше их размеров. Силы взаимодействия между молекулами на таких больших расстояниях малы, и каждая молекула движется вдоль прямой линии до очередного столкновения с другой молекулой или со стенкой сосуда. Среднее расстояние между молекулами воздуха при нормальных условиях порядка 10–8 м, то есть в десятки раз превышает размер молекул. Слабое взаимодействие между молекулами объясняет способность газов расширяться и заполнять весь объем сосуда.
Работа с моделью
Пользователь может выбрать одно из трех агрегатных состояний воды и наблюдать особенности микроструктуры вещества в выбранном состоянии. В твердой форме (лед) для молекул воды доступны лишь вращательные и колебательные движения, поступательные движения на заметные расстояния невозможны. Наблюдается четкая кристаллическая структура льда. Обратите внимание на ориентацию молекул (атомы водорода одних молекул направлены в сторону атомов кислорода других), каждая молекула воды соединена с четырьмя ближайшими к ней другими молекулами. Образуемые при этом пустоты в структуре льда приводят к уменьшению его плотности по сравнению с жидкой водой.
В жидкой форме вода все еще существует как единое целое (сохраняет объем), расстояния между молекулами по порядку величины совпадают с размерами самих молекул. Однако возможны далекие по сравнению с этими размерами смещения молекул от своих начальных положений, из-за этого не сохраняются ни взаимные ориентации молекул, ни форма жидкости как целого.
Наконец, в газе молекулы максимально обособлены друг от друга, и длина свободного пробега молекулы гораздо больше ее размеров.
Рекомендации по применению модели
Данная модель может быть применена в качестве иллюстрации на уроках изучения нового материала в 7 классе по теме «Агрегатные состояния вещества». На примере этой модели можно рассмотреть с учащимися характер движения и взаимного расположения молекул вещества в разных агрегатных состояниях на примере воды.
Пример планирования урока с использованием модели
Тема «Агрегатные состояния вещества»
Цель урока: ввести понятие агрегатное состояние вещества, определить в чем состоит сходство и отличия вещества в разных агрегатных состояниях с точки зрения макроскопических и микроскопических параметров.
|
|||||||||||||||||||||||||
|
Таблица 1. |
Примерные вопросы для составления теста
- Выберите правильное утверждение.
- Только твердые тела состоят из молекул.
- Только жидкости состоят из молекул.
- Только газы состоят из молекул.
- Только жидкости и газы состоят из молекул.
- Все тела состоят из молекул.
- Расстояния между молекулами воды в жидком состоянии…
a) много меньше размеров самих молекул; b) значительно больше размеров самих молекул; c) совпадает по порядку величины с размерами молекул. - Длина свободного пробега молекул воды в газообразном состоянии…
a) много меньше размеров самих молекул; b) значительно больше размеров самих молекул; c) совпадает по порядку величины с размерами молекул. - При переходе воды из жидкого в твердое состояние ее плотность…
a) увеличивается; b) уменьшается; c) не изменяется. - Какое агрегатное состояние воды отличается наличием кристаллической решетки?
- Твердая форма.
- Жидкая форма.
- Газ.
- Какое состояние воды соответствует приведенному рисунку?
Рис. 1.
- Твердая форма.
- Жидкая форма.
- Газ.
- Какое состояние воды соответствует приведенному рисунку?
Рис. 2.
- Твердая форма.
- Жидкая форма.
- Газ.
- Какое состояние воды соответствует приведенному рисунку?
Рис. 3.
- Твердая форма.
- Жидкая форма.
- Газ.
описать движение молекул вещества в твердом, жидком и газообразном состояниях
все твердые вещества имеют рештчаттую структуру молекул которые посаженые очень плотно друг другу все жидкие вещества имеют некоторое расстояние между молекулами и очень часто молекулы внутри жидкости сталкиваются. все газообразные вещества имеют огромное расстояние между молекулами и поетому они оч редко сталкиваются воть своими словами))
в твердом колебания, в газообразном хаотическое, жидком что-то среднее 🙂 (зависит от дифузии и конвекции)
Постоянное хаотичное движение молекул вещества проявляется в легко наблюдаемом явлении – диффузии. Диффузией называется явление проникновения двух или нескольких соприкасающихся веществ друг в друга. Наиболее быстро процесс протекает в газе, если он неоднороден по составу. Диффузия приводит к образованию однородной смеси независимо от плотности компонентов. Так, если в двух частях сосуда, разделенных перегородкой, находятся кислород O2 и водород h3, то после удаления перегородки начинается процесс взаимопроникновения газов друг в друга, приводящий к образованию взрывоопасной смеси – гремучего газа. Этот процесс идет и в том случае, когда легкий газ (водород) находится в верхней половине сосуда, а более тяжелый (вислород) – в нижней. Значительно медленнее протекают подобные процессы в жидкостях. Взаимопроникновение двух разнородных жидкостей друг в друга, растворение твердых веществ в жидкостях (например, сахара в воде) и образование однородных растворов – примеры диффузионных процессов в жидкостях. В реальных условиях диффузия в жидкостях и газах маскируется более быстрыми процессами перемешивания, например, из-за возникновения конвекционных потоков. Наиболее медленно процесс диффузии протекает в твердых телах. Однако, опыты показывают, что при контакте хорошо очищенных поверхностей двух металлов через длительное время в каждом из них обнаруживается атомы другого металла. В твердых телах молекулы совершают беспорядочные колебания около фиксированных центров (положений равновесия) . Эти центры могут быть расположены в пространстве нерегулярным образом (аморфные тела) или образовывать упорядоченные объемные структуры (кристаллические тела)

