Физические свойства алюминия зависят от его чистоты
Основные свойства
Алюминий — химический элемент третей группы периодической системы Д.И. Менделеева.
| Плотность , (кг/м3) | 2,7 |
| Температура плавления Тпл, °С | 660 |
| Температура кипения Ткип, °С | 2 327 |
| Скрытая теплота плавления, Дж/г | 393,6 |
| Теплопроводность l , Вт/м град (при 20° С) | 228 |
| Теплоемкость Ср, Дж/(г · град) (при 0–100°С) | 0,88 |
| Коэффициент линейного расширения α × 10-6, 1/°С (пр°С) | 24,3 |
| Удельное электросопротивление ρ × 10-8 | 2,7 |
| Предел прочности σ в, МПа | 40–60 |
| Относительное удлинение δ , % | 40–50 |
| Твердость по Бринеллю НВ | 25 |
| Модуль нормальной упругости E , ГПа | 70 |
Плотность алюминия
Плотность твердого и расплавленного алюминия снижается по мере увеличения его чистоты:
| Степень чистоты, % | 99,25 | 99,75 | 99. 97 97 | 99,996 | 99.9998 | |
| Плотность при 20°С, г/см3 | 2,727 | 2,706 | 2,703 | 2,6996 | 2,6989 | 2,69808 |
| Степень чистоты, % | 99,25 | 99.40 | 99.75 |
| Плотность, г/см3 | 2,311 | 2,291 | 2,289 |
Температура плавления и кипения.
В момент плавления алюминия возрастает объем металла: для алюминия чистотой 99,65 % — на 6,25%, для более чистого металла — на 6,60 %. По мере повышения степени чистоты алюминия температура его плавления возрастает:
| Степень чистоты, % | 99,2 | 99,5 | 99,6 | 99,97 | 99,996 |
| Температура плавления, °С | 657 | 658 | 659,8 | 660,24 |
Теплопроводность алюминия
Теплопроводность алюминия повышается с увеличением степени его чистоты. Для технического алюминия (99,49 и 99,70%) теплопроводность при 200°С равна соответственно 209 и 222 Вт/(м×К). Для электролитически рафинированного алюминия чистотой 99,9% теплопроводность при 190°С возрастает до 343 Вт/(м×К). Примеси меди, магния и марганца в алюминии снижают его теплопроводность. Например, добавка 2 % Mn к алюминию снижает теплопроводность с 209 до 126 Вт/(м×К).
Для технического алюминия (99,49 и 99,70%) теплопроводность при 200°С равна соответственно 209 и 222 Вт/(м×К). Для электролитически рафинированного алюминия чистотой 99,9% теплопроводность при 190°С возрастает до 343 Вт/(м×К). Примеси меди, магния и марганца в алюминии снижают его теплопроводность. Например, добавка 2 % Mn к алюминию снижает теплопроводность с 209 до 126 Вт/(м×К).
Электропроводность алюминия
На электропроводность алюминия влияет ряд факторов: степень деформации, режим термической обработки и т. д., решающую же роль играет природа примесей, присутствующих в алюминии. Примеси по их отрицательному влиянию на электропроводность алюминия можно расположить в следующий ряд: Cr, V, Mn, Ti, Mg, Ag, Сu, Zn, Si, Fe Ni.

Наиболее отрицательное влияние на электросопротивление алюминия оказывают примеси Сг, V, Мп и Ti . Поэтому в алюминии для электротехнической промышленности сумма Cr+V+Mn+Ti не должна превышать 0,015% (марка А5Е) и даже 0,01 % (А7Е) при содержании кремния соответственно 0,12 и 0,16 %.
Влияние примесей на электропроводность алюминия
Основными примесями в алюминии являются кремний, железо, медь, цинк и титан. При малых содержаниях кремния в алюминии (0,06%) величина Fe : Si (в пределах от 0,8 до 3,8) сравнительно мало влияет на его электросопротивление. При увеличении содержания кремния до 0,15—0,16% влияние Fe : Si возрастает. Ниже приведено влияние Fe : Si на электропроводность алюминия:
| Fe : Si | 1,07 | 1,44 | 2,00 | 2,68 | 3,56 |
| Удельное электросопротивление алюминия, ×10-2 мкОм·мм: | |||||
| нагартованного | 2,812 | 2,816 | 2,822 | 2,829 | 2,838 |
| отожженного | 2,769 | 2,771 | 2,778 | 2,783 | 2,788 |
Удельное электрическое сопротивление отожженной алюминиевой проволоки (ρ, мкОм·м) при 20°С в зависимости от содержания примесей можно приблизительно определить по следующей формуле: ρ=0,0264+0,007×(% Si)+0,0007×(% Fe) + 0,04×[% (Cr+V + Mn + Ti)].
Отражательная способность
С повышением степени чистоты алюминия возрастает его способность отражать свет от поверхности. Так, степень отражения белого света от прокатанных алюминиевых листов (фольги) в зависимости от чистоты металла, возрастает следующим образом: для Аl 99,2%—75%, Аl 99,5%—84% и для Аl 99,8%—86%. Поверхность листа, изготовленного из электролитически рафинированного алюминия чистотой 99,996%, отражает 90% падающего на него белого света.
Электропроводность — алюминий — Большая Энциклопедия Нефти и Газа, статья, страница 1
Cтраница 1
Электропроводность алюминия зависит от содержания в нем примесей. [1]
Электропроводность алюминия при добавлении различных металлов ( особенно марганца и титана) понижается. Сплавы типа твердых расгворов обладают наименьшей электропроводностью в закаленном состоянии и наибольшей-в отожженном. Обрабатываемость резанием чистого алюминия плохая.
[3]
Сплавы типа твердых расгворов обладают наименьшей электропроводностью в закаленном состоянии и наибольшей-в отожженном. Обрабатываемость резанием чистого алюминия плохая.
[3]
| Химический состав алюминия. [4] |
Электропроводность алюминия зависит от степени чистоты металла и понижается с увеличением содержания в нем примесей. [5]
Электропроводность алюминия, применяемого вместо меди для проводов, составляет 65 % электропроводности меди. [6]
Электропроводность алюминия сильно зависит от примесей и мало от механической и тепловой обработки. Чем чище состав алюминия, тем выше его электропроводность и лучше противодействие химическим воздействиям. Обработка, прокатка и отжиг значительно влияют на механическую прочность алюминия. При холодной обработке увеличивается его твердость, упругость и прочность на растяжение. [7]
Электропроводность алюминия составляет 60 % электропроводности меди, а плотность в 3 2 раза меньше, чем у меди. Таким образом, масса алюминиевого провода при равной электропроводности приблизительно в 2 раза меньше. Однако механические свойства алюминия, такие, как прочность — и текучесть, значительно ниже, чем у меди.
[8]
Таким образом, масса алюминиевого провода при равной электропроводности приблизительно в 2 раза меньше. Однако механические свойства алюминия, такие, как прочность — и текучесть, значительно ниже, чем у меди.
[8]
Электропроводность алюминия зависит от степени чистоты металла и понижается с увеличением содержания в нем примесей. [9]
Электропроводность алюминия составляет 60 % электропроводности меди. [10]
На электропроводность алюминия сильно влияет его чистота. [11]
Различные примеси влияют на электропроводность алюминия, но в неодинаковой степени. Наиболее сильно снижают электропроводность примеси хрома, ванадия и марганца. В небольшой степени электропроводность алюминия зависит от степени его деформации и режима термической обработки. Отрицательное влияние деформации на электропроводность устраняется отжигом. [12]
Микроструктура проволоки из обычной меди после отжига в течение 30 мин в среде водорода при 850 С. |
Примеси Si резко снижают электропроводность алюминия, так как они образуют с алюминием твердый раствор Al-Si. Железо с алюминием твердого раствора не образует, поэтому его влияние на электропроводность проволоки невелико. [14]
Так как примесь ванадия снижает электропроводность алюминия, то загрязнение гидроокиси алюминия ванадатом натрия недопустимо. Промывка гидроокиси алюминия горячей водой обычно обеспечивает достаточно полное удаление ванадата натрия. При относительно большом содержании V2O5 в боксите приходится принимать специальные меры для вывода ванадата натрия из цикла. Для этого часть оборотного раствора охлаждают до 25 — 30 С. При охлаждении из раствора выпадает ванадиевый шлам, представляющий собой смесь соды, фосфата и ванадата натрия. Ванадиевый шлам является источником получения ванадия. [15]
[15]
Страницы: 1 2 3 4
Проводит ли алюминий электричество? Что вам нужно знать
Если вы разрабатываете продукт, для которого важна электропроводность, вы можете рассматривать алюминий в качестве основного материала. Кроме того, у вас уже может быть изделие из алюминия, и вас просто интересуют электрические свойства этого популярного металла. В зависимости от вашего конкретного приложения электрические свойства материала могут быть важным фактором при проектировании.
Эта статья даст вам представление о том, как работает электропроводность, как легко электричество проходит через алюминий и чем этот металл отличается от других хорошо известных проводников, таких как медь.
Содержание
Является ли алюминий хорошим электрическим проводником?
Электричество определяется в очень сжатой форме как физическое явление потока электрического заряда. С субатомной точки зрения это означает поток электронов от одного атома к другому, что создает цепной эффект, который мы называем электрическим током.
Материалы, атомы которых позволяют электронам легко проходить через них, известны как хорошие проводники электричества, тогда как материалы, затрудняющие этот поток, являются плохими проводниками. Есть также материалы, атомы которых отказываются пропускать электроны, которые мы называем изоляторами.
В целом алюминий занимает четвертое место по электропроводности среди известных металлов. В этом списке первое и третье места занимают серебро и золото соответственно, которые слишком дороги для большинства обычных приложений. Таким образом, мы можем сказать, что алюминий занимает второе место среди наиболее доступных в практическом смысле проводящих материалов после меди.
Как объясняется в нашей статье «Марки алюминия», существует множество различных алюминиевых сплавов, классифицированных по классам или сериям, и каждый из них будет иметь разную электропроводность. Сплавы серий 1ХХХ, 6ХХХ и 8ХХХ обладают наилучшей электропроводностью среди алюминиевых сплавов.
Какие приложения используют алюминий в качестве электрического проводника?
Медь, вероятно, первый материал, который приходит на ум большинству людей, когда они думают о проводниках. Эта реакция понятна, поскольку медь является отличным выбором для многих применений. Однако алюминий уже давно используется и в энергетике.
Эта реакция понятна, поскольку медь является отличным выбором для многих применений. Однако алюминий уже давно используется и в энергетике.
Алюминий все чаще используется в качестве проводника для коммунальных сетей после окончания Второй мировой войны. Хотя медь показывает лучшую проводимость по объему, алюминий имеет значительные преимущества в весе и стоимости. Алюминиевый проводник весит в два раза меньше, чем эквивалентный медный проводник. Эти преимущества делают алюминий предпочтительным материалом для проводов передачи и распределения.
Лучшее отношение электропроводности к весу, которое демонстрирует алюминий по сравнению с медью, в последнее время поощряет его использование в электропроводке для жилых домов, самолетов, зданий и приборов.
Электрические шины, которые используются для распределения электроэнергии по различным цепям внутри здания, в настоящее время чаще всего изготавливаются из алюминия. Это часто делается, когда размер не является ограничением, но могут быть вес и стоимость меди.
Влияет ли алюминиевая отделка на электропроводность?
Выбор отделки поверхности алюминиевого изделия может сильно повлиять на электропроводность металла. Чтобы понять это, нам нужно рассмотреть естественный оксидный слой, который алюминий образует на своей поверхности.
Этот оксидный слой делает алюминий очень устойчивым к коррозии, что часто является желательным свойством. Однако слой оксида алюминия не проводит электричество; это изолятор. Учтите, что когда вы применяете обработку поверхности анодированием к алюминиевому изделию, оксидный слой становится намного толще. А последствием анодирования является то, что оно электрически изолирует нижележащий металл.
Другой типичной отделкой поверхности алюминиевых изделий является порошковое покрытие. Этот процесс придает алюминиевому изделию защитный и декоративный слой на поверхности, а также влияет на электропроводность. Полученный продукт по-прежнему будет иметь некоторую степень проводимости, поэтому он не станет изолированным, но он не будет таким проводящим, как чистый алюминий.
Если вы хотите узнать больше об этих двух типах обработки алюминиевой поверхности, вы можете прочитать нашу статью «Анодирование и порошковое покрытие».
Заключение
В целом, алюминий является отличным выбором для продуктов, которым требуются превосходные электрические проводники, вплоть до того, что во многих случаях он заменяет медь. Его превосходное отношение проводимости к весу и низкая стоимость делают его предпочтительным вариантом для все большего числа приложений, где важна электропроводность.
В конечном счете, выбор использования алюминия для электрических применений зависит от потребностей вашей конкретной конструкции.
Металлические субоксиды алюминия со сверхвысокой электропроводностью при высоком давлении
Алюминий, как самый распространенный металлический элемент, содержащийся в земной коре, обычно существует в форме оксида алюминия (Al 2 O 3 ). Однако степень окисления алюминия и кристаллические структуры оксидов алюминия в диапазоне давлений недр планет точно не установлены. Здесь мы предсказали два субоксида алюминия (Al 2 O, AlO) и два супероксида (Al 4 O 7 , AlO 3 ) с необычной стехиометрией при высоких давлениях с использованием расчетов из первых принципов и методов предсказания кристаллической структуры. Мы обнаружили, что P4/nmm Al 2 O становится стабильным при температуре выше ~765 ГПа и может сохраняться в глубоких слоях мантии или ядрах планет-гигантов, таких как Нептун. Интересно, что Al 2 O и AlO являются металлическими и имеют свойства электрида, в которых часть электронов локализована в междоузлиях между атомами. Мы находим, что Al 2 O имеет электропроводность на порядок выше, чем у железа при тех же термобарических условиях, что может влиять на общую проводимость планет-гигантов. Наши результаты дополняют фазовую диаграмму оксидов алюминия при высоком давлении и улучшают наше понимание внутренней структуры планет-гигантов.
Здесь мы предсказали два субоксида алюминия (Al 2 O, AlO) и два супероксида (Al 4 O 7 , AlO 3 ) с необычной стехиометрией при высоких давлениях с использованием расчетов из первых принципов и методов предсказания кристаллической структуры. Мы обнаружили, что P4/nmm Al 2 O становится стабильным при температуре выше ~765 ГПа и может сохраняться в глубоких слоях мантии или ядрах планет-гигантов, таких как Нептун. Интересно, что Al 2 O и AlO являются металлическими и имеют свойства электрида, в которых часть электронов локализована в междоузлиях между атомами. Мы находим, что Al 2 O имеет электропроводность на порядок выше, чем у железа при тех же термобарических условиях, что может влиять на общую проводимость планет-гигантов. Наши результаты дополняют фазовую диаграмму оксидов алюминия при высоком давлении и улучшают наше понимание внутренней структуры планет-гигантов.
1. Введение
Оксид алюминия – одно из самых распространенных веществ в мантии и ядре планет [1–5].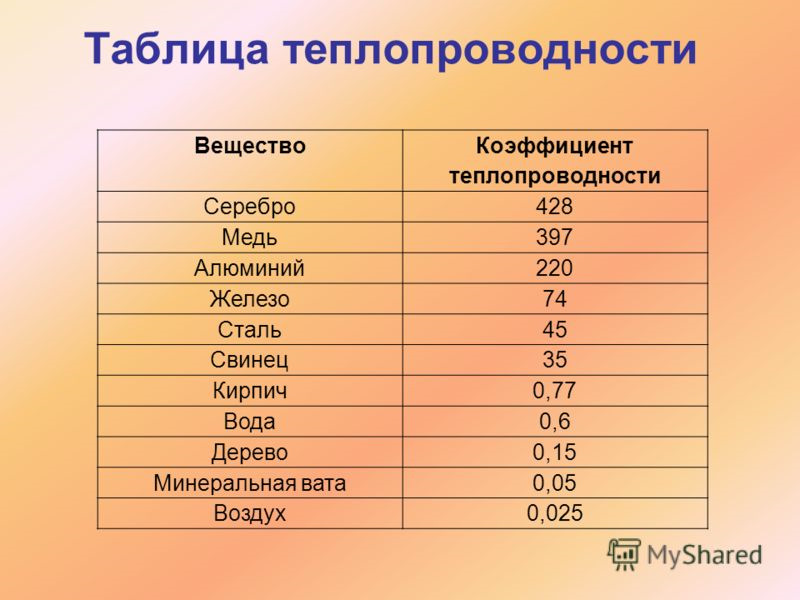 Что касается других основных составляющих планет, таких как железо [6, 7], кремнезем [8] и вода [9], изучение оксида алюминия и его свойств при высоких давлениях необходимо для понимания структуры, формирования и эволюции планет [10–12]. Как наиболее распространенный оксид алюминия, оксид алюминия (Al 2 O 3 ) обладает высокой твердостью, хорошими тепловыми и диэлектрическими свойствами, что делает его важным промышленным сырьем для абразивных и огнеупорных материалов и т. д. В качестве оконного материала в ударно-волновых экспериментов и один из основных компонентов мантии Земли, он также имеет большое значение как в технике высоких давлений [13], так и в геофизике [3]. Структурные фазовые переходы и химическая стабильность глинозема напрямую влияют на свойства планетарных ядер, такие как уравнение состояния, термоупругие свойства, электропроводность и окисление. Исследования при высоких давлениях, как теоретические, так и экспериментальные, позволили получить сложную фазовую диаграмму оксида алюминия [1–5, 14, 15].
Что касается других основных составляющих планет, таких как железо [6, 7], кремнезем [8] и вода [9], изучение оксида алюминия и его свойств при высоких давлениях необходимо для понимания структуры, формирования и эволюции планет [10–12]. Как наиболее распространенный оксид алюминия, оксид алюминия (Al 2 O 3 ) обладает высокой твердостью, хорошими тепловыми и диэлектрическими свойствами, что делает его важным промышленным сырьем для абразивных и огнеупорных материалов и т. д. В качестве оконного материала в ударно-волновых экспериментов и один из основных компонентов мантии Земли, он также имеет большое значение как в технике высоких давлений [13], так и в геофизике [3]. Структурные фазовые переходы и химическая стабильность глинозема напрямую влияют на свойства планетарных ядер, такие как уравнение состояния, термоупругие свойства, электропроводность и окисление. Исследования при высоких давлениях, как теоретические, так и экспериментальные, позволили получить сложную фазовую диаграмму оксида алюминия [1–5, 14, 15]. В свою очередь возникает последовательность фазовых переходов под давлением в глиноземе: корунд () → Rh 2 O 3 -TYPE ( PBCN ) → Каир 3 -TYPE ( CMCM ) → U 2 S 3 -TYPE ( PNMA ). В то же время два других стабильных соединения Al-O (AlO 2 и Al 4 O 7 ) были предсказаны первопринципным исследованием при высоком давлении [16]. В целом, все эти вышеупомянутые оксиды алюминия являются изолирующими с широкой запрещенной зоной.
В свою очередь возникает последовательность фазовых переходов под давлением в глиноземе: корунд () → Rh 2 O 3 -TYPE ( PBCN ) → Каир 3 -TYPE ( CMCM ) → U 2 S 3 -TYPE ( PNMA ). В то же время два других стабильных соединения Al-O (AlO 2 и Al 4 O 7 ) были предсказаны первопринципным исследованием при высоком давлении [16]. В целом, все эти вышеупомянутые оксиды алюминия являются изолирующими с широкой запрещенной зоной.
В то время как возможные кристаллические структуры оксида алюминия были тщательно исследованы в диапазоне давлений мантии и ядра Земли [1–5, 14, 15], у нас все еще есть ограниченные знания о соединениях, и структуры оксидов алюминия могут образовываться при более экстремальные условия, особенно в недрах планет-гигантов, таких как Юпитер, Сатурн, Уран и Нептун [11, 12, 17], где существуют гораздо более высокие температуры и давления. Текущие наблюдения Урана и Нептуна ограничены, и для соответствия этим данным были разработаны различные модели, в том числе модели с преобладанием льда и скалы. По сравнению с моделями с преобладанием льда, модели с преобладанием горных пород дают простое объяснение образования Нептуна [18]. Однако остается открытым вопрос о том, что формирование планетарных динамо [10, 19] требуются электропроводящие материалы. В связи с этим сообщается, что океан магмы в суперземлях может вносить вклад в магнитное поле, если его электропроводность достаточно высока. Например, для нескольких обычных мантийных соединений, таких как силикаты [20] и глинозем [21], уже было показано, что их электропроводность значительно увеличивается после плавления при экстремально высоких температурах. Кроме того, ударно-волновые эксперименты с кремнеземом показывают, что он может стать проводящим при давлении более 500 ГПа и 9000 К [8].
По сравнению с моделями с преобладанием льда, модели с преобладанием горных пород дают простое объяснение образования Нептуна [18]. Однако остается открытым вопрос о том, что формирование планетарных динамо [10, 19] требуются электропроводящие материалы. В связи с этим сообщается, что океан магмы в суперземлях может вносить вклад в магнитное поле, если его электропроводность достаточно высока. Например, для нескольких обычных мантийных соединений, таких как силикаты [20] и глинозем [21], уже было показано, что их электропроводность значительно увеличивается после плавления при экстремально высоких температурах. Кроме того, ударно-волновые эксперименты с кремнеземом показывают, что он может стать проводящим при давлении более 500 ГПа и 9000 К [8].
Помимо соединений мантии, недавние эксперименты по ударному сжатию показали, что вода и аммиак становятся ионно-проводящими при высоких давлениях, присутствующих в области генерации динамо ледяных гигантов [22, 23]. Кроме того, ожидается, что проводимость водородно-водных смесей будет быстро увеличиваться с глубиной во внешних слоях ледяных гигантов [24], где генерация вторичных магнитных полей, пространственно коррелирующих с зональными ветрами, может пролить свет на профили электропроводности солнечных системных гигантов вообще [25, 26]. Тем не менее, градиенты состава и, следовательно, профили электропроводности ледяных гигантов до сих пор неясны. Поэтому поиск новых структур оксидов алюминия как одного из важных компонентов каменистого ядра и/или мантии планет может улучшить наше понимание электропроводности планет-гигантов.
Тем не менее, градиенты состава и, следовательно, профили электропроводности ледяных гигантов до сих пор неясны. Поэтому поиск новых структур оксидов алюминия как одного из важных компонентов каменистого ядра и/или мантии планет может улучшить наше понимание электропроводности планет-гигантов.
Чтобы обогатить наше понимание физических свойств недр планеты, мы систематически исследовали кристаллические структуры оксида алюминия и другие возможные стехиометрии системы Al-O в диапазоне давлений, ожидаемом в планетарных ядрах, используя методы предсказания кристаллической структуры и первый принцип. расчеты. Здесь мы сообщаем о предсказании нескольких новых субоксидов и супероксидов алюминия с различной стехиометрией, включая Al 2 O, AlO, Al 4 O 7 и AlO 3 вместе с новой фазой высокого давления Al 2 O 3 . Наиболее важно то, что два из этих новых оксидов алюминия, Al 2 O и AlO, являются металлическими. Мы находим, что электропроводность Al 2 O выше, чем у ГПУ-железа в условиях давления и температуры вблизи границы мантии ядра Нептуна (если такая граница существует), что указывает на то, что это может влиять на планетарную электропроводность.
Мы находим, что электропроводность Al 2 O выше, чем у ГПУ-железа в условиях давления и температуры вблизи границы мантии ядра Нептуна (если такая граница существует), что указывает на то, что это может влиять на планетарную электропроводность.
Поиск кристаллической структуры системы Al-O под высоким давлением был выполнен с помощью MAGUS [27] (универсальный поиск структуры с помощью машинного обучения и теории графов), который был ускорен за счет использования байесовской оптимизации и теории графов [28]. Этот метод успешно применялся во многих системах под высоким давлением, например, в соединениях внутри планет [29–32]. Кроме того, мы перепроверили результаты поиска с помощью AIRSS [33, 34] в сочетании с CASTEP [35]. Расчеты DFT были выполнены с использованием программы Vienna 9.0067 Пакет моделирования Ab initio (VASP) [36] вместе с методом проекционно-дополненных волн (PAW) [37]. Моделирование молекулярной динамики Ab initio было выполнено с ансамблями NVT и NPT с использованием кубических суперячеек и периодических граничных условий. Ионную температуру контролировали с помощью термостата Нозе-Гувера [38, 39]. Моделирование в ансамбле NVT выполнялось в течение 10 пс с ионным временным шагом 1 фс, и 10 конфигураций были извлечены отдельно по времени на 0,8 пс за последние 8 пс, что гарантирует их статистическую нерелевантность. Мы приняли среднее значение проводимости этих ионных конфигураций в качестве электропроводности системы. Все электропроводности рассчитывались по формуле Кубо-Гринвуда, реализованной в коде Kg4vasp [40, 41]. Более подробную информацию о методе можно найти в дополнительных материалах.
Ионную температуру контролировали с помощью термостата Нозе-Гувера [38, 39]. Моделирование в ансамбле NVT выполнялось в течение 10 пс с ионным временным шагом 1 фс, и 10 конфигураций были извлечены отдельно по времени на 0,8 пс за последние 8 пс, что гарантирует их статистическую нерелевантность. Мы приняли среднее значение проводимости этих ионных конфигураций в качестве электропроводности системы. Все электропроводности рассчитывались по формуле Кубо-Гринвуда, реализованной в коде Kg4vasp [40, 41]. Более подробную информацию о методе можно найти в дополнительных материалах.
Мы тщательно искали возможные стехиометрии в системе Al-O при давлении до 2000 ГПа, которое может быть достигнуто в экспериментах с ударными волнами [42]. Результаты обобщены на рисунках 1 (а) и 1 (б). Для Al 2 O 3 мы обнаружили тетрагональную структуру с симметрией P4/mbm , что расширяет наши знания о структуре оксида алюминия при терапаскальных давлениях. Энтальпийные расчеты показывают, что эта структура P4/mbm более стабильна, чем структура U 2 S 3 — глинозем типа выше 1560 ГПа, как показано на рис. S1(a). Фононные расчеты демонстрируют отсутствие мнимых мод при 1600 ГПа, см. рис. S4(a), что подтверждает надежную динамическую стабильность этой фазы P4/mbm при экстремальном давлении. В отличие от описанных ранее структур оксида алюминия [5], эта фаза P4/mbm не имеет смешанных координационных чисел. В то время как фаза P4/mbm имеет аналогичную решетку атомов Al с U 2 S 3 -фаза, обе средние длины связей Al 1 -O/Al 2 -O уменьшаются с 1,69 Å/1,45 Å до 1,55 Å/1,44 Å, когда фазовый переход происходит при 1560 ГПа, образуя алюминиевые полиэдры с координационным числом 8, а не смесью 7 и 8 в фазе типа U 2 S 3 .
S1(a). Фононные расчеты демонстрируют отсутствие мнимых мод при 1600 ГПа, см. рис. S4(a), что подтверждает надежную динамическую стабильность этой фазы P4/mbm при экстремальном давлении. В отличие от описанных ранее структур оксида алюминия [5], эта фаза P4/mbm не имеет смешанных координационных чисел. В то время как фаза P4/mbm имеет аналогичную решетку атомов Al с U 2 S 3 -фаза, обе средние длины связей Al 1 -O/Al 2 -O уменьшаются с 1,69 Å/1,45 Å до 1,55 Å/1,44 Å, когда фазовый переход происходит при 1560 ГПа, образуя алюминиевые полиэдры с координационным числом 8, а не смесью 7 и 8 в фазе типа U 2 S 3 .
Помимо Al 2 O 3 , нами также идентифицированы оксиды алюминия необычной стехиометрии, в том числе Al 2 O, AlO, Al 4 O 7 и AlO 3 . Статические расчеты энтальпии образования и расчеты фононов свидетельствуют о термодинамической и динамической стабильности Al 2 O выше 765 ГПа, см. рис. S2(a) и рис. S5(a). Он образует фазу P4/nmm во всем исследованном нами диапазоне давлений. Интересно, что структура P4/nmm Al 2 O аналогична добавлению атомов O в ОЦК фазу алюминия, в которой добавление атомов O расширяет -ось ОЦК решетки атомов Al на 50 % по сравнению с -осью. Как показано на рис. 1(d), неравномерное распределение атомов O вынуждает некоторые атомы Al образовывать квадратные сетки, расположенные на плоскости ab. Соединение AlO на рис. 1(e) становится термодинамически и динамически стабильным и сохраняет P6 3 /mmc выше 1890 ГПа, как показано на рис. S2(b) и рис. S6(a). Атомы Al образуют ГПУ-решетку, а не ОЦК-решетку, хотя в чистом алюминии ОЦК-фаза является наиболее стабильной при этом давлении. Соединение AlO 3 становится стабильным и сохраняет структуру выше 1260 ГПа, см. рис. S2(c) и рис. S7(a). AlO 3 на рисунке 1(f) содержит алюминиевые полиэдры с координационным числом 12, которое является самым большим известным координационным числом в Al-O.
рис. S2(a) и рис. S5(a). Он образует фазу P4/nmm во всем исследованном нами диапазоне давлений. Интересно, что структура P4/nmm Al 2 O аналогична добавлению атомов O в ОЦК фазу алюминия, в которой добавление атомов O расширяет -ось ОЦК решетки атомов Al на 50 % по сравнению с -осью. Как показано на рис. 1(d), неравномерное распределение атомов O вынуждает некоторые атомы Al образовывать квадратные сетки, расположенные на плоскости ab. Соединение AlO на рис. 1(e) становится термодинамически и динамически стабильным и сохраняет P6 3 /mmc выше 1890 ГПа, как показано на рис. S2(b) и рис. S6(a). Атомы Al образуют ГПУ-решетку, а не ОЦК-решетку, хотя в чистом алюминии ОЦК-фаза является наиболее стабильной при этом давлении. Соединение AlO 3 становится стабильным и сохраняет структуру выше 1260 ГПа, см. рис. S2(c) и рис. S7(a). AlO 3 на рисунке 1(f) содержит алюминиевые полиэдры с координационным числом 12, которое является самым большим известным координационным числом в Al-O. Аль 4 O 7 , показанный на рис. S1 (b-d), образует фазу и фазу Cmcm от 850 ГПа до 1500 ГПа и 2000 ГПа соответственно.
Аль 4 O 7 , показанный на рис. S1 (b-d), образует фазу и фазу Cmcm от 850 ГПа до 1500 ГПа и 2000 ГПа соответственно.
Кроме того, мы исследовали их физические свойства, в частности, уравнение состояния и электронные свойства. Как показано на рисунке 2, в диапазоне давлений от 1 ТПа до 2 ТПа плотность фазы оксида алюминия P4/mbm лишь немного выше, чем у оксида алюминия типа U 2 S 3 . Однако, в отличие от U 2 S 3 , ширина запрещенной зоны фазы P4/mbm оксида алюминия намного меньше, уменьшаясь с 5,21 эВ до 3,28 эВ при 1,6 ТПа. Что касается Al 2 O, результаты расчетов плотности состояния позволяют предположить, что он является металлическим (см. рис. 2(c)). Полосы, пересекающие уровень Ферми (), в основном состоят из d-орбиталей атомов Al, а электроны проводимости, занимающие электронные состояния вблизи, обладают связующим распределением между двумя слоями атомов Al, как показано на рис. S11. Кроме того, ELF в плоскости (110), показанный на рисунке 2(e), показывает, что P4/nmm Al 2 O по аналогии с электридами высокого давления [43, 44] состоит из ионных остовов и локализованной электронной плотности. По результатам анализа заряда Бейдера, представленным в табл. S1 атомы Al теряют почти все валентные электроны, а атомы O получают около 1,7 электрона на атом. Остальные электроны (около 3,55 е) локализованы в междоузлиях между двумя слоями атомов Al, образуя связанную область локализации электронов, совпадающую с распределением электронов проводимости. Это говорит о том, что каналы локализации электронов, состоящие из d-орбиталей атомов Al, вносят вклад в металличность P4/nmm Al 2 O. Кроме того, P6 3 /mmc AlO является металлическим и имеет свойства электрида, которые хорошо видны на рисунках 2(d) и 2(f). В отличие от P4/nmm Al 2 O область электронной локализации P6 3 /mmc AlO изолирована.
S11. Кроме того, ELF в плоскости (110), показанный на рисунке 2(e), показывает, что P4/nmm Al 2 O по аналогии с электридами высокого давления [43, 44] состоит из ионных остовов и локализованной электронной плотности. По результатам анализа заряда Бейдера, представленным в табл. S1 атомы Al теряют почти все валентные электроны, а атомы O получают около 1,7 электрона на атом. Остальные электроны (около 3,55 е) локализованы в междоузлиях между двумя слоями атомов Al, образуя связанную область локализации электронов, совпадающую с распределением электронов проводимости. Это говорит о том, что каналы локализации электронов, состоящие из d-орбиталей атомов Al, вносят вклад в металличность P4/nmm Al 2 O. Кроме того, P6 3 /mmc AlO является металлическим и имеет свойства электрида, которые хорошо видны на рисунках 2(d) и 2(f). В отличие от P4/nmm Al 2 O область электронной локализации P6 3 /mmc AlO изолирована. Только около 0,03 электрона собираются в области с центрами (0,667 0,333 0,75) и (0,333 0,667 0,25) с образованием псевдоанионов.
Только около 0,03 электрона собираются в области с центрами (0,667 0,333 0,75) и (0,333 0,667 0,25) с образованием псевдоанионов.
Начиная с P4/nmm Al 2 O и P6 3 /mmc AlO являются металлическими, мы исследовали значения их электропроводности и сравнили их с таковой ГПУ-фазы железа [7, 45], которая является основным компонентом ядра Земли и оказывает значительное влияние на динамо Земли. Для расчета электропроводности ГПУ-железа в условиях ядра Земли было использовано несколько методов моделирования [6, 46, 47]. Здесь мы использовали метод молекулярной динамики Ab initial в сочетании с формулой Кубо-Гринвуда [40, 41]. Мы рассчитали электропроводность ГПУ-железа при 150 ГПа в диапазоне 1000-4000 К вместе с ГПУ-железом и P4/нмм Al 2 O при 800 ГПа в диапазоне 2000-8000 K.С учетом влияния температуры на кристаллическую решетку в рамках ансамбля NVT было выполнено AIMD-моделирование. Влияние размера моделирующей ячейки на электропроводность было протестировано с использованием 128, 150 и 250 атомов железа (см. рис. S12). Для железа в ГПУ-фазе наша расчетная электропроводность при 150 ГПа согласуется с результатами эксперимента при 157 ГПа, о которых сообщают Ohta et al. [7], подтвердив возможность реализации данного метода расчета. Более того, с повышением температуры длина свободного пробега электрона будет уменьшаться вплоть до межатомного расстояния (так называемое условие Иоффе-Регеля), что приводит к эффектам насыщения удельного сопротивления [48]. Это является причиной того, что электропроводность как железа, так и Al 2 O сходятся к константе при более высокой температуре, как ясно показано на рисунке 3. Самое главное, как показано в таблице 1, мы обнаружили, что электропроводность Al 2 O при 800 ГПа намного выше, чем у железа в интервале температур 2000-8000 К.Значения электропроводности AlO при 1,9 ТПа и Al 2 O при 800 ГПа находятся в одном порядке.
рис. S12). Для железа в ГПУ-фазе наша расчетная электропроводность при 150 ГПа согласуется с результатами эксперимента при 157 ГПа, о которых сообщают Ohta et al. [7], подтвердив возможность реализации данного метода расчета. Более того, с повышением температуры длина свободного пробега электрона будет уменьшаться вплоть до межатомного расстояния (так называемое условие Иоффе-Регеля), что приводит к эффектам насыщения удельного сопротивления [48]. Это является причиной того, что электропроводность как железа, так и Al 2 O сходятся к константе при более высокой температуре, как ясно показано на рисунке 3. Самое главное, как показано в таблице 1, мы обнаружили, что электропроводность Al 2 O при 800 ГПа намного выше, чем у железа в интервале температур 2000-8000 К.Значения электропроводности AlO при 1,9 ТПа и Al 2 O при 800 ГПа находятся в одном порядке.
| ||||||||||||||||||||||||||||||||
With such high electrical conductivities, the aluminum suboxides could possibly influence the total conductivities of the planetary interior, which makes it necessary исследовать распределение этих недавно обнаруженных субоксидов алюминия внутри планет. Таким образом, мы моделируем эволюцию этих соединений при конечных температурных условиях в квазигармоническом приближении. Рассчитанные кривые свободной энергии Гиббса могут помочь нам судить о наиболее стабильной фазе при конечной температуре. Мы суммировали наши расчеты до 10 000 K на рисунке 4, который представляет фазовую диаграмму сверхвысокого давления-температуры кристалла оксида алюминия и других кристаллов оксидов алюминия. Для Аль 2 O 3 фаза типа U 2 S 3 напрямую переходит в фазу P4/mbm при ~1560 ГПа и проявляет меньшую чувствительность к температуре. Для других стехиометрий в системе Al-O все они демонстрируют хорошую термическую стабильность и не будут разлагаться до 10 000 K, что также согласуется с нашими перекрестными проверками с моделированием AIMD.
Для Аль 2 O 3 фаза типа U 2 S 3 напрямую переходит в фазу P4/mbm при ~1560 ГПа и проявляет меньшую чувствительность к температуре. Для других стехиометрий в системе Al-O все они демонстрируют хорошую термическую стабильность и не будут разлагаться до 10 000 K, что также согласуется с нашими перекрестными проверками с моделированием AIMD.
Кроме того, адиабатические геотермы (фиолетовые и красные квадраты), предложенные для суперземли, также представлены на рисунке 4, чтобы проиллюстрировать условия давление-температура на границе ядра и мантии (CMB) по отношению к различным моделям планет [12]. Когда масса планеты увеличится до 4 M ⊕ , оксид алюминия типа U 2 S 3 может обрести стабильность как внутри земных, так и океанических формирующих суперземли. Что касается других оксидов, то P2 1 /c AlO 2 может существовать в ядре планет земной группы, а также планет-океанов между ~3 M ⊕ и ~6 M ⊕ , /nmm Al 2 Ожидается, что O появится на планетах земной группы с массой более 6 M ⊕ и планетах-океанах с массой более 7 M ⊕ . Для планет Солнечной системы условия температуры и давления на границе их ядра и мантии (CMB) плохо определены и зависят от модели [11, 17]. Граница мантии ядра Нептуна охватывает стабильные условия температуры и давления P4/nmm Al 2 O, что предполагает их возможное появление в недрах Нептуна. Кроме того, образование оксида алюминия AlO 3 , P4/mbm и P6 3 /mmc AlO встречаются при гораздо более высоком давлении и могут существовать в глубоких недрах Юпитера и Сатурна (см. рис. S13).
Для планет Солнечной системы условия температуры и давления на границе их ядра и мантии (CMB) плохо определены и зависят от модели [11, 17]. Граница мантии ядра Нептуна охватывает стабильные условия температуры и давления P4/nmm Al 2 O, что предполагает их возможное появление в недрах Нептуна. Кроме того, образование оксида алюминия AlO 3 , P4/mbm и P6 3 /mmc AlO встречаются при гораздо более высоком давлении и могут существовать в глубоких недрах Юпитера и Сатурна (см. рис. S13).
Приведенные выше рассуждения о стабильности этих неожиданных оксидов алюминия указывают на возможную широко распространенную связь с недрами планет. Однако на основании теории динамо [49, 50] сообщается, что необходимы как конвекция жидкости, так и электропроводность. При таких экстремальных давлениях субоксиды алюминия не могут плавиться ниже 10000 K, что исключает конвекцию и возможность самостоятельно генерировать магнитное поле. Тем не менее, высокая электропроводность Al 2 O может косвенно влиять на общую электропроводность планетарного ядра и магнитных полей. Например, они могут влиять на эволюцию и распределение проводящих соединений в недрах планет и способствовать формированию мультидипольности в магнитном поле планет-гигантов.
Например, они могут влиять на эволюцию и распределение проводящих соединений в недрах планет и способствовать формированию мультидипольности в магнитном поле планет-гигантов.
В заключение, мы исследуем структуры системы Al-O при экстремальном давлении до терапаскального диапазона и предсказываем основное состояние фазы P4/mbm Al 2 O 3 и несколько соединений субоксидов и супероксидов алюминия. P4/nmm Al 2 O может выжить на границе ядра и мантии Урана и Нептуна, в то время как AlO 3 , P4/mbm Al 2 O 3 и 67 P 3 /mmc AlO может существовать в недрах внешних планет Солнечной системы, а также в экзопланетах суперземли. Эти предсказания могли быть подтверждены ударно-волновыми экспериментами [8, 42]. Кроме того, мы находим, что P4/nmm Al 2 O и P6 3 /mmc AlO являются металлами и обладают интересными свойствами в качестве электридов. В условиях планетарного ядра или мантии электрическая проводимость P4/нмм Al 2 O составляет около Ом -1 м -1 , что почти на порядок выше, чем у железа при том же давлении- температурный режим, который может быть важен для понимания планетарной проводимости.
В условиях планетарного ядра или мантии электрическая проводимость P4/нмм Al 2 O составляет около Ом -1 м -1 , что почти на порядок выше, чем у железа при том же давлении- температурный режим, который может быть важен для понимания планетарной проводимости.
Доступность данных
Данные, подтверждающие графики в этой статье, и другие результаты этого исследования можно получить у соответствующего автора по обоснованному запросу.
Конфликт интересов
CJP является автором кода CASTEP и получает лицензионные отчисления от своих коммерческих продаж компанией Dassault Systemes.
Благодарности
Дж.С. выражает благодарность за финансовую поддержку Национального фонда естественных наук Китая (гранты № 12125404, 11974162 и 11834006) и фондов фундаментальных исследований центральных университетов. Расчеты проводились с использованием суперкомпьютеров Центра высокопроизводительных вычислений Совместного инновационного центра передовых микроструктур, высокопроизводительного суперкомпьютерного центра Нанкинского университета.
Supplementary Materials
Рис. S1: (a) энтальпии фаз Al 2 O 3 относительно структуры типа U 2 S 3 в диапазоне давлений от 300 00 ГПа до 0,0 ГПа. (б) Энтальпии фаз Al 4 O 7 относительно структуры Cmcm в диапазоне давлений от 800 ГПа до 2000 ГПа. Кристаллические структуры Al 4 O 7 (в) и Cmcm Al 4 O 7 (г) на 900 и 1500 ГПа соответственно. Красные и серебряные сферы обозначают атомы кислорода и алюминия соответственно. Рисунок S2: выпуклые оболочки для P4/nmm Al 2 O (a), P6 3 /mmc AlO (b), AlO 3 (c), и Cmcm Al 4 O 7 структур (г) соответственно. Рисунок S3: выпуклые оболочки для P4/nmm Al 2 O с использованием различных методов. Рисунок S4: фононная дисперсия и структура электронных зон P4/mbm Al 2 O 3 при 1600 ГПа. Рисунок S5: Фононная дисперсия и электронные зонные структуры P4/nmm Al 2 O при 800 ГПа. Рисунок S6: фононная дисперсия и электронные зонные структуры P6 3 /mmc AlO при 2 ТПа. Рисунок S7: Фононная дисперсия и электронные зонные структуры AlO 3 при 1300 ГПа. Рисунок S8: Фононная дисперсия и электронные зонные структуры Al 4 O 7 при 1000 ГПа. Рисунок S9: фононная дисперсия и электронные зонные структуры Cmcm Al 4 O 7 . Рисунок S10: уравнение состояния (a) и ширина запрещенной зоны (b) вновь обнаруженных оксидов алюминия. Рисунок S11: проекция зонной структуры и проекция зон, пересекающих уровень Ферми, для P4/nmm Al 2 O (а, б) и P6 3 /mmc AlO (в, г) в реальном пространстве. Рисунок S12: зависимость электропроводности от температуры ГПУ-железа в условиях ядра Земли. Рисунок S13: предлагаемые фазовые диаграммы давление-температура оксидов алюминия до 4 ТПа и 16000 K. AlO 3 становится стабильным в области II. Рисунок S14: результаты прогнозирования структуры переменного состава при 2 ТПа.
Рисунок S6: фононная дисперсия и электронные зонные структуры P6 3 /mmc AlO при 2 ТПа. Рисунок S7: Фононная дисперсия и электронные зонные структуры AlO 3 при 1300 ГПа. Рисунок S8: Фононная дисперсия и электронные зонные структуры Al 4 O 7 при 1000 ГПа. Рисунок S9: фононная дисперсия и электронные зонные структуры Cmcm Al 4 O 7 . Рисунок S10: уравнение состояния (a) и ширина запрещенной зоны (b) вновь обнаруженных оксидов алюминия. Рисунок S11: проекция зонной структуры и проекция зон, пересекающих уровень Ферми, для P4/nmm Al 2 O (а, б) и P6 3 /mmc AlO (в, г) в реальном пространстве. Рисунок S12: зависимость электропроводности от температуры ГПУ-железа в условиях ядра Земли. Рисунок S13: предлагаемые фазовые диаграммы давление-температура оксидов алюминия до 4 ТПа и 16000 K. AlO 3 становится стабильным в области II. Рисунок S14: результаты прогнозирования структуры переменного состава при 2 ТПа.


 53
53