Увеличиваются ли молекулы при нагревании? / Хабр
Все мы знаем, что если надуть пластиковую бутылку горячим воздухом, крепко-накрепко закрыть крышкой, а потом охладить, то бутылка сожмётся. Причина этого лежит в физике 8-го класса, или, если точнее, в законе Гей-Люссака, утверждающем, что отношение объёмов при разных температурах равно отношению абсолютных температур. То есть ещё со школьных времён (а может и раньше) нам всем известно, что при нагревании некоторого количества газа его объём увеличивается, а при охлаждении — уменьшается.
А что насчёт того, из чего этот газ состоит? Увеличивается ли объём самих частичек газа, то есть размер атомов и молекул? Банальный ответ на этот банальный вопрос под катом.
Ха-ха, попались!
Ответ на этот вопрос весьма прост: как мы определим
размер частиц (что такое размер атома/молекулы в зависимости от температуры), такой ответ мы и получим. Поскольку атомы по-своей сути — это одноатомные молекулы, то дальше мы будем называть все эти частицы единым термином «молекула«.
Поскольку атомы по-своей сути — это одноатомные молекулы, то дальше мы будем называть все эти частицы единым термином «молекула«.
Если взять бутылку с газом, и из этой бутылки взять одну единственную молекулу, то окажется, что для неё не возможно (по-честному) даже принципиально измерить температуру. Частица находится в каком-то конкретном (квантовом) состоянии, которое мы можем определить и измерить, но при этом мы не сможем засунуть ей в в неё термометр и узнать сколько там у неё градусов. Связанно это с тем, что «температура» — это свойство макроскопических (т.е. больших) систем, состоящих из большого числа частиц. А значит если молекул в системе мало, то и измерять у этой системы нечего. «Большое число частиц», конечно, это плавающее понятие, но обычно оно измеряется в молях, или в числах Авогадро (), поэтому очевидно, что одна молекула горааааздо меньше этого порядка величин, а значит само понятие температуры не применимо к одной, двум, да даже десяти молекулам.
Что такое температура?
Но что вообще такое температура? Ещё со школы мы знаем, что есть т.н. абсолютная температура T, измеряемая в градусах Кельвина. Именно она стоит во всех газовых законах, в частности в уравнении Менделеева-Клайперона.
Для забывших, как выглядит уравнение Менделеева-Клайперона
Это уравнение имеет вид , где P — давление, V — объём, n — количество вещества (в молях), R = 8.314 Дж/(моль · К) — универсальная газовая постоянная, а T — абсолютная температура в Кельвинах (К).
Абсолютная температура связанна с относительной температурой t, измеряемой в градусах Цельсия, как , и абсолютный ноль (T=0, или же ) — это недостижимая величина. Ещё всем в голову вбивают мантру:
абсолютная температура является мерой средней кинетической энергии молекул.
Но эта мантра не объясняет, что же именно из себя представляет температура.
Попробуем разобраться. Начнём с простого примера. Закроем глаза и представим себе Африку: жаркую, солнечную, заполненную равнинными саваннами, и с горой Килиманджаро торчащей посередине. А ещё там есть слоны.
Каждый слон имеет определённую (большую) массу, и поэтому любое поднятие своей туши из равнинной местности в горную — это большая затрата энергии.
Представим, что слоны голодные, поэтому энергии у них мало. Будучи слоном, я бы в таком состоянии не попёрся бы в гору, а тусовался бы в саванне. В горы бы я ходил только по очень-очень большой нужде. В результате, если бы мы сняли фотографию Африки со спутника, она бы выглядела примерно так, как показано на картинке ниже: много-много слонов на равнине, и очень мало смелых и отчаянных в горах, причём, чем выше — меньше вероятность найти слона.
А теперь представим, что слоны хорошенько поели, да ещё какой-нибудь [Роскомнадзор] ещё для скорости им в еду подсыпали, так что энергии у слонов много. В этом случае, что равнина, что гора, слоны будут туда переться без особой устали, поэтому теперь вероятность отыскать слона на равнине и в горах будет отличаться уже меньше, чем в предыдущем примере (см. картинку ниже), хотя всё ещё будет сохраняться правило: чем выше на гору — тем меньше слонов.
В этом случае, что равнина, что гора, слоны будут туда переться без особой устали, поэтому теперь вероятность отыскать слона на равнине и в горах будет отличаться уже меньше, чем в предыдущем примере (см. картинку ниже), хотя всё ещё будет сохраняться правило: чем выше на гору — тем меньше слонов.
Эти два примера весьма точно иллюстрируют случаи газа с низкой (первый) и высокой (второй) температурой. У каждой молекулы (слона) есть какая-то своя энергия, в нашем примере — это гравитационная энергия , где m — масса, g = 9.8 м/c2 — ускорение свободного падения, а h — высота над равниной. Из энергии каждой конкретной частицы (места, где нашли слона) мы не можем ничего сказать о том, как всех слонов покормили в целом, но именно то, сколько на всех выделили еды, или другими словами, сколько энергии вкачали в среднем во всю систему, даст нам распределение слонов по ландшафту Африки. Собственно, температура в наших примерах — это общая величина накормленности всех слонов во всей Африке.
Распределение Больцмана
Собственно, распределение Больцмана имеет вид:
где n(E) — это число частиц с энергией E, R — универсальная газовая постоянная (см. предыдущий спойлер), а T, само собой, температура.
В примере же со слонами мы иллюстрировали т.н. барометрическую формулу: частный случай распределения Больцмана, показывающий как меняется давление газа с увеличением высоты:
где P(h) — это давление на высоте h, , а M — это молярная масса газа.
Растут ли атомы от температуры?
Теперь, собственно, можно перейти к вопросу: а растут ли, например, атомы при росте температуры. Само собой, каждый конкретный атом находится в каком-то квантовом состоянии, поэтому от температуры его размер не зависит, но вот средний размер всех атомов в сосуде с газом от той самой температуры зависеть уже будет.
Представим себе, например, атом водорода: тяжёлый протон, а вокруг него летает электрон. Поскольку протон положительный, а электрон отрицательный, то один притягивает другой по закону Кулона, который выглядит точно так же как ньютоновская гравитация, поэтому в этом смысле атом вполне себе напоминает, например, Солнце и Землю, летающую вокруг него. Только, как говорит нам (далеко не полностью удачная, см. например, тут) атомная модель Бора, в отличие от системы «звезда + планета», электрон летает вокруг ядра только по орбитам определённого радиуса.
Так или иначе, чем больше энергии мы закачиваем в атом водорода, тем более широкая орбита будет доступна электрону для полёта вокруг ядра.![]()
Из неё видно, что чтобы начать замечать хоть какие-то изменения в размере электронной оболочки, нужно ооочень сильно нагреть атом (в данном случае до более 10000 градусов). Это в целом общий тренд.
Как была посчитана эта зависимость
Подробнее о формулах можно узнать в этом посте.
Если кратко, то радиус орбиты (R) в зависимости от главного квантового числа n=1,2,3… — это
где R0=5.3×10−11 метра − это боровский радиус. Энергия (E) же орбиты имеет вид
где Eh= 4. 3597447222071(85)×10−18 Джоулей − это энергия Хартри.
3597447222071(85)×10−18 Джоулей − это энергия Хартри.
Далее используя распределение Больцмана для одной частицы, мы можем посчитать среднее значение радиуса от температуры как
Знаменатель у нас появляется из-за того, что полная вероятность всех исходов измерений должна быть равна единице.
Иными словами,
ответ на вопрос поста: да, при нагревании электронные оболочки атомов (и молекул) в среднем расширяются. Но, это увеличение очень маленькое, и требует нагрева до очень высоких температур, к которым мы в обыденной жизни не привыкли.
Растут ли молекулы от температуры?
Теперь зададимся вопросом: а что если наша молекула составлена не из одного, а из двух, трёх или более атомов? Можем ли мы что-то сказать о межатомных расстояниях в ней, как ведут они себя при повышении температуры? Для простоты, естественно, ограничимся двухатомными молекулами, кои, в частности, составляют как минимум 98.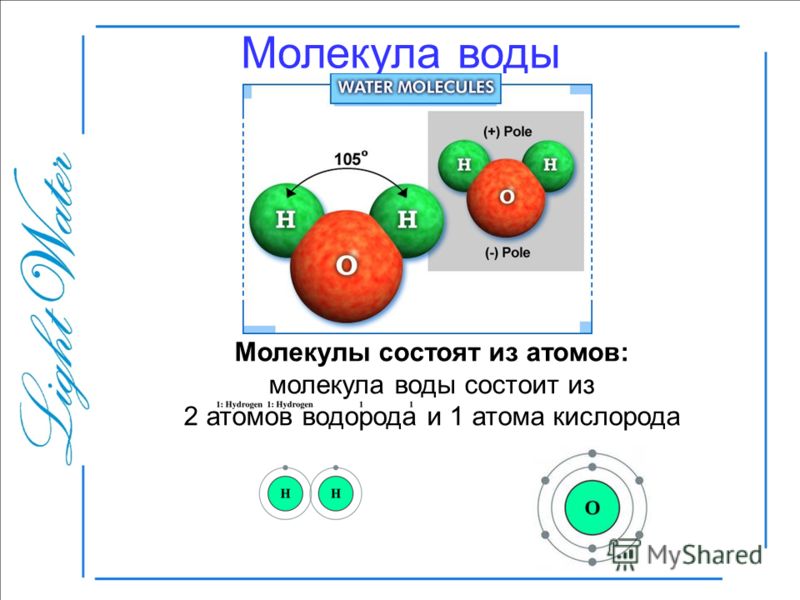
У нас есть один атом, у нас есть второй атом: ммммм, и расстояние между ними, обозначим его как R. Как ведёт себя потенциальная энергия взаимодействия этих атомов в зависимости от R?
- Если мы разведём атомы оооочень далеко друг от друга, то химическая связь между ними давно будет разорвана. Поэтому особой разницы от того, что расстояние мы увеличим от «очень много» до «очень много и ещё чуть-чуть», мы не заметим. Иными словами при R → ∞ у нас должна быть горизонтальная асимптота.
- Если же, наоборот, мы будем пытаться впихнуть один атом в другой (R → 0), то в какой-то момент мы выгоним из пространства между этими атомами все электроны, ибо те не идиоты, чтобы тусоваться в токсичной высокоэнергетической атмосфере, и у нас останутся два голых положительно заряженных ядра, отталкивающиеся друг от друга через Кулоновскую силу. Т.е. при R → 0 у нас будет вертикальная асимптота, стремящая потенциальную энергию взаимодействия атомов в высокоэнергетическую бесконечность.

- Ну и, логично, что не будь какого-то минимума на этой потенциальной кривой между R=0 и R → ∞, то самих молекул о которых мы говорим, не существовало бы.
В итоге мы понимаем, что кривая потенциальной энергии взаимодействия имеет следующий вид:
Атомы в молекуле всегда колеблются, даже при абсолютном нуле, когда никакой лишней энергии не осталось. Из-за принципа неопределённости они не могут просто скатиться в минимальную по энергии точку на потенциале и сдохнуть лежать, свернувшись калачиком: им приходится совершать т.н. нулевые колебания. Если же энергия у них выше, то и колеблются они с большей амплитудой. Поэтому возникает вопрос: а как конкретно колеблются атомы?
Если бы слева и справа от точки минимума потенциал был одинаков, как, например, в случае закона Гука, то атомы во время колебаний отклонялись бы в область малых значений межатомных расстояний ровно то же количество времени, сколько и в область больших значений.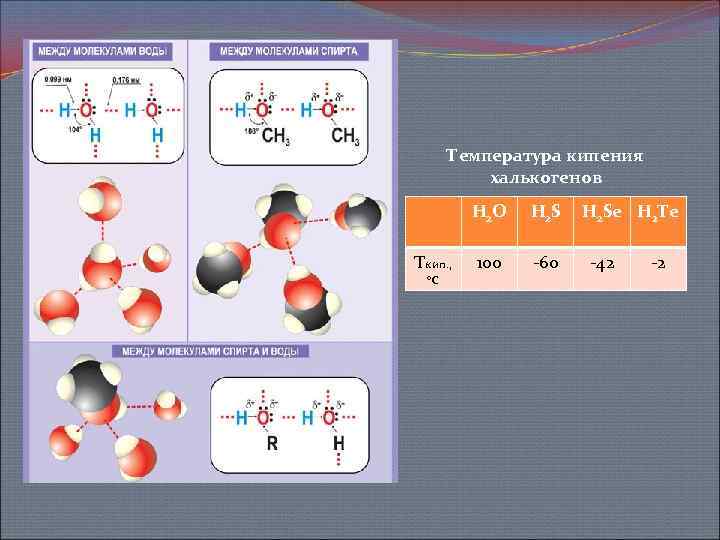 В этом случае бы среднее значение межатомного расстояния при любой температуре было бы равно значению расстояния в точке минимума. Иными словами, если бы мы взяли газ, и в любой момент времени сфоткали все молекулы, а потом посчитали бы среднее значение для всех расстояний между атомами, то в итоге получили бы расстояние в точке минимума.
В этом случае бы среднее значение межатомного расстояния при любой температуре было бы равно значению расстояния в точке минимума. Иными словами, если бы мы взяли газ, и в любой момент времени сфоткали все молекулы, а потом посчитали бы среднее значение для всех расстояний между атомами, то в итоге получили бы расстояние в точке минимума.
Но реальность у нас другая: слева от точки минимума (при R → 0) у молекулы стоит жёсткая стенка, а справа (при R → ∞) — мягкий диван. Вопрос: где будет больше времени проводить молекула: долбиться о стенку, или валяться на диване? Правильно: конечно на диване. Иными словами, распределение расстояний в молекуле, что при абсолютном нуле, что при какой-то температуре, будет несимметричным, поэтому среднее значение расстояний будет сдвинуто в сторону больших расстояний относительно минимального. Мало того, при повышении температуры, т.е. когда мы будем закачивать больше кинетической энергии в систему, увеличивая амплитуду колебаний, молекула будет видеть гораздо более жёсткую стенку, и гораздо более мягкий диван. Поэтому среднее значение межатомных расстояний будет расти с ростом температуры, а значит и средний размер молекул, причём всех, не только двухатомных, будет увеличиваться.
Поэтому среднее значение межатомных расстояний будет расти с ростом температуры, а значит и средний размер молекул, причём всех, не только двухатомных, будет увеличиваться.
К сожалению, чтобы посчитать этот рост среднего расстояния, потребуется много больше усилий, чем в случае атома водорода. Но можно пойти другим путём, и поискать, а не исследовался ли этот вопрос в экспериментах?
И порывшись на просторах этих наших Интернетов, можно набрести на следующую работу: J. Chem. Phys. 79, 170 (1983). В ней делали эксперимент буквально описанный выше:
- брали кучу молекул углекислого газа (CO2) и нагревали их до разных температур, в диапазоне температур от комнатной (300 K ≈ 25oC) до «ай как горячо» (1000 К ≈ 730oC ),
- при каждой выбранной температуре делали «фотку» всех молекул при помощи электронов (этот метод зовётся газовой электронографией, о нём можно немного почитать здесь),
- ну а дальше буквально измеряли средние значения для межатомных расстояний на каждой фотке.

В результате они, в частности, получили следующую зависимость средней длины двойной связи C=O в молекуле углекислого газа (O=C=O):
Из графика видно, что при нагреве от комнатной температуры до 1000 градусов К это среднее значение выросло почти на 0.004 Å (1 ангстрем, Å, = 10—10 метров). Конечно, в наших привычных величинах это очень мало, но сама длина связи C=O в этой молекуле составляет 1.2 Å, так что это рост на почти 0.3 %! Вполне себе заметная величина при нагреве, достижимом привычными средствами (например, газовой плитой).
Зачем это вообще знать?
Да хотя бы просто ради любопытства. Разве не прикольно поспорить с коллегой на чашку кофе, что при нагреве контейнера с едой в микроволновке помимо объёма газа увеличится и размер частиц газа? Ну и в практическом смысле это тоже важно. Все эти температурные расширения/уменьшения всяких макроскопических объектов, таких как рельсы, провода линий электропередач, да даже крышки банки под горячей водой, работают ровно по тому же механизму, что и для молекул газа: средние межатомные расстояния увеличиваются, т. к. в систему при увеличении температуры закачивается больше энергии движения частиц. И по-моему, осознание того, что за такими обыденными явлениями стоят такие нетривиальные процессы, вдохновляет на новые подвиги и свершения.
к. в систему при увеличении температуры закачивается больше энергии движения частиц. И по-моему, осознание того, что за такими обыденными явлениями стоят такие нетривиальные процессы, вдохновляет на новые подвиги и свершения.
Всех благ, и да пребудет с Вами межатомная сила.
Почему вода расширяется при замерзании?
Общие знания
17.06.2021
16 274 2 минут чтения
Когда вода замерзает, ее молекулы выстраиваются в кристаллическую структуру, тем самым приобретая определенную форму. Эта кристаллическая структура менее плотная, и поскольку между отдельными молекулами в структуре есть промежутки, общий объем увеличивается, и вода «расширяется».
С беглого взгляда фраза «вода расширяется, когда она замерзает» может не иметь смысла, потому что в жидкой форме вода не имеет определенной формы или очертаний и поэтому, кажется, занимает больше места. Кроме того, когда вода замерзает, она принимает четко определенную форму, которая кажется совершенно противоположной «расширению».
Действительно ли вода расширяется при замерзании?
Да, вода расширяется при замерзании. Обратите внимание, что слово «расширяется» в этом предложении означает увеличение объема. Поэтому технически правильно было бы сказать так: объем воды увеличивается при замерзании.
Это утверждение является точным, и вы можете проверить его правомерность с помощью простого эксперимента: если вы снизите температуру воды, вы заметите, что объем воды уменьшается, поскольку она становится все более и более «нетронутой».
Вы можете обратиться к следующей диаграмме, чтобы представить эту зависимость графически:
Обратите внимание, что объем воды начинает увеличиваться при понижении температуры ниже 4 градусов Цельсия.Теперь давайте поговорим о том, почему увеличивается объем воды или почему она расширяется, когда замерзает и достигает твердой формы.
Почему объем воды увеличивается, когда она замерзает?
Это явление связано с химическим составом воды. Видите ли, молекула воды состоит из двух атомов водорода и одного атома кислорода. Расположение этих атомов совершенно уникально, что придает воде некоторые особые свойства, такие как высокая теплоемкость воды, поверхностное натяжение, адгезия и когезия.
Расположение этих атомов совершенно уникально, что придает воде некоторые особые свойства, такие как высокая теплоемкость воды, поверхностное натяжение, адгезия и когезия.
Является ли вода полярной или неполярной?
Химическая структура молекулы воды.Такое расположение молекулы воды создает положительно заряженную сторону возле атомов водорода и отрицательно заряженную сторону возле атома кислорода.
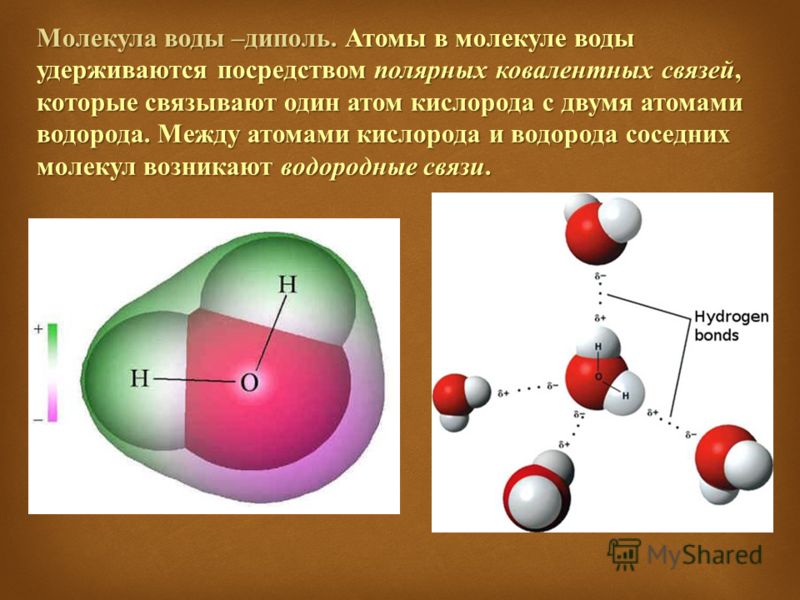
Когда две молекулы воды сближаются, положительная сторона одной молекулы цепляется за отрицательную сторону другой молекулы. Когда это происходит в больших масштабах (т.е. с миллионами молекул воды), получается уникальная структура, которая объясняет некоторые химические свойства воды.
В жидком состоянии молекулы воды могут свободно перемещаться, образуя и разрывая водородные связи, что объясняет неправильную форму воды (или любой другой жидкости, если на то пошло). Некоторые молекулы воды часто «уложены» друг на друга, что объясняет более высокую плотность воды по сравнению со льдом.
Расположение молекул воды в жидком состоянии.
Однако по мере снижения температуры и охлаждения воды межмолекулярные силы увеличиваются, свобода движения молекул воды уменьшается, и они становятся все менее энергичными (с понижением температуры).
Когда вода достигает точки замерзания, движение ее молекул становится незначительным, и они приобретают более определенную форму, располагаясь в виде шестигранных решеток.
Ниже приведен упрощенный вариант расположения молекул воды в кристаллической форме во льду:
Расположение молекул воды в твердой форме.Это кристаллическое расположение молекул воды менее плотное, поскольку оно не позволяет молекулам скапливаться (как это происходит в жидкой форме) из-за более сильных межмолекулярных сил.
Такое расстояние между молекулами и их фиксация в таком положении увеличивает объем воды, поэтому говорят, что вода расширяется при замерзании.
Почему лед плавает по воде
Вода расширяется, когда становится льдом, и, поскольку объем обратно пропорционален плотности вещества, лед менее плотен, чем вода. По этой причине лед, вещество, которое кажется более тяжелым, чем его жидкая форма, плавает на воде.
По этой причине лед, вещество, которое кажется более тяжелым, чем его жидкая форма, плавает на воде.
Если бы вода не расширялась при замерзании, лед был бы плотнее воды. Подумайте о влиянии на экосистему планеты! Лед на поверхности озер, морей и океанов утонет, и эти водоемы будут постепенно заполняться снизу вверх. С замерзшими озерами и океанами на Земле не было бы водной жизни.
С этой точки зрения очень хорошо, что вода расширяется в твердой форме!
Подпишитесь на нас:Дзен.Новости / Вконтакте / Telegram
Back to top button
(-1))Вопрос
Обновлено: 26/04/2023
NCERT FINGERTIPS-КИНЕТИЧЕСКАЯ ТЕОРИЯ-Поведение газов
20 видеоРЕКЛАМА
Текстовое решение
900 02 А3×10-28м3
B
3×10−29м3
C
1,5×10−28м3
D
1,5×10−29м3
Ответ
Правильный ответ: B
Решение
Молекулярная масса воды = 28
∴ Количество молекул в 18 г
или 0,018 кг воды =6×1023
∴ Масса молекулы воды =0,0186×1023=3×10−26
∴ Объем молекулы воды
=Плотность массы=3×10−261000=3×10−29м3
Ответьте
Пошаговое решение, разработанное экспертами, которое поможет вам избавиться от сомнений и получить отличные оценки на экзаменах.
Ab Padhai каро бина объявления ке
Khareedo DN Pro и дехо сари видео бина киси объявление ки rukaavat ке!
Видео по теме
Лодка плывет по воде, и три четверти ее объема находятся внутри воды. Плотность воды 103 кг/м3, найдите плотность материала лодки. 9(3) . Оцените размер («в» Å) молекулы воды.
12009397
Плотность воды при 4°C составляет 1,0×103 кгм−3. Объем, занимаемый одной молекулой воды, приблизительно равен (NA=6,0×1023):
16007350
्रिज्या ज्ञात कीजिये। जल का घनत्व 1000kg m3लीजिए।
234024732
जल का घनत्व 1000 кг м−3 है। 100∘C और 1 атм दाब पर जलवाष्प का घनत्व 0,6 кг м−3 है। एक अणु के आयतन को कुल अणुओं की संख्या से गुणा क रने पर हमें आण्विक आयतन प्राप्त होता है। ताप और दाब की उपरोक्त अवस्था में जलवाष्प के कु ल आयतन और इसके आण्विक आयतन का अनुपात ज्ञात कीजि ये। 923 .
376772278
Образец молока состоит из чистого молока (плотность = 1080 кг/м3), разбавленного водой (плотность = 1000 кг/м3) и имеет плотность 1042 кг/м3. Рассчитайте процентное содержание воды в молоке.
Рассчитайте процентное содержание воды в молоке.
415573615
एक मोल जल वाष्प का STP पर अणुओं द्वार ा घेरा गया वास्तविक आयतन है (अर्थात् एवोगेड्रो संख्या x एक अणु का आयतन)
555774145
वक्तव्य I जल के प्रति घन सेमी में अणुओं की संख्या लगभग 13×1022 изображение ी है।
वक्तव्य II जल के 1 मोल में अणुओं की संख्या, आवोग ाद्रो संख्या C=6,023×1023 /ग्राम मोल के बराबर होती है। 9(-3) . Объем, занимаемый одной молекулой воды, приблизительно равен
644811033
Text Solution
Плотность воды | Глава 3: Плотность
- Скачать
- Электронная почта
- Печать
- Добавить в закладки или поделиться
Тебе это нравится? Не нравится ? Пожалуйста, найдите время, чтобы поделиться с нами своими отзывами. Спасибо!
Урок 3.3
Ключевые понятия
- Так же, как и твердые тела, жидкости также имеют свою плотность.

- Объем жидкости можно измерить непосредственно мерным цилиндром.
- Молекулы разных жидкостей имеют разный размер и массу.
- Масса и размер молекул в жидкости и то, насколько плотно они упакованы вместе, определяют плотность жидкости.
- Как и твердое тело, плотность жидкости равна массе жидкости, деленной на ее объем; Д = м/об.
- Плотность воды 1 грамм на кубический сантиметр.
- Плотность вещества одинакова независимо от размера образца.
Резюме
Учащиеся измеряют объем и массу воды, чтобы определить ее плотность. Затем они измеряют массу различных объемов воды и обнаруживают, что плотность всегда одинакова. Учащиеся строят график зависимости объема и массы воды.
Цель
Учащиеся смогут измерить объем и массу воды и рассчитать ее плотность. Учащиеся смогут объяснить, что, поскольку любой объем воды всегда имеет одинаковую плотность при данной температуре, эта плотность является характерным свойством воды.
Оценка
Загрузите лист с заданиями учащегося и раздайте по одному учащемуся, если это указано в задании. Рабочий лист будет служить компонентом «Оценить» каждого плана урока 5-E.
Безопасность
Убедитесь, что вы и ваши ученики носите правильно подобранные очки.
Материалы для каждой группы
- Градуированный цилиндр, 100 мл
- Вода
- Весы в граммах (могут измерять более 100 г)
- Пипетка
Материалы для демонстрации
- Вода
- Два одинаковых ведра или больших контейнера
Проведите демонстрацию, чтобы представить идею плотности воды.
Материалы
- Вода
- Два одинаковых ведра или больших контейнера
Подготовка учителей
Наполните одно ведро наполовину, а в другое добавьте примерно 1 стакан воды.
Процедура
- Выберите ученика, который поднимет оба ведра с водой.

- Спросите у студента-добровольца, какое ведро имеет большую массу.
Ожидаемые результаты
Ведро, в котором больше воды, имеет большую массу.
Спросите студентов:
- В уроках 3.1 — Что такое плотность? и 3.2 — Метод вытеснения воды, вы нашли плотность твердых тел, измерив их массу и объем. Как вы думаете, может ли жидкость, например вода, иметь плотность?
- Учащиеся должны понять, что вода имеет объем и массу. Поскольку D=m/v, вода также должна иметь плотность.
- Как, по-вашему, можно найти плотность такой жидкости, как вода?
- На данном этапе учащиеся не смогут полностью ответить на этот вопрос. Он задуман как повод к расследованию. Но учащиеся могут понять, что сначала им нужно каким-то образом найти массу и объем воды.
- Могут ли маленькое и большое количество воды, поднятые вашим одноклассником, иметь одинаковую плотность?
- Учащиеся могут указать, что ведро с большим количеством воды имеет большую массу, но больший объем.
 Ведро с меньшей массой имеет меньший объем. Поэтому возможно, что разное количество воды может иметь одинаковую плотность.
Ведро с меньшей массой имеет меньший объем. Поэтому возможно, что разное количество воды может иметь одинаковую плотность.
Раздайте каждому учащемуся лист с заданиями.
Учащиеся записывают свои наблюдения и отвечают на вопросы о задании в листе задания. Разделы «Объясните это с помощью атомов и молекул» и «Воспримите это» в листе с заданиями будут выполняться в классе, в группах или индивидуально в зависимости от ваших инструкций. Посмотрите на версию листа с заданиями для учителя, чтобы найти вопросы и ответы.
Обсудите с учащимися, как найти объем и массу воды.
Скажите учащимся, что они попытаются определить плотность воды.
Спросите студентов:
- Какие две вещи нужно знать, чтобы найти плотность воды?
- Учащиеся должны понимать, что им нужны как объем, так и масса образца воды, чтобы найти ее плотность.
- Как можно измерить объем воды?
- Предложите учащимся использовать мерный цилиндр для измерения объема в миллилитрах.
 Напомните учащимся, что каждый миллилитр равен 1 см 3 .
Напомните учащимся, что каждый миллилитр равен 1 см 3 . - Как можно измерить массу воды?
- Предложите учащимся использовать весы для измерения массы в граммах. Скажите учащимся, что они могут найти массу, взвесив воду. Однако, поскольку вода является жидкостью, она должна находиться в каком-то контейнере. Таким образом, чтобы взвесить воду, они также должны взвесить контейнер. Объясните учащимся, что им придется вычесть массу пустого мерного цилиндра из массы цилиндра и воды, чтобы получить массу только воды.
Предложите учащимся найти массу различных объемов воды, чтобы показать, что плотность воды не зависит от размера образца.
Вопрос для расследования
Имеют ли разное количество воды одинаковую плотность?
Материалы для каждой группы
- Градуированный цилиндр, 100 мл
- Вода
- Весы в граммах (могут измерять более 100 г)
- Пипетка
Процедура
- Найдите массу пустого мерного цилиндра.
 Запишите массу в граммах в таблице на рабочем листе.
Запишите массу в граммах в таблице на рабочем листе. Налейте 100 мл воды в мерный цилиндр. Постарайтесь быть максимально точным, убедившись, что мениск находится прямо на отметке 100 мл. Используйте пипетку, чтобы добавить или удалить небольшое количество воды.
- Взвесьте мерный цилиндр с водой. Запишите массу в граммах.
- Найдите массу только воды, вычитая массу пустого градуированного цилиндра. Запишите массу 100 мл воды в таблицу.
- Используйте массу и объем воды для расчета плотности. Запишите плотность в г/см 3 в таблице.
- Сливайте воду, пока в мерном цилиндре не будет 50 мл воды. Если вы случайно вылили слишком много, добавляйте воду, пока не дойдете до 50 мл.
Найдите массу 50 мл воды. Запишите массу в лист активности. Рассчитайте и запишите плотность.
- Затем слейте воду, пока в мерном цилиндре не будет 25 мл воды. Найдите массу 25 мл воды и запишите ее в таблицу. Рассчитайте и запишите плотность.

Таблица 1. Нахождение плотности различных объемов воды. Объем воды 100 миллилитров 50 миллилитров 25 миллилитров Масса мерного цилиндра + вода (г) Масса пустого мерного цилиндра (г) Масса воды (г) Плотность воды (г/см 3 ) Ожидаемые результаты
Плотность воды должна быть близка к 1 г/см 3 . Это верно для 100, 50 или 25 мл.
Спросите студентов:
- Посмотрите на свои значения плотности в диаграмме.
 Одинакова ли плотность различных объемов воды?
Одинакова ли плотность различных объемов воды? - Помогите учащимся увидеть, что большинство различных значений плотности близки к 1 г/см 3 . Они могут задаться вопросом, почему не все их значения точно равны 1 г/см 3 . Одной из причин может быть неточность измерения. Другая причина заключается в том, что плотность воды меняется в зависимости от температуры. Вода имеет наибольшую плотность при 4 °C и при этой температуре имеет плотность 1 г/см 3 . При комнатной температуре, около 20–25 °C, плотность составляет около 0,99 г/см 3 .
- Какова плотность воды в г/см3?
- Ответы учащихся могут различаться, но в основном их значения должны быть около 1 г/см 3 .
Предложите учащимся начертить свои результаты.
Помогите учащимся построить график данных на листе с заданиями. По оси x должен быть объем, а по оси y масса.
Когда учащиеся наносят свои данные на график, должна быть прямая линия, показывающая, что при увеличении объема масса увеличивается на ту же величину.

Обсудите наблюдения учащихся, данные и графики.
Спросите студентов:
- Используйте свой график, чтобы найти массу 40 мл воды. Какова плотность этого объема воды?
- Масса 40 мл воды составляет 40 грамм. Поскольку D = m/v и mL = см 3 , плотность воды составляет 1 г/см 3 .
- Выберите объем от 1 до 100 мл. Используйте свой график, чтобы найти массу. Какова плотность этого объема воды?
- Независимо от того, весят ли ученики 100, 50, 25 мл или любое другое количество, плотность воды всегда будет равна 1 г/см 3 .
Скажите учащимся, что плотность – это характерное свойство вещества. Это означает, что плотность вещества одинакова независимо от размера образца.
Спросите студентов:
- Является ли плотность характерным свойством воды? Откуда вы знаете?
- Плотность является характеристическим свойством воды, поскольку плотность любой пробы воды (при одной и той же температуре) всегда одинакова.
 Плотность 1 г/см 3 .
Плотность 1 г/см 3 .
Объясните, почему плотность пробы воды любого размера всегда одинакова.
Спроецируйте изображение Плотность воды.
Молекулы воды имеют одинаковую массу и размер. Молекулы воды также упакованы довольно близко друг к другу. Они упакованы одинаково во всей пробе воды. Итак, если объем воды имеет определенную массу, удвоенный объем будет иметь удвоенную массу, трехкратный объем будет иметь трехкратную массу и т. д. Независимо от того, какой размер пробы воды вы измеряете, соотношение между массой и объемом всегда будет одинаковым. Поскольку D=m/v, плотность одинакова для любого количества воды.
Проект анимации «Жидкая вода».
Молекулы воды всегда в движении. Но в среднем они упакованы везде одинаково. Следовательно, соотношение между массой и объемом одинаково, что делает плотность одинаковой. Это верно независимо от размера выборки или места, откуда вы ее выбираете.
Предложите учащимся подумать, равна ли плотность большого куска твердого вещества плотности меньшего куска.

Дайте учащимся время рассчитать плотность каждого из трех образцов, нарисованных на листе с заданиями, и ответить на соответствующие вопросы.
Спросите студентов:
- Плотность жидкости одинакова независимо от размера образца. Может ли это быть верно и для твердых тел? Рассчитайте плотность каждого из трех образцов, чтобы выяснить это.
- Да. Плотность твердого вещества одинакова независимо от размера образца.
- Образец А имеет массу 200 г. Какова плотность образца А?
- Д = м/в
- D = 200 г/100 см 3
- D = 2 г/см 3
- Если вы разрежете образец A пополам и осмотрите только одну половину, вы получите образец B. Какова плотность образца B?
- Если учащиеся не знают, что такое масса, скажите им, что это половина массы образца A. Поскольку образец A весит 200 г, образец B составляет половину объема и, следовательно, половину массы (100 г).







 Ведро с меньшей массой имеет меньший объем. Поэтому возможно, что разное количество воды может иметь одинаковую плотность.
Ведро с меньшей массой имеет меньший объем. Поэтому возможно, что разное количество воды может иметь одинаковую плотность. Напомните учащимся, что каждый миллилитр равен 1 см 3 .
Напомните учащимся, что каждый миллилитр равен 1 см 3 . Запишите массу в граммах в таблице на рабочем листе.
Запишите массу в граммах в таблице на рабочем листе.
 Одинакова ли плотность различных объемов воды?
Одинакова ли плотность различных объемов воды?
 Плотность 1 г/см 3 .
Плотность 1 г/см 3 .
