Свойства воды в жидком состоянии. Видеоурок. Окружающий мир 3 Класс
Тема: Неживая природа
Урок: Свойства воды в жидком состоянии
В чистом виде вода не имеет вкуса, запаха и цвета, но она почти никогда не бывает такой, потому что активно растворяет в себе большинство веществ и соединяется с их частицами. Так же вода может проникать в различные тела (ученые нашли воду даже в камнях).

Рис. 1. Вода (Источник)
Если в стакан набрать воды из-под крана, она будет казаться чистой. Но на самом деле, это – раствор многих веществ, среди которых есть газы (кислород, аргон, азот, углекислый газ), различные примеси, содержащиеся в воздухе, растворенные соли из почвы, железо из водопроводных труб, мельчайшие нерастворенные частицы пыли и др.

Рис. 2. Вода в стакане (Источник)
Если нанести пипеткой капельки водопроводной воды на чистое стекло и дать ей испариться, останутся едва заметные пятнышки.

Рис. 3. Капли воды на стекле (Источник)
В воде рек и ручьев, большинства озер содержатся различные примеси, например, растворенные соли. Но их немного, потому что эта вода – пресная.

Рис. 4. Река (Источник)
Вода течет на земле и под землей, наполняет ручьи, озера, реки, моря и океаны, создает подземные дворцы.

Рис. 5. Подземная пещера (Источник)
Прокладывая себе путь сквозь легкорастворимые вещества, вода проникает глубоко под землю, унося их с собой, и через щелочки и трещинки в скальных породах, образуя подземные пещеры, капает с их свода, создавая причудливые скульптуры. Миллиарды капелек воды за сотни лет испаряются, а растворенные в воде вещества (соли, известняки) оседают на сводах пещеры, образуя каменные сосульки, которые называют сталактитами.

Рис. 6. Сталактиты (Источник)
Сходные образования на полу пещеры называются сталагмитами.

Рис. 7. Сталагмиты (Источник)
А когда сталактит и сталагмит срастается, образуя каменную колонну, это называют сталагнатом.

Рис. 8. Сталагнат (Источник)
Наблюдая ледоход на реке, мы видим воду в твердом (лед и снег), жидком (текущая под ним) и газообразном состоянии (мельчайшие частицы воды, поднимающиеся в воздух, которые ещё называют водяным паром).

Рис. 9. Ледоход на реке (Источник)
Вода может одновременно находится во всех трех состояниях: в воздухе всегда есть водяной пар и облака, которые состоят из капелек воды и кристалликов льда.

Рис. 10. Облако (Источник)
Водяной пар невидим, но его можно легко обнаружить, если оставить в теплой комнате охлаждавшийся в холодильнике в течение часа стакан с водой, на стенках которого сразу появятся капельки воды. При соприкосновении с холодными стенками стакана, водяной пар, содержащийся в воздухе, преобразуется в капельки воды и оседает на поверхности стакана.

По этой же причине в холодное время года запотевает внутренняя сторона оконного стекла. Холодный воздух не может содержать столько же водяного пара, сколько и теплый, поэтому какое-то его количество конденсируется – превращается в капельки воды.

Рис. 12. Запотевшее окно (Источник)
Белый след за летящим в небе самолетом – тоже результат конденсации воды.

Рис. 13. След за самолетом (Источник)
Если поднести к губам зеркальце и выдохнуть, на его поверхности останутся мельчайшие капельки воды, это доказывает то, что при дыхании человек вдыхает с воздухом водяной пар.
При нагревании вода «расширяется». Это может доказать простой опыт: в колбу с водой опустили стеклянную трубку и замерили уровень воды в ней; затем колбу опустили в сосуд с теплой водой и после нагревания воды повторно замерили уровень в трубке, который заметно поднялся, поскольку вода при нагревании увеличивается в объеме.
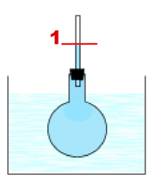
Рис. 14. Колба с трубкой, цифрой 1 и чертой обозначен первоначальный уровень воды
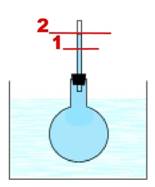
Рис. 15. Колба с трубкой, цифрой 2 и чертой обозначен уровень воды при нагревании
При охлаждении вода «сжимается». Это может доказать сходный опыт: в этом случае колбу с трубкой опустили в сосуд со льдом, после охлаждения уровень воды в трубке понизился относительно первоначальной отметки, потому что вода уменьшилась в объеме.
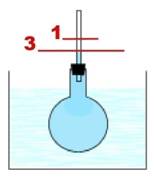
Рис. 16. Колба с трубкой, цифрой 3 и чертой обозначен уровень воды при охлаждении
Так происходит, потому что частицы воды, молекулы, при нагревании движутся быстрее, сталкиваются между собой, отталкиваются от стенок сосуда, расстояние между молекулами увеличивается, и поэтому жидкость занимает больший объем. При охлаждении воды движение её частиц замедляется, расстояние между молекулами уменьшается, и жидкости требуется меньший объем.

Рис. 17. Молекулы воды обычной температуры
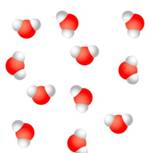
Рис. 18. Молекулы воды при нагревании

Рис. 19. Молекулы воды при охлаждении
Такими свойствами обладает не только вода, но и другие жидкости (спирт, ртуть, бензин, керосин).
Знание этого свойства жидкостей привело к изобретению термометра (градусника), где используется спирт или ртуть.

Рис. 20. Термометр (Источник)
При замерзании вода расширяется. Это можно доказать, если емкость, наполненную до краев водой, неплотно накрыть крышкой и поставить в морозильную камеру, через время мы увидим, что образовавшийся лед приподнимет крышку, выйдя за пределы емкости.
Это свойство учитывается при прокладывании водопроводных труб, которые обязательно утепляются, чтобы при замерзании образовавшийся из воды лед не разорвал трубы.
В природе замерзающая вода может разрушать горы: если осенью в трещинах скал скапливается вода, зимой она замерзает, и под напором льда, который занимает больший объем, чем вода, из которой он образовался, горные породы трескаются и разрушаются.
Вода, замерзающая в трещинах дорог, приводит к разрушению асфальтового покрытия.
Длинные гребни, напоминающие складки, на стволах деревьев – раны от разрывов древесины под напором замерзающего в ней древесного сока. Поэтому в холодные зимы можно услышать треск деревьев в парке или в лесу.
Список рекомендованной литературы
- Вахрушев А.А., Данилов Д.Д. Окружающий мир 3. М.: Баллас.
- Дмитриева Н.Я., Казаков А.Н. Окружающий мир 3. М.: ИД «Федоров».
- Плешаков А.А.Окружающий мир 3. М.: Просвещение.
Рекомендованные ссылки на ресурсы интернет
- Фестиваль педагогических идей (Источник).
- Наука и образование (Источник).
- Открытый класс (Источник).
Рекомендованное домашнее задание
- Составьте короткий тест (4 вопроса с тремя вариантами ответа) на тему «Вода вокруг нас».
- Проведите небольшой опыт: стакан с очень холодной водой поставьте на стол в теплой комнате. Опишите, что будет происходить, объясните, почему.
- *Нарисуйте движение молекул воды в нагретом, нормальном и охлажденном состоянии. Если нужно, сделайте подписи на своем рисунке.
Предложена новая теория, объясняющая, почему вода при нагревании от 0 до 4°C сжимается
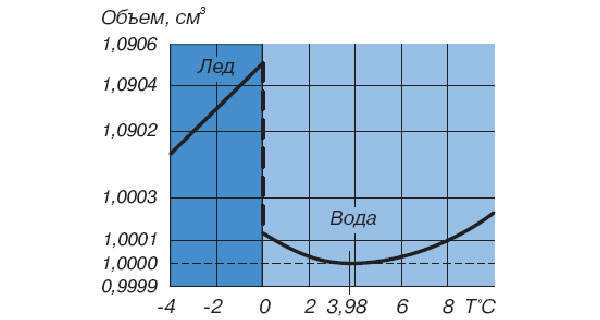
Японский физик Масакадзу Мацумото выдвинул теорию, которая объясняет, почему вода при нагревании от 0 до 4°C сжимается, вместо того чтобы расширяться. Согласно его модели, вода содержит микрообразования — «витриты», представляющие собой выпуклые пустотелые многогранники, в вершинах которых находятся молекулы воды, а ребрами служат водородные связи. При повышении температуры конкурируют между собой два явления: удлинение водородных связей между молекулами воды и деформация витритов, приводящая к уменьшению их полостей. В диапазоне температур от 0 до 3,98°C последнее явление доминирует над эффектом удлинения водородных связей, что в итоге и дает наблюдаемое сжатие воды. Экспериментального подтверждения модели Мацумото пока что нет — впрочем, как и других теорий, объясняющих сжатие воды.
В отличие от подавляющего большинства веществ, вода при нагревании способна уменьшать свой объем (рис. 1), то есть обладает отрицательным коэффициентом теплового расширения. Впрочем, речь идет не обо всём температурном интервале, где вода существует в жидком состоянии, а лишь об узком участке — от 0°C примерно до 4°C. При больших температурах вода, как и другие вещества, расширяется.
Между прочим, вода — не единственное вещество, имеющее свойство сжиматься при увеличении температуры (или расширяться при охлаждении). Подобным поведением могут «похвастать» еще висмут, галлий, кремний и сурьма. Тем не менее, в силу своей более сложной внутренней структуры, а также распространенности и важности в разнообразных процессах, именно вода приковывает внимание ученых (см. Продолжается изучение структуры воды, «Элементы», 09.10.2006).
Некоторое время назад общепринятой теорией, отвечающей на вопрос, почему вода увеличивает свой объем при понижении температуры (рис. 1), была модель смеси двух компонент — «нормальной» и «льдоподобной». Впервые эта теория была предложена в XIX веке Гарольдом Витингом и позднее была развита и усовершенствована многими учеными. Сравнительно недавно в рамках обнаруженного полиморфизма воды теория Витинга была переосмыслена. Отныне считается, что в переохлажденной воде существует два типа льдообразных нанодоменов: области, похожие на аморфный лед высокой и низкой плотности. Нагревание переохлажденной воды приводит к плавлению этих наноструктур и к появлению двух видов воды: с большей и меньшей плотностью. Хитрая температурная конкуренция между двумя «сортами» образовавшейся воды и порождает немонотонную зависимость плотности от температуры. Однако пока эта теория не подтверждена экспериментально.
С приведенным объяснением нужно быть осторожным. Не случайно здесь говорится лишь о структурах, которые напоминают аморфный лед. Дело в том, что наноскопические области аморфного льда и его макроскопические аналоги обладают разными физическими параметрами.
Японский физик Масакадзу Мацумото решил найти объяснение обсуждаемого здесь эффекта «с нуля», отбросив теорию двухкомпонентной смеси. Используя компьютерное моделирование, он рассмотрел физические свойства воды в широком диапазоне температур — от 200 до 360 К при нулевом давлении, чтобы в молекулярном масштабе выяснить истинные причины расширения воды при ее охлаждении. Его статья в журнале Physical Review Letters так и называется: Why Does Water Expand When It Cools? («Почему вода при охлаждении расширяется?»).
Изначально автор статьи задался вопросом: что влияет на коэффициент теплового расширения воды? Мацумото считает, что для этого достаточно выяснить влияние всего трех факторов: 1) изменения длины водородных связей между молекулами воды, 2) топологического индекса — числа связей на одну молекулу воды и 3) отклонения величины угла между связями от равновесного значения (углового искажения).
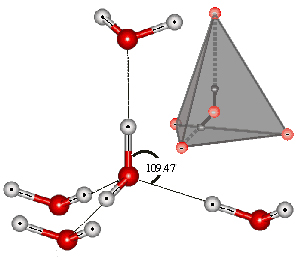
Перед тем как рассказать о результатах, полученных японским физиком, сделаем важные замечания и разъяснения по поводу вышеупомянутых трех факторов. Прежде всего, привычная химическая формула воды H2O соответствует лишь парообразному ее состоянию. В жидкой форме молекулы воды посредством водородной связи объединяются в группы (H2O)x, где x — количество молекул. Наиболее энергетически выгодно объединение из пяти молекул воды (x = 5) с четырьмя водородными связями, в котором связи образуют равновесный, так называемый тетраэдральный угол, равный 109,47 градуса (см. рис. 2).
Проанализировав зависимость длины водородной связи между молекулами воды от температуры, Мацумото пришел к ожидаемому выводу: рост температуры рождает линейное удлинение водородных связей. А это, в свою очередь, приводит к увеличению объема воды, то есть к ее расширению. Сей факт противоречит наблюдаемым результатам, поэтому далее он рассмотрел влияние второго фактора. Как коэффициент теплового расширения зависит от топологического индекса?
Компьютерное моделирование дало следующий результат. При низких температурах наибольший объем воды в процентном отношении занимают кластеры воды, у которых на одну молекулу приходится 4 водородных связи (топологический индекс равен 4). Повышение температуры вызывает уменьшение количества ассоциатов с индексом 4, но при этом начинает возрастать число кластеров с индексами 3 и 5. Проведя численные расчеты, Мацумото обнаружил, что локальный объем кластеров с топологическим индексом 4 с повышением температуры практически не меняется, а изменение суммарного объема ассоциатов с индексами 3 и 5 при любой температуре взаимно компенсирует друг друга. Следовательно, изменение температуры не меняет общий объем воды, а значит, и топологический индекс никакого воздействия на сжатие воды при ее нагревании не оказывает.
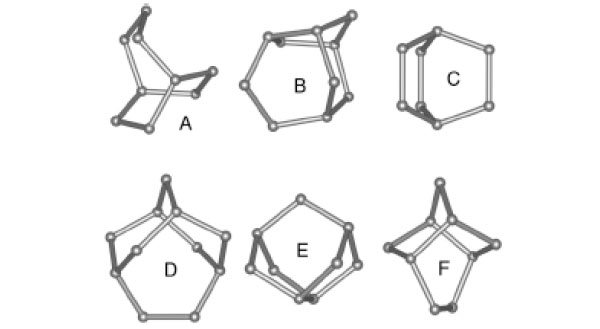
Остается выяснить влияние углового искажения водородных связей. И вот здесь начинается самое интересное и важное. Как было сказано выше, молекулы воды стремятся объединиться так, чтобы угол между водородными связями был тетраэдральным. Однако тепловые колебания молекул воды и взаимодействия с другими молекулами, не входящими в кластер, не дают им этого сделать, отклоняя величину угла водородной связи от равновесного значения 109,47 градуса. Чтобы как-то количественно охарактеризовать этот процесс угловой деформации, Мацумото с коллегами, основываясь на своей предыдущей работе Topological building blocks of hydrogen bond network in water, опубликованной в 2007 году в Journal of Chemical Physics, выдвинули гипотезу о существовании в воде трехмерных микроструктур, напоминающих выпуклые полые многогранники. Позднее, в следующих публикациях, такие микроструктуры они назвали витритами (рис. 3). В них вершинами являются молекулы воды, роль ребер играют водородные связи, а угол между водородными связями — это угол между ребрами в витрите.
Согласно теории Мацумото, существует огромное разнообразие форм витритов, которые, как мозаичные элементы, составляют большую часть структуры воды и которые при этом равномерно заполняют весь ее объем.
Молекулы воды стремятся создать в витритах тетраэдральные углы, поскольку витриты должны обладать минимально возможной энергией. Однако из-за тепловых движений и локальных взаимодействий с другими витритами некоторые микроструктуры не обладают геометрией с тетраэдральными углами (или углами, близкими к этому значению). Они принимают такие структурно неравновесные конфигурации (не являющиеся для них самыми выгодными с энергетической точки зрения), которые позволяют всему «семейству» витритов в целом получить наименьшее значение энергии среди возможных. Такие витриты, то есть витриты, которые как бы приносят себя в жертву «общим энергетическим интересам», называются фрустрированными. Если у нефрустрированных витритов объем полости максимален при данной температуре, то фрустрированные витриты, напротив, обладают минимально возможным объемом.
Компьютерное моделирование, проведенное Мацумото, показало, что средний объем полостей витритов с ростом температуры линейным образом уменьшается. При этом фрустрированные витриты значительно уменьшают свой объем, тогда как объем полости нефрустрированных витритов почти не меняется.
Итак, сжатие воды при увеличении температуры вызвано двумя конкурирующими эффектами — удлинением водородных связей, которое приводит к увеличению объема воды, и уменьшением объема полостей фрустрированных витритов. На температурном отрезке от от 0 до 4°C последнее явление, как показали расчеты, преобладает, что в итоге и приводит к наблюдаемому сжатию воды при повышении температуры.
Осталось дождаться экспериментального подтверждения существования витритов и такого их поведения. Но это, увы, очень непростая задача.
Источник: Masakazu Matsumoto. Why Does Water Expand When It Cools? // Phys. Rev. Lett. 103, 017801 (2009).
Юрий Ерин
Что происходит с водой при нагревании 🚩 Естественные науки
Воде присущи поразительные свойства, которые сильно отличают ее от прочих жидкостей. Но это и хорошо, иначе, обладай вода «обычными» свойствами, планета Земля была бы абсолютно другой.
Для подавляющего большинства веществ характерно при нагревании расширяться. Что довольно легко объяснить с позиции механической теории теплоты. Согласно ей, при нагревании атомы и молекулы вещества начинают двигаться быстрее. В твердых телах колебания атомов достигают большей амплитуды, и им необходимо больше свободного пространства. Как результат – происходит расширение тела.
Тот же самый процесс происходит и с жидкостями, и с газами. То есть, за счет повышения температуры увеличивается скорость теплового движения свободных молекул, и тело расширяется. При охлаждении же, соответственно, происходит сжатие тела. Это свойственно практически для всех веществ. За исключением воды.
При охлаждении в интервале от 0 до 4оС вода расширяется. И сжимается – при нагревании. Когда отметка температуры воды достигает 4оС, в этот момент вода имеет максимальную плотность, которая равна 1000 кг/м3. Если температура ниже или выше этой отметки, то плотность всегда немного меньше.
Благодаря этому свойству при понижении температуры воздуха осенью и зимой в глубоких водоемах происходит интересный процесс. Когда вода охлаждается, она опускается ниже, на дно, однако лишь до того момента, пока ее температура не станет +4оС. Именно по этой причине в больших водоемах более холодная вода находится ближе к поверхности, а более теплая – опускается на дно. Так что когда зимой поверхность воды замерзает, более глубокие слои продолжают сохранять температуру 4оС. Благодаря этому моменту рыба может спокойно зимовать в глубинах покрывшихся льдом водоемов.
Исключительные свойства воды при нагревании серьезным образом влияют на климат Земли, поскольку около 79% поверхности нашей планеты покрыто водой. За счет солнечных лучей происходит нагревание верхних слоев, которые затем опускаются ниже, а на их месте оказываются холодные слои. Те тоже, в свою очередь, постепенно нагреваются и опускаются ближе ко дну.
Таким образом, слои воды непрерывно меняются, что приводит к равномерному прогреванию, пока не достигается температура, соответствующая максимальной плотности. Затем, нагреваясь, верхние слои становятся менее плотными и уже не опускаются вниз, а остаются наверху и просто постепенно становятся теплее. За счет этого процесса огромные толщи воды довольно легко прогреваются солнечными лучами.
Почему вода бывает легче самой воды?!
Одно из самых распространенных веществ на Земле: вода. Она, как и воздух, необходима нам, но мы ее порой совсем не замечаем. Она просто есть. Но, оказывается
Одно из самых распространенных веществ на Земле: вода. Она, как и воздух, необходима нам, но мы ее порой совсем не замечаем. Она просто есть. Но, оказывается, обыкновенная вода может менять свой объем и весить то больше, то меньше. При испарении воды, ее нагревании и охлаждении происходят поистине удивительные вещи, о которых мы и узнаем сегодня.
Мюриэль Мэнделл в своей занимательной книге «Phycisc Experiments for Children» излагает интереснейшие мысли о свойствах воды, на основе которых не только юные физики могут узнать немало нового, но и взрослые освежат свои знания, которые давненько не приходилось применять, поэтому они оказались слегка забытыми.Сегодня речь пойдет об объеме и весе воды. Оказывается, один и тот же объем воды не всегда весит одинаково. И если налить воду в стакан и она не прольется через край — это еще не значит, что она поместится в нем при любых обстоятельствах.

1. При нагревании вода увеличивается в объеме
Поставьте наполненную водой банку в кастрюлю, наполненную сантиметров на пять кипящей водой, и на слабом огне поддерживайте кипение. Вода из банки начнет переливаться через край. Это происходит потому, что при нагревании вода, подобно другим жидкостям, начинает занимать больше пространства. Молекулы отталкиваются друг от друга с большей интенсивностью и это ведет к увеличению объема воды.2. При охлаждении вода сжимается
Дайте воде в банке остыть при комнатной температуре, или налейте новую воду, и поставьте ее в холодильник. Через некоторое время вы обнаружите, что полная прежде банка уже не полна. При охлаждении до температуры 3,89 градусов по Цельсию вода уменьшает свой объем по мере снижения температуры. Причиной тому стало снижение скорости движения молекул и их сближение друг с другом под воздействием охлаждения. Казалось бы, все очень просто: чем холоднее вода, тем меньший объем она занимает, но…
3. …объем воды вновь возрастает при замерзании
Наполните банку водой до краев и накройте куском картона. Поставьте ее в морозилку и дождитесь замерзания. Вы обнаружите, что картонную «крышку» вытолкнуло. На температурном интервале между 3,89 и 0 градусов по Цельсию, то есть на подходе к точке своего замерзания, вода вновь начинает расширяться. Она является одним из немногих известных веществ, обладающих подобным свойством. Если использовать плотную крышку, то лед просто разнесет банку. Приходилось ли вам слышать о том, что даже водопроводные трубы может разорвать льдом?4. Лед легче воды
Поместите пару кубиков льда в стакан с водой. Лед будет плавать на поверхности. Вода при замерзании увеличивается в объеме. И, вследствие этого, лед легче воды: его объем составляет около 91% соответствующего объема воды.Это свойство воды существует в природе не зря. У него есть вполне определенное предназначение. Говорят, что зимой реки замерзают. Но на самом деле это не совсем верно. Обычно замерзает лишь небольшой верхний слой. Это ледяной покров не тонет, поскольку он легче жидкой воды. Он замедляет замерзание воды на глубине реки и служит своеобразным одеялом, оберегая рыб и другую речную да озерную живность от лютых зимних морозов. Изучая физику, начинаешь понимать, что очень многое в природе устроено целесообразно.
5. Водопроводная вода содержит минералы
Влейте в небольшую стеклянную миску 5 столовых ложек обычной водопроводной воды. Когда вода испарится, на миске останется белая кайма. Эта кайма сформирована минералами, которые были растворены в воде, когда она проходила слои грунта. Посмотрите внутрь своего чайника и вы увидите там минеральный налет. Такой же налет образуется и на отверстии для стока воды в ванне. Попробуйте испарить дождевую воду, чтобы самостоятельно проверить, содержит ли она минералы.Жидкость — Википедия
Жи́дкость — вещество, находящееся в жидком агрегатном состоянии, занимающем промежуточное положение между твёрдым и газообразным состояниями[1].
При этом агрегатное состояние жидкости как и агрегатное состояние твёрдого тела является конденсированным, то есть таким, в котором частицы (атомы, молекулы, ионы) связаны между собой.
Основным свойством жидкости, отличающим её от веществ, находящихся в других агрегатных состояниях, является способность неограниченно менять форму под действием касательных механических напряжений, даже сколь угодно малых, практически сохраняя при этом объём.

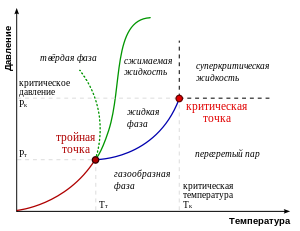
Жидкое состояние обычно считают промежуточным между твёрдым телом и газом: газ не сохраняет ни объём, ни форму, а твёрдое тело сохраняет и то, и другое[2].
Форма жидких тел может полностью или отчасти определяться тем, что их поверхность ведёт себя как упругая мембрана. Так, вода может собираться в капли. Но жидкость способна течь даже под своей неподвижной поверхностью, и это тоже означает несохранение формы (внутренних частей жидкого тела).
Молекулы жидкости не имеют определённого положения, но в то же время им недоступна полная свобода перемещений. Между ними существует притяжение, достаточно сильное, чтобы удержать их на близком расстоянии.
Вещество в жидком состоянии существует в определённом интервале температур, ниже которого переходит в твердое состояние (происходит кристаллизация либо превращение в твердотельное аморфное состояние — стекло), выше — в газообразное (происходит испарение). Границы этого интервала зависят от давления.
Как правило, вещество в жидком состоянии имеет только одну модификацию (наиболее важные исключения — это квантовые жидкости и жидкие кристаллы). Поэтому в большинстве случаев жидкость является не только агрегатным состоянием, но и термодинамической фазой (жидкая фаза).
Все жидкости принято делить на чистые жидкости и смеси. Некоторые смеси жидкостей имеют большое значение для жизни: кровь, морская вода и другие. Жидкости могут выполнять функцию растворителей.
Текучесть[править | править код]
Основным свойством жидкостей является текучесть. Если к участку жидкости, находящейся в равновесии, приложить внешнюю силу, то возникает поток частиц жидкости в том направлении, в котором эта сила приложена: жидкость течёт. Таким образом, под действием неуравновешенных внешних сил жидкость не сохраняет форму и относительное расположение частей, и поэтому принимает форму сосуда, в котором находится.
В отличие от пластичных твёрдых тел, жидкость не имеет предела текучести: достаточно приложить сколь угодно малую внешнюю силу, чтобы жидкость потекла.
Сохранение объёма[править | править код]
Одним из характерных свойств жидкости является то, что она имеет определённый объём. Жидкость чрезвычайно трудно сжать механически, поскольку, в отличие от газа, между молекулами очень мало свободного пространства. Давление, производимое на жидкость, заключённую в сосуд, передаётся без изменения в каждую точку объёма этой жидкости (закон Паскаля, справедлив также и для газов). Эта особенность, наряду с очень малой сжимаемостью, используется в гидравлических машинах.
Жидкости обычно увеличивают объём (расширяются) при нагревании и уменьшают объём (сжимаются) при охлаждении. Впрочем, встречаются и исключения, например, вода сжимается при нагревании, при нормальном давлении и температуре от 0 °C до приблизительно 4 °C.
Вязкость[править | править код]
Кроме того, жидкости (как и газы) характеризуются вязкостью. Она определяется как способность оказывать сопротивление перемещению одной из частей относительно другой — то есть как внутреннее трение.
Когда соседние слои жидкости движутся относительно друг друга, неизбежно происходит столкновение молекул дополнительно к тому, которое обусловлено тепловым движением. Возникают силы, затормаживающие упорядоченное движение. При этом кинетическая энергия упорядоченного движения переходит в тепловую — энергию хаотического движения молекул.
Жидкость в сосуде, приведённая в движение и предоставленная самой себе, постепенно остановится, но её температура повысится.
Образование свободной поверхности и поверхностное натяжение[править | править код]

Из-за сохранения объёма жидкость способна образовывать свободную поверхность. Такая поверхность является поверхностью раздела фаз данного вещества: по одну сторону находится жидкая фаза, по другую — газообразная (пар), и, возможно, другие газы, например, воздух.
Если жидкая и газообразная фазы одного и того же вещества соприкасаются, возникают силы, которые стремятся уменьшить площадь поверхности раздела — силы поверхностного натяжения. Поверхность раздела ведёт себя как упругая мембрана, которая стремится стянуться.
Поверхностное натяжение может быть объяснено притяжением между молекулами жидкости. Каждая молекула притягивает другие молекулы, стремится «окружить» себя ими, а значит, уйти с поверхности. Соответственно, поверхность стремится уменьшиться.
Поэтому мыльные пузыри и пузыри при кипении стремятся принять сферическую форму: при данном объёме минимальной поверхностью обладает шар. Если на жидкость действуют только силы поверхностного натяжения, она обязательно примет сферическую форму — например, капли воды в невесомости.
Маленькие объекты с плотностью, большей плотности жидкости, способны «плавать» на поверхности жидкости, так как сила тяготения меньше силы, препятствующей увеличению площади поверхности. (См. Поверхностное натяжение.)
Испарение и конденсация[править | править код]
 Водяной пар, содержащийся в воздухе, конденсируется в жидкость после соприкосновения с холодной поверхностью бутылки.
Водяной пар, содержащийся в воздухе, конденсируется в жидкость после соприкосновения с холодной поверхностью бутылки.Испарение — постепенный переход вещества из жидкости в газообразную фазу (пар).
При тепловом движении некоторые молекулы покидают жидкость через её поверхность и переходят в пар. Вместе с тем, часть молекул переходит обратно из пара в жидкость. Если из жидкости уходит больше молекул, чем приходит, то имеет место испарение.
Конденсация — обратный процесс, переход вещества из газообразного состояния в жидкое. При этом в жидкость переходит из пара больше молекул, чем в пар из жидкости.
Испарение и конденсация — неравновесные процессы, они происходят до тех пор, пока не установится локальное равновесие (если установится), причём жидкость может полностью испариться, или же прийти в равновесие со своим паром, когда из жидкости выходит столько же молекул, сколько возвращается.
Кипение[править | править код]
Кипение — процесс парообразования внутри жидкости. При достаточно высокой температуре давление пара становится выше давления внутри жидкости, и там начинают образовываться пузырьки пара, которые (в условиях земного притяжения) всплывают наверх.
Смачивание[править | править код]
Смачивание — поверхностное явление, возникающее при контакте жидкости с твёрдой поверхностью в присутствии пара, то есть на границах раздела трёх фаз.
Смачивание характеризует «прилипание» жидкости к поверхности и растекание по ней (или, наоборот, отталкивание и нерастекание). Различают три случая: несмачивание, ограниченное смачивание и полное смачивание.
Смешиваемость[править | править код]
Смешиваемость — способность жидкостей растворяться друг в друге. Пример смешиваемых жидкостей: вода и этиловый спирт, пример несмешиваемых: вода и жидкое масло.
Диффузия[править | править код]
При нахождении в сосуде двух смешиваемых жидкостей молекулы в результате теплового движения начинают постепенно проходить через поверхность раздела, и таким образом жидкости постепенно смешиваются. Это явление называется диффузией (происходит также и в веществах, находящихся в других агрегатных состояниях).
Перегрев и переохлаждение[править | править код]
Жидкость можно нагреть выше точки кипения таким образом, что кипения не происходит. Для этого необходим равномерный нагрев, без значительных перепадов температуры в пределах объёма и без механических воздействий, таких, как вибрация. Если в перегретую жидкость бросить что-либо, она мгновенно вскипает. Перегретую воду легко получить в микроволновой печи.
Переохлаждение — охлаждение жидкости ниже точки замерзания без превращения в твёрдое агрегатное состояние. Как и для перегрева, для переохлаждения необходимо отсутствие вибрации и значительных перепадов температуры.
Волны плотности[править | править код]
Хотя жидкость чрезвычайно трудно сжать, тем не менее, при изменении давления её объём и плотность всё же меняются. Это происходит не мгновенно; так, если сжимается один участок, то на другие участки такое сжатие передаётся с запаздыванием. Это означает, что внутри жидкости способны распространяться упругие волны, более конкретно, волны плотности. Вместе с плотностью меняются и другие физические величины, например, температура.
Если при распространении волны́ плотность меняется достаточно слабо, такая волна называется звуковой волной, или звуком.
Если плотность меняется достаточно сильно, то такая волна называется ударной волной. Ударная волна описывается другими уравнениями.
Волны плотности в жидкости являются продольными, то есть плотность меняется вдоль направления распространения волны. Поперечные упругие волны в жидкости отсутствуют из-за несохранения формы.
Упругие волны в жидкости со временем затухают, их энергия постепенно переходит в тепловую энергию. Причины затухания — вязкость, «классическое поглощение», молекулярная релаксация и другие. При этом работает так называемая вторая, или объёмная вязкость — внутреннее трение при изменении плотности. Ударная волна в результате затухания через какое-то время переходит в звуковую.
Упругие волны в жидкости подвержены также рассеянию на неоднородностях, возникающих в результате хаотического теплового движения молекул.
Волны на поверхности[править | править код]
 Волны на поверхности воды
Волны на поверхности водыЕсли сместить участок поверхности жидкости от положения равновесия, то под действием возвращающих сил поверхность начинает двигаться обратно к равновесному положению. Это движение, однако, не останавливается, а превращается в колебательное движение около равновесного положения и распространяется на другие участки. Так возникают волны на поверхности жидкости.
Если возвращающая сила — это преимущественно силы тяжести, то такие волны называются гравитационными волнами (не путать с волнами гравитации). Гравитационные волны на воде можно видеть повсеместно.
Если возвращающая сила — это преимущественно сила поверхностного натяжения, то такие волны называются капиллярными.
Если эти силы сопоставимы, такие волны называются капиллярно-гравитационными.
Волны на поверхности жидкости затухают под действием вязкости и других факторов.
Сосуществование с другими фазами[править | править код]
Формально говоря, для равновесного сосуществования жидкой фазы с другими фазами того же вещества — газообразной или кристаллической — нужны строго определённые условия. Так, при данном давлении нужна строго определённая температура. Тем не менее, в природе и в технике повсеместно жидкость сосуществует с паром, или также и с твёрдым агрегатным состоянием — например, вода с водяным паром и часто со льдом (если считать пар отдельной фазой, присутствующей наряду с воздухом). Это объясняется следующими причинами:
- Неравновесное состояние. Для испарения жидкости нужно время, пока жидкость не испарилась полностью, она сосуществует с паром. В природе постоянно происходит испарение воды, также как и обратный процесс — конденсация.
- Замкнутый объём. Жидкость в закрытом сосуде начинает испаряться, но поскольку объём ограничен, давление пара повышается, он становится насыщенным ещё до полного испарения жидкости, если её количество было достаточно велико. При достижении состояния насыщения количество испаряемой жидкости равно количеству конденсируемой жидкости, система приходит в равновесие. Таким образом, в ограниченном объёме могут установиться условия, необходимые для равновесного сосуществования жидкости и пара.
- Присутствие атмосферы в условиях земной гравитации. На жидкость действует атмосферное давление (воздух и пар), тогда как для пара должно учитываться практически только его парциальное давление. Поэтому жидкости и пару над её поверхностью соответствуют разные точки на фазовой диаграмме, в области существования жидкой фазы и в области существования газообразной соответственно. Это не отменяет испарения, но на испарение нужно время, в течение которого обе фазы сосуществуют. Без этого условия жидкости вскипали бы и испарялись очень быстро.
Механика[править | править код]
Изучению движения и механического равновесия жидкостей и газов и их взаимодействию между собой и с твёрдыми телами посвящён раздел механики — гидроаэромеханика (часто называется также гидродинамикой). Гидроаэромеханика — часть более общей отрасли механики, механики сплошной среды.
Гидромеханика — это раздел гидроаэромеханики, в котором рассматриваются несжимаемые жидкости. Поскольку сжимаемость жидкостей очень мала, во многих случаях ею можно пренебречь. Изучению сжимаемых жидкостей и газов посвящена газовая динамика.
Гидромеханика подразделяется на гидростатику, в которой изучают равновесие несжимаемых жидкостей, и гидродинамику (в узком смысле), в которой изучают их движение.
Движение электропроводных и магнитных жидкостей изучается в магнитной гидродинамике. Для решения прикладных задач применяется гидравлика.
Основной закон гидростатики — закон Паскаля.
Движение идеальной несжимаемой жидкости описывается уравнением Эйлера. Для стационарного потока такой жидкости выполняется закон Бернулли. Вытекание жидкости из отверстий описывается формулой Торричелли.
Движение вязкой жидкости описывается уравнением Навье-Стокса, в котором возможен и учёт сжимаемости.
Упругие колебания и волны в жидкости (и в других средах) исследуются в акустике. Гидроакустика — раздел акустики, в котором изучается звук в реальной водной среде для целей подводной локации, связи и др.
Молекулярно-кинетическое рассмотрение[править | править код]
Агрегатное состояние вещества определяется внешними условиями, главным образом давлением P{\displaystyle P} и температурой T{\displaystyle T}. Характерными параметрами являются средняя кинетическая энергия молекулы Ekin(P,T){\displaystyle E_{kin}(P,T)} и средняя энергия взаимодействия между молекулами (в расчёте на одну молекулу) Eint(P,T){\displaystyle E_{int}(P,T)}. Для жидкостей эти энергии приблизительно равны: Eint≈Ekin;{\displaystyle E_{int}\,\approx \,E_{kin};} для твёрдых тел энергия взаимодействия намного больше кинетической, для газов — намного меньше.
Классификация жидкостей[править | править код]
Структура и физические свойства жидкости зависят от химической индивидуальности составляющих их частиц и от характера и величины взаимодействия между ними. Можно выделить несколько групп жидкостей в порядке возрастания сложности.
- Атомарные жидкости или жидкости из атомов или сферических молекул, связанных центральными ван-дер-ваальсовскими силами (жидкий аргон, жидкий метан).
- Жидкости из двухатомных молекул, состоящих из одинаковых атомов (жидкий водород, жидкий(натрий, ртуть), в которых частицы (ионы) связаны дальнодействующими кулоновскими силами.
- Жидкости, состоящие из полярных молекул, связанных диполь-дипольным взаимодействием (жидкий бромоводород).
- Ассоциированные жидкости, или жидкости с водородными связями (вода, глицерин).
- Жидкости, состоящие из больших молекул, для которых существенны внутренние степени свободы.
Жидкости первых двух групп (иногда трёх) обычно называют простыми. Простые жидкости изучены лучше других, из не простых жидкостей наиболее хорошо изучена вода. В эту классификацию не входят квантовые жидкости и жидкие кристаллы, которые представляют собой особые случаи и должны рассматриваться отдельно.
В гидродинамике жидкости делятся на ньютоновские и неньютоновские. Течение ньютоновской жидкости подчиняется закону вязкости Ньютона, то есть касательное напряжение и градиент скорости линейно зависимы. Коэффициент пропорциональности между этими величинами известен как вязкость[3][4][5]. У неньютоновской жидкости вязкость зависит от градиента скорости.[6][7]
Статистическая теория[править | править код]
Наиболее успешно структура и термодинамические свойства жидкостей исследуются с помощью уравнения Перкуса-Йевика.
Если воспользоваться моделью твёрдых шаров, то есть считать молекулы жидкости шарами с диаметром d{\displaystyle d}, то уравнение Перкуса-Йевика можно решить аналитически и получить уравнение состояния жидкости:
- PnkT=1+η+η2(1−η)3,{\displaystyle {\frac {P}{n\,k\,T}}={\frac {1+\eta +\eta ^{2}}{(1-\eta )^{3}}}\quad ,}
где n{\displaystyle n} — число частиц в единице объёма, η=(1/6)πnd3{\displaystyle \eta =(1/6)\,\pi \,n\,d^{3}} — безразмерная плотность. При малых плотностях это уравнение переходит в уравнение состояния идеального газа: P/nkT=1{\displaystyle P/n\,k\,T=1} . Для предельно больших плотностей, η→1{\displaystyle \eta \to 1}, получается уравнение состояния несжимаемой жидкости: V=const{\displaystyle V\,=\,const}.
Модель твёрдых шаров не учитывает притяжение между молекулами, поэтому в ней отсутствует резкий переход между жидкостью и газом при изменении внешних условий.
Если нужно получить более точные результаты, то наилучшее описание структуры и свойств жидкости достигается с помощью теории возмущений. В этом случае модель твёрдых шаров считается нулевым приближением, а силы притяжения между молекулами считаются возмущением и дают поправки.
Кластерная теория[править | править код]
Тепловые колебания атомов в решётке кристалла: точки — атомы, соединяющие линейные отрезки — межатомные связи Поведение атомов жидкости после перехода кристалла через точку плавления, как в среднем постоянные для заданной температуры разрывы и восстановления межкластерных и внутрикластерных межатомных связей (короткие утолщённые отрезки — разорванные связи)[8]Одной из современных теорий служит «Кластерная теория». В её основе заключена идея, что жидкость представляется как сочетание твёрдого тела и газа. При этом частицы твёрдой фазы (кристаллы, двигающиеся на короткие расстояния) располагаются в облаке газа, образуя кластерную структуру. Энергия частиц отвечает распределению Больцмана, средняя энергия системы при этом остаётся постоянной (при условии её изолированности). Медленные частицы сталкиваются с кластерами и становятся их частью. Так непрерывно изменяется конфигурация кластеров, система находится в состоянии динамического равновесия. При создании внешнего воздействия система будет вести себя согласно принципу Ле Шателье. Таким образом, легко объяснить фазовое превращение:
- При нагревании система постепенно превратится в газ (кипение)
- При охлаждении система постепенно превратится в твёрдое тело (замерзание).
По другому представлению[9][10] в основе кластерной теории жидкости, как о веществе, находящемся в конденсированном (связанном) состоянии (сохранение объёма), а не в состоянии «газоплотного» беспорядка, лежит представление о кластерах, как остаточных после перехода через точку плавления квазикристаллических динамических структурах с постоянным (для заданной температуры) средним числом разрывающихся и восстанавливающихся межкластерных и внутрикластерных межатомных связей, обеспечивающих сохранение объёма и определяющих подвижность (текучесть) и химическую активность жидкости. С ростом температуры количество атомов в кластерах уменьшается за счёт увеличения разорванных связей. Образующиеся свободные атомы (молекулы) испаряются с поверхности жидкости или остаются в межкластерном пространстве в качестве растворённого газа (пара). При температуре кипения вещество переходит в моноатомное (мономолекулярное) газообразное (парообразное) состояние.
Структуру жидкостей изучают с помощью методов рентгеновского структурного анализа, электронографии и нейтронографии.
- ↑ Жидкость — статья из Физической энциклопедии
- ↑ В технической гидромеханике иногда жидкостью в широком смысле этого слова называют и газ; при этом жидкость в узком смысле слова называют капельной жидкостью.
- ↑ «Физическая энциклопедия». В 5 томах. М.: «Советская энциклопедия», 1988
- ↑ Физическая энциклопедия: Ньютоновская жидкость
- ↑ Ньютоновская жидкость — статья из Физической энциклопедии
- ↑ Уилкинсон У. Л., Неньютоновские жидкости, пер. с англ., М., 1964
- ↑ Астарита Д ж., Марруччи Д ж., Основы гидромеханики неньютоновских жидкостей, пер. с англ., М., 1978
- ↑ Андреев В. Д. Избранные проблемы теоретической физики.. — Киев: Аванпост-Прим,. — 2012.
- ↑ Андреев В. Д. Крэш (crash)-конформационная кинематика ковалентной решётки алмаза при плавлении. // Журнал структурной химии. — 2001. — № 3. — С. 486—495.
- ↑ Андреев В. Д. «Фактор плавления» при межатомных взаимодействиях в алмазной решётке. // Химическая физика. — 2002. — № 8,т.21. — С. 35—40.
Три состояния воды — урок. Окружающий мир, 3 класс.
Мы привыкли, что вода — это прозрачная жидкость без цвета и вкуса. Но она бывает и твёрдой, и газообразной. Лёд и снег — это тоже вода. А в воздухе всегда есть вода в виде пара.
Вода может быть в трёх состояниях: жидком, газообразном (пар, туман) и твёрдом (лёд, снег, град, иней).

Состояние воды зависит от температуры. Если на улице тепло, то вода жидкая. На морозе вода замерзает и превращается в лёд. А при нагревании она испаряется и становится водяным паром.
При этом изменяется расстояние между молекулами воды. В твёрдой воде молекулы располагаются совсем близко. В жидкой воде они дальше друг от друга, а в газообразной — совсем далеко.

Превращения воды
Превращение жидкой воды в лёд происходит при температуре ниже \(0\) градусов. Это замерзание.
Лёд начинает таять, если температура выше \(0\) градусов. Происходит таяние льда.
Превращение жидкой воды в пар — это испарение. Испарение происходит при любой температуре, а полностью вода становится газообразной, если температура выше \(100\) градусов.
Водяной пар превращается в жидкую воду при температуре ниже \(100\) градусов. Процесс называется конденсация.
Особые свойства льда
Обычно твёрдые вещества тяжелее, чем те же вещества в жидком состоянии. Например, кусочек воска тонет в расплавленном воске. Лёд не тонет в воде. Если бросить кусочек льда в воду, он будет плавать на поверхности.
При замерзании вода ведёт себя не так, как другие вещества. Если воду охлаждать, то она начинает сжиматься. Но как только температура воды становится ниже \(0\) градусов, всё изменяется. При замерзании вода опять расширяется. Лёд занимает больший объём, чем вода, и он легче воды.
Если стеклянную бутылку с водой оставить на морозе, то она лопается. То же самое происходит и с водопроводными трубами. Если в них вода замёрзнет, то они разрываются. В сильные морозы из-за этого происходят аварии, и люди остаются без тепла и воды.
Что происходит с объемом жидкости при нагревании. Что происходит с водой при нагревании. Опыт, демонстрирующий свойства воды при нагревании и охлаждении
Класс: 5
Цели урока:
- расширить знания о воде, ее свойствах, значении воды, ввести понятия раствор, взвесь, значение растворов в природе и жизни человека;
- развить наблюдательность, мыслительную деятельность, воспитывать бережное отношение к воде.
Оборудование:
- химическая посуда для опытов,
- спиртовка,
- вещества для опытов,
- костюмы для капелек, к
- арточки для самостоятельной работы.
Ход урока
Здравствуйте, ребята! Сегодня наш урок посвящен воде и называется “Ее величество – вода”. На уроке мы расширим свои знания о воде, познакомимся с ее свойствами, а также водой как растворителем веществ. Узнаем, что такое раствор и, что такое взвесь.
Открываем тетради, в которых записываем тему урока “Ее величество – вода”.
Каждый человек пользуется водой для приготовления пищи и других бытовых нужд, для промышленных предприятий, для выращивания растений и животных. Что же такое вода расскажут нам капельки.
Капелька 1: Вода – вещество привычное и необычное. Ученые абсолютно правы: нет на Земле вещества более важного для нас, чем обыкновенная вода. Почти три четверти поверхности нашей планеты занято морями и океанами. Твердой водой — снегом и льдом — покрыто 20% суши. От воды зависит климат нашей планеты. Земля давно бы остыла и превратилась в безжизненный камень, если бы не вода. Нагреваясь вода забирает тепло, а остывая отлает его. От космического холода предохраняет Землю та вода, которая рассеяна в атмосфере – в облаках в виде пара.
Капелька 2: У воды много удивительных свойств, которые делают ее не похожей на все другие вещества. Но среди них есть одно необычное — это ее бессмертие. Примерно один миллиард тонн воды расходуется человечеством за сутки. Но общее количество воды не уменьшается. Сколько ее было миллионы лет назад, столько же ее и в наше время.
Капелька 3: Велика роль воды в жизни на Земле. Живые организмы нашей планеты приспособились ко всяким условиям: к полному мраку, к жаре и холоду. Но ни одно живое существо не может обходиться без воды. Все растения и животные содержат в себе воду, да и наше собственное тело на три четверти состоит из воды. Знаете ли вы, что при потере человеком 1 литра воды (это примерно 2% массы тела) появляется ощущение жажды. При потери 6-8% влаги человек впадает в полуобморочное состояние. Потеря 10% воды вызывает галлюцинации. А потеря более 12% человек погибает.
Учитель: Так что же такое вода? (Ответы детей) Вода – это химическое вещество, которое имеет свои свойства. В тетрадях записываем: Свойства воды.
С некоторыми свойствами воды вы уже знакомы. Давайте вспомним их, а поможет нам в этом наш учебник (работа с учебником).
Свойства воды:
- прозрачна;
- бесцветна;
- без вкуса и без запаха;
- текуча;
- может находиться в трех агрегатных состояниях;
- может переходить из одного агрегатного состояния в другое.
(Свойства воды записываются в тетрадь)
А теперь давайте познакомимся еще с некоторыми ее свойствами. В этом помогут нам опыты.
Оборудование:
- 2 колбы с газоотводной трубкой,
- 2 кристаллизатора.
Вещества:
- вода,
- горячая вода,
Посмотрим, что произойдет, если мы возьмем две одинак

