Есть ли у воды память? Разбираемся, как возник популярный миф и почему наука его опровергает
29 сентября 2021 Образование Колонка
Увы, даже если очень ласково разговаривать с водой в стакане и включать ей Моцарта, она не станет целебной.
В эзотерике, мистике и даже вполне бытовых вопросах часто встречается термин «структурированная вода», подразумевающий некое сверхвещество, обладающее лекарственными и магическими свойствами, в том числе способностью переносить информацию. Есть люди, которые в это верят и тратят заметные деньги на «структурирование» воды и прочие оккультные действия. Давайте разберёмся, откуда появился этот миф и почему у воды не может быть памяти.
Денис Байгозин
Химик, преподаватель и автор блога о химии. Занимал должность ведущего разработчика компании «Аквафор».
Уникальна ли вода
В школьной программе за 8‑й класс есть урок под названием «Уникальные свойства воды». На нём рассказывают про «непредсказуемо экстремальные» температуры плавления и кипения, про диполи и ионные силы. К сожалению, этот урок, точнее плохое его усвоение, и закладывает первый фундамент для веры в мистическую структуру воды.
К сожалению, этот урок, точнее плохое его усвоение, и закладывает первый фундамент для веры в мистическую структуру воды.
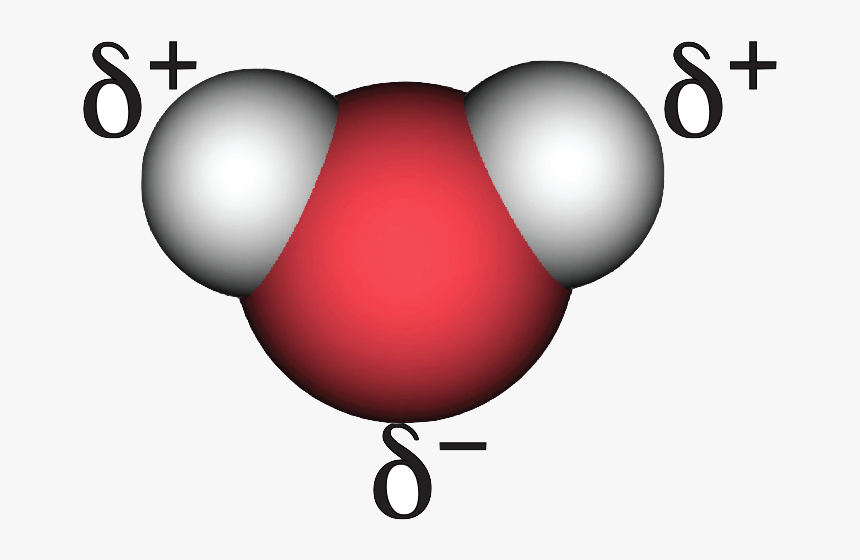
Уже много десятилетий прошло с тех пор, как учёные в деталях объяснили значительные отличия воды от соседей по группе: сероводорода, селеноводорода и теллуроводорода. Уникальные свойства h3O вызывает большой дипольный момент, помноженный на способность к образованию водородных связей.
Водородные связи между молекулами воды. Иллюстрация: ЛайфхакерКонцы молекулы h3O сильно заряжены, а водороды легко становятся общими, объединяя две и более молекулы и не давая им расцепиться и улететь в виде пара. Всё просто. Вернее, сложно, но объяснимо в рамках науки, без обращения к мистике. И кстати, «магически точные» значения температур плавления (0 °С) и кипения (100 °С) воды не несут символизма, а выбраны людьми для удобства. Это шкалу Цельсия подстраивали под воду, а не наоборот.
Понятно, почему вода уникальна. Но почему ей приписывают наличие памяти, а не процессора, монитора или других частей компьютера?
Не шарлатан, но и не гений — кто такой Жак Бенвенист
На многих сайтах, посвящённых «структуре воды», упоминается имя Жака Бенвениста как отца‑основателя информационной теории воды. Что же он сделал? Этот французский учёный‑иммунолог в 1988 году исследовал разведение анти‑IgE‑антител и их влияние на человеческие базофильные клетки. То есть изучал иммунный ответ. Результаты, которые Бенвенист хотел опубликовать в журнале Nature, казалось, соответствовали идеям гомеопатии: при разведении в миллионы раз активность препарата сохранялась.
Что же он сделал? Этот французский учёный‑иммунолог в 1988 году исследовал разведение анти‑IgE‑антител и их влияние на человеческие базофильные клетки. То есть изучал иммунный ответ. Результаты, которые Бенвенист хотел опубликовать в журнале Nature, казалось, соответствовали идеям гомеопатии: при разведении в миллионы раз активность препарата сохранялась.
Однако статью в первой редакции отозвали с просьбой уточнить эксперимент или объяснить его теоретически. Вместо того чтобы перепроверить странные результаты, Бенвенист ввёл понятие «памяти воды» и «информационной структуры», которую можно скопировать с лекарства и бесконечно множить в воде, делая её активной. Крутая идея, которая могла бы спасти многие жизни.
К сожалению, попытки повторить эксперимент в других лабораториях ждал провал. Более того, при введении двойного слепого метода Бенвенист лично не смог воспроизвести свои результаты. В другой ситуации научное сообщество покачало бы головой, пожурило незадачливого экспериментатора да и забыло бы, но идея уже очень понравилась журналистам и некоторым фармкомпаниям. Ведь можно ничего не синтезировать, а разливать по пузырькам чистую воду! Поэтому про разоблачение опытов Бенвениста мало кто помнит. А вот термин и его производные как раз остались.
Ведь можно ничего не синтезировать, а разливать по пузырькам чистую воду! Поэтому про разоблачение опытов Бенвениста мало кто помнит. А вот термин и его производные как раз остались.
Что могут услышать снежинки
Одна из самых коммерчески успешных кампаний, связанных со «структурой воды», была у Эмото Масару. Он прославился благодаря рекламе с фотографиями красивых и уродливых снежинок, которым при замерзании была послана различная информация. Позитивная якобы даёт симметричные снежинки, а негативная — асимметричные. Фирма Масару и его последователи широко и успешно продают «правильную воду», «структураторы», «музыку воды» и другие религиозно‑мифические продукты.
Иллюстрация: Анна Гуридова / ЛайфхакерК сожалению, в отличие от искренне заблуждавшегося Бенвениста, в данном случае это прямое жульничество. На таинство выбора одной из снежинок, образовавшихся под действием слов, допускали только посвящённых. Которые и выбирали подходящую среди тысяч. Двойной слепой метод грустно плачет в уголке.
Может ли звук влиять на воду и другие вещества? Да, но только высокой частоты и интенсивности. Этим даже занимается отдельная наука — сонохимия. Обычные же слова никак не влияют. Да и на каком языке говорить? Например, произнесённые слова «факт» или «Дед Мороз» в английском теряют свою позитивную эмоциональную окраску.
Что нужно знать о водных кластерах
Второе дыхание теория памяти воды получила в конце 90‑х — начале нулевых в связи с открытием водных кластеров. Это квазиструктуры, которые образуются в воде за счёт водородных связей. Сторонники структурирования сразу, не читая, подняли кластеры на знамя: «Вот так вода и запоминает! Кластеры — носители информации!» Но никто из них не прочитал в научных статьях время существования таких кластеров: 10-6–10-10 секунды.
Водный кластер. Frank N. Keutsch / Richard J. Saykally / PNASТак что, даже если предположить, что на воду можно что‑то записать, всё сотрётся после перераспределения кластеров. В лучшем случае такая «флешка» протянет 0,000001 секунды в переохлаждённой жидкой воде. Поэтому, к сожалению, предки были правы, когда говорили «вилами по воде писано».
В лучшем случае такая «флешка» протянет 0,000001 секунды в переохлаждённой жидкой воде. Поэтому, к сожалению, предки были правы, когда говорили «вилами по воде писано».
Как связаны гомеопатия и память воды
Куда же без неё? Чтобы не писать ещё одну статью, думаю, стоит направить вас к материалам про гомеопатию и эффект плацебо на Лайфхакере. А о психосоматике лучше пусть расскажут медики.
За одно я благодарен гомеопатам: они вдохновили на отличную задачку, которую я предлагаю ученикам в Химическом центре в первый учебный год. Звучит она так: «Сколько тонн препарата ХХХ нужно употребить, чтобы в организм попала одна молекула действующего вещества?» Чаще всего ребята сами идут в аптеку и считают, исходя из указанного на коробке количества разведений и числа Авогадро. Попробуйте и вы, можно взять любой гомеопатический препарат.
Число Авогадро (молярная константа) — самая запрещённая константа в среде гомеопатов. Проверено. Дело в том, что, как только разведение чего‑либо превышает примерно 1023 раз, то исходное вещество в препарате попросту исчезает. И ничего с этим не сделать, приходится переходить к памяти воды, структуре и прочему. Ну или просто ругаться нехорошими словами на въедливого учёного.
И ничего с этим не сделать, приходится переходить к памяти воды, структуре и прочему. Ну или просто ругаться нехорошими словами на въедливого учёного.
Зачем всё это людям
Некоторые скажут: ну пишут же про структуру. Значит, что‑то нечисто, учёные скрывают, наука не всё может объяснить. Может, и какая‑то польза от «структураторов» всё-таки есть?
Чтобы что‑то долгое время существовало в условиях рыночной экономики, оно должно быть выгодно хотя бы кому‑то. Как раз выгода и поддерживает этот миф. Если на фильтре для воды написать, что он структурирует воду, продажи увеличатся. Почему? Знающий покрутит у виска — и всё равно купит, если фильтр хороший. Не знающий же на полке выберет как раз «структурирующий» фильтр.
Гомеопатия ещё выгоднее: для производства лекарства не нужна разработка, тестирование на клетках, мышах, добровольцах, сертификаты. Нужен только сахар, крахмал и маркетинг. Выгода огромна, затраты почти нулевые. Жаль только, что не работает.
Ну и, конечно, информационная теория воды — хлеб для конспирологов, нужно же о чём‑то разговаривать, когда уже слишком многие мистические теории безжалостно разрушены наукой.
Что делать с продуктами на основе «памяти воды»? Избегайте их. Либо это пустышки, либо попытка вытянуть из вас дополнительные деньги, не увеличивая ценности товара. В любом случае покупать лучше у честных компаний.
Читайте также 🧐
- Почему БАДы бесполезны и даже опасны
- Как не тратить деньги на лекарства-пустышки
- Почему вам точно не надо пить серебряную воду
Фотографии свободно плавающих тел
Глеб Ингман, Леонид Свистов
«Квантик» №8, 2018
Пришла весна. Настало время сажать цветы на даче. Чтобы семена хорошо всходили, их рекомендуют до посадки замачивать в воде. Мы бросили семена настурции в тарелку с водой. Сначала они были распределены равномерно по поверхности воды. Но вдруг семена «ожили» и начали плыть друг к другу! По мере сближения они ускорялись. Через несколько минут семена на воде организовали плавучие цепочки и островки. После чего движение закончилось.
Настало время сажать цветы на даче. Чтобы семена хорошо всходили, их рекомендуют до посадки замачивать в воде. Мы бросили семена настурции в тарелку с водой. Сначала они были распределены равномерно по поверхности воды. Но вдруг семена «ожили» и начали плыть друг к другу! По мере сближения они ускорялись. Через несколько минут семена на воде организовали плавучие цепочки и островки. После чего движение закончилось.
Эти наблюдения нас так удивили, что мы стали испытывать другие плавающие предметы: спилы веток, крышечки от молочных бутылок и банок, плавающие парафиновые свечки и парниковые помидоры. Оказалось, что одинаковые плавающие предметы притягиваются. А вот неодинаковые ведут себя по-разному: одни притягиваются, а другие расталкиваются.
Чтобы разобраться в происходящем, давайте посмотрим на поверхность воды в стеклянном стакане. Поверхность воды выглядит плоской только вдали от стенок стакана. Рядом со стеклом поверхность воды искривляется: у стенки вода поднимается вверх. Как говорят, вода смачивает стекло. Но она не всегда ведёт себя так. Если налить воду в парафиновый стакан, то мы увидим, что уровень воды будет опускаться по мере приближения к парафиновой стенке. Парафин не смачивается.
Как говорят, вода смачивает стекло. Но она не всегда ведёт себя так. Если налить воду в парафиновый стакан, то мы увидим, что уровень воды будет опускаться по мере приближения к парафиновой стенке. Парафин не смачивается.
Какие силы поднимают или опускают воду вблизи стенки? Вода состоит из молекул, которые можно рассматривать как маленькие жёсткие шарики, притягивающиеся друг к другу. Обратим внимание на то, что состояние молекулы воды на её поверхности отличается от состояния такой же молекулы воды, находящейся вдали от поверхности. На молекулу, находящуюся внутри воды, силы со стороны ближайших соседей действуют во все стороны. В то же время у молекулы воды, находящейся на поверхности, соседи сверху отсутствуют. Значит, на молекулу воды у поверхности будет действовать суммарная сила, направленная внутрь жидкости. Благодаря этой силе молекула воды, находящаяся у поверхности, не вылетает из жидкости. Поверхностные силы и сила тяжести определяют форму поверхности жидкости. Например, свободно падающая капелька сжимается со всех сторон своим поверхностным слоем. Это определяет её сферическую форму. Эти же поверхностные силы обеспечивают внутри капельки давление, большее атмосферного.
Это определяет её сферическую форму. Эти же поверхностные силы обеспечивают внутри капельки давление, большее атмосферного.
Молекулы воды притягиваются не только к молекулам воды, но и к молекулам других материалов. Силы притяжения молекул воды к молекулам стекла больше, чем силы притяжения молекул воды между собой. Поэтому вода смачивает стекло, то есть уровень воды повышается у стенок стакана. А силы притяжения воды к парафину гораздо меньше сил притяжения между молекулами воды. Поэтому вода не смачивает парафин, и уровень воды у стенки понижается.
На фотографиях — плавающая свечка в бокале с водой. Вода смачивает стекло и не смачивает парафин свечки. Прежде чем сделать эти фотографии, мы подождали несколько минут. Свечка установилась в центре бокала! Это и понятно. Свечка соскальзывает с горок, образуемых водой и стеклом, в самую низшую точку. Вот почему смачиваемые и несмачиваемые плавающие тела расталкиваются!
Для проверки этой гипотезы мы изменили форму поверхности воды в бокале. Для этого аккуратно долили воду так, чтобы бокал оказался заполнен водой «с верхом». Верхняя точка воды теперь в середине бокала. Свечка, как мы и ожидали, соскользнула к краю. Чтобы посмотреть, как отталкивание от стенки заменяется притяжением, оказалось удобным добавлять воду медицинским шприцем.
Для этого аккуратно долили воду так, чтобы бокал оказался заполнен водой «с верхом». Верхняя точка воды теперь в середине бокала. Свечка, как мы и ожидали, соскользнула к краю. Чтобы посмотреть, как отталкивание от стенки заменяется притяжением, оказалось удобным добавлять воду медицинским шприцем.
Чтобы понять, почему одинаковые плавающие предметы (смачиваемые или несмачиваемые) притягиваются, мы провели дополнительные опыты: опустили два плоских стёклышка, находящихся на небольшом расстоянии друг от друга, в воду. Силы притяжения воды к стеклу подняли уровень воды на заметную высоту! Чем ближе находятся стёкла, тем выше поднимается вода. Чтобы проследить зависимость высоты подъёма воды от величины зазора между пластинами, мы сложили пластины в виде приоткрытой книжки. С одной стороны пластины сходятся вплотную, а с другой — расходятся на расстояние в несколько миллиметров. На фотографии видна граница воды и воздуха. При малых расстояниях между пластинами кривая очень похожа на гиперболу. Это указывает на обратно пропорциональную зависимость высоты подъёма от расстояния между пластинами. Постараемся разобраться, какие силы действуют на пластины. Для этого представим схематично вид сбоку.
Это указывает на обратно пропорциональную зависимость высоты подъёма от расстояния между пластинами. Постараемся разобраться, какие силы действуют на пластины. Для этого представим схематично вид сбоку.
На схеме 1 изображены две параллельные чистые стеклянные пластины, опущенные в воду. На схеме 2 — пластины, покрытые парафином (не смачиваемые водой). В воздухе и в точках 1, 2, 3 на обеих схемах (в соответствии с законом Паскаля) давление атмосферное: PA. Тогда на первой схеме в поднявшейся между пластинами воде давление меньше атмосферного. Воздух снаружи пластин будет давить сильнее, чем вода между пластинами. Пластины будут притягиваться. Удивительно, что в случае несмачиваемых пластин они тоже будут притягиваться! Чтобы понять это, надо сравнить давление воды в точке 4 и давление воздуха в точке 2 на второй схеме.
Уровень воды между плавающими телами изменяется, как и в случае опущенных в воду пластин. В случае смачивания и несмачивания плавающих тел давление с внешней стороны оказывается больше, чем между ними. Это приводит к их притяжению. Чем меньше расстояние между телами, тем больше изменение уровня воды в зазоре между ними. Поэтому сила притяжения растёт при сближении плавающих предметов.
Это приводит к их притяжению. Чем меньше расстояние между телами, тем больше изменение уровня воды в зазоре между ними. Поэтому сила притяжения растёт при сближении плавающих предметов.
После того как мы заметили взаимодействие свободно плавающих предметов, мы обнаружили, что результат действия этих сил можно найти почти в каждом водоёме. Например, на фото ряски и лягушек, которые мы нашли в интернете. Лягушка, наверное, не догадывается, какие силы тянут её к плавающей листве. (Значительны ли эти силы — попробуйте оценить сами.) Посмотреть притяжение и отталкивание плавающих тел в динамике можно в интернете. Хотя, конечно, лучше попытаться поставить свои собственные опыты.
Фото (кроме двух последних): Глеб Ингман, Леонид Свистов
Художник Мария Усеинова
Новый инструмент для визуализации молекулярной структуры воды и ее изменений, выраженных в шкале влияния температуры
1. Ле Бихан Д., Фукуяма Х. В кн.: Вода. Бихан Д., Фукуяма Х., редакторы. Издательство Пан Стэнфорд; Сингапур: 2010. [Google Scholar]
Издательство Пан Стэнфорд; Сингапур: 2010. [Google Scholar]
2. Болл П. Уотер. Непреходящая тайна. Природа. 2008; 452: 291–292. doi: 10.1038/452291a. [PubMed] [CrossRef] [Google Scholar]
3. Дэвисс Б. Журнал Scientist. LabX Media Group; Нью-Йорк, штат Нью-Йорк, США: 2004. стр. 14–15. [Академия Google]
4. Болл П. Вода – активная матрица жизни для клеточной и молекулярной биологии. проц. Натл. акад. науч. США. 2017;114:13327–13335. doi: 10.1073/pnas.1703781114. [Статья PMC free] [PubMed] [CrossRef] [Google Scholar]
5. Болл П. Вода как активный компонент в клеточной биологии. хим. 2008; 108:74–108. doi: 10.1021/cr068037a. [PubMed] [CrossRef] [Google Scholar]
6. Болл П. Вода как биомолекула. ХимФизХим. 2008; 9: 2677–2685. doi: 10.1002/cphc.200800515. [PubMed] [CrossRef] [Академия Google]
7. Ценкова Р. Аквафотомика: Динамическая спектроскопия водных и биологических систем описывает особенности воды. J. Ближний инфракрасный спектр. 2009;17:303–313. doi: 10.1255/jnirs.869. [CrossRef] [Google Scholar]
doi: 10.1255/jnirs.869. [CrossRef] [Google Scholar]
8. Ценкова Р., Мунчан Дж., Поллнер Б., Ковач З. Основы аквафотомики и ее хемометрических подходов. Передний. хим. 2018;6:363. doi: 10.3389/fchem.2018.00363. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
9. Мункан Дж., Ценкова Р. Аквафотомика — от инновационных знаний к интегративной платформе в науке и технике. Молекулы. 2019;24:2742. doi: 10,3390/молекулы24152742. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
10. Ван де Краатс Э.Б., Мунчан Дж., Ценкова Р.Н. Аквафотомика — происхождение, концепция, приложения и перспективы на будущее. Субстанция. 2019;3:13–28. [Google Scholar]
11. Манчинелли Р., Ботти А., Бруни Ф., Риччи М.А., Сопер А.К. Гидратация ионов натрия, калия и хлорида в растворе и концепция создателя/разрушителя структуры. Дж. Физ. хим. Б. 2007; 111:13570–13577. дои: 10.1021/jp075913в. [PubMed] [CrossRef] [Google Scholar]
12. Галло П., Коррадини Д., Ровере М. Ионная гидратация и структурные свойства воды в водных растворах в нормальных и переохлажденных условиях: проверка концепции создания и разрушения структуры . физ. хим. хим. физ. 2011;13:19814. doi: 10.1039/c1cp22166c. [PubMed] [CrossRef] [Google Scholar]
Ионная гидратация и структурные свойства воды в водных растворах в нормальных и переохлажденных условиях: проверка концепции создания и разрушения структуры . физ. хим. хим. физ. 2011;13:19814. doi: 10.1039/c1cp22166c. [PubMed] [CrossRef] [Google Scholar]
13. Джанджакомо Р. Исследование взаимодействия вода-сахар при увеличении концентрации сахара с помощью NIR-спектроскопии. Пищевая хим. 2006; 96: 371–379.. doi: 10.1016/j.foodchem.2005.02.051. [CrossRef] [Google Scholar]
14. Сегтнан В.Х.В., Шашич Ш., Исакссон Т., Озаки Ю., Шашич С., Исакссон Т., Озаки Ю., Сасич С., Исакссон Т., Озаки Ю. Исследования на структуру воды с помощью двумерной корреляционной спектроскопии ближнего инфракрасного диапазона и анализа главных компонент. Анальный. хим. 2001;73:3153–3161. doi: 10.1021/ac010102n. [PubMed] [CrossRef] [Google Scholar]
15. Гоуэн А.А., Амиго Дж.М., Ценкова Р. Характеристика возмущений водородных связей в водных системах с использованием аквафотомики и метода наименьших квадратов с переменным разрешением многомерной кривой. Анальный. Чим. Акта. 2013;759: 8–20. doi: 10.1016/j.aca.2012.10.007. [PubMed] [CrossRef] [Google Scholar]
Анальный. Чим. Акта. 2013;759: 8–20. doi: 10.1016/j.aca.2012.10.007. [PubMed] [CrossRef] [Google Scholar]
16. Гото Н., Базар Г., Ковач З., Кунисада М., Морита Х., Кизаки С., Сугияма Х., Ценкова Р., Нисигори С. Обнаружение УФ-индуцированных циклобутанпиримидиновых димеров с помощью спектроскопии в ближней инфракрасной области спектра и аквафотомики. науч. Отчет 2015; 5:11808. doi: 10.1038/srep11808. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
17. Джинендра Б. Диссертация доктора философии. Университет Кобе; Кобе, Япония: 2011. Спектроскопия в ближней инфракрасной области и аквафотомика: новый инструмент для диагностики биотического и абиотического стресса сои. [Академия Google]
18. Ценкова Р. Аквафотомика: Вода в биологическом и водном мире, освещенная невидимым светом. Спектроск. Евро. 2010; 22:6–10. [Google Scholar]
19. Киношита К., Миядзаки М., Морита Х., Васильева М., Тан С., Ли Д., Исикава О., Кусуноки Х., Ценкова Р. Спектральная картина мочевой воды как биомаркер течки у большой панды. науч. 2012; 2:856. doi: 10.1038/srep00856. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
науч. 2012; 2:856. doi: 10.1038/srep00856. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
20. Киношита К., Ценкова Р. Ближние инфракрасные спектры жидкостей организма выявляют взаимосвязь между спектральной картиной воды и эстральным циклом. Новости НИР. 2015; 26:4–5. doi: 10.1255/nirn.1539. [CrossRef] [Google Scholar]
21. Такемура Г., Базар Г., Икута К., Ямагути Э., Исикава С., Фурукава А., Кубота Ю., Ковач З., Ценкова Р. Акваграммы сырого молока для обнаружения течки у молочных коров. Воспр. Дом. Аним. 2015;50:522–525. doi: 10.1111/rda.12504. [PubMed] [CrossRef] [Google Scholar]
22. Славчев А., Ковач З., Кошиба Х., Нагаи А., Базар Г., Крастанов А., Кубота Ю., Ценкова Р. Мониторинг спектральной картины воды Выявляет различия в росте пробиотиков при использовании для быстрой селекции бактерий. ПЛОС ОДИН. 2015;10:e0130698. doi: 10.1371/journal.pone.0130698. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
23. Мунчан Дж., Милеушнич И., Шакота Росич Дж. , Васич-Милованович А., Матия Л. Водные свойства мягких контактных линз: сравнительный анализ Исследование двух гидрогелевых материалов в ближнем инфракрасном диапазоне. Междунар. Дж. Полим. науч. 2016;2016:1–8. doi: 10.1155/2016/3737916. [CrossRef] [Google Scholar]
, Васич-Милованович А., Матия Л. Водные свойства мягких контактных линз: сравнительный анализ Исследование двух гидрогелевых материалов в ближнем инфракрасном диапазоне. Междунар. Дж. Полим. науч. 2016;2016:1–8. doi: 10.1155/2016/3737916. [CrossRef] [Google Scholar]
24. Шакота Росич Дж., Мунчан Дж., Милеуснич И., Косич Б., Матия Л. Обнаружение белковых отложений с помощью NIR-спектроскопии. Мягкий Матер. 2016; 14: 264–271. дои: 10.1080/1539445X.2016.1198377. [CrossRef] [Google Scholar]
25. Мунчан Дж., Росич Дж., Милеуснич И., Матович В., Матия Л., Ценкова Р. Труды 18-й Международной конференции по ближней инфракрасной спектроскопии, Копенгаген, Дания, 11 –15 июня 2017 г. Публикации IM открыты; Западный Сассекс, Великобритания: 2019 г. Структура воды в мягких контактных линзах: исследование спектроскопии в ближней инфракрасной области и аквафотомики; стр. 99–104. [Google Scholar]
26. Scholz-Ahrens K.E., Ade P., Marten B., Weber P., Timm W., Aςil Y., Glüer C.-C.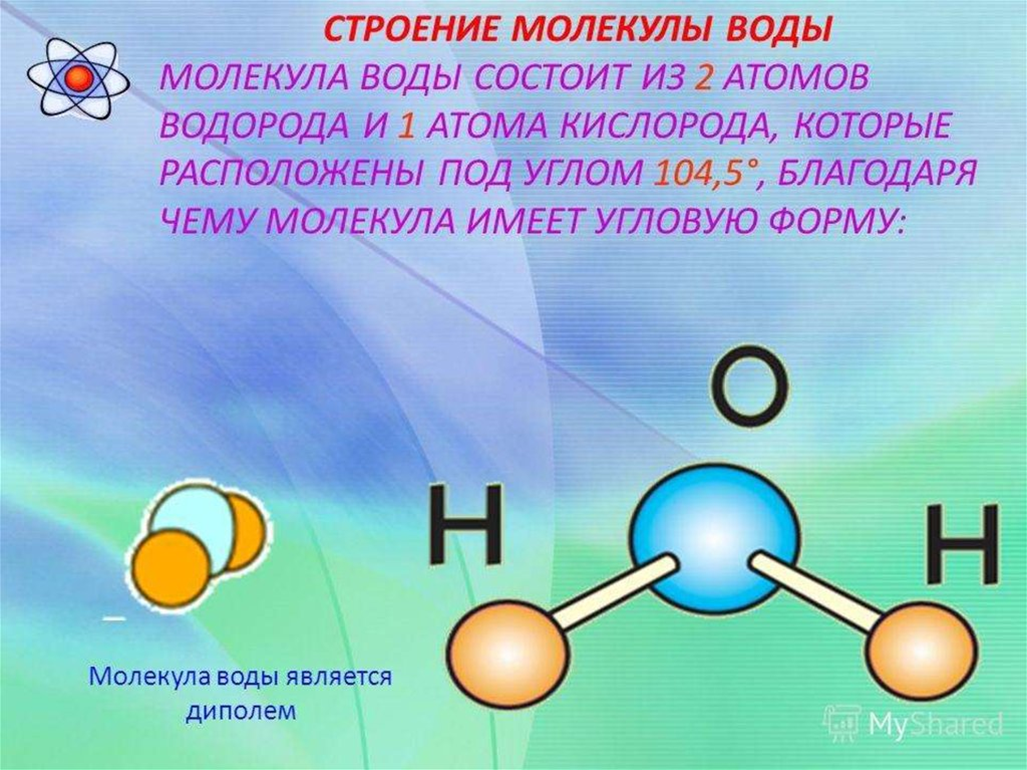 , Schrezenmeir J. Влияние пребиотиков, пробиотиков и синбиотиков Поглощение минералов, содержание минералов в костях и структура костей. Дж. Нутр. 2007; 137:838С–846С. дои: 10.1093/jn/137.3.838S. [PubMed] [CrossRef] [Google Scholar]
, Schrezenmeir J. Влияние пребиотиков, пробиотиков и синбиотиков Поглощение минералов, содержание минералов в костях и структура костей. Дж. Нутр. 2007; 137:838С–846С. дои: 10.1093/jn/137.3.838S. [PubMed] [CrossRef] [Google Scholar]
27. Куроки С., Ценкова Р., Моянкова Д. П., Мункан Дж., Морита Х., Атанасова С., Джилианов Д. Молекулярная структура воды лежит в основе чрезвычайной устойчивости воскресения к высыханию. растение Haberlea rhodopensis. науч. Отчет 2019;9:3049. doi: 10.1038/s41598-019-39443-4. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
28. Бернал Дж. Д., Фаулер Р. Х. Теория воды и ионного раствора с особым упором на ионы водорода и гидроксила. Дж. Хим. физ. 1933;1:515–548. doi: 10.1063/1.1749327. [CrossRef] [Google Scholar]
29. Маркус Ю. Влияние ионов на структуру воды: создание и разрушение структуры. хим. 2009; 109:1346–1370. doi: 10.1021/cr8003828. [PubMed] [CrossRef] [Google Scholar]
30. Hirschfeld T. Определение солености с помощью NIRA. заявл. Спектроск. 1985; 39: 740–741. doi: 10.1366/0003702854250293. [CrossRef] [Google Scholar]
заявл. Спектроск. 1985; 39: 740–741. doi: 10.1366/0003702854250293. [CrossRef] [Google Scholar]
31. Уильямс П., Норрис К. В кн.: Технология ближнего инфракрасного излучения в сельском хозяйстве и пищевой промышленности. 2-е изд. Уильямс П., Норрис К., редакторы. Американская ассоциация химиков-зерновых, Inc.; Сент-Пол, Миннесота, США: 2001. [Google Scholar]
32. Каффка К.Я., Хорват Л., Кульчар Ф., Варади М. Исследование состояния воды в волокнистых пищевых продуктах с помощью спектроскопии в ближней инфракрасной области. Акта Алимент. 1990; 19: 125–137. [Google Scholar]
33. Ивамото М., Уозуми Дж., Нишинари К. Предварительное исследование воды в пищевых продуктах с помощью спектроскопии в ближней инфракрасной области. В: Hello J., Kaffka KJ, Gonczy JL, редакторы. Материалы Международной конференции по спектроскопии диффузного отражения/пропускания в ближнем инфракрасном диапазоне. Академия Киадо; Будапешт, Венгрия: 1987. С. 3–12. [Google Scholar]
34. Маэда Х.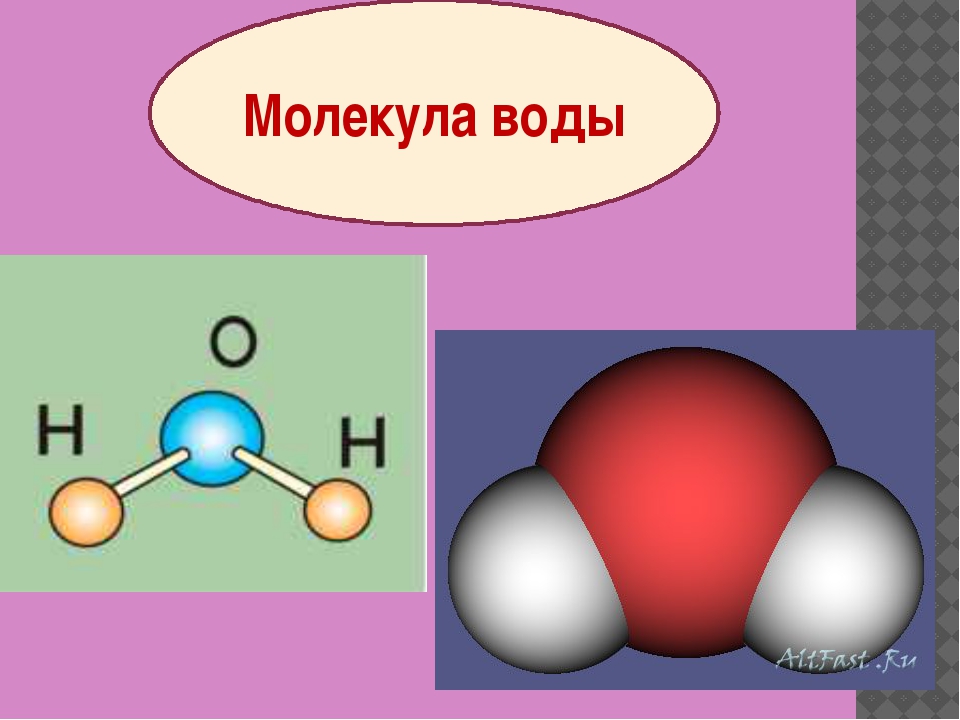 , Одзаки Ю., Танака М., Хаяси Н., Кодзима Т. Спектроскопия в ближней инфракрасной области и хемометрические исследования температурно-зависимых спектральных вариаций воды: связь между спектральными изменениями и водородными связями. J. Ближний инфракрасный спектр. 1995; 3: 191–201. doi: 10.1255/jnirs.69. [CrossRef] [Google Scholar]
, Одзаки Ю., Танака М., Хаяси Н., Кодзима Т. Спектроскопия в ближней инфракрасной области и хемометрические исследования температурно-зависимых спектральных вариаций воды: связь между спектральными изменениями и водородными связями. J. Ближний инфракрасный спектр. 1995; 3: 191–201. doi: 10.1255/jnirs.69. [CrossRef] [Google Scholar]
35. Гоуэн А.А., Эскерре К., О’Доннелл К.П., Дауни Г., Ценкова Р. Использование гиперспектральных изображений в ближней инфракрасной области для определения координат водной матрицы в грибах (Agaricus bisporus), подвергшихся воздействию к механической вибрации. J. Ближний инфракрасный спектр. 2009 г.;17:363–371. doi: 10.1255/jnirs.860. [CrossRef] [Google Scholar]
36. Smith J.D., Cappa C.D., Wilson K.R., Geissler P.L., Cohen R.C., Saykally R.J. Единое описание температурно-зависимых перегруппировок водородных связей в жидкой воде. проц. Натл. акад. науч. США. 2005;102:14171. doi: 10.1073/pnas.0506899102. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
37. Ценкова Р., Ковач З., Кубота Ю. Аквафотомика: спектроскопия в ближней инфракрасной области и состояние воды в биологических системах. В: ДиСальво Э.А., редактор. Мембранная гидратация. Спрингер; Чам, Швейцария: 2015. стр. 189.–211. [PubMed] [Google Scholar]
Ценкова Р., Ковач З., Кубота Ю. Аквафотомика: спектроскопия в ближней инфракрасной области и состояние воды в биологических системах. В: ДиСальво Э.А., редактор. Мембранная гидратация. Спрингер; Чам, Швейцария: 2015. стр. 189.–211. [PubMed] [Google Scholar]
38. Коллинз Дж. Р. Изменение спектра инфракрасного поглощения воды в зависимости от температуры. физ. 1925; 26: 771–779. doi: 10.1103/PhysRev.26.771. [CrossRef] [Google Scholar]
39. Фрэнкс Ф., редактор. Вода: всеобъемлющий трактат. Пленум Пресс; Нью-Йорк, штат Нью-Йорк, США: 1973. стр. 276–279. [Google Scholar]
40. Иноуэ А., Кодзима К., Танигучи Ю., Судзуки К. Ближние инфракрасные спектры воды и водных растворов электролитов при высоких давлениях. Дж. Солют. хим. 1984;13:811–823. doi: 10.1007/BF00647696. [CrossRef] [Google Scholar]
41. Мольт К., Нимеллер А., Чо Ю. Дж. Анализ водных растворов с помощью спектрометрии в ближней инфракрасной области (БИКС) II. Титрование слабых и очень слабых кислот сильными основаниями. Дж. Мол. Структура 1997; 410–411: 565–572. doi: 10.1016/S0022-2860(96)09706-2. [CrossRef] [Google Scholar]
Дж. Мол. Структура 1997; 410–411: 565–572. doi: 10.1016/S0022-2860(96)09706-2. [CrossRef] [Google Scholar]
42. Фрост В.Дж., Молт К. Анализ водных растворов методом спектрометрии в ближней инфракрасной области спектра (БИКС) III. Бинарные смеси неорганических солей в воде. Дж. Мол. Структура 1997;410:573–579. doi: 10.1016/S0022-2860(96)09707-4. [CrossRef] [Google Scholar]
43. Лин Дж., Браун К. В. Спектроскопическое измерение солености морской воды в ближнем ИК-диапазоне. Окружающая среда. науч. Технол. 1993; 27:1611–1615. doi: 10.1021/es00045a017. [CrossRef] [Google Scholar]
44. Ксантеас С.С. Неэмпирические исследования циклических кластеров воды (h3O)n, n=1–6. III. Сравнение функционала плотности с результатами MP2. Дж. Хим. физ. 1995;102:4505. дои: 10.1063/1.469499. [CrossRef] [Академия Google]
45. Robertson W.H., Diken E.G., Price E.A., Shin J.-W., Johnson M.A. Спектроскопическое определение сольватной оболочки OH- в кластерах OH-(h3O)n. Наука. 2003; 299:1367–1372. doi: 10.1126/science.1080695. [PubMed] [CrossRef] [Google Scholar]
doi: 10.1126/science.1080695. [PubMed] [CrossRef] [Google Scholar]
46. Cattaneo T.M.P., Cabassi G., Profaizer M., Giangiacomo R. Вклад рассеяния света в поглощение ближнего инфракрасного излучения молоком. J. Ближний инфракрасный спектр. 2009; 17: 337–343. doi: 10.1255/jnirs.867. [CrossRef] [Академия Google]
47. Siesler H.W., Ozaki Y., Kawata S., Heise H. In: Спектроскопия ближнего инфракрасного диапазона: принципы, инструменты, приложения. Siesler HW, Ozaki Y., Kawata S., Heise H., редакторы. Wiley-VCH Verlag GmbH; Weinheim, Germany: 2002. [Google Scholar]
48. Headrick J.M., Diken E.G., Walters R.S., Hammer N.I., Christie R.A., Cui J., Myshakin E.M., Duncan M.A., Johnson M.A., Jordan K.D. Спектральные признаки колебаний гидратированных протонов в кластерах воды. Наука. 2005; 308:1765–1769. doi: 10.1126/science.1113094. [PubMed] [CrossRef] [Google Scholar]
49. Чарник-Матусевич Б., Пилорз С. Исследование температурно-зависимых ближних инфракрасных спектров воды методами двумерной корреляционной спектроскопии и анализа главных компонент. Виб. Спектроск. 2006; 40: 235–245. doi: 10.1016/j.vibspec.2005.10.002. [CrossRef] [Google Scholar]
Виб. Спектроск. 2006; 40: 235–245. doi: 10.1016/j.vibspec.2005.10.002. [CrossRef] [Google Scholar]
50. Гоуэн А.А.А., Марини Ф., Цучисака Ю., Де Лука С., Бевилакуа М., О’Доннелл С., Дауни Г., Ценкова Р., О’Доннелл С. , Дауни Г. и др. О возможности спектроскопии в ближней инфракрасной области для обнаружения загрязнителей в воде с использованием растворов отдельных солей в качестве модельных систем. Таланта. 2015;131:609–618. doi: 10.1016/j.talanta.2014.08.049. [PubMed] [CrossRef] [Google Scholar]
51. Бюнинг-Пфауэ Х. Анализ воды в пищевых продуктах с помощью спектроскопии в ближней инфракрасной области. Пищевая хим. 2003; 82: 107–115. doi: 10.1016/S0308-8146(02)00583-6. [CrossRef] [Google Scholar]
52. Cowe I.A., McNicol J.W. Использование главных компонент в анализе спектров ближнего инфракрасного диапазона. заявл. Спектроск. 1985; 39: 257–266. doi: 10.1366/0003702854248944. [CrossRef] [Google Scholar]
53. Press W.H., Teukolsky S.A., Vetterling W.T., Flannery B. P. Численные рецепты в C: искусство научных вычислений. 2-е изд. Кембриджский университет Нажимать; Кембридж, Великобритания: 1992. [Google Scholar]
P. Численные рецепты в C: искусство научных вычислений. 2-е изд. Кембриджский университет Нажимать; Кембридж, Великобритания: 1992. [Google Scholar]
54. Чатани Э., Цучисака Ю., Масуда Ю., Ценкова Р. Динамика молекулярной системы воды, связанная с амилоидогенной нуклеацией, выявленная с помощью спектроскопии в ближней инфракрасной области спектра в реальном времени и аквафотомики. ПЛОС ОДИН. 2014;9:e101997. doi: 10.1371/journal.pone.0101997. [бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
55. Дэвисон А., Хинкли Д. Методы начальной загрузки и их применение (Кембриджская серия по статистической и вероятностной математике) Издательство Кембриджского университета; Кембридж, Великобритания: 1997. [Google Scholar]
56. RStudio . RStudio: интегрированная среда разработки для R. RStudio; Бостон, Массачусетс, США: 2012. [Google Scholar]
57. Основная группа R Development. R: язык и среда для статистических вычислений. Основная группа разработчиков R; Вена, Австрия: 2017. [Google Scholar]
[Google Scholar]
58. Ковач З., Поллнер Б. Аквафотомика Курс анализа данных и программное обеспечение; Труды аквафотомики: понимание воды в биологии — 2-й международный симпозиум; Кобе, Япония. 26–29Ноябрь 2016 г. [Google Scholar]
советов, как сделать отличные снимки молекул воды
Молекулы воды являются строительными блоками всей жизни. Они необходимы для всех известных форм жизни и играют жизненно важную роль во многих биохимических процессах. Несмотря на их важность, молекулы воды, как известно, трудно изучать из-за их небольшого размера и того факта, что они постоянно находятся в движении. Один из лучших способов изучить молекулы воды — это сфотографировать их. Это может показаться сложной задачей, но при наличии подходящего оборудования и терпения каждый может сделать красивые снимки молекул воды. Вот несколько советов, которые помогут вам начать работу: 1. Используйте мощный микроскоп. Молекулы воды очень малы, поэтому вам понадобится мощный микроскоп, чтобы их рассмотреть. Обычного светового микроскопа будет недостаточно. 2. Используйте камеру с высоким разрешением. Опять же, поскольку молекулы воды очень малы, вам понадобится камера с высоким разрешением, чтобы четко их увидеть. 3. Будьте терпеливы. Молекулы воды постоянно находятся в движении, поэтому для получения четкой картины может потребоваться некоторое время. Будьте терпеливы и продолжайте пробовать, пока не получите желаемый снимок. Имея в виду эти советы, вы сможете делать отличные снимки молекул воды в кратчайшие сроки.
Обычного светового микроскопа будет недостаточно. 2. Используйте камеру с высоким разрешением. Опять же, поскольку молекулы воды очень малы, вам понадобится камера с высоким разрешением, чтобы четко их увидеть. 3. Будьте терпеливы. Молекулы воды постоянно находятся в движении, поэтому для получения четкой картины может потребоваться некоторое время. Будьте терпеливы и продолжайте пробовать, пока не получите желаемый снимок. Имея в виду эти советы, вы сможете делать отличные снимки молекул воды в кратчайшие сроки.
Можем ли мы сфотографировать молекулы?
Image by – https://pluspng.com В течение достаточно долгого времени исследователи использовали для этой цели атомно-силовую микроскопию (АСМ) и сканирующую туннельную микроскопию (СТМ). Эти фотографии, в отличие от наших изображений, не представляют собой изображения, которые мы обычно используем для измерения составляющих молекул; скорее, они действуют как косвенные измерения свойств молекул.
Могу ли я видеть атомы и молекулы? В настоящее время определение структуры молекулы все еще остается сложной задачей. Усилия по решению этой проблемы значительно ускорились благодаря достижениям в таких методах, как спектроскопия ядерного магнитного резонанса (ядерно-магнитного резонанса) или дифракция рентгеновских лучей на монокристаллах. Исследователи ранее сообщали о визуализации легких атомов и молекул на графене, но это был первый случай обнаружения легких атомов и молекул. Исследователи из Оксфорда и IBM использовали СТМ-АСМ для создания и визуализации на месте первого аллотропа углерода первого порядка. С 2013 года атомная микроскопия позволила напрямую визуализировать молекулярные структуры в химических реакциях. 9Изображение , полученное с помощью атомно-силового микроскопа 0127, позволило наблюдать структурную структуру молекулы, где каждая часть головоломки была расположена правильно.
Это позволило выявить ранее неизвестную структуру молекулы (а). тиострептон определяет структуру сложных молекул , поскольку ее можно однозначно установить, анализируя их структуру. Похоже, что атомная микроскопия останется жизнеспособным инструментом для определения структуры в будущем; это может быть одним из инструментов, на которые химики будут чаще полагаться в будущем.
тиострептон определяет структуру сложных молекул , поскольку ее можно однозначно установить, анализируя их структуру. Похоже, что атомная микроскопия останется жизнеспособным инструментом для определения структуры в будущем; это может быть одним из инструментов, на которые химики будут чаще полагаться в будущем.
Электронная микроскопия, новый тип электронного микроскопа , использует пучки электронов для визуализации отдельных молекул. Микроэлектромеханические системы (МЭМС), как и увеличительные стекла, позволяют нам наблюдать за вещами в гораздо меньших масштабах. Молекулы имеют маленькие и хрупкие молекулы, которые быстро разрушаются при бомбардировке электронами на соответствующей длине волны. Из-за этого ограничения электронную микроскопию можно рассматривать только с источником видимого света. С другой стороны, электронная микроскопия может стать мощным инструментом для изучения структуры и поведения молекул. Эта информация будет полезна для понимания того, как работают молекулы и как создаются новые лекарства и материалы. Электронная микроскопия является важной технологией для понимания структуры и поведения молекул.
Электронная микроскопия является важной технологией для понимания структуры и поведения молекул.
Невероятные изображения молекул показывают сложные реакции
Молекулы чрезвычайно малы — размером всего несколько атомов — и их можно увидеть только в очень продвинутый микроскоп. Был разработан бесконтактный атомно-силовой микроскоп, который позволяет исследователям рассматривать молекулу непосредственно перед и после сложной органической реакции. Таким образом, они смогли наблюдать, как изменяется структура молекулы. Молекулы чрезвычайно малы, их диаметр составляет всего несколько атомов, и их можно увидеть только в самые современные микроскопы. электронные микроскопы обычно используются для исследования молекул, причем наиболее распространены просвечивающие электронные микроскопы.
Вы видите молекулы воды?
Изображение – https://nsf.gov Вы можете ответить на свой вопрос точно так же, как и на свой вопрос. Молекулы – это крошечные частицы в воде. На самом деле они намного меньше, чем это, что делает их невидимыми невооруженным глазом.
На самом деле они намного меньше, чем это, что делает их невидимыми невооруженным глазом.
Исследователи недавно использовали STM для изучения локальной структуры водопроводных сетей в ходе исследования. V-образные молекулы h3O образуются путем размещения двух атомов водорода по бокам от одного атома кислорода. СТМ — отличный инструмент для понимания взаимодействия молекул воды в сетях воды, потому что технология водородных связей позволяет им взаимодействовать с постоянной скоростью. Понимание локальной структуры водных сетей может помочь исследователям лучше понять, как вода ведет себя в0127 уровень одиночной молекулы .
Различные варианты использования сканирующего туннельного микроскопа
Сканирующий туннельный микроскоп (СТМ) представляет собой очень мощный инструмент, который можно использовать для исследования локальной структуры водных сетей на уровне одной молекулы. СТМ имеет множество преимуществ по сравнению с традиционными методами, помимо возможности изучать молекулы, которые менее чем в 100 000 раз шире человеческого волоса.

