Модель вулкана своими руками из бумаги или монтажной пены
Содержание
- Модель вулкана
- Модель вулкана промышленного изготовления
- Модель вулкана своими руками из бумаги и бутылки
- Модель вулкана из монтажной пены и бутылки
- Презентация состояний веществ в стаканах
- Плавление и кипение
- Демонстрация слоёв вещества в пробирке
Модель вулкана
Среди материалов зоны географии в школе Монтессори для детей от 6 до 12 лет особое место занимает модель вулкана. Она используется и в Большой истории №1, и сама по себе при изучении географических объектов и теории дрейфа континентов. Детям очень нравится этот материал, они готовы работать с ним бесконечно.
Такая модель может быть трёх типов.
Модель вулкана промышленного изготовления, сода, уксусная кислота, средство для мытья посуды
Модель вулкана промышленного изготовленияСамый простой и вместе с тем привлекательный вариант — поискать и приобрести в магазине развивающих игрушек материал из пластика. Помимо сборного конуса вулкана, он обычно включает трубку и шприц.
Помимо сборного конуса вулкана, он обычно включает трубку и шприц.
В модель насыпают пищевую соду и наливают немного жидкого мыла или средства для мытья посуды желательно красного цвета. В шприц набирают уксусную кислоту в концентрации от 3 до 9% или аналогичный раствор лимонной кислоты. Помните, что 70-процентная уксусная эссенция очень опасна!
Подсоединив шприц к трубке, ведущей снизу в жерло, и выдавливая в неё уксусную кислоту, мы получаем «извержение»: образующаяся в кратере пена начинает переливаться через край и стекать по склонам вулкана.
Интересно, что трубка и шприц не только необходимы для приведения макета в действие, но и сами демонстрируют роль глубинного магматического очага, в котором формируется магма, и вулканического канала, по которому магма поступает к кратеру. Стекающая по склонам конуса пена позволяет объяснить принцип образования гор аккумулятивного типа, состоящих из слоёв затвердевшей лавы нескольких извержений.
Вулкан из картона и бутылки
Модель вулкана своими руками из бумаги и бутылкиЕсли не удалось приобрести готовый макет, сделайте его своими руками. Можно привлечь к этому занятию детей.
Можно привлечь к этому занятию детей.
Нам потребуется стеклянная бутылка с широким горлом примерно на 200–250 мл, используемая при капельницах. Конус вулкана изготавливается из плотной бумаги или картона. Внутренний и внешний радиусы выкройки конуса подбираются из расчёта, что верхним вырезом фигура будет надеваться на горлышко бутылки, а нижней стороной стоять на подносе. Картонный конус следует раскрасить радиальными мазками коричневой и чёрной акриловой краской, придающей бумаге после высыхания водоотталкивающие свойства.
Чтобы привести такой вулкан в действие, в бутылку доверху насыпают соду, доливают в неё средство для мытья посуды или жидкое мыло. Затем прямо в «жерло» нужно долить раствор уксусной или лимонной кислоты.
Чтобы изготовить прочную конструкцию, сделайте вокруг бутылки конус из строительной пены
Модель вулкана из монтажной пены и бутылкиНедостаток бумажного макета — недолговечность картонного конуса. Он промокает и быстро приходит в негодность. Долговечную конструкцию можно изготовить из строительной пены.
Долговечную конструкцию можно изготовить из строительной пены.
Бутылку ставим в центр подноса и вокруг неё аккуратно делаем из пены концентрические круги. Делать такую модель лучше в отсутствие детей в проветриваемом помещении, поскольку пары от пены вредны. Также дети могут измазаться материалом, а он очень плохо удаляется с кожи и одежды.
Получившийся конус на сутки оставляем сохнуть, а потом срезаем лишнюю пену со склонов вулкана острым ножом, после чего раскрашиваем акриловыми красками.
Приводится в действие эта модель так же, как и бумажная.
Презентация состояний веществ в стаканах
Одна из базовых презентаций по географии (или лучше называть это естествознанием) в школьном Монтессори-курсе 6–12 по стандарту АМИ — демонстрация состояний вещества в стаканах. Она проводится в форме трёхэтапного урока.
Поясним, что по-английски его называют three period lesson — «урок, состоящий из трёх периодов». В России неизвестно откуда появился перевод «трёхступенчатый урок». Однако, «ступени» подразумевают, что одна из них выше, а другая ниже, и это пример того, как заимствуемые в русский язык термины и понятия искажают свой первоначальный смысл. Поэтому мы предлагаем использовать более адекватный оригиналу перевод «трёхэтапный урок» (вместо «трёхступенчатого», поскольку «трёхпериодный» коряво звучит по-русски).
Однако, «ступени» подразумевают, что одна из них выше, а другая ниже, и это пример того, как заимствуемые в русский язык термины и понятия искажают свой первоначальный смысл. Поэтому мы предлагаем использовать более адекватный оригиналу перевод «трёхэтапный урок» (вместо «трёхступенчатого», поскольку «трёхпериодный» коряво звучит по-русски).
Вернёмся к презентации и материалу для неё. Потребуется три гладких прозрачных стакана. Один оставляем пустым, во второй наливаем немного воды, в третий кладём небольшой металлический болт, гайку, шайбу. В небольшую банку кубической формы до половины насыпаем одинаковые круглые бусинки, похожие на бусины в зоне математики, а также берём куб 1000 (можно взять куб меньшего размера из кабинета цепей).
Также понадобится поднос педагога, на котором находятся:
- простой карандаш;
- ножницы;
- стиральная резинка;
- заранее нарезанные полоски бумаги шириной 2–2,5 см (скреплённые канцелярским зажимом).
Трёхэтапный урок по агрегатным состояниям веществ:
- 1-й этап: показываем ученикам сосуд с водой и спрашиваем: «В каком состоянии находится вещество?».

- 2-й этап: переставляем местами ёмкости и забираем подписи к ним, просим детей разложить полоски бумаги в правильном порядке. Если ученикам это удалось, значит, они правильно поняли тему. В первую очередь спрашивают детей, которые только начинают читать. Одновременно ученики тренируются в чтении рукописных букв (слов).

- 3-й этап урока: переставляем местами ёмкости и убираем надписи, просим детей назвать самостоятельно состояния вещества, сделать собственные надписи и разложить их. Гиду следует отстраниться от детей и дать им поработать самостоятельно.
Дальнейшая работа. Объясняем, с чем связаны отличия в состоянии веществ. Показываем баночку с бусинами, поворачивая её: «Посмотрите внимательно, как меняется форма бусинок при поворачивании. Эта жидкость из бусин как бы перетекает, принимая форму банки, но её количество и объём не изменяются. То же самое происходит в стакане с жидкостью, которая состоит из очень мелких частиц-молекул». Демонстрируем перетекающую в сосуде воду.
Теперь берём куб из бусин, показываем, как бусинки прочно скреплены и поэтому куб сохраняет форму и объём, говорим: «Вот так устроено твёрдое тело. Его частицы-атомы прочно скрепляются друг с другом, и твёрдое тело сохраняет не только объём, но и форму».
В пустой стакан кладём несколько бусинок, закрываем ладонью и сильно трясём. Бусины при этом летают и ударяются о стенки. «Вот так ведут себя молекулы газообразного вещества. Одни быстро движутся и сталкиваются друг с другом и со стенками. Поэтому газ легко меняет и форму и объём».
Бусины при этом летают и ударяются о стенки. «Вот так ведут себя молекулы газообразного вещества. Одни быстро движутся и сталкиваются друг с другом и со стенками. Поэтому газ легко меняет и форму и объём».
В заключение рекомендуем поиграть в следующую игру: просим учеников встать и показываем, как по команде «газообразное вещество» нужно просто бегать по ковру в классе и сталкиваться между собой. По команде «жидкое вещество» играющие берутся за руки и водят хоровод, изменяющий свою форму. По команде «твёрдое вещество» дети цепляются друг за друга локтями и медленно ходят как единое целое, не меняя образованной формы. Ученикам очень нравится играть в эту игру и чувствовать себя «молекулами» в различных состояниях.
Плавление и кипение
После того как мы познакомили детей с состояниями вещества, нужно показать им, как происходят переходы из одного состояния в другое.
Понадобятся:
- простейшая одноконфорочная электроплитка;
- три металлические формы для выпечки кексов;
- небольшой кусок парафина от свечи;
- лабораторные щипцы.

Электроплиту для безопасности ставим на большую керамическую плитку для пола. Приносим на подносе стаканы с теми образцами, которые использовали для демонстрации твёрдого, жидкого и газообразного состояний вещества.
Детям, которые соберутся на презентацию, говорим: «В прошлый раз мы изучали состояния веществ. Это…» И показываем стакан, в котором немного воды. Делаем паузу и ждём, пока участники припомнят и назовут состояние — «жидкое». Потом берём сосуд с болтиком, гайкой и шайбой, звеним ими: «А это вещество…», и не спешим отвечать сами. Ждём, пока нам не подскажут: «Твёрдое».
Показываем третий стакан — «пустой». Спрашиваем: «А что здесь? Какое это состояние вещества?» И дети отвечают: «Газ. Газообразное».
Ставим формочки на конфорку: спустя какое-то время парафин плавится, а вода закипает
Переходим к новой презентации: «Теперь посмотрим, можно ли превращать одно состояние вещества в другое. Давайте попробуем нагреть твёрдые и жидкие материалы и посмотрим, что с ними произойдёт».
Пересыпаем болт, гайку и шайбу из стакана в формочку для выпечки и ставим её на конфорку. Переливаем немного воды в другую форму и тоже ставим её на плиту. Говорим: «Давайте возьмём другое твёрдое вещество и посмотрим, что будет с ним».
Кладём в третью форму кусочки парафина от свечи и тоже ставим на конфорку. Включаем плитку и наблюдаем.
Спустя некоторое время начинает плавиться парафин. Как правило, дети сами замечают этот процесс. Помогаем им сформулировать вывод: «При нагревании парафин перешёл из твёрдого состояния в жидкое».
Затем закипает вода. На дне формочки появляются и растут пузырьки пара, потом они отрываются и всплывают. И вот парообразование переходит в бурное кипение.
Объясняем: «Вот у нас жидкое вещество переходит в газ, пар. Такое бурное парообразование называется кипением».
Болты после нагревания не изменили своего состояния, остались твёрдыми
Снимаем щипцами формочки с расплавленным парафином и кипящей водой и ставим на керамическую плиту. Обращаем внимание детей на то, что кипение сразу прекращается: «Для кипения нужно непрерывное нагревание».
Обращаем внимание детей на то, что кипение сразу прекращается: «Для кипения нужно непрерывное нагревание».
Теперь смотрим на болт, гайку и шайбу. Они не изменили своего состояния, остались твёрдыми. Спрашиваем у детей, почему это произошло. Если они затрудняются с ответом, подсказываем: «Видимо, нагревание на электроплитке было недостаточным. Существуют специальные печи, в которых температура намного выше, и тогда металл плавится, как и парафин».
К этому моменту формочка с расплавленным парафином уже остыла, и он начинает затвердевать. Наблюдаем за этим и обсуждаем с детьми то, что они видят: «А это обратное превращение из жидкого состояния в твёрдое, если происходит охлаждение. Какой ещё пример вы можете привести, когда жидкое вещество при остывании становится твёрдым?» И дети, как правило, вспоминают, что вода при охлаждении превращается в лёд и снег.
После снятия с плиты парафин застывает
Эта презентация и используемые материалы дают базовые понятия, необходимые для понимания процессов в природе и быту, а также подготавливают к Большой истории №1.
А вот ещё один опыт, который подготовит к Большой истории №1
Демонстрация слоёв вещества в пробирке
Чтобы показать это явление, нам понадобятся:
- стеклянная пробирка;
- три жидкости: тёмный мёд (или патока), вода и растительное масло;
- штатив (стойка) для пробирок.
Приглашаем школьников посмотреть презентацию. Собрав детей, медленно и осторожно, чтобы не запачкать стенки пробирки, наливаем на её дно мёд, затем — воду и в конце — масло. Спрашиваем: «Что получилось в пробирке?» Немного выждав, помогаем детям сформулировать выводы проведённого опыта: вещества образуют слои.
Показав пробирку, её следует поставить в стойку и на несколько дней оставить в комнате, чтобы дети могли её видеть и брать в руки.
Не нужно объяснять им, что внизу — самое плотное вещество, а вверху — самое лёгкое, ведь они ещё недостаточно знакомы с понятиями плотности или веса (тяжести). Наоборот, именно это наблюдение позволит школьникам потом освоить эти понятия.
Применение таких бытовых материалов, как мёд и масло, — важный приём: дети, всякий раз сталкиваясь с использованными в опыте веществами, будут вспоминать об этом наблюдении и возвращаться к его обдумыванию.
Эксперимент со слоями позволит представить себе:
- как возникли слои-оболочки Земли: атмосфера, гидросфера, литосфера, барисфера;
- как образовывались слои осадочных пород;
- как протекали геологические процессы горообразования.
Фото автора
Бесплатные уроки от экспертов
Помогут сделать первый шаг в создании развивающего пространства для вашего ребёнка дома
План-конспект урока физики в 5-м классе по теме «Строение вещества»
Тип урока: Урок изучения нового материала.
Цели урока:
- Образовательные: вызвать объективную необходимость изучения нового материала; способствовать овладению знаниями по теме “Строение вещества. Молекулы”.
- Развивающие: содействовать развитию речи, мышления, познавательных и общетрудовых умений; продолжить работу по формированию умений делать выводы из наблюдений.
- Воспитательные: формировать добросовестное отношение к учебному труду, положительную мотивацию к учению; способствовать воспитанию гуманности, дисциплинированности, эстетического восприятия мира.
Оборудование: компьютер, мультимедийный проектор, приборы и материалы для демонстрационных и фронтальных опытов.
Фронтальные опыты: делимость куска мела, испарение капельки спирта, сжатие воздуха в медицинском шприце, деформация растяжения резинового жгута.
Демонстрационные опыты: делимость воды, делимость воздуха, деформация
резинового шарика, заполненного воздухом, смешивание гороха и пшена, воды и
спирта, изменение объема стального шарика при изменении температуры, поднятие и
опускание уровня жидкости в трубке, в резервуаре термометра, растворение
кристаллика марганцовки в воде.
Ход урока
- Что такое температура?
- Чем её измеряют? В каких единицах?
- Расскажите об устройстве и принципе действия термометра.
Презентация
Учитель: Все окружающее человека – вода, воздух, горы, деревья –
обладают своими свойствами. Объекты отличаются по форме, цвету, запаху, у них
различные свойства. Две маленькие капли воды сливаются в одну, но в то же время
два стальных шарика при ударе отскакивают друг от друга. Немного нагрев кусок
воска, мы наблюдаем, как он превращается в жидкость. Почему это происходит?
Почему каучук упругий, а воск мягкий? Почему при нагревании твердые тела
превращаются в жидкости, а жидкости — в газ? Чтобы ответить на этот вопрос,
необходимо иметь представление о строении вещества. Знания о строении вещества
помогают не только объяснять суть явления, они помогают предсказывать, как будет
происходить явление, что нужно сделать, чтобы его ускорить или замедлить, т.е.
помогают управлять явлениями. Изучив строение тел, можно объяснить их свойства,
а также создать новые вещества с нужными свойствами – твердые и прочные сплавы,
жароупорные материалы. Так были созданы такие материалы, как пластмассы, каучук,
капрон, лавсан, нашедшие широкое применение в технике, медицине и быту (слайд
2). О строении вещества помогают судить некоторые явления и опыты. И сегодня мы
с вами проведём опыты, которые нам помогут узнать о строении вещества.
Знания о строении вещества
помогают не только объяснять суть явления, они помогают предсказывать, как будет
происходить явление, что нужно сделать, чтобы его ускорить или замедлить, т.е.
помогают управлять явлениями. Изучив строение тел, можно объяснить их свойства,
а также создать новые вещества с нужными свойствами – твердые и прочные сплавы,
жароупорные материалы. Так были созданы такие материалы, как пластмассы, каучук,
капрон, лавсан, нашедшие широкое применение в технике, медицине и быту (слайд
2). О строении вещества помогают судить некоторые явления и опыты. И сегодня мы
с вами проведём опыты, которые нам помогут узнать о строении вещества.
Опыт 1.
Учитель: У вас на парте лежит кусочек мела. Разломите его. Можно ли его ещё разделить на части?
Ученик: Да.
Учитель: Как?
Ученик: Разломить еще.
Учитель: Дробление веществ доказывает их дискретность (делимость). Проведите пальцем по поверхности мела. Что остаётся у вас на руках?
Ученик: Частички мела.
Учитель: Из чего же состоит кусок мела?
Ученик: Из частиц мела.
Опыт 2.
Учитель: Возьмём стакан с водой. Можем ли мы воду разделить на более мелкие порции?
Ученик: Да.
Учитель: Как?
Ученик: Отлить в другой стакан.
Учитель: А эти порции ещё на более мелкие?
Ученик: Да.
Учитель: И эта маленькая порция из чего будет состоять?
Ученик: Из частиц воды.
Опыт 3.
Учитель: А можно ли воздух поделить на более мелкие порции?
Ученик: Нет.
Учитель: Возьмем воздушный шарик. Выпустим из него часть воздуха. Потом
еще часть воздуха. И эта маленькая порция воздуха из чего будет состоять.
И эта маленькая порция воздуха из чего будет состоять.
Ученик: Из частиц.
Учитель: Возможен и обратный процесс – получение целого из отдельных частей (две капли воды могут слиться в одну большую каплю, из отдельных кирпичей можно построить большой дом, множество песчинок образуют песчаные дюны).
Опыт 4.
Учитель: Капнем немного спирта на фильтровальную бумагу. (Учитель проходит по рядам и капает на кусочки фильтровальной бумаги капельку спирта). Пятно через некоторое время исчезает. Куда исчез спирт?
Ученик: Испарился.
Учитель: Мгновенно ли он исчез?
Ученик: Нет.
Учитель: Видели ли вы, как спирт “покидал” бумагу?
Ученик: Нет.
Учитель: Какую гипотезу о строении вещества можно выдвинуть для объяснения такого постепенного исчезновения?
Ученик: Вещество состоит из частиц.
Учитель: Запишите в тетрадь этот вывод
“Вещество состоит из частиц” (слайд 3). То, что
вещества состоят из мельчайших частиц, объясняет распространение запаха,
испарение жидкости и твердых тел.
То, что
вещества состоят из мельчайших частиц, объясняет распространение запаха,
испарение жидкости и твердых тел.
Опыт 5.
Учитель: Возьмём воздушный шарик. Надавим на него. Что изменилось?
Ученик: И форма и объём.
Учитель: Какое вещество находится внутри шарика?
Ученик: Воздух.
Учитель: Из чего он состоит?
Ученик: Из частиц.
Учитель: Изменилось ли их число?
Ученик: Нет.
Учитель: А сами частицы могли уменьшиться в размере?
Ученик: Нет.
Учитель: Тогда как вы можете объяснить изменение объёма воздуха в шарике?
Ученик: Между частицами воздуха есть промежутки.
Опыт 6.
Учитель: Смешаем горох и пшено, взятые в равных объёмах (учитель смешивает вещества, тщательно встряхивает емкость со смесью). Что можно сказать об объеме смеси?
Ученик: Получили заметно меньший объем, чем сумма объёмов гороха и пшена,
взятых в отдельности.
Опыт 7.
Учитель: Смешаем воду и спирт, взятых в равных объемах. (Спирт можно заменить ацетоном или насыщенным раствором сульфатаммония). Получили заметно меньший объем, чем сумма объёмов воды и спирта, взятых в отдельности. Какой вывод можно сделать из этих опытов?
Ученик: Между частицами есть промежутки.
Опыт 8.
Учитель: Возьмите шприц, зажмите отверстие для иглы пальцем и попытайтесь сжать в нем как можно сильнее воздух. На какую часть своего объема он сжался?
Ученик: Больше, чем наполовину.
Учитель: Почему?
Ученик: Промежутки между частицами уменьшаются.
Опыт 9.
Учитель: Возьмите резиновый жгут. Растяните его. Что можно сказать о промежутках между частицами резины в этом случае?
Ученик: Промежутки между частицами увеличиваются
Учитель: Все эти опыты указывают на то, что вещества состоят из отдельных
частиц, разделенных промежутками. Изменение расстояния между частицами приводит
к изменению объема тела.
Изменение расстояния между частицами приводит
к изменению объема тела.
Запишите в тетрадь этот вывод “Между частицами есть промежутки” (слайд 4).
Опыт 10.
Учитель: Возьмем металлический шарик и кольцо. Легко ли проходит металлический шарик сквозь кольцо? (Слайд 5, рис.1)
Ученик: Легко.
Учитель: Возьмём и подержим его в пламени спиртовки? Проходит ли теперь шарик сквозь кольцо?
Ученик: Нет.
Учитель: Как вы думаете почему?
Ученик: При нагревании расстояние между частицами увеличивается.
Учитель: Охладим шарик. Проходит сквозь кольцо?
Ученик: Свободно.
Учитель: Что же произошло при охлаждении шарика?
Ученик: Расстояние между частицами уменьшилось.
Опыт 11.
Учитель: При нагревании расширяются и жидкости. Колбу с водой закроем
пробкой, в которую вставлена узкая стеклянная трубка. При нагревании воды в
колбе уровень воды в трубке повышается, при охлаждении — понижается. (Слайд 5,
рис. 2). На этом основан принцип действия обычного термометра для измерения
температуры. В трубке термометра спирт.
При нагревании воды в
колбе уровень воды в трубке повышается, при охлаждении — понижается. (Слайд 5,
рис. 2). На этом основан принцип действия обычного термометра для измерения
температуры. В трубке термометра спирт.
Опыт 12.
Учитель: Если опустим термометр в горячую воду, что произойдёт через некоторое время? (Погружает термометр в сосуд с горячей водой).
Ученик: Спиртовая жидкость в трубке термометра будет подниматься.
Учитель: А если опустим его в холодную воду? (Учитель опускает термометр в сосуд с холодной водой).
Ученик: Жидкость в трубке будет опускаться.
Учитель: Какой вывод можно сделать из этих опытов?
Ученики: При изменении температуры промежутки между частицами изменяются. При этом изменяется объём вещества. (Слайд 6)
Учитель: Мы с вами каждый день наблюдаем ряд окружающих нас предметов:
столы, стулья, книги, парты. Теперь вы знаете, что все они состоят из частиц,
между которыми есть промежутки. Посмотрите на эти предметы. Разве вы видите
промежутки?
Теперь вы знаете, что все они состоят из частиц,
между которыми есть промежутки. Посмотрите на эти предметы. Разве вы видите
промежутки?
Ученик: Нет.
Учитель: Почему же эти тела кажутся нам сплошными, или они на самом деле являются таковыми?
Ученик: Частицы очень маленькие и их очень много.
Учитель: Действительно, то, что любая жидкость или твердое тело кажутся сплошными, указывает на очень малые размеры частиц и промежутков между ними. Докажем это. Проведём следующий опыт.
Опыт 13.
Учитель: Растворим маленькую крупинку марганцовки в воде, налитой в стакан. Отольём немного окрашенной воды в другой стакан и дольём в него чистую воду. Что наблюдаем?
Ученик: Раствор окрашен слабее.
Учитель: Повторим предыдущее действие. Что теперь наблюдаем?
Ученик: Раствор окрашен ещё слабее.
Учитель: С каждым разом мы убеждаемся в том, что раствор окрашен всё
слабее. Рассмотрим последний раствор. Он хотя и слабо, но равномерно окрашен.
Сохранилось ли основное свойство вещества — цвет — при уменьшении концентрации
раствора?
Рассмотрим последний раствор. Он хотя и слабо, но равномерно окрашен.
Сохранилось ли основное свойство вещества — цвет — при уменьшении концентрации
раствора?
Ученик: Да.
Учитель: Можете ли вы сделать предположение о том, сколько частичек марганцовокислого калия еще осталось в последнем стакане? А сколько их тогда было в первом стакане?
Ученик: Их очень много.
Учитель: Вспомнив размеры кристалликов, брошенных нами в воду, можете ли вы сказать что-либо о размерах мельчайших частиц вещества?
Ученик: Они очень маленькие.
Учитель: Запишите в тетрадь этот вывод “Частицы очень маленькие. Их очень много” (слайд 7). А теперь перед нами стоит проблема: “Сможем ли мы дальше делить раствор марганцовки? Т.е при любом сколь угодно большом количестве стаканов марганцовка будет обнаружена в последнем из них?”.
Ученик: Нет.
Учитель: Следовательно, в самой малой порции вещества очень много частиц,
которые очень малы и по размерам, и по массе.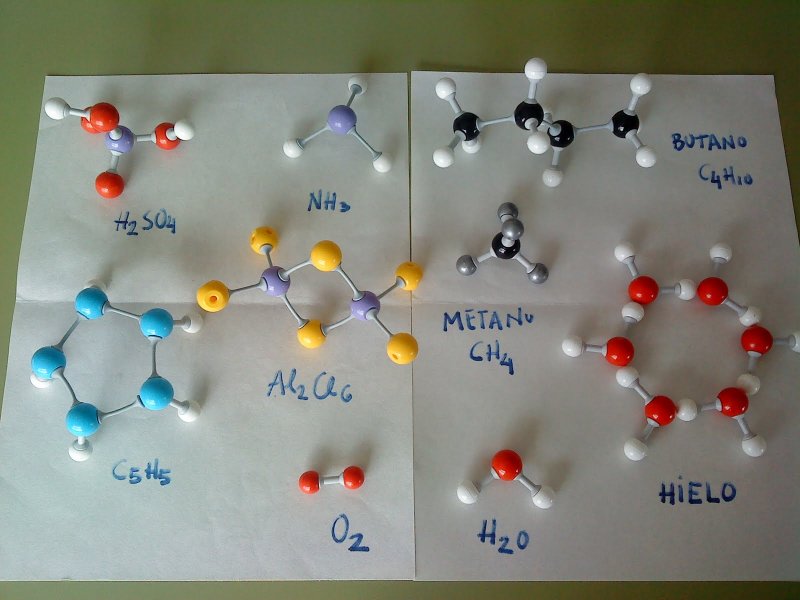 Запишите в тетрадях: “Молекула
– мельчайшая частица вещества” (слайд 8). Молекула — от лат “moles” —
масса с уменьшительным суффиксом “cula” — массочка. Сам термин появился в науке
сравнительно недавно (1647 г. фр. ученый Пьер Гассенди).
Самая малая частица воды – молекула воды. Самая малая частица сахара –
молекула сахара. Молекулы сохраняют основные свойства вещества. Молекула сахара
— сладкая. Молекула соли – солёная. Молекула марганцовки – розовая.
Запишите в тетрадях: “Молекула
– мельчайшая частица вещества” (слайд 8). Молекула — от лат “moles” —
масса с уменьшительным суффиксом “cula” — массочка. Сам термин появился в науке
сравнительно недавно (1647 г. фр. ученый Пьер Гассенди).
Самая малая частица воды – молекула воды. Самая малая частица сахара –
молекула сахара. Молекулы сохраняют основные свойства вещества. Молекула сахара
— сладкая. Молекула соли – солёная. Молекула марганцовки – розовая.
Учитель: А, как вы думаете, молекулы различных веществ одинаковы или нет?
Ученик: Нет.
Учитель: Лед, вода и водяной пар состоят из одних и тех же молекул или нет?
Ученик: Да.
Учитель: Почему?
Ученик: Потому что это одно и то же вещество, но в разном виде.
Учитель: Молекула сахара везде одна и та же: и в сахарнице и в варенье, и
в сладком чае. Нельзя отличить воду, полученную из сока или из молока, от воды,
полученной путем перегонки из морской воды. Запишите в тетрадях: “Молекулы
разных веществ различны. Молекулы одного вещества одинаковы” (слайд 9).
Запишите в тетрадях: “Молекулы
разных веществ различны. Молекулы одного вещества одинаковы” (слайд 9).
Учитель: Каковы же размеры молекул? Известно, что кусок сахара можно
растолочь на очень маленькие крупинки, зерно пшеницы размолоть в муку. Капля
масла, растекаясь по поверхности воды, может образовать плёнку, толщина которой
в десятки тысяч раз меньше диаметра человеческого волоса. Но в крупинке воды и в
толще масляной плёнки содержится не одна, а много молекул. Значит, размеры
молекул этих веществ ещё меньше, чем размеры крупинки муки и толщина плёнки.
Давай попробуем представить их размеры. Молекула во столько раз меньше яблока
среднего размера, во сколько раз яблоко меньше земного шара. (Слайд 11). Если бы
молекулы стали размером с точку на листе бумаги. Тогда все бы тела тоже
увеличились и верхушка Эйфелевой башни достала бы до Луны, люди бы были высотой
1700 км, мыши были бы длинной 100 км, а мухи – 7 км, каждый волос был бы
толщиной 100 м, красные тельца нашей крови – эритроциты имели бы в поперечнике 7
м. Вот еще пример: одна капля воды содержит столько же молекул, сколько таких
капель в Черном море. А вот примеры, дающие представление о количестве молекул в
небольшом объеме вещества. Если в океан вылить один литр спирта и дождаться
когда молекулы спирта распределятся равномерно по всей водной массе мирового
океана, то теперь в каком бы месте мирового океана мы ни зачерпнули воды
литровой кружкой, в ней найдется в среднем 7000 молекул того литра спирта,
который был вылит в океан. А в каждом зачерпнутом наперстке можно было бы
выловить 7 штук спиртовых молекул. А если взять число кирпичей, равное числу
молекул газа объемом с наперсток, и уложить их плотно, то эти кирпичи покрыли бы
поверхность всей суши земного шара слоем в 120 м, т.е. высотой в четыре
десятиэтажных дома.
Вот еще пример: одна капля воды содержит столько же молекул, сколько таких
капель в Черном море. А вот примеры, дающие представление о количестве молекул в
небольшом объеме вещества. Если в океан вылить один литр спирта и дождаться
когда молекулы спирта распределятся равномерно по всей водной массе мирового
океана, то теперь в каком бы месте мирового океана мы ни зачерпнули воды
литровой кружкой, в ней найдется в среднем 7000 молекул того литра спирта,
который был вылит в океан. А в каждом зачерпнутом наперстке можно было бы
выловить 7 штук спиртовых молекул. А если взять число кирпичей, равное числу
молекул газа объемом с наперсток, и уложить их плотно, то эти кирпичи покрыли бы
поверхность всей суши земного шара слоем в 120 м, т.е. высотой в четыре
десятиэтажных дома.
Учитель: Можно ли увидеть молекулы невооружённым глазом?
Ученик: Молекулы нельзя увидеть невооружённым глазом.
Учитель: Запишите в тетрадях: “Молекулы нельзя
увидеть невооружённым глазом” (слайд 12).
Учитель: Молекулы хоть и очень маленькие частицы, но они делимы. Молекулы состоят из атомов, частиц ещё более мелких. Запишите в тетрадях: “Молекулы состоят из атомов” (слайд 13). Истоки теории внутреннего строения вещества лежат в древности. Древнегреческий ученый Демокрит (слайд 14) впервые высказал гениальное предположение о том, что все тела состоят из мельчайших неделимых и неизменных частичек — атомов, которые находятся в движении и, взаимодействуя между собой, образуют все тела природы. Основные мысли учения Демокрита об атомах были изложены римским поэтом и философом Лукрецием Каром в классической поэме “О природе вещей”. Вот что он писал:
…Выслушай то, что скажу, и ты сам, несомненно, признаешь,
Что существуют тела, которых мы видеть не можем.
Ветер, во-первых, морей неистово волны бичует,
Рушит громады судов и небесные тучи разносит,
Или же, мчась по полям, стремительным кружится вихрем,
Мощные валит стволы, неприступные горные выси,
Лес низвергая, трясет порывисто: так, налетая,
Ветер, беснуясь, ревет и проносится с рокотом грозным.
Стало быть, ветры — тела, но только незримые нами…
…Далее, запахи мы обоняем различного рода,
Хоть и не видим совсем, как в ноздри они проникают.
Также палящей жары или холода нам не приметить
Зреньем своим никогда, да и звук увидать невозможно.
Но это все обладает, однако, телесной природой,
Если способно оно приводить наши чувства в движенье:
Ведь осязать, как и быть осязаемым, тело лишь может.
И, наконец, на морском берегу, разбивающем волны,
Платье сыреет всегда, а на солнце вися, оно сохнет;
Видеть, однако, нельзя, как влага на нем оседает,
Да и не видно того, как она исчезает от зноя.
Значит, дробится вода на такие мельчайшие части,
Что недоступны они совершенно для нашего глаза.
Так и кольцо изнутри, что долгое время на пальце
Носится, из году в год становится тоньше и тоньше;
Капля за каплей долбит, упадая, скалу; искривленный
Плуга железный сошник незаметно стирается в почве;
И мостовую дорог, мощенную камнями, видим
Стертой ногами толпы; и правые руки у статуй
Бронзовых возле ворот городских постепенно худеют
От припадания к ним проходящего мимо народа.
Нам очевидно, что вещь от стиранья становится меньше,
Но отделение тел, из нее каждый миг уходящих,
Нашим глазам усмотреть запретила природа ревниво.
Наблюдая различные природные явления, Демокрит пришел к убеждению, что тела только кажутся нам сплошными, на самом же деле они состоят из мельчайших частиц, но они настолько малы, что увидеть их невозможно. Демокрит предполагал, что у различных тел эти частицы различны по форме. Он назвал эти мельчайшие частички “атомами”, что по-гречески означает “неделимые”. Замечательная догадка Демокрита позднее была надолго забыта, и более тысячи лет в ученом мире безраздельно господствовало ошибочное учение Аристотеля, утверждавшего, что все вещества могут взаимно превращаться друг в друга. Аристотель категорически отрицал существование атомов. Любое тело можно делить до бесконечности — учил Аристотель.
В 1647 г. француз Пьер Гассенди издал книгу, в которой отрицал учение
Аристотеля и утверждал, что все вещества в мире состоят из неделимых частичек —
атомов, которые отличаются друг от друга формой, размерами и массой.
Таким образом, древние ученые высказали многое из современных представлений о строении вещества. В ту пору их высказывания являлись, конечно, лишь гениальными догадками, основанными на наблюдениях, но не подтвержденными никакими экспериментальными фактами.
Перед нами опять возникает проблема: Мы не видим атомов. Тела нам
представляются сплошными. Как же доказали их существование? Древние атомисты не
могли дать каких-либо прямых доказательств справедливости своей гипотезы. Только
наука XX в. представила многочисленные прямые доказательства существования
атомов и молекул. Ученые придумали приборы, которые помогают нам увидеть атомы. Атомы
можно увидеть в самые современные электронные и ионные микроскопы! (Слайды
15, 16, 17). Современные электронно-голографические микроскопы дают
увеличение в 70 миллионов раз. (Слайды 18 -24). Получены следы отдельных частиц
(камера Вильсона, пузырьковая камера). (Слайд 25).
(Слайд 25).
Учитель: Атомы каждого вида принято обозначать специальными символами. Например: (записываем на доске и в тетрадях): “О – атом кислорода, H – атом водорода, С – атом углерода” (слайд 26).
Молекулы также обозначаются специальными символами (химическими формулами). Например: О2 – молекула кислорода. Она состоит из 2-х атомов кислорода. Н2 – молекула водорода. Она состоит из 2-х атомов водорода. Н2О – молекула воды. Она состоит из 2-х атомов водорода и одного атома кислорода (слайд 27).
Учитель: Скажите, в состав молекулы входит один атом, два или более? И от чего зависит это количество?
Ученик: В состав молекулы может входить много атомов, это зависит от вещества.
Учитель: Атомов в природе чуть больше 100, но их комбинации создают то
огромное многообразие веществ, которое окружает нас. В природе 88 атомов,
остальные получены в лабораториях. Существуют молекулы-гиганты, в которых
содержатся тысячи и сотни тысяч атомов. Это молекулы каучука, клетчатки, других
органических веществ. Самые большие молекулы из известных – молекулы некоторых
белковых веществ- весят приблизительно в миллион раз больше молекулы воды.
Молекула гемоглобина, красящего вещества крови,
состоит из 1400 атомов, молекула пенициллина – из 41 атома. При помощи шариков
можно конструировать модели молекул. (Демонстрация пространственных
кристаллических решеток). М.В. Ломоносов (1711-1765) (слайд 28) — великий
просветитель и основатель науки в России писал, что молекула может быть
однородной и разнородной. В первом случае в молекуле группируются однородные
атомы, во втором -молекула состоит из нескольких видов атомов. Если какое-либо
тело составлено из однородных молекул, то его надо считать простым. Если тело
состоит из молекул, построенных из различных атомов, Ломоносов называл его
смешанным (слайд 29).
Существуют молекулы-гиганты, в которых
содержатся тысячи и сотни тысяч атомов. Это молекулы каучука, клетчатки, других
органических веществ. Самые большие молекулы из известных – молекулы некоторых
белковых веществ- весят приблизительно в миллион раз больше молекулы воды.
Молекула гемоглобина, красящего вещества крови,
состоит из 1400 атомов, молекула пенициллина – из 41 атома. При помощи шариков
можно конструировать модели молекул. (Демонстрация пространственных
кристаллических решеток). М.В. Ломоносов (1711-1765) (слайд 28) — великий
просветитель и основатель науки в России писал, что молекула может быть
однородной и разнородной. В первом случае в молекуле группируются однородные
атомы, во втором -молекула состоит из нескольких видов атомов. Если какое-либо
тело составлено из однородных молекул, то его надо считать простым. Если тело
состоит из молекул, построенных из различных атомов, Ломоносов называл его
смешанным (слайд 29). Не все тела состоят из молекул. Есть тела, состоящие из
атомов (алмаз, графит), ионов (поваренная соль). Атомы очень маленькие частицы,
но и они имеют сложное строение. Существуют ещё более мелкие частицы (протоны,
нейтроны, электроны), о которых вы узнаете позже.
Не все тела состоят из молекул. Есть тела, состоящие из
атомов (алмаз, графит), ионов (поваренная соль). Атомы очень маленькие частицы,
но и они имеют сложное строение. Существуют ещё более мелкие частицы (протоны,
нейтроны, электроны), о которых вы узнаете позже.
Учитель: Итак, вы теперь знаете, из чего состоят вещества. Глядя на свой опорный конспект в тетради, ответьте на вопросы:
- В чем заключается гипотеза о строении вещества?
- Почему не видны частицы, из которых состоят тела?
- Как объяснить высыхание белья после стирки?
Учитель: А теперь постарайтесь применить знания о строении вещества,
полученные на сегодняшнем уроке. Учитель предлагается ряд утверждений, ученики
записывают под соответствующим номером “да”, если считают утверждение верным,
или “нет”, если считают его неверным:
Учитель предлагается ряд утверждений, ученики
записывают под соответствующим номером “да”, если считают утверждение верным,
или “нет”, если считают его неверным:
I вариант
- Вещество состоит из мельчайших частиц, едва различимых невооруженным глазом (нет).
- Объем газа при нагревании увеличивается, так как каждая молекула становится больше по размеру (нет).
- Пленка масла, растекаясь по поверхности воды, может занять любую площадь (нет).
- Молекулы воды точно такие же, как и молекулы льда (да).
- Атомы состоят из молекул (нет).
II вариант
- Объем тела при нагревании уменьшается (нет).
- Объем жидкости при охлаждении уменьшается, так как промежутки между молекулами становятся меньше (да).
- При сжатии газа уменьшается размер молекул (нет).
 (слайд 30))
(слайд 30))
- Подведение итогов урока. Выставление оценок.
Учитель: Что ж, наш урок подходит к завершению. Я надеюсь, что полученные вами знания о строении вещества вы будете использовать не только на уроках по различным предметам, но и будете применять их в повседневной жизни. А теперь давайте подведём итоги. Выставим оценки.
- Домашнее задание:
- Выполнить домашнюю лабораторную работу “Наблюдение делимости вещества”.
- Придумать один или несколько опытов, доказывающих, что между молекулами имеются промежутки, и доказывающих, что размеры молекул малы.
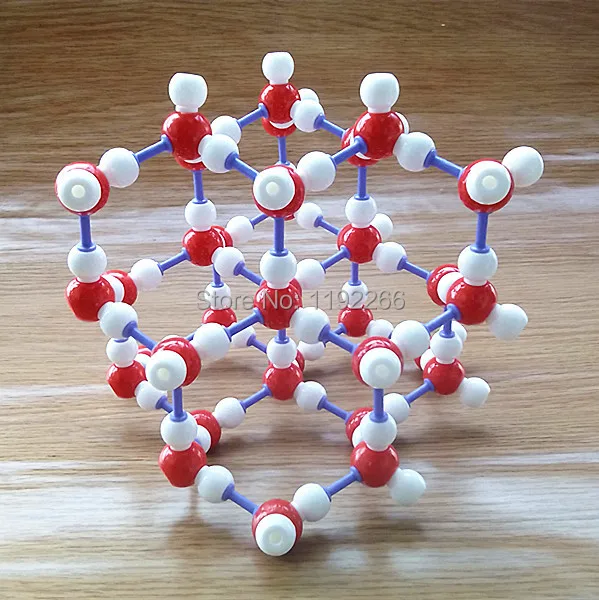
- Создать с помощью подручных средств (пластилина, бумаги, клея и т.д) макет молекулы воды.
Литература:
- Книга для чтения по физике: Учебн. Пособие для учащихся 6-7 классов сред. Шк.
/ Сост.
 И.Г. Кириллова. – 2-е изд., перераб. – М.: Просвещение, 1986. – 207 с.
И.Г. Кириллова. – 2-е изд., перераб. – М.: Просвещение, 1986. – 207 с. - Методика преподавания физики в 7-8 классах средней школы: Пособие для учителя/ А.В. Усова, В.П. Орехов, С.Е. Каменецкий и др.; Под ред. А.В. Усовой. – 4-е изд., перераб. – М.: Просвещение, 1990. – 319 с.
- А.Е. Гуревич, Д.А. Исаев, Л.С. Понтак. Физика и химия. 5-6 кл.: Учебн. для общеобразоват. учебн. заведений / А.Е. Гуревич, Д.А. Исаев, Л.С. Понтак. – М.: Дрофа, 2001. – 192 с.
- Перынкин А.В. Физика: Учебн. для 7 кл. сред. шк. – 2-е изд. – М.: Дрофа, 2004. – 192 с.
- Полянский С.Е. Поурочные разработки по физике. 7 класс. М.: “ВАКО”, 2004, 240 с.
PyMol Учебник
PyMol
[вернуться к КБ Вонга домашняя страница]Учебное пособие по использованию PyMOL для получения показателей качества публикации.
С помощью этого руководства вы сможете создать следующие цифры:
Файлы для учебных пособий можно скачать здесь.

Файлов включено:
1w2i.pdb — кристаллическая структура PH-ацилфосфатазы (PDB: 1W2I) (Cheung et al., Биохимия, 44:4601-4611.)
2fofc.map.xplor — карта электронной плотности из CNS/XPLOR (файл карты имя должно включать расширение .xplor)
1w2i_nowat.pdb — Молекулы воды и лиганда из 1w2i.pdb были удалены (для электростатический расчет). Поскольку PH-ацилфосфатаза существует в виде мономера в растворе включена только цепь А.
apbs.in — шаблон входного файла APBS для расчета электростатики
pymol.dx — расчетная карта электростатикиPyMOL можно загрузить с http://pymol.sourceforge.net/
. Помните, если вы делаете рисунки для публикации, не забудьте указать:
DeLano, W.L. Система молекулярной графики PyMOL (2002 г.) DeLano Scientific, Сан-Карлос, Калифорния, США.
1. Рисунок, показывающий карту электронной плотности
После этого урока вы сможете создать следующую цифру:
1. Загрузка файла PDB
Загрузка файла PDB
Файл -> Открыть -> 1w2i.pdb2. Загрузите файл карты
Файл -> Открыть -> 2fofc.map.xplor
Загрузка файла карты занимает некоторое время.3. Увеличить активный сайт
PyMOL> выберите актив, (рези 14-20,38) и цепочку A
PyMOL> зум активен
PyMOL> скрыть все
PyMOL> show stick, active4. Найдите и отобразите воду активного сайта
Мы знаем, что амидная группа Asn38 связана с активной водой.
PyMOL> выберите active_water, ( (рези 38 и имя ND2 и цепь A) около 3,5) и (резн. HOH)
Вышеупомянутая команда выбирает любые молекулы воды, которые составляют около 3,5 А. атом ND2 рези 38 в цепи A
PyMOL> показать сферы, active_water
Атом кислорода теперь показан в его радиусе vdw. Мы можем уменьшить размер сферы до 0,5А по:
PyMOL> изменить active_water, vdw=0,5
PyMOL> перестроить5. Отображение электронной плотности вокруг атомов активного центра в сигма уровень=1.
 0
0
PyMOL> isomesh mesh2, 2fofc.map, 1.0, (рези 14-20,38 и цепочка А), вырезать=1,6
Поскольку остаточные атомы ранее были определены как «активные», вы можно просто ввести:
PyMOL> isomesh mesh2, 2fofc.map, 1.0, active, carve=1.66. Вы можете изменить цвет карты на:
PyMOL> color grey, mesh27. Обычно вы хотите установить белый цвет фона для публикация
PyMOL> bg_color white8. Показатели качества публикации
Для визуализации фигуры с разрешением по умолчанию (640×480)
PyMOL> луч
Вы сможете просмотреть цифры с низким разрешением на экране. Если вы все сделали правильно, вы должны увидеть это:Для визуализации фигуры с высоким разрешением
PyMOL> луч 2400,2400
Ну, это занимает некоторое время, чтобы произвести его. Затем вы можете сохранить цифры в PNG на
Файл -> Сохранить изображение9. Вы можете сохранить сеанс:
Файл -> Сохранить сеанс
Сохраненный сеанс будет иметь расширение . pse. Вы можете перезагрузить его,
дважды щелкните файл .pse в Windows.
pse. Вы можете перезагрузить его,
дважды щелкните файл .pse в Windows.2. Мультяшное изображение и поверхность
После этого руководства вы сможете генерировать следующие цифры:1. Загрузите файл PDB
Файл -> Открыть -> 1w2i.pdb2. Скрыть все, а затем показать белковую коробку
PyMOL> скрыть все, все
PyMOL> показать мультфильм, все3. Раскрасить спираль, лист и петлю
PyMOL> цвет фиолетовый, сс h
PyMOL> цвет желтый, сс
PyMOL> цвет зеленый, сс «»4. Цепочка цветов А и В
PyMOL> цвет красный, цепь A
PyMOL> синий цвет, цепочка B5. Создайте поверхностный дисплей для цепочки A
PyMOL> создать obj_a, цепочку A
PyMOL> показать поверхность, obj_a
Вы можете сделать поверхность частично прозрачной.
PyMOL> установить прозрачность = 0,5
PyMOL> установить прозрачность=0,16. Окрасить остаток активного сайта
PyMOL> выберите активный, (рези 14-20,38 и цепь А)
PyMOL> цвет желтый, активен
Попробуйте повернуть молекулу. Вы видите дыру вокруг желтого
поверхность? Это колыбель активного центра для связывания фосфата.
Вы видите дыру вокруг желтого
поверхность? Это колыбель активного центра для связывания фосфата.Если вы не вращали молекулу, вы можете повернуть ее с помощью следующие команды для лучшего обзора базовой станции:
PyMOL> поворот у, -60; поворот х, -20
PyMOL> zoom active7. Найдите и отобразите связанный ион формиата в активном сайте.
PyMOL> выберите лиганд, активный около 3,5 и резн FMT
PyMOL> показать палочки, лиганд
PyMOL> показать сферы, лиганд
PyMOL> изменить лиганд, vdw=0,5
PyMOL> перестроить
PyMOL> установить прозрачность = 0,258. Рендеринг и вывод
PyMOL> bg_color белый
PyMOL> луч
Файл -> Сохранить изображение9. Отобразите боковую цепь остатков активного сайта поверх представление мультфильма
PyMOL> скрыть поверхность
PyMOL> выберите сайдчейн, а не (название c+n+o)
PyMOL> показать стики (активные и сайдчейн)
PyMOL> цвет синий, имя n*
PyMOL> цвет красный, имя о*
PyMOL> цвет белый, имя c*10.
 Отображение и измерение расстояний
Отображение и измерение расстояний
Мастер -> Измерение -> Расстояние
Щелкните два атома, чтобы получить расстояние между этими двумя щелчками атомов.
Используйте это для измерения расстояния между атомами азота аргинина и атомы кислорода формиат-иона.
Когда вы закончите, нажмите кнопку «Готово»Вы также можете измерить расстояние между двумя атомами:
PyMOL> расстояние рези 20 и имя Nh3 и цепь А, рези 1092 и имя O2 и цепь AМетку расстояния можно скрыть с помощью
PyMOL> скрыть метки11. создать цифру
PyMOL> луч
File -> Save Image3. Использование APBS и PyMOL для отображения электростатической поверхности
После этого урока вы сможете создать следующую фигуру:Вам необходимо удалить молекулу воды и лигандов из 1w2i.pdb.
1w2i_nowat.pdb — Молекулы воды и лиганда из 1w2i.pdb были удалены (для электростатический расчет). Поскольку PH-ацилфосфатаза существует в виде мономера в растворе включена только цепь А.

apbs.in — шаблон входного файла APBS для расчета электростатики
pymol.dx — рассчитанная карта электростатикиA. Использование APBS для расчета карта электростатики
Мы предполагаем, что вы установили APBS и PDB2PQR в линуксе машина.
1. Используйте PDB2PQR для преобразования формата PDB в формат PQR
. > pdb2pqr.py —ff=amber —apbs-in 1w2i_nowat.pdb pymol.pqr
Файл PQR будет выведен в pymol.pqr.2. Используйте psize.py для определения размеров сетки для расчета APBS
> psize.pypymol.pqr
Вы должны увидеть следующие результаты:Центр = 37,468 х 31,798 х 12,177 А
:
:
Размеры грубой сетки = 53,011 x 58,568 x 65,807 А
Размеры мелкой сетки = 51,183 x 54,452 х 58,710 А
номер мелкая сетка оч. = 97 x 97 x 97Запишите эти параметры.
3. Отредактируйте apbs.in
Вам необходимо ввести следующие параметры:cgcent 37.468 31.798 12.
 177 #
Сетка Центр
177 #
Сетка Центр
фгцент 37,468 31,798 12.177 # Сетка Центркглен 53,011 58,568 65.807 # грубый длина ячейки (A)
фглен 51,183 54,452 58.710 # штраф длина ячейки (A)десять центов 97 97 97 # Точки сетки
4. Запустите APBS
> apbs apbs.in
Через некоторое время он создаст карту электростатики под названием «pymol.dx».B. Использование PyMOL для визуализации карта электростатики
1. Откройте PDB и файлы pymol.dx.
Файл -> Открыть -> 1w2i_nowat.pdb
Файл -> Открыть -> pymol.dx2. Отобразить поверхность электростатики
Плагин -> Инструменты APBS -> Визуализация
Нажмите кнопку «Показать» в меню молекулярной поверхности.
Значение по умолчанию: Синяя поверхность: +1 кТл Красная поверхность: -1 kTТеперь измените настройки по умолчанию на -10 и +10 и нажмите кнопку «Показать». кнопку еще раз.

Можете ли вы найти люльку с синей поверхностью (т.е. положительно заряженных) на белковой молекуле? Это актив участок PH-ацилфосфатазы, связывающий отрицательно заряженный субстрат.4. Создайте серию файлов PNG для анимированного фильма GIF
1. Настройка фильмаФайл->Открыть->1w2i_nowat.pdb
PyMOL>ориент
PyMOL> скрыть все, все
PyMOL> покажи мульт, все
PyMOL> фиолетовый цвет, сс ч; цвет желтый, сс с; цвет зеленый, сс «»PyMOL> mset 1 x60
Эта команда создает ролик из 60 кадров
. PyMOL> util.mrock 1,60,180
Эта команда раскачивает белковую молекулу на +/- 180 градусов за 60 кадров
PyMOL> mplay
Эта команда воспроизводит фильм2. Теперь попробуйте следующее:
PyMOL> util.mroll 1,60
Эта команда поворачивает молекулу белка на 360 градусов за 60 кадров
. Введите «mstop», чтобы остановить анимацию3. Сохранение кадров в формате PNG
PyMOL> mpng кадр
Это создаст frame0001. png frame0002.png и т.д…
png frame0002.png и т.д…Если вы хотите использовать трассировку лучей для всех кадров, вы можете:
PyMOL> установить ray_trace_frames=1
PyMOL> mpng кадр
Анимация очень хорошего качества, но очень медленно создает все файлы PNG!4. Вы можете конвертировать эти файлы PNG пакетно в GIF с помощью программы XnView, а затем объединять эти файлы GIF файлы для создания анимированного GIF с помощью UnFREEz:
5. Структурное выравнивание двух гомологичных белков
В этом руководстве вы собираетесь выровнять PH-ацилфосфатазу и бычий ацилфосфатаза (2ACY.pdb)
Файл -> Открыть -> 1w2i_nowat.pdb
Файл -> Открыть -> 2ACY.pdbPyMOL> выровнять 1w2i_nowat, 2ACY
В текстовом окне вы должны увидеть следующее:
ExecutiveAlign: 446 атомов выровнены.
ExecutiveRMS: 23 атома отклонено во время цикла 1 (RMS = 0,86).
ExecutiveRMS: 20 атомов отклонено во время цикла 2 (RMS = 0,63).
Исполнительный: RMS = 0,541 (от 403 до 403 атомов)
В этом случае RMSD составляет 0,541 A.
Чаще люди сообщают значения RMSD Ca, которые можно определить автор:
PyMOL> align 1w2i_nowat and name ca, 2ACY and name ca, cycles=0Water Molecule Stok Videolar ve Detay Görüntü
İllüstrasyon
- Görsel
- Fotoğraf
- İllüstrasyon
- Vektörler
- Video
11.526
молекула воды безвозмездное сток иллюстраций векторной графики inceleyin veya daha fazla сток гурсель ве векторной графики keşfetmek için yeni bir arama başlatın.Sırala:
En popüler
köpüklü su logosu, soyut yuvarlak logo tipi şablonu, mavi noktalı amblem, beyaz arka planda vektör içecek etiket konsepti — water molecule stock illustrationsKöpüklü su logosu, soyut yuvarlak logo tipi şablonu, mavi noktalı
молекюль чизгиси симгелери. vektör illüstrasyon icon amino asit dahil, пептид, гормон, протеин, коллаген, озон, химия ичин о2 кимьясал формула и пиктограмма. 64×64 пикселя mükemmel ayarlanabilir vuruş — молекула воды стоковые иллюстрации
vektör illüstrasyon icon amino asit dahil, пептид, гормон, протеин, коллаген, озон, химия ичин о2 кимьясал формула и пиктограмма. 64×64 пикселя mükemmel ayarlanabilir vuruş — молекула воды стоковые иллюстрацииMolekül çizgisi simgeleri. Вектор иллюстрирует значок аминокислоты…
H3O на молекулу модели и химическую форму — молекула воды фондовых иллюстрацийH3O на молекулу модели и химическую форму
химическую модель молекулы на молекулярную форму h3o. entegre parçacıklar doğal inorganik 3d moleküler yapıdan oluşur. i̇ki hidrojen ve oksijen hacmi atom vektör küreleri — Water Molecule Stock IllustrationsМолекулярная модель молекулы по форме элемента h3O bilimsel. Entegre parç
молекулы фоновой иллюстрации — молекулы воды стоковые иллюстрацииМолекулы фоновой иллюстрации
Молекулы на H3O двухкомпонентные модели. entegre parçacıklar hidrojen ve oksijen doğal inorganik bileşik. 3d молекулярный вектор, иллюстрирующий изолей — молекулы воды, фондовые иллюстрацииМолекулы на h3O двухэлементных моделей Kimya.
ромб бир шекил ве мави tonları bağlı noktalar. су тема каврами. soyut tasarım öğesi. vektör çizim — молекула воды стоковые иллюстрации Entegre parçacıkla
Entegre parçacıklaRhombus bir şekil ve mavi tonları bağlı noktalar. Su Tema kavramı.
молекуль. 3d saydamlık moleküler yapılar, yansıma ile kimya macro modelleri. генетика и бийотекнолоджи, созданные из векторной сети — иллюстрации молекулы водыMolekül. 3d saydamlık moleküler yapılar, yansıma ile kimya macro…
hidrojen oksijen sodyum karbon azot ve klor moleküler kimyasal modellerin kombinasyonu topplama. beyaz arka planda izole edilmiş vektör molekülleri illüstrasyonu — молекула воды стоковые иллюстрацииHidrojen oksijen sodyum karbon azot ve klor moleküler kimyasal…
молекула воды — молекула воды иллюстрацииМолекула воды
ortak moleküller kümesi — молекула воды иллюстрацииOrtak Moleküller Kümesi
абстрактная синяя форма биотехнологии — молекула воды иллюстрацииабстрактная синяя форма биотехнологии bir logo şeklinde sıvı modern grafik görüntü — иллюстрации стоковых молекул воды
İçecek ve maden suyu reklamı için logo soyut tasarımı, bir logo şe
SOYUT çizgi NOKTA ARKA План — Иллюстрации молекулы водыSOYUT çizgi NOKTA ARKA План
03 Молекула воды — Иллюстрации молекулы воды03 Молекула вода
koleksiyonu -иллюстрации. иллюстрации
иллюстрацииHidrojen Yapıştırma
molekül su h3o bilimsel elemanlar kimya modeli. entegre parçacıklar hidrojen ve oksijen doğal inorganik bileşik. 3d moleküler yapı vektör illüstrasyon izole — молекула воды стоковые иллюстрацииMolekül su h3O bilimsel elemanlar Kimya modeli. Entegre parçacıkla
акан parçacıklar soyut vektör arka plan, pürüzsüz curvy şekil noktalar sıvı dizi dalga hattı. 3d şekil noktalarharmanlanmış сетка, gelecekteki teknoloji rahatlatıcı duvar kağıdı. — молекула воды стоковые иллюстрацииAkan parçacıklar soyut vektör arka plan, pürüzsüz Curvy şekil…
su molekülleri soyut arka plan yapısı, vektör illüstrasyon — Water Molecule Stock IllustrationsМолекуллери соютиллери план yapısısısısısısısıs
0016 tıbbi pipet ile sıvı ve düşen damlacık çizgiler, noktalar, üçgenler, yapılan koyu mavi arka plan üzerinde yıldız. bilimsel ilaç araştırma kavramı. — молекула воды иллюстрации
Тысячи пипеток, которые есть в день, ноябрь, üçgenle
коллажей алтын топлари.






 (слайд 30))
(слайд 30))
 И.Г. Кириллова. – 2-е изд., перераб. – М.: Просвещение, 1986. – 207 с.
И.Г. Кириллова. – 2-е изд., перераб. – М.: Просвещение, 1986. – 207 с.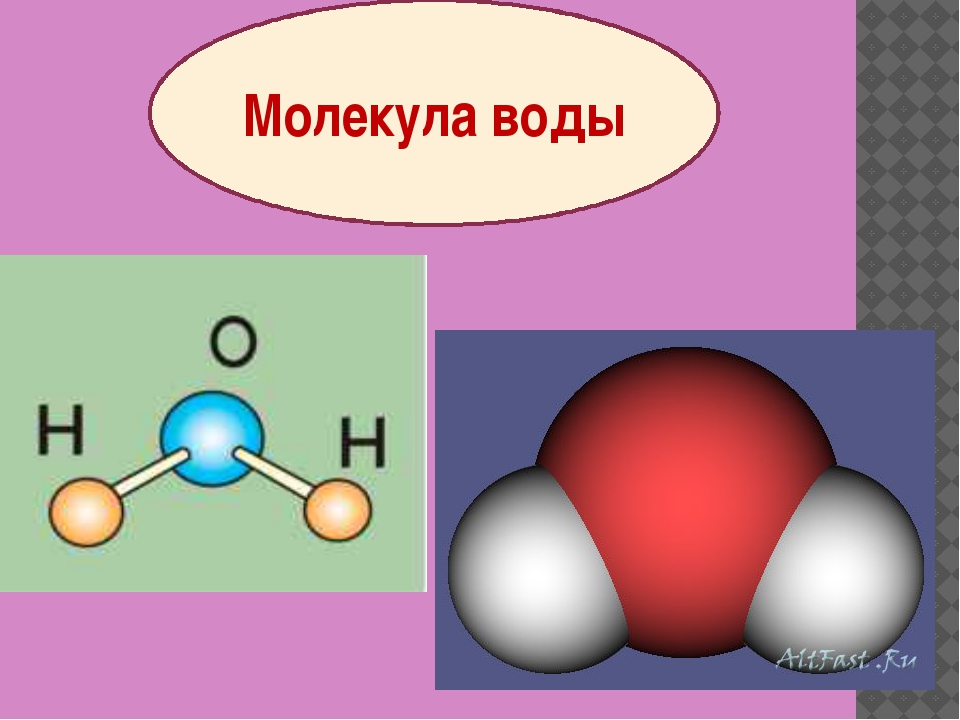
 Загрузка файла PDB
Загрузка файла PDB  0
0  pse. Вы можете перезагрузить его,
дважды щелкните файл .pse в Windows.
pse. Вы можете перезагрузить его,
дважды щелкните файл .pse в Windows. Вы видите дыру вокруг желтого
поверхность? Это колыбель активного центра для связывания фосфата.
Вы видите дыру вокруг желтого
поверхность? Это колыбель активного центра для связывания фосфата. Отображение и измерение расстояний
Отображение и измерение расстояний 
 177 #
Сетка Центр
177 #
Сетка Центр 
 png frame0002.png и т.д…
png frame0002.png и т.д…
 vektör illüstrasyon icon amino asit dahil, пептид, гормон, протеин, коллаген, озон, химия ичин о2 кимьясал формула и пиктограмма. 64×64 пикселя mükemmel ayarlanabilir vuruş — молекула воды стоковые иллюстрации
vektör illüstrasyon icon amino asit dahil, пептид, гормон, протеин, коллаген, озон, химия ичин о2 кимьясал формула и пиктограмма. 64×64 пикселя mükemmel ayarlanabilir vuruş — молекула воды стоковые иллюстрации Entegre parçacıkla
Entegre parçacıkla иллюстрации
иллюстрации