Электролиз расплавов и растворов — схема, правила и уравнения
Поможем понять и полюбить химию
Начать учиться
Электролиз расплавов и растворов встречается в заданиях на ЕГЭ, а значит, если вы планируете сдавать экзамен по химии, эту тему нужно знать на отлично. Наша статья поможет узнать или повторить, что такое электролиз, его правила и схема протекания.
Электролиз — это окислительно-восстановительная реакция, которая протекает на электродах и основана на пропускании электрического тока через раствор или расплав.
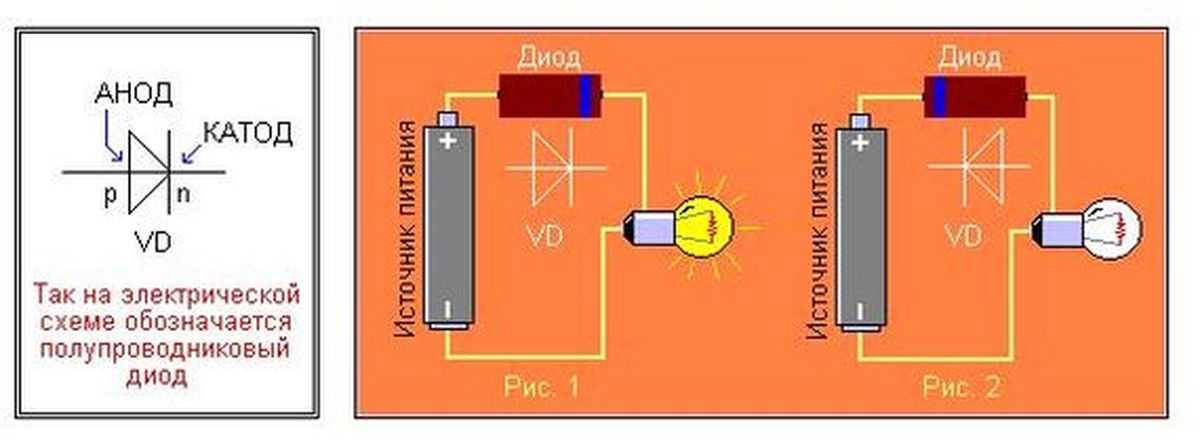
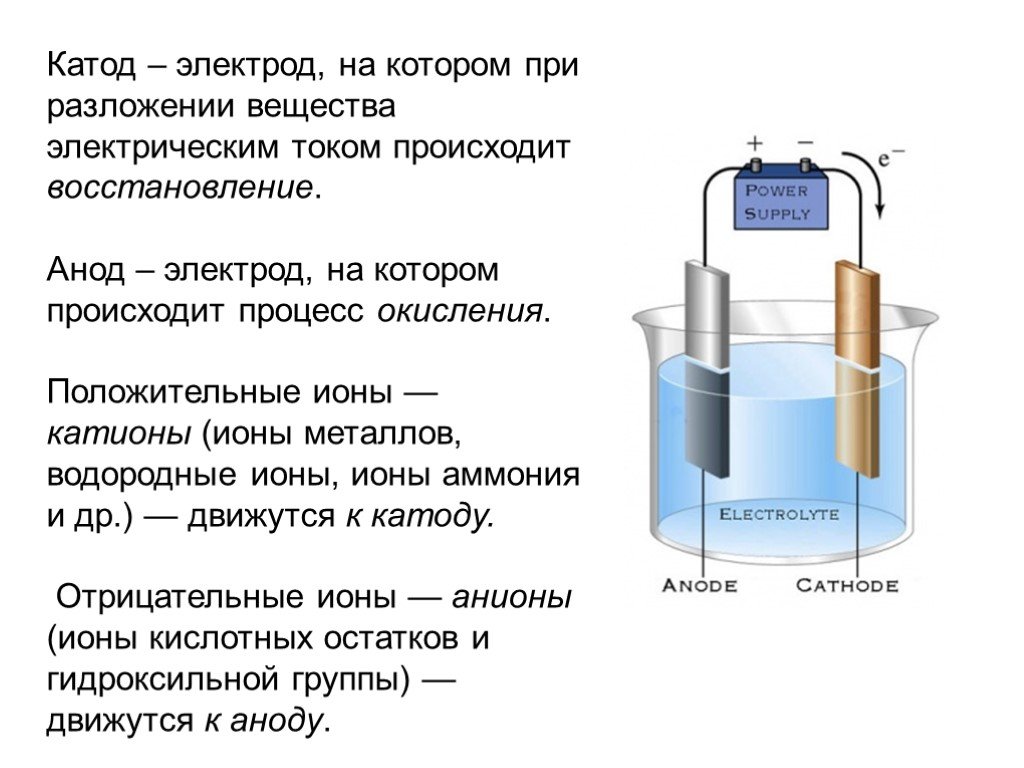
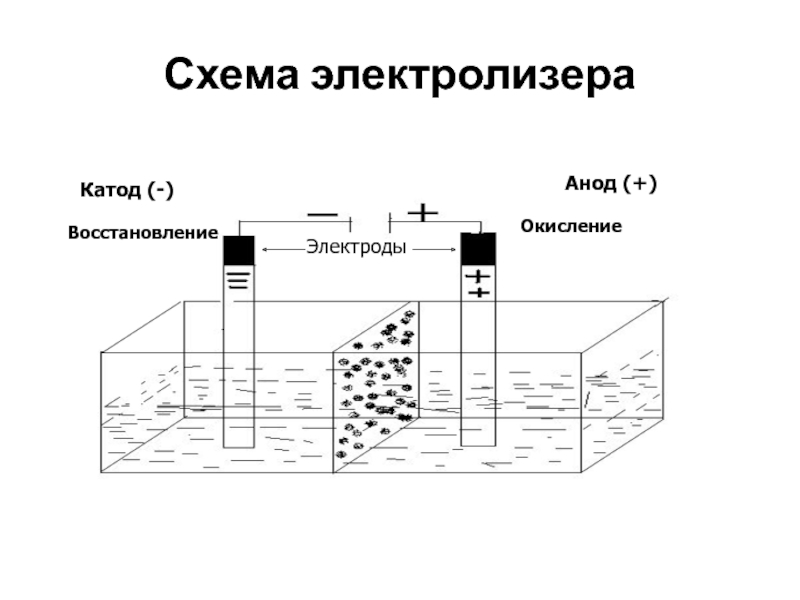
Не менее важными участниками электролиза являются электроды: катод и анод. Если вы вдруг забыли, что такое катод и анод в химии, напомним.
Катод — это отрицательно заряженный электрод, который притягивает положительно заряженные ионы (катионы). А анод — это положительно заряженный электрод, который притягивает к себе отрицательно заряженные ионы (анионы). Таким образом, на катоде всегда происходит процесс восстановления, а на аноде всегда происходит процесс окисления.
Таким образом, на катоде всегда происходит процесс восстановления, а на аноде всегда происходит процесс окисления.
Электроды бывают растворимые и инертные. Растворимые изготавливаются из металлов, например, меди и подвергаются химическим превращениям в ходе электролиза. А вот инертные или нерастворимые электроды не подвергаются химическим превращениям и остаются в неизменном виде как до реакции, так и после нее. Как правило, такие электроды изготавливают из графита или платины.
Виды электролиза
Различают два вида электролиза:
Электролиз расплава.
Электролиз водного раствора.
Прежде чем мы рассмотрим каждый процесс отдельно, давай познакомимся с общими для двух видов процессами на электродах.
Процесс на катоде K (−) Катион принимает электроны и восстанавливается: Me+n + ne− → Me0 (восстановление). Процесс на аноде A (+) Анион отдает электроны и окисляется: неMe−n − ne− → неMe0 (окисление). Процессы, протекающие при электролизе в общем случае: К− : Ме+n + ne− → Ме0; А+ : неМе−n − ne− → неМе0. Суммарное уравнение электролиза: |
|---|
Практикующий детский психолог Екатерина Мурашова
Бесплатный курс для современных мам и пап от Екатерины Мурашовой. Запишитесь и участвуйте в розыгрыше 8 уроков
Электролиз расплава
Рассмотрим электролиз расплава пищевой соли — хлорида натрия. При сильном нагревании кристаллический твердый хлорид натрия плавится. Полученный расплав содержит подвижные ионы хлора и натрия, освободившиеся из кристаллической решетки, и проводит электрический ток.
К−: 2Na+ + 2e− = 2Na0
А+: 2Cl− − 2e− = Cl2
Суммарное уравнение электролиза:
При опускании в расплав угольных (инертных) электродов, присоединенных к источнику тока, ионы приобретают направленное движение: катионы движутся к отрицательно заряженному электроду (катоду), анионы — к положительно заряженному электроду (аноду) и отдают электроны.
Теперь давайте рассмотрим электролиз расплава гидроксида калия.
На катоде происходит восстановление калия за счет принятия электронов. А на аноде протекает более сложная реакция. Гидроксогруппы отдают свой электрон и становятся нейтральными, но такое состояние для них крайне невыгодно, так как неустойчиво, и они объединяются в группы, чтобы потом разложиться с выделением газообразного кислорода и воды
Итог электролиза расплава — металлический калий на катоде, газообразный кислород и пары воды на аноде.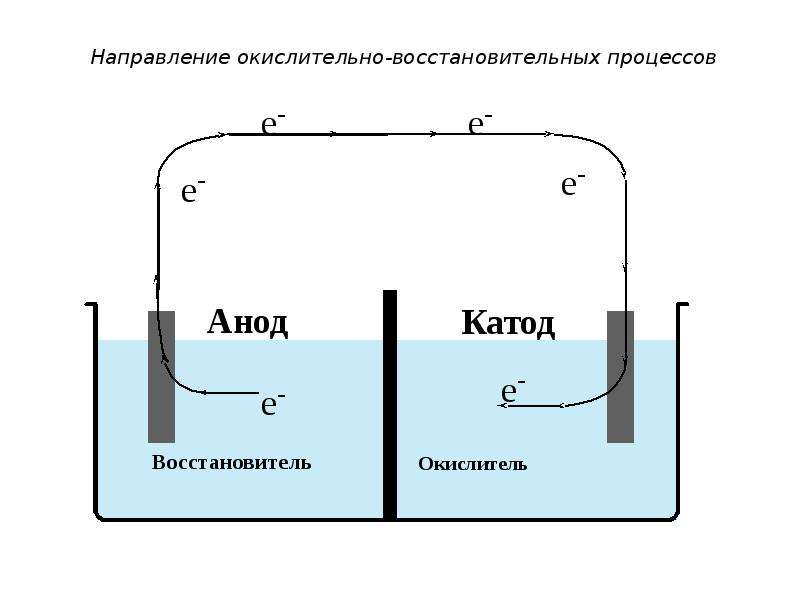
Электролиз раствора
Основным отличием водного раствора от расплава является присутствие молекул воды и ионов H+ и OH— как продуктов диссоциации воды. В связи с этим возле катода и анода скапливаются ионы, которые конкурируют как друг с другом, так и с молекулами воды. Рассмотрим электролиз на примере водного раствора KF:
К−: 4H2O + 4e− = 2H20 + 4OH−
А+: 2H2O − 4e− = O2 + 4H+
Суммарное уравнение электролиза:
Как видно, ни калий, ни фтор не фигурируют в продуктах электролиза. Почему так происходит?
Наиболее активные металлы — сильные восстановители. Калий — как раз такой металл, поэтому обратный процесс восстановления активных металлов из соединений осуществить сложно. При электролизе водных растворов солей активных металлов на катоде протекает восстановление не катионов этих металлов, а воды с образованием водорода.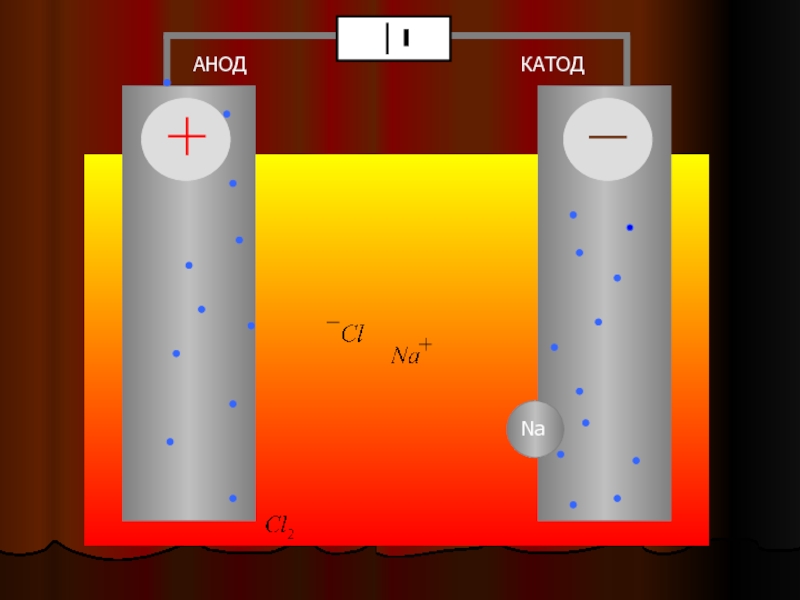
Разберем порядок восстановления катионов металлов на катоде в зависимости от их активности.
Последовательность разрядки катионов зависит от положения металла в электрохимическом ряду напряжения.
Если у катода накапливаются молекулы воды и катионы металла, который находится в ряду напряжения после водорода, то восстанавливаются ионы металла.
Если у катода накапливаются молекулы воды и катионы металла, который стоит в начале ряда напряжения от лития до алюминия включительно, то восстанавливаются ионы водорода из молекул воды. Катионы металла не восстанавливаются, остаются в растворе.
Если у катода накапливаются молекулы воды и катионы металла, который расположен в ряду напряжения между алюминием и водородом, то восстанавливаются и ионы металла, и частично ионы водорода из молекул воды.

Если в растворе находится смесь катионов разных металлов, то сначала восстанавливаются катионы менее активного металла.
При электролизе раствора кислоты на катоде восстанавливаются катионы водорода до газообразного водорода.
Для удобства мы собрали информацию об электролизе в таблице:
Теперь разберемся, что происходит с анионами в водных растворах при электролизе. Для начала познакомимся с последовательностью восстановления анионов на аноде:
Чем меньше выражена восстановительная активность, тем хуже анионы могут окисляться на аноде. К тому же процесс на аноде зависит от материала анода и от природы аниона.
Если анод инертный или нерастворимый, то на нем протекают следующие реакции:
При электролизе растворов солей бескислородных кислот (кроме фторидов!), на аноде происходит процесс окисления аниона.

При электролизе растворов солей кислородсодержащих кислот и фторидов на аноде выделяется газообразный кислород вследствие окисления молекул воды. Анион при этом не окисляется, оставаясь в растворе.
При электролизе растворов щелочей происходит окисление гидроксид-ионов.
Если анод растворимый, то на нем всегда происходит окисление металла анода — независимо от природы аниона.
Исключением является электролиз солей карбоновых кислот. Таблица выше не описывает происходящее на аноде. Давайте рассмотрим, что же там происходит.
В результате электролиза водных растворов солей щелочных металлов карбоновых кислот происходит образование углеводородов вследствие рекомбинации углеводородных радикалов.
В общем виде электролиз солей карбоновых кислот можно записать так:
На катоде образуется газообразный водород, а на аноде — углекислый газ, углеводород, полученный удвоением радикала.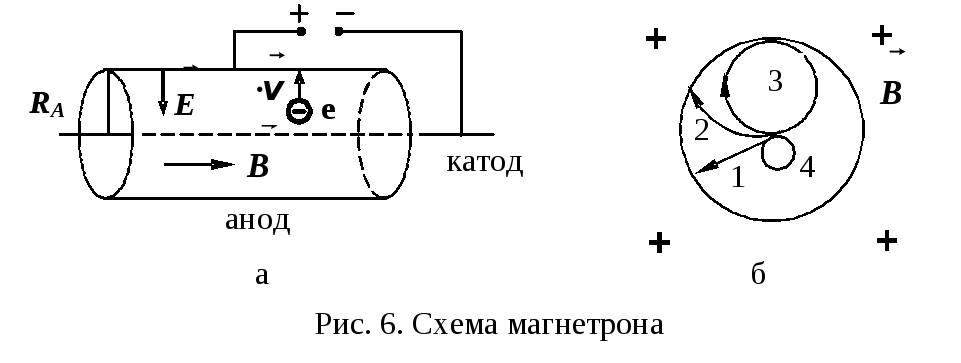 В катодном пространстве накапливается щелочь.
В катодном пространстве накапливается щелочь.
В случае разделения катодного и анодного пространства углекислый газ реагирует со щелочью с образованием гидрокарбоната.
Применение электролиза
А теперь самое главное: зачем вообще нужен электролиз? Рассмотрим применение этого вида ОВР:
С помощью электролиза расплавов природных соединений в металлургической промышленности получают активные металлы (калий, натрий, бериллий, кальций, барий). С помощью электролиза растворов солей — цинк, кадмий, кобальт и другие.
В химической промышленности электролиз используют для получения фтора, хлора, водорода, кислорода, щелочей, бертолетовой соли и других веществ.
Электролиз с растворимым анодом используют для нанесения металлических покрытий (из хрома, золота, никеля, серебра), что предохраняет металлические изделия от коррозии и придает им декоративный вид.

Вопросы для самопроверки
1. Выберите верное продолжение фразы «катод — это…»:
Положительно заряженный электрод, к которому притягиваются положительно заряженные ионы.
Положительно заряженный электрод, к которому притягиваются отрицательно заряженные ионы.
Отрицательно заряженный электрод, к которому притягиваются отрицательно заряженные ионы.
2. Продолжите фразу «электролиз — это…»:
ОВР с применением тока.
Реакция без изменения степеней окисления с применением тока.
ОВР с применением катализаторов.

Обменная реакция.
3. Как заряжен анион?
Положительно.
Отрицательно.
Нейтрально.
Не имеет заряда.
4. Чем отличается электролиз раствора от электролиза расплава?
Ничем.
В расплаве плавится твердое.
Присутствием молекул воды и продуктов ее диссоциации.
5. Если металл стоит в ряду активности металлов между алюминием и водородом, что выделится на катоде?
Этот металл.
Водород.
Металл и водород.

Оксид металла.
При электролиза водного раствора фторида лития что на аноде выделится?
Фтор.
Водород.
Кислород.
Вода.
Ответы
c
a
b
c
c
с
Ксения Боброва
К предыдущей статье
Азот
К следующей статье
Изомеры
Получите план обучения, который поможет понять и полюбить химию
На вводном уроке с методистом
Выявим пробелы в знаниях и дадим советы по обучению
Расскажем, как проходят занятия
Подберём курс
Катод — уверенность опыта!
Производство стартерных аккумуляторных батарей является одним из важных направлений деятельности Научно-Производственного Объединения «Катод».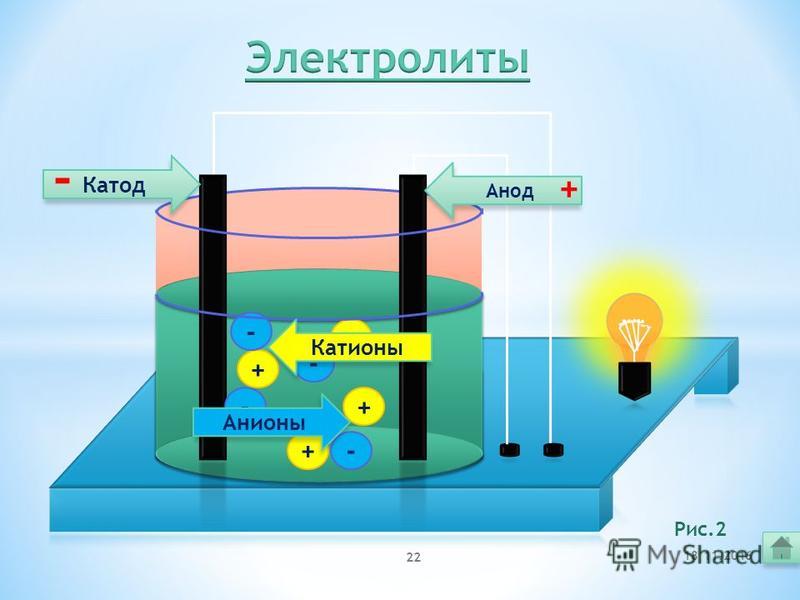 В его основу положены опыт отечественной оборонной промышленности, собственные разработки, а также технологии ведущих мировых производителей. Результат десятилетней работы — предложение потребителю аккумуляторных батарей под собственной торговой маркой «Катод», отвечающих всем требованиям современного рынка.
В его основу положены опыт отечественной оборонной промышленности, собственные разработки, а также технологии ведущих мировых производителей. Результат десятилетней работы — предложение потребителю аккумуляторных батарей под собственной торговой маркой «Катод», отвечающих всем требованиям современного рынка.
Потребительские свойства аккумуляторных батарей напрямую зависят от качества комплектующих деталей и узлов. На завод Катода они поставляются по специальным договорам от ведущих мировых производителей Korea Storage Battery и итальянского «Fiamm». В Санкт-Петербурге осуществляется завершающий важнейший этап производства — формировка аккумуляторных батарей.
Формировка — это основной электрохимический процесс, от правильного выполнения которого зависят пусковые характеристики и срок службы аккумулятора. Во время этого процесса происходит электрохимическое формирование кристаллической структуры активных материалов положительного и отрицательного электродов, что обеспечивает, при прочих равных условиях, в течение многократных зарядов и разрядов требуемые от аккумулятора пусковые характеристики и срок службы.
Производственный процесс состоит из нескольких этапов. На первом этапе в собранную батарею заливается электролит. Важным моментом в обеспечении качества выпускаемой «НПО Катод» продукции является собственное производство электролита. Для исходного сырья выбрана химически чистая аккумуляторная кислота, закупаемая на объединении «Фосфорит», а современное оборудование позволяет точно соблюсти все технологические особенности производства.
Затем батареи устанавливаются в шкафы с принудительной вентиляцией и подключаются к формировочным стойкам. Используемое на заводе «НПО Катод» формировочное оборудование соответствует всем стандартам и позволяет выпускать продукцию высокого качества, отвечающую требованиям современного рынка аккумуляторных батарей. Это оборудование сертифицировано крупнейшим европейским производителем аккумуляторных батарей — немецкой фирмой «VARTA». На пластины по специальной программе подается напряжение, эта длительная процедура занимает примерно 42 часа.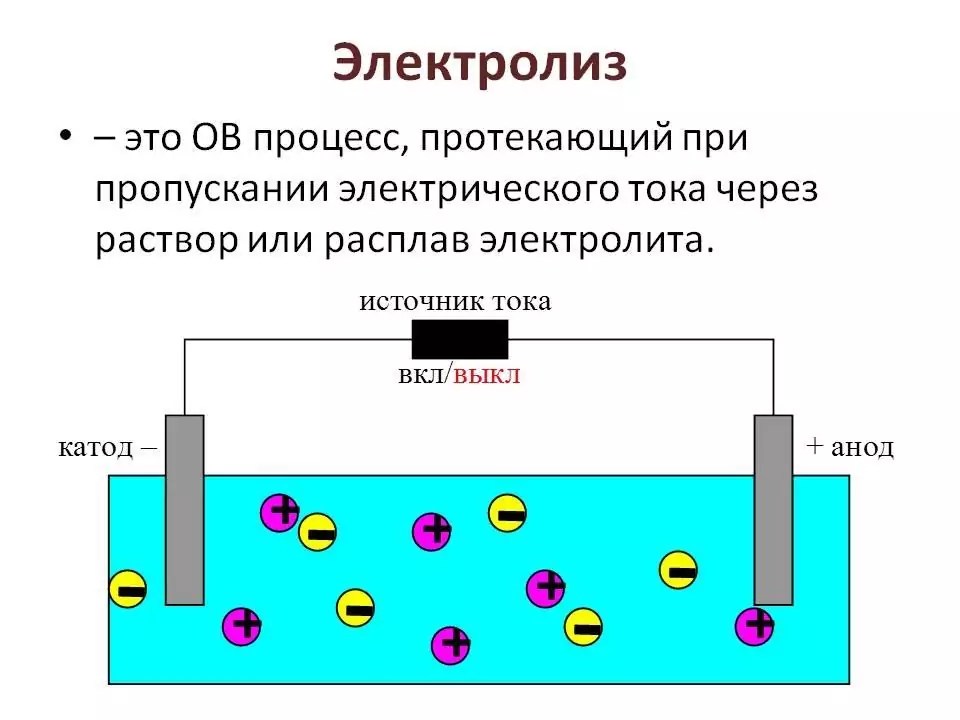 Все работы полностью автоматизированы.
Все работы полностью автоматизированы.
После окончания формировки уровень электролита в банках корректируется до нормативной величины. Затем производится мойка и сушка аккумуляторной батареи, и начинается следующий важный этап — проверка качества.
Качеству на предприятии уделяется самое серьезное внимание. Система контроля состоит из нескольких этапов. Сначала — входной контроль комплектующих деталей, затем — непосредственно процесса производства и, в завершении проводится инструментальная проверка. Если аккумулятор по своим электрическим характеристикам соответствует требованиям технических условий, то он готовится к продаже (маркируется и упаковывается).
Использование высококачественных материалов, полная автоматизация и контроль на всех этапах технологических процессов позволяют достигнуть стабильно высокого качества выпускаемой продукции и установить гарантийный срок эксплуатации 2 года.
На сегодняшний день «НПО Катод» освоено производство двух серий аккумуляторных батарей — собственно «Катод», с решетками из малосурьмянистого свинцового сплава и «Катод Calcium» с пластинами из кальциевого сплава. Все это позволяет предложить широкий ассортимент для использования практически во всех типах автомобилей. Аккумуляторные батареи, изготовленные по такой технологии, имеют улучшенные характеристики по сравнению со стандартными батареями. В батарее замедляется процесс коррозии решетки, а при заряде и саморазряде происходит полное отделение отходящих газов от электролита. Аккумулятор с решеткой из свинцово-кальциевого сплава лучше выдерживает повышенное напряжение, а при длительном хранении не происходит глубокой сульфатации электродов, и аккумулятор не теряет способности заряжаться.
Все это позволяет предложить широкий ассортимент для использования практически во всех типах автомобилей. Аккумуляторные батареи, изготовленные по такой технологии, имеют улучшенные характеристики по сравнению со стандартными батареями. В батарее замедляется процесс коррозии решетки, а при заряде и саморазряде происходит полное отделение отходящих газов от электролита. Аккумулятор с решеткой из свинцово-кальциевого сплава лучше выдерживает повышенное напряжение, а при длительном хранении не происходит глубокой сульфатации электродов, и аккумулятор не теряет способности заряжаться.
На предприятии строго подходят не только к соблюдению технических норм, но и к требованиям экологической безопасности.
Ассортимент аккумуляторных батарей «Катод» включает в себя широкий спектр типоразмеров, позволяющий использовать аккумуляторные батареи «Катод» в индивидуальных, коммерческих, промышленных целях. Аккумуляторные батареи «НПО Катод» могут применяться в любых отечественных и импортных легковых автомобилях; устанавливаться на тракторах, комбайнах, строительных и дорожных машинах. Высокая надежность позволяет эксплуатировать их в сложных российских условиях.
Высокая надежность позволяет эксплуатировать их в сложных российских условиях.
Что такое катод? | Определение из TechTarget
К
- Участник TechTarget
Катод — это металлический электрод, через который протекает ток в поляризованном электрическом устройстве.
И наоборот, анод — это электрод в поляризованном электрическом устройстве, через который протекает ток из внешней цепи. Катоды получили свое название от катионов (положительно заряженных ионов), а аноды от анионов (отрицательно заряженных ионов).
В устройстве, использующем электричество, катод представляет собой отрицательно заряженный электрод. К таким устройствам относятся диоды, электронные лампы, электронно-лучевые трубки, осциллографы, электролитические элементы в производстве водорода и элементы вторичной батареи в перезаряжаемых батареях.
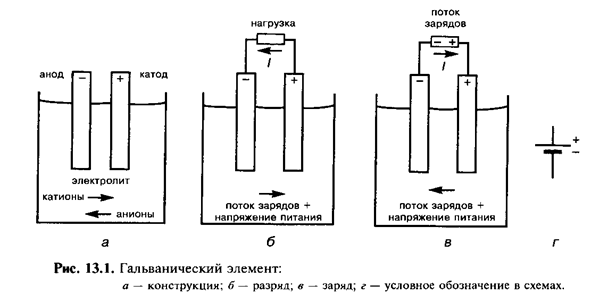
Однако в устройстве, производящем энергию, катод является положительной клеммой из-за обратного потока электронов. Такие устройства включают гальванические элементы и неперезаряжаемые батареи с первичными элементами, а также вторичные элементы батарей (перезаряжаемые), когда энергия внутри батареи потребляется.
Во многих приложениях, поскольку катод получает электроны для производства тока, он постепенно набирает массу за счет катионов, которые он притягивает.
Последнее обновление: июнь 2014 г.
Продолжить чтение О катоде- Как работают батареи?
- Аноды и катоды в батареях
- Отличие анода от катода
распознавание изображений
Распознавание изображений в контексте машинного зрения — это способность программного обеспечения идентифицировать объекты, места, людей, надписи и действия на цифровых изображениях.
Сеть
- телематика
Телематика — это термин, объединяющий слова «телекоммуникации» и «информатика» для описания использования средств связи и ИТ для .
 ..
.. - фильтрация пакетов
Фильтрация пакетов — это процесс пропуска или блокировки пакетов данных на сетевом интерфейсе брандмауэром на основе источника и …
- WAN (глобальная сеть)
Глобальная вычислительная сеть (WAN) — это географически распределенная частная телекоммуникационная сеть, которая соединяет между собой несколько локальных …
Безопасность
- FIDO (быстрая идентификация онлайн)
FIDO (Fast Identity Online) — это набор спецификаций безопасности, не зависящих от технологии, для строгой аутентификации.
- Альянс облачной безопасности (CSA)
Альянс по безопасности облачных вычислений (CSA) — это некоммерческая организация, которая продвигает исследования передовых методов обеспечения безопасности облачных …
- квантовое превосходство
Квантовое превосходство — это экспериментальная демонстрация доминирования и преимущества квантового компьютера над классическими компьютерами с помощью .
 ..
..
ИТ-директор
- сделка
В вычислительной технике транзакция представляет собой набор связанных задач, рассматриваемых как одно действие.
- бережливое управление
Бережливое управление — это подход к управлению организацией, который поддерживает концепцию постоянного совершенствования, долгосрочного …
- идентификатор устройства (идентификация устройства)
Идентификатор устройства (идентификация устройства) — это анонимная строка цифр и букв, которая однозначно идентифицирует мобильное устройство, такое как …
HRSoftware
- вовлечения сотрудников
Вовлеченность сотрудников — это эмоциональная и профессиональная связь, которую сотрудник испытывает к своей организации, коллегам и работе.
- кадровый резерв
Кадровый резерв — это база данных кандидатов на работу, которые могут удовлетворить немедленные и долгосрочные потребности организации.

- разнообразие, равенство и инклюзивность (DEI)
Разнообразие, справедливость и инклюзивность — термин, используемый для описания политики и программ, которые способствуют представительству и …
Служба поддержки клиентов
- лид, квалифицированный продуктом (PQL)
Лид, квалифицированный по продукту (PQL), — это физическое или юридическое лицо, которое получило выгоду от использования продукта в результате бесплатного …
- квалифицированный маркетолог лид (MQL)
Квалифицированный маркетолог (MQL) — это посетитель веб-сайта, уровень вовлеченности которого указывает на то, что он может стать клиентом.
- успех клиента
Успех клиента — это стратегия, направленная на то, чтобы продукция компании отвечала потребностям клиента.
Катод | электроника | Британика
- Развлечения и поп-культура
- География и путешествия
- Здоровье и медицина
- Образ жизни и социальные вопросы
- Литература
- Философия и религия
- Политика, право и правительство
- Наука
- Спорт и отдых
- Технология
- Изобразительное искусство
- Всемирная история
- В этот день в истории
- Викторины
- Подкасты
- Словарь
- Биографии
- Резюме
- Популярные вопросы
- Обзор недели
- Инфографика
- Демистификация
- Списки
- #WTFact
- Компаньоны
- Галереи изображений
- Прожектор
- Форум
- Один хороший факт
- Развлечения и поп-культура
- География и путешествия
- Здоровье и медицина
- Образ жизни и социальные вопросы
- Литература
- Философия и религия
- Политика, право и правительство
- Наука
- Спорт и отдых
- Технология
- Изобразительное искусство
- Всемирная история
- Britannica объясняет
В этих видеороликах Britannica объясняет различные темы и отвечает на часто задаваемые вопросы.
- Britannica Classics
Посмотрите эти ретро-видео из архивов Encyclopedia Britannica. - #WTFact Видео
В #WTFact Britannica делится некоторыми из самых странных фактов, которые мы можем найти. - На этот раз в истории
В этих видеороликах узнайте, что произошло в этом месяце (или любом другом месяце!) в истории. - Demystified Videos
В Demystified у Britannica есть все ответы на ваши животрепещущие вопросы.
- Студенческий портал
Britannica — это главный ресурс для учащихся по ключевым школьным предметам, таким как история, государственное управление, литература и т. д. - Портал COVID-19
Хотя этот глобальный кризис в области здравоохранения продолжает развиваться, может быть полезно обратиться к прошлым пандемиям, чтобы лучше понять, как реагировать сегодня. - 100 женщин
Britannica празднует столетие Девятнадцатой поправки, выделяя суфражисток и политиков, творящих историю.




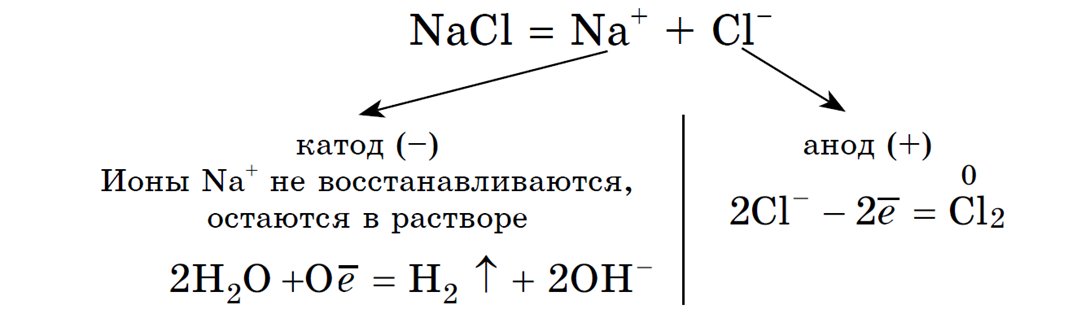


 ..
.. ..
..