Водородная вода
Москва
- Главная
- Поддержка
- Полезное
- Что такое водородная вода?
Водород вокруг нас
На долю водорода приходится 1% от массы Земли, это достаточно много. Но в мире вокруг нас он находится в основном в виде соединений с другими элементами — входит в состав растений, животных и, конечно, воды — самого распространенного на Земле вещества. А вот газообразного водорода «в чистом виде» не так уж много. Организму он не нужен: мы им не дышим, не едим его, не впитываем кожей.
Но в мире вокруг нас он находится в основном в виде соединений с другими элементами — входит в состав растений, животных и, конечно, воды — самого распространенного на Земле вещества. А вот газообразного водорода «в чистом виде» не так уж много. Организму он не нужен: мы им не дышим, не едим его, не впитываем кожей.
В учебнике химии за 8 класс четко сказано: при комнатной температуре h3 ни в какие реакции не вступает, и растворимость его в воде исключительно мала: в 1 л воды при 20°С растворяется всего 18 мл водорода. Его низкая активность объясняется прочной связью между атомами водорода.
Если не водородная, то какая?
Ни один научный сотрудник (не путать с маркетологом в белом халате!) не скажет, что такая вода полезна. Но вернемся к эффекту плацебо и положительному настрою: он действительно может творить чудеса.
Быстрые ссылки Регистрация фильтраЗарегистрируйте ваш фильтр и мы напомним, когда нужно его заменить
зарегистрировать Заказ установкиПрофессиональный монтаж и установка наших фильтров
заказать Связатьсясо службой поддержки
8 800 555-30-35 Круглосуточно
Адреса сервисных центровв Москве
Заявка на видеоконсультацию
1
мессенджер для связи
2
контактные данные
3
выбор даты
Заявка отправлена
Наш сотрудник проведет видеоконсультацию в выбранное время
Из чего состоит вода? Окружающий мир, 3 класс — Природа Мира
Содержание
- Состав воды
- Физические свойства
- Виды воды
- Таблица 1.
 Классификация воды по содержанию солей
Классификация воды по содержанию солей - Интересные факты
- Что мы узнали?
Вода – источник жизни на нашей голубой планете. Она есть в клетках всех живых организмов. Это самое распространённое в мире вещество. Вода – один из важнейших факторов, определяющих природные условия на Земле, и влияет на формирование климата и рельефа территории.
Слово «вода» происходит от древнегерманского «текучий, мокрый».
Состав воды
Схема структуры молекулы водыМолекула воды (H2O) складывается из 2-х атомов водорода и 1-го атома кислорода. Это два газообразных вещества, которые, соединяясь, образуют невероятно прочные связи. Главную роль в молекуле выполняет атом кислорода. Атомы водорода несут положительный заряд, а атом кислорода – отрицательный. Каждый из атомов водорода, крепко держась в образованной молекуле, одновременно притягивается к атому кислорода из соседней молекулы. Связи кислорода и водорода из соседних молекул гораздо слабее, чем внутри. Благодаря этим межмолекулярным связям, вода обладает рядом удивительных свойств.
Благодаря этим межмолекулярным связям, вода обладает рядом удивительных свойств.
Физические свойства
Дрейфующий ледВода – уникальное вещество на планете, способное быть в трех физических состояниях:
- Газообразное
- Жидкое
- Твердое
Если спросить человека, что такое вода, то самый популярный ответ будет: «Это жидкость» . Жидкое самое распространённое в природе состояние воды.
Изменение состояния воды возможно благодаря тому, что под действием температур меняется расстояние между молекулами. В твердой форме – молекулы наиболее близко расположены друг к другу. В жидкой – подальше. В газообразной – совсем далеко, что позволяет им отрываться. При температуре от 100°С и выше это пар. От 0°С до 100°С – это вода. А ниже 0°С – это лед.
Когда вода замерзает, ее молекулы выстраиваются в правильные шестигранные формы. Все кристаллы льда похожи друг на друга. Лед обладает уникальным свойством — он легче самой воды, из которой получен, и никогда не тонет в ней.
Поэтому этому водоемы всегда замерзают сверху, что позволяет сохранить жизнь на дне.
В атмосфере всегда есть мельчайшие капельки воды. Но присутствие влаги мы замечаем только тогда, когда её количество увеличивается, формируя облака и туман.
Виды воды
Морская водаВся вода делится на категории:
- Солёная (моря, океаны)
- Пресная (реки, озера, ледники, подземные воды)
- Дождевая
- Минеральная
- Вода, обработанная человеком (водопроводная, канализационная, дистиллированная, искусственная)
На планете примерно 96,5 % воды приходится на долю морской воды. Пресной — намного меньше. Её доля – около 2,5 %, причём большая часть – в ледниках и грунтовых водах. Менее 0,3 % от всей пресной воды содержится в реках, озёрах и атмосфере, а в живых организмах – всего 0,003 %.
У природных вод есть важный признак – прозрачность. От этого зависит, как глубоко смогут проникнуть солнечные лучи в толщу воды. Цветность определяется количеством растворенных органических соединений, которые окрашивают воду при прохождении её через торфяные и гумусные слои почвы.
Цветность определяется количеством растворенных органических соединений, которые окрашивают воду при прохождении её через торфяные и гумусные слои почвы.
Природная солёная вода содержит большое количество разных примесей минеральных и органических соединений. Количество этих веществ оказывает влияние на плотность воды. Самые плотные в природе это морская и минеральная воды. Самой плотной считается вода Мёртвого моря. По степени солёности вода делится на несколько категорий:
Таблица 1. Классификация воды по содержанию солей
| Наименование | Концентрация солей | Где встречаются |
|---|---|---|
| Рассолы | Более 50 г/л | Мертвое море, Озеро Ретба, Пруд Гаэтале |
| С повышенной солёностью | 10-35 г/л | Красное море, Средиземное море, Мировой океан |
| Солёные | 3-10 г/л | Мраморное море, Черное море |
| Солоноватые | 1-3 г/л | Азовское море, Белое море |
| С повышенной минерализацией | 0,5-0,1 г/л | Минеральная вода Боржоми, Нарзан |
В пресной воде тоже есть соли. В основном это кальций и магний. Для такой воды есть характеристика жёсткости. Чем больше содержание примесей, тем более жёсткой называют воду.
В основном это кальций и магний. Для такой воды есть характеристика жёсткости. Чем больше содержание примесей, тем более жёсткой называют воду.
Чистой воды в природе никогда не бывает. Вода хорошо растворяет в себе разные вещества – твердые, жидкие и газообразные. Даже дождевая вода пока падает на землю, захватывает из воздуха пыль и газы и растворяет их в себе.
Человек для своих нужд изменяет воду. В водопроводе течет пресная вода из рек и водохранилищ. Она проходит 5 стадий очистки, обеззараживается. В канализацию попадает вода загрязнённая примесями и частицами от человеческой жизнедеятельности. Прежде чем выпустить такую воду в окружающую среду, стоки очищают на специальных очистных сооружениях.
Дистиллированную воду используют в разных областях, чаще в научной и технической. Получают её, испаряя и затем осаждая пар на холодной поверхности. Примеси остаются в перегонном сосуде. Такая вода является наиболее чистой из всех возможных.
Пресная вода на планете распространена неравномерно. Есть области, где существует сильная её нехватка. Для решения проблемы в таких районах строят водоопреснительные станции. На этих станциях морскую воду выпаривают и получают дистиллированную воду, которая тоже непригодна для использования человеком. Её насыщают минеральными солями до показателей природной пресной воды.
Есть области, где существует сильная её нехватка. Для решения проблемы в таких районах строят водоопреснительные станции. На этих станциях морскую воду выпаривают и получают дистиллированную воду, которая тоже непригодна для использования человеком. Её насыщают минеральными солями до показателей природной пресной воды.
Интересные факты
Многие столетия вода считалась простым веществом. В 1783 году химик Лавуазье смог разложить воду на два вещества и предположить количественное их соотношение в молекуле.
В обычных условиях вода не имеет ни вкуса, ни запаха. Вода бесцветна, но при толщине более 2 метров она приобретает голубой цвет. Это происходит благодаря рассеиванию коротких лучей солнечного спектра.
Вода – сильный поглотитель солнечной энергии. У воды есть замечательное свойство – медленно нагреваясь, она и медленно остывает. Мировой океан планет накапливает тепло летом и отдаёт его зимой. Так сглаживаются скачки температуры на планете. Суточные и сезонные колебания температуры уменьшаются вблизи водных объектов. Чем меньше в той или иной местности крупных водоемов, тем более резкоконтинентальный там климат.
Суточные и сезонные колебания температуры уменьшаются вблизи водных объектов. Чем меньше в той или иной местности крупных водоемов, тем более резкоконтинентальный там климат.
Что мы узнали?
Вот краткий список основных сведений о воде, ее составе и свойствах:
- Молекула воды состоит из 2-х атомов водорода и 1 атома кислорода
- Лед легче воды
- Вода – единственное на планете вещество, способное пребывать в трех агрегатных состояниях: газообразном, твердом, жидком
- В воде всегда присутствуют примеси
- Количество морской воды на планете гораздо больше, чем пресной
- Вода регулирует температуру планеты
Гугломаг
Спрашивай! Не стесняйся!
Задать вопрос
Не все нашли? Используйте поиск по сайту
Search for:Впервые ученые увидели, как вода накапливает дополнительные протоны
Основы химии
Ученые фиксируют сложную структуру в бассейне льда глубиной молекул
22
Поделиться на Facebook
Поделиться на Twitter
Поделиться на Reddit
Поделиться на LinkedIn
900 12Отправить по электронной почте
Версия для печати
Чтобы воплотить в жизнь эффективную технологию водородной энергетики — от производства водорода путем электролиза до химических топливных элементов следующего поколения — ученым необходимо точно знать, как отдельные атомы водорода перемещаются в воде.
Нейтральная молекула воды состоит из двух атомов водорода, связанных с одним атомом кислорода, при этом вся структура изгибается, чтобы дать молекуле частично положительную сторону и частично отрицательную сторону, как у магнита. Если бы вы могли увеличить стакан с водой, вы бы увидели триллионы таких молекул, а также несколько избыточных отдельных атомов водорода, которые потеряли свои электроны (другими словами, просто протоны). В течение 200 лет исследователи предполагали, что эти протоны перескакивают с одной молекулы воды на другую, прикрепляясь к ближайшей молекуле и отталкивая один из уже связанных там протонов. Затем этот протон связывается со следующим соседом. Теперь группа ученых из Пекина впервые получила изображение таких частиц под микроскопом, что помогло понять, как происходят эти скачки.
Модели предсказывали, что этот процесс чаще всего происходит двумя способами. В одном протон связывается непосредственно с одной молекулой воды, превращая ее из нейтральной молекулы в положительный ион. Три окружающие нейтральные молекулы воды ориентируются таким образом, что их частично отрицательные стороны стабилизируют этот заряд. В другом варианте лишний протон находится между отрицательными концами двух нейтральных молекул воды, так что каждая из них разделяет нагрузку положительного заряда.
Три окружающие нейтральные молекулы воды ориентируются таким образом, что их частично отрицательные стороны стабилизируют этот заряд. В другом варианте лишний протон находится между отрицательными концами двух нейтральных молекул воды, так что каждая из них разделяет нагрузку положительного заряда.
Исследователи смогли проверить эти ориентации с помощью атомно-силовой микроскопии — метода, который генерирует изображения путем отслеживания наноскопического острия специальной иглы по неровностям на поверхности. Используя это оборудование, Цзин Го, химик из Пекинского педагогического университета, и ее коллеги изобразили сеть воды толщиной в молекулу, застывшую на металлическом листе, и показали, как дополнительные протоны изменили эту сеть. Их работа была опубликована в Наука.
Потребовались невероятно точные измерения, чтобы различить две конфигурации воды. «Положение протонов вдоль водородной связи отличалось всего примерно на 20 пикометров, — говорит Го, — это меньше половины длины самого атома водорода. «Мы очень, очень рады выяснить основные картины после долгой борьбы».
«Мы очень, очень рады выяснить основные картины после долгой борьбы».
Команда обнаружила, что эти две конфигурации возникают с разной частотой и в разных соотношениях в зависимости от того, к какому типу металла была заморожена вода. Они также использовали электричество, чтобы заставить воду переключаться между различными установками. «Очень поразительно, что они могут [непосредственно] наблюдать за этими вещами», — говорит Томас Кун, химик-теоретик из Падерборнского университета в Германии, не участвовавший в этой работе. «Это открывает двери для изучения механизмов [выработки водорода]», — говорит он. «И, может быть, из этого выйдет что-то хорошее».
Эта статья была первоначально опубликована под названием «Водная сеть» в журнале Scientific American 327, 5, 26 (ноябрь 2022 г.)
doi:10.1038/scientificamerican1122-26a
ОБ АВТОРЕ(АХ)

Фионна, доктор медицины, Сэмюэлс была научным сотрудником AAAS по средствам массовой информации в 2022 году в Scientific American . Она получает докторскую степень. по химии в Университете штата Колорадо. Подпишитесь на нее в Твиттере @Fairy__Hedgehog
Читать дальше
Информационный бюллетень
Будьте умнее. Подпишитесь на нашу новостную е-мэйл рассылку.
Регистрация
Поддержка научной журналистики
Откройте для себя науку, которая изменит мир. Изучите наш цифровой архив с 1845 года, включая статьи более 150 лауреатов Нобелевской премии.
Подпишитесь прямо сейчас!ЭСА — Капля воды
Наука и исследования10919 просмотров 16 лайков
Введение
Вода – самое распространенное вещество на поверхности Земли. Без него жизнь не могла бы существовать. Ваше тело примерно на 70% состоит из воды.
Вода может существовать в 3 состояниях:
- Твердое (лед)
- Жидкость (вода) и
Его состояние можно изменить путем нагревания или охлаждения (или изменения давления)
Как меняется состояние воды?
Когда лед слегка нагревается, он начинает таять и превращается в жидкость.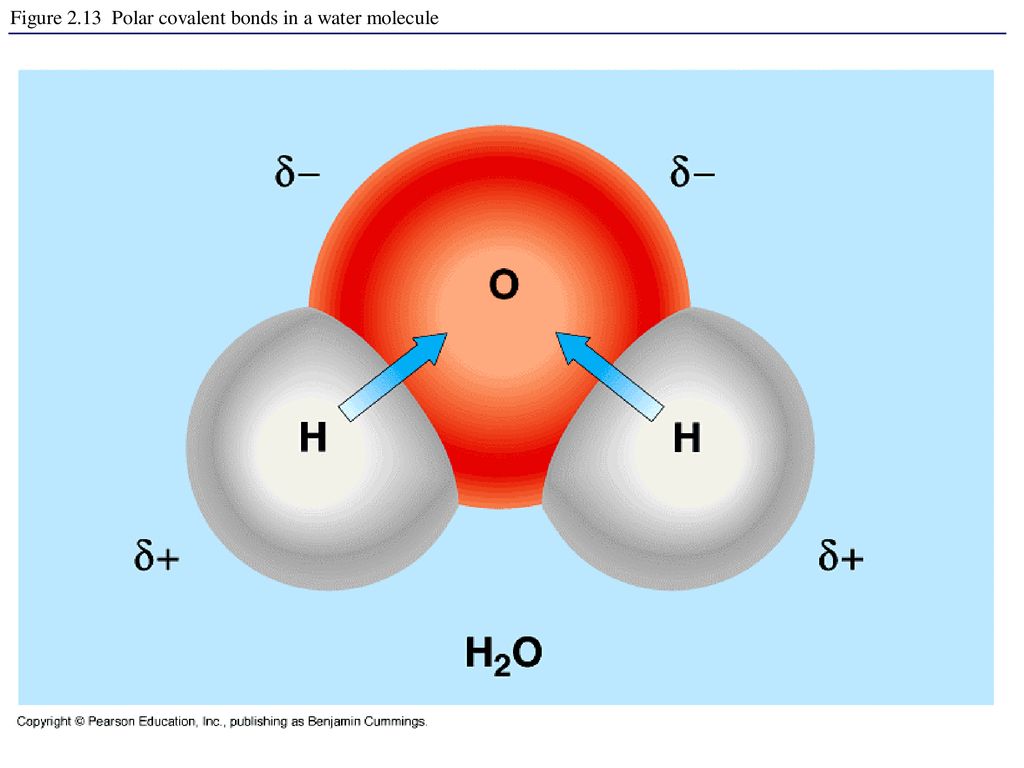 Когда вы продолжаете нагревать до температуры около 100° по Цельсию, он превращается в газ.
Когда вы продолжаете нагревать до температуры около 100° по Цельсию, он превращается в газ.
Почему это происходит?
Вода представляет собой молекулу с химической формулой h3O, где два атома водорода присоединены к одному атому кислорода. Частицы твердого льда плотно упакованы и соединены химическими связями, называемыми водородными связями. Все время вибрируют. Когда вы нагреваете лед, энергия, которую вы вкладываете, усиливает вибрации. Некоторые связи разрываются, и частицы могут немного свободно перемещаться — тогда лед становится жидким. По мере того, как применяется больше тепла, частицы получают достаточно энергии, чтобы разорвать все свои связи и выйти в виде газа или пара.
Свойства воды
Вода, нагретая примерно до 100° по Цельсию, становится газом Физическое свойство материи, которое описывает, насколько плотно упакованы отдельные частицы вещества, называется плотностью.
Плотность (D) является мерой количества материала (масса или m) в данном пространстве (объем или V) и выражается в виде отношения:

Разница в плотности материи Земли — это то, что движет океанскими течениями, ветром и тектоникой плит.
Обычно плотность вещества увеличивается по мере того, как оно переходит из газа в жидкость, а затем снова из жидкого состояния в твердое. Плотность также увеличивается при понижении температуры, потому что понижение температуры вызывает меньшую вибрацию атомов. Поскольку атомы не так сильно перемещаются, они упаковываются более плотно или плотно друг к другу. Вода, однако, другая! Вода обладает очень необычными физическими и химическими свойствами, что делает ее одним из самых важных веществ на нашей планете.
Посмотрите видеозапись того, как астронавт ЕКА Франк Де Винн демонстрирует несколько демонстраций поведения воды в условиях невесомости на Международной космической станции. Педагоги могут использовать этот клип вместе с примечаниями к уроку ниже, чтобы позволить маленьким детям сравнить поведение воды на Земле и в космосе.
1. Твердая вода – как необычно это твердое вещество!
Почему твердая вода (лед) необычна?
Можно было бы ожидать, что твердое вещество, такое как лед, утонет. Однако вы знаете, что когда вы кладете в напиток несколько кубиков льда, он всплывает. Наполните пластиковую бутылку водой и закройте крышку. Поместите его в морозилку и посмотрите, как он будет выглядеть на следующий день. Вы заметите, что верхняя часть может отскочить, и бутылка с водой выглядит так, как будто она расширилась.
Однако вы знаете, что когда вы кладете в напиток несколько кубиков льда, он всплывает. Наполните пластиковую бутылку водой и закройте крышку. Поместите его в морозилку и посмотрите, как он будет выглядеть на следующий день. Вы заметите, что верхняя часть может отскочить, и бутылка с водой выглядит так, как будто она расширилась.
Твердая форма воды (лед) МЕНЕЕ плотна, чем жидкая форма. Плотность чистой воды при четырех градусах Цельсия составляет 1,0 г/см в кубе, а плотность льда при 0 градусов Цельсия составляет всего 0,92 г/см в кубе. Жидкая вода и лед имеют разную плотность, потому что во льду молекулы находятся дальше друг от друга, занимая больше места, чем в молекуле жидкой воды.
В космосе: Фрэнк берет небольшой кусок льда и кладет его в каплю воды. Что происходит со льдом внутри капли воды? Он плавает или тонет или делает что-то еще?
Ответы:
На Международной космической станции все находится в состоянии СВОБОДНОГО ПАДЕНИЯ, поэтому кажется, что сила ТЯЖЕСТИ отсутствует. Гравитация — это то, что не дает нам уплыть здесь, на Земле. Если вы что-то бросите, оно всегда упадет на землю. Ой!
Гравитация — это то, что не дает нам уплыть здесь, на Земле. Если вы что-то бросите, оно всегда упадет на землю. Ой!
Это притяжение, притягивающее все к земле, называется Силой Гравитации. Так что точно так же, как космонавты (и все, что не привязано крепко!) Все будут плавать на МКС. Даже вода. Лед не будет плавать или тонуть, а просто будет двигаться вокруг капли воды.
2. Полярность воды
Вода представляет собой диполярную молекулу. Вода имеет химическую формулу H
Демонстрация дипольной природы воды
Материалы:
- Работа у источника воды (например, у крана)
- Стеклянная палочка или пластиковая линейка
Метод:
- Позвольте слабой струе воды течь из крана.

- Возьмите линейку или стержень и поднесите к потоку воды. Что-нибудь происходит?
- Теперь несколько раз потрите линейкой или стержнем ткань или футболку. Поднесите его ближе к воде. Что происходит сейчас? Как вы думаете, почему это происходит?
На Международной космической станции Фрэнк Де Винн использует кусок пластика (вместо стержня), чтобы создать некоторый заряд (например, положительный + заряд). Натирая этим пластиком свою одежду, он вызывает накопление положительного заряда на поверхности. Поднеся его ближе к капле воды, заряд пластика будет притягивать противоположный заряд молекул воды (отрицательный заряд кислорода).
Вопрос для размышления:
Почему у Фрэнка не может быть потока воды на МКС? Что происходит с каплей воды, когда он приближает к ней пластик?
Ответ:
Стержень или линейка будут притягивать к себе поток, так как на стержне имеется положительный заряд, а на молекуле воды он притягивает отрицательный заряд.
Когда Фрэнк подносит пластик близко к воде, капля должна двигаться, пока он перемещает заряженный пластик. Отрицательно заряженный кислород будет притягиваться к положительному заряду заряженного пластика.
Фрэнк не может использовать поток воды на МКС, потому что все плавает (находится в свободном падении) и вода может легко попасть в электрооборудование и повредить его. Вода должна поступать из специального мешка для питьевой воды, после чего ее необходимо вытирать.
3. Растворимость в воде
Вода прозрачная, поэтому, если в ней что-то растворить, вода может изменить цвет.Вода обладает очень важным свойством растворять многие твердые вещества и газы. Что происходит, когда вы добавляете сахар (твердое вещество) в кофе? Говорят, что сахар растворяется в воде. Некоторые вещи нерастворимы (не растворяются). Вы можете думать о любом? Вода прозрачная, поэтому, если что-то в ней растворить, вода может изменить цвет.
Попробовать: Что растворяется?
Материалы:
кубиков сахара, крупинки соли, растворимый кофе и кофейная гуща, небольшие кусочки дерева (стружка, сено), мелкие стружки пластика, стружка свечей, стеклянные банки, ложка или мешалка, источник воды и место для утилизации отходов.


 Классификация воды по содержанию солей
Классификация воды по содержанию солей Поэтому этому водоемы всегда замерзают сверху, что позволяет сохранить жизнь на дне.
Поэтому этому водоемы всегда замерзают сверху, что позволяет сохранить жизнь на дне.