строительные блоки молекул / Хабр
Если молекулы – основные структуры, задействованные в химии – это слова, из которых состоят все окружающие нас материалы, тогда атомы – это буквы, строительные блоки молекул. Слова бывают разной длины, и типичная молекула тоже может содержать несколько атомов, или несколько сотен, или даже сто тысяч атомов. Молекула столовой соли NaCl состоит из двух атомов, натрия Na и хлора Cl. Молекула воды H2O содержит два атома водорода и один кислорода. Молекула столового сахара C12H22O11 содержит 12 атомов углерода, 11 кислорода и 22 водорода, организованных определённым образом.Откуда нам известно о существовании атомов? Иногда их можно «видеть», так же, как мы видим молекулы, которые они могут формировать. Не глазами, но более продвинутыми устройствами. Один из методов использует сканирующий туннельный микроскоп, способный показывать атомы в кристалле или даже передвигать их по одному. Другой метод использует нашу возможность захвата ионов (немного изменённых атомов – подробности ниже).
На фото – три иона, пойманных одновременно. На них падает свет, они поглощают его и снова испускают. Повторно испущенный свет можно обнаружить, благодаря чему мы можем увидеть, где находятся ионы – примерно так отражение света от небольшого, но яркого бриллианта может помочь нам найти его.
Сколько же типов атомов существует? Типы называются «химическими элементами» и точное их количество зависит от того, как их считать. Но допустим, что атомный алфавит состоит из примерно сотни химических элементов, а к тонкостям подсчёта вернёмся позже. Так же, как мы могли назначить буквам алфавита от А до Я номера от 1 до 33, каждому элементу назначается не только имя, но и атомный номер (обозначается «Z»). Самые простые атомы – у водорода, их атомный номер = 1. Самые сложные в изобилии встречаются в природе, это уран с атомным номером 92. Другие – кислород (8), азот (7), кальций (20), криптон (36), лантан (57), платина (78). Полный список ищите в периодической системе элементов Менделеева.
Вопросы, которые можно задать об атомах:
1. Из чего состоят атомы?
2. В чём смысл атомного номера?
3. Каков главный источник различий в химическом поведении атомов разных элементов?
4. До какой степени разные атомы одного элемента схожи между собой?
5. Как части атома удерживаются вместе?
6. Почему атомы удерживаются вместе и образуют молекулы?
Оказывается, на все эти вопросы лучше всего отвечать, начав с первого: из чего состоят атомы? Атомы состоят из того, что обычно называют «субатомными частицами» (к сожалению, этот термин некорректен, поскольку у этих «частиц» есть некоторые свойства, частицам не присущие). Конкретнее, атомы состоят из набора небольших и очень лёгких электронов, окружающих крохотное, но тяжёлое атомное ядро, в котором содержится большая часть массы атома.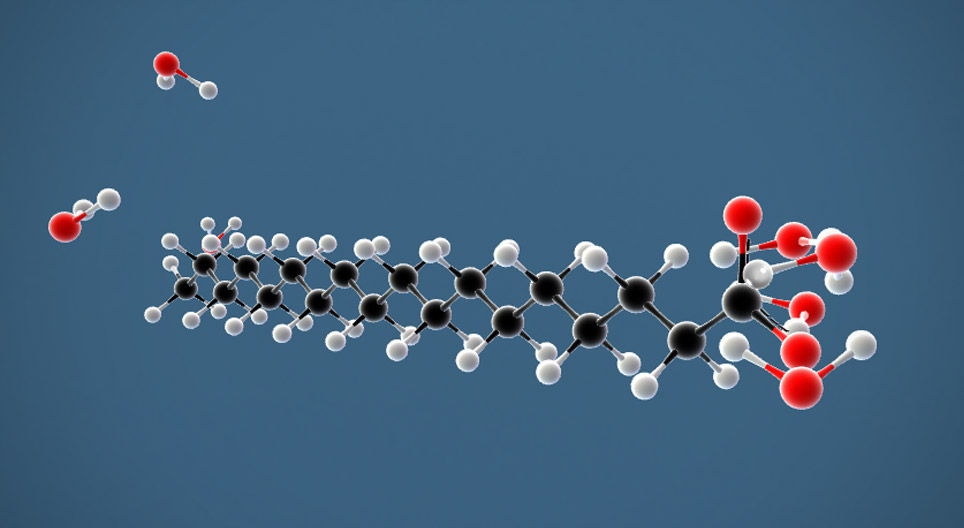
Рисованный атом
Частенько мы видим изображения атомов, нарисованные на книгах по химии, на рекламках и предупреждающих знаках. Пример – рис. 1. Он передаёт очень грубую идею того, как устроен атом: снаружи у него есть определённое количество электронов (синие), и они вращаются вокруг центрального атомного ядра. Ядро – это скопление протонов (красные) и нейтронов (белые).
Рис. 1
Теперь мы можем ответить на 2-й вопрос: что означает атомное число Z? Это просто количество протонов в ядре. У кислорода атомный номер 8, и у него в ядре 8 протонов.
В простейших условиях атомное число также равняется количеству электронов атома. С количеством нейтронов всё сложнее, мы вернёмся к этому позже. У электронов отрицательный электрический заряд (-е), а у протонов – положительный (+е). Нейтроны нейтральны, электрического заряда у них нет. Когда количество электронов и протонов совпадает, их заряды взаимно уничтожаются, и у атома электрического заряда не наблюдается – такой атом нейтрален.
Но нет ничего необычного – к примеру, в процессе формирования молекул – если атом приобретёт или потеряет один или несколько внешних, валентных электронов. В этом случае электрические заряды электронов и протонов не уничтожаются, и получившийся заряженный атом называют ионом.
Более реалистичный атом
Хотя рис. 1 примерно описывает архитектуру атома – электроны действительно находятся снаружи, а ядро, состоящее из протонов и нейтронов, в середине – он совершенно не передаёт реальную форму и суть атома, поскольку он выполнен не в масштабе, а мы живём в квантовом мире, в котором объекты ведут себя так, что их сложно нарисовать или представить.
С проблемой масштаба можно разобраться, нарисовав более точное (хотя всё ещё несовершенное) изображение, рис. 2.

Вот, что я попытался передать этим изображением. Во-первых, электроны очень, очень малы, настолько малы, что мы так и не смогли измерить их размер – может статься, что они точечные и не имеют размера, но они точно не больше, чем 1/100 000 000 от диаметра атома. Во-вторых, ядра (и протоны с нейтронами, их составляющие) также крайне малы, хотя они и больше, чем электроны. Их размер измерен, и он примерно в 10 000 – 100 000 раз меньше диаметра атома. Атом немного похож на деревню. Протоны и нейтроны в ядре – большие дома, находящиеся в центре деревни, а электроны – далеко разбросанные фермерские домики. На большей части сельской местности растут зерновые культуры и нет домов. И хотя территория, считающаяся частью деревни, может быть большой, реально занимаемая домами площадь очень мала.
Но эта аналогия не полная, поскольку электроны, в отличие от фермерских домиков, очень быстро двигаются по серому региону на картинке и вокруг ядра со скоростями порядка 1% от скорости света.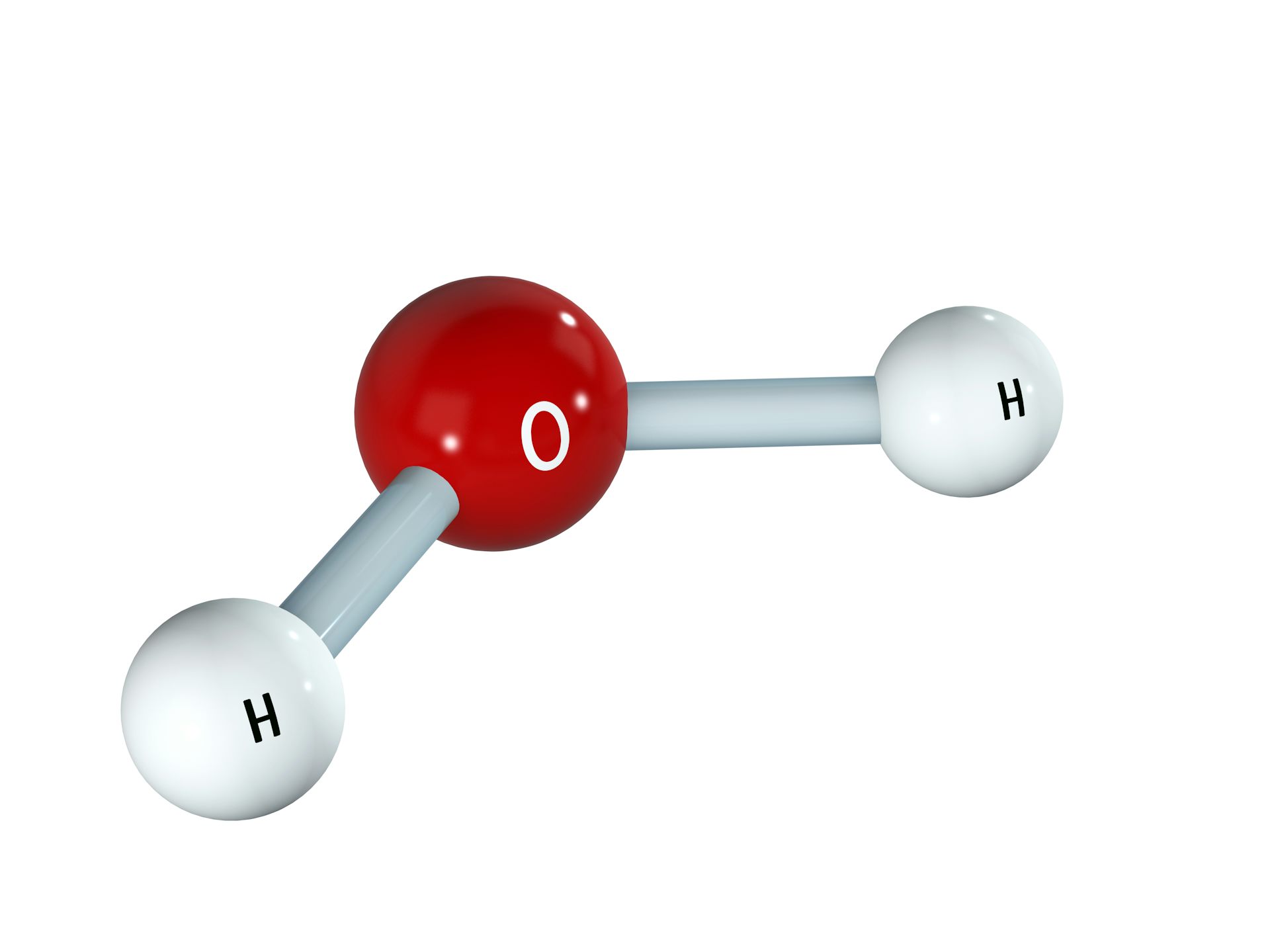
Но, как я вас предупреждал, рис. 2 тоже не точный. Во-первых, нужно было бы нарисовать ядро в тысячи раз меньше, а электроны – в миллионы раз меньше, только тогда их не было бы видно. Если бы атом был размером с вашу спальню, то его ядро было бы размером с пылинку. По сравнению со своими компонентами, атомы огромны! В каком-то смысле большую часть атома составляет пустота!
Во-вторых, изображение не передаёт мутную природу квантовой механики. Уравнения квантовой механики описывают и предсказывают поведение молекул, атомов и субатомных частиц, и эти уравнения говорят нам, что у этих частиц могут быть очень странные и неинтуитивные свойства. Хотя электроны в каком-то смысле точечные (допустим, если вы захотите столкнуть два электрона друг с другом, то обнаружите, что можете сдвинуть их вместе на сколь угодно малое расстояние, и они ничем не выдадут своей внутренней структуры, если она вообще есть), есть возможность сделать так, что они, будучи оставленными в покое, будут распространяться как волна и заполнят всё серое пространство на рис.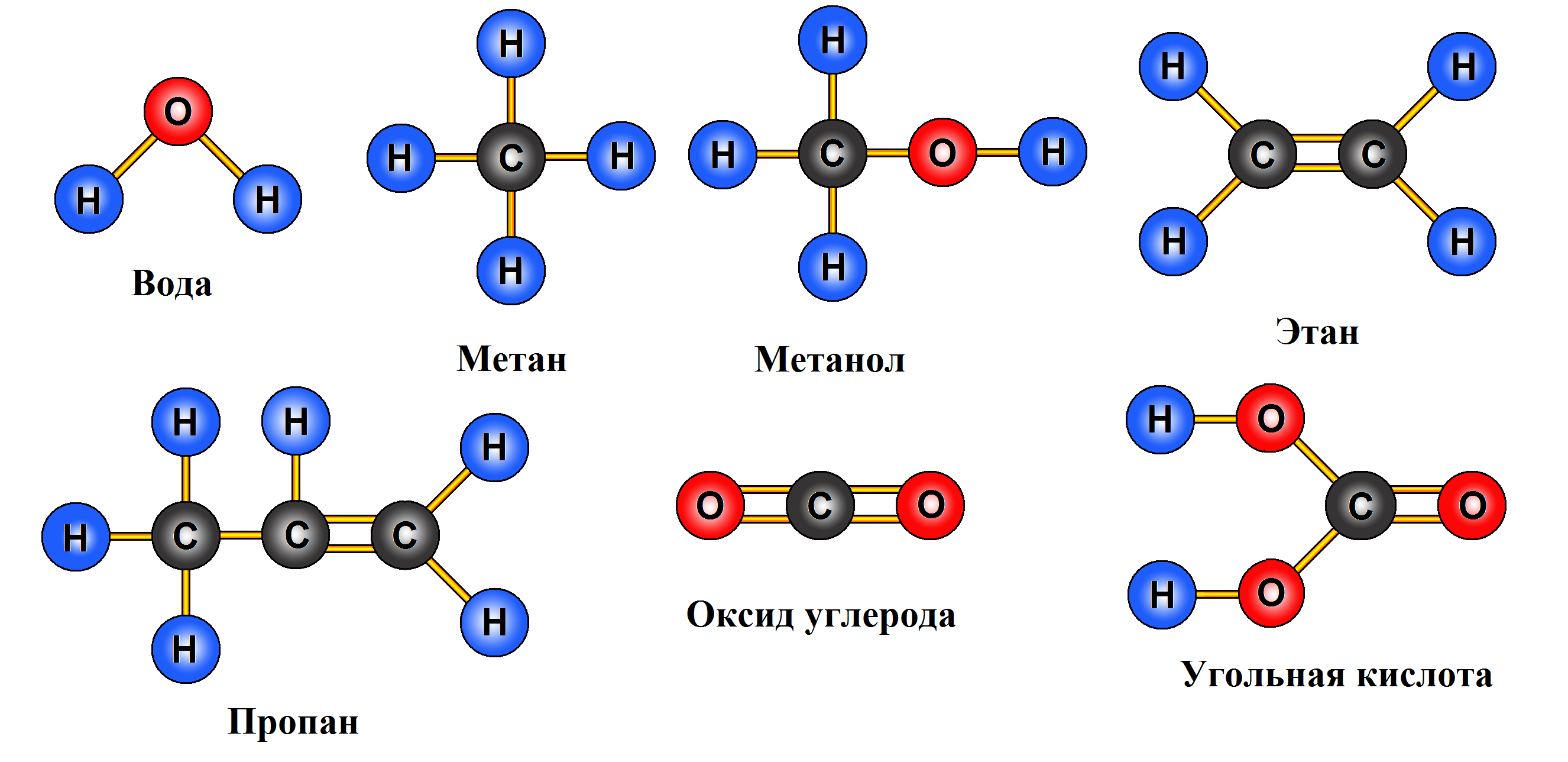
Размер электрона слишком мал для измерения, и его масса настолько мала, что электрон может распространиться по всему атому. А вот у ядра есть вполне измеренный и известный размер, а его масса так велика – больше 99,9% массы всего атома – что оно вообще не распределяется в пространстве. Ядро сидит в середине серой области.
Атом и его химия
Лучший приходящий мне в голову способ описать атом: большая часть массы атома содержится в ядре, находящемся в его центре, вокруг которого распределились чрезвычайно мелкие электроны гораздо меньшей массы, причём сделали это совершенно не так, как ведут себя частицы, заполнив всю серую область рис. 2.
 Химия происходит – то есть, формируются и меняются молекулы – когда атомы приближаются друг к другу, а это происходит, когда внешние, валентные электроны одного атома близко подходят к внешним электронам другого – когда край серой области одного атома приближается к краю серой области другого. В химических процессах атомное ядро остаётся в центрах атомов, и никогда не приближается к другим ядрам. Основная роль ядра – обеспечение положительного заряда, удерживающего электроны, и большей части массы (определяющей, как сложно другим объектам передвигать этот атом).
Химия происходит – то есть, формируются и меняются молекулы – когда атомы приближаются друг к другу, а это происходит, когда внешние, валентные электроны одного атома близко подходят к внешним электронам другого – когда край серой области одного атома приближается к краю серой области другого. В химических процессах атомное ядро остаётся в центрах атомов, и никогда не приближается к другим ядрам. Основная роль ядра – обеспечение положительного заряда, удерживающего электроны, и большей части массы (определяющей, как сложно другим объектам передвигать этот атом).Это отвечает на 3-й вопрос: химию атома в основном определяют подробности, связанные с его внешними электронами. Эти детали можно узнать (сложным способом, через уравнения квантовой механики), исходя из атомного номера Z.
Вместо того, чтобы заняться химией – темой, которой хватит на целый курс – мы перейдём на уровень ниже, к субатомным частицам, по пути отвечая на другие вопросы. Перечислим вопросы, с которыми мы разобрались, и вопросы, которые ещё предстоит изучить.
1. Из чего состоят атомы? Снаружи – электроны, в центре – атомное ядро (из протонов и нейтронов).
2. В чём смысл атомного номера? Это количество протонов в ядре атома, которое, в обычных условиях равно количеству электронов, его окружающих.
3. Каков главный источник различий в химическом поведении атомов разных элементов? Свойства внешних электронов, определяемые общим количеством электронов у каждого элемента, к примеру, атомным номером.
4. До какой степени разные атомы одного элемента схожи между собой? Обсудим это в статье про изотопы.
5. Как части атома удерживаются вместе? Обсудим это в статье о роли электрических сил и квантовой механики.
6. Почему атомы удерживаются вместе и образуют молекулы? Обсудим это в статье о роли электронов и электрических сил в построении молекул из атомов.
А вот вам ещё вопрос, который мог возникнуть при изучении рис. 2:
Если атом – по большей части пуст, почему объекты кажутся твёрдыми? Почему нельзя протянуть руку через экран компьютера, если экран состоит из атомов, по большей части пустых?
Мощные лазеры помогли ученым увидеть, как вращается одиночная молекула
https://ria. ru/20190729/1556966223.html
ru/20190729/1556966223.html
Мощные лазеры помогли ученым увидеть, как вращается одиночная молекула
Мощные лазеры помогли ученым увидеть, как вращается одиночная молекула — РИА Новости, 29.07.2019
Мощные лазеры помогли ученым увидеть, как вращается одиночная молекула
Датские и немецкие физики впервые сняли на видео то, как вращается одиночная молекула, состоящая из трех разных атомов, и сравнили эти наблюдения с… РИА Новости, 29.07.2019
2019-07-29T13:11
2019-07-29T13:11
2019-07-29T13:11
молекулы
атомы
физика
открытия — риа наука
германия
наука
/html/head/meta[@name=’og:title’]/@content
/html/head/meta[@name=’og:description’]/@content
https://cdn25.img.ria.ru/images/155696/38/1556963841_32:16:2000:1123_1920x0_80_0_0_154e96d345c763a17c148af3a9ae6835.jpg
МОСКВА, 29 июл – РИА Новости. Датские и немецкие физики впервые сняли на видео то, как вращается одиночная молекула, состоящая из трех разных атомов, и сравнили эти наблюдения с предсказаниями теории.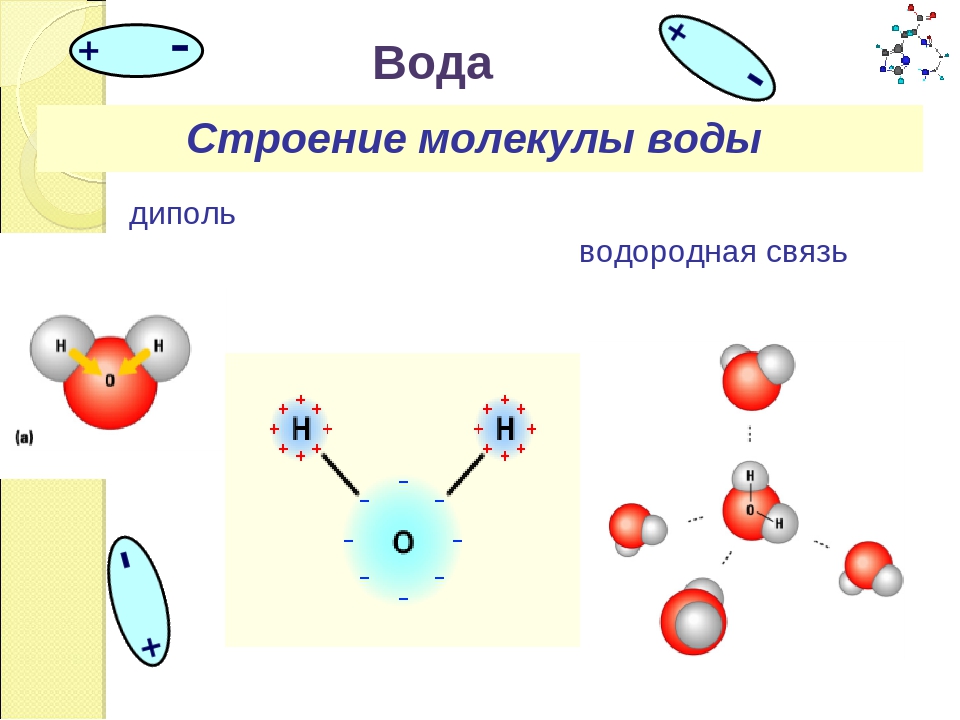 Их выводы были опубликованы в журнале Nature Communications.В последние годы, благодаря постройке мощных рентгеновских лазеров, способных вырабатывать пучки света с огромной скоростью, ученые смогли заглянуть в самые далекие глубины мира молекул и элементарных частиц. К примеру, в начале этого десятилетия они получили первые «атомные» фотографии вирусов и белков. В последующие годы физики смогли снять химическую реакцию на видео, сфотографировать электроны внутри алмаза, а также получить первые фотоснимки одиночной водородной связи, играющей ключевую роль в формировании белковых молекул, ДНК и других «молекул жизни».Все эти достижения, как отмечает Кюппер, не позволяли ученым решить более простую задачу – увидеть то, как вращается молекула и меняет свою структуру в ходе взаимодействий с соседями или во время простых химических реакций. Этому мешало то, что рентгеновские лазеры разрушают изучаемую молекулу практически сразу после того, как импульс света пролетает через нее.Немецкие физики нашли остроумное решение для этой проблемы, используя не одну, а несколько сотен молекул, два разных типа лазеров, а также определенные закономерности квантовой механики, упростившие им задачу.
Их выводы были опубликованы в журнале Nature Communications.В последние годы, благодаря постройке мощных рентгеновских лазеров, способных вырабатывать пучки света с огромной скоростью, ученые смогли заглянуть в самые далекие глубины мира молекул и элементарных частиц. К примеру, в начале этого десятилетия они получили первые «атомные» фотографии вирусов и белков. В последующие годы физики смогли снять химическую реакцию на видео, сфотографировать электроны внутри алмаза, а также получить первые фотоснимки одиночной водородной связи, играющей ключевую роль в формировании белковых молекул, ДНК и других «молекул жизни».Все эти достижения, как отмечает Кюппер, не позволяли ученым решить более простую задачу – увидеть то, как вращается молекула и меняет свою структуру в ходе взаимодействий с соседями или во время простых химических реакций. Этому мешало то, что рентгеновские лазеры разрушают изучаемую молекулу практически сразу после того, как импульс света пролетает через нее.Немецкие физики нашли остроумное решение для этой проблемы, используя не одну, а несколько сотен молекул, два разных типа лазеров, а также определенные закономерности квантовой механики, упростившие им задачу. В качестве первого «подопытного» ученые избрали сульфоксид углерода – вещество, состоящее из атомов углерода, серы и кислорода, соединенных прочными ковалентными связями. Подготовив облако из подобных молекул, физики пропустили через него два очень коротких импульса инфракрасного лазера.Пауза между этими вспышками света была подобрана таким образом, что она была короче, чем тот промежуток времени, которое сульфоксид углерода тратит на совершение одного оборота вокруг своей оси. Благодаря этому, вращение всех молекул, через которые проходили обе вспышки света, синхронизировалось под действием принципов квантовой механики.Это позволило ученым получить набор из фактически одинаковых молекул, каждую из которых они обстреливали второй, более мощной вспышкой света, позволявшей им увидеть это вещество, но разрушавшей его при контакте.»Подсвечивая» каждую копию сульфоксида углерода в «пачке», физики смогли получить короткое видео из 650 кадров, на котором можно увидеть то, как эта молекула совершает полтора оборота вокруг своей оси.
В качестве первого «подопытного» ученые избрали сульфоксид углерода – вещество, состоящее из атомов углерода, серы и кислорода, соединенных прочными ковалентными связями. Подготовив облако из подобных молекул, физики пропустили через него два очень коротких импульса инфракрасного лазера.Пауза между этими вспышками света была подобрана таким образом, что она была короче, чем тот промежуток времени, которое сульфоксид углерода тратит на совершение одного оборота вокруг своей оси. Благодаря этому, вращение всех молекул, через которые проходили обе вспышки света, синхронизировалось под действием принципов квантовой механики.Это позволило ученым получить набор из фактически одинаковых молекул, каждую из которых они обстреливали второй, более мощной вспышкой света, позволявшей им увидеть это вещество, но разрушавшей его при контакте.»Подсвечивая» каждую копию сульфоксида углерода в «пачке», физики смогли получить короткое видео из 650 кадров, на котором можно увидеть то, как эта молекула совершает полтора оборота вокруг своей оси. На один такой оборот, как показали ученые, она тратит 82 пикосекунды, триллионных долей секунды.В целом, результаты этого эксперимента полностью совпали с результатами компьютерных расчетов. Это говорит о том, что физики достаточно хорошо понимают то, как устроены молекулы и какие законы мироздания управляют их вращением. В ближайшее время Кюппер и его команда планируют применить эту методику для изучения различных «закрученных» молекул, чья форма влияет на характер их взаимодействий с другими веществами. Яркий пример этого – аминокислоты и сахара в нашем теле, присутствующие в нем в исключительно «правой» и «левой» конфигурации.
На один такой оборот, как показали ученые, она тратит 82 пикосекунды, триллионных долей секунды.В целом, результаты этого эксперимента полностью совпали с результатами компьютерных расчетов. Это говорит о том, что физики достаточно хорошо понимают то, как устроены молекулы и какие законы мироздания управляют их вращением. В ближайшее время Кюппер и его команда планируют применить эту методику для изучения различных «закрученных» молекул, чья форма влияет на характер их взаимодействий с другими веществами. Яркий пример этого – аминокислоты и сахара в нашем теле, присутствующие в нем в исключительно «правой» и «левой» конфигурации.
https://ria.ru/20170513/1494214972.html
https://ria.ru/20120829/733143098.html
германия
РИА Новости
7 495 645-6601
ФГУП МИА «Россия сегодня»
https://xn--c1acbl2abdlkab1og.xn--p1ai/awards/
2019
РИА Новости
7 495 645-6601
ФГУП МИА «Россия сегодня»
https://xn--c1acbl2abdlkab1og.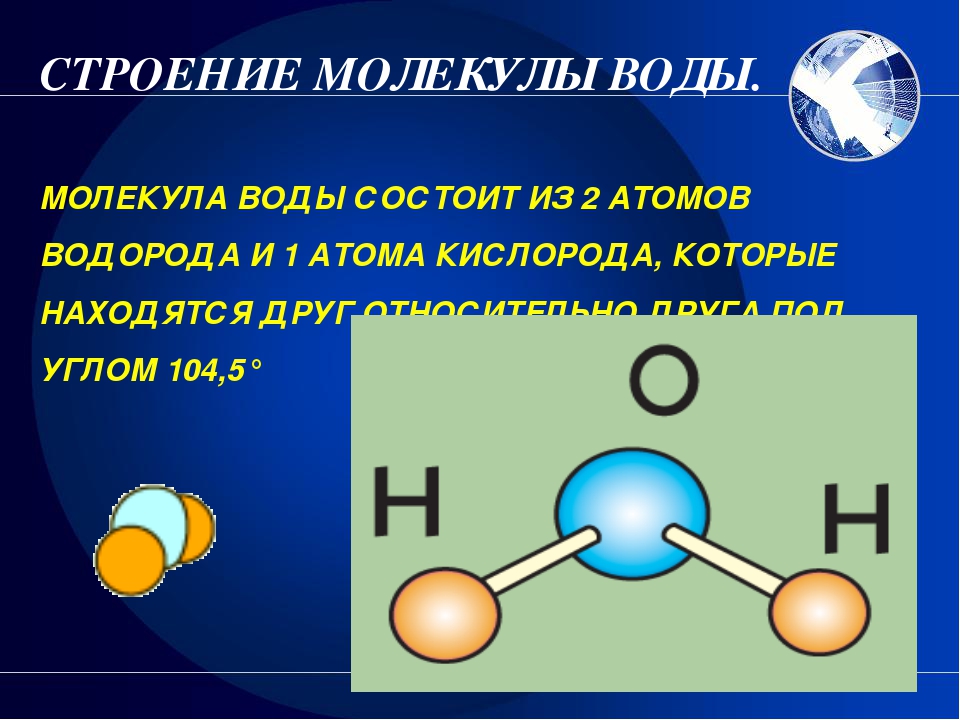 xn--p1ai/awards/
xn--p1ai/awards/
Новости
ru-RU
https://ria.ru/docs/about/copyright.html
https://xn--c1acbl2abdlkab1og.xn--p1ai/
РИА Новости
7 495 645-6601
ФГУП МИА «Россия сегодня»
https://xn--c1acbl2abdlkab1og.xn--p1ai/awards/
https://cdn24.img.ria.ru/images/155696/38/1556963841_0:0:2000:1500_1920x0_80_0_0_89d7860c34f0a565ca54a3bf38461fd9.jpgРИА Новости
7 495 645-6601
ФГУП МИА «Россия сегодня»
https://xn--c1acbl2abdlkab1og.xn--p1ai/awards/
РИА Новости
7 495 645-6601
ФГУП МИА «Россия сегодня»
https://xn--c1acbl2abdlkab1og.xn--p1ai/awards/
молекулы, атомы, физика, открытия — риа наука, германия
МОСКВА, 29 июл – РИА Новости. Датские и немецкие физики впервые сняли на видео то, как вращается одиночная молекула, состоящая из трех разных атомов, и сравнили эти наблюдения с предсказаниями теории. Их выводы были опубликованы в журнале Nature Communications.
Их выводы были опубликованы в журнале Nature Communications.«Физики давно мечтали, что мы сможем запечатлеть движение атомов в каких-то сверхбыстрых процессах. Сделать это сложно, так как молекулы вращаются совсем не так, как это делает набор из шариков и палочек. Их движением управляют законы квантовой механики — положение и импульс каждого атома нельзя точно измерить», — объясняет Йохен Кюппер (Jochen Kuepper) из Гамбургского университета (Германия).
В последние годы, благодаря постройке мощных рентгеновских лазеров, способных вырабатывать пучки света с огромной скоростью, ученые смогли заглянуть в самые далекие глубины мира молекул и элементарных частиц. К примеру, в начале этого десятилетия они получили первые «атомные» фотографии вирусов и белков.
В последующие годы физики смогли снять химическую реакцию на видео, сфотографировать электроны внутри алмаза, а также получить первые фотоснимки одиночной водородной связи, играющей ключевую роль в формировании белковых молекул, ДНК и других «молекул жизни».
Все эти достижения, как отмечает Кюппер, не позволяли ученым решить более простую задачу – увидеть то, как вращается молекула и меняет свою структуру в ходе взаимодействий с соседями или во время простых химических реакций. Этому мешало то, что рентгеновские лазеры разрушают изучаемую молекулу практически сразу после того, как импульс света пролетает через нее.
Немецкие физики нашли остроумное решение для этой проблемы, используя не одну, а несколько сотен молекул, два разных типа лазеров, а также определенные закономерности квантовой механики, упростившие им задачу.
В качестве первого «подопытного» ученые избрали сульфоксид углерода – вещество, состоящее из атомов углерода, серы и кислорода, соединенных прочными ковалентными связями. Подготовив облако из подобных молекул, физики пропустили через него два очень коротких импульса инфракрасного лазера.
Пауза между этими вспышками света была подобрана таким образом, что она была короче, чем тот промежуток времени, которое сульфоксид углерода тратит на совершение одного оборота вокруг своей оси. Благодаря этому, вращение всех молекул, через которые проходили обе вспышки света, синхронизировалось под действием принципов квантовой механики.
Благодаря этому, вращение всех молекул, через которые проходили обе вспышки света, синхронизировалось под действием принципов квантовой механики.
Это позволило ученым получить набор из фактически одинаковых молекул, каждую из которых они обстреливали второй, более мощной вспышкой света, позволявшей им увидеть это вещество, но разрушавшей его при контакте.
«Подсвечивая» каждую копию сульфоксида углерода в «пачке», физики смогли получить короткое видео из 650 кадров, на котором можно увидеть то, как эта молекула совершает полтора оборота вокруг своей оси. На один такой оборот, как показали ученые, она тратит 82 пикосекунды, триллионных долей секунды.
В целом, результаты этого эксперимента полностью совпали с результатами компьютерных расчетов. Это говорит о том, что физики достаточно хорошо понимают то, как устроены молекулы и какие законы мироздания управляют их вращением.
Это говорит о том, что физики достаточно хорошо понимают то, как устроены молекулы и какие законы мироздания управляют их вращением.
В ближайшее время Кюппер и его команда планируют применить эту методику для изучения различных «закрученных» молекул, чья форма влияет на характер их взаимодействий с другими веществами. Яркий пример этого – аминокислоты и сахара в нашем теле, присутствующие в нем в исключительно «правой» и «левой» конфигурации.
29 августа 2012, 21:02НаукаРентгеновский лазер помог физикам взглянуть на электроны внутри алмазаФизики использовали сверхмощный рентгеновский лазер LCLS для получения первых фотоснимков отдельных электронов, обращающихся вокруг атомов углерода в кристалле алмаза, и опубликовали результаты своей работы в статье в журнале Nature.Молекулы и звезды — ЗНАНИЕ-СИЛА
О чем мы сегодня будем говорить? Молекулы и звезды в названии этой лекции ─ объекты абсолютно разных масштабов. Они отличаются по размерам, по крайней мере, на два десятка порядков. Мы будем упоминать и другие объекты, еще на 10 порядков более крупные, чем звезды. Но, тем не менее, вы увидите, как они взаимосвязаны. Например, без молекул, невозможно образовать звезды. Без молекул не может быть звездного неба над нашей головой. С другой стороны, именно звезды ответственны за образование молекул.
Мы будем упоминать и другие объекты, еще на 10 порядков более крупные, чем звезды. Но, тем не менее, вы увидите, как они взаимосвязаны. Например, без молекул, невозможно образовать звезды. Без молекул не может быть звездного неба над нашей головой. С другой стороны, именно звезды ответственны за образование молекул.
Но сначала мы вами сделаем простое введение на тему «что такое молекулы?».
Кому-то кажется, особенно школьникам 8-9 классов, которые начали изучать химию, что они уже все знают про молекулы. На самом деле, даже само определение молекулы вызывает некоторые разночтения. Нырнем в кладезь знания (которое сила), т.е. в Википедию, и посмотрим там на определение молекулы. Молекула – уменьшительное от латинского moles(масса), ну и дальше идет определение, что это электрически нейтральная частица, образованная из двух или более связанных ковалентными связями атомов. Но вот оказывается, что в молекулярно-кинетической теории, которую преподают не только в школах, но и в ВУЗах, – под молекулами понимают также и просто отдельные атомы. Здесь, на слайде, вы видите определение. согласно которому, молекула состоит из двух или более атомов, но есть и такое определение, по которому даже всего лишь 1 атом – называется молекула («моноатомная молекула»). Каждый, кто помнит формулу 3/2 kТ… поднимите руку, хоть кто-нибудь слышит, помнит? Молодцы! Так вот эта формула относится к тепловой энергии моноатомной молекулы или атома. Это частица с тремя степенями свободы. А мы в дальнейшем все-таки будем придерживаться классического определения молекулы, как частицы, которая состоит, по крайней мере, из 2-х атомов (и имеет число степеней свободы побольше трех).
Здесь, на слайде, вы видите определение. согласно которому, молекула состоит из двух или более атомов, но есть и такое определение, по которому даже всего лишь 1 атом – называется молекула («моноатомная молекула»). Каждый, кто помнит формулу 3/2 kТ… поднимите руку, хоть кто-нибудь слышит, помнит? Молодцы! Так вот эта формула относится к тепловой энергии моноатомной молекулы или атома. Это частица с тремя степенями свободы. А мы в дальнейшем все-таки будем придерживаться классического определения молекулы, как частицы, которая состоит, по крайней мере, из 2-х атомов (и имеет число степеней свободы побольше трех).
Еще есть некоторые определения, которые я буду использовать, не пугайтесь. Молекулы могут быть ионизованы, т.е. если оторван электрон от нейтральной молекулы, то тогда получается молекулярный ион. Молекулы могут иметь несколько неспаренных электронов во внешней оболочке, например, всего один электрон, по аналогии с атомами щелочных металлов. И эта частица будет называться радикал.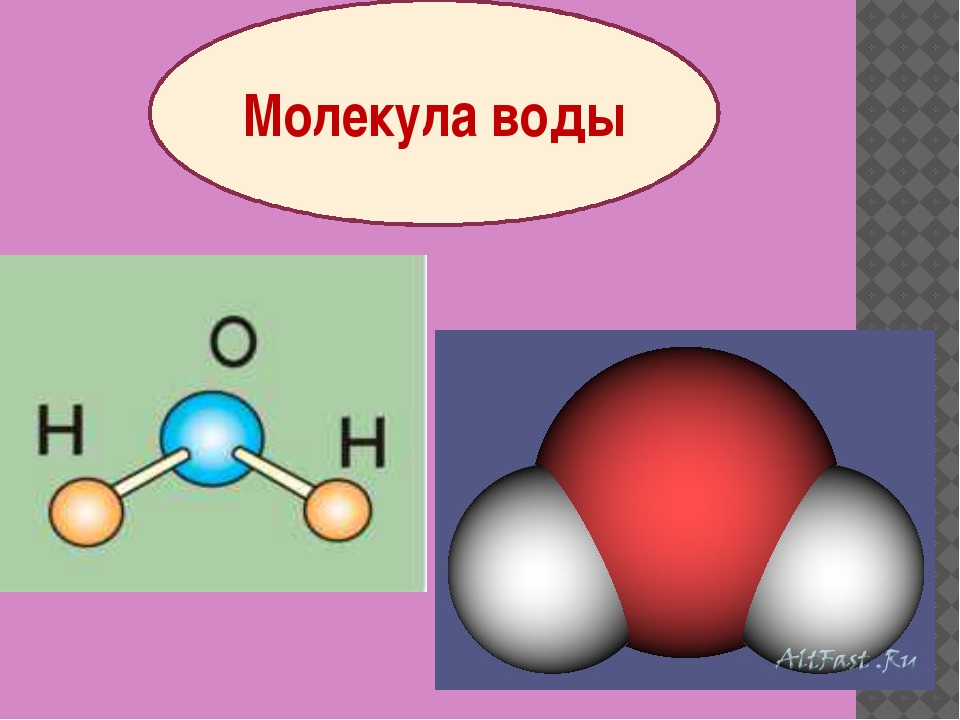 Радикал – это очень активное химическое вещество. Это может быть нейтральная частица или ион, Как правило, ионы являются радикалами – они очень химически активны (не обязательно, но чаще всего). Ну вот, пожалуй, потом мы будем далее эти понятия использовать. По крайней мере, вы об этом уже услышали. А дальше, если вопросы возникнут, то узнаем побольше.
Радикал – это очень активное химическое вещество. Это может быть нейтральная частица или ион, Как правило, ионы являются радикалами – они очень химически активны (не обязательно, но чаще всего). Ну вот, пожалуй, потом мы будем далее эти понятия использовать. По крайней мере, вы об этом уже услышали. А дальше, если вопросы возникнут, то узнаем побольше.
Оказывается, о том вещество имеет молекулярное строение, догадывались давно (конечно, и Ломоносова вы вспомните и других), но экспериментально это было доказано совсем недавно по исторической шкале. В 1906 году Жан Батист Перрен, который через 20 лет получил Нобелевскую премию, за работу «по дискретной природе материи», на основе анализа броуновского движения доказал, что вещество, в частности, жидкости, состоит из молекул. Кто не знает, что такое броуновское движение? Весь зал знает. Вот молодцы! Отлично подготовлен зал. Здесь на слайде показана марочка с Жаном Батистом. Как звучит! Сколько великих людей носило это имя ─ Жан Батист Мольер, Жан Батист Ламарк и т. д.
д.
Давайте, мы википедийное знание еще немножко освежим. Молекула – это не просто составная конструкция, состоящая из 2-х или нескольких атомов, а с точки зрения квантовой химии, она рассматривается как система, состоящая из отдельных атомных ядер и одной или нескольких общих электронных оболочек. То есть молекулы воедино объединяются электронными оболочками, и определяет свойство молекулы самая внешняя электронная оболочка. Здесь нарисована молекула, всем хорошо известная, Н2О в разных представлениях. Тут вот, например, в таком вот представлении. Вот атом О (кислород), тут атом водорода. Естественно, что настоящий размер молекулы очень мал – несколько ангстрем, а ангстрем — это 10 в минус 8-ой степени сантиметра. Вот такие характерные размеры простых молекул. Вы видите, что на рисунке молекула раскрашена, кислород тут красный, а водород какой-то такой бледноватый, но еще и внешняя оболочка тоже покрашена, причем неоднородно. Что это означает? А значит это, что ядро кислорода, более массивное, тяжелое, немножко оттягивает на себя электроны водорода и на этом (водородном) краю (полюсе) молекулы проявляется положительный заряд, а вот здесь, на другом краю (полюсе) – отрицательный.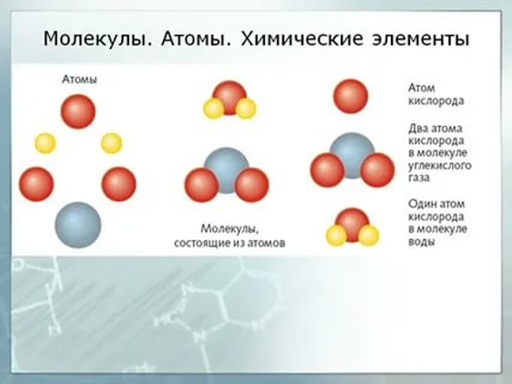 Молекула получается полярной. То полярная молекула — это конструкция, где заряды разнесены, на одном конце один заряд, на другом – другой. Полярность молекулы. важна с точки зрения возможностей ее наблюдений.
Молекула получается полярной. То полярная молекула — это конструкция, где заряды разнесены, на одном конце один заряд, на другом – другой. Полярность молекулы. важна с точки зрения возможностей ее наблюдений.
Вот в левом углу слайда показана самая главная молекула в космосе, мы много раз ее будем упоминать, – молекула водорода. Это симметричный объект. Вот объединились 2 атома водорода, у них появилась общая электронная оболочка. Абсолютно симметричная картинка. Никакой полярности нет. Неполярная молекула. Оказывается, это важное свойство, которое не позволяет наблюдать эту молекулу в самом «популярном» для наблюдений молекул радиодиапазоне.
А вот еще другой вид, точнее изображение, молекулы воды. Правая эта картинка – приближение квантово-механического представления о молекуле воды. Электрон в атоме водорода изображен в виде так называемой орбитали. Мы привыкли, старшее поколение особенно, (а младшее уже, наверно, нет), что атом изображается как некое ядро (например, протон для атома водорода), а вокруг него летает легкий электрон.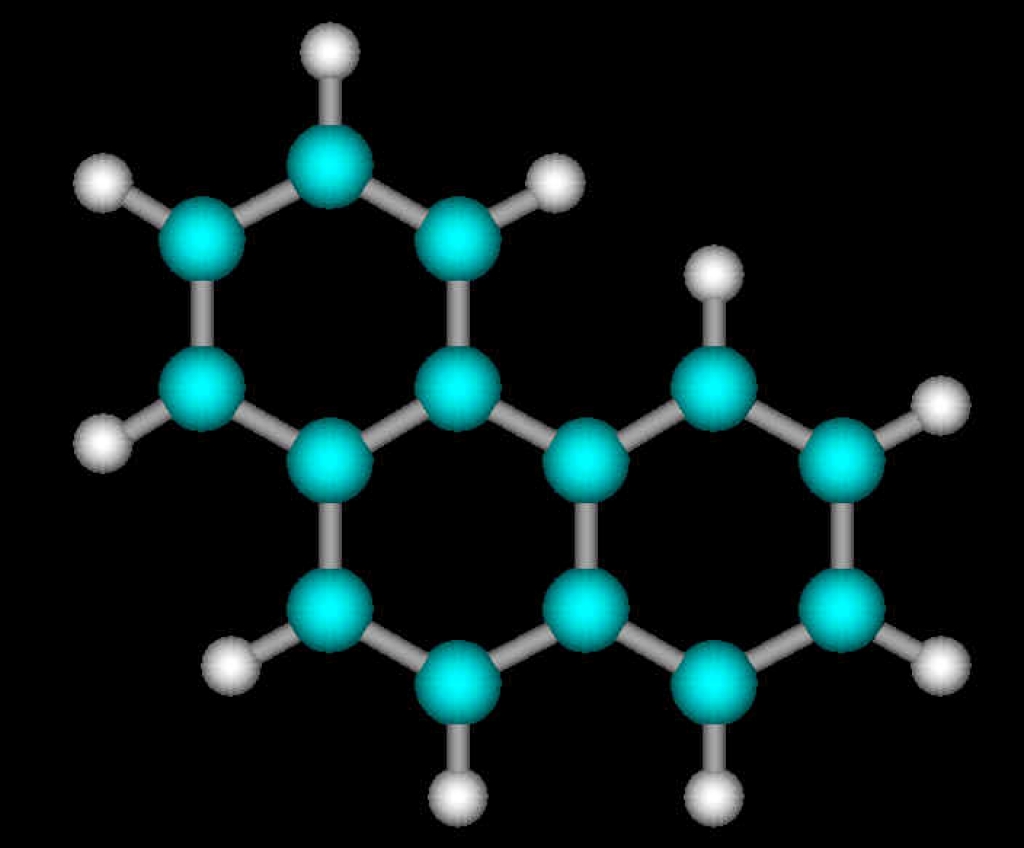 Такая вот картинка. Если взять более тяжелые атомы, то будет несколько протонов и нейтронов в ядре, и несколько электронов летает вокруг. Это — планетарная модель атома. На самом деле, конечно, такой простоты нет. Протоны и нейтроны действительно сидят в ядре, а электроны рассматриваются не как частицы, а как размытые оболочки – такие облачка вероятности что ли. Электрон может находиться с разной степенью вероятности здесь, и здесь, и здесь. И вот эти электронные оболочки – это не просто оболочки как шкурка апельсина, а некое представление о распределении их волновой функции, так называемые орбитали. Самые сложные вещи я уже рассказал. Теперь будет, наверное, чуть попроще.
Такая вот картинка. Если взять более тяжелые атомы, то будет несколько протонов и нейтронов в ядре, и несколько электронов летает вокруг. Это — планетарная модель атома. На самом деле, конечно, такой простоты нет. Протоны и нейтроны действительно сидят в ядре, а электроны рассматриваются не как частицы, а как размытые оболочки – такие облачка вероятности что ли. Электрон может находиться с разной степенью вероятности здесь, и здесь, и здесь. И вот эти электронные оболочки – это не просто оболочки как шкурка апельсина, а некое представление о распределении их волновой функции, так называемые орбитали. Самые сложные вещи я уже рассказал. Теперь будет, наверное, чуть попроще.
Один из моих учеников сейчас работает в Самарском Университете и занимается настоящей алхимией. Но алхимией не средневековой, как это было раньше, а современной. Здесь плохо немножко плоховато видно, но все же ссылку. Потом кто захочет посмотреть после лекции – увидит ссылку, и может по ней сам посмотреть, как все делается.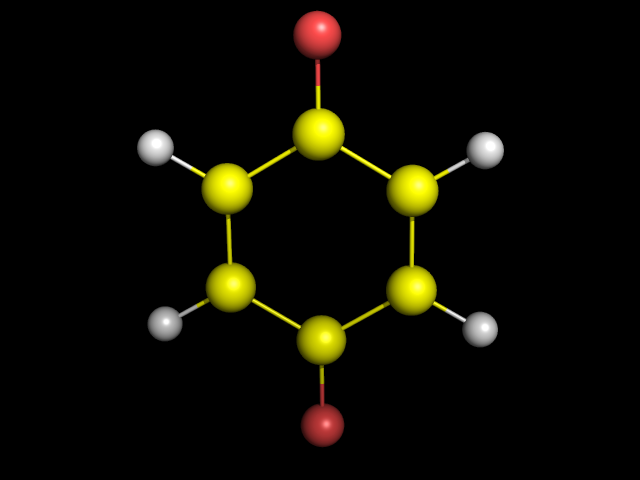 Чем занимается Артем Кабанов? Занимается тем, что использует теорию функционала плотности. Простыми словами, это теория, которая описывает, как распределены облака электронов. Это очень важно, потому что мы уже видели, что для молекулы самое главное – именно форма электронной оболочки, т.е. распределение электронных облаков. Именно она ответственна за все химические взаимодействия. За эти работы в 1998 г. была получена Нобелевская премия. Это, конечно, не Артем, Артему еще далеко до Нобелевской, но оказывается он математически уже многое может сделать. Можно взять модель молекулы, т.е. сконструировать модель из разных атомов, попробовать их соединить, убедиться – получается или не получается. Решение, т.е. общая электронная оболочка с минимальной энергией, необязательно получается. Если получается, то теоретически можно предсказать, какие будут свойства вещества. Если это твердое тело, то предсказать плотность, температуру плавления и т.д. То есть комбинируя различные атомы, соединяя их в молекулы, строя из них кристаллы, можно теоретически предсказать какие будут характеристики смоделированного вещества.
Чем занимается Артем Кабанов? Занимается тем, что использует теорию функционала плотности. Простыми словами, это теория, которая описывает, как распределены облака электронов. Это очень важно, потому что мы уже видели, что для молекулы самое главное – именно форма электронной оболочки, т.е. распределение электронных облаков. Именно она ответственна за все химические взаимодействия. За эти работы в 1998 г. была получена Нобелевская премия. Это, конечно, не Артем, Артему еще далеко до Нобелевской, но оказывается он математически уже многое может сделать. Можно взять модель молекулы, т.е. сконструировать модель из разных атомов, попробовать их соединить, убедиться – получается или не получается. Решение, т.е. общая электронная оболочка с минимальной энергией, необязательно получается. Если получается, то теоретически можно предсказать, какие будут свойства вещества. Если это твердое тело, то предсказать плотность, температуру плавления и т.д. То есть комбинируя различные атомы, соединяя их в молекулы, строя из них кристаллы, можно теоретически предсказать какие будут характеристики смоделированного вещества. И наоборот –задавая требуемые свойства – подбирать под эти требования атомы, конструировать молекулы и т.д.. Другое дело – технология, как потом выстроить эти атомы. Нахождение этих комбинаций – и есть современная алхимия.
И наоборот –задавая требуемые свойства – подбирать под эти требования атомы, конструировать молекулы и т.д.. Другое дело – технология, как потом выстроить эти атомы. Нахождение этих комбинаций – и есть современная алхимия.
А как все-таки люди узнают строение молекулы? Самое мощное средство сейчас – это рентгеновские дифракционные спектрографы, вот тут по-английски написано Экс-рэй дифракшен. Это значит, что если облучать молекулы рентгеновским излучением, то они работают как решетки дифракционные, и по картине спектра можно сказать, как устроена молекула. А можно облучать не рентгеновскими квантами, а электронами. Та же самая, но еще более детальная картина получается. Если, скажем, вы берете молекулу, про которую вы не знаете, как она устроены, облучили и ее узнали ее строение, то дальше с помощью теории функционала плотности можно определить ее свойства. Даже не задумываясь о том, что нужно смешивать что-то в пробирках, или что-нибудь нагревать, крылом летучей мыши размахивать (как там алхимиков всегда рисуют). Ну я просто для образа.
Ну я просто для образа.
Тут сидит несколько людей, которые профессионально занимаются астрофизикой молекул и даже, конкретнее – так называемыми, полициклическими ароматическими углеводородами (ПАУ). Это очень популярные частицы, очень важный вид, молекулярных соединений в химии. Сейчас пару слов об этом скажем. Вот по этой базе данных, можно найти заранее построенные модели инфракрасных спектров полициклических ароматических углеводородов. Потом когда из спектров, которые мы наблюдаем, от разных, наземных и космических источников мы пытаемся понять что мы наблюдаем, эта база данных может помочь. Если наблюдаемые и модельные спектры совпадают, мы говорим, что, мы знаем, что это за частица, имеющая такой спектр. Итак, вот они эти самые ПАУ — полициклические, ароматические углеводороды.
Здесь на этой схемке нарисовано несколько молекул. Некоторые из них вам известны, названия, по крайней мере. Некоторые не совсем, но я вот пару слов сначала скажу про эту.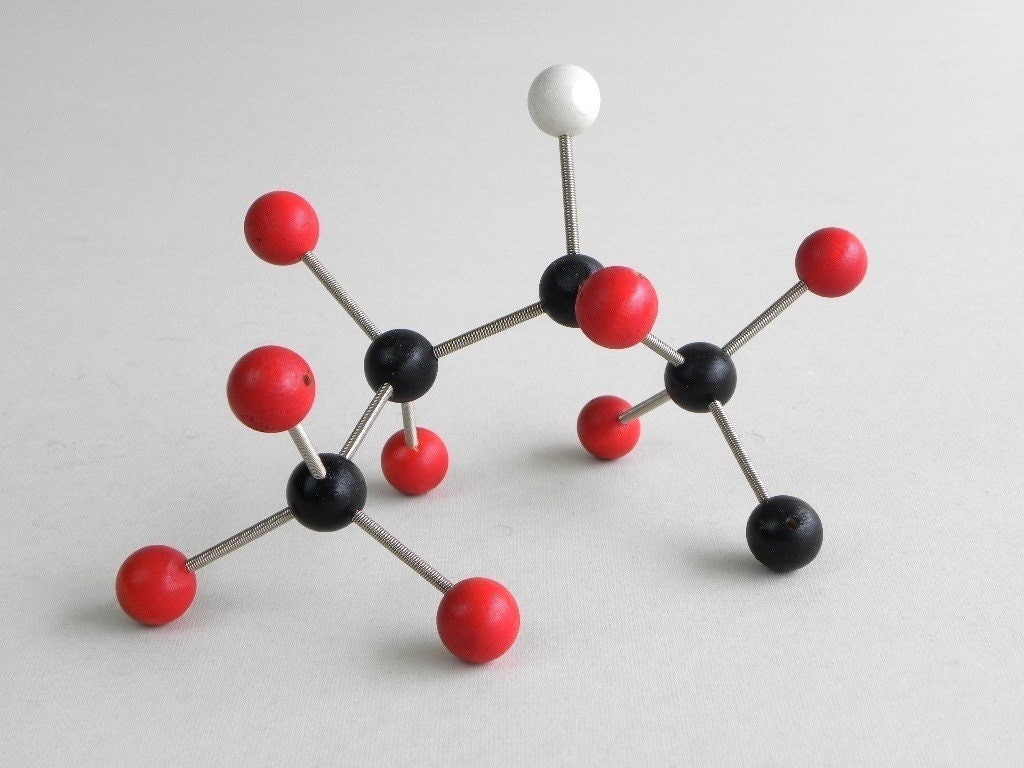 Здесь по-английски написано Пи Эй Эйч, это ПАУ. Вот такая решеточка из бензольных колец, они называются ароматические потому, что (мы еще потом вернемся) первые исследованные ПАУ были довольно пахучие вещества, например, нафталин. Сейчас почти все органические вещества делят на ароматические (хотя не все из них пахнут) и на алифатические, так называемые, жирные вещества, но это тоже необязательно, что они действительно жирные. Так уж получилось.
Здесь по-английски написано Пи Эй Эйч, это ПАУ. Вот такая решеточка из бензольных колец, они называются ароматические потому, что (мы еще потом вернемся) первые исследованные ПАУ были довольно пахучие вещества, например, нафталин. Сейчас почти все органические вещества делят на ароматические (хотя не все из них пахнут) и на алифатические, так называемые, жирные вещества, но это тоже необязательно, что они действительно жирные. Так уж получилось.
И вот какие молекулы вы здесь видите замечательные. Я сам не выговорю сразу. Вы прочитайте. (Знаете, когда в химический справочник заглянешь, то все сломаешь, язык, глаза, и веру в себя.)
Вот этанол. А кто знает, что такое этанол? По-русски говоря… Это настоящий питьевой этиловый, спирт. Ну и дальше тоже вот эти молекулы, видите, имеют трехмерную сложной структуры, это так называемые нелинейные молекулы. Вы видите, их оболочки окрашены. Это что у нас значит? Это — полярные молекулы. Заряды разнесены, это важно, потому, что если молекула полярная, то при ее вращении – излучаются или поглощаются электромагнитные волны.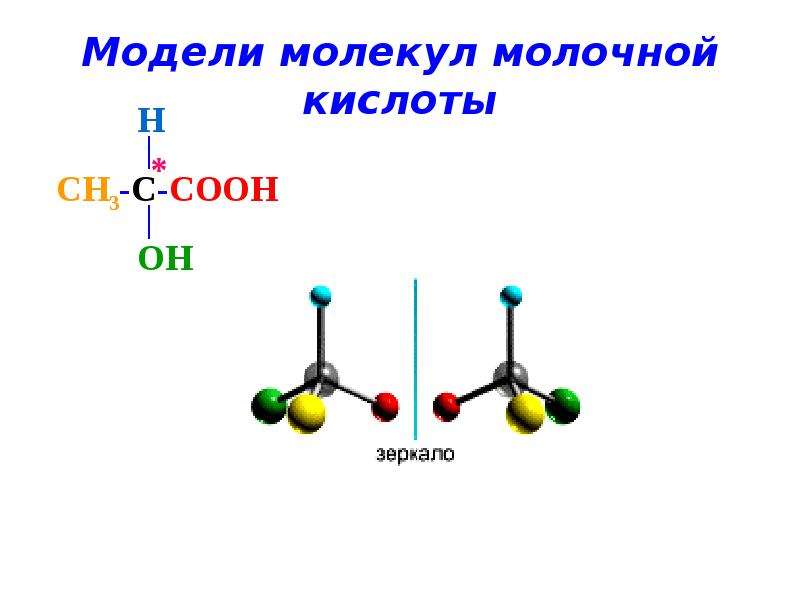 Это очень важно с точки зрения наблюдений.
Это очень важно с точки зрения наблюдений.
Это синильная кислота. Линейная полярная молекула. Тоже всем понятно.
Вернемся еще раз к этим самым ПАУ. Когда вы видите дым, который выходит из выхлопной трубы вашего двигателя или из сигареты (я надеюсь, молодежь не курит, правда?), так вот, это те же самые ПАУ. Немножко странное вещество, поскольку в нем соединяется жизнь и смерть (тот самый дуализм). Как вы знаете, этот дым, эти частицы, с одной стороны – канцерогены. То есть приводят к смерти. А с другой – биохимики считают, что на основании именно бензольных колец начали строиться наши молекулы жизни. РНК прежде всего. Ну и как подвид – ДНК. Да, те самые. Поэтому, все в мире связано, и великий, Энгельс был прав, ну и философы, которые до него были.
Мы все говорим про наземные молекулы, хотя часть из них, конечно, есть и в космосе. А теперь все-таки, про молекулы в космосе. Это ведь тема лекции. Мы сами состоим из молекул. Есть, конечно, кристаллы, состоящие из атомов, скажем, металлов и т.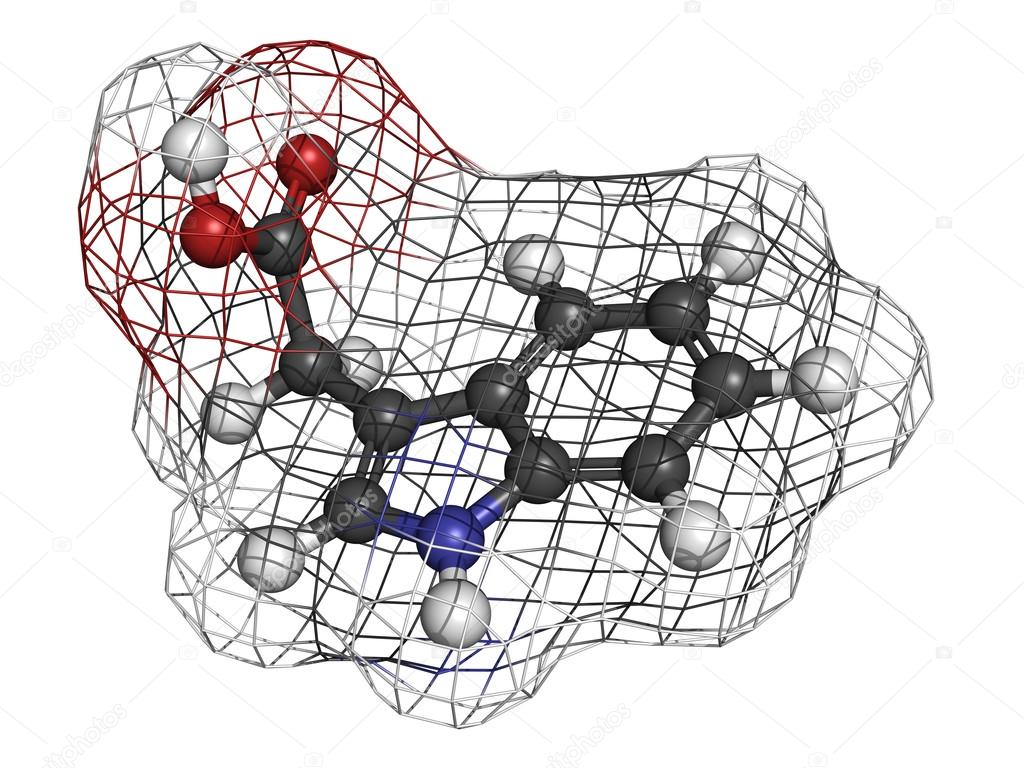 д., но все, что окружает нас вот здесь, например, в этой аудитории – молекулы, макросоединения молекул и пр., их здесь гораздо больше, чем атомарных веществ. А вот, что касается космоса, то еще сравнительно недавно, до 30-х годов прошлого века считалось, что молекул там нет. Считалось, в частности, что молекулы, будь они помещены в межзвездное, межпланетное пространство под жесткое излучение звезд будут просто разваливаться. Прилетит энергичный квант от звезды и развалит молекулу. Но, тем не менее, молекулы в космосе были обнаружены. В оптическом диапазоне удалось обнаружить несколько видов молекул (затем 20 лет других молекул не было найдено). Это обнаружение было выполнено по оптическим линиям поглощения в спектрах звезд. Повезло, что некоторые линии молекул лежат в оптическом диапазоне. Но их мало. Вот все они и были обнаружены в тридцатых годах. Наш замечательный астрофизик Иосиф Самойлович Шкловский предсказал еще в 52-ом году, что в космосе, несмотря на вот эти опасения, должно быть очень много разных молекул.
д., но все, что окружает нас вот здесь, например, в этой аудитории – молекулы, макросоединения молекул и пр., их здесь гораздо больше, чем атомарных веществ. А вот, что касается космоса, то еще сравнительно недавно, до 30-х годов прошлого века считалось, что молекул там нет. Считалось, в частности, что молекулы, будь они помещены в межзвездное, межпланетное пространство под жесткое излучение звезд будут просто разваливаться. Прилетит энергичный квант от звезды и развалит молекулу. Но, тем не менее, молекулы в космосе были обнаружены. В оптическом диапазоне удалось обнаружить несколько видов молекул (затем 20 лет других молекул не было найдено). Это обнаружение было выполнено по оптическим линиям поглощения в спектрах звезд. Повезло, что некоторые линии молекул лежат в оптическом диапазоне. Но их мало. Вот все они и были обнаружены в тридцатых годах. Наш замечательный астрофизик Иосиф Самойлович Шкловский предсказал еще в 52-ом году, что в космосе, несмотря на вот эти опасения, должно быть очень много разных молекул. И действительно, как только появились мощные радиотелескопы (ну, первые радиотелескопы с нашей точки зрения были не мощные, но тогда это все равно был прорыв), т.е. инструменты, с помощью которых можно было принимать радиоизлучения из космоса, вскоре были обнаружены молекулы. Их много. Сейчас известно около 200 молекул в космосе. Это основных видов. И плюс еще (мы еще коснемся этого общеобразовательного момента) еще несколько сотен (может быть до 400) изомеров. Потом поясню, что это такое. Так что молекул в космосе много разных.
И действительно, как только появились мощные радиотелескопы (ну, первые радиотелескопы с нашей точки зрения были не мощные, но тогда это все равно был прорыв), т.е. инструменты, с помощью которых можно было принимать радиоизлучения из космоса, вскоре были обнаружены молекулы. Их много. Сейчас известно около 200 молекул в космосе. Это основных видов. И плюс еще (мы еще коснемся этого общеобразовательного момента) еще несколько сотен (может быть до 400) изомеров. Потом поясню, что это такое. Так что молекул в космосе много разных.
Вот список молекул, обнаруженных в космосе по состоянию на начало года. Видите, от 2-х-атомных до 13-атомных. Красным выделены ну наиболее, наверное, известные, важные, интересные. Вот это самая главная молекула, самая распространенная молекула в космосе Н2 – молекулярный водород, вода H2O, очень интересный для любого химика ион Н3 плюс, особенно для астрохимика, (через него идет множество реакций в космосе). Вот аммиак, метан. Вот, кстати, кто интересовался какой спирт не надо пить – это вот этот. А вот этот можно. А вот это уксусная кислота – тоже не надо пить. А эта молекула возможно элемент белка. Это очень интересно, они (такие соединения) пока под вопросом. Их то открывают, то закрывают, но когда в космосе нашли элементы белков, то это стало мощнейшим или станет, когда будет полностью установлено, мощнейшим подтверждением того, что даже белковая жизнь, точнее ее истоки, могут находиться именно там в космосе. За пределами нашей Галактики найдено 60 видов молекул, а в нашей, как уже говорилось, около 200.
Вот аммиак, метан. Вот, кстати, кто интересовался какой спирт не надо пить – это вот этот. А вот этот можно. А вот это уксусная кислота – тоже не надо пить. А эта молекула возможно элемент белка. Это очень интересно, они (такие соединения) пока под вопросом. Их то открывают, то закрывают, но когда в космосе нашли элементы белков, то это стало мощнейшим или станет, когда будет полностью установлено, мощнейшим подтверждением того, что даже белковая жизнь, точнее ее истоки, могут находиться именно там в космосе. За пределами нашей Галактики найдено 60 видов молекул, а в нашей, как уже говорилось, около 200.
Спектры молекул. Это главный источник информации о молекулах и о тех областях, где они обнаружены. Как, например, мы знаем, что в данном месте есть такие-то молекулы? Каждая молекула, как и каждый атом, имеет свой спектр. Спектр поглощения или спектр излучения, это неважно. Атомы и молекулы в газе, излучают или поглощают не непрерывно. А в линиях. Все из вас слышали, что такое спектр Фраунгофера, и видели эти полосатые спектры. Отличие от твердого вещества состоит в том, что в твердом веществе гораздо больше (я говорю физическим языком) степеней свободы для частиц, и твердые вещества излучают или поглощают в непрерывном спектре. Вот, например, слева, на этой картинке спектра – вот так поглощает молекула СО2 в газе, видите сколько полос, сколько разных линий, очень сложный спектр. Молекулярные спектры несравненно сложнее атомных. Просто больше степеней свободы и больше возможностей, как говорится, запутаться. А вот это просто твердый лед, замерзшая двуокись углерода, он дает без всяких деталей просто одну линию, очень широкую но одну. Итак, твердые вещества, как правило, дают спектр непрерывный, а газы, молекулы, атомы –линейчатые спектры. Именно эти линии и позволяют узнать точно, какой это элемент, какая молекула, какой газ мы наблюдаем. Справа – типичный пример спектральных проявлений молекул в спектре планетарной туманности. Кто не знает, что такое планетарная туманность хотя бы в принципе? Знаете – молодцы! Значит, вы все знаете, что последняя стадия эволюции звезд сопровождается сбросом оболочки, эта оболочка в течение нескольких тысяч лет ионизуется излучением звезды и светится, как вот на этой картинке справа внизу.
Отличие от твердого вещества состоит в том, что в твердом веществе гораздо больше (я говорю физическим языком) степеней свободы для частиц, и твердые вещества излучают или поглощают в непрерывном спектре. Вот, например, слева, на этой картинке спектра – вот так поглощает молекула СО2 в газе, видите сколько полос, сколько разных линий, очень сложный спектр. Молекулярные спектры несравненно сложнее атомных. Просто больше степеней свободы и больше возможностей, как говорится, запутаться. А вот это просто твердый лед, замерзшая двуокись углерода, он дает без всяких деталей просто одну линию, очень широкую но одну. Итак, твердые вещества, как правило, дают спектр непрерывный, а газы, молекулы, атомы –линейчатые спектры. Именно эти линии и позволяют узнать точно, какой это элемент, какая молекула, какой газ мы наблюдаем. Справа – типичный пример спектральных проявлений молекул в спектре планетарной туманности. Кто не знает, что такое планетарная туманность хотя бы в принципе? Знаете – молодцы! Значит, вы все знаете, что последняя стадия эволюции звезд сопровождается сбросом оболочки, эта оболочка в течение нескольких тысяч лет ионизуется излучением звезды и светится, как вот на этой картинке справа внизу. Уильям Гершель называл такой объект планетарной туманностью просто по аналогии с планетами (он тогда не знал основ физики и эволюции звезд). Так вот спектр показывает, что даже в планетарной туманности, где все-таки температура высокая, 10 в 4-ой кельвинов, даже там выживают молекулы. Вот эти молекулы вверху справа на врезках, а это спектр молекул или молекулярных комплексов, которые называются фуллеренами. Это еще одно слово, которое вы часто, может быть, слышали, но не все знают, что это такое. Теперь я рассказываю чуть подробнее.
Уильям Гершель называл такой объект планетарной туманностью просто по аналогии с планетами (он тогда не знал основ физики и эволюции звезд). Так вот спектр показывает, что даже в планетарной туманности, где все-таки температура высокая, 10 в 4-ой кельвинов, даже там выживают молекулы. Вот эти молекулы вверху справа на врезках, а это спектр молекул или молекулярных комплексов, которые называются фуллеренами. Это еще одно слово, которое вы часто, может быть, слышали, но не все знают, что это такое. Теперь я рассказываю чуть подробнее.
Фуллерены – это макромолекулы, их еще по-английски называют бакиболз (buckyballs) – это такие шарики красивые, математически хорошо описываемые, вот они слева. Пустые углеродные шарики ажурной конструкции, которые назвали фуллеренами по имени архитектора, философа, и также геодезиста Ричарда Бакминстера Фуллера. Их иногда еще называют бакиболз. В 1967-м году был ЭКСПО – всемирная выставка, в Монреале. Там по проекту Фуллера была построена, так называемая биосфера. Разрешение на экране не очень хорошее, но видно, что это шар был построен из регулярных элементов. Биосфера напоминает структуру фуллеренов, выявленную методами, которые я описывал ранее. Частиц (атомов) углерода в сфере этой может быть 60, а может быть и 70, может быть и больше, до 400 известно. Вот такие интересные молекулы с конструкцией как перекати-поле, чрезвычайно оказались интересными и важными для наземных технологий. В технологиях, а здесь перечислены далеко не все, фуллерены, как здесь написано, широко используются. И для полупроводниковой техники и т.д. За фуллерены тоже была получена Нобелевская премия.
Разрешение на экране не очень хорошее, но видно, что это шар был построен из регулярных элементов. Биосфера напоминает структуру фуллеренов, выявленную методами, которые я описывал ранее. Частиц (атомов) углерода в сфере этой может быть 60, а может быть и 70, может быть и больше, до 400 известно. Вот такие интересные молекулы с конструкцией как перекати-поле, чрезвычайно оказались интересными и важными для наземных технологий. В технологиях, а здесь перечислены далеко не все, фуллерены, как здесь написано, широко используются. И для полупроводниковой техники и т.д. За фуллерены тоже была получена Нобелевская премия.
Я здесь показываю свежий результат обнаружения фуллеренов как раз по тем базам данных, о которых мы говорили. Сравнили лабораторные спектры, какие должны быть теоретически, со спектрами, которые получили в наблюдениях, и сделали вывод – это фуллерены. Вот так было сделано в 2015-ом году, это свежая работа.
Дальше идем. Еще интересные факты. В окрестностях молодой звезды с помощью радиотелескопа АЛМА (я покажу его на следующей картинке) или АЛьМА, так иногда произносят, были обнаружены молекулы гликолевого альдегида. Это сахар, один из видов сахаров. А сахара – это довольно такой серьезный, глубокий признак ну не жизни, но, по крайней мере, тех процессов, которые приводят к образованию живого. Это уже высокоорганизованное органическое вещество. Вот на слайде знаменитая для астрономов область – молекулярное облако ρ Змееносца. Показано, где эти фуллерены были найдены.
Это сахар, один из видов сахаров. А сахара – это довольно такой серьезный, глубокий признак ну не жизни, но, по крайней мере, тех процессов, которые приводят к образованию живого. Это уже высокоорганизованное органическое вещество. Вот на слайде знаменитая для астрономов область – молекулярное облако ρ Змееносца. Показано, где эти фуллерены были найдены.
АЛМА – это самый крупный радиотелескоп. Состоит из 66 вот таких тарелок, антенн, радиотелескопов единичных, но они все соединены в сеть, и это позволяет работать с ними как с единым телескопом. Причем они могут ездить, раздвигаться и работают как один огромный телескоп, а может и каждый единично работать. Это великий инструмент, запущенный в строй сравнительно недавно. Создан усилиями очень большого консорциума европейских стран. Он находится на высоте 5 километров в Южной Америке в сухом-сухом месте, которое называется плато Чайнантор. Качество проектора неважное, и я совершенно не могу профессионально интересующимся людям показать те полосы пропускания в рабочем диапазоне АЛМА от 50 до 900 гигагерц, которые позволяет атмосфера на этом плато. Давайте прикинем, частота 30 гигагерц – это длина волны 1 сантиметр. Значит, 50 гигагерц будет, соответственно, 3/5 сантиметра. А 900 гигагерц это примерно в 20 раз больше. То есть мы имеем субсантиметровый и субмиллиметровый диапазон. В этом диапазоне излучают молекулы, и в этом диапазоне излучает пыль. АЛМА – телескоп, который позволяет увидеть излучение самых запыленных, холодных и самых насыщенных молекулами областей во Вселенной.
Давайте прикинем, частота 30 гигагерц – это длина волны 1 сантиметр. Значит, 50 гигагерц будет, соответственно, 3/5 сантиметра. А 900 гигагерц это примерно в 20 раз больше. То есть мы имеем субсантиметровый и субмиллиметровый диапазон. В этом диапазоне излучают молекулы, и в этом диапазоне излучает пыль. АЛМА – телескоп, который позволяет увидеть излучение самых запыленных, холодных и самых насыщенных молекулами областей во Вселенной.
Дальше. Есть странные молекулы, которые обнаружили только в космосе Они теоретически известны, но все же на Земле их нет, потому что они слишком активны. На земле такая молекула как CH+ не проживет и микросекунды, она мгновенно прореагирует. Это сверхактивный радикал. Нигде на Земле они не могут выжить.
Или, например, совершенно странная с точки зрения тех, кто слушал курсы химии, молекула – аргониум. Аргон как известно, газ благородный, который вообще в химические реакции не вступает, а вот тут нашли соединения аргона, который соединился с водородом. Вот он — ион аргония ArH+. Спрашивается, как это может быть. Ну посчитали, подумали, как может образоваться такое соединение. Оказывается, что при очень серьезной бомбардировке космическими лучами, то есть быстро летящими частицами, которые возникают, например, при взрывах сверхновых, аргон может превратиться в ион и есть условия, когда он захватывает атом водорода. Сейчас считается, что, если наблюдается аргониум, то значит там очень много (высокая плотность) космических лучей.
Вот он — ион аргония ArH+. Спрашивается, как это может быть. Ну посчитали, подумали, как может образоваться такое соединение. Оказывается, что при очень серьезной бомбардировке космическими лучами, то есть быстро летящими частицами, которые возникают, например, при взрывах сверхновых, аргон может превратиться в ион и есть условия, когда он захватывает атом водорода. Сейчас считается, что, если наблюдается аргониум, то значит там очень много (высокая плотность) космических лучей.
Я произносил слово «изомеры». Это понятие простое, но крайне важное, интересное и по поводу изомеров нужно сделать важные замечания. Вот вы взяли набор атомов, и составили из них молекулу, а могли из тех же атомов составить другую молекулу. Просто в другом порядке. Здесь так и нарисовано. И это разные вещества. Вот видите, здесь даже написаны разные названия. Не пьется, сразу скажу. Казалось бы, изменения незначительны, ан нет. Вот видите, переехал один атом водорода сюда, показан звездочкой, и это уже другое вещество. В молекулах, еще раз повторю, это очень важно, это основа химии, понять, что все определяется свойствами электронной оболочки. Если вы изменили структуру внешней электронной оболочки – будут другие химические свойства. Другой запах, другой вкус, другой цвет, другие реакции и все. Этим все определяется. Хотя составляющие атомы те же самые. Изомеры поэтому важны. В промышленности много используется изомеров самых разнообразных.
В молекулах, еще раз повторю, это очень важно, это основа химии, понять, что все определяется свойствами электронной оболочки. Если вы изменили структуру внешней электронной оболочки – будут другие химические свойства. Другой запах, другой вкус, другой цвет, другие реакции и все. Этим все определяется. Хотя составляющие атомы те же самые. Изомеры поэтому важны. В промышленности много используется изомеров самых разнообразных.
Но вот на нижнем рисунке представлен еще один довольно интересный вид изомерии. Здесь даже порядок расположения атомов тот же самый, но, правда, в зеркальном отражении. Здесь недаром нарисованы две руки. Молекулы, которые являются копией друг друга в зеркальном отражении – называются хиральными. Слово это происходит от греческого слова хейр, это не прическа, это рука. Отсюда слово, которым называют некоторых из тех, кто пытается обдурить население. Как называются люди? Хироманты это от руки, конечно, гадальщики по рукам. Теперь, я все-таки этот тест всегда проведу, потому что мне интересно, как развивается культура молодежи. Кто читал «Понедельник начинается в субботу»? Ой, какие молодцы. Бальзам до сердца. Как вы помните, там упоминался некий спор между гекатонхейрами. Мы сразу догадываемся, что гекто это 100, значит это сторукие великаны. Так вот эти молекулы, казалось бы, совпадают, это одна и та же молекула, электронная оболочка выглядит также, но нет. Совместить их положение в пространстве невозможно никакими поворотами (как правую и левую руку). Если вы рассмотрите те молекулы, что составляют органику, особенно живую органику, т.е. молекулы из которых состоим и мы, то оказывается, что почти все молекулы живого, по крайней мере, на Земле, являются, так называемыми левыми, левовращающим. По-английски их называют леворукими. А праворуких нет, хотя, казалось бы, из простой статистики, когда атомы соединяются в молекулы – и такие и такие должны получаться, но оказывается, нет. Живые системы, как самоорганизующиеся, отбирают и создают только то, что им подходит. Здесь проявляется естественный отбор.
Кто читал «Понедельник начинается в субботу»? Ой, какие молодцы. Бальзам до сердца. Как вы помните, там упоминался некий спор между гекатонхейрами. Мы сразу догадываемся, что гекто это 100, значит это сторукие великаны. Так вот эти молекулы, казалось бы, совпадают, это одна и та же молекула, электронная оболочка выглядит также, но нет. Совместить их положение в пространстве невозможно никакими поворотами (как правую и левую руку). Если вы рассмотрите те молекулы, что составляют органику, особенно живую органику, т.е. молекулы из которых состоим и мы, то оказывается, что почти все молекулы живого, по крайней мере, на Земле, являются, так называемыми левыми, левовращающим. По-английски их называют леворукими. А праворуких нет, хотя, казалось бы, из простой статистики, когда атомы соединяются в молекулы – и такие и такие должны получаться, но оказывается, нет. Живые системы, как самоорганизующиеся, отбирают и создают только то, что им подходит. Здесь проявляется естественный отбор. Вот поэтому левовращающая молекула в основном доминирует, хотя кажется, что так не должно быть, поскольку по формальной статистике, из набора атомов в случайном процессе должны формироваться молекулы разной хиральности. Хиральность ˗_ это существенно. Если вы, например, принимаете лекарства, то лекарство из левовращающих молекул на вас действует, а из правовращающих таких же молекул – действовать не будет. Эти молекулы пахнут, а такие же, но другой хиральности – нет. Потому что все ваши рецепторы, состоящие из молекул, настроены на левоориентированные молекулы.. Вот такая штука странная – хиральность и обусловленная ею избирательность.
Вот поэтому левовращающая молекула в основном доминирует, хотя кажется, что так не должно быть, поскольку по формальной статистике, из набора атомов в случайном процессе должны формироваться молекулы разной хиральности. Хиральность ˗_ это существенно. Если вы, например, принимаете лекарства, то лекарство из левовращающих молекул на вас действует, а из правовращающих таких же молекул – действовать не будет. Эти молекулы пахнут, а такие же, но другой хиральности – нет. Потому что все ваши рецепторы, состоящие из молекул, настроены на левоориентированные молекулы.. Вот такая штука странная – хиральность и обусловленная ею избирательность.
Наблюдения в космосе доказывают, что в космосе, где живых существ нет, этой системы отбора, этой машины самоорганизующей – наблюдаются и такие и такие молекулы. Вот эта работа совсем свежая — 2016 года. С помощью Грин Бэнк Телескопа – вот его фотография (это тоже радиотелескоп) молекулы пропиленоксида были обнаружена в хиральных вариантах. Кстати , этот, обзорный проект называется «Обзор межзвездных пребиотических молекул». Так что вы видите, как далеко мы заходим.
Кстати , этот, обзорный проект называется «Обзор межзвездных пребиотических молекул». Так что вы видите, как далеко мы заходим.
Молекулы и первые звезды
А теперь мы чуть-чуть ближе начинаем к звездам подходить. Я думаю тоже здесь очень подготовленная аудитория, молодцы.
Вы, наверно, знаете каков современный итог инвентаризации Вселенной. Он дает примерно такой результат. Масса барионов где-то 4%. А так называемого темного вещества в разы больше. Мне не нравится словосочетание «темная материя» – это прямой перевод с английского darkmatterили с немецкого dunkleMaterie, поскольку Фриц Цвикки написал исходную работу по-немецки. Материя, как мы считаем – это вещество плюс поля излучений и так далее. Поэтому лучше говорить, конечно, про вещество, и правильнее переводить – темное вещество. Что это такое – непонятно, но оно но доминирует в общей массе вещества во Вселенной. То есть вы видите, что масса темного вещества в 5-6 раз больше, чем масса барионов. А барионы – это то самое обычное вещество, из которого мы с вами состоим и вообще все понятное нам. А вот что это такое темное вещество? (Я читал лекцию в Планетарии несколько лет назад, она называлась «Скрытая масса – великая загадка космоса», если кто захочет, она в youtube выложена, посмотрите. Там довольно интересно, мне кажется, и что можно что-то почерпнуть).
А барионы – это то самое обычное вещество, из которого мы с вами состоим и вообще все понятное нам. А вот что это такое темное вещество? (Я читал лекцию в Планетарии несколько лет назад, она называлась «Скрытая масса – великая загадка космоса», если кто захочет, она в youtube выложена, посмотрите. Там довольно интересно, мне кажется, и что можно что-то почерпнуть).
Итак, а нашей Вселенной доминирует темное вещество. Считается, его в 5-6 раз больше чем обычного вещества. А теперь немножко про историю нашей Вселенной. Большой взрыв мы опускаем, я сам не понимаю до конца всей физики этого процесса и его математики. Это довольно сложная для представления на уровне пальцев уровня материя. Итак, в первые несколько секунд после Большого взрыва во Вселенной появились атомы – водород, гелий и крайне малое количество дейтерия и лития. Крайне малое. То есть можно сказать, что газ был водородно-гелиевый. Газ были раскален, Вселенная расширялась. Расширяющийся газ охлаждается, и как только температура упала где-то до нескольких тысяч градусов, то ионы, в данном случае протоны (ион водорода – это протон) и электроны стали соединяться в атомы, началась реионизация. То есть барионное вещество стало нейтральным. Но главным было не оно. А главным было то самое темное вещество, о котором мы говорим. И его, еще раз напомню, в 5-6 раз больше чем обычного (барионного). Поэтому следить нужно прежде всего за судьбой темного вещества. Поскольку в гравитационном плане оно доминировало. Вот здесь нарисованы возмущения плотности.
То есть барионное вещество стало нейтральным. Но главным было не оно. А главным было то самое темное вещество, о котором мы говорим. И его, еще раз напомню, в 5-6 раз больше чем обычного (барионного). Поэтому следить нужно прежде всего за судьбой темного вещества. Поскольку в гравитационном плане оно доминировало. Вот здесь нарисованы возмущения плотности.
Если кто-то любит заморачиваться с расчетами (это иногда очень полезно, помогает понять физический смысл), смоделируйте огромное облако гравитирующих точек, пусть одинаковой массы, это не важно, равномерно распределенных, хотя вы равномерно распределить никогда не сможете, будут небольшие флуктуации. Так вот, если вы отпустите облако эволюционировать (и будете довольно точно считать) – у вас обязательно вот эти мелкие начальные возмущения плотности, которые всегда есть (из-за округления, из-за чего хочешь), будут приводить к тому, что в некоторых местах гравитирующие точки будут накапливаться, сгущаться. За счет гравитации. И появятся уже заметные неоднородности – возмущения плотности. На слайде так и написано – рост возмущений плотности. Эти возмущения плотности нарастают в том самом темном веществе, потому что гравитирующие точки и есть модель темного вещества. Напомним, что темное вещество обладает одним свойством – гравитацией. Его существование обнаруживают только по гравитационным воздействиям.
На слайде так и написано – рост возмущений плотности. Эти возмущения плотности нарастают в том самом темном веществе, потому что гравитирующие точки и есть модель темного вещества. Напомним, что темное вещество обладает одним свойством – гравитацией. Его существование обнаруживают только по гравитационным воздействиям.
На слайде картинка, которая была получена в 2001 году, в проекте Миллениум. Было взято огромное количество, даже гигантское – триллионы вот этих самых гравитирующих точек, и запущена эволюция. К темному веществу был подмешан, конечно, еще и барионный газ, но главная доминанта была темное вещество. И вот вы видите структуры, которые появляются со временем. Это вот слева было очень давно – 210 миллионов лет после Большого взрыва. Это одна структура, здесь просто масштаб разный. На верхней картинке, масштаб помельче, здесь, внизу, покрупнее. А справа показано то, что получилось к нашему времени. Та же самая область во что превратилась. В сгустки. То есть первоначальные слабовыраженные сгустки – они собрались в такие уже весьма заметные и крупные. Мы их называем гало темного вещества, это огромные скопления темного вещества массой до 1015 масс Солнца.
Мы их называем гало темного вещества, это огромные скопления темного вещества массой до 1015 масс Солнца.
Теперь еще немного на наглядном уровне. Вот видите возмущения плотности, которые всегда есть. Некоторые из возмущений плотности были такими большими, что их самогравитация (Гравитация – это важнейший фактор, который доминирует в эволюции всей Вселенной) определила их судьбу. Иногда появлялись настолько массивные и плотные сгустки, что самогравитация уже не позволила им рассыпаться. Когда перейден некоторый (джинсовский) порог, эти гравитирующие сгустки стали самостоятельными. Их называют гравитационно связанными объектами, и они и есть первые темные гало. А вот эти небольшие флуктуации рассыпались, потом появлялись новые. Выглядит как волнение такое переменчивое, оно всегда было, но иногда на фоне волнения появлялись устойчивые сгустки. Сгустки начали жить своей жизнью. Они перемещались, но главный процесс в их жизни – это слияния. Оказывается, что если вы возьмете сгустки, состоящие из темного вещества (первые сгустки были массой порядка 10 в 4-ой масс Солнца), то в отличие от Кеплеровкой механики 2-х точек (из 2-х точек, из двух звезд, которые сближаются с очень большого расстояния, вы никогда не образуете двойную звезду. Это невозможно. Нужно уменьшить полную энергию системы, какую-то ее долю удалить, только тогда образуется двойная) эти вот сгустки могут спокойно соединиться и слиться. Этот процесс слияния происходил многократно.
Эта тема затрагивалась 2 года назад, я читал лекцию по эволюции галактик, показывал, как это делалось. Слайд взял оттуда. Итак, слияние возможны и даже неизбежны. Тонкие детали процесса его еще до конца не исследованы. Если кто захочет сделать кандидатскую диссертацию – приходите, поговорим на эту тему. На слайде показаны эти самые слияния в виде дерева слияний. Были слияния большого с малым, слияния объектов одинакового размера и так далее. Слияния, их иногда называют мержинги (merging) шли боттом-ап (bottom-up). Это слово означает, что процесс шел снизу вверх. То есть от мелкого к крупному. Еще говорят «боттом-ап» на Западе, и даже в Китае, когда хотят сказать «пей до дна». Не путать со Вселенной.
Вот картинка, которая иллюстрирует эволюцию темного вещества и барионов. Вот видите, темное гало, вот это его гравитационная потенциальная яма. Я никого не пугаю, вы все знаете, что такое потенциальная яма. И естественно, что ведомые, влекомые барионы – они просто падали в эту яму. Падали, накапливались, а поскольку барионное вещество, мы говорим, диссипативное, то есть может терять энергию, то уплотнения могли происходить очень сильные. Поэтому барионы в области их скопления начинали доминировать над темным веществом. Если поговорить об образовании галактик, то вот здесь на дне потенциальной ямы, изначально сформированной сгустком темного вещества и сильно углубленной попавшими в нее барионами, образовался уже барионный сгусток, а вокруг него простиралось темное гало. Здесь, на краях ямы доминирует темное вещество, поскольку, как вы видите, нет разницы между красной и черной кривыми. А вот здесь, на дне ямы, где накопились барионы, из них образовались галактики или скопления галактик.
Но сначала, прежде чем дойти до галактик, из этого вещества образовались первые звезды. Это были очень странные объекты, поскольку содержали газ из водорода и гелия, который не мог эффективно охлаждаться, а для того, чтобы образовать звезду, ее нужно охладить. (Мы вскоре к этому вернемся.). Эти первые звезды, образовавшиеся из плохо охлаждающегося горячего газа, были массивными, в 1000 массивнее Солнца, может в 100, варианты есть всякие, но в любом случае очень массивные.
Эти массивные звезды взорвались, а перед взрывом в недрах этих звезд были синтезированы первые тяжелые элементы, элементы тяжелее гелия. Мы называем их также металлами (это жаргон астрономический, мне он не нравится, но вынужден использовать), или тяжелыми элементами. Итак, в межзвездном газе появились тяжелые элементы. Например, углерод, кремний и др.. Здесь, на слайде, конечно, не фотография, это просто рисунок художника. Металлы, которые были выброшены из первых звезд в межзвездную среду обогатили ее – и впоследствии межзвездный газ был уже обогащен этими тяжелыми элементами. Тяжелые элементы являются прекрасными охладителями. И пока их не было, нечем было охлаждать. Для того, чтобы сжать газ и образовать звезду – его нужно охладить. Иначе газ будет как резиновый. Его можно толкнуть, он будет вот так болтаться, это называется адиабатическое колебание. И все. Для непрерывного сжатия надо обязательно потерять энергию, чтобы эти колебания сходились и, наконец, плотность достигала тех самых звездных значений. Так вот, оказывается, охладителями в первичном газе, где металлов не было) могли быть только молекулы.
Конечно, молекулы не могли существовать, потому что газ был нагрет до температуры 10 в 4-ой кельвинов, точнее не могли существовать долго. Но при некоторых реакциях, например, в реакции трехчастичных столкновений (плотность-то была большая и если в обычном космосе 3 частицы сталкиваются практически никогда, то здесь в первых звездах это были частые события) было возможно образование молекулы Н2. А вот молекула Н2 – мы на следующем кадре увидим – она уже является охладителем. То есть, что такое охладитель, как он действует. Это значит тепловая энергия частиц, которые летают в газе, и сталкиваются, в частности, с молекулами, уходит на возбуждение энергетических уровней молекул. Молекулы сбрасывают эту энергию через инфракрасное, например, излучение, для которого звезда прозрачна. То есть тепловая энергия тратится на молекулу, а молекула сбрасывает энергию, и она, уходит в космос в виде излучения, а вещество при этом охлаждается. Вот такой охладитель – молекула Н2. При более низкой плотности работала и такая реакция.
Итак, закрепим. Без молекул Н2 не появились бы первые звезды. Без первых звезд не появились бы металлы, хорошие охладители. Без металлов не появились бы звезды, которые мы сейчас наблюдаем. Все современные наши звезды образуются из вещества, из холодного газа, газопылевой среды, которые охлаждаются при сжатии путем излучения молекулами и пылью, т.е. микрообъектами, содержащими тяжелые элементы.
Теперь один научный слайд – скорость охлаждения. Молекулы Н2 – хорошие охладители, при высоких температурах, т.е. скорость охлаждения высокая. Эта кривая — для высокой плотности, эта – для низкой плотности. Высокая температура означает, что столкновений больше, чаще образовывались и возбуждались молекулы Н2. А вот здесь где-то уже на температуре 200 градусов порог, здесь уже молекулы так редко образовывались и сталкивались, что охлаждением можно пренебречь. Итак, первичный горячий газ был охлажден до температуры в несколько сотен, скажем до 200 кельвинов, как раз излучением молекул.
В аннотации лекции было написано: без молекул не было бы звезд – вы все это прекрасно теперь сами понимаете, что звезд ни первых, ни последующих не было бы. Кстати, скорее всего самый дорогой астрономический проект, который называется Джеймс Уэбб, Телескоп, и который будет запущен в космос, скорее всего, после 18-го года (Вот он 6-метровый космический телескоп с составным зеркалом, предназначенный для наблюдений в инфракрасном диапазоне. Здесь много экранов, которые защищают его, потому что он предназначен для инфракрасного диапазона и его нужно охлаждать, потому что если он будет горячий, то собственное излучение «забьет» детекторы.), так вот этот телескоп предназначен, в частности, для обнаружения вспышек этих самых первых звезд через невероятные дали и миллиардолетия. Вспышка, которая, конечно же, происходит в энергетичном ультрафиолетовом или даже рентгеновском диапазоне, но из-за космологического увеличения длины волны излучения (космологический фактор z где-то тридцатка, а длину волны излученного фотона нужно умножить на z, чтобы получить длину волны регистрируемого фотона) из ультрафиолетового перемещается в инфракрасный. Поэтому вспышки, которые должен увидеть этот телескоп, это вспышки инфракрасные, они будут свидетельствовать о том, что мы видим взрывы этих самых-самых первых звезд.
Молекулы и звезды в нашу эпоху
Теперь молекулы и звезды в нашу эпоху.
Я здесь поместил портрет академика Виктора Амазасповича Амбарцумяна. Молодежь, может быть, забыла, но это был выдающийся математик, прежде всего, и еще астроном. На основе довольно простых соображений, изучая трапецию Ориона (это тесная группа молодых звезд, которые расположены примерно на сравнимых расстояниях друг от друга), он показал, что эти динамическая система не стабильна. Она должна разрушаться очень быстро, за времена в сотни тысяч лет. И это говорит о том, что раз такие мы наблюдаем системы, значит, эти звезды образовались только что, иначе они уже разлетелись бы.
Итак, звезды образуются в нашу эпоху. Виктор Амазаспович считал, что, звезды образуются из некого дозвездного сверхплотного тела, но все-таки сейчас доминирует главная точка зрения и она уже единственная, состоящая в том, что звезды образуются в самых плотных участках (ядрах) межзвездных, плотных так называемых молекулярных облаков в процессе их сжатия. Мы еще эту картинку увидим.
Молекулярные облака – у нас новый термин появился.
Если вы посмотрите на небо глазом, вы увидите темное небо и звездочки. Если вы посмотрите в телескоп – возможно, вы увидите гораздо больше звездочек, еще там побольше каких-нибудь пятнышек вроде планетарных туманностей и т.д. но если вы «посмотрите» в радиотелескоп, то увидите сплошную такую губку как на слайде. Так радиотелескоп «видит» небо в линиях СО. Здесь поплотнее, здесь поменьше, картина очень тонко структурирована. Если эту картину разглядывать, то вложенность вот этой губчатости – она вот такая, что ее можно назвать почти бесконечной. Такие математические конструкции называют фракталами. Здесь даже указана фрактальная размерность.
Молекулярные облака наблюдаются не только в линиях СО, но и в линиях других молекул они тоже видны. Просто в некоторых линиях молекул вы видите, довольно обширные, не очень плотные, так называемые, диффузные облака, в других очень плотные небольшие облака. Выглядят как ядрышки. Ну и вот, здесь (на слайде неважно видно) представлено описание иерархии молекулярных облаков. Указано, какие размеры, температуры, магнитное поле структур, но это все довольно специальные знания. Самые большие структуры имеют массы чуть ли не 10 в 7-ой масс Солнц, т.е. 10миллионов. Вот они – самые большие. А самые маленькие? А самые маленькие ядра молекулярных облаков уже имеют плотности (точнее, концентрации) частиц 10 в 4-ой в кубическом сантиметре и более, и характерные массы там порядка одной массы Солнца, а температуры более низкие, чем в диффузных облаках. Эти самые ядра, сгустки в молекулярных облаках – это именно те места, где образуются звезды. Именно здесь. В ядрах молекулярных облаков. В самых плотных сгустках.
Как наблюдают молекулы, в частности, в областях звездообразования? Прежде всего отметим важность радиотелескопов. Я уже говорил вам, показывая один из первых слайдов, что радиотелескопы – мощнейшее средство наблюдения молекул. Потому что молекулы излучают и поглощают в радиодиапазоне. В оптике очень мало, в ультрафиолете побольше, но в миллиметровом радиодиапазоне линий молекул наблюдается очень много. И в инфракрасном диапазоне тоже наблюдается излучение и поглощение молекул и пыли. Тот самый телескоп миллиметрового диапазона, о котором мы говорили – АЛМА (ALMA) – он предназначен в частности для таких наблюдений. Здесь другой нарисован инструмент – космический телескоп Гершель. Инструментов довольно много сейчас в мире и наземных и космических. Ну а в спектрах молодых звезд есть линии поглощения в ультрафиолетовом диапазоне.
Несколько лет назад я читал здесь лекцию «Ультрафиолетовая Вселенная». Мы уже говорили о том, что электронные переходы, при которых поглощаются или излучаются кванты в ультрафиолетовом диапазоне – самые энергетичные. Похоже на атомные переходы, показанные на слайде (здесь анимация работает хреновенько, но все-таки что-то есть). То есть электрон переходит с одного уровня на другой и либо излучается, либо поглощается, довольно значительный квант энергии, соответствующий длине волны, которая лежит, как правило, в ультрафиолетовом, иногда в оптическом диапазоне. Пониже проиллюстрированы колебательные переходы, молекула уже не единичный шарик, а система ядер и электронов (заряженных частиц), связанная электронными связями, вот она колеблется, а что происходит, когда заряды движутся? Движущийся заряд генерирует излучение электромагнитных волн. Для молекул, колебательные переходы, как правило, вызывают излучение (поглощение) в инфракрасном диапазоне. Ну и вращающиеся молекулы (на нижнем рисунке) тоже излучают (поглощают), но уже в субмиллиметровом в и миллиметровом радио диапазоне. Как получается линия поглощения? Если молекулы стукнуть, возбудить – она сбрасывает энергию, она излучает, т.е. появляется эмиссия. Что значит стукнуть? Стукают другие молекулы, которые движутся в газе. А если у вас есть источник излучения, и молекула находится на луче зрения к нему, то фотон от источника, который придет, он тоже может поглотиться и возбудить эту молекулу. Молекула потом переизлучает фотон, но уже не в том же направлении, а во все стороны. И значит, получается, на фоне источника ослабление потока, т.е. поглощение.
На слайде я просто продемонстрирую, что по отношению к молекуле Н2, все остальные молекулы очень малочисленны. По массе их где-то 10 в минус 5-ой (может быть 10 в минус 4-ой только для СО – главной молекулы после Н2), всех остальных еще меньше. Но тем не менее, все эти молекулы важны. Я уже про некоторые говорил, все они важны, в различном плане, но важны.
Молекула Н2симметричная, неполярная и она излучает или поглощает только в ультрафиолетовом диапазоне (электронные переходы), либо в инфракрасном (колебательные переходы). Так вот прямое обнаружение молекул Н2в ультрафиолетовом было сделано при помощи ультрафиолетового телескопа, который был запущен на метеоракете. Вот она показана — Аэропчела-150. И первый спектр был получен вот такой. Качество его (даже если бы у вас был хороший проектор) немногим лучше, чем вы тут видите. Такое туманное пятнышко. Более современный спектр конечно уже детальный. Вот мощные линии поглощения молекулы Н2 в ультрафиолетовом диапазоне. Здесь же близко линия дейтерированного водорода, молекулы HD.
Молекулярная спектроскопия – это самый главный инструмент, который позволяет нам понимать, что за свойства в этих самых облаках, где образуются звезды.
Даже один факт, что мы видим эту молекулу, мы ее наблюдаем – означает, что плотность этого облака, или лучше говорить – концентрации частиц такая-то. Если бы концентрация была меньше, то частоты столкновений не хватает, чтобы эту молекулу возбудить в достаточном количестве, чтобы много было излучения. Если облако слишком плотное, то работает ударная деэкситация (девозбуждение), то есть не успеет молекула излучить, как ее уже толкнула другая молекула, сняла энергию и все. Поэтому, если мы видим линию данной молекулы – мы уже знаем, какова концентрация частиц в данном объекте. Вот здесь показана, так называемая, критическая плотность. От 10 в третьей до 10 в восьмой частиц в кубике. Размах серьезный.
Наша группа в Институте астрономии, которая занимается вопросами астрохимии и звездообразованием. Одна из членов группы здесь присутствует, ну и я присутствую. У нас хорошая интересная работа, занимаемся разными вещами, вообще говоря, довольно свободно, нет у нас диктаторства никакого. Эта свобода позволяет творчески развиваться. Вот здесь на слайде 4 доктора наук. Один из них защитил буквально месяц назад диссертацию. Ярослав Павличенков. Он еще молодой человек. То есть 38 лет – это нормально. Другие тоже защитят, и все будет хорошо. Итого у нас 4 доктора, 3 кандидата и студенты есть, приходят.
Что и как мы делаем? Должен признать с горечью, что в России инструментов субмиллиметрового и миллиметрового диапазона – нет. Это беда. Есть проект, так называемый телескоп Суффа (радиоастрономическая обсерватория, создаваемая Астрокосмическим центром ФИАН. Обсерватория располагается на высокогорном плато Суффа в отрогах Туркестанского хребта в Республике Узбекистан), но это долгострой, и когда это будет построено – непонятно. Поэтому для наблюдения мы объединяемся с командами астрономамов из Германии, из Дании, из Франции, США и т.д., т.е. наблюдаем совместно. Ну естественно, а что делать.
А вот здесь на слайде упомянуты модели и обработка наблюдений. У нас особенно развиты теоретические работы по моделям, переноса излучения, динамические и химические модели. Мы используем и лабораторные данные. Часть лабораторных данных просто берем из мировых центров по астрохимии. Что такое центр мировых данных по астрохимии? Лаборатория, в которой приближают условия космического вакуума, температуры, излучения и измеряют скорости химических реакций, которые должны происходить и происходят в космосе. Мы же знаем, что молекулы образуются в результате химических реакций. Так вот скорость этих реакций и меряют. Ну и квантовые химические расчеты, один из них я вам показал в самом начале лекции, когда говорил про работу Артема Кабанова.
Спектры, которые мы получаем, в кооперации с нашими коллегами, выглядят примерно так. В одном месте куча линий, в других меньше. Я сейчас чуть-чуть поподробнее.
В одном месте облака эта линия выглядит так, в другом так, в третьем так, и вот догадайся, что это означает. Тут не догадываться нужно, нужно проводить расчет.
Расчет сложный, формулы на экране не видны, и хорошо, что не видны. Это такая кухня теоретическая, решается сложные интегральные уравнения переноса излучения в среде. Она позволяет из анализа спектров линий узнать, какова плотность, каково распределение плотности в объекте, какова температура, каково распределение температуры, какие скорости движения вещества в этом теле, как распределены химические вещества, в частности, молекулы того или иного вида, т.е. структуру, физические и химические свойства этого самого протозвездного объекта. То есть, узнать в каких условиях рождается звезда.
На слайде иллюстрация, как мы работаем. Показана так называемая карта вкладов, помогающая проанализировать составляющие, ответственные за форму линии. Ну, вот наблюдаемый спектр (внизу) мы проанализировали и думаем, что получили замечательный результат, знаем, как устроено это облако, и все остальное о нем знаем.
Но всегда в астрономии, в любых наблюдениях, есть такой дамоклов даже не меч, бог его знает, сколько там клинков, как на троне в «Игре престолов. А клинки эти означают множество решений. Может быть, мы нашли одно из решений, может быть оно не основное, не главное или вообще не физичное. Поэтому всегда, когда решается обратная задача по астрономическим наблюдениям восстановить структуру и свойства какого-то объекта, нужно доказать, что получено единственное решение. А для этого нужна дополнительная информация. А дополнительная информация идет из нашего понимания, как эти объекты могли образоваться. Поэтому мы строим, так называемые, химико-динамические модели. Они помогают понять что возможно, я что нет. Ведь математика может дать вам что угодно. Всегда нужно подходить с точки зрения, а возможно ли это со стороны физики и как это получить. Поэтому я привел высказывание Гейзенберга, перевел его так, а, проще говоря, – какой мы вопрос природе ставим, такой получаем ответ, а потом думаем, что это истина и есть. А если бы поставили другой вопрос? Тут непросто.
На слайде картина, которая наверняка известна всем любителям астрономии, – диаграмма образования звезды из молекулярного облака. Есть молекулярное облако. В нем, пока оно малой плотности, присутствуют молекулы СО. Это облако сжимается, в частности, из-за охлаждения молекулами и пыли. Появляются ядра, сгустки. Ядро, которое, сжимаясь, переходит под так называемый гравитационный предел Джинса уже будет сжиматься и далее. Тепловая энергия не может противодействовать сжатию, потому что тепло сбрасывается из ядра (излучается молекулами). Если бы не было охлаждения, то сжатие в какой-то момент остановилось бы. А поскольку есть молекулы и пыль, которые сбрасывают тепловую энергию, то ядро продолжает сжиматься. Появляются, поскольку плотность растет, все более и более сложные молекулы. Вот они обозначены здесь, слева внизу. Ну и, наконец, появляется протопланетный диск, а затем что-то вроде нашей планетной системы. Молекулы здесь везде присутствуют. Эти молекулы – свидетели всех процессов, которые происходят в протозвезде или в протопланетном диске. Мы этот процесс умеем моделировать с помощью компьютера.
Здесь просто я перечисляю, какие основные задачи решаются. Динамика, перенос излучения, астрохимия. Астрохимия в этих объектах довольно сложная. Я уже сказал, что видов молекул около 200, несколько сотен изомеров, которые тоже играют большую роль, а реакций аж под семь с половиной тысяч. И эту гигантскую матрицу нужно уметь решать. Это серьезная очень задача. Добавлю только, что мы берем скорости химических реакций из лабораторий. Они, как правило, самые точные, но некоторые скорости известны лишь теоретически и там может быть ошибка в 3 раза и даже в 10.
Пожалуй, самые сложные и самые интересные реакции – это не те, которые происходят в газовой фазе, а те, что протекают на поверхности пылинок, т.е. на каталитической поверхности. На поверхности пылинок может образоваться молекула, которая никогда не образуется в обычном межзвездном веществе в газовой фазе. Например, та же самая молекула Н2. Для ее образования там (в газе) слишком мала плотность. В первых звездах плотность была большая, поэтому они временно образовывались, как вы помните, а здесь нет. Молекула образуется, когда 2 атома водорода садятся на пылинку, гуляют по квантово-механическим коридорам, и если время их жизни на пылинке достаточное, т.е. если они не улетят с пылинки прежде чем успеют встретиться в какой-то потенциальной ямке, а на поверхности твердого тела они (такие ямки) всегда есть, то там есть возможность соединиться, и получается молекула Н2. Кроме молекул Н2 там могут образовываться очень сложные молекулы. В том числе и высокая органика. Кроме того, даже из льдов, ну, скажем, из углекислого льда или из воды под жестким облучением ультрафиолетовым от звезды образуются очень сложные соединения. Здесь вот такая картинка и показана. Что-то очень сложное. Например, дегти образуются и т.д. Считается, что именно на космической пыли образуются самые сложные молекулы. А потом эти пылинки слипаются в сгустки – планетезимали. Из них образуются планеты, планеты разогреваются, вся органика разрушается, погибает, но потом остальные планетезимали падают на планеты и приносят органику. Органический суп, из которого, в конце концов, мы не знаем, как, точнее я не знаю, как, (может быть кто-то из вас знает), образуется жизнь.
Ну вот, похвастаться хочу. Несколько лет назад наша команда в сотрудничестве с коллегой из Германии по фамилии Семенов смоделировали, как бы выглядели вот эти самые диски, которые образуются вокруг молодых звезд. Вот эта модель. А сравнительно недавно, сейчас мы только пишем статью, я даже там не участвую, потому что это мои молодые коллеги все сделали, оказалось, что наблюдения на АЛМА показывает, как реальные диски выглядят и есть почти полное совпадение с нашей моделью. Это предсказательная сила теории. Здесь можно гордиться.
Молекулы в звездах и возле звезд
Ну и последний очень небольшой раздел, тема которого – а есть ли молекулы в звездах. В современных звездах. Да, есть.
Вот картинка, на ней указано какие основные элементы мы наблюдаем в звездах. В горячих звездах классов до G, до Солнца, в основном наблюдается водород и некоторое количество металлов. Молекул нет. Например, в спектрах звезд спектрального класса А доминирует, водород. А вот уже в холодных звездах доминируют молекулы, например, окись титана. И на Солнце эти молекулы есть, но мало. Здесь доминируют другие элементы кальций, железо и т.д. На диаграмме Солнце – вот здесь. А в коричневых карликах этих недозвездах, молекул вообще много. Ну понятно, холодные, плотные объекты, в которых молекулы легко образуются. Вот они тут (справа) некоторые молекулы перечислены. Далеко не все. Молекулы есть и в звездах, и в околозвездном веществе. Как молекулы вообще могут образоваться, и как образуется пыль – в одной фразе сказать сложно. В прошлом году я прочитал лекцию «Пыль в космосе», в частности о том, как образуется пыль. Пыль очень важная компонента. Собственно, мы все родились из этого праха, и все обратимся в прах, так говорит великая книга. (Библия. От Экклезиаста).
Молекулы в протопланетных дисках опускаю, на слайде вы прочитать не сможете, но их там полно.
Ну и, наконец, молекулы в атмосферах экзопланет. Вы знаете, что сейчас обнаружено около 3000 планет вокруг других звезд и мы астрономы (я в общем, здесь никаких моих личных заслуг нет) наблюдаем молекулы, в том числе в этих объектах. Молекулы есть везде. И мы особенно пытаемся найти молекулы, которые называются биомаркерами. Это метан, вода и т.д., которые, как правило, сопровождают жизнь нашего типа. Скажем, углеродные формы.
Ну и вот выводы. Вы уже их прочитали. Ну и, пожалуй, просто это моя традиция, всегда в конце нужно немножко похулиганить. Поэтому, пусть не про все поведал я, впадать ни в грусть, ни в раж мне не дадут молекулы С2 Н5 ОН. Ну и дальше предупреждение. Коллеги, спасибо. Вопросы.
Вопрос из зала: Скажите, отличимы ли молекулы, обладающие хиральностью?
Космические молекулы различной хиральности различаются по поляризации их излучения. Молекулы, обладающие другой (для нас) хиральностью могут быть нашими органами чувств (химически) неразличимы. Наш организм воспринять их не сможет. Есть гипотезы на тему того, каким образом мы заполучили именно левую хиральность. Я в этом не эксперт.
Я чуть-чуть упомянул, что, вообще говоря, по законам статистики рождаются как те, так и другие. Но самоорганизующаяся система обязательно обладает свойством самопроизводства. А самопроизводство означает определенную унификацию Вот у вас есть машинка, которая РНК, и которая заточена на производство левовращающих белков и самое себя. И значит такие левовращающие белки будут и образовываться. В изначально стохастической ситуации развивается неустойчивость и начинает превалировать один канал воспроизводства, то есть имеем несимметричное воспроизводство. И в конце концов вы получаете, что все белки у вас левовращающие. Эта система не уравновешена, а в неуравновешенной системе тот, кто первый встал, того и тапки. Вот, пожалуйста.
Автор вопроса: Я имел в виду те вещества, которые получают растительные организмы.
Свойства хиральности для неорганики, оно в принципе тоже возможно, но самое главное это именно органика. Органика причем живая органика. Там, где есть системы самоорганизации. Системы самоорганизации избирательны в том плане, что они всегда отбирают то, что им подходит, а что не подходит – нет. Это главное. Но начальный выбор происходит, по-видимому, случайным образом. Это мы такие левые оказались. Может быть, где-то там инопланетянин или инопланетянка будут правой хиральности, и как с ними взаимодействовать не знаю.
«Самая главная молекула»
Мы привыкли к мысли о том, что в начале ХХ века главная роль в научном мире принадлежала физикам, открывшим теорию относительности и квантовую механику. Менее известно, что ряд важнейших физических идей привел к прорыву в совершенно другой области — генетике. В книге Максима Франк-Каменецкого «Самая главная молекула» (издательство «Альпина нон-фикшн»), вошедшей в лонг-лист премии научно-популярной литературы «Просветитель» 2017 года, не только рассказывается о молекуле ДНК и ее роли в воспроизводстве жизни, но и освещаются те вопросы молекулярной биологии, которые тесно связаны с физикой и математикой.
От новой физики к новой биологии
Потрясающие вещи происходят в биологии.
Мне кажется, Джим Уотсон сделал открытие,
сравнимое с тем, что сделал Резерфорд в 1911 году.
Из письма Макса Дельбрюка Нильсу Бору
от 14 апреля 1953 года
1930-е годы
В первой трети ХХ века наиболее значительные, революционные преобразования происходили в физике. Создание теории относительности и квантовой механики до самого основания потрясло эту старую науку, дав ей новый, неслыханной силы импульс к дальнейшему развитию как вглубь, в поисках универсальных физических законов, так и вширь, в смежные области.
Одной из главных вех на пути создания новой физики было открытие Резерфордом в 1911 году атомного ядра. Само существование атома Резерфорда находилось в вопиющем противоречии с основными законами классической физики. На смену старой физике пришла новая, квантовая физика, которая призвана была объяснить устойчивость атомов и их удивительные линейчатые спектры.
Эта теория, разработка которой была начата Планком, Эйнштейном и Бором, нашла замечательно ясную формулировку в 1926 году в виде знаменитого уравнения Шрёдингера. Квантовая механика не только позволила физикам решить все головоломки, которые накопились в области атомных спектров. Она поставила на прочный теоретический фундамент всю химию. Наконец-то был понят сокровенный смысл атомного номера в таблице Менделеева! Стал ясен истинный смысл валентности, выяснена природа химической связи, скрепляющей атомы в молекулах.
К началу 1930-х годов у физиков появилось ощущение всемогущества. Итак, с атомами все ясно, с молекулами тоже, что там еще? Ага, непонятно, как устроено атомное ядро. Занялись ядром. «Ну, здесь вряд ли есть работа на всех, — считали лидеры. — Надо бы придумать что-нибудь покрупнее». И их взоры обратились к святая святых, к тому, о чем физики раньше не могли и помышлять, — к самой жизни. Не поможет ли новая физика разгадать тайну жизни? Или, может быть, наоборот, окажется, что жизнь противоречит квантовой механике, и тогда придется опять изобретать какие-то новые законы? Это было бы особенно интересно.
В то время молодой немецкий физик-теоретик Макс Дельбрюк искал себе занятие по вкусу. Он попробовал заняться квантовой химией, потом ядерной физикой. Интересно, конечно, но не очень. И вот, будучи на стажировке в Институте Бора в Копенгагене, он в августе 1932 года попал на лекцию Бора на международном конгрессе по световой терапии. Лекция называлась «Свет и жизнь». В ней Бор поделился своими мыслями о проблеме жизни в связи с последними достижениями квантовой механики. И хотя Дельбрюк в то время был полным профаном в биологии, лекция Бора так его вдохновила, что он твердо решил посвятить себя этой науке. Вернувшись в Берлин, Дельбрюк стал искать контакты с биологами. Ему повезло. В это время в Берлине работал русский генетик Николай Владимирович Тимофеев-Ресовский.
Дельбрюк стал собирать у себя дома друзей-физиков. Он приглашал Тимофеева-Ресовского, и тот часами обучал их своей науке — генетике. Рассказывая, Тимофеев-Ресовский, по своему обыкновению, бегал из угла в угол, словно тигр в клетке. Он говорил о математически строгих законах Менделя, управляющих наследственностью. О генах и о замечательных работах Моргана, доказавших, что гены расположены цепочкой в хромосомах — маленьких червеобразных тельцах, находящихся в клеточных ядрах. Он говорил о плодовой мушке дрозофиле и о мутациях, т. е. об изменениях генов, которые можно вызвать рентгеновскими лучами. Этим последним вопросом он как раз занимался вместе с физиком-экспериментатором Циммером.
Дельбрюка крайне заинтересовала их работа. Вообще, в генетике было столько созвучного квантовой механике, что дух захватывало. Ведь квантовая механика принесла в физику дискретность, скачкообразность. Она также заставила серьезно относиться к случайности. И вот оказывается, что биологи тоже обнаружили дискретную неделимую частицу (ген), которая случайно переходит из основного состояния (генетики называют его «диким типом») в «возбужденное», «мутантное» состояние.
Что же такое ген? Как он устроен? Об этом часто спорили на вечерах у Дельбрюка. Тимофеев-Ресовский говорил, что, вообще-то, этот вопрос мало интересовал генетиков. Для них ген был тем же, чем для физиков электрон, — элементарной частицей наследственности.
«Вот, я вас спрошу, — сказал как-то Тимофеев-Ресовский, когда от него особенно настойчиво требовали ответа на вопрос об устройстве гена, — из чего состоит электрон?» Все рассмеялись. «Вот видите, так же смеются генетики, когда их спрашивают, из чего состоит ген». «Вопрос о том, что такое ген, выходит за рамки генетики, и его бессмысленно адресовать генетикам, — продолжал Тимофеев. — Вы, физики, должны искать ответ на него».
«Ну, все же, — настаивал Дельбрюк, — неужели нет никаких гипотез, пусть чисто умозрительных?» Тимофеев-Ресовский задумался на минутку и воскликнул: «Ну, как же! Мой учитель Николай Константинович Кольцов считает, что ген — это полимерная молекула, скорее всего, молекула белка». «Ну и что это объясняет?» — длинный Дельбрюк прямо-таки кричал на широкоплечего, могучего Тимофеева-Ресовского. «От того, что мы назовем ген белком, мы поймем, как гены удваиваются? Ведь главная-то загадка в этом! Ты же сам рассказывал нам, как в роду Габсбургов из поколения в поколение переходила характерная форма губы? Что делает возможным столь точное копирование генов в течение веков? Каков механизм? Разве химия дает нам такие примеры? Во всяком случае я никогда ничего подобного не слышал. Нет, тут нужна совершенно иная идея. Тут действительно таится загадка. Великая загадка. Возможно, новый закон природы. Сейчас главный вопрос — как к этому подступиться экспериментально».
Благодаря Тимофееву-Ресовскому Дельбрюк стал неплохо разбираться в генетике. Главное, его больше не смущала эта дьявольская терминология, как будто специально придуманная, чтобы отпугивать непосвященных. Раньше, когда ему случалось слушать выступления генетиков, он недоумевал, зачем им понадобилось придумывать специальный, тарабарский язык. Уж не жулики ли они? Ведь это уголовники изобретают свой особый жаргон, чтобы их преступные намерения не были понятны окружающим.
Знакомство с Тимофеевым-Ресовским изменило его отношение к генетикам. И даже знаменитая фраза, которой генетики особенно любят поражать непосвященных, «рецессивный аллель влияет на фенотип, только если генотип гомозиготен», стала казаться ему не только кристально ясной, но и прямо-таки красивой. «Черт возьми, — думал он. — А ведь и вправду иначе-то не скажешь!»
Фаговая группа
Великая тайна, скрывавшаяся за коротким словом «ген», окончательно пленила Дельбрюка. Как происходит удвоение или, опять-таки на жаргоне, репликация генов при делении клеток? В особенно сильное возбуждение пришел Дельбрюк, когда узнал о существовании бактериальных вирусов или, как их чаще называют, бактериофагов (буквально — «пожиратели бактерий»).
Эти удивительные частицы, которых и живыми-то не назовешь, вне клетки ведут себя просто как большие молекулы — из них даже выращивают кристаллы. Но когда вирус попадает в клетку, то через 20 минут клеточная оболочка лопается, и из нее вываливается сотня абсолютно точных копий исходной частицы. Дельбрюка осенило, что на бактериофагах гораздо легче будет изучать процесс репликации (удвоения генов), чем на бактериях, не говоря уже о животных; возможно, удастся понять наконец как устроен ген. «Вот он — ключ к разгадке, думал Дельбрюк. — Это очень простое явление, гораздо более простое, чем деление целой клетки. Здесь нетрудно будет разобраться. В самом деле, надо посмотреть, как внешние условия будут влиять на воспроизводство вирусных частиц. Надо провести эксперименты при разных температурах, в разных средах, с разными вирусами».
Так физик-теоретик превратился в биолога-экспериментатора. Но мышление — мышление осталось чисто физическим.
А главное — цель. Во всем мире не было другого человека, который занимался бы вирусами с единственной целью — раскрыть физическое строение гена.
В 1937 году Дельбрюк покинул нацистскую Германию. В этот знаменательный во многих отношениях год Рокфеллеровский фонд начал субсидировать работы по применению физических и химических идей и методов в биологии. Распорядитель фонда Уоррен Уивер посетил Берлин и предложил Дельбрюку переехать в США, чтобы целиком посвятить себя проблеме репликации бактериофагов. Уивер, сам получивший физико-математическое образование, ясно понимал значение работ, проводимых Дельбрюком. (Кстати, это он первым назвал новую область науки, финансовую поддержку которой стал оказывать Рокфеллеровский фонд, молекулярной биологией.) Разумеется, Дельбрюк поспешил воспользоваться предоставленной ему возможностью, так как жизнь в Германии становилась просто невыносимой.
В Америке Дельбрюк собрал вокруг себя горстку энтузиастов, заразившихся его идеей изучения природы наследственности на бактериофагах. Так возникла «фаговая группа». Шли годы, и участники фаговой группы все больше и больше узнавали о том, как протекает фаговая инфекция и как процесс воспроизведения фагового потомства зависит от внешних условий и т. д. Было проведено много замечательных исследований, в особенности в области изучения мутационного процесса у бактерий и бактериофагов. Именно за работы этого периода много лет спустя Дельбрюк был удостоен Нобелевской премии, и я подробно обсуждаю его важнейшую работу этого периода в главе 6. Но все эти исследования, казалось, даже не приближали к решению основной проблемы: проблемы физической природы гена.
Как часто бывает в науке, люди, объединившиеся для решения большой и очень важной задачи, постепенно занялись скрупулезным изучением частных вопросов, сделались маститыми специалистами в той или иной узкой области, но перестали видеть исходные цели. Так путники видят издалека сияющие горные вершины, но по мере приближения к ним попадают в лесистые предгорья, откуда этих вершин уже не видно. К тому же эти леса изобилуют ягодами, грибами и прочими маленькими радостями.
Если долго бродить по предгорьям, то виденные издалека снежные вершины постепенно начинают казаться миражом. Да, скорее всего, это были лишь облака, похожие на снежные горы. Но если это и в самом деле были горы, зачем туда спешить? Ведь здесь, в почти нехоженых лесах, так хорошо. Для того чтобы путники вновь вспомнили о главной цели, нужен зычный голос лидера.
И такой голос прозвучал — это был голос Эрвина Шрёдингера, автора основного уравнения квантовой механики.
Эрвин Шрёдингер
Об истории создания квантовой механики написаны горы научно-популярной и исторической литературы. Центральное место во всех этих книгах по праву занимает исполинская фигура Нильса Бора. Но возьмите любой учебник по квантовой механике. Вы увидите, что уравнение Шрёдингера — альфа и омега этой науки. Безусловно, квантовая механика, как и любая другая наука, создавалась усилиями многих замечательных ученых. Несомненно, на Шрёдингера радикальное влияние оказала гениальная догадка де Бройля о волнах материи. Все это так. Но решающий шаг сделал все же Шрёдингер. Он собрал воедино все накопленное до него, чтобы совершить скачок замечательной интеллектуальной смелости и силы.
Хотя имя Шрёдингера не столь известно широкой публике, как имена Эйнштейна и Бора, оно глубоко почитается в кругах физиков и химиков. В 1944 году вышла в свет его небольшая книжка под броским заголовком «Что такое жизнь?», в которой обсуждалась связь между новой физикой и генетикой. Поначалу книга не привлекла почти никакого внимания. Шла война, и большинство тех, кому адресована была эта книга, с головой ушли в научно-технические проблемы, от решения которых во многом зависел исход борьбы с гитлеровской Германией.
Но когда война кончилась, появилось много специалистов, особенно среди физиков, которым надо было все начинать с начала, снова искать себе место в мирной науке, — вот для них книга Шрёдингера оказалась как нельзя кстати.
В своей книжке (на русском языке она вышла впервые в 1947 году) Шрёдингер прежде всего дал очень ясное и сжатое изложение основ генетики. Физикам представилась уникальная возможность узнать (причем в блестящем изложении их прославленного коллеги), в чем же состоит суть этой затуманенной тарабарской терминологией и все-таки загадочно привлекательной науки. Но этого мало. Шрёдингер популяризовал и развил идеи Дельбрюка и Тимофеева-Ресовского о связи генетики и квантовой механики. Пока эти идеи выдвигались неизвестными физикам людьми, им не придавали особого значения. Но когда об этом заговорил сам Шрёдингер…
По признанию всех, кто в последующие годы штурмовал проблему гена, включая основных действующих лиц — Уотсона, Крика и Уилкинса, книга Шрёдингера послужила важным толчком к этому штурму. Шрёдингер был именно тем человеком, кто крикнул: «Вот они, сияющие вершины, посмотрите, они совсем уже близко. Что же вы мешкаете?»
Рентгеноструктурный анализ
Среди тех мест, где был услышан призыв Шрёдингера, особенно большую роль суждено было сыграть двум английским научным центрам — прославленной Кавендишской лаборатории в Кембридже, главой которой некогда был Резерфорд, и Королевскому колледжу в Лондоне. Здесь разыгрались завершающие сцены драмы, развязкой которой стало выяснение физической природы гена.
Место действия не было случайным. Именно в Великобритании сформировалась к тому времени (начало 1950-х годов) самая сильная в мире научная школа рентгеноструктурного анализа. И именно этот метод оказался тем инструментом, который помог физикам проникнуть в тайну жизни.
Квантовая механика явилась теоретическим фундаментом для понимания внутреннего строения окружающих нас веществ — атомов, молекул и всевозможных состоящих из них материалов, будь то кусок железа или кристалл обыкновенной поваренной соли. Но многообразие структур, которые могут получаться из атомов, необозримо. Как узнать, какова структура того или иного конкретного материала? Тут теория обычно мало помогает. Можно, конечно, выдвинуть те или иные предположения, но нельзя утверждать наверняка — слишком много мыслимых вариантов. Необходим экспериментальный метод, который позволял бы напрямую выяснить атомное строение вещества. Именно таким методом и является рентгеноструктурный анализ.
Рентгеновские лучи знакомы всем — ими просвечивают, если вы сломали ногу или заболели воспалением легких. Физическая природа этих лучей та же, что и у видимого света или у радиоволн. Это все разные варианты электромагнитного излучения, различающиеся только длиной волны. Для рентгеновских лучей характерна длина волны порядка 10–10 м. Расстояние между атомами в молекулах и кристаллах имеет тот же масштаб. Это обстоятельство навело немецкого физика Макса фон Лауэ на мысль, что при прохождении рентгеновских лучей через кристалл, в котором атомы расположены строго регулярно, должна возникать дифракционная картина, подобная той, которая наблюдается при прохождении видимого света сквозь дифракционную решетку.
Опыты, проведенные в 1912 году, полностью подтвердили эту догадку. Когда пучок рентгеновских лучей направили на кристалл, за которым поместили фотопластинку, то после проявления фотопластинки на ней обнаружили причудливую, но весьма регулярную систему пятен (рис. 1). Вскоре стало ясно, что по распределению пятен на рентгенограмме и по их яркости можно судить о взаимном расположении атомов или молекул, образующих кристалл, и в случае молекул — даже об их внутреннем строении. Так возник метод рентгеноструктурного анализа. Наибольший вклад в его развитие внесли британские ученые Генри (отец) и Лоуренс (сын) Брэгги. Рентгеноструктурный анализ позволил точно определить структуру всех минералов, а также бесчисленного множества молекул.
Мало-помалу «рентгеноструктурщики» переходили к все более сложным объектам исследования и наконец в 1930-е годы обратили свои взоры к биологическим молекулам. Однако после первых же попыток стало ясно, что решение задачи им пока еще не по плечу. Прежде всего из биологических молекул очень трудно получить кристаллы. Но даже если это удавалось, десятки тысяч атомов, входящих в каждую молекулу, создавали на рентгенограмме такой причудливый узор, что восстановить по нему координаты всей этой массы атомов было просто невозможно. Потребовались многие годы, пока ученые научились решать столь сложные задачи.Преодолением этих трудностей занимались в Кавендишской лаборатории в довоенные и послевоенные годы. Усилия лаборатории, руководимой Лоуренсом Брэггом, были сосредоточены на определении пространственного строения белков. Это и понятно. В те годы все были убеждены, что главная молекула живой природы — молекула белка. В самом деле, ферменты, т. е. молекулы, проводящие в клетке всевозможные химические превращения, — это всегда белки. Белок представляет собой главный строительный материал клетки. Неудивительно, что всеобщим было убеждение, что и гены устроены из белка. Казалось несомненным, что путь к разгадке всех тайн жизни лежит через изучение строения белков.
Белок представляет собой полимерную молекулу, мономерными звеньями, «кирпичиками» которой служат аминокислотные остатки (рис. 2). Аминокислотные остатки располагаются всегда строго линейно, плечом к плечу, подобно солдатам, стоящим по стойке смирно. Но так устроен и биологически активный белок, и белок, нагретый, скажем, до 60°С, когда он уже полностью теряет свою биологическую активность. Значит, одного химического строения белка, т. е. последовательности аминокислотных остатков, недостаточно для того, чтобы белок был биологически активен. Необходима еще совершенно определенная укладка в пространстве групп, закодированных на рис. 2 в виде сокращенных названий аминокислот, которые на самом деле вовсе не кружочки и не шарики, а имеют каждая свою весьма причудливую форму. Вот за то, чтобы определять пространственную структуру всей молекулы белка по рентгенограммам типа приведенной на рис. 1, и велась затяжная борьба в стенах Кавендишской лаборатории. Лишь в середине 1950-х годов Джону Кендрю и Максу Перуцу удалось добиться успеха — они научились определять трехмерную структуру белков. Это случилось уже после того, как была решена проблема устройства гена, — к чему, как оказалось, белки отношения вовсе не имеют.
Уотсон и Крик
Из тех, кто откликнулся на призыв Шрёдингера, двоим посчастливилось первыми подняться на вершину. Это были совсем еще юный воспитанник фаговой группы Джим Уотсон и не столь юный, но в то время мало кому известный сотрудник Кавендишской лаборатории Фрэнсис Крик.
Будучи одержим идеей узнать, как устроен ген, и считая, что фаговой группе эта задача не по плечу, Уотсон добился в 1951 году, чтобы его отправили поработать в Европу. Вскоре он осел в Кавендишской лаборатории, так как встретил там Крика, который был настроен так же по-боевому, как и он сам. Уотсон к тому времени уже был уверен, что ключ к разгадке тайны гена лежит вовсе не в определении структуры белка, а в выяснении структуры ДНК.
Вообще-то, молекула дезоксирибонуклеиновой кислоты, а это неуклюжее название и кроется за сокращением ДНК, не была чем-то новым. Она была открыта в клеточных ядрах швейцарским врачом Фрицем Мишером еще в 1868 году. Затем было показано, что ДНК сосредоточена в хромосомах, и это, казалось бы, говорило о ее возможной роли в качестве генетического материала. Однако в 1920-х и 1930-х годах прочно утвердилось мнение, что ДНК — это регулярный полимер, состоящий из строго повторяющихся четверок мономерных звеньев (аденинового, гуанинового, тиминового и цитозинового), и поэтому эта молекула не может нести генетическую информацию.
Считали, что ДНК играет в хромосомах какую-то структурную роль, а гены состоят из белка, который входит в состав хромосом. Что же заставило Уотсона и Крика усомниться в справедливости концепции белковой природы гена? Главную роль здесь сыграла работа, законченная к 1944 году тремя американскими бактериологами из Рокфеллеровского университета во главе с О. Эвери. Эвери многие годы изучал явление генетической трансформации, открытое в опытах с пневмококками — возбудителями пневмонии (воспаления легких). Эти удивительные опыты состояли в следующем. Брали два вида пневмококков. Одни были способны вызывать болезнь, а другие — нет. Затем болезнетворные клетки убивали путем нагревания и к ним добавляли живые «безобидные» клетки. И вот оказалось, что некоторые из живых клеток после контакта с убитыми каким-то образом «научились» вызывать болезнь. Получалось, что живые клетки как-то трансформировались мертвыми клетками. Отсюда и название явления: генетическая трансформация. Было ясно, что в этих опытах что-то переходит из убитых бактерий к живым. Но что? На этот вопрос и удалось дать ответ Эвери и его соавторам. И хотя их работа была напечатана в медицинском журнале, ею заинтересовались скорее генетики, химики, физики, чем медики. В этой скрупулезно выполненной работе было показано, что при трансформации способность вызывать болезнь переносится от убитой бактерии к живой только с одним веществом — с ДНК. Ни белки, ни какие-либо другие составляющие клетки в передаче признака при трансформации никакой роли не играют. Собственно, эта работа Эвери теперь считается первой работой, в которой было доказано, что вещество наследственности, или гены, есть именно молекула ДНК.
Так что же, выходит, Эвери и его помощники, а вовсе не Уотсон и Крик первыми побывали на вершине?
Бесспорно, Эвери сделал очень важный шаг в нужном направлении, но до вершины он не добрался. Эйнштейн как-то сказал изумительные по своей глубине слова: «Лишь теория решает, что мы ухитряемся наблюдать». У Эвери не было в запасе ничего такого, что можно было бы назвать теорией, и он предпочел ограничиться сухим изложением фактов. Тем не менее несогласие его данных с концепцией белковой природы гена было очевидным.
Генетики оказались перед выбором — либо не поверить данным Эвери, либо признать, что веществом наследственности оказался не белок, как принято было считать, а ДНК. Опровергнуть Эвери было трудно — в его работе просто-напросто не к чему было придраться. Но и от устоявшихся представлений о белковой природе гена отказаться было не так-то просто. Опытам Эвери было дано следующее объяснение: ДНК, конечно, никаких генов не содержит и содержать не может. Но она может вызывать мутации, т. е. изменять гены, которые, как им и положено, состоят из белка. Правда, ДНК оказалась весьма необычным мутагеном, вызывающим от опыта к опыту одни и те же мутации, в отличие от обычных мутагенов, которые вызывают мутации случайным образом, ненаправленно. Это не могло не заинтересовать генетиков, уже давно искавших способы направленного изменения наследственности. Так удалось спасти, казалось бы, уже испускавшую дух белковую теорию гена, но при этом генетики и все те, кто занимался проблемой химической (или физической) природы наследственности, вынуждены были наконец признать, что на ДНК следует обратить серьезное внимание.
Итак, работа Эвери заставила усомниться в том, что ДНК — это всего лишь полимерная молекула, выполняющая в хромосомах структурную роль. Стало ясно, что в ДНК есть что-то еще… Но — не более того. Той теорией, которая решила, что же на самом деле ухитрился наблюдать Эвери, была модель строения молекулы ДНК, придуманная Уотсоном и Криком в 1953 году.
Уотсон и Крик не имели собственных экспериментальных данных. Вообще, в то время в Кавендишской лаборатории, где работал Крик и стажировался Уотсон, никто не занимался ДНК. Ею занимались Морис Уилкинс и Розалинда Франклин в Королевском колледже в Лондоне.
Исследовать ДНК с помощью рентгеноструктурного анализа оказалось даже сложнее, чем белок. Молекулы ДНК как следует не кристаллизовались и давали весьма бедные рентгенограммы вроде той, что приведена на рис. 3. Нечего было даже пытаться решить с помощью таких рентгенограмм обратную задачу рентгеноструктурного анализа, т. е. научиться восстанавливать пространственную структуру молекулы, как это пытались сделать для белков Перуц и Кендрю.Однако кое-какие очень важные параметры молекулы все же удалось извлечь. Эти параметры, полученные Р. Франклин, а также детальные данные о химическом строении ДНК и были положены Уотсоном и Криком в основу их работы. То, как они действовали, больше всего походило на игру. Они знали, как устроены отдельные элементы — мономерные звенья ДНК. Из этих элементов, как из деталей детского конструктора, надо было собрать структуру, отвечающую рентгеновским данным. Результатом этой «игры» стало одно из величайших научных открытий в истории человечества.
Собственно, тому, что в результате получилось, посвящена вся эта книга. Мы постепенно расскажем обо всех главных особенностях строения молекулы ДНК и о том, к каким головокружительным последствиям в понимании основ явления жизни они привели и как возникшие в результате биотехнологии вторглись в нашу повседневную жизнь, произведя революцию в сельском хозяйстве, в криминалистике, в здравоохранении. Но сначала давайте выделим в модели Уотсона и Крика только ее суть, самую главную «изюминку».
Итак, согласно модели Уотсона и Крика, молекула ДНК состоит из двух полимерных цепочек. Каждая цепочка построена из звеньев четырех сортов — А (адениновое), Г (гуаниновое), Т (тиминовое) и Ц (цитозиновое). Последовательность звеньев в каждой цепи может быть совершенно произвольна. Но эти последовательности в одной молекуле ДНК строго связаны друг с другом следующим принципом комплементарности, или дополнительности (рис. 4):
Против А должно быть Т, против Т должно быть А, против Г должно быть Ц, против Ц должно быть Г.
В открытии этого правила комплементарности, которое и составляет главную «изюминку» модели Уотсона и Крика, очень большую роль сыграли данные о том, в каком соотношении встречаются в ДНК различные звенья, т. е. нуклеотиды. Данные эти были получены чуть ранее в замечательных химических работах Эрвина Чаргаффа.
Если внутри каждой полимерной цепочки атомы скреплены очень мощными ковалентными связями, то между комплементарными цепями действуют сравнительно слабые взаимодействия, подобные тем, которые удерживают молекулы друг возле друга в кристаллах.
Самой замечательной особенностью модели Уотсона–Крика было то, что она необыкновенно изящно решала самую главную проблему — проблему репликации гена. Если мы разведем в стороны две цепи, а потом на каждой нарастим, согласно принципу комплементарности, по новой цепи, то получим из одной молекулы ДНК две, причем обе будут идентичны исходной (рис. 5).
Можно представить себе, в какое возбуждение пришел Дельбрюк, когда получил от Уотсона письмо, содержащее наконец-то решение загадки удвоения гена. Он сразу и безоговорочно поверил в предложенную модель. Под впечатлением письма Уотсона Дельбрюк и написал Бору те слова, которые взяты эпиграфом для этой главы.Не только Дельбрюк, очень многие были сразу покорены красотой модели Уотсона и Крика. И хотя некоторые генетики продолжали фанатично держаться за белки, их единственным аргументом осталось такое общее соображение: не может быть, чтобы такая сложная штука, как жизнь, была в своей основе устроена столь просто. Аргумент, прямо скажем, не из сильных.
Так было установлено, что ДНК является самой главной молекулой живой природы. Нет, новых законов физики в биологии не обнаружили. Но центральную проблему, проблему строения гена, решить удалось.
Теперь, более полувека спустя, можно констатировать, что открытие структуры ДНК сыграло в развитии биологии такую же роль, как в физике — открытие атомного ядра. Выяснение строения атома привело к рождению новой, квантовой физики, а открытие строения ДНК привело к рождению новой, молекулярной биологии. Но на этом параллель не заканчивается. Чисто теоретические, фундаментальные исследования атома позволили человеку овладеть практически неисчерпаемым источником энергии и радикально изменили нашу повседневную жизнь благодаря компьютеру, Интернету, мобильному телефону. Развитие молекулярной биологии открыло возможность неслыханным образом вмешиваться в свойства живой клетки, направленно изменять наследственность. Это уже начинает оказывать не менее радикальное воздействие на жизнь людей, чем овладение энергией атомного ядра и всеобщее распространение Интернета. Мы уже вступили в век ДНК.
Читайте подробнее:
Франк-Каменецкий, Максим. Самая главная молекула. От структуры ДНК к биомедицине XXI века. — М.: Альпина нонфикшн, 2017. — 336 с.
Урок 19. молекулярная структура живого — Естествознание — 10 класс
Естествознание, 10 класс
Урок 19. «Молекулярная структура живого»
Перечень вопросов, рассматриваемых в теме:
- Какие химические элементы входят в состав живой клетки;
- Какую роль играют углеводы и липиды;
- Как устроены белки, и как их молекулы приобретают определённую пространственную форму;
- Что такое ферменты, и как они распознают свои субстраты;
- Какое строение имеют молекулы РНК и ДНК;
- Какие особенности молекулы ДНК позволяют ей играть роль носителя генетической информации.
Глоссарий по теме:
Органические соединения – химические соединения, основой строения которых являются атомы углерода; составляют отличительный признак живого.
Полимер – (от греч поли – много, мерос – часть) – многозвеньевая цепь, образующаяся при соединении друг с другом относительно простых молекул – мономеров. Их называют высокомолекулярными соединениями или макромолекулами. К ним относят белки, полисахариды, нуклеиновые кислоты.
Мономеры – низкомолекулярные соединения, способные к образованию макромолекул. Мономерами белков являются аминокислоты; полисахаридов – моносахариды; нуклеиновых кислот – нуклеотиды.
Денатурация – нарушение природной структуры белка (изменение пространственной формы молекулы).
Принцип комплементарности – возможность возникновения водородной связи между определёнными (соответствующими) азотистыми основаниями. Комплементарные основания: А – Т, Г – Ц. Также компилементарными являются пары А – У.
Репликация – свойство молекулы ДНК заключающееся в самодублировании молекулы на основе принципа комплементарности. Этот процесс лежит в основе наследственности.
Основная и дополнительная литература по теме урока (точные библиографические данные с указанием страниц):
- Естествознание. 10 класс [Текст]: учебник для общеобразоват. организаций: базовый уровень / И.Ю. Алексашина, К.В. Галактионов, И.С. Дмитриев, А.В. Ляпцев и др. / под ред. И.Ю. Алексашиной. – 3-е изд., испр. – М.: Просвещение, 2017.: с 88-93.
Электронные ресурсы:
Основы биохимии. Портал открытая биология // Электронный доступ: https://biology.ru/textbook/chapter8/section1/paragraph2/
Химические вещества клетки .Проект «вся биология» // Электронный доступ: http://www.sbio.info/materials/obbiology/obbkletka/
Теоретический материал для самостоятельного изучения
Чтобы познакомиться с сущностью процессов, протекающих в живых организмах, следует, в первую очередь, познакомиться с их химическим составом. Представление о мельчайших структурах даёт понимание – как способствовать сохранению своего здоровья и биологических систем более высокого ранга.
Вы уже знаете, что из 104 элементов системы Д. И. Менделеева около 70 были обнаружены в живых организмах. Т.е., химический состав живой и неживой природы один и тот же, что свидетельствует об их единстве.
Атомы в клетках не существуют самостоятельно, они образуют различные соединения, которые выполняют определённую функцию.
Одним из важнейших неорганических соединений является вода, которая в клетках вода составляет 70-80%. Из школьного курса химии, вы знаете, что вода является хорошим растворителем. Из физики, что она обладает высокой теплоёмкостью и низкой теплопроводностью. Биологическая роль воды в организме состоит в том, что вода способствует движению веществ и нормальному ходу биохимических реакций, в ней хранится тепло. При недостатке воды, температура тела спортсмена может увеличиваться на 10°, а при движении – и более, так как метаболизм проходит непрерывно и интенсивно.
Основные вещества клетки представляют собой молекулы, состоящие из взаимосвязанных атомов углерода. Такие соединения углерода получили название органические соединения. Органические соединения клетки образуют макромолекулы, представляющие собой многозвеньевые цепи – полимеры. В их числе базовыми являются белки, жиры (липиды), углеводы и нуклеиновые кислоты. Липиды и углеводы играют важную роль в построении структур организмов, выполняют энергетическую и другие важные функции.
Однако, вторую по величине группу в вашем организме составляют белки, на их долю приходится около 50% соединений. Белки выполняют самые разнообразные задачи в организме: участвуют в построении мышечных волокон или соединительной ткани; порождают движение нашего тела; выполняют другие важные функции в организме. Например, – транспортную (гемоглобин), рецепторную, сигнальную, или регуляторную (белки-гормоны), каталитическую (белки-ферменты), защитную (антитела, интерфероны), энергетическую (при расщеплении 1г. белка выделяется 17,6 кДж энергии). Можно сказать, что практически нет таких процессов в биологической системе, которые бы шли без участия белков.
Структура белков. Белки (полипептиды) представляют собой высокомолекулярные соединения, которые состоят из большого количества остатков α-аминокислот соединённых пептидной связью . Эта молекулярная (или полипептидная) цепь (первичная структура) складывается всего из 20 аминокислот, несмотря на их огромное количество в природе. Вторичная структура (пространственное расположение молекулярной цепи) является результатом возникновения водородных связей между близко расположенных аминокислот в молекулярной цепи. В результате молекула приобретает форму спирали. Дальнейшая упаковка молекулы в компактные структуры приводит к образованию клубочков (глобул) – так называемой Третичной структуре. Под Четвертичной структурой понимают форму упаковки сложных белков, состоящих из двух или более полипептидных цепочек (например, гемоглобин, хлорофилл и др). Упаковка каждого типа белка уникальна, поскольку связана с первичной структурой, т.е. определённым набором и последовательностью аминокислот в цепочке. Именно в третичной и четвертичной структурах белок способен выполнять свои непосредственные функции.
Белок может терять, присущую ей, трёхмерную структуру (денатаруция). Это изменение может носить временный или постоянный характер, но и в том и в другом случае последовательность аминокислот белка остаётся неизменной. При денатурации молекула развёртывается и теряет способность выполнять свою обычную биологическую функцию. Вызвать денатурацию могут нагревание, воздействие различных излучений, взаимодействие с сильными кислотами, щелочами и концентрированными растворами солей, органическими растворителями. Обратный процесс – приобретение начальной структуры, получил название – ренатурация.
Такая способность к самоорганизации – уникальное свойство белков, определяющее выполнение ими функций. Свернувшись определённым образом, молекула-фермент может связаться только со своим специфичным веществом (субстратом), присоединив его к активному центру. При помощи белка-фермента происходят химические преобразования субстрата в конечный продукт. Например, фермент пищеварительного тракта липаза расщепляет только жиры. Биологическое значение ферментов – ускорение протекания биохимических реакций, т.е. являются биологическими катализаторами.
Собранные из 20-ти аминокислот белки можно представить как буквы в словах – их разные комбинации создают многообразие слов (белков). Набор белков для каждого организма уникален! Именно сочетание уникальных белков определяет различия и сходства организмов.
Каждому организму ежедневно требуется производить огромное количество белков. Как при этом не допускаются ошибки? В этом механизме безошибочной сборки белков участвуют нуклеиновые кислоты.
Нуклеиновые кислоты представляют собой многозвеньевые цепи, звеньями которых являются нуклеотиды. Нуклеотиды состоят из остатка фосфорной кислоты, углевода и азотистого основания. Различаются нуклеотиды по последнему компоненту: аденин, тимин, цитозин, гуанин и урацил (А, Т, Г, Ц, У – сокращённые буквенные обозначения).
Соединение нуклеотидов в цепочку происходит благодаря связи между углеводом одного нуклеотида и остатком фосфорной кислоты другого, что определяет направленность молекулы (начало-конец).
В зависимости от того, какой углевод входит в состав нуклеотида (рибоза или дезоксирибоза), различают рибонуклеиновые кислоты (РНК) и дезоксирибонуклеиновые кислоты (ДНК).
Модель строения молекулы ДНК предложили ДЖ.Уотсон и Ф.Крик в 1953 году. На основе экспериментальных данных было установлено, что количество А=Т, Г=Ц. Молекула ДНК состоит из двух цепочек закрученных спирально вправо. Цепочки удерживаются друг возле друга за счёт водородных связей, которые возникают между комплементарными азотистыми основаниями: А — Т и Г – Ц. Пара полинуклеотидных цепей расположенных комплементарно друг другу называют комплементарными цепями.
Принцип комплементарности позволяет не только молекуле безошибочно само восстанавливаться, но и само удваиваться. Процесс самодублирования молекулы ДНК – репликации, происходит при участии сложного набора ферментов, которые разъединяют комплементарные цепи. На каждой одиночной (материнской) полинуклеотидной цепи начинается сборка новых цепей ДНК. Под действием группы ферментов, так называемой ДНК-полимеразы, нуклеотиды соединяются в цепи и в результате воссоздаются две идентичные двойные спирали ДНК. Репликация молекулы ДНК может происходить безошибочно многократно.
Порядок расположения нуклеотидов в молекулах ДНК определяет порядок аминокислот в молекулах белков. ДНК организма хранит информацию о всём наборе белков, определяющим свойства клеток и организма в целом. Благодаря наличию механизма репликации, эта информация может быть передана поколениям потомков. Поэтому молекулы ДНК являются носителями наследственной информации.
В отличие от ДНК молекула РНК состоит из одной полинуклеотидной цепи. Существует несколько типов РНК, которые выполняют в клетке разные функции:
— информационная или матричная РНК (мРНК) – играет роль посредника при передаче генетической информации от ДНК к структурам клетки, синтезирующим белок, — рибосомам;
— рибосомные РНК (р-РНК) – вместе с белками формируют рибосомы,
— транспортные РНК (тРНК), доставляют аминокислоты к месту синтеза белка,
и некоторые другие.
Вывод
Клетки всех живых существ обладают схожестью элементного химического состава, а также обнаруживает общность живого и неживого. Молекулярную структуру живого составляют белки, липиды, углеводы и нуклеиновые кислоты. Органические соединения клетки образуют макромолекулы, представляющие собой многозвеньевые цепи – полимеры. Такое сходство химического состава является подтверждением единства происхождения всего живого.
Белки принимают участие практически во всех биохимических реакциях клетки и организма. Цепочки молекул белка построены из 20 аминокислот в разных комбинациях и последовательностях. Для каждого организма состав белков уникален. Последовательность аминокислот белков организма зашифрована в молекула ДНК. Способность ДНК к самокопированию (репликации) обеспечивает возможность передачи генетической информации в живой природе.
Примеры и разбор решения заданий тренировочного модуля:
Задание 1. Выберите один ответ:
Пространственную структуру в виде глобулы характерно для структуры белка называемой:
- Первичной;
- Вторичной;
- Третичной;
Ответ: Третичной
Пояснение: первичная структура линейная последовательность аминокислот белка, вторичная – молекула образует спираль.
Задание 2. Найдите ошибку (ошибки) и вычеркните их.
«Молекулы белков состоят из остатков аминокислот и азотистых оснований. Замена одного аминокислотного звена другим в белковой молекуле не изменяет её свойств. Нарушение природной структуры белка называется денатурацией. При этом белки не утрачивают биологическую активность. Денатурация может происходить под действием радиации, низкой температуры, ряда органических растворителей (спирт, ацетон), воды.»
Ответ: «Молекулы белков состоят из остатков аминокислот и азотистых оснований. Замена одного аминокислотного звена другим в белковой молекуле не изменяет её свойств. Нарушение природной структуры белка называется денатурацией. При этом белки не утрачивают биологическую активность. Денатурация может происходить под действием радиации, низкой температуры, ряда органических растворителей (спирт, ацетон), воды.»
Пояснение: азотистые основания не входят в состав белков, это составная часть нуклеотидов (мономеров нуклеиновых кислот).
Мембраны. Немного физики — «BASK»
Высокие технологии, изначально работающие в космосе или на сложном производстве, со временем становятся повседневными. Так мембранные материалы, несколько десятилетий назад родившиеся в научных лабораториях, теперь служат нам в одежде и обуви.
Мембрана – это барьер, который пропускает через себя одни вещества и останавливает другие. Впервые применить это свойство мембран в одежде догадались в фирме Gore в 70-годах прошлого века. Именно в это время стало технологически возможным создать прочную поровую мембрану на основе полимеров. Радиус пор подбирался так, чтобы они не пропускали капли воды из внешней среды и не создавали препятствия для выхода пара наружу.
Капля тумана – 0,1 мм (100000 нм)
Крупная капля дождя – 6,5 мм (6500000 нм)
Молекула воды – 0,2 нм
d пор в мембране = 140 — 200 нм
Зачем это нужно?
Простой полиэтиленовый плащ отлично защитит от дождя и ветра, но не спасёт от намокания. А всё потому, что одной из важнейших постоянных человеческого тела является температура. Она может колебаться в узких пределах. При любой активности мы вырабатываем тепло, излишки которого незамедлительно сбрасываются в окружающую среду. Одним из механизмов отвода тепла является потоотделение: ежесуточно человек выделяет не менее полулитра пота в нормальных условиях, при высоких нагрузках и температурах это значение достигает 12 литров.
Но полиэтилен препятствует отводу паров воды и она конденсируется на его поверхности, опять превращаясь в воду – порочный круг замыкается, под плащом пасмурно и сыро, особенно если снаружи тепло и солнечно.
Как работают поровые мембраны?
Поровая мембрана позволяет избежать «застоя» паров воды под одеждой.
Водяной пар – газообразное состояние той же воды, что падает на нас снаружи в жидком состоянии в виде капель.
Расстояние между молекулами воды в паре так велико, что каждая молекула выступает как отдельный «игрок»: поровая мембрана для неё не является серьёзным препятствием и молекула свободно выходит наружу. Движение пара в поровой мембране можно описать как поток через отверстия.
В капле те же молекулы воды связаны силой поверхностного натяжения, они живут плотными сообществами. Такой конгломерат не может разом пройти сквозь пору пока не растечётся по поверхности монослоем в размер молекулы. В этот момент мембрана начинает пропускать воду. Чтобы предотвратить такой ход событий на поверхность мембраны наносят специальное гидрофобное покрытие с плохой смачиваемостью – DWR. С этим покрытием молекулы воды не могут прореагировать и капля не растекаясь скатывается с поверхности. Да и сама пористая мембрана производится из гидрофобных полимеров, например, политетрафторэтилена, чтобы у молекул пара не было возможности остаться на стенке поры по пути наружу.
Политетрафторэтилен (ПТФЭ) – превосходит по химической стойкости все полимеры: не смачивается водой и не растворяется в обычных растворителях. Полимер с самой большой молекулярной массой.
Почему молекулы пара начинают целенаправленно двигаться наружу? Кто их подталкивает?
Всё мире стремится к равновесию, по крайне мере, так говорит физика. Любое движение обусловлено избытком энергии/вещества в одном месте и недостатком в другом. Когда парциальное давление водяного пара под мембраной (под курткой) превышает его парциальное давление во внешней среде, молекулы воды начинают двигаться сквозь мембрану наружу. Процесс останавливается когда давление пара внутри и снаружи выравнивается.
Значит, если снаружи влажно, то отвод водяного пара прекращается и мы промокаем? Да, но только в случае, когда температуры под курткой и снаружи близки по значениям. Если стоит холодная влажная погода, то отвод водяного пара будет продолжаться даже в таких условиях, так как парциальное давление зависит от температуры и разница в давлениях сохранится.
Особенности поровых мембран
Рабочие характеристики поровой мембраны в первую очередь определяются количеством пор, их размером, распределением по поверхности и толщиной мембраны, а не химическими свойствами материала из которого она изготовлена. Со временем на поверхности мембраны появляются грязевые отложения, они сильно снижают её качество, закупоривая поры и меняя свойства. Неправильно подобранное моющее средство, например порошок, так же забивает поры. Поэтому уход за поровыми мембранами требует особого внимания и осторожности. А поддержание гидрофобности внешней ткани – пропитка, основой правильной работы этого сложного механизма.
Непоровые мембраны. Зачем нужны они?
Непоровые мембраны – отдельный класс мембран, работа которых основана на совершенно иных физических процессах. Как следует из названия, в них нет пор, однако материал мембраны имеет неравномерную структуру, причина которой свободный объём между большими молекулами полимера. Этот объём достаточен для движения небольших молекул воды по мембране – диффузии. Молекулярный размер этих полостей не сравним с размерами пор.
Водяной пар химически связывается с гидрофильной внутренней поверхностью мембраны. В случае интенсивной работы с повышенным потоотделением влага конденсируется на ней. Материал мембраны, обычно полиуретан, начинает набухать, впитывая в себя молекулы воды. Все молекулы под действием температуры начинают двигаться быстрее: гибкий, за счёт влаги, полимер расширяется, пространство между цепочками увеличивается и диффузия молекул воды ускоряется. Она происходит до тех пор, пока концентрация молекул воды в мембране не станет одинаковой по всей толщине мембраны. Основными движущими силами процессов в непоровой мембране являются: разница концентрации молекул воды в ней и разница температур с двух сторон от мембраны. Движение направлено из области с высокой концентрацией воды в область с низкой концентрацией воды. Молекулы, проходящие через свободные полости в мембране, достигают наружней поверхности и уходят в окружающую среду.
Внешняя поверхность непоровой мембраны всегда защищена гидрофобной тканью с плотным плетением, которая не пропускает капли воды снаружи и не препятствует отводу пара.
Полиуретан – прочный, устойчивый к старению, эластичный материал. Гидрофилен. Плёнки из полиуретана легко наносятся на поверхности любой конфигурации. Обладает относительно низкой молекулярной массой.
Непоровая мембрана меньше загрязняется, так как в ней нет пор и нечему забиваться. Эластичность этого полимера даёт возможность производить тянущиеся ткани на его основе
И здесь не обошлось без слабых мест
Тесты показывают, что поровые мембраны более устойчивы к образованию конденсата на внутренней поверхности и лучше работают в условиях повышенной влажности – JIS L 1099 A1.
Проблемным местом непоровой мембраны нужно назвать ограничение её работы при низких температурах. Влага на внутренней поверхности мембраны превращается в изморозь, это затрудняет отведение пара и причиняет дискомфорт. В случае с поровой мембраной изморозь не во всех случаях образуется на внутренней стороне мембраны, так как точка росы может оказаться в другом месте за счёт интенсивного потока пара через мембрану.
Непоровая мембрана начинает работать с небольшой задержкой: ей требуется время на набухание (намокание), чтобы выйти на максимальные рабочие показатели. Тесты показывают, что эффективность непоровой мембраны возрастает с ростом абсолютной влажности под одеждой, поровые мембраны мало зависят от этого параметра. В условиях активной работы при невысокой влажности окружающего воздуха, хорошие непоровые мембраны обходят поровые по паропроницаемости – JIS L 1099 B1.
Из-за гидрофильности самой мембраны её водостойкость ниже, чем у полностью гидрофобной пористой. Когда верхний защитный слой ткани с непоровой мембраной начинает пропускать влагу, она мгновенно проникает внутрь.
Комбинированные мембраны
Хорошие результаты часто получают на стыке методов. В последнее время всё больше интереса вызывают комбинированные мембраны, которые включают поровую мембрану у наружнего слоя и тонкую непориовую со стороны тела. Таким образом производители защищают пористую мембрану от загрязнений тела и увеличивают показатели паропроницаемости.
Так же интересен опыт создания поровой мембраны из волокон полиуретана, реализованный в тканях Polartec® NeoShell®.
Характеристики мембран
Влагостойкость
Паропроницаемость (A1, B1)
Ret
Подробнее читайте в статье
Поровые мембраны в снаряжении Баск:
Polartec® Neoshell
Advance® Alaska
Advance® Perfomance
Advance® 2.5L
Непоровые мембраны в снаряжении Баск:
Gelanots®
Dermizax® 3L
Читать так же:
Разумно о мембранах
Из чего делают мембраны?
Мембраны: «Взгляд изнутри» – как это устроено и работает
Методы определения паропроницаемости и Ret мембраны
как масс-спектрометрия меняет представления о мире
На февральской естественнонаучной программе о том, зачем нужна масс-спектрометрия и как измеряют массу веществ, школьникам рассказал член-корреспондент РАН, профессор Евгений Николаев.
Если отойти от определения понятия масс-спектрометрии из учебников, простыми словами можно сказать, что это «взвешивание» молекул, находящихся в исследуемом веществе.
Зародившаяся в конце XIX века масс-спектрометрия в первой половине XX веке помогла разобраться, как устроен наш мир на атомном уровне, из каких атомов и их изотопов он состоит. В середине XX века на огромном масс-спектрометре, который назывался «калютрон», был получен 235 уран в достаточном количестве чтобы создать атомную бомбу (Хиросима).
В начале 30-ых годов с помощью масс-спектрометра была доказана эквивалентность массы энергии, которую постулировал Эйнштейн.
Важную роль масс-спектрометрия сыграла в исследовании космоса. Например, в 1976 году на Марс отправили два масс-спектрометра. До этого исследования считалось что на Марсе нет азота, только СО2, а оказалось, что азот на этой планете существует и даже в относительно большом количестве.
В эру химической масс-спектроскопии, которая началась где-то в 1940 году, были выпущены промышленные масс-спектрометры для анализа нефти и органических молекул. Это сыграло огромную роль в химии, в понимании природы химической связи, в определении структуры сложных органических молекул. Современные методы позволяют увидеть и идентифицировать в нефти более 100 тысяч соединений за один анализ.
В конце 70-ых масс-спектрометрия бурно вошла в биологию и медицину. И сегодня, когда геном расшифрован и встает вопрос о том, сколько белков в организме, и как они модифицированы химически, масс-спектрометрия помогает детально рассмотреть и охарактеризовать эти молекулярные машины нашего организма.
Сейчас биохимические и биомедицинские применения масс-спектрометрии являются одной из наиболее бурно развивающаяся областей. Масс-спектрометрия находит применение в нескольких десятках сфер: фармацевтика, пищевая промышленность, нефтедобыча, нефтепераработка и нефтехимия, контроль окружающей среды, медицина и токсикология, криминалистика, допинговый контроль, геология, гидрология, минералогия, археология, ядерная промышленность и энергетика, металлургия косметика и парфюмерия.
2.3 Биологические молекулы — Концепции биологии — 1-е канадское издание
К концу этого раздела вы сможете:
- Опишите, почему углерод имеет решающее значение для жизни
- Объясните влияние незначительных изменений аминокислот на организмы
- Опишите четыре основных типа биологических молекул
- Понимать функции четырех основных типов молекул
Посмотрите видео о белках и белковых ферментах.
Большие молекулы, необходимые для жизни и состоящие из более мелких органических молекул, называются биологическими макромолекулами . Существует четыре основных класса биологических макромолекул (углеводы, липиды, белки и нуклеиновые кислоты), каждый из которых является важным компонентом клетки и выполняет широкий спектр функций. Вместе эти молекулы составляют большую часть массы клетки. Биологические макромолекулы являются органическими, что означает, что они содержат углерод. Кроме того, они могут содержать водород, кислород, азот, фосфор, серу и дополнительные второстепенные элементы.
Часто говорят, что жизнь «основана на углероде». Это означает, что атомы углерода, связанные с другими атомами углерода или другими элементами, образуют фундаментальные компоненты многих, если не большинства, молекул, уникальных для живых существ. Другие элементы играют важную роль в биологических молекулах, но углерод определенно квалифицируется как элемент «фундамент» для молекул в живых существах. Это связывающие свойства атомов углерода, которые ответственны за его важную роль.
Углерод содержит четыре электрона во внешней оболочке.Следовательно, он может образовывать четыре ковалентные связи с другими атомами или молекулами. Простейшая молекула органического углерода — метан (CH 4 ), в котором четыре атома водорода связаны с атомом углерода.
Рис. 2.12. Углерод может образовывать четыре ковалентные связи, образуя органическую молекулу. Самая простая молекула углерода — это метан (Ch5), изображенный здесь.Однако более сложные конструкции изготавливаются с использованием углерода. Любой из атомов водорода может быть заменен другим атомом углерода, ковалентно связанным с первым атомом углерода.Таким образом могут быть образованы длинные и разветвленные цепи углеродных соединений (рис. 2.13 a ). Атомы углерода могут связываться с атомами других элементов, таких как азот, кислород и фосфор (рис. 2.13 b ). Молекулы также могут образовывать кольца, которые сами могут связываться с другими кольцами (рис. 2.13 c ). Это разнообразие молекулярных форм объясняет разнообразие функций биологических макромолекул и в значительной степени основано на способности углерода образовывать множественные связи с самим собой и другими атомами.
Рис. 2.13. Эти примеры показывают три молекулы (обнаруженные в живых организмах), которые содержат атомы углерода, различным образом связанные с другими атомами углерода и атомами других элементов. (а) Эта молекула стеариновой кислоты имеет длинную цепочку атомов углерода. (б) Глицин, компонент белков, содержит атомы углерода, азота, кислорода и водорода. (c) Глюкоза, сахар, имеет кольцо из атомов углерода и один атом кислорода.Углеводы — это макромолекулы, с которыми большинство потребителей в некоторой степени знакомо.Чтобы похудеть, некоторые люди придерживаются «низкоуглеводной» диеты. Спортсмены, напротив, часто «нагружают углеводы» перед важными соревнованиями, чтобы убедиться, что у них достаточно энергии для соревнований на высоком уровне. Фактически, углеводы являются неотъемлемой частью нашего рациона; злаки, фрукты и овощи — все это естественные источники углеводов. Углеводы обеспечивают организм энергией, в частности, через глюкозу, простой сахар. Углеводы также выполняют другие важные функции у людей, животных и растений.
Углеводы можно представить формулой (CH 2 O) n , где n — количество атомов углерода в молекуле. Другими словами, соотношение углерода, водорода и кислорода в молекулах углеводов составляет 1: 2: 1. Углеводы подразделяются на три подтипа: моносахариды, дисахариды и полисахариды.
Моносахариды (моно- = «один»; sacchar- = «сладкий») представляют собой простые сахара, наиболее распространенным из которых является глюкоза.В моносахаридах количество атомов углерода обычно составляет от трех до шести. Большинство названий моносахаридов оканчиваются суффиксом -ose. В зависимости от количества атомов углерода в сахаре они могут быть известны как триозы (три атома углерода), пентозы (пять атомов углерода) и гексозы (шесть атомов углерода).
Моносахариды могут существовать в виде линейной цепи или кольцевых молекул; в водных растворах они обычно находятся в кольцевой форме.
Химическая формула глюкозы: C 6 H 12 O 6 .У большинства живых существ глюкоза является важным источником энергии. Во время клеточного дыхания из глюкозы выделяется энергия, которая используется для выработки аденозинтрифосфата (АТФ). Растения синтезируют глюкозу, используя углекислый газ и воду в процессе фотосинтеза, а глюкоза, в свою очередь, используется для удовлетворения потребностей растений в энергии. Избыток синтезированной глюкозы часто хранится в виде крахмала, который расщепляется другими организмами, которые питаются растениями.
Галактоза (входит в состав лактозы или молочного сахара) и фруктоза (содержится во фруктах) — другие распространенные моносахариды.Хотя глюкоза, галактоза и фруктоза имеют одинаковую химическую формулу (C 6 H 12 O 6 ), они различаются структурно и химически (и известны как изомеры) из-за разного расположения атомов в углеродной цепи. .
Рис. 2.14. Глюкоза, галактоза и фруктоза — изомерные моносахариды, что означает, что они имеют одинаковую химическую формулу, но немного разные структуры.Дисахариды (ди- = «два») образуются, когда два моносахарида подвергаются реакции дегидратации (реакции, при которой происходит удаление молекулы воды).Во время этого процесса гидроксильная группа (–OH) одного моносахарида соединяется с атомом водорода другого моносахарида, высвобождая молекулу воды (H 2 O) и образуя ковалентную связь между атомами в двух молекулах сахара.
Обычные дисахариды включают лактозу, мальтозу и сахарозу. Лактоза — это дисахарид, состоящий из мономеров глюкозы и галактозы. Он содержится в молоке. Мальтоза, или солодовый сахар, представляет собой дисахарид, образующийся в результате реакции дегидратации между двумя молекулами глюкозы.Наиболее распространенным дисахаридом является сахароза или столовый сахар, который состоит из мономеров глюкозы и фруктозы.
Длинная цепь моносахаридов, связанных ковалентными связями, известна как полисахарид (поли- = «много»). Цепь может быть разветвленной или неразветвленной, и она может содержать разные типы моносахаридов. Полисахариды могут быть очень большими молекулами. Крахмал, гликоген, целлюлоза и хитин являются примерами полисахаридов.
Крахмал — это хранимая в растениях форма сахаров, состоящая из амилозы и амилопектина (оба полимера глюкозы).Растения способны синтезировать глюкозу, а избыток глюкозы откладывается в виде крахмала в различных частях растений, включая корни и семена. Крахмал, который потребляется животными, расщепляется на более мелкие молекулы, такие как глюкоза. Затем клетки могут поглощать глюкозу.
Гликоген — это форма хранения глюкозы у людей и других позвоночных, состоящая из мономеров глюкозы. Гликоген является животным эквивалентом крахмала и представляет собой сильно разветвленную молекулу, обычно хранящуюся в клетках печени и мышц.Когда уровень глюкозы снижается, гликоген расщепляется с высвобождением глюкозы.
Целлюлоза — один из самых распространенных природных биополимеров. Клеточные стенки растений в основном состоят из целлюлозы, которая обеспечивает структурную поддержку клетки. Дерево и бумага в основном целлюлозные по своей природе. Целлюлоза состоит из мономеров глюкозы, которые связаны связями между определенными атомами углерода в молекуле глюкозы.
Каждый второй мономер глюкозы в целлюлозе переворачивается и плотно упаковывается в виде удлиненных длинных цепей.Это придает целлюлозе жесткость и высокую прочность на разрыв, что так важно для растительных клеток. Целлюлоза, проходящая через нашу пищеварительную систему, называется пищевыми волокнами. Хотя связи глюкозы и глюкозы в целлюлозе не могут быть разрушены пищеварительными ферментами человека, травоядные животные, такие как коровы, буйволы и лошади, способны переваривать траву, богатую целлюлозой, и использовать ее в качестве источника пищи. У этих животных определенные виды бактерий обитают в рубце (часть пищеварительной системы травоядных) и секретируют фермент целлюлазу.В аппендиксе также содержатся бактерии, которые расщепляют целлюлозу, что придает ей важную роль в пищеварительной системе жвачных животных. Целлюлазы могут расщеплять целлюлозу на мономеры глюкозы, которые могут использоваться животным в качестве источника энергии.
Углеводы выполняют другие функции у разных животных. У членистоногих, таких как насекомые, пауки и крабы, есть внешний скелет, называемый экзоскелетом, который защищает их внутренние части тела. Этот экзоскелет состоит из биологической макромолекулы , хитина , азотистого углевода.Он состоит из повторяющихся единиц модифицированного сахара, содержащего азот.
Таким образом, из-за различий в молекулярной структуре углеводы могут выполнять самые разные функции хранения энергии (крахмал и гликоген), а также структурной поддержки и защиты (целлюлоза и хитин).
Рис. 2.15. Хотя их структура и функции различаются, все полисахаридные углеводы состоят из моносахаридов и имеют химическую формулу (Ch3O) n.Зарегистрированный диетолог: ожирение является проблемой для здоровья во всем мире, и многие болезни, такие как диабет и болезни сердца, становятся все более распространенными из-за ожирения.Это одна из причин, почему к зарегистрированным диетологам все чаще обращаются за советом. Зарегистрированные диетологи помогают планировать пищевые продукты и программы питания для людей в различных условиях. Они часто работают с пациентами в медицинских учреждениях, разрабатывая планы питания для профилактики и лечения заболеваний. Например, диетологи могут научить пациента с диабетом контролировать уровень сахара в крови, употребляя в пищу правильные типы и количества углеводов. Диетологи также могут работать в домах престарелых, школах и частных клиниках.
Чтобы стать дипломированным диетологом, нужно получить как минимум степень бакалавра в области диетологии, питания, пищевых технологий или в смежных областях. Кроме того, дипломированные диетологи должны пройти программу стажировки под руководством и сдать национальный экзамен. Те, кто занимается диетологией, проходят курсы по питанию, химии, биохимии, биологии, микробиологии и физиологии человека. Диетологи должны стать экспертами в химии и функциях пищи (белков, углеводов и жиров).
Через призму коренных народов (Сюзанна Вилкерсон и Чарльз Мольнар)
Я работаю в колледже Камосун, расположенном в красивой Виктории, Британская Колумбия, с кампусами на традиционных территориях народов леквунгенов и васаней. Подземная луковица для хранения цветка камас, показанная ниже, была важным источником пищи для многих коренных народов острова Ванкувер и всей западной части Северной Америки. Луковицы камас по-прежнему употребляются в пищу как традиционный источник пищи, и приготовление луковиц камас относится к этому текстовому разделу об углеводах.
Рис. 2.16 Изображение синего цветка камас и насекомого-опылителя. Подземная лампочка камаса запекается в костре. Тепло действует как фермент панкреатическая амилаза и расщепляет длинные цепи неперевариваемого инулина на усвояемые моно- и дисахариды.Чаще всего растения вырабатывают крахмал как запасенную форму углеводов. Некоторые растения, например камас, создают инулин. Инулин используется в качестве пищевых волокон, однако он не переваривается людьми. Если бы вы откусили сырую луковицу камаса, она была бы горькой и имела липкую консистенцию.Коренные народы используют метод, чтобы сделать камас одновременно удобоваримым и вкусным, — это медленно запекать луковицы в течение длительного периода в подземной чаше для костра, покрытой специфическими листьями и почвой. Тепло действует как фермент амилаза поджелудочной железы и расщепляет длинные цепи инулина на легкоусвояемые моно- и дисахариды.
Правильно запеченные луковицы камас по вкусу напоминают смесь печеной груши и инжира. Важно отметить, что, хотя синие камы являются источником пищи, их не следует путать с белыми камасами смерти, которые особенно токсичны и смертельны.Цветки выглядят по-разному, но луковицы очень похожи.
Липиды включают разнообразную группу соединений, которые объединены общим признаком. Липиды гидрофобны («водобоязненные») или нерастворимы в воде, потому что они неполярные молекулы. Это потому, что они являются углеводородами, которые включают только неполярные углерод-углеродные или углерод-водородные связи. Липиды выполняют в клетке множество различных функций. Клетки хранят энергию для длительного использования в виде липидов, называемых , жирами .Липиды также обеспечивают изоляцию растений и животных от окружающей среды. Например, они помогают водным птицам и млекопитающим оставаться сухими из-за их водоотталкивающих свойств. Липиды также являются строительными блоками многих гормонов и важной составляющей плазматической мембраны. Липиды включают жиры, масла, воски, фосфолипиды и стероиды.
Рис. 2.17. Гидрофобные липиды в мехе водных млекопитающих, таких как речная выдра, защищают их от непогоды.Молекула жира, такая как триглицерид, состоит из двух основных компонентов — глицерина и жирных кислот.Глицерин — это органическое соединение с тремя атомами углерода, пятью атомами водорода и тремя гидроксильными (–OH) группами. Жирные кислоты имеют длинную цепь углеводородов, к которой присоединена кислая карбоксильная группа, отсюда и название «жирная кислота». Количество атомов углерода в жирной кислоте может составлять от 4 до 36; наиболее распространены те, которые содержат 12–18 атомов углерода. В молекуле жира жирная кислота присоединена к каждому из трех атомов кислорода в -ОН-группах молекулы глицерина ковалентной связью.
Фигура 2.18 Липиды включают жиры, такие как триглицериды, которые состоят из жирных кислот и глицерина, фосфолипидов и стероидов.Во время образования этой ковалентной связи высвобождаются три молекулы воды. Три жирные кислоты в жире могут быть похожими или разными. Эти жиры также называют триглицеридами , потому что они содержат три жирные кислоты. Некоторые жирные кислоты имеют общие названия, указывающие на их происхождение. Например, пальмитиновая кислота, насыщенная жирная кислота, получают из пальмы.Арахидовая кислота получена из Arachis hypogaea , научного названия арахиса.
Жирные кислоты могут быть насыщенными и ненасыщенными. В цепи жирной кислоты, если есть только одинарные связи между соседними атомами углерода в углеводородной цепи, жирная кислота является насыщенной. Насыщенные жирные кислоты насыщены водородом; другими словами, количество атомов водорода, прикрепленных к углеродному скелету, максимально.
Когда углеводородная цепь содержит двойную связь, жирная кислота представляет собой ненасыщенную жирную кислоту .
Большинство ненасыщенных жиров являются жидкими при комнатной температуре и называются маслами . Если в молекуле есть одна двойная связь, то он известен как мононенасыщенный жир (например, оливковое масло), а если имеется более одной двойной связи, то он известен как полиненасыщенный жир (например, масло канолы).
Насыщенные жиры плотно упаковываются и остаются твердыми при комнатной температуре. Животные жиры со стеариновой кислотой и пальмитиновой кислотой, содержащиеся в мясе, и жир с масляной кислотой, содержащиеся в масле, являются примерами насыщенных жиров.Млекопитающие хранят жиры в специализированных клетках, называемых адипоцитами, где жировые шарики занимают большую часть клетки. У растений жир или масло хранятся в семенах и используются в качестве источника энергии во время эмбрионального развития.
Ненасыщенные жиры или масла обычно растительного происхождения и содержат ненасыщенные жирные кислоты. Двойная связь вызывает изгиб или «перегиб», который препятствует плотной упаковке жирных кислот, сохраняя их жидкими при комнатной температуре. Оливковое масло, кукурузное масло, масло канолы и жир печени трески являются примерами ненасыщенных жиров.Ненасыщенные жиры помогают повысить уровень холестерина в крови, тогда как насыщенные жиры способствуют образованию бляшек в артериях, что увеличивает риск сердечного приступа.
В пищевой промышленности масла искусственно гидрогенизируются для придания им полутвердого состояния, что приводит к меньшей порче и увеличению срока хранения. Проще говоря, газообразный водород пропускают через масла, чтобы отвердить их. Во время этого процесса гидрирования двойные связи цис -конформации в углеводородной цепи могут быть преобразованы в двойные связи в транс -конформации.Это образует , транс, -жир, , из -цис, -жир. Ориентация двойных связей влияет на химические свойства жира.
Рис. 2.19. В процессе гидрогенизации ориентация двойных связей изменяется, в результате чего из цис-жира образуется трансжир. Это изменяет химические свойства молекулы.Маргарин, некоторые виды арахисового масла и шортенинг являются примерами искусственно гидрогенизированных транс -жиров. Недавние исследования показали, что увеличение транс -жиров в рационе человека может привести к увеличению уровня липопротеидов низкой плотности (ЛПНП) или «плохого» холестерина, что, в свою очередь, может привести к отложению бляшек в организме человека. артерии, что приводит к болезни сердца.Многие рестораны быстрого питания недавно отказались от использования жиров транс и , а на этикетках пищевых продуктов в США теперь требуется указывать содержание жира транс .
Незаменимые жирные кислоты — это жирные кислоты, которые необходимы, но не синтезируются человеческим организмом. Следовательно, их необходимо дополнять с помощью диеты. Омега-3 жирные кислоты попадают в эту категорию и являются одной из двух известных незаменимых жирных кислот для человека (другая — омега-6 жирные кислоты).Они представляют собой тип полиненасыщенных жиров и называются омега-3 жирными кислотами, потому что третий углерод на конце жирной кислоты участвует в двойной связи.
Лосось, форель и тунец являются хорошими источниками жирных кислот омега-3. Жирные кислоты омега-3 важны для работы мозга, нормального роста и развития. Они также могут предотвратить сердечные заболевания и снизить риск рака.
Как и углеводы, жиры получили широкую огласку. Это правда, что чрезмерное употребление жареной и другой «жирной» пищи приводит к увеличению веса.Однако жиры выполняют важные функции. Жиры служат долгосрочным накопителем энергии. Они также обеспечивают изоляцию тела. Поэтому «здоровые» ненасыщенные жиры в умеренных количествах следует употреблять регулярно.
Фосфолипиды являются основным компонентом плазматической мембраны. Как и жиры, они состоят из цепей жирных кислот, прикрепленных к глицерину или подобной основной цепи. Однако вместо трех жирных кислот есть две жирные кислоты, а третий углерод глицериновой цепи связан с фосфатной группой.Фосфатная группа модифицируется добавлением спирта.
Фосфолипид имеет как гидрофобные, так и гидрофильные участки. Цепи жирных кислот гидрофобны и исключаются из воды, тогда как фосфат гидрофильный и взаимодействует с водой.
Клетки окружены мембраной, которая имеет бислой фосфолипидов. Жирные кислоты фосфолипидов обращены внутрь, от воды, тогда как фосфатная группа может быть обращена либо к внешней среде, либо к внутренней части клетки, которые оба являются водными.
Через призму коренных народов
Для первых народов Тихоокеанского Северо-Запада богатый жиром рыбный оолиган с содержанием жира 20% от веса тела был важной частью рациона нескольких коренных народов. Почему? Потому что жир является наиболее калорийной пищей, и наличие компактного высококалорийного источника энергии, способного хранить, было бы важным для выживания. Характер жира также сделал его важным товаром. Как и лосось, оолиган возвращается в свое русло после долгих лет в море. Его прибытие ранней весной сделало его первым свежим продуктом в году.В цимшианских языках о прибытии оолигана … традиционно объявляли криком: «Хлаа аат’иксши халимоотхв!», Что означает: «Наш Спаситель только что прибыл!»
Рисунок 2.20 Изображение приготовленного оолигана. Эта жирная рыба с содержанием жира 20% от веса тела является важной частью диеты коренных народов.Как вы уже узнали, все жиры гидрофобны (ненавидят воду). Чтобы отделить жир, рыбу отваривают, а плавающий жир снимают. Жирный состав улигана состоит из 30% насыщенных жиров (например, сливочного масла) и 55% мононенасыщенных жиров (например, растительных масел).Важно отметить, что это твердая смазка при комнатной температуре. Поскольку в нем мало полиненасыщенных жиров (которые быстро окисляются и портятся), его можно хранить для дальнейшего использования и использовать в качестве предмета торговли. Считается, что его состав делает его таким же полезным, как оливковое масло, или лучше, поскольку он содержит жирные кислоты омега-3, которые снижают риск диабета и инсульта. Он также богат тремя жирорастворимыми витаминами A, E и K.
Стероиды и воски
В отличие от фосфолипидов и жиров, обсуждавшихся ранее, стероиды и имеют кольцевую структуру.Хотя они не похожи на другие липиды, они сгруппированы с ними, потому что они также гидрофобны. Все стероиды имеют четыре связанных углеродных кольца, а некоторые из них, как и холестерин, имеют короткий хвост.
Холестерин — стероид. Холестерин в основном синтезируется в печени и является предшественником многих стероидных гормонов, таких как тестостерон и эстрадиол. Он также является предшественником витаминов Е и К. Холестерин является предшественником солей желчных кислот, которые помогают в расщеплении жиров и их последующем усвоении клетками.Хотя о холестерине часто говорят отрицательно, он необходим для правильного функционирования организма. Это ключевой компонент плазматических мембран клеток животных.
Воски состоят из углеводородной цепи со спиртовой (–OH) группой и жирной кислотой. Примеры восков животного происхождения включают пчелиный воск и ланолин. У растений также есть воск, например покрытие на листьях, которое помогает предотвратить их высыхание.
Концепция в действии
Чтобы получить дополнительную информацию о липидах, исследуйте «Биомолекулы: Липиды» с помощью этой интерактивной анимации.
Белки являются одними из наиболее распространенных органических молекул в живых системах и обладают самым разнообразным набором функций среди всех макромолекул. Белки могут быть структурными, регуляторными, сократительными или защитными; они могут служить для транспортировки, хранения или перепонки; или они могут быть токсинами или ферментами. Каждая клетка живой системы может содержать тысячи различных белков, каждый из которых выполняет уникальную функцию. Их структуры, как и их функции, сильно различаются. Однако все они представляют собой полимеры аминокислот, расположенных в линейной последовательности.
Функции белков очень разнообразны, потому что существует 20 различных химически различных аминокислот, которые образуют длинные цепи, и аминокислоты могут располагаться в любом порядке. Например, белки могут функционировать как ферменты или гормоны. Ферменты , которые вырабатываются живыми клетками, являются катализаторами биохимических реакций (например, пищеварения) и обычно являются белками. Каждый фермент специфичен для субстрата (реагента, который связывается с ферментом), на который он действует. Ферменты могут разрушать молекулярные связи, переупорядочивать связи или образовывать новые связи.Примером фермента является амилаза слюны, которая расщепляет амилозу, компонент крахмала.
Гормоны представляют собой химические сигнальные молекулы, обычно белки или стероиды, секретируемые эндокринной железой или группой эндокринных клеток, которые контролируют или регулируют определенные физиологические процессы, включая рост, развитие, метаболизм и размножение. Например, инсулин — это белковый гормон, который поддерживает уровень глюкозы в крови.
Белки имеют разную форму и молекулярную массу; некоторые белки имеют глобулярную форму, тогда как другие имеют волокнистую природу.Например, гемоглобин — это глобулярный белок, а коллаген, обнаруженный в нашей коже, — это волокнистый белок. Форма белка имеет решающее значение для его функции. Изменения температуры, pH и воздействие химикатов могут привести к необратимым изменениям формы белка, что приведет к потере функции или денатурации (более подробно это будет обсуждаться позже). Все белки состоят из 20 одних и тех же аминокислот по-разному.
Аминокислоты — это мономеры, из которых состоят белки.Каждая аминокислота имеет одинаковую фундаментальную структуру, которая состоит из центрального атома углерода, связанного с аминогруппой (–NH 2 ), карбоксильной группы (–COOH) и атома водорода. Каждая аминокислота также имеет другой вариабельный атом или группу атомов, связанных с центральным атомом углерода, известную как группа R. Группа R — единственное различие в структуре между 20 аминокислотами; в остальном аминокислоты идентичны.
Рис. 2.21. Аминокислоты состоят из центрального углерода, связанного с аминогруппой (–Nh3), карбоксильной группой (–COOH) и атомом водорода.Четвертая связь центрального углерода варьируется среди различных аминокислот, как видно из этих примеров аланина, валина, лизина и аспарагиновой кислоты.Химическая природа группы R определяет химическую природу аминокислоты в ее белке (то есть, является ли она кислотной, основной, полярной или неполярной).
Последовательность и количество аминокислот в конечном итоге определяют форму, размер и функцию белка. Каждая аминокислота присоединена к другой аминокислоте ковалентной связью, известной как пептидная связь, которая образуется в результате реакции дегидратации.Карбоксильная группа одной аминокислоты и аминогруппа второй аминокислоты объединяются, высвобождая молекулу воды. Полученная связь представляет собой пептидную связь.
Продукты, образованные такой связью, называются полипептидами . Хотя термины полипептид и белок иногда используются взаимозаменяемо, полипептид технически представляет собой полимер аминокислот, тогда как термин белок используется для полипептида или полипептидов, которые объединились вместе, имеют различную форму и имеют уникальную функцию.
Эволюция в действии
Эволюционное значение цитохрома c Цитохром c является важным компонентом молекулярного механизма, который собирает энергию из глюкозы. Поскольку роль этого белка в производстве клеточной энергии имеет решающее значение, за миллионы лет он очень мало изменился. Секвенирование белков показало, что существует значительное сходство последовательностей между молекулами цитохрома с разных видов; эволюционные отношения можно оценить путем измерения сходства или различий между белковыми последовательностями различных видов.
Например, ученые определили, что цитохром с человека содержит 104 аминокислоты. Для каждой молекулы цитохрома с, которая к настоящему времени была секвенирована у разных организмов, 37 из этих аминокислот находятся в одном и том же положении в каждом цитохроме с. Это указывает на то, что все эти организмы произошли от общего предка. При сравнении последовательностей белков человека и шимпанзе различий в последовательностях не обнаружено. При сравнении последовательностей человека и макаки-резуса было обнаружено единственное различие в одной аминокислоте.Напротив, сравнение человека и дрожжей показывает разницу в 44 аминокислотах, предполагая, что люди и шимпанзе имеют более недавнего общего предка, чем люди и макака-резус или люди и дрожжи.
Структура белка
Как обсуждалось ранее, форма белка имеет решающее значение для его функции. Чтобы понять, как белок приобретает свою окончательную форму или конформацию, нам необходимо понять четыре уровня структуры белка: первичный, вторичный, третичный и четвертичный .
Уникальная последовательность и количество аминокислот в полипептидной цепи — это ее первичная структура. Уникальная последовательность каждого белка в конечном итоге определяется геном, кодирующим этот белок. Любое изменение в последовательности гена может привести к добавлению другой аминокислоты к полипептидной цепи, вызывая изменение структуры и функции белка. При серповидно-клеточной анемии β-цепь гемоглобина имеет единственную аминокислотную замену, вызывающую изменение как структуры, так и функции белка.Что наиболее примечательно, так это то, что молекула гемоглобина состоит из двух альфа-цепей и двух бета-цепей, каждая из которых состоит примерно из 150 аминокислот. Таким образом, молекула содержит около 600 аминокислот. Структурное различие между нормальной молекулой гемоглобина и молекулой серповидноклеточных клеток, которое резко снижает продолжительность жизни у пораженных людей, заключается в одной аминокислоте из 600.
Из-за этого изменения одной аминокислоты в цепи обычно двояковогнутые или дискообразные эритроциты принимают форму полумесяца или «серпа», что закупоривает артерии.Это может привести к множеству серьезных проблем со здоровьем, таких как одышка, головокружение, головные боли и боли в животе у людей, страдающих этим заболеванием.
Паттерны сворачивания, возникающие в результате взаимодействий между частями аминокислот, не принадлежащих к R-группам, приводят к вторичной структуре белка. Наиболее распространены альфа (α) -спиральные и бета (β) -пластинчатые листовые структуры. Обе структуры удерживаются в форме водородными связями. В альфа-спирали связи образуются между каждой четвертой аминокислотой и вызывают поворот аминокислотной цепи.
В β-складчатом листе «складки» образованы водородными связями между атомами в основной цепи полипептидной цепи. Группы R прикреплены к атомам углерода и проходят выше и ниже складок складки. Гофрированные сегменты выровнены параллельно друг другу, а водородные связи образуются между одинаковыми парами атомов на каждой из выровненных аминокислот. Структуры α-спирали и β-складчатых листов обнаруживаются во многих глобулярных и волокнистых белках.
Уникальная трехмерная структура полипептида известна как его третичная структура.Эта структура вызвана химическим взаимодействием между различными аминокислотами и участками полипептида. Прежде всего, взаимодействия между группами R создают сложную трехмерную третичную структуру белка. Могут быть ионные связи, образованные между группами R на разных аминокислотах, или водородные связи, помимо тех, которые участвуют во вторичной структуре. Когда происходит сворачивание белка, гидрофобные группы R неполярных аминокислот лежат внутри белка, тогда как гидрофильные группы R лежат снаружи.Первые типы взаимодействий также известны как гидрофобные взаимодействия.
В природе некоторые белки образованы из нескольких полипептидов, также известных как субъединицы, и взаимодействие этих субъединиц образует четвертичную структуру. Слабые взаимодействия между субъединицами помогают стабилизировать общую структуру. Например, гемоглобин представляет собой комбинацию четырех полипептидных субъединиц.
Рис. 2.22 На этих иллюстрациях можно увидеть четыре уровня белковой структуры.Каждый белок имеет свою уникальную последовательность и форму, удерживаемую химическими взаимодействиями.Если белок подвержен изменениям температуры, pH или воздействию химикатов, структура белка может измениться, потеряв свою форму в результате так называемой денатурации , как обсуждалось ранее. Денатурация часто обратима, потому что первичная структура сохраняется, если денатурирующий агент удаляется, позволяя белку возобновить свою функцию. Иногда денатурация необратима, что приводит к потере функции. Один из примеров денатурации белка можно увидеть, когда яйцо жарят или варят.Белок альбумина в жидком яичном белке денатурируется при помещении на горячую сковороду, превращаясь из прозрачного вещества в непрозрачное белое вещество. Не все белки денатурируются при высоких температурах; например, бактерии, которые выживают в горячих источниках, имеют белки, которые адаптированы для работы при этих температурах.
Концепция в действии
Чтобы получить дополнительную информацию о белках, исследуйте «Биомолекулы: Белки» с помощью этой интерактивной анимации.
Нуклеиновые кислоты являются ключевыми макромолекулами в непрерывности жизни.Они несут генетический план клетки и несут инструкции для функционирования клетки.
Двумя основными типами нуклеиновых кислот являются дезоксирибонуклеиновая кислота (ДНК) и рибонуклеиновая кислота (РНК) . ДНК — это генетический материал, содержащийся во всех живых организмах, от одноклеточных бактерий до многоклеточных млекопитающих.
Другой тип нуклеиновой кислоты, РНК, в основном участвует в синтезе белка. Молекулы ДНК никогда не покидают ядро, а вместо этого используют посредника РНК для связи с остальной частью клетки.Другие типы РНК также участвуют в синтезе белка и его регуляции.
ДНК и РНК состоят из мономеров, известных как нуклеотидов . Нуклеотиды объединяются друг с другом с образованием полинуклеотида, ДНК или РНК. Каждый нуклеотид состоит из трех компонентов: азотистого основания, пентозного (пятиуглеродного) сахара и фосфатной группы. Каждое азотистое основание в нуклеотиде присоединено к молекуле сахара, которая присоединена к фосфатной группе.
Рис. 2.23. Нуклеотид состоит из трех компонентов: азотистого основания, пентозного сахара и фосфатной группы. ДНКимеет двойную спиральную структуру. Он состоит из двух цепей или полимеров нуклеотидов. Нити образованы связями между фосфатными и сахарными группами соседних нуклеотидов. Нити связаны друг с другом в своих основаниях водородными связями, и нити наматываются друг на друга по своей длине, отсюда и описание «двойной спирали», что означает двойную спираль.
Рис. 2.24. Химическая структура ДНК с цветной меткой, обозначающей четыре основания, а также фосфатный и дезоксирибозный компоненты основной цепи.Чередующиеся сахарные и фосфатные группы лежат на внешней стороне каждой цепи, образуя основу ДНК. Азотистые основания сложены внутри, как ступени лестницы, и эти основания соединяются в пару; пары связаны друг с другом водородными связями. Основания спариваются таким образом, чтобы расстояние между скелетами двух цепей было одинаковым по всей длине молекулы. Правило состоит в том, что нуклеотид A соединяется с нуклеотидом T, а G — с C, см. Раздел 9.1 для более подробной информации.
Живые существа основаны на углероде, потому что углерод играет такую важную роль в химии живых существ. Четыре позиции ковалентной связи атома углерода могут дать начало широкому разнообразию соединений с множеством функций, что объясняет важность углерода для живых существ. Углеводы — это группа макромолекул, которые являются жизненно важным источником энергии для клетки, обеспечивают структурную поддержку многих организмов и могут быть обнаружены на поверхности клетки в качестве рецепторов или для распознавания клеток.Углеводы классифицируются как моносахариды, дисахариды и полисахариды, в зависимости от количества мономеров в молекуле.
Липиды — это класс макромолекул, которые по своей природе неполярны и гидрофобны. Основные типы включают жиры и масла, воски, фосфолипиды и стероиды. Жиры и масла представляют собой запасенную форму энергии и могут включать триглицериды. Жиры и масла обычно состоят из жирных кислот и глицерина.
Белки — это класс макромолекул, которые могут выполнять широкий спектр функций для клетки.Они помогают метаболизму, обеспечивая структурную поддержку и действуя как ферменты, переносчики или гормоны. Строительными блоками белков являются аминокислоты. Белки организованы на четырех уровнях: первичный, вторичный, третичный и четвертичный. Форма и функция белка неразрывно связаны; любое изменение формы, вызванное изменениями температуры, pH или химического воздействия, может привести к денатурации белка и потере функции.
Нуклеиновые кислоты — это молекулы, состоящие из повторяющихся единиц нуклеотидов, которые направляют клеточную деятельность, такую как деление клеток и синтез белка.Каждый нуклеотид состоит из пентозного сахара, азотистого основания и фосфатной группы. Есть два типа нуклеиновых кислот: ДНК и РНК.
аминокислота: мономер белка
углевод: биологическая макромолекула, в которой соотношение углерода, водорода и кислорода составляет 1: 2: 1; углеводы служат источниками энергии и структурной поддержкой в клетках
целлюлоза: полисахарид, который составляет клеточные стенки растений и обеспечивает структурную поддержку клетки
хитин: вид углеводов, образующих внешний скелет членистоногих, таких как насекомые и ракообразные, и клеточные стенки грибов
денатурация: потеря формы белка в результате изменений температуры, pH или воздействия химических веществ
дезоксирибонуклеиновая кислота (ДНК): двухцепочечный полимер нуклеотидов, несущий наследственную информацию клетки
дисахарид: два мономера сахара, которые связаны между собой пептидной связью
фермент : катализатор биохимической реакции, который обычно представляет собой сложный или конъюгированный белок
жир: липидная молекула, состоящая из трех жирных кислот и глицерина (триглицерида), которая обычно существует в твердой форме при комнатной температуре
гликоген: запасной углевод у животных
гормон: химическая сигнальная молекула, обычно белок или стероид, секретируемая эндокринной железой или группой эндокринных клеток; действия по контролю или регулированию определенных физиологических процессов
липиды: класс макромолекул, неполярных и нерастворимых в воде
макромолекула: большая молекула, часто образованная полимеризацией более мелких мономеров
моносахарид: отдельная единица или мономер углеводов
нуклеиновая кислота: биологическая макромолекула, несущая генетическую информацию клетки и инструкции для функционирования клетки
нуклеотид: мономер нуклеиновой кислоты; содержит пентозный сахар, фосфатную группу и азотистое основание
масло: ненасыщенный жир, являющийся жидкостью при комнатной температуре
фосфолипид: основной компонент мембран клеток; состоит из двух жирных кислот и фосфатной группы, присоединенной к основной цепи глицерина
полипептид: длинная цепь аминокислот, связанных пептидными связями
полисахарид: длинная цепь моносахаридов; могут быть разветвленными и неразветвленными
белок: биологическая макромолекула, состоящая из одной или нескольких цепочек аминокислот
рибонуклеиновая кислота (РНК): одноцепочечный полимер нуклеотидов, участвующий в синтезе белка
насыщенная жирная кислота: длинноцепочечный углеводород с одинарными ковалентными связями в углеродной цепи; количество атомов водорода, прикрепленных к углеродному скелету, максимально
крахмал: запасной углевод в растениях
стероид: тип липида, состоящего из четырех конденсированных углеводородных колец
транс-жиры: форма ненасыщенного жира с атомами водорода, соседствующими с двойной связью, напротив друг друга, а не на одной стороне двойной связи
триглицерид: молекула жира; состоит из трех жирных кислот, связанных с молекулой глицерина
ненасыщенная жирная кислота: длинноцепочечный углеводород, имеющий одну или несколько двойных связей в углеводородной цепи
Атрибуция в СМИ
Передайте привет своим внутренним молекулам | Биохимия и молекулярная биология
Я хотел бы показать вам вашу внутреннюю молекулу, но, честно говоря, я не думаю, что вам это интересно.Что довольно неприятно для таких ученых, как я, которые посвятили карьеру структурной биологии изучению того, как выглядят молекулы человеческой жизни. Вы знаете — белки, нуклеиновые кислоты, углеводы, липиды. То, из чего мы все сделаны.
Может показаться странным жаловаться на отсутствие интереса к нашей молекулярной природе, потому что люди, кажется, бесконечно очарованы — если не одержимы — ДНК, одной из самых известных биологических молекул всех времен. У нас нет проблем с пониманием его важности, как материала наших генов, в формировании нашей идентичности и опыта.Через эволюцию он связывает нас со всеми остальными живыми существами на Земле и является важной частью истории того, кем мы являемся. Наши индивидуальные истории могут принимать неприятные повороты, когда наши гены дают сбой в результате мутаций, вызывающих наследственные заболевания или рак. А в последнее время манипуляции с ДНК стали движущей силой увлекательного, хотя и спорного, бизнеса по генетической модификации животных и растений на наших фермах; сейчас обсуждаются даже изменения в ДНК человека, как показали недавние дебаты о переносе митохондрий и редактировании генома.
Но в случае с ДНК основное внимание уделяется идее генетики как объяснительной основы, а не самой молекуле. Вы можете сказать, что это так, потому что, как только кто-то упоминает продукты гена , бесчисленное множество белковых молекул, кодируемых генами, внезапно происходит отключение. Эти крохотные молекулярные машины выполняют широкий спектр задач внутри и вне живой клетки — включая синтез практически всех других интересных молекул в нашем теле — но даже в этом случае разговор заходит в тупик.Мы просто не говорим о белках. У большинства людей нет ощущения связи, несмотря на то, что для того, чтобы что-либо почувствовать, необходимы ионно-белковые каналы и рецепторы нейромедиаторов в нашем мозгу, передающие электрические и химические сигналы, составляющие мысль. Почему нас больше не интересуют молекулы, из которых мы состоим?
Думаю, мне не стоит жаловаться. Трудно полюбить молекулу белка. Трудно даже узнать одного. Они такие маленькие, что вряд ли вы когда-нибудь взглянете на них, если у вас нет доступа в лабораторию.Кажется несправедливым, что эти жизненно важные микромашины должны быть такими инкогнито.
Если бы я прямо сейчас попросил вас подумать о протеине, любом протеине, какая картина пришла бы вам в голову? Я не хочу быть осуждающим, но полагаю, что вы, возможно, ничего не сделали. Всем известно, как выглядит ДНК с ее такой элегантной двойной спиралью. Но как насчет миоглобина, первого белка, структура которого была разработана в трех измерениях — всего через несколько лет после того, как ДНК привлекла всеобщее внимание? Не такая уж знаменитость.
Отчасти проблема в плохом PR. Работа Джона Кендрю по выяснению структуры миоглобина, удобного хранилища кислорода в мышечных клетках, на самом деле была более впечатляющим научным достижением, чем определение ДНК (само по себе немаловажное достижение). Но в конечном продукте не было пиццы. Конечно, это было не зрелище. Вы можете убедиться в этом сами в лондонском Музее науки, где оригинальная модель атома, кропотливо построенная Кендрю в 1960 году, экспонируется в рамках выставки «Ученые Черчилля ».Его стоит посетить, если вы хотите познакомиться с одной из своих внутренних молекул. Модель миоглобина на дисплее от кашалота, но версия в вашем теле в основном выглядит идентично. (Это одна из умных и недооцененных особенностей структурной биологии: она выявляет сходства на молекулярном уровне, свидетельствующие об эволюционном единстве всех живых существ, на уровне даже более глубоком, чем соответствия между последовательностями ДНК.)
Выставлено в музее: Модель миоглобина Кендрю, похороненная в лесу прутьев. Фотография: Стивен Карри / Personal Collection. Может быть, это не красиво, но в модели Кендрю есть определенное величие.Он большой — около полутора метров по бокам — и фантастически детализирован. Каждый атом выставлен на обозрение. Однако это не совсем просто, потому что каркасная модель должна опираться на густой лес деревянных прутьев, а они, скорее, доминируют в процессе. Вы должны внимательно вглядываться, чтобы различить проволочные связи между атомами и понять, как молекула принимает форму. Со всех сторон вид затемнен и фрагментирован. Трудно понять, что внутри таится великолепная природная инженерия.
Но проблема не только в стержнях. Тысячи белковых структур, которые ежегодно выпадают из лабораторий, теперь могут быть мгновенно отображены в вашем веб-браузере. Вы можете зайти в банк данных белков (PDB), где они хранятся, и посмотреть. В последние годы PDB упорно работает над тем, чтобы сделать эти структуры доступными для неспециалистов, но мне интересно, сколько из них попадет?
Я подозреваю, что привлечь посетителей сложно, потому что большинство людей не чувствуют достаточной связи со своей молекулярной сущностью, чтобы иметь причину для исследования.Дело не только в внешности — значительную часть проблемы составляет сложность. Чтобы по-настоящему оценить большую биологическую молекулу, вам нужно кое-что знать о том, что она делает, и это часто требует изрядного количества химии. В любом случае предыстория полна загадочных подробностей. Модная компьютерная графика в наши дни может смягчить некоторые из сложных граней и сделать молекулу более дружелюбной и привлекательной, но этого недостаточно, если вы не можете понять, как белок вписывается в схему вещей.
Компьютерные представления белка (серый) и РНК (оранжевый и желтый) в молекулярном объятии (аминоацил тРНК синтетаза) Фотография: Стивен Карри / Personal CollectionСитуация еще больше усугубляется тем фактом, что молекулы часто обрабатываются и представлены миру по одному. Из-за этой изоляции может быть трудно понять суть вещи, не говоря уже о том, чтобы усвоить идею о том, что белок, на который вы смотрите, является частью вас.
Вот почему я такой поклонник работ Дэвида Гудселла, доцента молекулярной биологии в Исследовательском институте Скриппса в Калифорнии.В дополнение к своей повседневной работе в качестве ученого, он столкнулся со сложностью и изоляцией, присущими научному анализу бимолекулярной структуры, создав прекрасные картины клеточных внутренностей. Эти изображения помещают молекулы жизни в богатый и значимый контекст. Конечно, в его работах есть некоторая художественная лицензия, но она основана на последних научных достижениях — масштабы, формы и количество молекулярных участников этих живых ландшафтов основаны на самой лучшей доступной информации.Если вы хотите заглянуть внутрь себя в великолепных молекулярных деталях, я настоятельно рекомендую его иллюстрированную книгу The Machinery of Life , о которой я писал ранее.
Картина Дэвида Гудселла, изображающая клеточное ядро. Фотография: Дэвид Гудселл / http: //mgl.scripps.edu/people/goodsell/. Молекулярный мир становится еще более живым в анимациях Дрю Берри, биомедицинского аниматора из «Уолтера и Элизы». Институт медицинских исследований Холла в Мельбурне. Берри привнес поистине кинематографическое видение в изображение биологических молекул.Он приблизил нас ближе всего к тому, что мы когда-либо подошли к пониманию того, что действительно происходит на молекулярном уровне внутри клеток нашего тела — процессов, которые заставляют нас работать, таких как репликация ДНК, необходимая перед делением каждой клетки, или трансляция последовательности генов в белки, которые структурируют наши клетки и поддерживают биохимию жизни в движении. Здесь он выступает с докладом на TEDx в Сиднее в 2011 году, демонстрируя некоторые из своих лучших работ. Пожалуйста, посмотрите — анимация начинается в 2:48.
Дрю Берри рассказывает о своем искусстве и науке на TEDx Sydney, 2011Анимация Берри просто фантастическая.Как и Гудселл, он стремится привнести как можно больше строгости и научных подробностей в свои изображения махинаций жизни. (В сопроводительном посте он объясняет философию и процесс своей работы). Здесь впечатляющая точность в сочетании со страстью показать нам, что мы из себя представляем, на гранулированном уровне, выходящем за рамки наших чувств.
Сила этих анимаций в раскрытии нашей молекулярной сущности неоспорима. И все же … существует неизбежная уловка, которая поднимает еще один барьер между нами и нашими молекулярными компонентами.Белки и ДНК внутри нас невозможно увидеть даже в лучший световой микроскоп, поскольку они намного меньше длины волны света. Поэтому ученым приходится прибегать к причудливому набору косвенных методов, таких как рентгеновская кристаллография, ядерный магнитный резонанс или криоэлектронная микроскопия, чтобы получить данные, позволяющие реконструировать трехмерные молекулярные модели на компьютере. Ничего не видно напрямую, хотя мы можем быть уверены, что эти методы дают достаточно точные координаты атомов, чтобы определить, как устроены молекулы.В своих фильмах Берри может выбирать, как лучше всего визуализировать полученные структуры — с отдельными атомами в виде сфер или, возможно, просто отображать молекулярные поверхности — и раскрасить их, чтобы усилить различия между различными молекулярными частями и игроками (на самом деле, большинство белков являются довольно бесцветный). Эти решения вполне разумны и помогают нам увидеть, что происходит, но факт остается фактом: ни одно из использованных представлений не показывает, как на самом деле выглядят молекулы, потому что никто никогда их не видел.
Ничто из этого не умаляет работу Берри. Вы можете сказать из его выступления на TEDx, что он серьезно относится к этому делу. Как структурный биолог я ценю больше, чем другие, за то, на что он пошел, чтобы все исправить. Но даже несмотря на то, что я ежедневно погружаюсь в этот мир, есть одна последняя проблема с установлением связи с нашими внутренними молекулами, которую я обнаружил, наблюдая за осторожными, искусными анимациями Берри. Сколько бы раз я ни говорил себе, что весь механизм, изображающий его фильмы, работает каждую секунду каждого дня внутри каждой клетки моего тела, почему-то это все еще не кажется мне вполне реальным.То же самое и с тщательно продуманными научными картинами Гудселла. Сложность представленного шоу ошеломляет, но сразу же возникает тревожный вопрос: как, черт возьми, весь этот шебанг может продолжаться десятилетия человеческой жизни, не останавливаясь?
Разве это слишком много для разума, чтобы принять свою зависимость от стольких тысяч молекулярных столкновений — встреч, которые кажутся слепыми и механическими? Сталкивающие действия простых молекул неудобно сочетаются с моим ощущением себя как рационального агента, и, возможно, это в конечном итоге то, что разрушает любое глубоко укоренившееся чувство молекулярной самости.Не имеет значения, что я, , знаю, , что все эти молекулярные взаимодействия жизненно важны для жизни, что я, , знаю, , что они были сформированы и направлялись невидимой рукой эволюционного отбора на протяжении миллиардов лет, или что мне вполне комфортно. с моими эволюционными связями с историей жизни на Земле. Ничто из этого не помогает мне наладить отношения с моими внутренними молекулами, которые я могу чувствовать.
Здесь наблюдается серьезный когнитивный диссонанс, который беспокоит как в личном, так и в профессиональном плане.Несмотря на все мои годы работы в структурной биологии, кажется, что знания недостаточно.
@Stephen_Curry — разочарованный профессор структурной биологии Имперского колледжа.
Что такое молекулярная биология? | Thermo Fisher Scientific
*Выберите страну / regionUnited StatesCanadaAfghanistanAlbaniaAlgeriaAmerican SamoaAndorraAngolaAnguillaAntarcticaAntigua и BarbudaArgentinaArmeniaArubaAustraliaAustriaAzerbaijanBahamasBahrainBangladeshBarbadosBelarusBelgiumBelizeBeninBermudaBhutanBoliviaBosnia и HerzegovinaBotswanaBouvet IslandBrazilBritish Индийский океан TerritoryBrunei DarussalamBulgariaBurkina FasoBurundiCambodiaCameroonCape VerdeCayman IslandsCentral африканских RepublicChadChileChinaChristmas IslandCocos (Килинг) IslandsColombiaComorosCongoCongo, Демократическая Республика ofCook IslandsCosta RicaCote D’IvoireCroatiaCubaCyprusCzech RepublicDenmarkDjiboutiDominicaDominican RepublicEast TimorEcuadorEgyptEl SalvadorEquatorial GuineaEritreaEstoniaEthiopiaFalkland острова (Мальвинские ) Фарерские острова, Фиджи, Финляндия, Югославская Республика Македония, Франция, Французская Гвиана, Французская Полинезия, Южные территории Франции, Габон, Гамбия, Грузия, Германия, Гана, Гибралтар, Греция, Гренландия, Гренада, Гваделупа, Гуам, Гватемала, Подлинная aGuinea-BissauGuyanaHaitiHeard и McDonald IslandsHoly Престол (Ватикан) HondurasHong KongHungaryIcelandIndiaIndonesiaIran (Исламская Республика) IraqIrelandIsraelItalyJamaicaJapanJordanKazakstanKenyaKiribatiKorea, Корейские Народно-Демократической RepKorea, Республика ofKuwaitKyrgyzstanLao Народный Демократической RepLatviaLebanonLesothoLiberiaLibyan Arab JamahiriyaLiechtensteinLithuaniaLuxembourgMacauMadagascarMalawiMalaysiaMaldivesMaliMaltaMarshall IslandsMartiniqueMauritaniaMauritiusMayotteMexicoMicronesia, Федеративные StatesMoldova, Республика ofMonacoMongoliaMontserratMoroccoMozambiqueMyanmarNamibiaNauruNepalNetherlandsNetherlands AntillesNew CaledoniaNew ZealandNicaraguaNigerNigeriaNiueNorfolk IslandNorthern Mariana IslandsNorwayOmanPakistanPalauPanamaPapua Нового GuineaParaguayPeruPhilippinesPitcairnPolandPortugalPuerto RicoQatarReunionRomaniaRussian FederationRwandaSaint HelenaSaint Китс и НевисСент-ЛюсияСент-Пьер и МикелонСамоаСан-МариноСао-Томе и ПринсипиСаудовская АравияСенегалСейшельские островаSi ERRA LeoneSingaporeSlovakiaSloveniaSolomon IslandsSomaliaSouth AfricaSpainSri LankaSth Georgia & Sth Sandwich Институт социальных Винсент и GrenadinesSudanSurinameSvalbard и Ян MayenSwazilandSwedenSwitzerlandSyrian Arab RepublicTaiwan, провинция ChinaTajikistanTanzania, Объединенная Республика ofThailandTogoTokelauTongaTrinidad и TobagoTunisiaTurkeyTurkmenistanTurks и Кайкос IslandsTuvaluUgandaUkraineUnited Арабские EmiratesUnited KingdomUruguayUS Малые отдаленные IslandsUzbekistanVanuatuVenezuelaVietnamVirgin острова (Британские) Виргинские острова (U.S.) Острова Уоллис и ФутунаЗападная СахараЙеменЮгославияЗамбияЗимбабве
Биологические молекулы | Биология I
Цели обучения
К концу этого раздела вы сможете:
- Опишите, почему углерод имеет решающее значение для жизни
- Объясните влияние незначительных изменений аминокислот на организмы
- Опишите четыре основных типа биологических молекул
- Понимать функции четырех основных типов молекул
Большие молекулы, необходимые для жизни, которые состоят из более мелких органических молекул, называются биологическими макромолекулами.Существует четыре основных класса биологических макромолекул (углеводы, липиды, белки и нуклеиновые кислоты), каждый из которых является важным компонентом клетки и выполняет широкий спектр функций. Вместе эти молекулы составляют большую часть массы клетки. Биологические макромолекулы являются органическими, что означает, что они содержат углерод. Кроме того, они могут содержать водород, кислород, азот, фосфор, серу и дополнительные второстепенные элементы.
Часто говорят, что жизнь «основана на углероде.Это означает, что атомы углерода, связанные с другими атомами углерода или другими элементами, образуют фундаментальные компоненты многих, если не большинства, молекул, уникальных для живых существ. Другие элементы играют важную роль в биологических молекулах, но углерод определенно квалифицируется как элемент «фундамент» для молекул в живых существах. Это связывающие свойства атомов углерода, которые ответственны за его важную роль.
Рис. 1. Углерод может образовывать четыре ковалентные связи, образуя органическую молекулу.Самая простая молекула углерода — это метан (CH 4 ), изображенный здесь.
Углерод содержит четыре электрона во внешней оболочке. Следовательно, он может образовывать четыре ковалентные связи с другими атомами или молекулами. Простейшей молекулой органического углерода является метан (CH 4 ), в котором четыре атома водорода связаны с атомом углерода (рис. 1).
Однако более сложные конструкции изготавливаются с использованием углерода. Любой из атомов водорода может быть заменен другим атомом углерода, ковалентно связанным с первым атомом углерода.Таким образом могут быть образованы длинные и разветвленные цепи углеродных соединений (рис. 2a ). Атомы углерода могут связываться с атомами других элементов, таких как азот, кислород и фосфор (рис. 2b ). Молекулы также могут образовывать кольца, которые сами могут связываться с другими кольцами (рис. 2 c ). Это разнообразие молекулярных форм объясняет разнообразие функций биологических макромолекул и в значительной степени основано на способности углерода образовывать множественные связи с самим собой и другими атомами.
Рис. 2. Эти примеры показывают три молекулы (обнаруженные в живых организмах), которые содержат атомы углерода, различным образом связанные с другими атомами углерода и атомами других элементов. (а) Эта молекула стеариновой кислоты имеет длинную цепочку атомов углерода. (б) Глицин, компонент белков, содержит атомы углерода, азота, кислорода и водорода. (c) Глюкоза, сахар, имеет кольцо из атомов углерода и один атом кислорода.
Углеводы — это макромолекулы, с которыми большинство потребителей знакомо.Чтобы похудеть, некоторые люди придерживаются «низкоуглеводной» диеты. Спортсмены, напротив, часто «нагружают углеводы» перед важными соревнованиями, чтобы убедиться, что у них достаточно энергии для соревнований на высоком уровне. Фактически, углеводы являются неотъемлемой частью нашего рациона; злаки, фрукты и овощи — все это естественные источники углеводов. Углеводы обеспечивают организм энергией, в частности, через глюкозу, простой сахар. Углеводы также выполняют другие важные функции у людей, животных и растений.
Углеводы можно представить формулой (CH 2 O) n , где n — количество атомов углерода в молекуле. Другими словами, соотношение углерода, водорода и кислорода в молекулах углеводов составляет 1: 2: 1. Углеводы подразделяются на три подтипа: моносахариды, дисахариды и полисахариды.
Моносахариды (моно- = «один»; sacchar- = «сладкий») представляют собой простые сахара, наиболее распространенным из которых является глюкоза.В моносахаридах количество атомов углерода обычно составляет от трех до шести. Большинство названий моносахаридов оканчиваются суффиксом -ose. В зависимости от количества атомов углерода в сахаре они могут быть известны как триозы (три атома углерода), пентозы (пять атомов углерода) и гексозы (шесть атомов углерода).
Моносахариды могут существовать в виде линейной цепи или кольцевых молекул; в водных растворах они обычно находятся в кольцевой форме.
Химическая формула глюкозы: C 6 H 12 O 6 .У большинства живых существ глюкоза является важным источником энергии. Во время клеточного дыхания из глюкозы выделяется энергия, которая используется для выработки аденозинтрифосфата (АТФ). Растения синтезируют глюкозу, используя углекислый газ и воду в процессе фотосинтеза, а глюкоза, в свою очередь, используется для удовлетворения потребностей растений в энергии. Избыток синтезированной глюкозы часто хранится в виде крахмала, который расщепляется другими организмами, которые питаются растениями.
Рисунок 3.Глюкоза, галактоза и фруктоза являются изомерными моносахаридами, что означает, что они имеют одинаковую химическую формулу, но немного разные структуры.
Галактоза (входит в состав лактозы или молочного сахара) и фруктоза (содержится во фруктах) — другие распространенные моносахариды. Хотя глюкоза, галактоза и фруктоза имеют одинаковую химическую формулу (C 6 H 12 O 6 ), они различаются структурно и химически (и известны как изомеры) из-за разного расположения атомов в углеродной цепи. (Рисунок 3).
Дисахариды (ди- = «два») образуются, когда два моносахарида подвергаются реакции дегидратации (реакции, при которой происходит удаление молекулы воды). Во время этого процесса гидроксильная группа (–OH) одного моносахарида соединяется с атомом водорода другого моносахарида, высвобождая молекулу воды (H 2 O) и образуя ковалентную связь между атомами в двух молекулах сахара.
Обычные дисахариды включают лактозу, мальтозу и сахарозу. Лактоза — это дисахарид, состоящий из мономеров глюкозы и галактозы.Он содержится в молоке. Мальтоза, или солодовый сахар, представляет собой дисахарид, образующийся в результате реакции дегидратации между двумя молекулами глюкозы. Наиболее распространенным дисахаридом является сахароза или столовый сахар, который состоит из мономеров глюкозы и фруктозы.
Длинная цепь моносахаридов, связанных ковалентными связями, известна как полисахарид (поли- = «много»). Цепь может быть разветвленной или неразветвленной, и она может содержать разные типы моносахаридов. Полисахариды могут быть очень большими молекулами.Крахмал, гликоген, целлюлоза и хитин являются примерами полисахаридов.
Крахмал — это хранимая в растениях форма сахаров, состоящая из амилозы и амилопектина (оба полимера глюкозы). Растения способны синтезировать глюкозу, а избыток глюкозы откладывается в виде крахмала в различных частях растений, включая корни и семена. Крахмал, который потребляется животными, расщепляется на более мелкие молекулы, такие как глюкоза. Затем клетки могут поглощать глюкозу.
Гликоген — это форма хранения глюкозы у людей и других позвоночных, состоящая из мономеров глюкозы.Гликоген является животным эквивалентом крахмала и представляет собой сильно разветвленную молекулу, обычно хранящуюся в клетках печени и мышц. Когда уровень глюкозы снижается, гликоген расщепляется с высвобождением глюкозы.
Целлюлоза — один из самых распространенных природных биополимеров. Клеточные стенки растений в основном состоят из целлюлозы, которая обеспечивает структурную поддержку клетки. Дерево и бумага в основном целлюлозные по своей природе. Целлюлоза состоит из мономеров глюкозы, которые связаны связями между определенными атомами углерода в молекуле глюкозы.
Каждый второй мономер глюкозы в целлюлозе переворачивается и плотно упаковывается в виде удлиненных длинных цепей. Это придает целлюлозе жесткость и высокую прочность на разрыв, что так важно для растительных клеток. Целлюлоза, проходящая через нашу пищеварительную систему, называется пищевыми волокнами. Хотя связи глюкозы и глюкозы в целлюлозе не могут быть разрушены пищеварительными ферментами человека, травоядные животные, такие как коровы, буйволы и лошади, способны переваривать траву, богатую целлюлозой, и использовать ее в качестве источника пищи.У этих животных определенные виды бактерий обитают в рубце (часть пищеварительной системы травоядных) и секретируют фермент целлюлазу. В аппендиксе также содержатся бактерии, которые расщепляют целлюлозу, что придает ей важную роль в пищеварительной системе жвачных животных. Целлюлазы могут расщеплять целлюлозу на мономеры глюкозы, которые могут использоваться животным в качестве источника энергии.
Углеводы выполняют другие функции у разных животных. У членистоногих, таких как насекомые, пауки и крабы, есть внешний скелет, называемый экзоскелетом, который защищает их внутренние части тела.Этот экзоскелет состоит из биологической макромолекулы хитина, азотистого углевода. Он состоит из повторяющихся единиц модифицированного сахара, содержащего азот.
Таким образом, из-за различий в молекулярной структуре углеводы могут выполнять самые разные функции хранения энергии (крахмал и гликоген), а также структурной поддержки и защиты (целлюлоза и хитин) (рис. 4).
Рис. 4. Хотя их структура и функции различаются, все полисахаридные углеводы состоят из моносахаридов и имеют химическую формулу (CH 2 O) n .
Карьера в действии
Зарегистрированный диетолог
Ожирение является проблемой здравоохранения во всем мире, и многие болезни, такие как диабет и болезни сердца, становятся все более распространенными из-за ожирения. Это одна из причин, почему к зарегистрированным диетологам все чаще обращаются за советом. Зарегистрированные диетологи помогают планировать пищевые продукты и программы питания для людей в различных условиях. Они часто работают с пациентами в медицинских учреждениях, разрабатывая планы питания для профилактики и лечения заболеваний.Например, диетологи могут научить пациента с диабетом контролировать уровень сахара в крови, употребляя в пищу правильные типы и количества углеводов. Диетологи также могут работать в домах престарелых, школах и частных клиниках.
Чтобы стать дипломированным диетологом, нужно получить как минимум степень бакалавра в области диетологии, питания, пищевых технологий или в смежных областях. Кроме того, дипломированные диетологи должны пройти программу стажировки под руководством и сдать национальный экзамен. Те, кто занимается диетологией, проходят курсы по питанию, химии, биохимии, биологии, микробиологии и физиологии человека.Диетологи должны стать экспертами в химии и функциях пищи (белков, углеводов и жиров).
Рис. 5. Гидрофобные липиды в мехе водных млекопитающих, таких как речная выдра, защищают их от непогоды. (кредит: Кен Босма)
Липиды включают разнообразную группу соединений, объединенных общим признаком. Липиды гидрофобны («водобоязненные») или нерастворимы в воде, потому что они неполярные молекулы. Это потому, что они являются углеводородами, которые включают только неполярные углерод-углеродные или углерод-водородные связи.Липиды выполняют в клетке множество различных функций. Клетки хранят энергию для длительного использования в виде липидов, называемых жирами. Липиды также обеспечивают изоляцию растений и животных от окружающей среды. Например, они помогают водным птицам и млекопитающим оставаться сухими из-за их водоотталкивающих свойств. Липиды также являются строительными блоками многих гормонов и важной составляющей плазматической мембраны. Липиды включают жиры, масла, воски, фосфолипиды и стероиды.
Молекула жира, такая как триглицерид, состоит из двух основных компонентов — глицерина и жирных кислот.Глицерин — это органическое соединение с тремя атомами углерода, пятью атомами водорода и тремя гидроксильными (–OH) группами. Жирные кислоты имеют длинную цепь углеводородов, к которой присоединена кислая карбоксильная группа, отсюда и название «жирная кислота». Количество атомов углерода в жирной кислоте может составлять от 4 до 36; наиболее распространены те, которые содержат 12–18 атомов углерода. В молекуле жира жирная кислота присоединена к каждому из трех атомов кислорода в -ОН-группах молекулы глицерина ковалентной связью (рис. 6).
Рисунок 6.Липиды включают жиры, такие как триглицериды, которые состоят из жирных кислот и глицерина, фосфолипидов и стероидов.
Во время образования этой ковалентной связи высвобождаются три молекулы воды. Три жирные кислоты в жире могут быть похожими или разными. Эти жиры также называют триглицеридами, потому что они содержат три жирные кислоты. Некоторые жирные кислоты имеют общие названия, указывающие на их происхождение. Например, пальмитиновая кислота, насыщенная жирная кислота, получают из пальмы. Арахидовая кислота получена из Arachis hypogaea , научного названия арахиса.
Жирные кислоты могут быть насыщенными и ненасыщенными. В цепи жирной кислоты, если есть только одинарные связи между соседними атомами углерода в углеводородной цепи, жирная кислота является насыщенной. Насыщенные жирные кислоты насыщены водородом; другими словами, количество атомов водорода, прикрепленных к углеродному скелету, максимально.
Когда углеводородная цепь содержит двойную связь, жирная кислота является ненасыщенной жирной кислотой.
Большинство ненасыщенных жиров являются жидкими при комнатной температуре и называются маслами.Если в молекуле есть одна двойная связь, то он известен как мононенасыщенный жир (например, оливковое масло), а если имеется более одной двойной связи, то он известен как полиненасыщенный жир (например, масло канолы).
Насыщенные жиры плотно упаковываются и остаются твердыми при комнатной температуре. Животные жиры со стеариновой кислотой и пальмитиновой кислотой, содержащиеся в мясе, и жир с масляной кислотой, содержащиеся в масле, являются примерами насыщенных жиров. Млекопитающие хранят жиры в специализированных клетках, называемых адипоцитами, где жировые шарики занимают большую часть клетки.У растений жир или масло хранятся в семенах и используются в качестве источника энергии во время эмбрионального развития.
Ненасыщенные жиры или масла обычно растительного происхождения и содержат ненасыщенные жирные кислоты. Двойная связь вызывает изгиб или «перегиб», который препятствует плотной упаковке жирных кислот, сохраняя их жидкими при комнатной температуре. Оливковое масло, кукурузное масло, масло канолы и жир печени трески являются примерами ненасыщенных жиров. Ненасыщенные жиры помогают повысить уровень холестерина в крови, тогда как насыщенные жиры способствуют образованию бляшек в артериях, что увеличивает риск сердечного приступа.
Рис. 7. В процессе гидрогенизации ориентация двойных связей изменяется, в результате чего из цис-жира образуется транс-жир. Это изменяет химические свойства молекулы.
В пищевой промышленности масла искусственно гидрогенизируются для придания им полутвердого состояния, что приводит к меньшей порче и увеличению срока хранения. Проще говоря, газообразный водород пропускают через масла, чтобы отвердить их. Во время этого процесса гидрирования двойные связи цис -конформации в углеводородной цепи могут быть преобразованы в двойные связи в транс- -конформации.В результате образуется транс -жир из цис- -жира. Ориентация двойных связей влияет на химические свойства жира (рис. 7).
Маргарин, некоторые виды арахисового масла и шортенинг являются примерами искусственно гидрогенизированных транс -жиров. Недавние исследования показали, что увеличение транс -жиров в рационе человека может привести к увеличению уровня липопротеинов низкой плотности (ЛПНП) или «плохого» холестерина, что, в свою очередь, может привести к отложению бляшек в организме человека. артерии, что приводит к болезни сердца.Многие рестораны быстрого питания недавно отказались от использования транс--жиров, и теперь в США на этикетках продуктов питания требуется указывать содержание транс--жиров.
Незаменимые жирные кислоты — это жирные кислоты, которые необходимы, но не синтезируются человеческим организмом. Следовательно, их необходимо дополнять с помощью диеты. Омега-3 жирные кислоты попадают в эту категорию и являются одной из двух известных незаменимых жирных кислот для человека (другая — омега-6 жирные кислоты). Они представляют собой тип полиненасыщенных жиров и называются омега-3 жирными кислотами, потому что третий углерод на конце жирной кислоты участвует в двойной связи.
Лосось, форель и тунец являются хорошими источниками жирных кислот омега-3. Жирные кислоты омега-3 важны для работы мозга, нормального роста и развития. Они также могут предотвратить сердечные заболевания и снизить риск рака.
Как и углеводы, жиры получили широкую огласку. Это правда, что чрезмерное употребление жареной и другой «жирной» пищи приводит к увеличению веса. Однако жиры выполняют важные функции. Жиры служат долгосрочным накопителем энергии. Они также обеспечивают изоляцию тела.Поэтому «здоровые» ненасыщенные жиры в умеренных количествах следует употреблять регулярно.
Фосфолипиды являются основным компонентом плазматической мембраны. Как и жиры, они состоят из цепей жирных кислот, прикрепленных к глицерину или подобной основной цепи. Однако вместо трех жирных кислот есть две жирные кислоты, а третий углерод глицериновой цепи связан с фосфатной группой. Фосфатная группа модифицируется добавлением спирта.
Фосфолипид имеет как гидрофобные, так и гидрофильные участки.Цепи жирных кислот гидрофобны и исключаются из воды, тогда как фосфат гидрофильный и взаимодействует с водой.
Клетки окружены мембраной, которая имеет бислой фосфолипидов. Жирные кислоты фосфолипидов обращены внутрь, от воды, тогда как фосфатная группа может быть обращена либо к внешней среде, либо к внутренней части клетки, которые оба являются водными.
Стероиды и воски
В отличие от фосфолипидов и жиров, рассмотренных ранее, стероиды имеют кольцевую структуру.Хотя они не похожи на другие липиды, они сгруппированы с ними, потому что они также гидрофобны. Все стероиды имеют четыре связанных углеродных кольца, а некоторые из них, как и холестерин, имеют короткий хвост.
Холестерин — стероид. Холестерин в основном синтезируется в печени и является предшественником многих стероидных гормонов, таких как тестостерон и эстрадиол. Он также является предшественником витаминов Е и К. Холестерин является предшественником солей желчных кислот, которые помогают в расщеплении жиров и их последующем усвоении клетками.Хотя о холестерине часто говорят отрицательно, он необходим для правильного функционирования организма. Это ключевой компонент плазматических мембран клеток животных.
Воски состоят из углеводородной цепи со спиртовой (–OH) группой и жирной кислотой. Примеры восков животного происхождения включают пчелиный воск и ланолин. У растений также есть воск, например покрытие на листьях, которое помогает предотвратить их высыхание.
Концепция в действии Чтобы получить дополнительную информацию о липидах, исследуйте «Биомолекулы: Липиды» с помощью этой интерактивной анимации.Белки являются одними из наиболее распространенных органических молекул в живых системах и обладают самым разнообразным набором функций среди всех макромолекул. Белки могут быть структурными, регуляторными, сократительными или защитными; они могут служить для транспортировки, хранения или перепонки; или они могут быть токсинами или ферментами. Каждая клетка живой системы может содержать тысячи различных белков, каждый из которых выполняет уникальную функцию. Их структуры, как и их функции, сильно различаются. Однако все они представляют собой полимеры аминокислот, расположенных в линейной последовательности.
Функции белков очень разнообразны, потому что существует 20 различных химически различных аминокислот, которые образуют длинные цепи, и аминокислоты могут располагаться в любом порядке. Например, белки могут функционировать как ферменты или гормоны. Ферменты, которые вырабатываются живыми клетками, являются катализаторами биохимических реакций (например, пищеварения) и обычно являются белками. Каждый фермент специфичен для субстрата (реагента, который связывается с ферментом), на который он действует. Ферменты могут разрушать молекулярные связи, переупорядочивать связи или образовывать новые связи.Примером фермента является амилаза слюны, которая расщепляет амилозу, компонент крахмала.
Гормоны — это химические сигнальные молекулы, обычно белки или стероиды, секретируемые эндокринной железой или группой эндокринных клеток, которые контролируют или регулируют определенные физиологические процессы, включая рост, развитие, метаболизм и размножение. Например, инсулин — это белковый гормон, который поддерживает уровень глюкозы в крови.
Рис. 8. Аминокислоты состоят из центрального углерода, связанного с аминогруппой (–NH 2 ), карбоксильной группой (–COOH) и атомом водорода.Четвертая связь центрального углерода варьируется среди различных аминокислот, как видно из этих примеров аланина, валина, лизина и аспарагиновой кислоты.
Белки имеют разную форму и молекулярную массу; некоторые белки имеют глобулярную форму, тогда как другие имеют волокнистую природу. Например, гемоглобин — это глобулярный белок, а коллаген, обнаруженный в нашей коже, — это волокнистый белок. Форма белка имеет решающее значение для его функции. Изменения температуры, pH и воздействие химикатов могут привести к необратимым изменениям формы белка, что приведет к потере функции или денатурации (более подробно это будет обсуждаться позже).Все белки состоят из 20 одних и тех же аминокислот по-разному.
Аминокислоты — это мономеры, из которых состоят белки. Каждая аминокислота имеет одинаковую фундаментальную структуру, которая состоит из центрального атома углерода, связанного с аминогруппой (–NH 2 ), карбоксильной группы (–COOH) и атома водорода. Каждая аминокислота также имеет другой вариабельный атом или группу атомов, связанных с центральным атомом углерода, известную как группа R. Группа R — единственное различие в структуре между 20 аминокислотами; в остальном аминокислоты идентичны (рис. 8).
Химическая природа группы R определяет химическую природу аминокислоты в ее белке (то есть, является ли она кислотной, основной, полярной или неполярной).
Последовательность и количество аминокислот в конечном итоге определяют форму, размер и функцию белка. Каждая аминокислота присоединена к другой аминокислоте ковалентной связью, известной как пептидная связь, которая образуется в результате реакции дегидратации. Карбоксильная группа одной аминокислоты и аминогруппа второй аминокислоты объединяются, высвобождая молекулу воды.Полученная связь представляет собой пептидную связь.
Продукты, образованные такой связью, называются полипептидами. Хотя термины полипептид и белок иногда используются взаимозаменяемо, полипептид технически представляет собой полимер аминокислот, тогда как термин белок используется для полипептида или полипептидов, которые объединились вместе, имеют различную форму и имеют уникальную функцию.
Эволюция в действии
Эволюционное значение цитохрома c
Цитохром c — важный компонент молекулярного механизма, который извлекает энергию из глюкозы.Поскольку роль этого белка в производстве клеточной энергии имеет решающее значение, за миллионы лет он очень мало изменился. Секвенирование белков показало, что существует значительное сходство последовательностей между молекулами цитохрома с разных видов; эволюционные отношения можно оценить путем измерения сходства или различий между белковыми последовательностями различных видов.
Например, ученые определили, что цитохром с человека содержит 104 аминокислоты. Для каждой молекулы цитохрома с, которая к настоящему времени была секвенирована у разных организмов, 37 из этих аминокислот находятся в одном и том же положении в каждом цитохроме с.Это указывает на то, что все эти организмы произошли от общего предка. При сравнении последовательностей белков человека и шимпанзе различий в последовательностях не обнаружено. При сравнении последовательностей человека и макаки-резуса было обнаружено единственное различие в одной аминокислоте. Напротив, сравнение человека и дрожжей показывает разницу в 44 аминокислотах, предполагая, что люди и шимпанзе имеют более недавнего общего предка, чем люди и макака-резус или люди и дрожжи.
Структура белка
Как обсуждалось ранее, форма белка имеет решающее значение для его функции.Чтобы понять, как белок приобретает свою окончательную форму или конформацию, нам необходимо понять четыре уровня структуры белка: первичный, вторичный, третичный и четвертичный (рис. 8).
Уникальная последовательность и количество аминокислот в полипептидной цепи — это ее первичная структура. Уникальная последовательность каждого белка в конечном итоге определяется геном, кодирующим этот белок. Любое изменение в последовательности гена может привести к добавлению другой аминокислоты к полипептидной цепи, вызывая изменение структуры и функции белка.При серповидно-клеточной анемии β-цепь гемоглобина имеет единственную аминокислотную замену, вызывающую изменение как структуры, так и функции белка. Что наиболее примечательно, так это то, что молекула гемоглобина состоит из двух альфа-цепей и двух бета-цепей, каждая из которых состоит примерно из 150 аминокислот. Таким образом, молекула содержит около 600 аминокислот. Структурная разница между нормальной молекулой гемоглобина и молекулой серповидноклеточных клеток, которая резко снижает продолжительность жизни, состоит в одной из 600 аминокислот.
Из-за этого изменения одной аминокислоты в цепи обычно двояковогнутые или дискообразные эритроциты принимают форму полумесяца или «серпа», что закупоривает артерии. Это может привести к множеству серьезных проблем со здоровьем, таких как одышка, головокружение, головные боли и боли в животе у людей, страдающих этим заболеванием.
Паттерны сворачивания, возникающие в результате взаимодействий между частями аминокислот, не принадлежащих к R-группам, приводят к вторичной структуре белка. Наиболее распространены альфа (α) -спиральные и бета (β) -пластинчатые листовые структуры.Обе структуры удерживаются в форме водородными связями. В альфа-спирали связи образуются между каждой четвертой аминокислотой и вызывают поворот аминокислотной цепи.
В β-складчатом листе «складки» образованы водородными связями между атомами в основной цепи полипептидной цепи. Группы R прикреплены к атомам углерода и проходят выше и ниже складок складки. Гофрированные сегменты выровнены параллельно друг другу, а водородные связи образуются между одинаковыми парами атомов на каждой из выровненных аминокислот.Структуры α-спирали и β-складчатых листов обнаруживаются во многих глобулярных и волокнистых белках.
Уникальная трехмерная структура полипептида известна как его третичная структура. Эта структура вызвана химическим взаимодействием между различными аминокислотами и участками полипептида. Прежде всего, взаимодействия между группами R создают сложную трехмерную третичную структуру белка. Могут быть ионные связи, образованные между группами R на разных аминокислотах, или водородные связи, помимо тех, которые участвуют во вторичной структуре.Когда происходит сворачивание белка, гидрофобные группы R неполярных аминокислот лежат внутри белка, тогда как гидрофильные группы R лежат снаружи. Первые типы взаимодействий также известны как гидрофобные взаимодействия.
В природе некоторые белки образованы из нескольких полипептидов, также известных как субъединицы, и взаимодействие этих субъединиц образует четвертичную структуру. Слабые взаимодействия между субъединицами помогают стабилизировать общую структуру. Например, гемоглобин представляет собой комбинацию четырех полипептидных субъединиц.
Рис. 9. На этих иллюстрациях можно увидеть четыре уровня белковой структуры. (кредит: модификация работы Национального исследовательского института генома человека)
Каждый белок имеет свою уникальную последовательность и форму, удерживаемую химическими взаимодействиями. Если белок подвержен изменениям температуры, pH или воздействию химикатов, структура белка может измениться, потеряв свою форму в результате так называемой денатурации, как обсуждалось ранее. Денатурация часто обратима, потому что первичная структура сохраняется, если денатурирующий агент удаляется, позволяя белку возобновить свою функцию.Иногда денатурация необратима, что приводит к потере функции. Один из примеров денатурации белка можно увидеть, когда яйцо жарят или варят. Белок альбумина в жидком яичном белке денатурируется при помещении на горячую сковороду, превращаясь из прозрачного вещества в непрозрачное белое вещество. Не все белки денатурируются при высоких температурах; например, бактерии, которые выживают в горячих источниках, имеют белки, которые адаптированы для работы при этих температурах.
Концепция в действииЧтобы получить дополнительную информацию о белках, исследуйте «Биомолекулы: Белки» с помощью этой интерактивной анимации.
Нуклеиновые кислоты являются ключевыми макромолекулами в непрерывной жизни. Они несут генетический план клетки и несут инструкции для функционирования клетки.
Двумя основными типами нуклеиновых кислот являются дезоксирибонуклеиновая кислота (ДНК) и рибонуклеиновая кислота (РНК). ДНК — это генетический материал, содержащийся во всех живых организмах, от одноклеточных бактерий до многоклеточных млекопитающих.
Другой тип нуклеиновой кислоты, РНК, в основном участвует в синтезе белка.Молекулы ДНК никогда не покидают ядро, а вместо этого используют посредника РНК для связи с остальной частью клетки. Другие типы РНК также участвуют в синтезе белка и его регуляции.
Рис. 10. Нуклеотид состоит из трех компонентов: азотистого основания, пентозного сахара и фосфатной группы.
ДНК и РНК состоят из мономеров, известных как нуклеотиды. Нуклеотиды объединяются друг с другом с образованием полинуклеотида, ДНК или РНК. Каждый нуклеотид состоит из трех компонентов: азотистого основания, пентозного (пятиуглеродного) сахара и фосфатной группы (рис. 10).Каждое азотистое основание в нуклеотиде присоединено к молекуле сахара, которая присоединена к фосфатной группе.
Другой тип нуклеиновой кислоты, РНК, в основном участвует в синтезе белка. Молекулы ДНК никогда не покидают ядро, а вместо этого используют посредника РНК для связи с остальной частью клетки. Другие типы РНК также участвуют в синтезе белка и его регуляции.
ДНК и РНК состоят из мономеров, известных как нуклеотиды. Нуклеотиды объединяются друг с другом с образованием полинуклеотида, ДНК или РНК.Каждый нуклеотид состоит из трех компонентов: азотистого основания, пентозного (пятиуглеродного) сахара и фосфатной группы (рис. 10). Каждое азотистое основание в нуклеотиде присоединено к молекуле сахара, которая присоединена к фосфатной группе.
Рис. 11. Модель двойной спирали показывает ДНК как две параллельные нити переплетающихся молекул. (кредит: Джером Уокер, Деннис Мытс)
ДНКимеет двойную спиральную структуру (рис. 11). Он состоит из двух цепей или полимеров нуклеотидов.Нити образованы связями между фосфатными и сахарными группами соседних нуклеотидов. Нити связаны друг с другом в своих основаниях водородными связями, и нити наматываются друг на друга по своей длине, отсюда и описание «двойной спирали», что означает двойную спираль.
Чередующиеся сахарные и фосфатные группы лежат на внешней стороне каждой цепи, образуя основу ДНК. Азотистые основания сложены внутри, как ступени лестницы, и эти основания соединяются в пару; пары связаны друг с другом водородными связями.Основания спариваются таким образом, чтобы расстояние между скелетами двух цепей было одинаковым по всей длине молекулы.
Сводка раздела
Живые существа основаны на углероде, потому что углерод играет такую важную роль в химии живых существ. Четыре позиции ковалентной связи атома углерода могут дать начало широкому разнообразию соединений с множеством функций, что объясняет важность углерода для живых существ. Углеводы — это группа макромолекул, которые являются жизненно важным источником энергии для клетки, обеспечивают структурную поддержку многих организмов и могут быть обнаружены на поверхности клетки в качестве рецепторов или для распознавания клеток.Углеводы классифицируются как моносахариды, дисахариды и полисахариды, в зависимости от количества мономеров в молекуле.
Липиды — это класс макромолекул, которые по своей природе неполярны и гидрофобны. Основные типы включают жиры и масла, воски, фосфолипиды и стероиды. Жиры и масла представляют собой запасенную форму энергии и могут включать триглицериды. Жиры и масла обычно состоят из жирных кислот и глицерина.
Белки — это класс макромолекул, которые могут выполнять широкий спектр функций для клетки.Они помогают метаболизму, обеспечивая структурную поддержку и действуя как ферменты, переносчики или гормоны. Строительными блоками белков являются аминокислоты. Белки организованы на четырех уровнях: первичный, вторичный, третичный и четвертичный. Форма и функция белка неразрывно связаны; любое изменение формы, вызванное изменениями температуры, pH или химического воздействия, может привести к денатурации белка и потере функции.
Нуклеиновые кислоты — это молекулы, состоящие из повторяющихся единиц нуклеотидов, которые направляют клеточную деятельность, такую как деление клеток и синтез белка.Каждый нуклеотид состоит из пентозного сахара, азотистого основания и фосфатной группы. Есть два типа нуклеиновых кислот: ДНК и РНК.
Дополнительные упражнения для самопроверки
1. Объясните, по крайней мере, три функции, которые липиды выполняют у растений и / или животных.
2. Объясните, что происходит, если в полипептидной цепи даже одна аминокислота заменяется другой. Приведите конкретный пример.
ответов
1. Жир служит для животных ценным способом сохранения энергии.Он также может обеспечить изоляцию. Фосфолипиды и стероиды — важные компоненты клеточных мембран.
2. Изменение последовательности гена может привести к добавлению другой аминокислоты к полипептидной цепи вместо нормальной. Это вызывает изменение структуры и функции белка. Например, при серповидно-клеточной анемии β-цепь гемоглобина имеет единственную аминокислотную замену. Из-за этого изменения дискообразные эритроциты принимают форму полумесяца, что может привести к серьезным проблемам со здоровьем.
Глоссарий
структура альфа-спирали (α-спираль) тип вторичной структуры белков, образованный сворачиванием полипептида в форму спирали с водородными связями, стабилизирующими структуру
аминокислота мономера белка; имеет центральный углерод или альфа-углерод, к которому присоединены аминогруппа, карбоксильная группа, водород и R-группа или боковая цепь; группа R различна для всех 20 аминокислот
бета-складчатый лист (β-складчатый) вторичная структура, обнаруженная в белках, в которой «складки» образованы водородными связями между атомами в основной цепи полипептидной цепи
углевод биологическая макромолекула, в которой отношение углерода к водороду и к кислороду составляет 1: 2: 1; углеводы служат источниками энергии и структурной опорой в клетках и образуют клеточный экзоскелет членистоногих
целлюлоза полисахарид, составляющий клеточную стенку растений; обеспечивает структурную поддержку ячейки
шаперон (также шаперонин) белок, который помогает возникающему белку в процессе сворачивания
хитин тип углеводов, образующих внешний скелет всех членистоногих, включая ракообразных и насекомых; он также образует клеточные стенки грибов
денатурация потеря формы белка в результате изменений температуры, pH или воздействия химических веществ
дисахарид два мономера сахара, которые связаны вместе гликозидной связью
фермент катализатор в биохимической реакции, который обычно представляет собой сложный или конъюгированный белок
гликоген запасной углевод у животных
гликозидная связь связь, образованная реакцией дегидратации между двумя моносахаридами с отщеплением молекулы воды
гормон химическая сигнальная молекула, обычно белок или стероид, секретируемая эндокринными клетками, которые контролируют или регулируют определенные физиологические процессы
липид макромолекула, неполярная и нерастворимая в воде
моносахарид отдельное звено или мономер углеводов
омега-жир тип полиненасыщенных жиров, необходимых организму; нумерация углеродного омега начинается с метильного конца или конца, наиболее удаленного от карбонового конца
пептидная связь связь, образованная между двумя аминокислотами в результате реакции дегидратации
фосфолипид основной компонент мембран; состоит из двух жирных кислот и фосфатсодержащей группы, присоединенной к основной цепи глицерина
полипептид длинная цепь аминокислот, связанных пептидными связями
полисахарид длинная цепь моносахаридов; могут быть разветвленными и неразветвленными
первичная структура линейная последовательность аминокислот в белке
белок биологическая макромолекула, состоящая из одной или нескольких цепочек аминокислот
четвертичная структура ассоциация дискретных полипептидных субъединиц в белке
насыщенная жирная кислота длинная цепь углеводорода с одинарными ковалентными связями в углеродной цепи; количество атомов водорода, прикрепленных к углеродному скелету, максимально
вторичная структура регулярная структура, образованная белками за счет внутримолекулярной водородной связи между атомом кислорода одного аминокислотного остатка и водородом, присоединенным к атому азота другого аминокислотного остатка
крахмал запасные углеводы в растениях
стероид тип липида, состоящий из четырех конденсированных углеводородных колец, образующих плоскую структуру
третичная структура трехмерная конформация белка, включая взаимодействия между вторичными структурными элементами; образуется в результате взаимодействия между боковыми цепями аминокислот
транс-жир жир, образованный искусственно путем гидрогенизации масел, приводящий к другому расположению двойных связей, чем те, которые содержатся в природных липидах
триацилглицерин (также триглицерид) молекула жира; состоит из трех жирных кислот, связанных с молекулой глицерина
ненасыщенная жирная кислота длинноцепочечный углеводород, имеющий одну или несколько двойных связей в углеводородной цепи
воск липид, состоящий из длинноцепочечной жирной кислоты, этерифицированной до длинноцепочечного спирта; служит защитным покрытием на некоторых перьях, мехе водных млекопитающих и листьях
Устройство и функции
Структура макромолекул определяет функцию и регуляцию
Студенты должны уметь объяснять и применять основные концепции макромолекулярной структуры и функции, включая природу биологических макромолекул, их взаимодействие с водой, взаимосвязь между структурой и функцией, а также часто встречающиеся механизмы регулирования их функции.
Цели обучения, указанные ниже, подразделяются на вводные A, промежуточные B и верхние C.
1. Биологические макромолекулы большие и сложные
Макромолекулы состоят из основных молекулярных единиц. Они включают белки (полимеры аминокислот), нуклеиновые кислоты (полимеры нуклеотидов), углеводы (полимеры сахаров) и липиды (с различными модульными составляющими). Биосинтез и разложение биологических макромолекул включает линейную полимеризацию, стадии разрушения (белки, нуклеиновые кислоты и липиды), а также могут включать разветвление / разветвление (углеводы).Эти процессы могут включать мультибелковые комплексы (например, рибосомы, протеасомы) со сложной регуляцией.
Связанные цели обучения
- Учащиеся должны уметь обсуждать разнообразие и сложность различных биологически значимых макромолекул и макромолекулярных ансамблей с точки зрения эволюционной пригодности. A
- Учащиеся должны уметь описывать основные единицы макромолекул и типы связей между ними. A
- Учащиеся должны уметь сравнивать и противопоставлять процессы, участвующие в биосинтезе основных типов макромолекул (белков, нуклеиновых кислот и углеводов).B
- Учащиеся должны уметь сравнивать и противопоставлять процессы, участвующие в деградации основных типов макромолекул (белков, нуклеиновых кислот и углеводов).
- Студенты должны понимать, что белки состоят из доменов, и уметь обсуждать, как семейства белков возникают в результате дублирования первичного гена. C
2. Структура определяется несколькими факторами
Ковалентные и нековалентные связи определяют трехмерные структуры белков и нуклеиновых кислот, влияющие на их функцию.Аминокислотные последовательности, наблюдаемые в природе, тщательно отбираются по биологической функции, но не обязательно имеют уникальную складчатую структуру. Структура (и, следовательно, функция) макромолекул регулируется основополагающими принципами химии, такими как ковалентные связи и полярность, вращения и колебания связей, нековалентные взаимодействия, гидрофобный эффект и динамические аспекты молекулярной структуры. Последовательность (и, следовательно, структура и функция) белков и нуклеиновых кислот могут быть изменены путем альтернативного сплайсинга, мутации или химической модификации.Последовательности (и, следовательно, структура и функция) макромолекул могут развиваться, создавая измененные или новые биологические активности.
Связанные цели обучения
- Учащиеся должны уметь распознавать повторяющиеся единицы в биологических макромолекулах и уметь обсуждать структурные воздействия вовлеченных ковалентных и нековалентных взаимодействий. A
- Учащиеся должны уметь обсуждать состав, эволюционные изменения и, следовательно, структурное разнообразие различных типов биологических макромолекул, обнаруженных в организмах.A
- Студенты должны уметь обсуждать химические и физические отношения между составом и структурой макромолекул. A
- Студенты должны уметь сравнивать и противопоставлять первичные, вторичные, третичные и четвертичные структуры белков и нуклеиновых кислот. B
- Студенты должны уметь использовать различные подходы биоинформатики для анализа первичной последовательности и структуры макромолекул. B
- Учащиеся должны уметь сравнивать и противопоставлять эффекты химической модификации конкретных аминокислот на трехмерную структуру белка.B
- Учащиеся должны уметь сравнивать и противопоставлять способы, которыми конкретная макромолекула может принимать новые функции в результате эволюционных изменений. B
- Студенты должны уметь использовать различные биоинформатические и вычислительные подходы для сравнения первичных последовательностей и определения влияния сохранения и / или эволюционных изменений на структуру и функцию макромолекул. C
- Учащиеся должны уметь предсказывать влияние мутаций на активность, структуру или стабильность белка и разрабатывать соответствующие эксперименты для оценки эффектов мутаций.C
- Учащиеся должны уметь предлагать подходящие химические или химические биологические подходы для изучения локализации и взаимодействия биологических макромолекул. C
- Учащиеся должны уметь обсуждать, как мутации дублированного гена создают функциональное разнообразие. C
- Учащиеся должны уметь оценивать химический и энергетический вклад в соответствующие уровни структуры макромолекулы и прогнозировать влияние конкретных изменений структуры на динамические свойства молекулы.C
3. Структура и функции взаимосвязаны
Макромолекулы взаимодействуют с другими молекулами, используя множество нековалентных взаимодействий. Специфичность и сродство этих взаимодействий имеют решающее значение для биологической функции. Некоторые макромолекулы катализируют химические реакции или способствуют физическим процессам (например, молекулярному переносу), позволяя им протекать в условиях окружающей среды. Эти процессы могут быть количественно описаны с помощью законов скорости и термодинамических принципов (например,грамм. теория столкновений, теория переходного состояния, законы скорости и равновесия, эффекты температуры и структуры и химической реакционной способности, закон Кулона, законы движения Ньютона, энергия и стабильность, трение, диффузия, термодинамика и концепция случайности и вероятности).
Связанные цели обучения
- Учащиеся должны уметь использовать механистические рассуждения, чтобы объяснить, как фермент или рибозим катализирует определенную реакцию. A
- Студенты должны уметь обсуждать основы различных типов ферментативных механизмов.A
- Студенты должны уметь рассчитывать ферментативные уровни и сравнивать их, а также соотносить эти показатели с гомеостазом клеток или организма. B
- Студенты должны уметь обсуждать различные методы, которые можно использовать для определения аффинности и стехиометрии комплекса лиганд-макромолекула, и соотносить результаты как с термодинамическими, так и с кинетическими данными. B
- Студенты должны уметь критически оценивать вклад в специфичность в комплексе лиганд-макромолекула и планировать эксперименты для оценки вкладов в специфичность и проверки гипотез о специфичности лиганда в комплексе.C
- Учащиеся должны уметь предсказывать биологические и химические эффекты мутации или структурных изменений лиганда на аффинность связывания и планировать соответствующие эксперименты для проверки своих прогнозов. C
4. Макромолекулярные взаимодействия
Взаимодействия между макромолекулами и другими молекулами основаны на тех же слабых нековалентных взаимодействиях, которые играют главную роль в стабилизации трехмерных структур самих макромолекул.Важны гидрофобный эффект, ионные взаимодействия и взаимодействия водородных связей. Структурная организация взаимодействующих химических групп в сайте связывания или активном сайте придает этим взаимодействиям высокую степень специфичности. Специфичность и сродство этих взаимодействий имеют решающее значение для биологической функции.
Связанные цели обучения
- Учащиеся должны уметь обсуждать влияние изменений специфичности или аффинности на биологическую функцию и любое потенциальное эволюционное влияние.A
- Студенты должны уметь обсуждать различные методы, которые можно использовать для определения сродства и стехиометрии для комплекса лиганд-макромолекула, и соотносить результаты как с термодинамическими, так и с кинетическими данными. B
- Учащиеся должны уметь обсуждать взаимодействия между различными биологическими молекулами (включая белки, нуклеиновые кислоты, липиды, углеводы, мелкие органические вещества и т. Д.) И описывать, как эти взаимодействия влияют на специфичность или сродство, приводя к изменениям биологической функции.B
- Учащиеся должны уметь предсказать влияние мутации или структурного изменения лиганда на сродство связывания и спланировать соответствующие эксперименты для проверки своих прогнозов. C
- Учащиеся должны уметь обсуждать взаимосвязь между температурой, необходимой для денатурации (Tm), и структурой макромолекул. C
5. Структура макромолекул динамична
Макромолекулярная структура динамична в широком диапазоне временных масштабов, и динамические структурные изменения, большие и малые, часто имеют решающее значение для биологической функции.Небольшие изменения могут проявляться в виде локализованных молекулярных колебаний, которые могут облегчить доступ малых молекул к внутренним частям макромолекулы. Большие конформационные изменения могут происходить в виде движений различных макромолекулярных доменов относительно друг друга, чтобы облегчить катализ или другие формы работы. Белки могут содержать внутренне неструктурированные домены. Отсутствие структуры в растворе может способствовать функции, при которой взаимодействия должны происходить беспорядочно с несколькими другими молекулами.Динамическая структура макромолекул делает возможными быстрые изменения, влияющие на гомеостаз биохимических и молекулярно-биологических процессов.
Связанные цели обучения
- Учащиеся должны уметь обсуждать временные масштабы различных конформационных эффектов в биологических макромолекулах А и планировать соответствующие эксперименты для исследования изменений конформации и динамики, вызванных лигандом. C
- Учащиеся должны уметь обсуждать структурную основу динамических свойств макромолекул и предсказывать эффекты изменений динамических свойств A, которые могут возникнуть в результате изменения первичной последовательности.C
- Учащиеся должны уметь предсказать, является ли последовательность упорядоченной или неупорядоченной C, и обсудить потенциальную роль неупорядоченных областей белков. B
- Студенты должны уметь критически обсуждать доказательства за и против роли динамики в функции макромолекул. C
6. Биологическая активность макромолекул часто регулируется
Биологическая активность макромолекул часто регулируется одним или несколькими иерархическими способами (например,грамм. ингибиторы, активаторы, модификаторы, синтез, разложение и компартментализация).
Связанные цели обучения
- Учащиеся должны уметь сравнивать и противопоставлять различные механизмы регуляции функции макромолекулы, ферментативной реакции или пути. A
- Студенты должны уметь аллостерически обсуждать преимущества и недостатки регулирования реакции. B
- Студенты должны уметь обсуждать примеры аллостерической регуляции, ковалентной регуляции и изменений на уровне генов макромолекулярной структуры-функции.B
- Студенты должны использовать экспериментальные данные для оценки типа регуляции в ответ на гомотропные или гетеротропные лиганды на макромолекуле. C
- Учащиеся должны уметь создавать модели, объясняющие регуляцию структуры-функции макромолекул. C
- Учащиеся должны уметь описывать, как эволюция повлияла на регуляцию макромолекул и процессов. C
- Студенты должны уметь описывать, как изменения клеточного гомеостаза влияют на сигнальные и регуляторные молекулы и промежуточные продукты метаболизма.C
7. Структура (и, следовательно, функция) макромолекул регулируется основополагающими принципами химии и физики
Структура (и, следовательно, функция) макромолекул регулируется основополагающими принципами химии (включая ковалентные связи и полярность; вращения и колебания связей; водородные связи и нековалентные взаимодействия; гидрофобный эффект; динамические аспекты молекулярной структуры; теория столкновений ; теория переходного состояния; законы скорости и равновесия; эффекты температуры и структуры и химической реактивности) и физика (включая закон Кулона; законы движения Ньютона; энергия и стабильность; трение; диффузия; термодинамика; а также концепция случайности и вероятности). .
Связанные цели обучения
- Учащиеся должны уметь связывать основные принципы законов скорости и равновесия с реакциями и взаимодействиями и вычислять соответствующие термодинамические параметры для реакций и взаимодействий. A
- Студенты должны быть в состоянии объяснить, как лиганд, введенный в раствор, содержащий макромолекулу, с которой он может связываться, взаимодействует с макромолекулой. A
- Учащиеся должны уметь объяснять, используя основные принципы, влияние температуры на реакцию, катализируемую ферментами.B
- Учащиеся должны уметь обсуждать динамические свойства макромолекул, используя фундаментальные принципы физики. B
8. Для наблюдения и количественного измерения структуры, динамики и функции биологических макромолекул могут использоваться различные экспериментальные и вычислительные подходы
Для наблюдения и количественного измерения структуры, динамики и функции биологических макромолекул можно использовать различные экспериментальные и вычислительные подходы.Уравнения можно выводить из моделей и использовать для прогнозирования результатов или анализа данных. Данные можно анализировать статистически, чтобы оценить правильность модели и надежность данных.
Связанные цели обучения
- Учащиеся должны уметь предложить схему очистки для конкретной молекулы в смеси с учетом биофизических свойств различных молекул в смеси. B
- Студенты должны уметь либо предлагать эксперименты, которые определяют четвертичную структуру молекулы, либо уметь интерпретировать данные, относящиеся к третичной и четвертичной структуре молекул.B
- Студенты должны быть в состоянии объяснить, как вычислительные подходы могут быть использованы для изучения взаимодействий белок-лиганд, и обсудить, как результаты таких вычислений могут быть исследованы экспериментально. C
- Студенты должны уметь сравнивать и противопоставлять доступные вычислительные подходы, чтобы предложить трехмерную структуру макромолекулы, и обсудить, как предложенная структура может быть подтверждена экспериментально. C
- Учащиеся должны уметь анализировать кинетические или связывающие данные для получения соответствующих параметров и оценки достоверности модели, используемой для описания явления.C
Биомолекула — обзор | Темы ScienceDirect
Введение
Биомолекулы, такие как ферменты, антитела, аффинные белки, лиганды клеточных рецепторов и лекарственные средства всех видов, были иммобилизованы на поверхностях биоматериалов и внутри них для широкого спектра терапевтических, диагностических, регенерации тканей, разделения и биопроцессов. Приложения. Иммобилизация гепарина на полимерных поверхностях — один из самых ранних примеров биологически функционального биоматериала с модифицированной поверхностью (Gott et al., 1963). Живые клетки также можно комбинировать с биоматериалами, особенно когда их поверхности содержат пептиды или белки клеточной адгезии, а области клеточной культуры, искусственных органов и тканевой инженерии включают важные примеры взаимодействий клетка-поверхность. Эти «гибридные» комбинации натуральных и синтетических материалов придают синтетическому биоматериалу «биологическую функциональность». Многие разделы и главы в этом учебнике охватывают различные аспекты этой темы, включая адсорбцию белков и адгезию клеток и бактерий на поверхностях биоматериалов, не обрастающих поверхностях, культуру клеток, тканевую инженерию, искусственные органы, доставку лекарств и другие; В этой главе основное внимание будет уделено методологии, включающей физическую адсорбцию и химическую иммобилизацию биомолекул на поверхности биоматериалов, особенно для приложений, требующих биологической активности иммобилизованной биомолекулы.
Среди различных классов биоматериалов, которые могут быть биологически модифицированы, синтетические полимеры особенно интересны, потому что их поверхности могут содержать реактивные группы, такие как –OH, –COOH или NH 2 группы, или они могут быть легко модифицированы другими реактивными группами такие как азидные, алкиновые и SH-группы. Все эти группы можно использовать для ковалентного связывания биомолекул.
Еще одно преимущество полимеров в качестве носителей для биомолекул состоит в том, что полимеры можно изготавливать во многих формах, включая пленки, мембраны, трубки, волокна, ткани, частицы, капсулы и пористые структуры.Кроме того, макромолекулярные структуры также могут существенно различаться. Последние могут включать гомополимеры, статистические, чередующиеся, блок-сополимеры и привитые сополимеры, гиперразветвленные (гребенчатые) и звездообразные структуры (см. Главу I.2.2 о полимерах).
Методы живой анионной полимеризации, наряду с новыми методами живой свободнорадикальной полимеризации, теперь обеспечивают точный контроль молекулярной массы с узким распределением. Молекулярные формы твердых полимеров включают несшитые цепи, которые нерастворимы в физиологических условиях, поперечно-сшитые сети, физические смеси и взаимопроникающие сети (IPN) (e.г., Пискин и Хоффман, 1986; см. также главу I.2.2). «Умные» полимеры резко реагируют на поведение растворимости на стимулы, такие как температура, pH и концентрация соли (см. Главу I.2.11 «Умные» полимеры).
Для поверхностей из металлов, оксидов металлов, неорганических стекол или керамики биологическая функциональность иногда может быть добавлена через химически иммобилизованный или физически адсорбированный полимерный или поверхностно-активный адгезионный слой, или с использованием таких методов, как плазменный газовый разряд, коронный разряд в воздухе или озон для модификации поверхностных полимерных композиций с помощью функциональных групп (см. также главу I.2.12). Несколько исследователей применили химию клея мидий, основанную на самоконденсации дофамина, для образования плотных связывающих слоев полидофамина на различных поверхностях, включая металлы, оксиды металлов и стекло (Lee et al., 2007; Ku et al., 2010) . Аминные группы в этих полимерах могут быть дополнительно функционализированы биомолекулами.
Что такое ячейка? | Изучайте науку в Scitable
Как упоминалось ранее, цитоплазма клетки содержит множество функциональных и структурных элементов.Эти элементы существуют в форме молекул и органелл — представьте их как инструменты, приспособления и внутренние помещения клетки. Основные классы внутриклеточных органических молекул включают нуклеиновые кислоты, белки, углеводы и липиды, все из которых необходимы для функций клетки.
Нуклеиновые кислоты — это молекулы, которые содержат и помогают выражать генетический код клетки. Существует два основных класса нуклеиновых кислот: дезоксирибонуклеиновая кислота (ДНК) и рибонуклеиновая кислота (РНК) .ДНК — это молекула, которая содержит всю информацию, необходимую для построения и поддержания клетки; РНК выполняет несколько функций, связанных с выражением информации, хранящейся в ДНК. Конечно, сами по себе нуклеиновые кислоты не отвечают за сохранение и экспрессию генетического материала: клетки также используют белки, чтобы помочь реплицировать геном и осуществить глубокие структурные изменения, лежащие в основе деления клеток .
Белки — это второй тип внутриклеточных органических молекул.Эти вещества состоят из цепочек более мелких молекул, называемых аминокислотами , и они выполняют множество функций в клетке, как каталитических, , так и структурных. Например, белки, называемые ферментами , преобразуют клеточные молекулы (будь то белки, углеводы, липиды или нуклеиновые кислоты) в другие формы, которые могут помочь клетке удовлетворить свои потребности в энергии, построить поддерживающие структуры или выкачать отходы.
Углеводы , крахмалы и сахара в клетках, являются еще одним важным типом органических молекул. Простые углеводы используются для удовлетворения немедленных потребностей клетки в энергии, тогда как сложных углеводов служат в качестве внутриклеточных хранилищ энергии. Сложные углеводы также находятся на поверхности клетки, где они играют решающую роль в распознавании клеток.
Наконец, липидов или молекул жира являются компонентами клеточных мембран — как плазматической мембраны, так и различных внутриклеточных мембран. Они также участвуют в хранении энергии, а также в передаче сигналов внутри клеток и из кровотока внутрь клетки (рис. 2).
Некоторые клетки также имеют упорядоченное расположение молекул, называемых органеллами . Подобно комнатам в доме, эти структуры отделены от остального интерьера клетки собственной внутриклеточной мембраной. Органеллы содержат высокотехнологичное оборудование, необходимое для выполнения определенных работ внутри клетки. Одним из примеров является митохондрия , широко известная как «энергетическая установка» клетки, которая представляет собой органеллу, которая удерживает и поддерживает механизмы, участвующие в химических реакциях, производящих энергию (рис. 3).
Рисунок 2: Состав бактериальной клетки
Большая часть клетки состоит из воды (70%). Остальные 30% содержат различные пропорции структурных и функциональных молекул.
Рис. 3. Относительный масштаб биологических молекул и структур
Клетки могут варьироваться от 1 микрометра (мкм) до сотен микрометров в диаметре.

