Материал из целлюлозы многократно поменял форму от погружения в воду
Материаловеды из Германии и Китая предложили аналог пластика, которому можно придать любую форму, просто опустив в воду. Новый материал состоит из возобновляемого сырья — целюлозы. а изделия из него можно перерабатывать много раз, после причем после десяти циклов формования они даже становятся прочнее. Результаты исследования опубликованы в журнале Nature Sustainability.
Ежегодно
человечество
производит
более
360 миллионов тонн различных
изделий из пластика,
причем
200
миллионов тонн приходится
на упаковку и другие предметы с коротким
сроком использования.
С
переработкой
пластиковых
изделий
у
нас все еще большие трудности.
Большинство
популярных пластиковых
материалов
— ПЭТ,
полиэтилен,
полипропилен
и
некоторые другие — относятся к
термопластам, то есть переходят
в пластичное состояние при нагревании
и снова затвердевают при охлаждении.
Чтобы переработать
изделия
из
термопластов,
их
нагревают до
нескольких сот градусов Цельсия. Это
требует
больших затрат энергии, поэтому
такая
переработка не
всегда экономически выгодна.
Это
требует
больших затрат энергии, поэтому
такая
переработка не
всегда экономически выгодна.
Китайские и немецкие материаловеды под руководством Кая Чжана (Kai Zhang) научились управлять пластичностью полимеров более простым способом — просто опуская их в воду. За основу материала Чжан и его коллеги взяли природный полимер целлюлозу. Смешав ее с хлоридом коричной кислоты в присутствии основания они получили циннамат целлюлозы (cellulose cinnamate, CCi) — полимер, в котором часть гидроксильных групп в целлюлозных фрагментах превратили в сложноэфирный фрагмент c остатком коричной кислоты. Затем из CCi изготовили прямоугольные ленты размером и толщиной 10-20 микрометров. В воде такие ленты становились гибкими и пластичными и их можно было сгибать и закручивать в любом направлении. А когда ленты извлекали, из воды пластичность снижалась и форма изделия фиксировались.
Такие
свойства повышения
пластичности в воде
есть и у самой целлюлозы, но авторы
усилили их, внедрив фрагмент
коричной кислоты. Все
дело в
более
эффективном
транспорте
молекул воды,
который позволяет воде
быстро проникать внутрь материала.
После извлечения из воды молекулы так
же быстро продвигаются
из глубины материала к поверхности и
испаряются
— таким
образом форма изделий быстро фиксируется.
Все
дело в
более
эффективном
транспорте
молекул воды,
который позволяет воде
быстро проникать внутрь материала.
После извлечения из воды молекулы так
же быстро продвигаются
из глубины материала к поверхности и
испаряются
— таким
образом форма изделий быстро фиксируется.
Авторы работы изготовили из CCi лент пять изделий разной формы, которые оказались стабильны на воздухе и сохраняли свою форму в течение как минимум шестнадцати месяцев. После использования ленты можно снова сделать пластичным и придать им другую форму. Для этого не требуется нагревание — достаточно опустить изделие в воду комнатной температуры на пять минут, причем цикл с одной лентой можно повторять много раз.
Гидропластик
имеет отличную
механическую прочность:
предел
прочности
на разрыв 92,4 ± 2,2 мегапаскалей,
модуль
Юнга
2,6 ± 0,1 гигапаскалей
и
удлинением
при разрыве 15,2 ± 1,8 процентов. После пяти
циклов
формования
прочность немного
снижается, но затем
снова идет
вверх,
и после
десятого цикла
становится даже выше, чем в начале:
предел
прочности
на разрыв
повышается до 120.
Чжан и его коллеги полагают, что на основе CСi можно будет создавать и другие материалы, меняющие пластичность под действием растворителей. Такие материалы смогут стать альтернативой традиционным видам пластика, особенно если удастся заменить воду на другие менее распространенные растворители.
Для
того, чтобы уменьшить экологический
след пластиковой упаковки ученые пробуют
разные методы: не только синтезируют
новые материалы, но и ищут более
эффективные пути переработки для уже
известных пластиков. Еще
одна альтернатива термомеханической
переработке пластика — химическая
переработка. В этом случае молекулу
полимера разбирают на составные части,
превращая его в смесь мономеров. Полученные
продукты можно использовать для синтеза
новых полимеров или для других целей.
Например,
в прошлом месяце шотландские химики
получили
модифицированный
штамм кишечной палочки
Полученные
продукты можно использовать для синтеза
новых полимеров или для других целей.
Например,
в прошлом месяце шотландские химики
получили
модифицированный
штамм кишечной палочки
Наталия Самойлова
Нашли опечатку? Выделите фрагмент и нажмите Ctrl+Enter.
В Германии создали вещество для расщепления воды на кислород и водород подобно растениям — Газета.Ru
В Германии создали вещество для расщепления воды на кислород и водород подобно растениям — Газета.Ru | Новости
close
100%
Ученые разработали вещество, способное расщеплять молекулы воды на водород и кислород. Статья об этом опубликована в Nature Catalysis.
Работа была проведена Франком Вюртнером из Вюрцбургского университета. Он и его научная группа в течение многих лет работают над искусственным воспроизведением фотосистемы-II, которая в растениях связана с разложением воды в ходе фотосинтеза. Несколько лет назад им удалось создать сложную химическую систему из нескольких различных молекул на базе ионов рутения и органических веществ, которая была способна разлагать молекулы воды.
Несколько лет назад им удалось создать сложную химическую систему из нескольких различных молекул на базе ионов рутения и органических веществ, которая была способна разлагать молекулы воды.
В ходе этой работы исследователям пришла в голову идея сделать из рутения искусственный фермент для разложения воды. Это было невозможно без нового каталитического центра, способного взять на себя функции сразу нескольких молекул из прошлой работы.
Руководствуясь этой идеей, ученые изучили то, как органические молекулы, окружающие атомы рутения, влияют на характер взаимодействий между водой и центром катализатора. Благодаря этому авторам удалось подобрать требуемую форму трехмерной «оболочки» вокруг ионов рутения, которая заставляла молекулы воды принять оптимальное положение для расщепления.
Впоследствии профессор Вюртнер и его коллеги синтезировали две разных формы этого катализатора, а также детально изучили их структуру и работу на практике. Эти опыты показали, что синтетический фермент действительно способен активно расщеплять воду столь же быстро, как это делает фотосистема-II.
Подобная технология может пригодиться для водородной энергетики, поскольку сейчас основную массу водорода извлекают из природного газа.
Ранее геологи спрогнозировали образование единого суперконтинента через 300 млн лет.
Подписывайтесь на «Газету.Ru» в Новостях, Дзен и Telegram.
Чтобы сообщить об ошибке, выделите текст и нажмите Ctrl+Enter
Новости
Дзен
Telegram
Анастасия Миронова
Дичь за МКАДом
Зачем заставлять студентов ездить по России
Юлия Меламед
Умер отец всех популистов
О тайнах популярности Сильвио Берлускони
Георгий Бовт
Когда загрызут – тогда и приходите
Помогут ли штрафы ответственному обращению с домашними животными
Марина Ярдаева
Уравниловка или база?
О преимуществах единой образовательной программы в школах
Дмитрий Самойлов
Мутное пойло
Что привело к массовому отравлению сидром в России
Вода — Энергетическое образование
Энергетическое образованиеМеню навигации
ИСТОЧНИКИ ЭНЕРГИИ ИСПОЛЬЗОВАНИЕ ЭНЕРГИИ ЭНЕРГЕТИЧЕСКОЕ ВОЗДЕЙСТВИЕИНДЕКС
Поиск
Рисунок 1. Изображение общего количества воды в мире. Большой пузырь — это вся вода (в основном соленая вода), второй пузырь — это вся пресная вода, а маленький крошечный пузырь к югу от него — это вода в озерах и реках. Вода — это молекула, состоящая из одного атома кислорода и двух атомов водорода.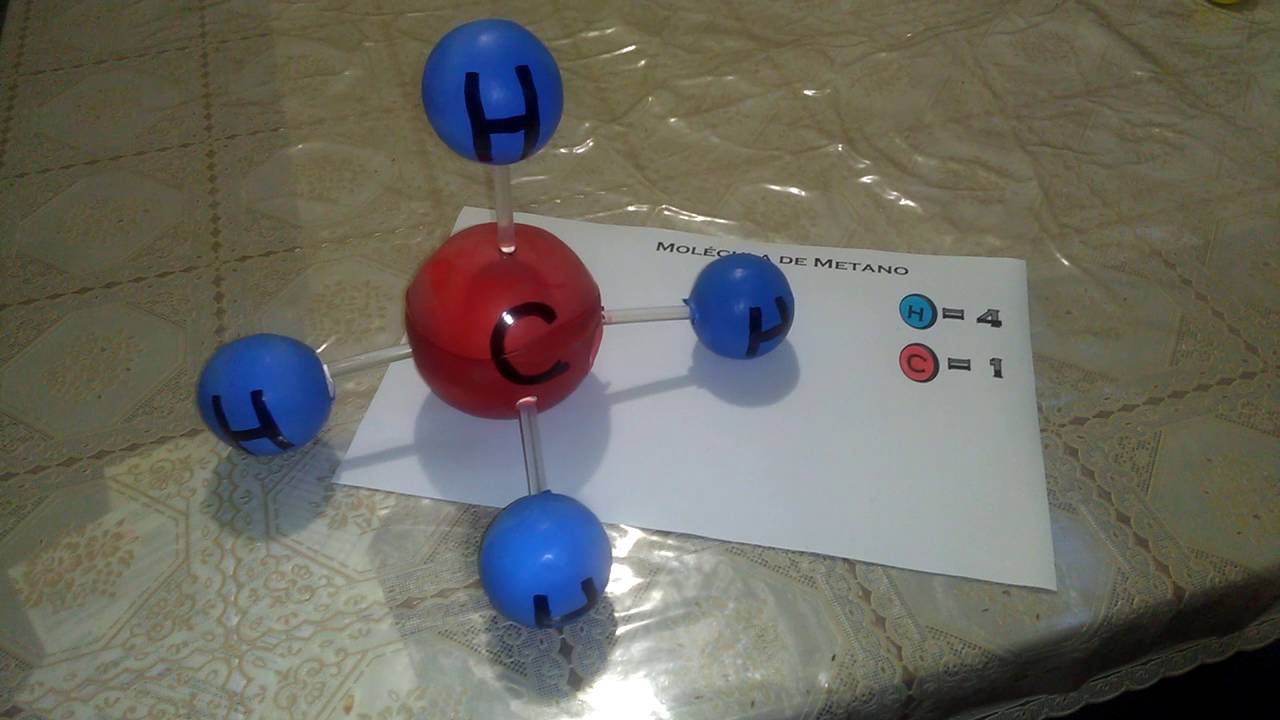 Вода является самым важным химическим веществом для жизни на Земле. Вода составляет большую часть каждого живого существа, поэтому каждое живое существо нуждается в воде. Вот почему вода важна для орошения сельскохозяйственных культур, здоровья скота, а также для непосредственного потребления человеком (питьевая, умывающаяся и т. д.). Вода также является важной частью преобразования первичной энергии в энергетические услуги (см. использование воды в энергетических системах).
Вода является самым важным химическим веществом для жизни на Земле. Вода составляет большую часть каждого живого существа, поэтому каждое живое существо нуждается в воде. Вот почему вода важна для орошения сельскохозяйственных культур, здоровья скота, а также для непосредственного потребления человеком (питьевая, умывающаяся и т. д.). Вода также является важной частью преобразования первичной энергии в энергетические услуги (см. использование воды в энергетических системах).
Как видно из рисунка 1, на Земле много воды, но большая ее часть соленая, известная как соленая вода. Эта вода не пригодна для питья, поэтому не употребляется человеком. Большая часть пресной воды, необходимой для жизни, заключена в криосфере (ледники и постоянные снежные покровы), в то время как большая часть доступной пресной воды хранится в подземных водах. Самый маленький из трех пузырьков на картинке — это поверхностная вода; вода, к которой люди могут получить прямой доступ на поверхности Земли. Поскольку имеется такое небольшое количество этой потребляемой воды, загрязнение воды вызывает озабоченность. В некоторых частях мира отсутствие доступа к чистой пресной воде является серьезной проблемой.
В некоторых частях мира отсутствие доступа к чистой пресной воде является серьезной проблемой.
Характеристики
Рис. 2. Молекула воды, состоящая из двух атомов водорода и одного атома кислорода. [2]Молекула воды — одна из самых легких существующих молекул (хотя есть несколько более легких молекул), и это, безусловно, самая легкая молекула, которая образует жидкость на Земле. Вода образует жидкость при комнатной температуре, потому что у нее такой сильный электрический диполь. У воды самый сильный дипольный момент среди всех молекул из-за ее небольшого размера. Эта дипольная природа означает, что водород в воде сильно притягивается электронами вокруг кислорода, что называется водородной связью. Эта водородная связь воды не только делает воду жидкостью, но и делает ее мощным растворителем благодаря этим электрическим взаимодействиям. Это позволяет многим важным химическим реакциям происходить в воде.
Вода существует на Земле в трех фазах: жидкая вода, которая является наиболее распространенной, твердая вода (называемая льдом) и водяной пар в газообразной форме.
Вода и климат
Вода оказывает огромное влияние на климат Земли, а также является основным фактором погоды (см. разницу между климатом и погодой). Погода часто включает осадки, такие как дождь, снег и град. Облака состоят в основном из мелких капель воды или замороженных кристаллов. Водяной пар также является парниковым газом, оказывающим наибольшее влияние на температуру Земли, и он оказывает усиливающее воздействие на глобальное потепление из-за двуокиси углерода (CO 2 ). Другими словами, водяной пар сам по себе не вызывает изменения климата, однако усиливает его воздействие, поскольку чем больше CO 2 , тем больше водяного пара будет в атмосфере.
Слишком мало воды вызывает засуху, что является проблемой. Слишком много вызывает затопление, что также является проблемой. Одна из самых больших проблем, связанных с изменением климата, заключается в том, что оно повлияет на то, сколько воды будет в разных частях мира. Это можно резюмировать так: «мокрое станет еще влажнее, а сухое станет суше». См. более подробную информацию о влиянии изменения климата на воду. Совершенно независимо от изменения климата, есть немало опасений по поводу загрязнения воды такими вещами, как кислотные дожди.
См. более подробную информацию о влиянии изменения климата на воду. Совершенно независимо от изменения климата, есть немало опасений по поводу загрязнения воды такими вещами, как кислотные дожди.
Вода движется через различные системы на планете, принимает различные формы и транспортируется различными способами, включая испарение, конденсацию, таяние, замерзание, сублимацию и просто течение воды. Это движение воды по всей планете называется гидрологическим циклом.
Интересные факты
- Вода составляет три четверти поверхности Земли.
- Вода составляет 60-78% массы человека (в зависимости от возраста у младенцев больше воды, чем у взрослых) [3]
- Вода является побочным продуктом горения, обычно в виде водяного пара.
- Вода используется для преобразования тепла в работу на угольных электростанциях, электростанциях, работающих на природном газе, и атомных электростанциях.
- Вода также часто используется в качестве поглотителя холода на тех же электростанциях путем сброса отработанного тепла в реки, озера или океан.

- Вода часто переносит тепло из глубины земли для получения геотермальной энергии.
Чтобы узнать больше о воде, посетите страницу водных ресурсов Геологической службы США.
Для дальнейшего чтения
- Гидрологический цикл
- Водородная связь
- Энергия воды
- Силовая установка
- Гидроэнергетика
- Жизненный цикл
- Или просмотрите случайную страницу
Ссылки
- ↑ Геологическая служба США. (2 августа 2015 г.). Сколько воды в мире. [Онлайн]. Доступно: http://water.usgs.gov/edu/earthhowmuch.html
- ↑ Wikimedia Commons [в сети], доступно: https://commons.wikimedia.org/wiki/File:Water_molecule_3D.svg
- ↑ Геологическая служба США, школа водных ресурсов (2 августа 2015 г.). Вода в тебе доступно: http://water.usgs.gov/edu/propertyyou.html
Молекула воды и ее взаимодействия | Вода: очень краткое введение
Фильтр поиска панели навигации Oxford AcademicWater: A Very Short IntroductionVery Short IntroductionsФизическая химияVery Short IntroductionBooksJournals Мобильный телефон Введите поисковый запрос
ЗакрытьФильтр поиска панели навигации Oxford AcademicWater: A Very Short IntroductionVery Short IntroductionsФизическая химияVery Short IntroductionBooksJournals Введите поисковый запрос
Расширенный поиск
Иконка Цитировать Цитировать
Разрешения
- Делиться
- Фейсбук
- Твиттер
- Электронная почта
Укажите
Финни, Джон, «Молекула воды и ее взаимодействия», Water: A Very Short Introduction , Very Short Introductions ( Oxford , 2015; онлайн-издание, Oxford Academic, 27 августа 2015 г. ), https://doi. org/10.1093/actrade/9780198708728.003.0002, по состоянию на 14 июня 2023 г.
), https://doi. org/10.1093/actrade/9780198708728.003.0002, по состоянию на 14 июня 2023 г.Выберите формат Выберите format.ris (Mendeley, Papers, Zotero).enw (EndNote).bibtex (BibTex).txt (Medlars, RefWorks).
ЗакрытьФильтр поиска панели навигации Oxford AcademicWater: A Very Short IntroductionVery Short IntroductionsФизическая химияVery Short IntroductionBooksJournals Мобильный телефон Введите поисковый запрос
ЗакрытьФильтр поиска панели навигации Oxford AcademicWater: A Very Short IntroductionVery Short IntroductionsФизическая химияVery Short IntroductionBooksJournals Введите поисковый запрос
Advanced Search
Abstract
В разделе «Молекула воды и ее взаимодействия» обсуждаются структурные и электрические свойства молекулы воды. Молекула воды состоит из двух атомов водорода, соединенных ковалентными связями с одним атомом кислорода. Молекулы воды взаимодействуют друг с другом через тип взаимодействия, называемый водородной связью. Тетраэдрическое расположение четырех молекул воды вокруг центральной является ключом к пониманию воды. Это помогает объяснить структуру воды в ее различных состояниях, ее свойства и то, как она взаимодействует с другими видами молекул, позволяя исследовать свойства и поведение широкого спектра химических, физических и биологических систем, в которых участвует вода. .
Молекула воды состоит из двух атомов водорода, соединенных ковалентными связями с одним атомом кислорода. Молекулы воды взаимодействуют друг с другом через тип взаимодействия, называемый водородной связью. Тетраэдрическое расположение четырех молекул воды вокруг центральной является ключом к пониманию воды. Это помогает объяснить структуру воды в ее различных состояниях, ее свойства и то, как она взаимодействует с другими видами молекул, позволяя исследовать свойства и поведение широкого спектра химических, физических и биологических систем, в которых участвует вода. .
Ключевые слова: атомная теория, двуокись углерода, Джон Дальтон, водород, водородная связь, молекула, тетраэдрический угол, вода
Предмет
Физическая химияСерия
Очень краткое введениеКоллекция: Очень короткие вступления
В настоящее время у вас нет доступа к этой главе.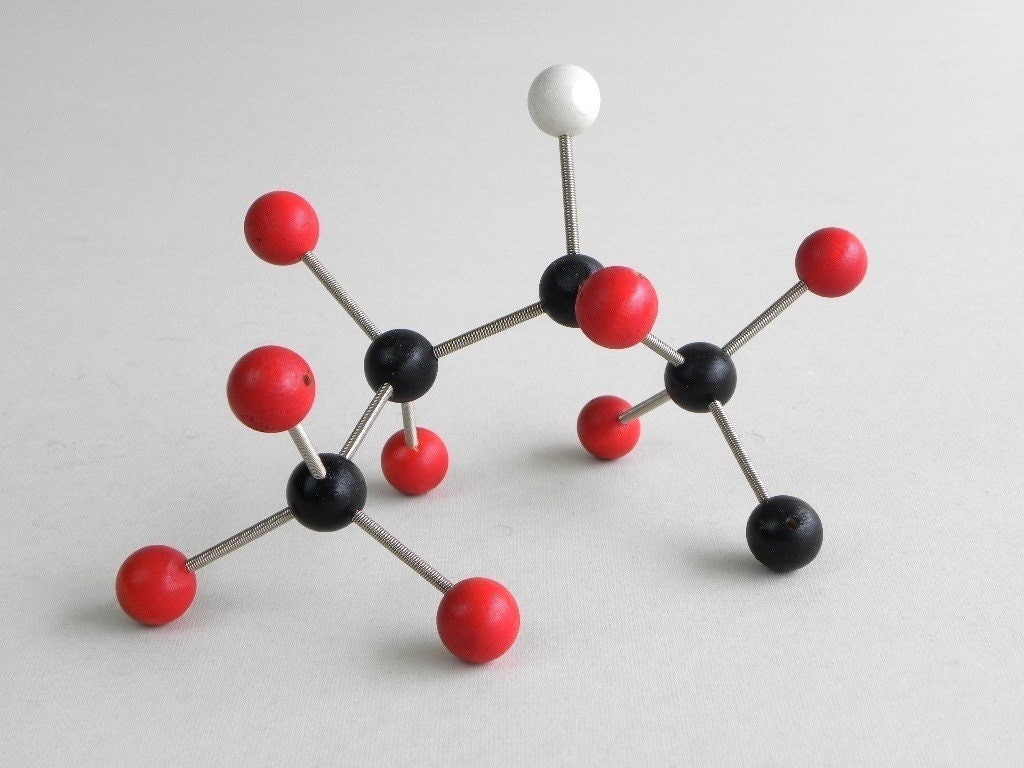
Войти
Получить помощь с доступомПолучить помощь с доступом
Институциональный доступ
Доступ к контенту в Oxford Academic часто предоставляется посредством институциональных подписок и покупок. Если вы являетесь членом учреждения с активной учетной записью, вы можете получить доступ к контенту одним из следующих способов:
Доступ на основе IP
Как правило, доступ предоставляется через институциональную сеть к диапазону IP-адресов. Эта аутентификация происходит автоматически, и невозможно выйти из учетной записи с IP-аутентификацией.
Войдите через свое учреждение
Выберите этот вариант, чтобы получить удаленный доступ за пределами вашего учреждения. Технология Shibboleth/Open Athens используется для обеспечения единого входа между веб-сайтом вашего учебного заведения и Oxford Academic.
- Щелкните Войти через свое учреждение.
- Выберите свое учреждение из предоставленного списка, после чего вы перейдете на веб-сайт вашего учреждения для входа.
- При посещении сайта учреждения используйте учетные данные, предоставленные вашим учреждением. Не используйте личную учетную запись Oxford Academic.
- После успешного входа вы вернетесь в Oxford Academic.
Если вашего учреждения нет в списке или вы не можете войти на веб-сайт своего учреждения, обратитесь к своему библиотекарю или администратору.
Вход с помощью читательского билета
Введите номер своего читательского билета, чтобы войти в систему. Если вы не можете войти в систему, обратитесь к своему библиотекарю.
Члены общества
Доступ члена общества к журналу достигается одним из следующих способов:
Войти через сайт сообщества
Многие общества предлагают единый вход между веб-сайтом общества и Oxford Academic. Если вы видите «Войти через сайт сообщества» на панели входа в журнале:
Если вы видите «Войти через сайт сообщества» на панели входа в журнале:
- Щелкните Войти через сайт сообщества.
- При посещении сайта общества используйте учетные данные, предоставленные этим обществом. Не используйте личную учетную запись Oxford Academic.
- После успешного входа вы вернетесь в Oxford Academic.
Если у вас нет учетной записи сообщества или вы забыли свое имя пользователя или пароль, обратитесь в свое общество.
Вход через личный кабинет
Некоторые общества используют личные учетные записи Oxford Academic для предоставления доступа своим членам. См. ниже.
Личный кабинет
Личную учетную запись можно использовать для получения оповещений по электронной почте, сохранения результатов поиска, покупки контента и активации подписок.
Некоторые общества используют личные учетные записи Oxford Academic для предоставления доступа своим членам.
Просмотр учетных записей, вошедших в систему
Щелкните значок учетной записи в правом верхнем углу, чтобы:
- Просмотр вашей личной учетной записи и доступ к функциям управления учетной записью.
- Просмотр институциональных учетных записей, предоставляющих доступ.
Выполнен вход, но нет доступа к содержимому
Oxford Academic предлагает широкий ассортимент продукции. Подписка учреждения может не распространяться на контент, к которому вы пытаетесь получить доступ. Если вы считаете, что у вас должен быть доступ к этому контенту, обратитесь к своему библиотекарю.
Ведение счетов организаций
Для библиотекарей и администраторов ваша личная учетная запись также предоставляет доступ к управлению институциональной учетной записью. Здесь вы найдете параметры для просмотра и активации подписок, управления институциональными настройками и параметрами доступа, доступа к статистике использования и т.


