Какие вещества не проводят электрический ток
Статьи › Школа › Чем отличается переменный ток от постоянного › Что не передает ток
Растворы сахара, спирта, глюкозы и некоторых других веществ не проводят электрический ток. Вещества, растворы которых не проводят электрический ток, называют неэлектролитами.
- Некоторые растворы, такие как сахар, спирт и глюкоза, не проводят электрический ток и называются неэлектролитами.
- Дистиллированная вода не содержит свободных зарядов и не проводит электрический ток, она является диэлектриком.
- Хорошими проводниками электрического тока являются металлы, такие как серебро, медь, алюминий, железо и золото.
- Диэлектриками или непроводниками электрического тока являются материалы, которые не могут переносить заряды, такие как бумага, стекло, фарфор, янтарь, резина и пластмассы.
- Газы, такие как воздух, являются хорошими диэлектриками и не проводят электрический ток.

- Диэлектрики — это вещества, в которых отсутствуют свободные носители заряда и которые не проводят электрический ток, такие как слюда, керамика, стекло и резина.
- Металлы, электролиты и ионизированные газы являются хорошими проводниками электрического тока.
- Которая в чистом виде не проводит электрический ток
- Какие вещества способны пропускать электрический ток
- Который не проводит электрический заряд
- Какие вещества проводят электрический ток
- Какие вещества не пропускают электрический ток
- Какие элементы не проводят электрический ток
- Какое название носят вещества которые не проводят ток
- Какие вещества способны проводить электрический ток
- Почему одни вещества проводят электрический ток а другие нет
- Какие химические вещества проводят электрический ток
- Как называются вещества которые проводят электрический ток
Которая в чистом виде не проводит электрический ток
Из школьного курса физики мы помним, что электрическим током считается движение заряженных частиц. Вода, как известно, состоит из молекул, которые электрически нейтральны. Поэтому дистиллированная вода считается диэлектриком, то есть ток она проводить не может.
Вода, как известно, состоит из молекул, которые электрически нейтральны. Поэтому дистиллированная вода считается диэлектриком, то есть ток она проводить не может.
Какие вещества способны пропускать электрический ток
Проводники К этой группе можно отнести вещества, которые проводят электрический ток великолепно. Это — металлы, электролиты и ионизированные газы.
Который не проводит электрический заряд
Тела, а также вещества и материалы, через которые электрические заряды не могут переходить с заряженного тела на незаряженное тело, называют непроводниками электрического тока или диэлектриками. К веществам, не проводящим электричество, относят бумагу, стекло, фарфор, янтарь, резину, эбонит, пластмассы, сухой воздух.
Какие вещества проводят электрический ток
Хорошими проводниками электрического тока являются металлы, например, серебро, медь, алюминий, железо, золото и другие. Тела, а также вещества и материалы, через которые электрические заряды не могут переходить с заряженного тела на незаряженное тело, называют непроводниками электрического тока или диэлектриками.
Какие вещества не пропускают электрический ток
Самым лучшим диэлектриком является газ. Другие непроводящие электрический ток материалы — это стеклянные, фарфоровые, керамические изделия, а также резина, картон, сухое дерево, смолы и пластмассы. Диэлектрические предметы — это изоляторы, свойства которых главным образом зависимы от состояния окружающей атмосферы.
Какие элементы не проводят электрический ток
Неэлектролиты — вещества, растворы или расплавы которых не проводят электрический ток. К ним относятся: кислород, водород, многие органические вещества (сахара, эфиры, бензол и др.). В молекулах этих веществ существуют ковалентные неполярные или малополярные связи.
Какое название носят вещества которые не проводят ток
Диэлектрики Вещества, в которых свободные носители заряда отсутствуют. Диэлектрики не проводят электрический ток, ни при каких условиях, их еще называют изоляторами. К ним относятся слюда, керамика, стекло, резина.
Какие вещества способны проводить электрический ток
К этой группе можно отнести вещества, которые проводят электрический ток великолепно. Это — металлы, электролиты и ионизированные газы.
Это — металлы, электролиты и ионизированные газы.
Почему одни вещества проводят электрический ток а другие нет
Почему одни материалы проводят электричество, а другие — нет? Материалы, которые имеют свободно движущиеся электроны, такие как металлы, могут проводить электрический ток, потому что электроны могут передаваться от атома к атому, образуя электрический поток.
Какие химические вещества проводят электрический ток
Электролиты — это вещества, которые после диссоциации на ионы в растворах и расплавах проводят электроток. Обычно в их молекулах ионные или полярные ковалентные связи.
Как называются вещества которые проводят электрический ток
Проводники — вещества, которые хорошо проводят электрический ток. К ним относятся металлы, растворы солей, кислот, щелочей в воде. Для них характерно наличие свободных заряженных частичек (электронов, ионов), которые под действием электрического поля двигаются.
Российские ученые выяснили, почему «жидкие соли» проводят ток
https://ria. ru/20190610/1555447481.html
ru/20190610/1555447481.html
Российские ученые выяснили, почему «жидкие соли» проводят ток
Российские ученые выяснили, почему «жидкие соли» проводят ток — РИА Новости, 10.06.2019
Российские ученые выяснили, почему «жидкие соли» проводят ток
Ученые из «Сколтеха» и зарубежных научных центров выяснили, как так называемые ионные жидкости, жидкие соли, могут проводить электрический ток. Их выводы и… РИА Новости, 10.06.2019
2019-06-10T15:20
2019-06-10T15:20
2019-06-10T15:20
наука
москва
открытия — риа наука
сколковский институт науки и технологий
химия
физика
/html/head/meta[@name=’og:title’]/@content
/html/head/meta[@name=’og:description’]/@content
https://cdnn21.img.ria.ru/images/150834/40/1508344063_0:3:1036:586_1920x0_80_0_0_c87168730dc7aa80130e729bd5a39cf8.jpg
МОСКВА, 10 июн – РИА Новости. Ученые из «Сколтеха» и зарубежных научных центров выяснили, как так называемые ионные жидкости, жидкие соли, могут проводить электрический ток.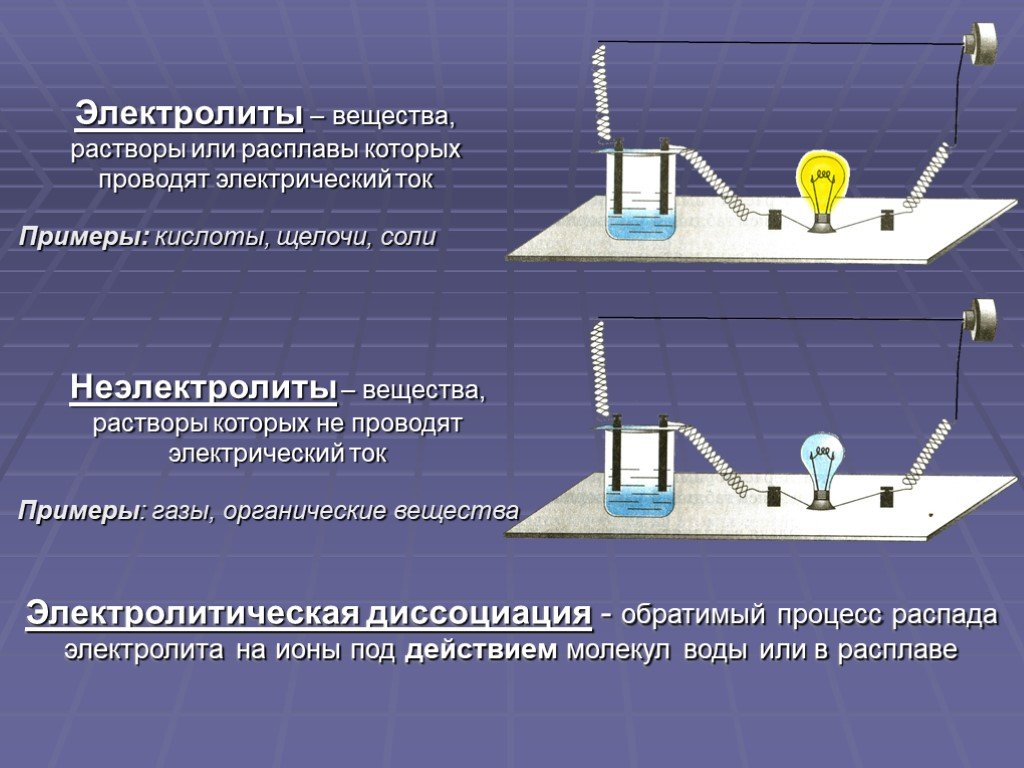 Их выводы и возможные применения подобных соединений были представлены в журнале Physical Review X."Мы с коллегами ожидаем, что явления, наблюдаемые в полупроводниках, будут обнаружены в ионных жидкостях комнатной температуры. Нам кажется, что они найдут множество важных применений", — заявил Николай Бриллиантов, профессор Сколковского института науки и технологий.Ионные жидкости, по сути, представляют собой жидкие соли. В то время как их обычные «кузены», такие как вода или бензин, состоят из электрически нейтральных молекул, молекулы ионных жидкостей несут электрические заряды.Неорганические соли переходят в подобное состояние только при высоких температурах, однако в последние годы химики открыли сразу несколько сложных органических веществ с подобным устройством, которые остаются жидкими при комнатной температуре. Ионные жидкости обладают массой интересных свойств, которые позволят в будущем использовать их для создания нетоксичных, но при этом жидких проводников, экзотических растворителей, суперконденсаторов и различных компонентов электроники и электрических сетей, в том числе движущихся частей роботов.
Их выводы и возможные применения подобных соединений были представлены в журнале Physical Review X."Мы с коллегами ожидаем, что явления, наблюдаемые в полупроводниках, будут обнаружены в ионных жидкостях комнатной температуры. Нам кажется, что они найдут множество важных применений", — заявил Николай Бриллиантов, профессор Сколковского института науки и технологий.Ионные жидкости, по сути, представляют собой жидкие соли. В то время как их обычные «кузены», такие как вода или бензин, состоят из электрически нейтральных молекул, молекулы ионных жидкостей несут электрические заряды.Неорганические соли переходят в подобное состояние только при высоких температурах, однако в последние годы химики открыли сразу несколько сложных органических веществ с подобным устройством, которые остаются жидкими при комнатной температуре. Ионные жидкости обладают массой интересных свойств, которые позволят в будущем использовать их для создания нетоксичных, но при этом жидких проводников, экзотических растворителей, суперконденсаторов и различных компонентов электроники и электрических сетей, в том числе движущихся частей роботов. Проблема, как отмечает Бриллиантов, заключается в том, что ученые до сих пор не до конца понимают и спорят о том, как именно ионные жидкости проводят ток. Дело в том, что подобные соединения должны содержать в себе равное число положительно и отрицательно заряженных ионов, нейтрализующих друг друга при сближении.Иными словами, свободных носителей заряда в подобной жидкости не должно быть и она должна быть изолятором, а не проводником, однако в реальности наблюдается совершенно обратная картина. Российские физики и их зарубежные коллеги, как сообщает пресс-служба «Сколтеха», нашли объяснение этому, создав математическую модель «жидкой соли».Как оказалось, механизм электропроводности в таких жидкостях весьма необычен. Большую часть времени ионы внутри них действительно проводят в нейтральном состоянии, объединяясь в пары с носителями противоположного заряда или в более крупные структуры.С другой стороны, как показали расчеты ученых, почти незаметные тепловые флуктуации, неизбежно возникающие в разных частях жидкости, заставляют подобные структуры распадаться на очень короткое время и потом заново соединяться.
Проблема, как отмечает Бриллиантов, заключается в том, что ученые до сих пор не до конца понимают и спорят о том, как именно ионные жидкости проводят ток. Дело в том, что подобные соединения должны содержать в себе равное число положительно и отрицательно заряженных ионов, нейтрализующих друг друга при сближении.Иными словами, свободных носителей заряда в подобной жидкости не должно быть и она должна быть изолятором, а не проводником, однако в реальности наблюдается совершенно обратная картина. Российские физики и их зарубежные коллеги, как сообщает пресс-служба «Сколтеха», нашли объяснение этому, создав математическую модель «жидкой соли».Как оказалось, механизм электропроводности в таких жидкостях весьма необычен. Большую часть времени ионы внутри них действительно проводят в нейтральном состоянии, объединяясь в пары с носителями противоположного заряда или в более крупные структуры.С другой стороны, как показали расчеты ученых, почти незаметные тепловые флуктуации, неизбежно возникающие в разных частях жидкости, заставляют подобные структуры распадаться на очень короткое время и потом заново соединяться. В результате этого, электричество движется через «жидкие соли», подобно атлетам, участвующим в своеобразном многоборье. Пока ионы находятся в свободном состоянии, они поддерживают электрический ток, а затем «передают эстафету» следующей партии частиц. Нечто похожее, как отмечают ученые, происходит в полупроводниках, через которые электричество движется благодаря взаимодействию «дырок» и электронов.С другой стороны, как отмечает Бриллиантов, эта идея не может объяснить всех парадоксов ионных жидкостей. Дело в том, что число свободных ионов, которые фиксируются внутри жидких солей во время экспериментов с ними, значительно ниже, чем предсказывает данная теория. Почему это так, ученым еще предстоит выяснить.
В результате этого, электричество движется через «жидкие соли», подобно атлетам, участвующим в своеобразном многоборье. Пока ионы находятся в свободном состоянии, они поддерживают электрический ток, а затем «передают эстафету» следующей партии частиц. Нечто похожее, как отмечают ученые, происходит в полупроводниках, через которые электричество движется благодаря взаимодействию «дырок» и электронов.С другой стороны, как отмечает Бриллиантов, эта идея не может объяснить всех парадоксов ионных жидкостей. Дело в том, что число свободных ионов, которые фиксируются внутри жидких солей во время экспериментов с ними, значительно ниже, чем предсказывает данная теория. Почему это так, ученым еще предстоит выяснить.
https://ria.ru/20190418/1552813187.html
https://ria.ru/20190530/1555114436.html
москва
РИА Новости
1
5
4.7
96
7 495 645-6601
ФГУП МИА «Россия сегодня»
https://xn--c1acbl2abdlkab1og.xn--p1ai/awards/
2019
РИА Новости
1
5
4. 7
7
96
7 495 645-6601
ФГУП МИА «Россия сегодня»
https://xn--c1acbl2abdlkab1og.xn--p1ai/awards/
Новости
ru-RU
https://ria.ru/docs/about/copyright.html
https://xn--c1acbl2abdlkab1og.xn--p1ai/
РИА Новости
1
5
4.7
96
7 495 645-6601
ФГУП МИА «Россия сегодня»
https://xn--c1acbl2abdlkab1og.xn--p1ai/awards/
1920
1080
true
1920
1440
true
https://cdnn21.img.ria.ru/images/150834/40/1508344063_127:0:911:588_1920x0_80_0_0_89b069094b73f65c85a42e2b260520d8.jpg1920
1920
true
РИА Новости
1
5
4.7
96
7 495 645-6601
ФГУП МИА «Россия сегодня»
https://xn--c1acbl2abdlkab1og.xn--p1ai/awards/
РИА Новости
1
5
4.7
96
7 495 645-6601
ФГУП МИА «Россия сегодня»
https://xn--c1acbl2abdlkab1og. xn--p1ai/awards/
xn--p1ai/awards/
москва, открытия — риа наука, сколковский институт науки и технологий, химия, физика
Наука, Москва, Открытия — РИА Наука, Сколковский институт науки и технологий, Химия, Физика
МОСКВА, 10 июн – РИА Новости. Ученые из «Сколтеха» и зарубежных научных центров выяснили, как так называемые ионные жидкости, жидкие соли, могут проводить электрический ток. Их выводы и возможные применения подобных соединений были представлены в журнале Physical Review X.
«
«Мы с коллегами ожидаем, что явления, наблюдаемые в полупроводниках, будут обнаружены в ионных жидкостях комнатной температуры. Нам кажется, что они найдут множество важных применений», — заявил Николай Бриллиантов, профессор Сколковского института науки и технологий.
Ионные жидкости, по сути, представляют собой жидкие соли. В то время как их обычные «кузены», такие как вода или бензин, состоят из электрически нейтральных молекул, молекулы ионных жидкостей несут электрические заряды.
Неорганические соли переходят в подобное состояние только при высоких температурах, однако в последние годы химики открыли сразу несколько сложных органических веществ с подобным устройством, которые остаются жидкими при комнатной температуре.
Российские физики подобрали идеальный материал для создания лазеров18 апреля 2019, 14:24
Ионные жидкости обладают массой интересных свойств, которые позволят в будущем использовать их для создания нетоксичных, но при этом жидких проводников, экзотических растворителей, суперконденсаторов и различных компонентов электроники и электрических сетей, в том числе движущихся частей роботов.
Проблема, как отмечает Бриллиантов, заключается в том, что ученые до сих пор не до конца понимают и спорят о том, как именно ионные жидкости проводят ток. Дело в том, что подобные соединения должны содержать в себе равное число положительно и отрицательно заряженных ионов, нейтрализующих друг друга при сближении.
Иными словами, свободных носителей заряда в подобной жидкости не должно быть и она должна быть изолятором, а не проводником, однако в реальности наблюдается совершенно обратная картина. Российские физики и их зарубежные коллеги, как сообщает пресс-служба «Сколтеха», нашли объяснение этому, создав математическую модель «жидкой соли».
Российские физики и их зарубежные коллеги, как сообщает пресс-служба «Сколтеха», нашли объяснение этому, создав математическую модель «жидкой соли».
Как оказалось, механизм электропроводности в таких жидкостях весьма необычен. Большую часть времени ионы внутри них действительно проводят в нейтральном состоянии, объединяясь в пары с носителями противоположного заряда или в более крупные структуры.
С другой стороны, как показали расчеты ученых, почти незаметные тепловые флуктуации, неизбежно возникающие в разных частях жидкости, заставляют подобные структуры распадаться на очень короткое время и потом заново соединяться.
Ученые из МФТИ превратили кинескоп телевизора в «вечную» лампочку30 мая 2019, 16:40
В результате этого, электричество движется через «жидкие соли», подобно атлетам, участвующим в своеобразном многоборье. Пока ионы находятся в свободном состоянии, они поддерживают электрический ток, а затем «передают эстафету» следующей партии частиц. Нечто похожее, как отмечают ученые, происходит в полупроводниках, через которые электричество движется благодаря взаимодействию «дырок» и электронов.
С другой стороны, как отмечает Бриллиантов, эта идея не может объяснить всех парадоксов ионных жидкостей. Дело в том, что число свободных ионов, которые фиксируются внутри жидких солей во время экспериментов с ними, значительно ниже, чем предсказывает данная теория. Почему это так, ученым еще предстоит выяснить.
Проводимость (электропроводность) и вода
Школа водных наук 6 июня 2018 г.
Проводимость (электропроводность) и вода
Свойства воды Фотогалерея
Узнайте о свойствах воды с помощью изображений
Дом школы водных наук
- Обзор
- Наука
- Публикации
Вода и электричество несовместимы, верно? На самом деле чистая вода является отличным изолятором и не проводит электричество. Дело в том, что чистой воды в природе не найти, так что не смешивайте электричество и воду. На странице нашей школы водных наук вы найдете все подробности.
Дело в том, что чистой воды в природе не найти, так что не смешивайте электричество и воду. На странице нашей школы водных наук вы найдете все подробности.
• Школа наук о воде ДОМАШНЯЯ СТРАНИЦА • Темы о свойствах воды • Темы о качестве воды •
Проводимость (электропроводность) и вода
Источники/использование: общественное достояние. Посетите СМИ, чтобы узнать подробности.
Многопараметрический монитор, используемый для записи измерений качества воды. Никогда не поздно научиться чему-то новому. Всю свою жизнь я слышал, что вода и электричество вместе составляют опасную пару. И почти всегда это правда — смешивать воду и электричество, будь то от молнии или электрической розетки в доме, очень опасно. Но что я узнал из исследования этой темы, так это то, что чистая вода на самом деле является отличным изолятором и не проводит электричество. Вода, которая будет считаться «чистой», будет дистиллированной водой (водой, сконденсированной из пара) и деионизированной водой (используемой в лабораториях), хотя даже вода такой чистоты может содержать ионы.
Но в реальной жизни мы обычно не встречаем чистой воды. Если вы читали нашу статью о том, что вода является «универсальным растворителем », вы знаете, что вода может растворять больше веществ, чем любая другая жидкость. Вода — превосходнейший растворитель. Не имеет значения, течет ли вода из вашего кухонного крана, находится в бассейне или собачьей миске, течет из-под земли или падает с неба, вода будет содержать значительное количество растворенных веществ, минералов и химических веществ. Это вещества, растворенные в воде. Впрочем, не беспокойтесь — если вы проглотите снежинку, она вам не повредит; он может даже содержать некоторые полезные минералы, необходимые вашему телу, чтобы оставаться здоровым.
Свободные ионы в воде проводят электричество
Источники/использование: общественное достояние.
Сотрудники Геологической службы США занимаются электроловом в реке Фрио, штат Техас. Вода перестает быть отличным изолятором, когда начинает растворять окружающие ее вещества.
Интересно, что если вода содержит очень большое количество растворенных веществ и ионов, то вода становится настолько эффективным проводником электричества, что электрический ток может фактически игнорировать человеческое тело в воде и придерживаться лучшего пути для проведения себя — массы ионов в воде. Вот почему опасность поражения электрическим током в морской воде меньше, чем в ванне.
Вот почему опасность поражения электрическим током в морской воде меньше, чем в ванне.
Источники/использование: общественное достояние.
Хотите узнать больше о проводимости и воде ? Следуйте за мной на веб-сайт, посвященный хлоридам, солености и растворенным веществам!
Ниже приведены другие научные темы, связанные с электропроводностью и водой.
Ниже приведены публикации, связанные с электропроводностью и водой.
5.3: Электролиты — Химия LibreTexts
- Последнее обновление
- Сохранить как PDF
- Идентификатор страницы
- Мухаммад Ариф Малик
- Hampton University, Hampton, VA
Что такое электролит?
Электрический ток определяется как движение электрических зарядов. Вещества, по которым может протекать электрический ток, называются электрическими проводниками, а остальные – электрическими непроводниками. Металлы являются электрическими проводниками, потому что валентные электроны атомов металла могут перемещаться в куске металла. Ионные соединения состоят из катионов и анионов, но ионы в твердом теле не могут перемещаться. Следовательно, твердые ионные соединения являются электрическими непроводниками. Чистая вода не имеет в себе достаточной концентрации ионов и является электрическим диэлектриком. Ионные соединения диссоциируют на ионы при растворении в воде. Раствор ионных соединений в воде является электрическим проводником, поскольку ионы могут перемещаться в растворе, как показано на рис. 5.3.1.
Следовательно, твердые ионные соединения являются электрическими непроводниками. Чистая вода не имеет в себе достаточной концентрации ионов и является электрическим диэлектриком. Ионные соединения диссоциируют на ионы при растворении в воде. Раствор ионных соединений в воде является электрическим проводником, поскольку ионы могут перемещаться в растворе, как показано на рис. 5.3.1.
Вещества, образующие электропроводящий раствор при растворении в воде (или в другом полярном растворителе), называются
Все ионные соединения, кислоты и основания образуют ионы в воде и классифицируются как электролиты.
Вещества, образующие неэлектропроводный раствор при растворении в воде, называются неэлектролитами .
Молекулярные соединения, отличные от кислот и оснований, такие как метанол, ацетон, сахар и глюкоза, остаются нейтральными молекулами при растворении в воде. Молекулярные растворенные вещества, кроме кислот и оснований, являются неэлектролитами.
Сильные и слабые электролиты
Вещества, почти на 100% диссоциирующие на ионы при растворении в воде, относятся к сильные электролиты .
- Все ионные соединения, растворимые в воде, являются сильными электролитами.
- Сильные кислоты являются сильными электролитами.
- Сильные основания — это ионные соединения и сильные электролиты.
Сильный электролит не обязательно хорошо растворим в воде. Это означает, что та часть растворенного вещества, которая растворяется, также диссоциирует на 100% на ионы в воде, например, все ионные соединения. Растворимость Ca(OH) 2 содержит только 0,16 г Ca(OH) 2 /100 г воды при 20 o C, но весь растворенный Ca(OH) 2 диссоциирует на Ca 2 + и OH — ионы.
Сильные основания представляют собой гидроксиды щелочных металлов, т. е. LiOH, NaOH, KOH, RbOH и CsOH, и гидроксиды тяжелых щелочноземельных металлов, т. е. Ca(OH) 2 , Sr(OH) 2 и Ba (OH) 2 , которые являются сильными электролитами. Сильные кислоты, т. е. HCl, HBr, HI, HClO 9{1-}(\mathrm{aq})\nonumber
\end{equation}
Вещества, которые частично диссоциируют на ионы при растворении в воде, являются слабыми электролитами . Слабые кислоты и слабые основания являются слабыми электролитами.
Слабые кислоты и слабые основания, такие как уксусная кислота (CH 3 COOH) и аммиак (NH 3 ), растворимы в воде, но частично диссоциируют на ионы. Например, если 1 моль уксусной кислоты или 1 моль аммиака растворить в 1 л воды при комнатной температуре, то между растворенными молекулами и диссоциированными ионами устанавливается следующее равновесие: 9{1-}(\mathrm{aq}),
\end{aligned}\nonumber
\end{equation}
, где только около 0,4% растворенных молекул диссоциируют на ионы, остальные около 99,6% молекул остаются нейтральными . Слабые кислоты и слабые основания являются слабыми электролитами.
Слабые кислоты и слабые основания являются слабыми электролитами.
На рис. 5.3.2 показаны различия между неэлектролитами, сильными электролитами и слабыми электролитами.
Рисунок \(\PageIndex{2}\): Иллюстрация неэлектролита, не проводящего электричество, сильного электролита с высокой электропроводностью и слабого электролита с низкой электропроводностью. Источник: Karishma50/ (https;//creativecommons.org/licences/by-sa/4.0)
Эквивалент
Количество молекул и атомов обычно измеряется в молях. Ионные соединения состоят из ионов, но в целом нейтральны, потому что положительный заряд уравновешивается отрицательным зарядом. Поэтому молярное отношение катионов к анионам не всегда равно один к одному. Например, NaCl имеет молярное соотношение Na + и Cl — один к одному, а CaCl 2 имеет соотношение один к двум Ca 2 + и Cl — . . Вводится новая единица, называемая эквивалентом (официально сокращенно эквив, но обычно сокращенно экв), чтобы различать моль иона и моль заряда иона. {2+}}\номер\] 9{2+}}\nonumber\]
{2+}}\номер\] 9{2+}}\nonumber\]
Первый коэффициент преобразования переводит данное количество в эквивалентах в моли, а второй преобразует заданное количество в молях в эквиваленты иона, как объяснено в следующих примерах.
Пример \(\PageIndex{1}\)
a) Рассчитать мг-экв Fe 3 + в 0,0200 моль Fe 3 + ? б) если хлорид-ион является единственным анионом в растворе, сколько мг-экв Cl — присутствует в растворе?
9{3+}\nonumber\]Пример \(\PageIndex{2}\)
Солевой раствор для внутривенного введения содержит 145 мэкв/л Na + . Сколько молей Na + содержится в 0,500 л раствора?
Раствор
a) Дано: 145 мэкв Na + /л раствора и 0,500 л раствора. Желаемое: ? моль Na +
Необходимые коэффициенты пересчета: Концентрация в мэкв/л является первым фактором для преобразования л в мэкв, равенство 1 мэкв Na + = 1 ммоль Na + дает второе преобразование, необходимое для преобразования мэкв в ммоль, и равенство 1000 ммоль Na + = 1 моль Na + дает третий коэффициент преобразования, необходимый для преобразования мэкв в моль. {+}\номер\]
{+}\номер\]
Обратите внимание, как единицы числителя одной дроби сокращаются единицами знаменателя следующей дроби, оставляя несокращенными только нужные единицы, которые становятся единицами числа ответа.
Электролиты в жидкостях организма
На рис. 5.3.3 показаны электролиты и их концентрации, обычно встречающиеся в жидкостях организма. Они играют важную роль в функционировании клеток и организма. Например, ионы натрия регулируют содержание воды и играют роль в передаче электрических импульсов в нервной системе. Ионы калия играют роль в поддержании регулярного сердцебиения, а также в передаче электрических импульсов. Ионы хлорида уравновешивают заряд. Ионы карбоната участвуют в поддержании рН крови.
Концентрации электролитов в жидкостях организма недостаточно высоки, чтобы их можно было указать в молях или эквивалентных единицах. Электролиты в жидкостях организма обычно указываются в единицах миллимолей (ммоль) или миллиэквивалентов (мэкв), где: \(1000 \mathrm{~ммоль}=1 \mathrm{~моль}\) и \(1000 \mathrm{~ mEq}=1 \mathrm{~Eq}\).


